Académique Documents
Professionnel Documents
Culture Documents
Biokimia Metabolisme
Transféré par
Heriyanto Shiddiq AlfaruqDescription originale:
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Biokimia Metabolisme
Transféré par
Heriyanto Shiddiq AlfaruqDroits d'auteur :
Formats disponibles
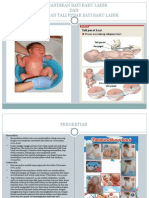
Metabolisme karbohidrat
Dr. Suparyanto, M.Kes APA ITU pencernakan
Pencernakan: proses pemecahan makanan dari bentuk komplek menjadi bentuk sederhana Karbohidrat: dari polisakarida dirubah menjadi Monosakarida (galaktose, fruktose, glukose) Glukose merupakan Monosakarida terbanyak dalam sirkulasi (70 - 110 mg / ml)
Galaktose dan fruktose dikonversi oleh hati dengan enzim yang sesuai menjadi glukose, kemudian masuk sirkulasi
Metabolisme karbohidrat Terdiri 3 fase: 1. Glikolisis 2. Siklus Kreb 3. Fosforilasi oksidatif
Glikolisis Proses perubahan glukose menjadi asam piruvat atau Asetil coenzim-A Glikolisis terjadi di sitoplasma
Glukose tidak dapat langsung diffusi ke sel Glukose harus berikatan dulu dengan carrier: G + C GC GC dapat berdiffusi kedalam sel Didalam sel GC G + C C keluar sel lagi untuk mengikat G yang lain sampai semua G masuk sel
Proses ini dipercepat oleh H. Insulin, jika H. Insulin kurang proses masuknya G kedalam sel lambat G menumpuk didalam darah DM G di sitoplasma mengalami fosforilasi glukose 6-PO4 (enzim glukokinase) Fruktokinase fruktose fruktose 6-PO4 Galaktokinase galaktose galaktose 6-PO4
Glikolisis: proses perubahan glukose menjadi asam piruvat atau asam laktat Glikolisis terdiri 2 lintasan:
Katabolisme glukosa (glikolisis) melalui triose (dihidroksi aseton fosfat atau gliseraldehid 3-PO4) disebut lintasan Embden Meyerhof Katabolisme glukosa (glikolisis) melalui 6-fosfoglukonat disebut lintasan oksidatif langsung (pintas heksosmonofosfat)
Siklus krebs Proses perubahan Asetil co-A H Proses ini terjadi didalam mitokondria
Pengambilan Asetil co-A di sitoplasma dilakukan oleh: oxalo asetat proses pengambilan ini terus bertahan sampai Asetil co-A di sitoplasma habis Jika dalam asupan nutrisi kekurangan KH akan kekurangan oxaloasetat
Kekurangan oxaloasetat pengambilan Asetil co-A di sitoplasma terhambat Asetil co-A menumpuk di sitoplasma Penumpukan Asetil co-A berikatan sesama Asetil co-A asam aseto asetat Asam aseto asetat senyawa tidak setabil mudah mengurai: aseton + asam hidroksi butirat
Ketiga senyawa: asam aseto asetat, aseton dan asam hidroksi butirat disebut Badan Keton Meningkatnya badan keton dalam darah ketosis
Badan keton bersifat racun bagi otak koma, karena biasanya terdapat pada penderita DM koma diabeticum
Fosforilasi oksidatif Dalam proses rantai respirasi dihasilkan energi yang tinggi energi tsb ditangkap oleh senyawa yang disebut ATP Fosforilasi oksidatif adalah proses pengikatan fosfor menjadi ikatan berenergi tinggi dalam proses rantai respirasi
Fosforilasi oksidatif: proses perubahan ADP ATP dengan cara mengambil energi yang dihasilkan Rantai Respirasi (reaksi H + O2 H2O)
RINGKASAN metabolisme karbohidrat
1. 2. 3. 4. 5. 6.
Glikolisis: perubahan glukose asam piruvat R / Glukose + 2 ADP + 2 PO4 2 asam piruvat + 2 ATP + 4 H Hasil utama glikolisis: asam piruvat Energi dihasilkan: 2 ATP Tempat reaksi glikolisis: sitoplasma Terdiri 2 lintasan: Embden Meyerhof dan Heksosmonofosfat
1. Siklus Kreb: perubahan Asetil co-A H 2. R / 2 Asetil Ko-A + 6 H2O + 2 ADP 4 CO2 + 16 H + 2 Ko-A + 2 ATP 3. Hasil utama: H 4. Energi dihasilkan: 2 ATP 5. Tempat berlangsung: mitokondria 6. Sisa metabolisme CO2 berasal dari hasil samping Siklus Krebs / Siklus Asam Sitrat / Siklus Asam Trikarboksilat 1. Fosforilasi oksidatif: proses perubahan ADP ATP dengan cara mengambil energi yang dihasilkan Rantai Respirasi (reaksi H + O2 H2O) 2. R / 2 H + O2 + 2e + ADP H2O + ATP 3. Energi yang dihasilkan: 34 ATP 4. Total hasil energi metabolisme karbohidrat: 38 ATP
REFERENSI 1. 2. 3. 4. 5. 6. Harper, Rodwell, Mayes, 1977, Review of Physiological Chemistry Colby, 1992, Ringkasan Biokimia Harper, Alih Bahasa: Adji Dharma, Jakarta, EGC Wirahadikusumah, 1985, Metabolisme Energi, Karbohidrat dan Lipid, Bandung, ITB Harjasasmita, 1996, Ikhtisar Biokimia dasar B, Jakarta, FKUI Toha, 2001, Biokimia, Metabolisme biomolekul, Bandung, Alfabeta Poedjiadi, Supriyanti, 2007, dasr-dasar Biokimia, Bandung, UI Press
Diposkan oleh dr. Suparyanto, M.Kes di 10:43 Tidak ada komentar Link ke posting ini Kirimkan Ini lewat EmailBlogThis!Berbagi ke TwitterBerbagi ke Facebook Label: BIOKIMIA
Reaksi:
MINGGU, 29 MEI 2011
Sintesa protein
Dr. Suparyanto, M.Kes Sintesa protein Replikasi DNA Model Replikasi (penggandaan DNA): 1. Model konservatif. Model dimana 2 rantai DNA yang bereplikasi tanpa memisahkan rantai-rantainya. 2. Model semi konservatif.
Model dimana 2 rantai DNA berpisah kemudian bereplikasi. 3. Model dispersi. Model dimana DNA terpecah menjadi potongan-potongan yang kemudian bereplikasi. Meselson dan Stahl membuktikan bahwa DNA bereplikasi sesuai model semi-konservatif
PROSES RIPLIKASI 1. Inisiasi 2. Elongasi 3. Terminasi INISIASI Replikasi tidak berlangsung pada titik acak pada DNA namun berlangsung pada awal yang disebut tempat awal replikasi. Protein inisiator menempel pada daerah tersebut kemudian menyebabkan rantai heliks terbuka untuk membangun rantai baru. ELONGASI DNA polimerase bertugas untuk memasangkan basa nitrogen baru dengan rantai DNA lama sehingga terbentuklah rantai DNA yang baru. Triplet AUG merupakan sinyal untuk memulai proses sintesis, sehingga triplet ini dinamakan kodon start. Terminasi Replikasi berakhir saat DNA polimerase mengenali daerah basa nitrogen yang diulang-ulang, daerah ini disebut telomer. Maka terbentuklah rantai DNA yang baru. Pada Sintesis protein, salah satu rantai DNA akan dikodekan oleh mrna. Rantai yang dikodekan tersebut disebut DNA Sense atau DNA template
Sedangkan rantai pasangannya yang tidak dicetak disebut DNA Antisense atau DNA komplementer. Triplet kode-kode genetik DNA yang dikodekan oleh mrna disebut kodogen.
RNA Berbeda dengan DNA, RNA merupakan rantai panjang lurus yang berfungsi dalam sintesis protein. Ada 3 jenis RNA yaitu: 1. mrna (messenger RNA atau RNA duta / RNAd), bertugas untuk mengkodekan kode genetik dari DNA untuk sintesis protein. Ada di anak inti.sel. Triplet kode genetik pada mrna disebut kodon. 2. tRNA (transfer RNA atau RNAt), bertugas untuk mencocokkan triplet yang ada pada mrna dengan protein yang sesuai. Ada di sitoplasma. Triplet kode genetik pada tRNA disebut antikodon. 3. rRNA (ribosomal RNA atau RNAr), bertugas untuk memasangkan kodon mrna dengan antikodon tRNA dan menggeser rantai supaya terbentuk polipeptida (protein). Ada di ribosom.
ATURAN pencetakan Gula yang dicetak Ribose Basa pada adn: A (adenin) T (timin) G (guanin) C (citosin)
Basa pada ARN: A (adenin) U (urasil) G (guanin) C (citosin) Adn ARN AU GC TA CG 3 jaringan basa pada Adn disebut: KODOGEN 3 jaringan basa yang tercetak pada ARN m disebut: kodon 3 jaringan basa pada ARN t yang setangkup dengan ARN m disebut: ANTIKODON
Sintesa protein Sintesa protein terdiri 2 tahap: 1. Transkripsi yaitu pencetakan arnd oleh Adn yang bertahan di dalam inti sel. Arnd inilah yang akan membawa kode genetik dari Adn. 2. Translasi yaitu penerjemahan kode genetik yang dibawa arnd oleh ARNt.
Gambar Sintesa Protein 1
Gambar Sintesa Protein 1 Transkripsi Proses ini berlangsung di dalam inti sel. Pertama sebagian dari "double helix" adn membuka di bawah pengaruh enzim ARN polymerase. Setelah 'double helix "adn sebagian membuka, maka arnd dibentuk sepanjang salah satu pita adn itu. DNA membuka menjadi 2 rantai terpisah. Karena mrna berantai tunggal, maka salah satu rantai DNA ditranskripsi (dicopy).
Rantai yang ditranskripsi dinamakan DNA sense atau template dan kode genetik yang dikode disebut kodogen. Rantai yang tidak ditranskripsi disebut DNA antisense / komplementer. Arnd yang telah selesai menerima pesan genetik dari adn segera meninggalkan inti melalui poripori dari membran nukleus menuju ribosom dalam sitoplasma. Arnd menempatkan diri pada leher ribosom. Pada rantai sense adn tersedia pasangan tiga basa nitrogen (triplet) yang disebut kodogen. Triplet ini akan mencetak triplet pada rantai arnd yang disebut kodon.
Kodon inilah yang disebut kode genetika yang berfungsi mengkodekan jenis asam amino tertentu yang diperlukan dalam sintesis protein. Pasangan tiga basa nitrogen disebut triplet. Triplet yang terdapat pada rantai sense Adn yang mencetak arnd disebut kodogen. Triplet yang terdapat pada arnd disebut kodon.
Triplet yang terdapat pada ARNt disebutantikodon. Translasi Setelah arnd keluar dari dalam inti, selanjutnya ia bergabung dengan ribosom dalam sitoplasma. Langkah berikutnya adalah penerjemahan kode genetik (kodon) yang dilakukan oleh ARNt. Caranya, ARNt akan mengikat asam amino tertentu sesuai yang dikodekan oleh kodon, lalu membawa asam amino tersebut dan bergabung dengan arnd yang telah ada di ribosom. Langkah tersebut dilakukan secara bergantian oleh banyak ARNt yang masing-masing mengikat satu jenis asam amino yang lain. ARNt memiliki triplet yang merupakan pasangan kodon dan disebut antikodon. Setiap ARNt hanya dapat mengikat satu jenis asam amino sesuai yang dikodekan oleh kodon.
Jadi dalam translasi terjadi penerjemahan kode genetik yang dibawa arnd (kodon) oleh ARNt (antikodon) dengan cara ARNt mengikat satu asam amino yang sesuai. Proses pengikatan asam amino ini membutuhkan enzim amino asil sintetase, dan ada 20 enzim yang bekerja. Setelah asam amino dibawa ARNt bergabung dengan arnd di ribosom, selanjutnya akan terjadi ikatan antar asam amino membentuk polipeptida.Protein akan terbentuk setelah berlangsung proses polimerisasi. KESIMPULAN 1. 2. 3. 4. 5.
Simpulan singkat langkah sintesis protein berlangsung sebagai berikut: Adn mencetak arnd dalam proses transkripsi yang berlangsung di dalam inti. Arnd keluar dari dalam inti bergabung dengan ribosom di sitoplasma. Datang ARNt membawa asam amino yang sesuai dengan kodon. Terjadi ikatan antar asam amino sehingga terbentukprotein.
Diposkan oleh dr. Suparyanto, M.Kes di 10:04 1 komentar: Link ke posting ini Kirimkan Ini lewat EmailBlogThis!Berbagi ke TwitterBerbagi ke Facebook Label: BIOKIMIA
Reaksi:
RABU, 23 JUNI 2010
MINERAL
Dr. Suparyanto, M.Kes MINERAL Makanan atau Nutrisi
Makanan: zat yang biasa dikonsumsi manusia untuk memenuhi kebutuhan hidupnya (gizi) Gizi adalah: zat yang diperlukan tubuh untuk memenuhi kebutuhan hidupnya Macam zat gizi: Karbohidrat, lemak, protein, vitamin, mineral, air
Makanan berenergi: makanan yang dapat menghasilkan energi, yaitu makanan yang mengandung: Karbohidrat, lemak, protein Makanan bergizi adalah makanan yang mengandung zat gizi Makanan bergizi seimbang: makanan yang mengandung zat gizi dalam komposisi seimbang, artinya sesuai yang diperlukan tubuh Zat gizi yang masuk tubuh harus sesuai yang dibutuhkan tubuh, tidak bisa kurang atau berlebih Semua makanan dibutuhkan dalam jumlah cukup dengan komposisi seimbang
Vitamin dan Mineral sebagai zat pengatur juga berfungsi sebagai cofactor enzim, antioksidan dan metabolisme Pembagian Mineral
Makromineral adalah mineral yang dibutuhkan tubuh dalam jumlah> 100 mg / hari Contoh: Ca, P, Na, K, Cl, Mg Mikromineral (unsur renik) adalah mineral yang dibutuhkan tubuh dalam jumlah <100 mg / hari Contoh: Cr, Co, Cu, I, Fe, Mn, Mo, Se, Si, Zn, F
Calsium (Ca) Fungsi: pembentuk tulang, gigi, pengaturan fungsi saraf dan otot Metabolisme: absorpsi perlu protein pengikat-Ca; diatur oleh vit.D, hormon paratiroid dan kalsitonin Defisiensi: rakitis, osteomalasia, osteoporosis Beracun: nausea, diare, iritabilitas Sumber: susu, kacang-kacangan, sayuran
Phosphor (P) Fungsi: pembentuk tulang, gigi, ATP, asam nukleat Metabolisme: penilaian dalam serum diatur oleh reabsorbsi ginjal Defisiensi: riketsia, osteomalasia (dewasa) Beracun: hipertiroidisme, osteoporosis Sumber: Zat aditif yang mengandung fosfat
Natrium (Na) Fungsi: kation utama CES, mengatur volume plasma, keseimbangan asam basa, fungsi saraf dan otot, Na / K-ATP-ase Metabolisme: diatur oleh aldosteron Defisiensi: tidak dikenal dalam diet Beracun: hipertensi Sumber: garam dapur
Kalium (K) Fungsi: kation utama CIS, fungsi saraf otot, Na / K-ATP-ase Metabolisme: diatur aldosteron Defisiensi: akibat diuretik, kelemahan otot, paralisis, kekacauan mental Beracun: henti jantung, ulkus usus halus Sumber: sayuran, buah, kacang-kacangan
Clorida (Cl) Fungsi: keseimbangan cairan dan elektrolit, karet lambung, transport HCO3 dalam eritrosit Defisiensi: akibat vomitus, diuretik, penyakit ginjal Sumber: garam meja
Magnesium (Mg) Fungsi: Pembentuk tulang, gigi, cofaktor enzim Defisiensi: akibat malabsorbsi, diare, pemabuk Beracun: reflek tendon menurun, penurunan respirasi Sumber: sayuran hijau
Chromium (Cr) Fungsi: membentuk insulin Defisiensi: gangguan toleransi glukose Sumber: daging, hati, ragi, padi-padian, kacang-kacangan, keju
Cobalt (Co) Fungsi: konstituen vit.B12 Defisiensi: sama seperti defisiensi vit.B12 menyebabkan Asiduria metilmalonat, anemia megaloblastik Sumber: makanan yang berasal dari hewan
Tembaga (Cu) Fungsi: konstituen enzim oksidase, sitokrom oksidase, berperan dalam absorbsi besi Metabolisme: diangkut oleh albumin, terikat dengan serulo plasmin Defisiensi: anemia (hipokromik-mikrositer) Beracun: penyakit Wilson Sumber: hati
Iodium (I) Fungsi: konstituen tiroksin, trijodotironin Metabolisme: disimpan dalam tiroid berupa tiroglobulin Defisiensi: kretinisme, goiter, hipotiroid, miksedemia Beracun: tirotoksikosis, goiter Sumber: garam berjodium, ikan laut
Besi (Fe) Fungsi: konstituen heme, Hb, sitokrom Metabolisme: diangkut sebagai transferin, disimpan sebagai feritin / hemosiderin, hilang lewat perdarahan Defisiensi: anemia (hipokromik mikrositer) Beracun: siderosis, hemokromatosis herediter Sumber: daging, hati, telur, alat masak dari besi
Mangan (Mn) Fungsi: co-factor enzim hidrolase, dekarboksilase, transferase, sintesis glikoprotein, proteoglikan Beracun: inhalasi benda beracun menyebabkan psikotik dan parkinsonisme
Molibdenium (Mo) Fungsi: konstituen enzim oksidase (xantin oksidase) yaitu enzim yang diperlukan dalam metabolisme purin menjadi asam urat Penyakit, sumber: tidak ada ada
Selenium (Se) Fungsi: konstituen glutation peroksidase Metabolisme: antioksidan sinergistik dengan vit.E Defiensi: terjadi jika konten dalam tanah rendah
Beracun: rambut rontok, dermatitis, irtabilitas Sumber: tumbuhan
Silicon (Si) Fungsi: kalsifikasi tulang, metabolisme glukose-minoglikan pada kartilago dan jaringan ikat Defisiensi: gangguan pertumbuhan Beracun: silikosis Sumber: tumbuhan
Zenk (Zn) Fungsi: co-factor enzim laktat dehidrogenase, alkalin fosfatase, karbonik anhidrase Defisiensi: hipogonadisme, kegagalan pertumbuhan, kegagalan penyembuhan luka, penurunan kemampuan mengecap dan mencium Beracun: iritasi gastrointestinal, muntah
Fluorida (F) Fungsi: meningkatkan kekerasan tulang dan gigi Defisiensi: karies dentis, osteoporosis Toksis: fluorosis dentis
Sumber: air minum REFERENSI 1. 2. 3. 4. 5. Harper, Rodwell, Mayes, 1977, Review of Physiological Chemistry Colby, 1992, Ringkasan Biokimia Harper, Alih Bahasa: Adji Dharma, Jakarta, EGC Wirahadikusumah, 1985, Metabolisme Energi, Karbohidrat dan Lipid, Bandung, ITB Harjasasmita, 1996, Ikhtisar Biokimia dasar B, Jakarta, FKUI Toha, 2001, Biokimia, Metabolisme biomolekul, Bandung, Alfabeta
Diposkan oleh dr. Suparyanto, M.Kes di 11:52 Tidak ada komentar Link ke posting ini Kirimkan Ini lewat EmailBlogThis!Berbagi ke TwitterBerbagi ke Facebook Label: BIOKIMIA
Reaksi:
SENIN, 21 JUNI 2010
HORMON
Dr. Suparyanto, M.Kes Apa Itu Hormon Uni organik yang dihasilkan oleh kelenjar endokrin yang dibawa oleh darah, terdiri dari derivat protein atau steroid, yang bertindak sebagai pembawa pesan kimiawi dimana tubuh mengkoordinasi fungsi-fungsinya Apa itu Kelenjar Endokrin Kelenjar endokrin memiliki fitur: Tidak memiliki saluran Hasilnya hormon Distribusi hasilnya melalui darah
Kelenjar eksokrin memiliki fitur: Memiliki saluran Hasilnya enzim atau mucus Distribusi hasilnya melalui saluranya
Macam Kelenjar Endokrin Hipotalamus G. Pituitaria / hipofise G. Thiroid G. Paratiroid G. Timus G. Adrenal G. Pancreas Ovarium / Testis Plasenta
Alur Perintah Hormon
Alur produksi ASI
Alur Perkembangan Folikel
Hormon Hipotalamus
Hormon hipofise
Hormon Tiroid dan Paratiroid
Hormon Adrenal
Hormon Pankreas
Hormon gonad
Hormon Plasenta
Hormon Saluran Cerna
Negative Fedback Mechanisme Jika produksi hormon meningkat rangsangan ke hipotalamus menurun Hormon / faktor releasing menurun hormon hipofise menurun produksi hormon menurun Negative Feedback Mechanisme
Produksi ASI
KB Hormonal
Cara Kerja Hormon Hormon reseptor sel di membran plasma merangsang keluarnya adenil siklase merubah ATP 3,5 AMP siklik respon fisiologik: Mengaktivasi enzim Mengubah permiabilitas sel Menyebabkan kontraksi / relaksasi otot Menyebabkan sintesa protein Menyebabkan sekresi
Cara kerja Hormon
REFERENSI 1. 2. 3. 4. 5. Harper, Rodwell, Mayes, 1977, Review of Physiological Chemistry Colby, 1992, Ringkasan Biokimia Harper, Alih Bahasa: Adji Dharma, Jakarta, EGC Wirahadikusumah, 1985, Metabolisme Energi, Karbohidrat dan Lipid, Bandung, ITB Harjasasmita, 1996, Ikhtisar Biokimia dasar B, Jakarta, FKUI Toha, 2001, Biokimia, Metabolisme biomolekul, Bandung, Alfabeta
Diposkan oleh dr. Suparyanto, M.Kes di 19:58 Tidak ada komentar Link ke posting ini Kirimkan Ini lewat EmailBlogThis!Berbagi ke TwitterBerbagi ke Facebook Label: BIOKIMIA
Reaksi:
KESEIMBANGAN cairan dan elektrolit
Dr. Suparyanto, M.Kes KESEIMBANGAN cairan dan elektrolit Cairan Tubuh
Sel organisme multiseluler (manusia) hidup dalam lautan cairan yang dibungkus oleh kulit organisme tsb disebut Cairan Ekstra Sel (CES)
Semua sel organisme multiseluler perlu nutrisi dan O2 dari CES Semua sel organisme multiseluler membuang sisa metabolisme kedalam CES
Tugas CES adalah menyediakan nutrisi sel dan membersihkan sisa metabolisme sel, juga merupakan medium transport substansi kimia / transmisi impuls dari satu sel ke sel yang lain CIS: merupakan medium reaksi kimia (aktivitas biokimiawi sel)
Sel dan Cairan Tubuh
Kehidupan Sel
Komposisi Cairan Cairan tubuh terdiri 57% BB terdiri dari: CIS = 70% dan CES = 30% Cairan Intra Seluler (CIS): Cairan yang terletak didalam sel tubuh Cairan Ekstra Seluler (CES): Cairan yang terletak diluar sel tubuh
CES atau Cairan interstisial: cairan yang terdapat pada celah antar sel, terdiri: Plasma darah, cairan serebrospinal, cairan limfe, Cairan intraokuler, Cairan persendian, Cairan gastrointestinal Macam Larutan Larutan isotonis: larutan yang memiliki tekanan osmosis sama dengan cairan tubuh (CES) Larutan hipotonis: cairan yang tekanan osmosis cairan tubuh (CES)
Efek Perbedaan Tekanan Osmosis Jika tekanan osmosis CES> CIS cairan CIS keluar sel mengkerut Jika tekanan osmosis CES 20:1 (normal = 10:1) Berat jenis urine tinggi Osmolalitas urine> 450 mOsmol / kg Ion Na urine <10 meq / L (causa ekstrarenal) Ion Na urine> 20 meq / L (causa renal / adrenal)
Penatalaksanaan Ketentuan Umum: Berikan maintenance cairan dan ganti cairan yang hilang Ganti kehilangan cairan yang masih berlangsung, volume per volume Pemberian cairan dibagi rata dalam 24 jam, kecuali keadaan khusus
Kelebihan Volume Edema: penumpukan cairan interstisial yang berlebihan Edema disebabkan oleh 4 mekanisme: Peningkatan tekanan hidrostatis kapiler (gagal gantung kongestif) COP (Colloid osmotic presure) yang menurun (hipoalbumin pd sirosis) Peningkatan permiabilitas kapiler pada peradangan Obstruksi aliran limfe (post mastektomi)
Gambaran Klinis Destensi vena jugularis Peningkatan tekanan v sentral (> 11 cm H2O) Peningkatan tekanan darah Denyut nadi penuh, kuat Melambatnya waktu pengosongan vena tangan (> 3-5 detik) Edeme perifer dan periorbita Asites, efusi pleura
Perubahan Laboratorium Penurunan hematokrit Protein serum rendah Ion Na serum normal, ion Na urine rendah (> 10 mEq/24jam) Penambahan 2% = kelebihan ringan Penambahan 5% = kelebihan sedang Penambahan 8% = kelebihan berat Penatalaksanaan Tergantung penyebabnya prinsip pembatasan asupan ion Na dan cairan Edema paru perlu tindakan cepat, untuk menghindari preload yang besar (beban yang masuk jantung) dengan cara: Posisi Fowler Pemberian diuretik kuat Pemberian oksigen Ketidakseimbangan Osmolalitas Ketidakseimbangan osmolalitas adalah ketidakseimbangan konsentrasi zat yang terlarut (mineral) dalam cairan tubuh Karena ion Na merupakan partikel utama ECF hipo / hiperosmolalitas mencerminkan hipo / hipernatremia hiperglikemia kejadian khusus pada kasus DM, akibat defisiensi H. Insulin Hiponatremia Disebabkan air yang berlebihan atau ion Na yang berkurang (Na + serum <135 meq / L) Menyebabkan pembengkakan sel (karena perpindahan air dari ECF ke ICF) mengancam jiwa jika Edem sel otak Terapi membuang air yang berlebihan atau menganti ion Na Hipernatremia Hipernatremia: penilaian Na serum> 145 meq / L menyebabkan hiperosmolalitas, sehingga terjadi dehidrasi ICF dan pengerutan sel Penyebab utamanya:
Kehilangan air (mengandung Na) Penambahan ion Na dengan kekurangan air Terapi: Hipernatremia dengan normovolemia D5 per oral atau IV Hipernatremia dengan hipervolemik D5 dan diuretik
Hipokalemia Hipokalemia penilaian ion K serum <3,5 meq / L (K ion utama ICF) Hipokalemia berkaitan dengan alkalosis, karena alkalosis menyebabkan ion K berpindah dari dari ECF ke ICF Terapi: Infus KCL Efek Hipokalemia CNS dan neuromaskuler: lelah, tidak enak badan, parestesis, reflek tendon menghilang, kelemahan otot Pernafasan: otot nafas lemah, napas dangkal Saluran cerna: motilitas usus besar menurun, anoreksia, mual, muntah, ileus kardiovaskuler: hipotensi postural, disritmia, Ginjal: poliuria, nokturia Hiperkalemia Hiperkalemia: peningkatan kadar ion K serum> 5,5 meq / L (asidosis, kerusakan jaringan) Hiperkalemia adalah keadaan darurat medis yang perlu segera dikenali dan ditangani untuk menghindari disritmia dan henti jantung Terapi: Kalsium glukonat 10% IV secara perlahan, dengan pemantauan EKG Glukose 10% dengan insulin dalam waktu 30 menit
Efek Hiperkalemia Neuromaskuler: kelemahan otot, paralisis Saluran cerna: mual, diare, kolik usus Ginjal: oliguria anuria Kardiovaskuler: disritmia jantung, bradikardia, henti jantung
Diposkan oleh dr. Suparyanto, M.Kes di 13:45 Tidak ada komentar Link ke posting ini Kirimkan Ini lewat EmailBlogThis!Berbagi ke TwitterBerbagi ke Facebook Label: BIOKIMIA
Reaksi:
MINGGU, 20 JUNI 2010
KESEIMBANGAN ASAM BASA TUBUH
Dr. Suparyanto, M.Kes keseimbangan asam basa TUBUH
7,45
Keseimbangan asam basa adalah homeostasis dari penilaian ion hidrogen dalam tubuh Penilaian normal ion hidrogen (H) arteri adalah: 4x10-8 atau pH = 7,4 (7,35 - 7,45) Asidosis = asidemia penilaian pH darah <7,35 Alkalemia = alkalosis penilaian pH darah> Penilaian pH darah <6,8 atau> 7,8 tidak dapat diatasi oleh tubuh
Sistem Buffer Tubuh Sistem buffer ECF asam karbonat-bikarbonat (NaHCO3 dan H2CO3) Sistem buffer ICF fosfat monosodium-disodium (Na2HPO4 dan NaH2PO4) Sistem buffer ICF eritrosit oksihemoglobin-hemoglobin (HbO2-dan HHb) Sistem buffer ICF dan ECF protein (Pr-dan HPr)
Pertahanan pH darah normal tercapai melalui kerja gabungan dari buffer darah, paru dan ginjal
Persamaan Handerson Hasselbach: 20 [HCO3-] pH = 6,1 + log --------------------1PaCO2 [HCO3-] faktor metabolik, dioperasikan ginjal PaCO2 faktor respiratorik, dioperasikan paru pH 6,1 efek buffer dari asam karbonat-bikarbonat Selama perbandingan [HCO3-]: PaCO2 = 20: 1 pH darah selalu = 6,1 + 1,3 = 7,4
Gangguan Asam Basa darah Asidosis metabolik [HCO3-] dikompensasi dengan PaCO2 Alkalosis metabolik [HCO3-] dikompensasi dengan PaCO2 Asidosis respiratorik PaCO2 dikompensasi dengan [HCO3-] Alkalosis respiratorik PaCO2 dikompensasi dengan [HCO3-]
Asidosis Metabolik Fitur: [HCO3-] <22mEq / L dan pH <7,35 kompensasi dengan hiperventilasi PaCO2 , kompensasi akhir ginjal ekskresi H +, sebagai NH4 + atau H3PO4 Penyebab: Penambahan asam terfiksasi: ketoasidosis diabetik, asidosis laktat (henti jantung atau syok), overdosis aspirin Gagal ginjal mengekskresi beban asam Hilangnya HCO3-basa diare Gejala asidosis Metabolik Tidak jelas dan asimptomatis kardiovaskuler: disritmia, penurunan kontraksi jantung, vasodilatasi perifer dan serebral neurologis: letargi, stupor, koma Pernafasan: hiperventilasi (Kussmal) Perubahan fungsi tulang: osteodistrofi ginjal (dewasa) dan retardasi pada anak Penatalaksanaan asidosis Metabolik Tujuan: meningkatkan pH darah sampai ke tingkat aman (7,20 sampai 7,25) dan mengobati penyakit dasar NaHCO3 dapat digunakan bila pH <7,2 atau [HCO3-] <15mEq / L Risiko NaHCO3 yang berlebihan: penekanan pusat napas, alkalosis respiratorik, hipoksia jaringan, alkalosis metabolik, hipokalsemia, kejang, tetani Alkalosis Metabolik Fitur: [HCO3-] > 26mEq / L dan pH>; 7,45 kompensasi dengan hipoventilasi PaCO2 , kompensasi akhir oleh ginjal ekskresi [HCO3-] yang berlebihan Penyebab: Hilangnya H + (muntah, diuretik, perpindahan H + dari ECF ke ICF pada hipokalemia) Retensi [HCO3-] (asidosis metabolik pasca hiperkapnia)
Gejala Alkalosis Metabolik Gejala dan tanda tidak spesifik Kejang dan kelemahan otot akibat hipokalemia dan dehidrasi Disritmia jantung, kelainan EKG hipokalemi Parestesia, kejang otot hipokalsemia
Penatalaksanaan Alkalosis Metabolik Tujuan: menghilangkan penyakit dasar Pemberian KCL secara IV dalam salin 0,9% (diberikan jika Cl-urine <10mEq / L) menghilangkan rangsangan aldosteron ekskresi NaHCO3 Jika Cl-urine> 20mEq / L disebabkan aldosteron yang berlebihan tidak dapat diobati dengan salin IV, tapi dengan diuretik
Asidosis Respiratorik Fitur: PaCO2 > 45mmHg dan pH <7,35 kompensasi ginjal retensi dan peningkatan [HCO3-] Penyebab: hipoventilasi (retensi CO2), inhibisi pusat nafas (overdosis sedatif, henti jantung), penyakit dinding dada dan otot nafas (fraktur costae, miastemia Gravis), gangguan pertukaran gas (COPD), obstruksi jalan napas atas Gejala asidosis Respiratorik Tidak spesifik Hipoksemia (dominan) asidosis respiratorik akut akibat obstruksi napas Somnolen progresif, koma asidosis respiratorik kronis vasodilatasi serebral meningkatkan ICV papiledema dan pusing Penatalaksanaan asidosis Respiratorik Pemulihan ventilasi yang efektif sesegera mungkin pemberian O2 dan mengobati penyebab penyakit dasar PaO2 harus ditingkatkan> 60mmHg dan pH> 7,2 Alkalosis Respiratorik Fitur: penurunan PaCO2 <35mmHg dan peningkatan pH serum> 7,45 kompensasi ginjal meningkatkan ekskresi HCO3 Penyebab: hiperventilasi (tersering psikogenik karena stress dan kecemasan), hipoksemia (pneumonia, gagal jantung kongestif, hipermetabolik (demam), stroke, stadium dini keracunan aspirin, septikemia Gejala Alkalosis Respiratorik Hiperventilasi (penilaian gas, frekuensi napas) Menguap, mendesak, merasa sulit bernafas Darurat: mulut kering, palpitasi, kelelahan, telapak tangan dan kaki dingin dan berkeringat Parastesia, otot berkedut, tetani Vasokontriksi serebal hipoksia cerebral kepala dingin dan sulit konsentrasi
Penatalaksanaan Alkalosis Respiratorik Menghilangkan penyebab dasar Kecemasan dapat dihilangkan dengan pernafasan kantong kertas yang dipegang erat disekitar hidung dan mulut dapat memulihkan serangan akut Hiperventilasi mekanik diatasi dengan mengurangi ventilasi dalam satu menit, menambahkan ruang hampa udara atau menghirup 3% CO2 dalam waktu singkat
Diposkan oleh dr. Suparyanto, M.Kes di 21:42 Tidak ada komentar Link ke posting ini Kirimkan Ini lewat EmailBlogThis!Berbagi ke TwitterBerbagi ke Facebook Label: BIOKIMIA
Reaksi:
RABU, 02 JUNI 2010
METABOLISME HEME
Dr. Suparyanto, M, Kes APA ITU HEME
Heme adalah senyawa besi forfirin yang terdapat dalam Hemoglobin eritrosit Eritrosit 120 hari mati dikatabolisme dihati Eritrosit Hemoglobin Heme + Globin (protein, digunakan lagi oleh tubuh) Heme Forfirin + Besi (digunakan lagi)
METABOLISME HEME Metabolisme Heme dilaksanakan di sel retikuloendotel pada hati, limpa & sumsum tulang Katabolisme heme dilaksanakan oleh enzim komplek yang disebut Oksigenase heme Heme Forfirin biliverdin bilirubin Bilirubin yang terbentuk dalam jaringan perifer akan diangkut kedalam hati oleh albumin plasma
TIGA PROSES METABOLISME HEME 1. 2. 3. Pengambilan bilirubin oleh sel perenkim hati Konjugasi bilirubin dalam retikulum endoplasma hati Ekskresi bilirubin terkonjugasi kedalam empedu
PENGAMBILAN bilirubin OLEH SEL HATI Bilirubin hasil metabolisme eritrosit oleh hati, limpa & sumsum tulang disebut bilirubin Indirex Sifat bilirubin Indirex tidak larut air non polar Agar dapat larut air harus diolah di Hati dikonjugasikan dengan asam glukoronat
Konjugasi bilirubin (DALAM HATI) Bilirubin Indirex dibuat larut air dan polar dengan cara direaksikan dengan asam glukoronat dikonjugasikan Tempat konjugasi di sel sinusoid hepar Hasil bilirubin Direx / konjugasi Bilirubin Direx larut air dan bersifat polar Diekskresikan empedu
Ekskresi bilirubin (KE empedu) Bilirubin Direx masuk empedu transport aktif Bilirubin Direx bersama getah empedu yang lain masuk duodenum
Di duodenum bilirubin Direx direduksi bakteri usus Urobilinogen (tidak berwarna) di colon dioksidasi oleh flora colon Urobilin (kuning) memberi warna feses (sterkobilinogen) PERJALANAN bilirubin dalam usus halus Sebagian Urobilin diabsorbsi oleh usus halus masuk darah diekskresi lewat ginjal memberi warna urine Ikterus Kenaikan tingkat bilirubin dalam darah (> 1mg/dl) disebut hiperbilirubinemia
Hiperbilirubinemia> (2 - 2,5 mg / dl) akan berdifusi kedalam jaringan kulit kuning, kondisi ini disebut Jaundice / ikterus PENYEBAB ikterus 1. Prehepatik (misal: anemia hemolitik)
2. 3.
Hepatik (misal: hepatitis) Post hepatik (misal: obstruksi ductus koledukus)
Ikterus FISIOLOGIK neonatorum Terjadi akibat hemolisis yang lebih cepat dan konsumsi, konjugasi dan sekresi bilirubin yg belum sempurna (fungsi hati belum sempurna). Terapi dengan penyinaran belum diketahui mekanismenya, tetapi dengan penyinaran bilirubin tak terkonjugasi berubah menjadi fragmen maleimida dan Isomer geometrik yang diekskresikan kedalam empedu Anemia hemolitik Eritrosit banyak rusak / lisis bilirubin Indirex meningkat di darah Hiperbilirubinemia ikterus Konjugasi di hepar normal bilirubin Direx normal Hasil Laboratorium: Bilirubin Indirex darah meningkat, Bilirubin urine negative
HEPATITIS Sel hati rusak konjugasi terganggu bilirubin direx menurun, bilirubin Indirex menumpuk didarah ikterus Urine Sel hati rusak Obstruksi ductus hepaticus bilirubin direx Refluk kedarah Ginjal Hasil Laboratorium: Bilirubin Indirex darah meningkat, Bilirubin urine positif
Obstruksi ductus KOLEDUKUS Obstruksi sal empedu Bilirubun Direx tidak dapat masuk duodenum reflux ke hati ke darah ginjal Urine Hasil laboratorium: Bilirubin Direx darah meningkat Bilirubine urine positif
REFERENSI 1. 2. 3. 4. 5. 6. Harper, Rodwell, Mayes, 1977, Review of Physiological Chemistry Colby, 1992, Ringkasan Biokimia Harper, Alih Bahasa: Adji Dharma, Jakarta, EGC Wirahadikusumah, 1985, Metabolisme Energi, Karbohidrat dan Lipid, Bandung, ITB Harjasasmita, 1996, Ikhtisar Biokimia dasar B, Jakarta, FKUI Toha, 2001, Biokimia, Metabolisme biomolekul, Bandung, Alfabeta Poedjiadi, Supriyanti, 2007, dasr-dasar Biokimia, Bandung, UI Press
Diposkan oleh dr. Suparyanto, M.Kes di 05:22 Tidak ada komentar Link ke posting ini Kirimkan Ini lewat EmailBlogThis!Berbagi ke TwitterBerbagi ke Facebook Label: BIOKIMIA
Reaksi:
ENZIM
Dr. Suparyanto, M.Kes APA ITU ENZIM
Enzim adalah biokatalisator yang mengatur kecepatan berlangsungnya semua proses fisiologis (reaksi kimia dalam tubuh) Tanpa adanya enzim, kehidupan tidak pernah ada, karena semua reaksi kimia dalam tubuh membutuhkan enzim Kegagalan tubuh mensintesa enzim dapat menimbulkan penyakit bahkan kematian Contoh: perubahan amoniak urea Enzim tersusun dari komponen protein yang disebut apoenzim Beberapa enzim membutuhkan komponen non protein yang disebut kofaktor Enzim yang terikat dengan kofaktor disebut holoenzim
Isoenzim: suatu zat yang bentuk molekulnya berbeda dengan enzim, tetapi fungsinya sama dengan enzim Koenzim adalah substrat yang mengaktifkan kerja enzim Koenzim banyak yang merupakan derivat vitamin B defisiensi vit. B mengganggu kerja enzim
SIFAT UMUM ENZIM Enzim adalah protein Enzim bekerja secara spesifik Enzim berfungsi sebagai biokatalis Enzim diperlukan dalam jumlah sedikit Enzim dapat bekerja secara bolak-balik Enzim dipengaruhi faktor lingkungan (suhu, pH, aktivator, inhibitor, konsentrasi substrat)
MACAM ENZIM Oksidoreduktase: enzim yang cara kerjanya berdasar reaksi oksidasi dan reduksi Oksidasi: reaksi yang mengeluarkan elektron H H + + e Reduksi: reaksi yang membutuhkan elektron Cl + e ClTransferase: enzim yang mengkalisis reaksi transfer / pertukaran dua gugus dalam dua zat Contoh: R-OH + R'-NH2 R-NH2 + R'-OH
Hydrolase: enzim yang mempercepat proses pemecahan suatu zat dengan cara direaksikan dengan air (hidrolisis) Contoh: AB + H2O A-OH + HB
Lyase: enzim yang memecah dua zat menjadi dua komponen AB A + B Isomerase: enzim yang mengkatalisis perubah suatu zat dari Isomer ke Isomer lainnya Isomer: suatu zat yang RM sama tetapi RB berbeda Contoh Isomerase: Arabinose ribose Lygase: enzim yang mengkatalisis pemutusan formasi ikatan gugus suatu zat Contoh: C = O, C-OH, COC, C-COOH, CS, CN atau CC
Enzim Oksidase: enzim yang mengkatalisis produksi hidrogen (H2) dari substrat dengan menggunakan oksigen (O2) sebagai akseptor hidrogen AH2 + O2 A + H2O
Enzim tersebut membentuk air (H2O) atau hidrogen peroksida (H2O2) sebagai produk reaksi Enzim Dehidrogenase: enzim yang mengeluarkan hidrogen dari suatu substrat dengan menggunakan carier sebagai akseptor hirogen, tidak dapat menggunakan oksigen sebagai akseptor hidrogen AH2 + B A + BH2
Enzim Hidroperoksidase: enzim yang mengeluarkan unsur oksigen dari substrat hidrogen peroksida (H2O2) Contoh: Peroksidase Katalase Enzim Oksigenase: enzim yang mengkatalisis reaksi suatu substrat dengan oksigen (O2) A + O2 AO2
FAKTOR YANG MEMPENGARUHI ENZIM Kerja enzim dipengaruhi oleh:
Temperatur, makin tinggi makin cepat, sampai suhu optimal, diatas suhu optimal menurunkan kecepatan pH, optimal pada pH: 5 - 9 Konsentrasi enzim: penambahan kosentrasi tidak menambah kecepatan (yang penting ada) Konsentrasi substrat: makin tinggi makin cepat Inhibitor: menghambat reaksi
TUGAS INDIVIDU 1. Apa yang dimaksud dengan enzim 2. Apa beda enzim dengan katalisator 3. Mengapa tanpa adanya enzim, kehidupan tidak pernah ada 4. Apa yang dimaksud dengan: 1. Apoenzim 2. Holoenzim 3. Koenzim 4. isoenzim 5. Sebutkan sifat2 enzim 6. Sebutkan faktor yang mempengaruhi kerja enzim 7. Sebutkan fungsi enzim berikut: 1. Transferase 2. Hidrolase 3. Oksidoreduktase 4. Lygase 8. Apa beda enzim dehidrogenase
dengan enzim oksidase 9. Apa beda enzim oksidase dengan enzim oksigenase REFERENSI 1. Harper, Rodwell, Mayes, 1977, Review of Physiological Chemistry 2. Colby, 1992, Ringkasan Biokimia Harper, Alih Bahasa: Adji Dharma, Jakarta, EGC 3. Wirahadikusumah, 1985, Metabolisme Energi, Karbohidrat dan Lipid, Bandung, ITB 4. Harjasasmita, 1996, Ikhtisar Biokimia dasar B, Jakarta, FKUI 5. Toha, 2001, Biokimia, Metabolisme biomolekul, Bandung, Alfabeta
Diposkan oleh dr. Suparyanto, M.Kes di 05:20 Tidak ada komentar Link ke posting ini Kirimkan Ini lewat EmailBlogThis!Berbagi ke TwitterBerbagi ke Facebook Label: BIOKIMIA
Reaksi:
PENGANTAR BIOKIMIA (INTRODUCTION of Biochemistry)
Dr. Suparyanto, M.Kes APA ITU BIOKIMIA
hidup
Biokimia adalah ilmu yang mempelajari reaksi kimia yang terjadi dalam sel atau organisme yang Kehidupan tergantung pada reaksi biokimianya
Reaksi biokimia yang harmonis dalam tubuh menyebabkan kondisi tubuh sehat, sebaliknya penyakit mencerminkan abnormalitas biomolekul, reaksi biokimia atau proses biokimia APA ITU PROSES FISIKA Reaksi Fisika: adalah perubahan bentuk suatu zat dan tidak menghasilkan zat baru
Hasilnya masih zat yang sama, hanya bentuknya atau wujudnya yang berubah, misal dari besar menjadi kecil (lembut) atau dari padat jadi cair Misal: perubahan beras tepung, atau es air
APA ITU REAKSI KIMIA Reaksi Kimia: adalah reaksi dua zat atau lebih yang menghasilkan zat baru, zat baru tsb berbeda dengan zat asalnya Misal: Perubahan beras nasi Amilum glukose Protein asam amino
Lemak asam lemak Reaksi kimia dalam tubuh (reaksi biokimia) selalu menggunakan enzim TUJUAN BIOKIMIA
Menguraikan dan menjelaskan semua proses kimiawi pada sel hidup dalam pengertian molekuler Upaya untuk memahami bagaimana kehidupan dimulai
HUBUNGAN BIOKIMIA DENGAN ILMU LAIN Biokimia asam nukleat (DNA dan RNA) inti ilmu genetika Fisiologi: ilmun tentang faal tubuh, pengkajianya overlaping dengan biokimia
Imunologi: penjelasan proses reaksi antigen antibodi (imunoglobulin), reaksi alergi perlu ilmu biokimia Farmakologi: metabolisme obat perlu ilmu biokimia dan fisiologi Toksikologi: ilmu yang mempelajari racun tubuh, perlu biokimia Patologi: ilmu tentang penyakit (inflamasi, cedera sel, kanker), perlu biokimia Mikrobiologi: ilmu tentang bakteri, perlu biokimia Zoologi dan botani: juga perlu biokimia
BEDA UNSUR, SENYAWA DAN MOLEKUL Unsur: zat terkecil, yang tidak dapat dibagi lagi Contoh unsur kimia: Na, K, Ca, Fe, O, C Gabungan dua atau lebih unsur yang sama disebut: molekul Contoh: O + O O2 Cl + Cl Cl2 Gabungan dua atau lebih unsur yang tidak sama disebut: senyawa Contoh: H + O H2O Na + Cl NaCl
UNSUR DAN biomolekul TUBUH MANUSIA Karbon, oksigen, hidrogen dan nitrogen merupakan unsur utama tubuh manusia
Kalsium, fosfor, kalium, natrium, klor, magnesium, besi, mangan, yodiun dan unsur lainya memiliki makna biologis dan medis yang sangat penting Air, DNA, RNA, protein, polisakarida dan lipid merupakan biomolekul utama tubuh
UNSUR TUBUH MANUSIA 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. C = 50% O = 20% H = 10% N = 8,5% Ca = 2,5% K = 1% S = 0,8% Na = 0,4% Cl = 0,4% Mg = 0,1% Fe = 0,01% Mn = 0,001% I = 0,00005%
Biomolekul TUBUH MANUSIA biomolekul PERSENTASE
1. 2. 3. 4. 5.
AIR 61,6% PROTEIN 17,0% LEMAK 13,8% MINERAL 6,1% Karbohidrat 1,5%
Biomolekul DAN FUNGSI DNA bahan genetik (gen) RNA template (cetakan) sintesa protein (membawa pesan genetik) Protein bahan enzim, hormon, antibodi Karbohidrat sumber energi utama Lipid membran sel, pelarut vitamin ADEK, penyimpanan energi
APA ITU SEL Sel merupakan unit fundamental biologi Sel merupakan unit terkecil organisme yang mampu mempertahankan kehidupan sendiri Sel memiliki organel dengan fungsi khusus Tiap organel menjalankan fungsi dengan reaksi kimia masing-masing
MANFAAT BIOKIMIA Hasil penelitian biokimia turut menentukan diagnosis, prognosis dan pengobatan penyakit
Pendekatan biokimia sering menjadi unsur fundamental untuk menjelaskan sebab penyakit dan merancang terapi yang tepat
Penggunaan berbagai pemeriksaan biokimia laboratorium secara bijaksana merupakan komponen integral dalam penegakan diagnosis dan pemantauan hasil terapi PENYEBAB PENYAKIT (BIOKIMIA) Penyebab fisik: trauma mekanis, suhu tinggi / rendah, perubahan mendadak tekanan atmosfer, radiasi, syok listrik Penyebab kimia dan obat2an: toksin, obat Penyebab biologis: virus, riketsia, bakteri, jamur, parasit Kekurangan O2: penurunan sirkulasi darah, kekurangan Hb, peracunan enzim oksidatif Genetik: kongenital, molekuler Reaksi imunologis: anafilaksis, hipersensitivitas, autoimune Gangguan keseimbangan gizi: defisiensi gizi, kelebihan gizi Gangguan keseimbangan hormon: defisiensi atau kelebihan hormon
LATIHAN 1. Apa yang dimaksud Biokimia 2. Apa beda reaksi fiasika dan reaksi kimia 3. Apa beda unsur, molekul dan senyawa 4. Apa yang menyebabkan manusia hidup, dan bagaimana cara mempertahankan hidup 5. Sebutkan unsur dan molekul utama manusia 6. Mengapa orang yang asupan makanannya kekurangan protein mudah sakit 7. Mengapa orang yang menderita gangguan nafas jadi loyo 8. Mengapa orang yang sering terekspos dengan radiasi dapat menderita kanker dan bayi yang cacat REFERENSI 1. 2. 3. 4. 5. 6. Harper, Rodwell, Mayes, 1977, Review of Physiological Chemistry Colby, 1992, Ringkasan Biokimia Harper, Alih Bahasa: Adji Dharma, Jakarta, EGC Wirahadikusumah, 1985, Metabolisme Energi, Karbohidrat dan Lipid, Bandung, ITB Harjasasmita, 1996, Ikhtisar Biokimia dasar B, Jakarta, FKUI Toha, 2001, Biokimia, Metabolisme biomolekul, Bandung, Alfabeta Poedjiadi, Supriyanti, 2007, dasr-dasar Biokimia, Bandung, UI Press
Diposkan oleh dr. Suparyanto, M.Kes di 05:14 Tidak ada komentar Link ke posting ini Kirimkan Ini lewat EmailBlogThis!Berbagi ke TwitterBerbagi ke Facebook Label: BIOKIMIA
Reaksi:
MINGGU, 10 JANUARI 2010
METABOLISME PURIN DAN PIRIMIDIN
Dr. Suparyanto, M.Kes asam nukleat
Asam nukleat atau asam inti, dikatakan demikian karena asam tersebut pertama kali diketemukan didalam inti sel Didalam inti sel asam nukleat ada dalam bentuk: DNA dan RNA DNA (Deoksiribo Nukleic Acid) merupakan bahan genetik yang disebut Gen RNA (ribo Nukleic Acid) merupakan bahan cetakan (template) informasi genetic
NUKLEOPROTEIN Nukleoprotein asam nukleat + protein Asam nukleat kombinasi nukleotida Nukleotida nukleosida + asam fosfat Nukleosida basa purin / pirimidin + pentosa Hidrolisis nukleoprotein protein, asam fosfat, pentosa, basa purin atau basa pirimidin
MACAM asam nukleat Macam asam nukleat:
1. 2. DNA: RNA:
DNA (deoksiribonucleic acid) RNA (ribonucleic acid)
Pentosa: deoksiribosa Basa: adenin, guanin, sitosin, timin
Pentosa: ribosa Basa: adenin, guanin, sitosin, urasil
PURIN DAN PIRIMIDIN Inti Purin dan Pirimidin adalah inti dari senyawa komponen molekul nukleotida asam nukleat RNA dan DNA Derivat Purin berupa senyawa: Adenin dan guanin Derivat Pirimidin berupa senyawa: sitosin, urasil dan timin Basa Purin (adenin, guanin) Basa Pirimidin (sitosin, urasil, timin)
Nukleosida diberi nama sesuai nama basa pembentuknya: adenin nukleisida (adenosin), guanin nukleisida (guanosin), urasil nukleosida (uridin), timin nukleisida (timidin), sitosin nukleisida (sitidin) Nukleosida ALAM Adenin nukleotida / Adenosin Mono fosfat (AMP) Guanin nukleotida / Guanosin Mono fosfat (GMP) Hipoksantin nukleotida / Inosin Mono fosfat (IMP) Urasil nukleotida / Uridin Mono fosfat (UMP) Sitidin nukleotida / Sitidin Mono fosfat (SMP)
Timin nukleotida / Timidin Mono fosfat (TMP) Adenosin trifosfat (ATP) ikatan energi tinggi Uridin trifosfat (UTP) ikatan energi tinggi
BEDA DNA DAN RNA
MACAM RNA mrna (messenger RNA): membawa kode genetik dari inti ke ribosom (sebagai tempat sintesa protein), kode terdiri 3 nukleotida yang disebut kodon tRNA (transfer RNA): membawa bahan sintesa protein dari sitoplasma ke ribosom, sesuai kode yang dibawa mrna, kode dalam rRNA disebut: Antikodon rRNA (ribosomal RNA): tempat sintesa protein
PURIN DAN PIRIMIDIN Purin dan pirimidin merupakan komponen utama DNA, RNA, koenzim, (NAD, NADP, ATP, UDPG) Contoh Purin: (adenin, guanin, hipoxantin, xantin) dimetabolisme jadi asam urat Contoh Pirimidin: (sitosin, urasil, timin) dimetabolisme jadi CO2 dan NH3
Katabolisme asam nukleat Nukleoprotein dalam pencernakan akan dipecah jadi molekul yang lebih kecil Nukleoprotein asam nukleat + protein Asam nukleat Nukleotida nukleosida + asam fosfat Nukleosida basa purin / pirimidin + pentosa Hidrolisis nukleoprotein protein, asam fosfat, pentosa, basa purin atau basa pirimidin
Katabolisme PURIN Adenosin Inosin Hiposantin Santin Asam Urat Guanosin guanin Santin Asam Urat
Santin oksidase adalah enzim yang merubah santin asam urat, enzim tsb banyak terdapat di: hati, ginjal, usus halus
Penyakit Gout (pirai) ditandai oleh tingginya asam urat dalam tubuh, sehingga terjadi penimbunan dibawah kulit berbentuk tophi Katabolisme PIRIMIDIN Sitosin Urasil Dihidrourasil Asam ureidopropionat CO2 + NH3 Timin Dihidrotimin Asam ureidoisobutirat CO2 + NH3 Katabolisme pirimidin terutama bertahan di hati
ASAM URAT Asam urat dibentuk dari metabolisme purin Asam urat diekskresi melalui ginjal
Jika produksi purin meningkat atau ekskresi menurun penumpukan asam urat dalam darah penyakit Gout PENYAKIT GOUT Gout adalah penyakit artritis berulang pada sendi articulatio matatarso falangealis akibat peningkatan kadar asam urat Peningkatan asam urat disebabkan: Produksi meningkat (leukemia, pneumonia) Ekskresi menurun (gangguan ginjal) Terapi: Mengurangi produksi (kolkisin, alopurinol)
Gout adalah penyakit di mana terjadi penumpukan asam urat dalam tubuh secara berlebihan, baik akibat produksi yang meningkat, atau pembuangan melalui ginjal yang menurun, atau akibat peningkatan asupan makanan kaya purin. Gout terjadi ketika cairan tubuh sangat jenuh akan asam urat karena kadarnya yang tinggi. Gout ditandai dengan: Serangan berulang dari arthritis (peradangan sendi) yang akut Kkadang-kadang disertai pembentukan kristal natrium urat besar yang dinamakan tophus Deformitas (kerusakan) sendi secara kronis, dan Cedera pada ginjal. Hiperuricemia (kadar asam urat dalam darah lebih dari 7,5 mg / dL)
PENGOBATAN GOUT Ketika terjadi serangan arthritis akut, penderita diberikan terapi untuk mengurangi peradangannya. Hal ini dapat dilakukan dengan memberikan obat analgesik / NSAID, kortikosteroid, tirah baring, atau dengan pemberian kolkisin. Setelah serangan akut berakhir, terapi ditujukan untuk menurunkan kadar asam urat dalam tubuh.
Hal ini dapat dilakukan dengan memberikan kolkisin atau obat yang memacu pembuangan asam urat lewat ginjal (misal probenesid) atau obat yang menghambat pembentukan asam urat (misal allopurinol). PENCEGAHAN GOUT Pasien gout juga harus menghindari penggunaan obat yang dapat menaikkan kadar asam urat dalam darah. Contoh dari obat tersebut adalah diuretik, aspirin, dan niasin. Alkohol merupakan sumber purin dan juga dapat menghambat pembuangan purin melalui ginjal sehingga disarankan tidak sering mengonsumsi alkohol. Pasien juga dianjurkan untuk meminum cairan dalam jumlah banyak karena jumlah air kemih sebanyak 2 liter atau lebih setiap harinya akan membantu pembuangan urat dan meminimalkan pengendapan urat dalam saluran kemih Ada beberapa jenis makanan yang diketahui kaya purin, antara lain daging, baik daging sapi, babi, kambing, jerohan, bebek, angsa, merpati, ayam, sapi atau makanan dari laut (seafood), kacangkacangan, bayam, jamur, dan kembang kol. REFERENSI 1. 2. 3. 4. 5. 6. Harper, Rodwell, Mayes, 1977, Review of Physiological Chemistry Colby, 1992, Ringkasan Biokimia Harper, Alih Bahasa: Adji Dharma, Jakarta, EGC Wirahadikusumah, 1985, Metabolisme Energi, Karbohidrat dan Lipid, Bandung, ITB Harjasasmita, 1996, Ikhtisar Biokimia Dasar B, Jakarta, FKUI Toha, 2001, Biokimia, Metabolisme biomolekul, Bandung, Alfabeta Poedjiadi, Supriyanti, 2007, dasr-Dasar Biokimia, Bandung, UI Press
Diposkan oleh dr. Suparyanto, M.Kes di 07:43 15 komentar: Link ke posting ini Kirimkan Ini lewat EmailBlogThis!Berbagi ke TwitterBerbagi ke Facebook Label: BIOKIMIA
Reaksi:
METABOLISME XENOBIOTIK
Dr. Suparyanto, M.Kes APA ITU XENOBIOTIK
Xenobiotik berasal dari bahasa Yunani: Xenos yang artinya asing Xenobiotik adalah zat asing yang masuk dalam tubuh manusia
Contoh: obat obatan, insektisida, zat kimia tambahan pada makanan (pemanis, pewarna, pengawet) dan zat karsinogen lainya MENGAPA XENOBIOTIK DI METABOLISME Xenobiotik umumnya tidak larut air, sehingga kalau masuk tubuh tidak dapat diekskresi
Untuk dapat diekskresi xenobiotik harus dimetabolisme menjadi zat yang larut, sehingga bisa diekskresi
Organ yang paaling berperan dalam metabolisme xenobiotik adalah hati Ekskresi xenobiotik melalui empedu dan urine
METABOLISME XENOBIOTIK Metabolisme xenobiotik dibagi 2 fase Fase Hidroksilasi dan Fase konjugasi Fase Hidroksilasi fase mengubah xenobiotik aktif menjadi inaktif
Fase konjugasi fase mereaksikan xenobiotik inaktik dengan zat kimia tertentu dalam tubuh menjadi zat yang larut, sehingga mudah diekresi baik lewat empedu maupun urine Fase Hidroksilasi fase mengubah xenobiotik aktif menjadi inaktif, oleh enzim Mono oksidase atau sitokrom P450 Enzim sitokrom P450 memiliki banyak di Retikulum endoplasma Fungsi enzim ini adalah sebagai katalisator perubahan Hidrogen (H) pada xenobiotik menjadi gugus hidroksil (OH) Reaksi Hidroksilasi oleh enzim sitokrom P450 adalah sbb: RH + O2 R-OH + H2O
Sitokrom P450 merupakan hemoprotein seperti Hemoglobin, banyak terdapat pada membran retikulum endoplasma sel hati Pada beberapa kondisi produk hidroksilasi bersifat mutagenik atau karsinogenik
Fase konjugasi fase mereaksikan xenobiotik inaktik dengan zat kimia tertentu dalam tubuh menjadi zat yang larut, sehingga mudah diekskresi baik lewat empedu maupun urine Zat dalam tubuh yang biasa dipergunakan untuk proses konjugasi adalah: asam glukoronat, sulfat, acetat, glutation atau asam amino tertentu Glukuronidasi: proses menkonjugasi xenobiotik dengan asam glukorunat, dengan enzim glukuronil transferase Xenobiotik yang mengalami glukorunidasi adalah: asetilaminofluoren (karsinogenik), anilin, asam benzoat, meprobamat, fenol dan senyawa steroid Sulfasi: proses konjugasi xenobiotik dengan asam sulfat, dengan enzim sulfotransferase Xenobiotik yang mengalami sulfasi adalah: alkohol, arilamina, fenol
Konjugasi dengan Glutation, yang terdiri dari tripeptida (glutamat, sistein, glisin) dan biasa disingkat GSH, menggunakan enzim glutation S-transferase atau epoksid hidrolase Xenobiotik yang berkonjugasi dengan GSH adalah xenobiotik elektrofilik (karsinogenik)
Metabolisme xenobiotik kadang disebut proses detoksifikasi, tetapi istilah ini tidak semuanya benar, sebab tidak semua xenobiotik bersifat toksik Respon metabolisme xenobiotik mencakup efek farmakologik, toksik, imunologik dan karsinogenik METABOLISME XENOBIOTIK OBAT
Pada metabolisme obat, pada obat yang sudah aktif metabolisme xenobiotik fase 1 berfungsi mengubah obat aktif menjadi inaktif, sedang paa obat yang belum aktif metabolisme xenobiotik fase 1 berfungsi mengubah obat inaktif menjadi aktif RESPON METABOLISME XENOBIOTIK
Respon metabolisme xenobiotik dapat menguntungkan karena metabolit yang dihasilkan menjadi zat yang polar sehingga dapat diekskresi keluar tubuh Respon metabolisme xenobiotik dapat merugikan karena: Berikatan dengan makromolekul dan menyebabkan cidera sel
Berikatan dengan makromolekul menjadi hapten merangsang pembentukan antibodi dan menyebabkan reaksi hipersensitivitas yang berakibat cidera sel Berikatan dengan makromolekul menjadi zat mutan yang menyebabkan timbulnya sel kanker
REFERENSI 1. 2. 3. 4. 5. 6. Harper, Rodwell, Mayes, 1977, Review of Physiological Chemistry Colby, 1992, Ringkasan Biokimia Harper, Alih Bahasa: Adji Dharma, Jakarta, EGC Wirahadikusumah, 1985, Metabolisme Energi, Karbohidrat dan Lipid, Bandung, ITB Harjasasmita, 1996, Ikhtisar Biokimia Dasar B, Jakarta, FKUI Toha, 2001, Biokimia, Metabolisme biomolekul, Bandung, Alfabeta Poedjiadi, Supriyanti, 2007, dasr-Dasar Biokimia, Bandung, UI Press
Diposkan oleh dr. Suparyanto, M.Kes di 07:38 6 komentar Link ke posting ini Kirimkan Ini lewat EmailBlogThis!Berbagi ke TwitterBerbagi ke Facebook Label: BIOKIMIA
Reaksi:
SABTU, 09 JANUARI 2010
METABOLISME PROTEIN
Dr. Suparyanto. M.Kes PROTEIN TUBUH
zat padat tubuh terdiri dari protein (otot, enzim, protein plasma, antibodi, hormon) Protein merupakan jaringan asam amino dengan ikatan peptide
Banyak protein terdiri ikatan komplek dengan fibril protein fibrosa
Macam protein fibrosa: kolagen (tendon, kartilago, tulang); elastin (arteri); keratin (rambut, kuku); dan aktin-miosin MACAM PROTEIN Peptide: 2 - 10 asam amino Polipeptide: 10 - 100 asam amino Protein:> 100 asam amino Antara asam amino saling berikatan dengan ikatan peptide Glikoprotein: gabungan glukose dengan protein Lipoprotein: gabungan lipid dan protein
Asam amino Asam amino dibedakan: asam amino esensial dan asam amino non esensial
Asam amino esensial: T2L2V HAMIF (treonin, triptofan, lisin, leusin, valin histidin, arginin, metionin, isoleusin, fenilalanin) Asam amino non esensial: SAGA SATGA (serin, alanin, glisin, asparadin sistein, asam aspartat, tirosin, glutamin, asam glutamat) TRANSPORT PROTEIN Protein diabsorpsi di usus halus dalam bentuk asam amino masuk darah Dalam darah asam amino disebar keseluruh sel untuk disimpan Didalam sel asam amino disimpan dalam bentuk protein (dengan menggunakan enzim) Hati merupakan jaringan utama untuk menyimpan dan mengolah protein
PENGGUNAAN PROTEIN UNTUK ENERGI Jika jumlah protein terus meningkat protein sel dipecah jadi asam amino untuk dijadikan energi atau disimpan dalam bentuk lemak Pemecahan protein jadi asam amino terjadi di hati dengan proses: deaminasi atau transaminasi Deaminasi: proses pembuangan gugus amino dari asam amino Transaminasi: proses perubahan asam amino menjadi asam keto
PEMECAHAN PROTEIN 1. Transaminasi:
alanin + alfa-ketoglutarat piruvat + glutamat 1. Diaminasi: asam amino + NAD + asam keto + NH3
NH3 merupakan racun bagi tubuh, tetapi tidak dapat dibuang oleh ginjal harus diubah dahulu jadi urea (di hati) agar dapat dibuang oleh ginjal Ekskresi NH3
NH3 tidak dapat diekskresi oleh ginjal NH3 harus dirubah dulu menjadi urea oleh hati
Jika hati ada kelainan (sakit) proses perubahan NH3 urea terganggu penumpukan NH3 dalam darah uremia NH3 bersifat racun meracuni otak coma Karena hati yang rusak disebut Koma hepatikum
PEMECAHAN PROTEIN Deaminasi maupun transaminasi merupakan proses perubahan protein zat yang dapat masuk kedalam siklus Krebs Zat hasil deaminasi / transaminasi yang dapat masuk siklus Krebs adalah: alfa ketoglutarat, suksinil ko-A, fumarat, oksaloasetat, sitrat
Singkatan asam amino ARG, His, Gln, Pro: arginin, Histidin, Glutamin, Proline Ile, Met, Val: isoleusin, Metionin, Valin Tyr, Phe: Tyrosin, Phenilalanin karboksikinase Ala, Cys, Gly, Hyp, Ser, Thr: alanin , Cystein, Glysin, Hydroksiprolin, Serin, Threonin Leu, Lys, Phe, Trp, Tyr: Leusin, Lysin, Phenilalanin, triptofan, Tyrosin siklus krebs
Proses perubahan Asetil ko-A H + CO2 Proses ini terjadi didalam mitokondria
Pengambilan Asetil co-A di sitoplasma dilakukan oleh: oxalo asetat proses pengambilan ini terus bertahan sampai Asetil co-A di sitoplasma habis Oksaloasetat berasal dari asam piruvat Jika asupan nutrisi kekurangan KH kurang as. Piruvat kurang oxaloasetat
RANTAI respirasi H hasil utama dari siklus Krebs ditangkap oleh carrier NAD menjadi Nadh H dari nadh ditransfer ke Flavoprotein Quinon sitokrom b sitokrom c sitokrom aa3 terus direaksikan dengan O2 H2O + E
Jaringan transfer H dari satu carrier ke carrier lainya disebut Rantai respirasi Rantai Respirasi terjadi didalam mitokondria transfer atom H antar carrier memakai enzim Dehidrogenase sedangkan reaksi H + O2 memakai enzim Oksidase Urutan carrier dalam rantai respirasi adalah: NAD Flavoprotein Quinon sitokrom b sitokrom c sitokrom aa3 direaksikan dengan O2 H2O + E fosforilasi oksidatifDalam proses rantai respirasi dihasilkan energi yang tinggi energi tsb ditangkap oleh ADP untuk menambah satu gugus fosfat menjadi ATP fosforilasi oksidatif adalah proses pengikatan fosfor menjadi ikatan berenergi tinggi dalam proses rantai respirasi fosforilasi oksidatif proses merubah ADP ATP
KREATIN DAN kreatinin Kreatin disintesa di hati dari: metionin, glisin dan arginin Dalam otot rangka difosforilasi membentuk fosforilkreatin (penyimpanan energi) istirahat Kreatin + ATP Fosforilkreatin kreatinin gerak urineREFERENSI
1. 2. 3.
Harper, Rodwell, Mayes, 1977, Review of Physiological Chemistry Colby, 1992, Ringkasan Biokimia Harper, Alih Bahasa: Adji Dharma, Jakarta, EGC Wirahadikusumah, 1985, Metabolisme Energi, Karbohidrat dan Lipid, Bandung, ITB
4. 5. 6.
Harjasasmita, 1996, Ikhtisar Biokimia dasar B, Jakarta, FKUI Toha, 2001, Biokimia, Metabolisme biomolekul, Bandung, Alfabeta Poedjiadi, Supriyanti, 2007, dasr-dasar Biokimia, Bandung, UI Press
Diposkan oleh dr. Suparyanto, M.Kes di 07:47 23 komentar: Link ke posting ini Kirimkan Ini lewat EmailBlogThis!Berbagi ke TwitterBerbagi ke Facebook Label: BIOKIMIA
Reaksi:
Metabolisme lemak (LIPID / FAT metabolism)
Dr. Suparyanto, M.Kes MACAM LEMAK
Lemak biologis yang terpenting: lemak netral (trigliserida), fosfolipid, steroid Asam lemak: 1. Asam palmitat: CH3 (CH2) 14-COOH 2. Asam stearat: CH3 (CH2) 16-COOH 3. Asam oleat: CH3 (CH2) 7CH = CH (CH2) 7COOH Trigliserida: ester gliserol + 3 asam lemak Fosfolipid: ester gliserol + 2 asam lemak + fosfat Steroid: kolesterol dan turunanya (hormon steroid, asam lemak dan vitamin)
Absorpsi LEMAK Lemak diet diserap dalam bentuk: kilomikron diabsorpsi usus halus masuk ke limfe (ductus torasikus) masuk darah Kilomikron dalam plasma disimpan dalam jaringan lemak (adiposa) dan hati Proses penyimpananya: kilomikron dipecah oleh enzim lipoprotein lipase (dalam membran sel) asam lemak dan gliserol Didalam sel asam lemak disintesis kembali jadi trigliserida (penyimpanan lemak)
MACAM LEMAK PLASMA Asam lemak bebas (FFA = free fatty acid) ada dalam plasma darah dan terikat dengan albumin Kolesterol, trigliserida dan fosfolipid dalam plasma berbentuk lipoprotein 1. Kilomikron 2. VLDL: very low density lipoprotein
3. 4. 5.
IDL: intermediate density lipoprotein LDL: low density lipoprotein HDL: high density lipoprotein
ASAM LEMAK BEBAS Bila lemak sel akan digunakan untuk energi simpanan lemak (trigliserida) dihidrolisis menjadi asam lemak dan gliserol (oleh enzim lipase sel) Asam lemak berdiffusi masuk aliran darah sebagai asam lemak bebas (Free Fatty Acid) dan berikatan dengan albumin plasma PENGGUNAAN FFA SEBAGAI ENERGI FFA dalam plasma dibawa ke mitokondria dengan carrier karnitin FFA dalam sel dipecah menjadi Asetil koenzim-A dengan beta oksidasi Asetil koenzim-A hasil beta oksidasi masuk siklus Krebs untuk diubah menjadi H dan CO2
METABOLISME LEMAK Ada 3 fase: oksidasi Siklus Kreb Fosforilasi oksidatif
1. 2. 3.
BETA OKSIDASI Proses pemutusan / perubahan asam lemak Asetil co-A
Asetil co-A terdiri 2 atom C sehingga jumlah Asetil co-A yang dihasilkan = jumlah atom C dalam rantai carbon asam lemak: 2 Misal: asam palmitat (C15H31COOH) oksidasi ?? Asetil co-A
CONTOH ASAM LEMAK NAMA UMUM RUMUS NAMA KIMIA Asam oleat C17H33COOH Oktadeca 9enoad As risinoleat C17H32 (OH)-COOH 12 hidroksi okladeca-9-enoad Asam linoleat C17H31COOH Okladeca-9, 12 dienoad As linolenat C17H29COOH Okladeca-9, 12,15 trienoad As araksidat C19H39COOH Asam eicosanoad siklus krebs
Proses perubahan Asetil ko-A H + CO2 Proses ini terjadi didalam mitokondria
Pengambilan Asetil co-A di sitoplasma dilakukan oleh: oxalo asetat proses pengambilan ini terus bertahan sampai Asetil co-A di sitoplasma habis Oksaloasetat berasal dari asam piruvat Jika asupan nutrisi kekurangan KH kurang as. Piruvat kurang oxaloasetat
Ketosis Degradasi asam lemak Asetil koa terjadi di Hati, tetapi hati hanya mengunakan sedikit Asetil koa akibatnya sisa Asetil koa berkondensasi membentuk Asam Asetoasetat Asam asetoasetat merupakan senyawa labil yang mudah pecah menjadi: Asam hidroksibutirat dan aseton. Ketiga senyawa diatas (asam asetoasetat, asam hidroksibutirat dan aseton) disebut BADAN keton. Adanya badan keton dalam sirkulasi darah disebut: ketosis
Ketosis terjadi saat tubuh kekurangan karbohidrat dalam asupan makannya kekurangan oksaloasetat Jika Oksaloasetat menurun maka terjadi penumpukan Asetil koa didalam aliran darah jadi badan keton keadaan ini disebut ketosis Badan keton merupakan racun bagi otak mengakibatkan Coma, karena sering terjadi pada penderita DM disebut Koma Diabetikum Ketosis terjadi pada kondisi: Kelaparan Diabetes Melitus Diet tinggi lemak, rendah karbohidrat
RANTAI respirasi H adalah hasil utama dari siklus Krebs ditangkap oleh carrier NAD menjadi Nadh
H dari nadh ditransfer ke Flavoprotein Quinon sitokrom b sitokrom c sitokrom aa3 terus direaksikan dengan O2 H2O + Energi Jaringan transfer H dari satu carrier ke carrier lainya disebut Rantai respirasi Rantai Respirasi terjadi didalam mitokondria transfer atom H antar carrier memakai enzim Dehidrogenase sedangkan reaksi H + O2 memakai enzim Oksidase
Urutan carrier dalam rantai respirasi adalah: NAD Flavoprotein Quinon sitokrom b sitokrom c sitokrom aa3 direaksikan dengan O2 H2O + Energi fosforilasi oksidatif
Dalam proses rantai respirasi dihasilkan energi yang tinggi energi tsb ditangkap oleh ADP untuk menambah satu gugus fosfat menjadi ATP Fosforilasi oksidatif adalah proses pengikatan fosfor menjadi ikatan berenergi tinggi dalam proses rantai respirasi Fosforilasi oksidatif proses merubah ADP ATP (dengan menngunakan energi hasil reaksi H2 + O2 H2O + E)
Sintesis trigliserida dari karbohidrat Bila KH dalam asupan banyak dari yang dibutuhkan KH diubah jadi glikogen dan kelebihanya diubah jadi trigliserida disimpan dalam jaringan adiposa Tempat sintesis di hati, kemudian ditransport oleh lipoprotein ke jaringan disimpan di jaringan adiposa sampai siap digunakan tubuh Sintesis trigliserida DARI PROTEIN Banyak asam amino dapat diubah menjadi Asetil koenzim-A Dari Asetil koenzim-A dapat diubah menjadi trigliserida
Jadi saat asupan protein berlebih, kelebihan asam amino disimpan dalam bentuk lemak di jaringan adipose PENGATURAN HORMON ATAS PENGGUNAAN LEMAK Penggunaan lemak tubuh terjadi pada saat kita gerak badan berat Gerak badan berat menyebabkan pelepasan epineprin dan nor epineprin
Kedua hormon diatas mengaktifkan lipase trigliserida yang sensitif hormon pemecahan trigliserida asam lemak Asam lemak bebas (FFA) dilepas ke darah dan siap untuk dirubah jadi energi
Arteriosklerosis Jika kadar kolesterol tinggi dalam darah endapan lipid yang disebut: plak ateroma / endapan kolesterol Pada stadium penyakit fibroblast menginfiltrasi ateroma sklerosis Ca juga mengendap bersama plak kalsifikasi Kedua proses diatas menyebabkan arteri menjadi sangat keras arteriosklerosis Arteriosklerosis menyebabkan vaskuler mudah pecah Dinding vaskuler arteriosklerosis kasar menyebabkan tombus dan emboli Efek samping: darah tinggi, PJK, trombus stroke emboli
REFERENSI 1. 2. 3. 4. 5. 6. Harper, Rodwell, Mayes, 1977, Review of Physiological Chemistry Colby, 1992, Ringkasan Biokimia Harper, Alih Bahasa: Adji Dharma, Jakarta, EGC Wirahadikusumah, 1985, Metabolisme Energi, Karbohidrat dan Lipid, Bandung, ITB Harjasasmita, 1996, Ikhtisar Biokimia dasar B, Jakarta, FKUI Toha, 2001, Biokimia, Metabolisme biomolekul, Bandung, Alfabeta Poedjiadi, Supriyanti, 2007, dasr-dasar Biokimia, Bandung, UI Press
Diposkan oleh dr. Suparyanto, M.Kes di 06:42 16 komentar: Link ke posting ini Kirimkan Ini lewat EmailBlogThis!Berbagi ke TwitterBerbagi ke Facebook Label: BIOKIMIA
Reaksi:
Metabolisme karbohidrat (Carbohydrate Metabolism)
Dr. Suparyanto, M.Kes APA ITU pencernakan
Pencernakan: proses pemecahan makanan dari bentuk komplek menjadi bentuk sederhana Karbohidrat: dari polisakarida dirubah menjadi Monosakarida (galaktose, fruktose, glukose) Glukose merupakan Monosakarida terbanyak dalam sirkulasi (70 - 110 mg / ml)
Galaktose dan fruktose dikonversi oleh hati dengan enzim yang sesuai menjadi glukose, kemudian masuk sirkulasi Metabolisme karbohidrat Terdiri 3 fase:
1. 2. 3.
Glikolisis Siklus Kreb Fosforilasi oksidatif
Glikolisis Proses perubahan glukose menjadi asam piruvat atau Asetil coenzim-A Glikolisis terjadi di sitoplasma
Glukose tidak dapat langsung diffusi ke sel Glukose harus berikatan dulu dengan carrier: G + C GC GC dapat berdiffusi kedalam sel
Didalam sel GC G + C C keluar sel lagi untuk mengikat G yang lain sampai semua G masuk sel
Proses ini dipercepat oleh H. Insulin, jika H. Insulin kurang proses masuknya G kedalam sel lambat G menumpuk didalam darah DM G di sitoplasma mengalami fosforilasi glukose 6-PO4 (enzim glukokinase) Fruktokinase fruktose fruktose 6-PO4 Galaktokinase galaktose galaktose 6-PO4
Glikolisis: proses perubahan glukose menjadi asam piruvat atau asam laktat Glikolisis terdiri 2 lintasan:
Katabolisme glukosa (glikolisis) melalui triose (dihidroksi aseton fosfat atau gliseraldehid 3-PO4) disebut lintasan Embden Meyerhof Katabolisme glukosa (glikolisis) melalui 6-fosfoglukonat disebut lintasan oksidatif langsung (pintas heksosmonofosfat)
Siklus krebs Proses perubahan Asetil co-A H Proses ini terjadi didalam mitokondria
Pengambilan Asetil co-A di sitoplasma dilakukan oleh: oxalo asetat proses pengambilan ini terus bertahan sampai Asetil co-A di sitoplasma habis
Jika dalam asupan nutrisi kekurangan KH akan kekurangan oxaloasetat
Kekurangan oxaloasetat pengambilan Asetil co-A di sitoplasma terhambat Asetil co-A menumpuk di sitoplasma Penumpukan Asetil co-A berikatan sesama Asetil co-A asam aseto asetat Asam aseto asetat senyawa tidak setabil mudah mengurai: aseton + asam hidroksi butirat
Ketiga senyawa: asam aseto asetat, aseton dan asam hidroksi butirat disebut Badan Keton Meningkatnya badan keton dalam darah ketosis
Badan keton bersifat racun bagi otak koma, karena biasanya terdapat pada penderita DM koma diabeticum Fosforilasi oksidatif Dalam proses rantai respirasi dihasilkan energi yang tinggi energi tsb ditangkap oleh senyawa yang disebut ATP Fosforilasi oksidatif adalah proses pengikatan fosfor menjadi ikatan berenergi tinggi dalam proses rantai respirasi
Fosforilasi oksidatif: proses perubahan ADP ATP dengan cara mengambil energi yang dihasilkan Rantai Respirasi (reaksi H + O2 H2O)
RINGKASAN metabolisme karbohidrat Glikolisis: perubahan glukose asam piruvat R / Glukose + 2 ADP + 2 PO4 2 asam piruvat + 2 ATP + 4 H Hasil utama glikolisis: asam piruvat Energi dihasilkan: 2 ATP Tempat reaksi glikolisis: sitoplasma Terdiri 2 lintasan: Embden Meyerhof dan Heksosmonofosfat Siklus Kreb: perubahan Asetil co-A H R / 2 Asetil Ko-A + 6 H2O + 2 ADP 4 CO2 + 16 H + 2 Ko-A + 2 ATP Hasil utama: H Energi dihasilkan: 2 ATP
Tempat berlangsung: mitokondria
Sisa metabolisme CO2 berasal dari hasil samping Siklus Krebs / Siklus Asam Sitrat / Siklus Asam Trikarboksilat Fosforilasi oksidatif: proses perubahan ADP ATP dengan cara mengambil energi yang dihasilkan Rantai Respirasi (reaksi H + O2 H2O) R / 2 H + O2 + 2e + ADP H2O + ATP Energi yang dihasilkan: 34 ATP Total hasil energi metabolisme karbohidrat: 38 ATP
REFERENSI 1. 2. 3. 4. 5. 6. Harper, Rodwell, Mayes, 1977, Review of Physiological Chemistry Colby, 1992, Ringkasan Biokimia Harper, Alih Bahasa: Adji Dharma, Jakarta, EGC Wirahadikusumah, 1985, Metabolisme Energi, Karbohidrat dan Lipid, Bandung, ITB Harjasasmita, 1996, Ikhtisar Biokimia dasar B, Jakarta, FKUI Toha, 2001, Biokimia, Metabolisme biomolekul, Bandung, Alfabeta Poedjiadi, Supriyanti, 2007, dasr-dasar Biokimia, Bandung, UI Press
FISIOLOGI METABOLISME
Dr. Suparyanto, M.Kes
Apa Itu Metabolisme Metabolisme adalah suatu proses komplek perubahan makanan menjadi energi dan panas melalui proses fisika dan kimia, berupa proses pembentukan dan penguraian zat didalam tubuh organisme untuk kelangsungan hidupnya. Macam Metabolisme Metabolisme dibedakan 2 macam : sel. Katabolisme : proses penguraian makanan menjadi energi, yang terjadi pada proses respirasi
Anabolisme : proses pembentukan (sintesa) zat organik komplek yang berasal dari zat yang lebih sederhana Contoh Metabolisme Contoh Katabolisme : Glikogenolisis : proses pemecahan glikogen menjadi glukose Glikolisis : proses pemecahan glukose menjadi asam piruvat
Contoh Anabolisme : Glikogenesis : proses pembentukan glikogen dari glukose Glikoneogenesis : proses pembentukan glukose dari prtein atau lemak
Alur Metabolisme
Hasil Metabolisme Hasil metabolisme berupa energi dan panas energi tersebut belum dapat digunakan langsung oleh sel berikatan adenin, fosfat dan ribose ATP (Adenosin Tri Fosfat). ATP tersebut merupakan simpanan energi siap digunakan oleh sel untuk : transport membran, sintesis senyawa kimia, kerja mekanik. Jika sel memerlukan energi, maka energi diambil dari ATP dengan cara melepas satu gugus fosfat menjadi ADP (Adenosin Di Phosfat) dengan melepas 8.000 kalori. Penggunaan ATP ATP ADP + PO4 + 8.000 kalori ADP AMP + PO4 + 8.000 kalori
AMP sudah tidak dapat mengeluarkan energi lagi harus diisi lagi dengan energi baru yang berasal dari metabolisme makanan menjadi ATP. Metabolisme proses merubah makanan ATP Kreatin + ATP Fosforil kreatin + ADP
Kreatin di otot dalam keadaan istirahat mampu mengikat ATP menjadi Fosforil kreatin (simpanan energi) Jika otot perlu energi untuk gerak maka fosforil kreatin dipecah Kreatin + ATP. ATP inilah yang digunakan untuk gerak
Fase Metabolisme Karbohidrat Glikolisis proses merubah glukose asetil Co-A Siklus Kreb proses merubah asetil Co-A H
Fosforilasi Oksidatif proses mereaksikan H + O H2O + ATP
Glikolisis Glikolisis: glukose asam piruvat/ asetil co-A
R/ Glukose + 2 ADP + 2 PO4 2 Asam Piruvat + 2 ATP + 4 H Hasil akhir glikolisis: Asam piruvat / Acetil co-A 2 ATP
Siklus Asam Sitrat Siklus Kreb: asetil co-A H R/ 2 Asetil Ko-A + 6 H2O + 2 ADP 4 CO2 + 16 H + 2 Ko-A + 2 ATP Hasil utama: H (hidrogen) dan 2ATP
Fosforilasi Oksidatif Rantai Respirasi transfer H dari satu karier ke karier lainya dengan enzim dehidrogenase H + O2 H2O + ATP R/ 2 H + O2 + 2e + ADP H2O + ATP ATP hasil fosforilasi oksidatif = 34 ATP
Metabolisme Lemak Ada 3 fase: oksidasi proses merubah asam lemak asetil Co-A Siklus Kreb proses merubah asetil Co-A H Fosforilasi Oksidatif proses mereaksikan H + O H2O + ATP
Metabolisme Protein Ada 3 tahap Deaminasi proses merubah asam amino asetil Co-A Siklus Kreb proses merubah asetil Co-A H Fosforilasi Oksidatif proses mereaksikan H + O H2O + ATP
Keseimbangan Energi Energi didalam tubuh kita dikatakan seimbang, jika jumlah energi yang masuk melalui makanan sama besar dengan jumlah energi yang dikeluarkan untuk kelangsungan hidup Basal Metabolisme Rate (BMR) Basal Metabolisme Rate ( BMR ) : adalah keadaan metabolisme tubuh dalam keadaan istirahat fisik maupun mental
Jadi dalam keadaan BMR, diperlukan jumlah tenaga minimal untuk kelangsungan hidup yang terpenting : gerak nafas, suhu tubuh, sirkulasi darah. BMR rata rata: 2.000 kalori / hari,
Kebutuhan energi manusia > 2.000 kalori / hari yang dipergunakan untuk: BMR, kegiatan fisik dan SDA SDA( Specifik Dinamic Action ) yaitu energi yang dibutuhkan untuk metabolisme makanan Laju metabolik jumlah tenaga yang dibebaskan per satuan waktu
Cara Pengukuran BMR Tidak makan minimal 12 jam Tidur nyenyak semalam Tanpa gerak badan setelah tidur Menghilangkan faktor psikis dan fisik yang merangsang metabolisme Suhu harus nyaman ( 25 300 C )
Faktor BMR 1. 2. 3. 4. 5. 6. 7. 8. 9. Gerak badan Makan / minum Suhu lingkungan Tinggi badan, Berat badan Jenis kelamin Suhu tubuh Kehamilan, menstruasi Hormon tiroid Hormon epineprin dan nonepineprin
Cara Menghitung Kebutuhan Energi Untuk menghitung kebutuhan energi seseorang, maka harus diketahui BMR nya dan kegiatan fisiknya, dan untuk memperkirakan jumlah energi yang diperlukan dapat dihitung dengan menggunakan rumus berikut Rumus BMR
Energi Aktivitas Fisik
Suhu Tubuh Suhu tubuh normal rata rata per oral = 37oC (36,40C - 37,2OC). Kehilangan panas tubuh melalui cara: Radiasi : 60 % Konduksi ke tempat lain : 3 % Konveksi ke udara: 15 % Evaporasi: 22 %
Perpindahan Panas Konduksi perpindahan kalor melalui suatu medium, tanpa disertai perpindahan partikel medium tersebut Misal: perpindahan panas tubuh ke kursi Konveksi: perpindahan kalor melalui suatu medium, yang disertai perpindahan partikel medium tersebut Misal: perpindahan panas tubuh ke udara Radiasi perpindahan panas tanpa melalui medium, dalam bentuk gelombang elektromagnetik Misal: sinar, sinar gama, sinar X, sinar infra merah Evaporasi perpindahan panas melalui penguapan Misal: penguapan keringat memerlukan kalori
Keseimbangan Panas Panas secara terus menerus dihasilkan oleh tubuh sebagai hasil sampingan metabolisme, dan panas juga dibuang ke lingkungan sekitar. Bila kecepatan pembentukan panas tepat sama dengan kehilangan panas maka tubuh dalam keadaan keseimbangan panas. Tetapi bila keduanya diluar keseimbangan, maka suhu tubuh akan meningkat atau menurun. Jika suhu tubuh > suhu lingkungan panas akan hilang dengan cara radiasi dan konduksi
Jika suhu tubuh < suhu lingkungan tubuh dapat panas dari radiasi dan konduksi lingkungan membuang panas dengan Evaporasi. Pengaturan Suhu Tubuh Pusat pengatur suhu tubuh Termostat Hipotalamus Reseptor suhu tubuh : Neuron di area Preoptika Hipotalamus Reseptor suhu kulit Reseptor suhu didalam Medulla spinalis, Abdomen.
Mekanisme Pembuangan Panas Perangsangan kelenjar keringat pembuangan panas secara penguapan.
Menghambat pusat simpatis di Hipotalamus posterior, sehingga menghilangkan tonus vasokonstriksi normal pada pembuluh kulit terjadi vasodilatasi dan kehilangan banyak panas dari tubuh Mekanisme Pembentukan Panas Vasokonstriksi pada kulit mencegah konduksi panas dari dalam tubuh ke kulit.
Piloereksi rambut berdiri membentuk isolator pada kulit, efek ini tidak begitu penting pada manusia. Peniadaan keringat penguapan terhenti.
Peningkatan pembentukan panas :
Menggigil (Pusat motorik efek menggigil terletak pada bagian Dorsomedial Hipotalamus Posterior) Peningkatan rangsangan simpatis pembentukan panas Hormon epinefrin dan norepinefrin meningkatkan metabolisme. Peningkatan pengeluaran Hormon Tiroksin meningkatkan metabolisme.
Fisiologi Demam Demam adalah suhu tubuh diatas batas normal biasa, yang disebabkan oleh zat toksik (Pirogen), penyakit bakteri, tumor otak, atau dehidrasi yang mempengaruhi pusat pengaturan suhu (termostat hipotalamus). Pirogen tsb merangsang termostat hipotalamus, untuk di set pada suhu yang lebih tinggi
Karena suhu tubuh lebih rendah dari pada setelan ( set ) termostat hipotalamus maka terjadi peningkatan suhu tubuh dan terjadilah demam (diatas normal) sampai mencapai suhu kritis (38,6OC) Pada suhu kritis tsb (38,6OC) maka tubuh berusaha men-set termostat hipotalamus pada suhu normal (37OC) maka terjadi vasodilatasi, dan berkeringat. Perubahan peristiwa yang mendadak pada demam dari suhu kritis menuju normal disebut Kritis atau FLUSH Bila suhu tubuh meningkat sampai melebihi 40,5OC terjadi sengatan panas (HEAD STROKE) dengan gejala : dizziness, distress abdomen, delirium, kehilangan kesadaran. Obat anti Piretik (Aspirin) mempunyai kasiat menurunkan panas, dengan jalan menurunkan penyetelan termostat hipotalamus (kebalikan efek Pirogen).
PENGANTAR METABOLISME (Introduction of Metabolism)
Dr. Suparyanto, M.Kes APA ITU METABOLISME Metabolisme = perubahan Metabolisme: semua proses perubahan kimia dan tenaga (energi) yang terjadi didalam tubuh
Metabolisme adalah suatu proses komplek perubahan makanan menjadi energi dan panas melalui proses fisika dan kimia, berupa proses pembentukan dan penguraian zat didalam tubuh organisme untuk kelangsungan hidupnya.
MACAM METABOLISME Metabolisme dibedakan 2 macam: 1. Katabolisme : proses penguraian/ pemecahan makanan menjadi energi, yang terjadi pada proses respirasi sel. 2. Anabolisme : proses pembentukan (sintesa) zat organik komplek yang berasal dari zat yang lebih sederhana CONTOH KATABOLISME Glikogenolisis : proses pemecahan glikogen menjadi glukose
Glikogen merupakan simpanan karbohidrat (sumber energi), disimpan di semua sel, terbanyak di hati dan otot Pada saat kurang makan dipecah jadi energi Glikolisis : proses pemecahan glukose menjadi asam piruvat Glikolisis terjadi dlm sitoplasma Glikolisis merupakan metabolisme antara pembentukan energi
CONTOH ANABOLISME Glikogenesis : proses pembentukan glikogen dari glukose Glikogenesis terjadi pada saat kita kelebihan makanan Glikoneogenesis : proses pembentukan glukose dari protein atau lemak Glikoneogenesis terjadi pada saat kita kekurangan karbohidrat (sumber energi)
HASIL METABOLISME Metabolisme makanan menghasilkan energi yang disebut ATP (Adenosin Tri Fosfat).
ATP merupakan senyawa yang terdiri dari 3 gugus yaitu: Adenin (asam amino), ribose (senyawa karbohidrat) dan fosfat. ATP merupakan simpanan energi (hasil metabolisme sel) yang siap digunakan sel untuk kelangsungan hidup: transport membran, sintesis senyawa kimia, kerja mekanik. Jika sel memerlukan energi, maka energi diambil dari ATP dengan cara melepas satu gugus fosfat menjadi ADP ( Adenosin Di Phosfat ) dengan melepas 8.000 kalori. PENGGUNAAN ATP ATP ADP + PO4 + 8.000 kalori
ADP masih dapat melepas satu gugus Fosfat lagi ADP AMP + PO4 + 8.000 kalori AMP (Adenosin Mono Phospat ) sudah tidak dapat mengeluarkan energi lagi.
Untuk itu AMP harus diisi lagi dengan energi baru yang berasal dari metabolisme makanan menjadi ATP. AMP ADP ATP
ATP (hasil metabolisme makanan) didalam otot diikat oleh kreatin (rangkaian asam amino metionin, glisin dan arginin) menjadi simpanan energi yang disebut fosforil kreatin Kreatin + ATP Fosforil kreatin + ADP Jika otot perlu energi untuk gerak maka fosforil kreatin dipecah Kreatin + ATP. ATP inilah yang digunakan untuk gerak
METABOLISME KARBOHIDRAT Terdiri 3 fase: 1. 2. 3.
Glikolisis Siklus Kreb Fosforilasi Oksidatif
METABOLISME LEMAK Terdiri 3 fase: 1. 2. 3. oksidasi Siklus Kreb Fosforilasi Oksidatif
METABOLISME PROTEIN Terdiri 3 fase 1. 2. 3.
Deaminasi Siklus Kreb Fosforilasi oksidatif
TAHAP PERTAMA METABOLISME KARBOHIDRAT Glikolisis: proses perubahan glukose menjadi asam piruvat atau asetil ko-enzim A Glikolisis merupakan proses awal metabolisme karbohidrat Glikolisis terjadi didalam sitoplasma sel, dan telah menghasilkan 2 ATP Glukose asam piruvat + 2 ATP
TAHAP PERTAMA METABOLISME LEMAK A Beta oksidasi: proses pemecahan lemak menjadi asetil koenzim-A Asetil koenzim-A adalah senyawa organik yang mempunyai 2 rantai karbon Beta oksidasi memecah lemak (rantai C yang panjang) menjadi asetil koenzim-A (2 rantai C) Lemak dengan x rantai carbon akan dipecah dengan beta oksidasi menjadi: (x/2) asetil koenzim-
TAHAP PERTAMA METABOLISME PROTEIN Deaminasi: proses pembuangan gugus amino dari asam amino Asam -ketoglutarat + Asam Amino Asam keto + Asam Glutamat + NH3
Deaminasi adalah proses pengambilan gugus amino dari asam amino menjadi zat yang dapat masuk siklus Krebs Zat yang dapat masuk siklus Krebs adalah: asam alfa keto glutarat, suksinil koenzim-A, asam fumarat, oksaloasetat, asam sitrat SIKLUS KREB Proses perubahan asetil ko-A H + CO2 Proses ini terjadi didalam mitokondria
Pengambilan asetil co-A di sitoplasma dilakukan oleh: oxalo asetat , proses pengambilan ini terus berlangsung sampai asetil co-A di sitoplasma habis Oksaloasetat berasal dari asam piruvat Jika asupan nutrisi kekurangan Karbohidrat, akan menyebabkan kurang asam. piruvat yang juga akan mengakibatkan kekurangan oxaloasetat
RANTAI RESPIRASI H hasil utama dari siklus Krebs ditangkap oleh carrier NAD menjadi NADH
H dari NADH Flavoprotein Quinon sitokrom c sitokrom b sitokrom aa3 terus direaksikan dengan O2 H2O Rangkaian transfer H dari satu carrier ke carrier lainya disebut Rantai respirasi Proses ini terjadi didalam mitokondria transfer atom H antar carrier memakai enzim Dehidrogenase sedangkan reaksi H + O2 memakai enzim Oksidase
FOSFORILASI OKSIDATIF Dalam proses rantai respirasi dihasilkan energi yang tinggi, energi tsb ditangkap oleh senyawa yang disebut ATP Fosforilasi oksidatif adalah proses pengikatan fosfor menjadi ikatan berenergi tinggi dalam proses rantai respirasi Fosforilasi oksidatif adalah proses merubah ADP menjadi ATP
REFERENSI 1. 2. 3. 4. 5. 6. Harper, Rodwell, Mayes, 1977, Review of Physiological Chemistry Colby, 1992, Ringkasan Biokimia Harper, Alih Bahasa: Adji Dharma, Jakarta, EGC Wirahadikusumah, 1985, Metabolisme Energi, Karbohidrat dan Lipid, Bandung, ITB Harjasasmita, 1996, Ikhtisar Biokimia dasar B, Jakarta, FKUI Toha, 2001, Biokimia, Metabolisme Biomolekul, Bandung, Alfabeta Poedjiadi, Supriyanti, 2007, Dasr-dasar Biokimia, Bandung, UI Press
ENZIM BIOKIMIA (Enzyme Biochemistry)
Dr. Suparyanto, M.Kes APA ITU ENZIM
Enzim adalah biokatalisator yang mengatur kecepatan berlangsungnya semua proses fisiologis (reaksi kimia dalam tubuh) Tanpa adanya enzim, kehidupan tidak pernah ada, karena semua reaksi kimia dalam tubuh membutuhkan enzim Kegagalan tubuh mensintesa enzim dapat menimbulkan penyakit bahkan kematian Contoh: perubahan amoniak urea
Enzim tersusun dari komponen protein yang disebut apoenzim Beberapa enzim membutuhkan komponen non protein yang disebut kofaktor Enzim yang terikat dengan kofaktor disebut holoenzim
Isoenzim: suatu zat yang bentuk molekulnya berbeda dengan enzim, tetapi fungsinya sama dengan enzim Koenzim adalah substrat yang mengaktifkan kerja enzim Koenzim banyak yang merupakan derivat vitamin B defisiensi vit. B mengganggu kerja enzim SIFAT UMUM ENZIM
Enzim adalah protein Enzim bekerja secara spesifik Enzim berfungsi sebagai biokatalis Enzim diperlukan dalam jumlah sedikit Enzim dapat bekerja secara bolak-balik Enzim dipengaruhi faktor lingkungan (suhu, pH, aktivator, inhibitor, konsentrasi substrat)
MACAM ENZIM
Oksidoreduktase: enzim yang cara kerjanya berdasar reaksi oksidasi dan reduksi Oksidasi: reaksi yang mengeluarkan elektron H H + + e Reduksi: reaksi yang membutuhkan elektron Cl + e Cl Transferase: enzim yang mengkalisis reaksi transfer / pertukaran dua gugus dalam dua zat Contoh: R-OH + R'-NH2 R-NH2 + R'-OH
Hydrolase: enzim yang mempercepat proses pemecahan suatu zat dengan cara direaksikan dengan air (hidrolisis) Contoh: AB + H2O A-OH + HB
Lyase: enzim yang memecah dua zat menjadi dua komponen AB A + B Isomerase: enzim yang mengkatalisis perubah suatu zat dari Isomer ke Isomer lainnya Isomer: suatu zat yang RM sama tetapi RB berbeda Contoh Isomerase: Arabinose ribose Lygase: enzim yang mengkatalisis pemutusan formasi ikatan gugus suatu zat Contoh: C = O, C-OH, COC, C-COOH, CS, CN atau CC
Enzim Oksidase: enzim yang mengkatalisis produksi hidrogen (H2) dari substrat dengan menggunakan oksigen (O2) sebagai akseptor hidrogen
AH2 + O2 A + H2O Enzim tersebut membentuk air (H2O) atau hidrogen peroksida (H2O2) sebagai produk
reaksi
Enzim Dehidrogenase: enzim yang mengeluarkan hidrogen dari suatu substrat dengan menggunakan carier sebagai akseptor hirogen, tidak dapat menggunakan oksigen sebagai akseptor hidrogen AH2 + B A + BH2
Enzim Hidroperoksidase: enzim yang mengeluarkan unsur oksigen dari substrat hidrogen peroksida (H2O2) Contoh: o Peroksidase o Katalase
Enzim Oksigenase: enzim yang mengkatalisis reaksi suatu substrat dengan oksigen (O2) A + O2 AO2
FAKTOR YANG MEMPENGARUHI ENZIM
Kerja enzim dipengaruhi oleh: Temperatur, makin tinggi makin cepat, sampai suhu optimal, diatas suhu optimal menurunkan kecepatan pH, optimal pada pH: 5 - 9 Konsentrasi enzim: penambahan kosentrasi tidak menambah kecepatan (yang penting ada) Konsentrasi substrat: makin tinggi makin cepat Inhibitor: menghambat reaksi TUGAS INDIVIDU 1. 2. 3. 4. Apa yang dimaksud dengan enzim Apa beda enzim dengan katalisator Mengapa tanpa adanya enzim, kehidupan tidak pernah ada Apa yang dimaksud dengan: 1. Apoenzim 2. Holoenzim 3. Koenzim 4. isoenzim Sebutkan sifat2 enzim Sebutkan faktor yang mempengaruhi kerja enzim Sebutkan fungsi enzim berikut: 1. Transferase 2. Hidrolase 3. Oksidoreduktase 4. Lygase Apa beda enzim dehidrogenase dengan enzim oksidase Apa beda enzim oksidase dengan enzim oksigenase
5. 6. 7.
8. 9. REFERENSI 1. 2. EGC 3. ITB 4. 5.
Harper, Rodwell, Mayes, 1977, Review of Physiological Chemistry Colby, 1992, Ringkasan Biokimia Harper, Alih Bahasa: Adji Dharma, Jakarta, Wirahadikusumah, 1985, Metabolisme Energi, Karbohidrat dan Lipid,Bandung, Harjasasmita, 1996, Ikhtisar Biokimia dasar B, Jakarta, FKUI Toha, 2001, Biokimia, Metabolisme biomolekul, Bandung, Alfabeta
Ada 4 kelas molekul utama dalam biokimia yaitu: karbohidrat , lipid , protein , dan asam nukleat . Banyak molekul biologi merupakan "polimer": dalam kasus ini, monomer adalah mikromolekul yang relatif kecil yang bergabung menjadi satu untuk membentukmakromolekul -makromolekul, yang kemudian disebut sebagai "polimer". Ketika banyak monomer bergabung untuk mensintesis sebuah polimer biologis , mereka melalui proses / tahap yang disebut dengan sintesis dehidrasi .
Karbohidrat
Artikel utama untuk bagian ini adalah: Karbohidrat , Monosakarida , disakarida , dan polisakarida
Molekul sukrosa(glukosa + fruktosa), sebuah disakarida .
Karbohidrat tersusun dari monomer yang disebut sebagai Monosakarida . Contoh dari Monosakarida adalahglukosa (C 6 H 12 O 6 ), fruktosa (C 6 H 12 O 6 ), dan deoksiribosa (C 5 H 10 O 4 ). Ketika 2 Monosakarida melalui proses sintesis dehidrasi, maka air akan terbentuk, karena 2 atom hidrogen dan satu atom oksigentelepas dari 2 gugus hidroksil Monosakarida. [ sunting ]Lipid Artikel utama untuk bagian ini adalah: Lipid , gliserol , dan Asam lemak
Sebuah trigliserida dengan satu molekul gliserol ( kiri ) dan 3 molekul asam lemak.
Lipid biasanya terbentuk dari satu molekul gliserol yang bergabung dengan molekul lain. Di trigliserida , ada satu mol gliserol dan tiga molekul asam lemak . Asam lemak merupakan monomer disini. Lipid, terutama fosfolipid , juga digunakan di beberapa produk obat-obatan, misalnya sebagai bahan pelarut (misalnya di infus parenteral ) atau sebagai komponen pembawa obat (misalnya di liposom atautransfersom ). [ sunting ]Protein Artikel utama untuk bagian ini adalah: Protein dan Asam amino
Struktur umum dari asam -amino, dengan grup aminodi sebelah kiri dan grup karboksil di sebelah kanan.
Protein merupakan molekul yang sangat besar-atau makrobiopolimer-yang tersusun dari monomer yang disebutasam amino . Ada 20 asam amino standar , yang masing-masing terdiri dari sebuah gugus karboksil , sebuahgugus amino , dan rantai samping (disebut sebagai grup "R"). Grup "R" ini yang menjadikan setiap asam amino berbeda, dan fitur-fitur dari rantai samping ini akan berpengaruh keseluruhan terhadap suatu protein. Ketika asam amino bergabung, mereka membentuk ikatan khusus yang disebut ikatan peptida melalui sintesis dehidrasi, dan menjadi Polipeptida , atau protein. [ sunting ]Asam
nukleat
Artikel utama untuk bagian ini adalah: Asam nukleat , DNA , RNA , dan Nukleotida
Struktur dari asam deoksiribosa nukleat (DNA), gambar ini menunjukkan monomernya diletakkan bersamaan.
Asam nukleat adalah molekul yang membentuk DNA , substansi yang sangat penting yang digunakan oleh semua organisme seluler untuk menyimpan informasi genetik. Jenis asam nukleat yang paling umum adalah asam deoksiribosa nukleat dan asam ribonukleat . Monomernya disebut nukleotida . Nukleotida yang paling umum diantaranyaAdenin , Sitosin , guanin , timin , dan Urasil . Adenin berpasangan dengan timin dan urasil, timin hanya berpasangan dengan adenin; sitosin dan guanin hanya dapat berpasangan satu sama lain.
Vous aimerez peut-être aussi
- Suhu Dan MetabolismeDocument182 pagesSuhu Dan MetabolismeFanny Silvira OktarinaPas encore d'évaluation
- FORMAT ASkep Transkultural NursingDocument2 pagesFORMAT ASkep Transkultural NursingTafrihatul FauziPas encore d'évaluation
- Hubungan Sistem Limfatik Dengan Keseimbangan Cairan TubuhDocument5 pagesHubungan Sistem Limfatik Dengan Keseimbangan Cairan Tubuhdevi yuliantiPas encore d'évaluation
- Virus Dengue dan Mekanisme Penularannya melalui Nyamuk Aedes AegyptyDocument1 pageVirus Dengue dan Mekanisme Penularannya melalui Nyamuk Aedes AegyptySanti SantiPas encore d'évaluation
- Adaptasi Fisiologi Dan Psikologis Wanita HamilDocument28 pagesAdaptasi Fisiologi Dan Psikologis Wanita HamildianPas encore d'évaluation
- MODEL PENDOKUMENTASIAN ASUHAN KEPERAWATAN - 2020 PDF 13-Apr-2020 06-03-58-DikonversiDocument14 pagesMODEL PENDOKUMENTASIAN ASUHAN KEPERAWATAN - 2020 PDF 13-Apr-2020 06-03-58-DikonversiRizky KhoirulPas encore d'évaluation
- BEDSIDE TEACHING PROPOSALDocument7 pagesBEDSIDE TEACHING PROPOSAL201702075Nur Vika Indah SariPas encore d'évaluation
- Penerapan Fisika MedisDocument14 pagesPenerapan Fisika MedismdrasyiddPas encore d'évaluation
- Memandikan BayiDocument17 pagesMemandikan Bayisidessy26Pas encore d'évaluation
- Jaringan Dan Sistem Tubuh ManusiaDocument13 pagesJaringan Dan Sistem Tubuh ManusiaNur BaetyPas encore d'évaluation
- Pengaturan SuhuTubuhDocument3 pagesPengaturan SuhuTubuhOctadio Eka Bayu putraPas encore d'évaluation
- Chapter 8Document45 pagesChapter 8Arista AnggrainiPas encore d'évaluation
- Keperawatan Dan AntropologiDocument26 pagesKeperawatan Dan AntropologiFADJRIPas encore d'évaluation
- Biomedik Kel 1Document21 pagesBiomedik Kel 1Rila Halimatu100% (1)
- Modul Konsep Dasar Keperawatan LengkapDocument70 pagesModul Konsep Dasar Keperawatan LengkapDINAPas encore d'évaluation
- 4 - Tanggung Jawab Dan Tanggung Gugat Dalam Praktik Kep NewDocument16 pages4 - Tanggung Jawab Dan Tanggung Gugat Dalam Praktik Kep NewEvi SilvianiPas encore d'évaluation
- Asuhan Keperawatan Pada Klien Dengan Gangguan Citra TubuhDocument22 pagesAsuhan Keperawatan Pada Klien Dengan Gangguan Citra TubuhOverlinda limbongPas encore d'évaluation
- Suhu Tubuh BIOMEDIK 2Document23 pagesSuhu Tubuh BIOMEDIK 2Karina SingarimbunPas encore d'évaluation
- Metabolism-Thermo-HormoneDocument30 pagesMetabolism-Thermo-HormoneWahyu Ismail SiagianPas encore d'évaluation
- Anfis UrologyDocument30 pagesAnfis UrologyWahyu sarwono AjiPas encore d'évaluation
- ANATOMIDocument7 pagesANATOMIYesi RahmawatiPas encore d'évaluation
- Kebutuhan Istirahat Dan TidurDocument40 pagesKebutuhan Istirahat Dan TidurDesi RahmasariPas encore d'évaluation
- Askep Dengan Jantung BawaanDocument56 pagesAskep Dengan Jantung BawaanRay RsulPas encore d'évaluation
- Soal Soal Kelas BDocument20 pagesSoal Soal Kelas BIzfaningrum Melati SukmaPas encore d'évaluation
- Sistem Pencernaan ManusiaDocument45 pagesSistem Pencernaan ManusiaIka May HartatiPas encore d'évaluation
- Peran Perawat Dalam Patient SafetyDocument6 pagesPeran Perawat Dalam Patient SafetyRiza Ikhsan Mulia0% (1)
- Anfisman Sistem UrinariaDocument25 pagesAnfisman Sistem UrinariaDede WiharyaPas encore d'évaluation
- EKGDocument36 pagesEKGMelinda Aprilia Eka MavirohPas encore d'évaluation
- Monev Keselamatan PasienDocument16 pagesMonev Keselamatan PasienfitriPas encore d'évaluation
- Bioetika KeperawatanDocument30 pagesBioetika KeperawatanFEBRIA RAMADONAPas encore d'évaluation
- RPS Managemen Keperawatan.2021 22.D3.Document10 pagesRPS Managemen Keperawatan.2021 22.D3.Rika Novita SariPas encore d'évaluation
- Konsep Lansia 2Document19 pagesKonsep Lansia 2Thiia TamberanPas encore d'évaluation
- Dokumentasi KeperawatanDocument8 pagesDokumentasi Keperawatandamai yantiPas encore d'évaluation
- Revisi Kangaroo CareDocument10 pagesRevisi Kangaroo CareKatarina OktavianiPas encore d'évaluation
- Modul Praktikum Ilmu Biomedik DasarDocument135 pagesModul Praktikum Ilmu Biomedik DasarArdila OktafianiPas encore d'évaluation
- Buku Panduan KMB 2-1Document102 pagesBuku Panduan KMB 2-1Khoiril AnwarPas encore d'évaluation
- Program Bank BRO Meningkatkan Minat Baca dan Kreativitas AnakDocument30 pagesProgram Bank BRO Meningkatkan Minat Baca dan Kreativitas AnakNadya PrimeswariPas encore d'évaluation
- Safe Patient Handling and Mobility (SPHM) : RatnasariDocument32 pagesSafe Patient Handling and Mobility (SPHM) : RatnasariAnisa Rahma AzizaPas encore d'évaluation
- Tonsilitis Dan Adenoiditis. Abses Peritonsilar, LaryngitisDocument27 pagesTonsilitis Dan Adenoiditis. Abses Peritonsilar, LaryngitisMerlyantiPas encore d'évaluation
- Biologi Dan Prinsip GenetikaDocument50 pagesBiologi Dan Prinsip GenetikaNur ChrysantiPas encore d'évaluation
- Makalah Islam KesehatanDocument15 pagesMakalah Islam KesehatanHaris WandiPas encore d'évaluation
- Pasien Keselamatan dalam Berbagai Kasus MedisDocument2 pagesPasien Keselamatan dalam Berbagai Kasus MedisindahPas encore d'évaluation
- PKKMB Prodi Keperawatan PangkalpinangDocument3 pagesPKKMB Prodi Keperawatan PangkalpinangLianda KimakPas encore d'évaluation
- UTS Patofisiologi Soal Pilihan GandaDocument14 pagesUTS Patofisiologi Soal Pilihan GandaErsya NurriaPas encore d'évaluation
- Praktikum ImunisasiDocument10 pagesPraktikum ImunisasiAininur FarihahPas encore d'évaluation
- Uas TK Ii KMB-1Document5 pagesUas TK Ii KMB-1Resty Fitria AntikaPas encore d'évaluation
- Konsep NeonatusDocument37 pagesKonsep NeonatusFathia khoerunnisaPas encore d'évaluation
- Mekanisme Kontraksi OtotDocument6 pagesMekanisme Kontraksi OtotKamila JasminePas encore d'évaluation
- Jurnal TerapeutikDocument5 pagesJurnal TerapeutiksafitriPas encore d'évaluation
- ASKEP HIPOSPADIADocument12 pagesASKEP HIPOSPADIAAnonymous PWUtjUV100% (2)
- Pathway AsmaDocument1 pagePathway AsmaRiskaYantiPas encore d'évaluation
- TenkesDocument27 pagesTenkesrianiwulandari31Pas encore d'évaluation
- Dokumentasi Keperawatan PPTDocument39 pagesDokumentasi Keperawatan PPTyuda puspita ningrumPas encore d'évaluation
- Bab I Pendahuluan ADocument17 pagesBab I Pendahuluan ANurlela BacoPas encore d'évaluation
- STIKes YARSIDocument4 pagesSTIKes YARSIZahratul HayatiPas encore d'évaluation
- Slide Transcultural Keperawatan Leininger Utk Manaj AskepDocument33 pagesSlide Transcultural Keperawatan Leininger Utk Manaj AskepEka ChairunPas encore d'évaluation
- SOP Sistem PerkemihanDocument13 pagesSOP Sistem PerkemihanDiasPas encore d'évaluation
- KekuranganGiziAnakDocument26 pagesKekuranganGiziAnaknyimas heny purwatiPas encore d'évaluation
- Biokimia MolekulerDocument5 pagesBiokimia MolekulerIsti YaniPas encore d'évaluation
- Energi Dan MetabolismeDocument3 pagesEnergi Dan MetabolismeDessy Christina SimorangkirPas encore d'évaluation
- Analisa SituasiDocument9 pagesAnalisa SituasiHeriyanto Shiddiq AlfaruqPas encore d'évaluation
- Pemberdayaan Masyarakat WiniDocument20 pagesPemberdayaan Masyarakat WiniHeriyanto Shiddiq AlfaruqPas encore d'évaluation
- KesenjanganDocument30 pagesKesenjanganpuskesmas cisolokPas encore d'évaluation
- Form Keluarga PDFDocument6 pagesForm Keluarga PDFpkmkediri100% (3)
- Form Keluarga PDFDocument6 pagesForm Keluarga PDFpkmkediri100% (3)
- Uraian Tugas Puskesmas ContohDocument36 pagesUraian Tugas Puskesmas ContohHeriyanto Shiddiq AlfaruqPas encore d'évaluation
- Alur PendaftaranDocument1 pageAlur PendaftaranHeriyanto Shiddiq AlfaruqPas encore d'évaluation
- Alur PonedDocument1 pageAlur PonedHeriyanto Shiddiq AlfaruqPas encore d'évaluation
- Rencana Kegiatan PuskesmasDocument3 pagesRencana Kegiatan Puskesmasirawati hamzahPas encore d'évaluation
- SEHAT DAN BERSIHDocument1 pageSEHAT DAN BERSIHHeriyanto Shiddiq AlfaruqPas encore d'évaluation
- Inilah Seruan KamiDocument32 pagesInilah Seruan KamiAbu Nabila As SundawyPas encore d'évaluation
- CERVICITIS DAN ENDOMETRITISDocument3 pagesCERVICITIS DAN ENDOMETRITISHeriyanto Shiddiq AlfaruqPas encore d'évaluation
- Keselamatan Dan Kesehatan Kerja RSDocument2 pagesKeselamatan Dan Kesehatan Kerja RSHeriyanto Shiddiq AlfaruqPas encore d'évaluation
- Anatomi Fisiologi Sistem KardiovaskularDocument49 pagesAnatomi Fisiologi Sistem KardiovaskularEky Madyaning Nastiti89% (18)
- 17 Kisah Penuh HikmahDocument55 pages17 Kisah Penuh Hikmahlaskar22Pas encore d'évaluation
- Fisika Kesehatan BiolistrikDocument3 pagesFisika Kesehatan BiolistrikHeriyanto Shiddiq Alfaruq100% (2)
- Therapi Modalitas Senam Diabetes Melitus Pada LansiaDocument9 pagesTherapi Modalitas Senam Diabetes Melitus Pada LansiaHeriyanto Shiddiq Alfaruq100% (1)
- SENAM DIABETESDocument2 pagesSENAM DIABETESHeriyanto Shiddiq AlfaruqPas encore d'évaluation
- FilsafatDocument5 pagesFilsafatHeriyanto Shiddiq AlfaruqPas encore d'évaluation