Académique Documents
Professionnel Documents
Culture Documents
VOLUMETRIA DE NEUTRALIZACIÓN - Estudiantes
Transféré par
bessieolivaTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
VOLUMETRIA DE NEUTRALIZACIÓN - Estudiantes
Transféré par
bessieolivaDroits d'auteur :
Formats disponibles
ESCUELA DE QUMICA DEPARTAMENTO DE ANLISIS INORGNICO
ANLISIS INORGNICO II
UNIDAD IV VOLUMETRA CIDO-BASE 1. cidos Poliprticos Se sabe que el cido diprtico H2A, se ionizar en dos etapas y habr una constante de disociacin para cada uno de sus protones. Durante una titulacin, es posible convertir todo el H2A en HA- antes de que se observe una cantidad significativa de A2-, entonces es posible tratar cada paso por separado y obtener bsicamente con dos curvas de titulacin. Una curva de titulacin de A-2 a HA- o visceversa. Y la otra de HA- a H2A. 1.1. Para el cido fosfrico: [ [ [ [ [ [ Se observaran tres curvas de titulacin. 1.2. Para el cido carbnico: [ [ [ [ Se observaran dos curvas de titulacin. Sin embargo la ionizacin del ltimo protn, siempre es menor que los anteriores por lo tanto debe tomarse en cuenta que para poder titular un cido poliprtico debe cumplirse uno de los siguientes requisitos: a) b) [ ] Cuando se pueden dividir la constante de disociacin mayor entre la menor. Segn la cantidad de protones que pueda donar. Se divide la constante de disociacin entre la concentracin inicial de in hidronio. ][ ] ][ ] ] ] ][ ] ][ ] ] ][ ] ] ]
Ionizacin del cido H2A [ [ [ [ ][ ] ][ ] ] ]
Documento de Apoyo No. 3 Volumetra de Neutralizacin
Ejemplo 1.1. Cuntas etapas son factibles para titular una disolucin de H3PO4 0,1N? Qu indicador usara? PARA LA PRIMERA PREGUNTA: PASO 1: Planteamiento: El cido fosfrico es un cido triprtico, por lo tanto es posible que se presenten tres etapas.
H3PO4
H2PO4-
HPO4-2
PO4-3
Primera Etapa
Segunda Etapa
Tercera Etapa
PASO 2: De estas etapas cules son factibles? Esto depende de si cumple uno de los requisitos: Para la primera etapa es factible pues la relacin entre Ka1 y Ka2 es mayor que 1x104. Para la segunda etapa es factible pues la relacin entre Ka2 y Ka3 es mayor que 1x104. Para la tercera etapa no es factible la titulacin pues la relacin entre Ka3 y [H+] es menor que 1x10-8.
Esto indica que puede tratarse cada paso separadamente durante la titulacin para la primera y segunda etapa, pero no para la tercera etapa en las condiciones dadas. PARA LA SEGUNDA PREGUNTA: PASO 1: Planteamiento: Los indicadores indican el final de la titulacin, y debe encontrarse cerca del punto de equivalencia. Cuando se tiene un cido poliprtico, el punto de equivalencia de la primera curva de titulacin debe encontrarse antes de comenzar a titular el segundo protn. Por lo tanto el pH en el punto de equivalencia debe estar a la mitad de la suma de los pKa del cido. PASO 2: Realizar clculos. PRIMERA ETAPA: ( ( SEGUNDA ETAPA: ( ( ) ) Indicador: Fenolftalena Rango: 8,30 -10,00 Cambio: incoloro-fucsia ) ) Indicador: Verde de bromocresol Rango: 3,80 5,40 Cambio: amarillo - azul
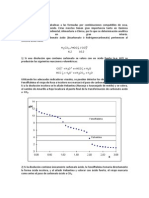
2. Anlisis Cualitativo Y Cuantitativo De Mezclas De Carbonatos Debido a que el cido carbnico se descompone fcilmente en dixido de carbono y agua, las titulaciones involucradas se refieren al in carbonato y el in bicarbonato que s pueden existir en disolucin acuosa. Por ser iones bsicos se titulan con un cido, regularmente es el cido clorhdrico;
Pgina 2 de 8
Documento de Apoyo No. 3 Volumetra de Neutralizacin
y los indicadores a utilizar son: Fenolftalena (FN), Naranja de metilo (NM), Verde de bromocresol (VBC) y Rojo de metilo (RM). En las mezclas compatibles de hidrxido de sodio, carbonato de sodio y bicarbonato de sodio los constituyentes presentes pueden determinarse por valoraciones que implican la utilizacin de dos indicadores. Las mezclas compatibles de estos compuestos son: 2.1. Carbonato: CO32El titulante ser el H+ proveniente del HCl, HNO3, HClO4 y otros cidos fuertes. Las reacciones son: (1) CO3-2 + H+ HCO3(2) HCO3- + H+ H2CO3 El indicador es la fenolftalena. El indicador puede ser VBC, NM, RM.
Para neutralizarse debe obtener dos iones hidronio y formar el cido carbnico. La neutralizacin se da en dos etapas: en la primera etapa el in carbonato reacciona con el in hidronio y forma el in bicarbonato; y en la segunda etapa el in bicarbonato reacciona con el segundo in hidronio y forma el cido carbnico. Por lo tanto, el volumen usado en la titulacin de la primera etapa (V1) y el volumen usado en la titulacin de la segunda etapa (V2) ser el mismo; porque se necesita el mismo volumen de HCl para formar HCO3- y el mismo volumen para llegar a H2CO3. Cuando el V1 es igual al V2, la muestra es carbonato.
2.2.
Carbonato e Hidrxido: CO32-/OHEl titulante ser el H+ proveniente del HCl, HNO3, HClO4 y otros cidos fuertes. Las reacciones son: (1) OH- + H+ H2O (2) CO3-2 + H+ HCO3(3) HCO3- + H+ H2CO3 El indicador es la fenolftalena. El indicador es la fenolftalena. El indicador puede ser VBC, NM, RM.
En esta mezcla se presentan dos neutralizaciones, la del hidroxilo y la del in carbonato; tanto el hidroxilo como el carbonato son sustancias bsicas por lo que el indicador a utilizar es la FN, esto quiere decir, en la titulacin de hidroxilo a agua y de carbonato a bicarbonato, se obtendr un volumen de titulante total (incluye el volumen para que reaccione el primer protn con carbonato y el volumen para reaccionar con el in hidroxilo.
12
10
V1 V2
0 10 20 30 40 50 60 70
Cuando se titule el bicarbonato se determinar el volumen de titulante que equivale al carbonato, porque el bicarbonato titulado proviene del carbonato y el volumen utilizado ser el mismo que para titular carbonato. Por lo tanto se debe asumir que el volumen de titulante gastado usando como indicador la fenolftalena debe ser mayor que el volumen gastado usando como indicador NM, RM o VBC, porque el volumen con fenolftalena incluye el volumen de titulante gastado con el hidroxilo y con el carbonato.
Para conocer el volumen de titulante gastado con el hidrxido, se resta del volumen gastado con FN como indicador, el volumen gastado con NM, RM o VBC. Cuando el V1 es mayor que el V2, la muestra es la mezcla de carbonato e hidrxido.
Pgina 3 de 8
2.3.
Carbonato y Bicarbonato: CO32- y HCO3El titulante ser el H+ proveniente del HCl, HNO3, HClO4 y otros cidos fuertes. Las reacciones son: (1) CO3-2 + H+ HCO3(2) HCO3- + H+ H2CO3 El indicador es la fenolftalena. El indicador puede ser VBC, NM, RM.
Documento de Apoyo No. 3 Volumetra de Neutralizacin
En esta mezcla se neutraliza el carbonato a cido carbnico y el bicarbonato a cido carbnico; por tanto el volumen del titulante ser mayor cuando se est haciendo la titulacin del bicarbonato. El volumen gastado de titulante utilizando como indicador la FN, indica el volumen de titulante gastado para titular el carbonato. El volumen de titulante gastado utilizando como indicador NM, VBC o RM ser mayor porque incluye el bicarbonato que se encuentra en la muestra y el bicarbonato formado por la titulacin del carbonato; y la diferencia de volmenes ser el volumen gastado para titular el carbonato. Cuando V1 es menor que el V2, la muestra es la mezcla de carbonato y bicarbonato.
2.4.
Bicarbonato: HCO3El titulante ser el H+ proveniente del HCl, HNO3, HClO4 y otros cidos fuertes. La reaccin es: (1) HCO3- + H+ H2CO3 El indicador puede ser VBC, NM, RM.
Se inicia la titulacin con FN, porque se desconoce cul es el analito presente, al agregar el indicador este tendr su fase incolora y es porque no existen componentes bsicos, slo componentes cidos. Al agregar NM, VBC o RM se inicia la titulacin, obtenindose un nico volumen.
2.5.
Hidrxido: OHEl titulante ser el H+ proveniente del HCl, HNO3, HClO4 y otros cidos fuertes. Las reacciones son: (1) OH- + H+ H2O El indicador es la fenolftalena.
12
10
V1
El nico volumen gastado deber ser el obtenido con la FN como indicador, al llegar a incoloro con la fenolftalena y se inicia la titulacin con el otro indicador (NM, VBC o RM) al agregar una gota del titulante este cambiar de color inmediatamente, pues no hay otra sustancia que titular. Al agregar la gota de cido, el pH inmediatamente se convierte en cido porque todo el hidroxilo ya se neutraliz y se ha convertido en agua.
0 0 0.5 1 1.5 2 2.5 3 3.5
Pgina 4 de 8
Documento de Apoyo No. 3 Volumetra de Neutralizacin
Ejemplo 2.1. Para una muestra alcalina pura de 1,8550 g, se utilizaron 43,80 mL de HCl 0,5000 N para el viraje de FN; y 18,87 mL adicionales para el viraje con el NM. Cul es la analita y cul es el % de la misma en la muestra original como sales de sodio? Determinar el analito 1. Utilizando como indicador FN se puede titular el in hidroxilo y el in carbonato. 2. Utilizando como indicador NM se puede titular bicarbonato. 3. El problema me dice que al volumen de HCl utilizado para virar FN, se le adiciona ms, esto quiere decir que la titulacin se est haciendo en un solo recipiente. 4. El volumen con FN es mayor que el volumen con NM, por lo tanto tiene mayor cantidad de componentes bsicos que bicarbonato. 5. Por lo tanto el bicarbonato que titule con NM debe ser el que proviene del carbonato; y como el volumen de FN es mayor al de NM quiere decir que aparte del carbonato existe un componente que tiene que ser el hidrxido. Entonces el analito es Carbonato e Hidrxido.
Las analitas son carbonato de sodio e hidrxido de sodio, se encuentra en la muestra en un porcentaje de 53,91% y 26,88%. Ejemplo 2.2. Una muestra de 0,527 g de una mezcla que contiene carbonato de sodio, carbonato cido de sodio e impurezas inertes se titula con cido clorhdrico 0,109 N con un consumo de 15,7 mL para alcanzar el punto final con fenolftalena, y en otro recipiente un total de 43,8 mL para el punto final con anaranjado de metilo. Cules son los porcentajes de individuales de carbonato cido de sodio y carbonato de sodio en la mezcla? Determinar el analito 1. Con la fenolftalena se puede titular OH- H2O, CO3-2 HCO32. Con el anaranjado de metilo se puede titular HCO3- H2CO3 3. Debido a que se realiza en dos recipientes distintos: en el recipiente uno slo se titula carbonato o hidroxilo, en el recipiente 2 que contiene el anaranjado de metilo primero se debe agregar 15,7 mL de HCl para llegar al bicarbonato que es el punto donde quedo en el recipiente 1; y el resto del volumen utilizado en el recipiente dos ser el gastado con la titulacin del bicarbonato que es o que se titula con el anaranjado de metilo. 4. En el recipiente 1 se utilizan 15,7 mL (V1) y en el recipiente 2 se utilizan 43,8 mL, si a 43,8 le restamos 15,7, nos da como resultado que con anaranjado de metilo se utilizaron 28,1 mL (V2). 5. Como el volumen con naranja de metilo es mayor que con la fenolftalena se tiene una mezcla de carbonato y bicarbonato. Entonces el analito es Carbonato y bicarbonato.
Las analitas son carbonato de sodio y bicarbonato de sodio, se encuentra en la muestra en un porcentaje de 34,4% y 21,5%. Ejemplo 2.3. Una serie de disoluciones que contienen lcalis, solos o en combinaciones compatibles, se valora con HCl 0,2500 N. La tabla siguiente muestra los volmenes de cido necesario para valorar alcuotas de 25,00 mL de cada disolucin hasta puntos finales con FN y VBC, en un mismo recipiente. Deduzca la composicin de las disoluciones y calcule la concentracin del soluto en ppm (sales de sodio).
Pgina 5 de 8
Documento de Apoyo No. 3 Volumetra de Neutralizacin
DISOLUCIN A B C D E
FN (mL) 22,42 15,67 36,42 16,12 0,00
VBC (mL) 22,44 42,13 29,64 0,01 33,33
DISOLUCIN A: 1. El volumen utilizado con FN es igual al utilizado con VBC, la diferencia de 0,02 puede deberse a un error del analista. 2. Por lo tanto la muestra es Carbonato. El carbonato con la primera titulacin se transformo a bicarbonato y el bicarbonato a cido carbnico. 2,376x104 ppm de carbonato de sodio. DISOLUCIN B: 1. El volumen utilizado con FN es menor que con NM, por lo tanto se tiene una mezcla de carbonato y bicarbonato. 1,661x104 ppm de carbonato de sodio y 2,223x104 ppm de bicarbonato de sodio. DISOLUCIN C: 1. El volumen mayor es con FN por lo tanto la mayor cantidad de analito son componentes bsicos, entonces la analita es carbonato e hidrxido. 3,142x104 ppm de carbonato de sodio y 2712 ppm de hidrxido de sodio. DISOLUCIN D: 1. El volumen considerado ser slo el utilizado con FN, porque el otro es insignificante al comparar los volmenes, por lo que la analita es hidrxido. 6448 ppm de hidrxido de sodio. DISOLUCIN E: 1. Slo se titula bicarbonato, por lo tanto esta es la analita. 2,800x104 ppm de bicarbonato de sodio.
MRML/mrml 27082012
Pgina 6 de 8
ESCUELA DE QUMICA DEPARTAMENTO DE ANLISIS INORGNICO ANLISIS INORGNICO II Gua de Estudio No. 2 Volumetra de Neutralizacin Instrucciones: Al finalizar la lectura del Documento de Apoyo No. 3; realice la Gua de Estudio No. 2 Parte 1. Parte 1: Fecha de entrega: 20 de septiembre de 2 012 1. Qu es un cido poliprtico? 2. Cules son los parmetros que se utilizan para determinar las etapas factibles para titular un cido poliprtico? 3. Cmo se determina el indicador a utilizar en la titulacin de un cido poliprtico? 4. Es posible que exista la mezcla de carbonato y bicarbonato? S o No. Por qu? 5. Es posible que exista la mezcla de carbonato e hidrxido? S o No. Por qu? 6. Es posible que exista la mezcla de hidrxido y bicarbonato? S o No. Por qu? 7. En un recipiente se desea determinar los analitos de la muestra, se sabe que es una muestra alcal. Al realizar el anlisis agrega como indicador Fenolftalena se le agregan 25,0 mL de cido clorhdrico; seguidamente se agrega el indicador naranja de metilo y se adicionan 10,0 mL del mismo cido. Cul es el analito presente o los analitos presentes. 8. Se determina la composicin de una muestra que puede contener carbonato, bicarbonato e hidrxido. En un recipiente con FN se agregan 15,2 mL de cido clorhdrico hasta su viraje. En otro recipiente con NM se agregan 15,2 mL de cido clorhdrico hasta su viraje. 9. Se sabe que una muestra contiene bicarbonato y carbonato. Si se va a cuantificar en un solo recipiente como esperara que fuera la relacin de volmenes. 10. Si se gastan 25,6 mL de cido en la titulacin con FN y 50,0 mL adicionales con NM, cules o cul es el analito? Parte 2. Para resolver con ayuda de su profesor en clase. NO SON PARA QUE EL PROFESOR LAS RESUELVA. Fecha de entrega: 25 de septiembre de 2012 1. Para el anlisis cualitativo de mezclas de carbonatos, se sabe que el titulante ser HCl 0.1 N. La titulacin se realiza en el mismo recipiente y para la primera etapa se utiliza fenolftalena como indicador y para la segunda etapa se utiliza naranja de metilo como indicador. En el cuadro de abajo se indica el volumen de cido utilizado en la primera y segunda etapas. En base a cada titulacin, indique cul es la mezcla compatible que se est titulando? No. Valor en mL, de HCl utilizado para la valoracin de la primera etapa 12,9 9,5 19,6 4,3 Valor en mL, de HCl utilizado para la valoracin de la segunda etapa 10,3 9,5 0,0 7,8 Relacin de volmenes V1 -- V2 Analita o analitas
1.1. 1.2. 1.3. 1.4.
Gua de Estudio No. 2 Volumetra de Neutralizacin
1.5. 1.6. 1.7. 1.8. 1.9. 1.10.
0,0 3,8 5,7 10,4 6,8 14,9
8,4 3,8 16,2 9,3 0,0 14,9
2. Para una muestra alcalina pura de 1,0332 g, se utilizaron 23,20 mL de HCl 0,3100N para el viraje de FN, y 23,20mL adicionales para el viraje con el NM. Cul es la analita o analitas y cul es el % de la misma en la muestra original como sales de sodio? 3. Una muestra de 3,100 g formada por una mezcla de lcalis, consume 71,04 mL de HCl 0,2100 N en su neutralizacin completa. Otra muestra idntica se trata con 50,00 mL de NaOH 0,0810 N; despus se le aade BaCl2 y la mezcla consume 10,80 mL del mismo cido con FN. Calcular el % de cada componente en la muestra (como sales de sodio). 4. Para el cido oxlico, indique si es posible llevar a cabo la titulacin de sus dos protones. Para el clculo de la segunda disociacin, asuma que la concentracin de iones H+ es igual a 0,01 M. % de carbonato de sodio y 49.0% de hidrxido de sodio. 5. Se analiza un NaHCO3 comercial que esta impurificado con Na2CO3. Se pesan 2,9225 g, se lleva a un volumen de 250,0 mL y una alcuota de 20,0 mL se titula con HCl 0,090 N, consumiendo un volumen de cambio con indicador fenolftalena de 2,20 mL y un segundo volumen de cambio observable con indicador naranja de metilo de 27,20 mL. Determinar: a) %Na2CO3 en la muestra original. 9.97%. b) %NaHCO3 en la muestra original. 89.8%. 6. Una mezcla que contiene solo carbonato de bario y carbonato de litio pesa 0,150 g. si se consumen 25,0 mL de cido clorhdrico 0,120 N para completar la neutralizacin; cul es el porcentaje de carbonato de bario en la muestra. 7. Una muestra de 0,1401 g de carbonato purificado se disuelve en 50,00 mL de cido clorhdrico 0,1140 N y se lleva a ebullicin para eliminar el CO2. La valoracin por retroceso del exceso de cido clorhdrico requiere 24,21 mL de hidrxido de sodio 0,09802 N. Identifique el carbonato. 8. Una muestra de sosa (carbonato sdico) de 0,5800 g consume 30,00 mL de cido clorhdrico para su neutralizacin completa. 35,00 mL de la disolucin de cido clorhdrico equivalen a 42,00 mL de una disolucin de hidrxido sdico, 45,00 mL de la cual neutralizan a 0,2553 g de patrn primario cido oxlico dihidratado. Calcular el porcentaje de carbonato de sodio en la muestra.
MRML/mrml 27082012
Pgina 8 de 8
Vous aimerez peut-être aussi
- Aplicaciones Clasicas de Valoraciones de NeutralizaciónDocument10 pagesAplicaciones Clasicas de Valoraciones de NeutralizaciónPabloSanchezPas encore d'évaluation
- Volumetría Por Precipitación 1Document3 pagesVolumetría Por Precipitación 1Juan Luciano100% (1)
- Volumetría Por PrecipitaciónDocument5 pagesVolumetría Por PrecipitaciónAlejandra RuizPas encore d'évaluation
- TALLER PH y Amortiguadores 2020-2Document10 pagesTALLER PH y Amortiguadores 2020-2VANESSA LEONOR PRIETOPas encore d'évaluation
- Reporte 1, Análisis Químico P11Document3 pagesReporte 1, Análisis Químico P11Jose Enrique Mendoza RodriguezPas encore d'évaluation
- PermanganometriaDocument3 pagesPermanganometriaAlejandra CorsiPas encore d'évaluation
- Aplicación Industrial de La Yodometria 2Document2 pagesAplicación Industrial de La Yodometria 2Jair Ayesta100% (1)
- A-Ejercicios Vólumetría Precipitación y GravimetríaDocument3 pagesA-Ejercicios Vólumetría Precipitación y GravimetríaMaksim Kéldysh100% (1)
- Taller GravimetriaDocument15 pagesTaller GravimetriaAndreina VillanPas encore d'évaluation
- Ejercicios de Uímica AnaliticaDocument34 pagesEjercicios de Uímica AnaliticamarcosPas encore d'évaluation
- Guía: GravimetríaDocument4 pagesGuía: GravimetríaRulos QueteimportaPas encore d'évaluation
- Cuestionario 7Document2 pagesCuestionario 7erizoPas encore d'évaluation
- 2do Trabajo MetodosDocument12 pages2do Trabajo MetodosSaul Fernando Sandoval0% (1)
- 2st BalanceDocument19 pages2st BalancePedro Velazquez100% (1)
- Deber de VolumetriaDocument3 pagesDeber de VolumetriaGabriela MejiaPas encore d'évaluation
- Cuestionario VolumetríaDocument3 pagesCuestionario VolumetríaAlonso AlegríaPas encore d'évaluation
- Ejercicio 5Document5 pagesEjercicio 5David Vp KydPas encore d'évaluation
- Taller 2 - Gravimetria - Paula MenesesDocument4 pagesTaller 2 - Gravimetria - Paula MenesesPaula MenesesPas encore d'évaluation
- Info 7 QA Determinación de Hierro en Mena ESPOLDocument8 pagesInfo 7 QA Determinación de Hierro en Mena ESPOLDobe Hernan YepezPas encore d'évaluation
- Taller para Entregar AnaliticaDocument3 pagesTaller para Entregar AnaliticavalmerPas encore d'évaluation
- Problemas de PermanganatoDocument7 pagesProblemas de PermanganatoFrida TenorioPas encore d'évaluation
- Taller Primer CorteDocument2 pagesTaller Primer Cortesantiago cardonaPas encore d'évaluation
- Taller N°3Document3 pagesTaller N°3Jaider FlórezPas encore d'évaluation
- Ejercicios Con YodoDocument2 pagesEjercicios Con YodoSebastian Bueno GaleanoPas encore d'évaluation
- Tarea Sobre Análisis Gravimétrico Guia de Ejercicios 2Document4 pagesTarea Sobre Análisis Gravimétrico Guia de Ejercicios 2Pamela VarelaPas encore d'évaluation
- Q.A. - Clase 09 - Gravimetría Fundamentos PDFDocument29 pagesQ.A. - Clase 09 - Gravimetría Fundamentos PDFAngel CondoriPas encore d'évaluation
- Ejercicios de Quimica Analitica para Resolver Solo PropuestosDocument1 pageEjercicios de Quimica Analitica para Resolver Solo PropuestosmercedesPas encore d'évaluation
- Probleemas de Precipitacion para AgroindustriasDocument1 pageProbleemas de Precipitacion para AgroindustriasFrank Lopez0% (2)
- Taller VolumetríaDocument2 pagesTaller VolumetríaSergio GomezPas encore d'évaluation
- Practica # - 3 Volumetria Por RetrocesoDocument6 pagesPractica # - 3 Volumetria Por RetrocesoQUÍMICA75% (8)
- Taller 4 Qa 1Document3 pagesTaller 4 Qa 1LauraMilenaJaramilloRodriguezPas encore d'évaluation
- Cuestionario Dra. NigdDocument9 pagesCuestionario Dra. NigdChristiansito AndresitoPas encore d'évaluation
- Guia 06 Estequiometria en Solucion QUI080Document4 pagesGuia 06 Estequiometria en Solucion QUI080Alan John AndradesPas encore d'évaluation
- Informe 3Document10 pagesInforme 3Stefano D'AmicoPas encore d'évaluation
- Tarea 23Document5 pagesTarea 23ODALYSPas encore d'évaluation
- Un Tanque Contiene 10Document2 pagesUn Tanque Contiene 10barlosPas encore d'évaluation
- Desea Que Los Resultados Se Obtengan Con Cuatro Cifras SignificativasDocument1 pageDesea Que Los Resultados Se Obtengan Con Cuatro Cifras SignificativasBrando Kevin Palomino MorenoPas encore d'évaluation
- Ejercicios de Volumetría de PrecipitaciónDocument17 pagesEjercicios de Volumetría de PrecipitaciónEudo NavaPas encore d'évaluation
- Estandarización de Solución de AgNO3 Con Solución de Bromuro de PotasioDocument2 pagesEstandarización de Solución de AgNO3 Con Solución de Bromuro de PotasioNNNPas encore d'évaluation
- Titulaciones ComplejométricasDocument3 pagesTitulaciones ComplejométricasTorres Mark Antonio100% (1)
- Taller 4. Valoraciones Directras y Por RetrocesoDocument5 pagesTaller 4. Valoraciones Directras y Por Retrocesojuan paPas encore d'évaluation
- Practica #4 Obtencion de AcetamidaDocument6 pagesPractica #4 Obtencion de AcetamidaRoberto PalominosPas encore d'évaluation
- Soluciones BufferDocument4 pagesSoluciones Buffershunashi lorenzanaPas encore d'évaluation
- Ejercicios Resueltos #6Document3 pagesEjercicios Resueltos #6RENATO JAIR COSTA MINGAPas encore d'évaluation
- Ecuaciones Temoquimicas y Ley de HessDocument7 pagesEcuaciones Temoquimicas y Ley de Hessalejandro IntriagoPas encore d'évaluation
- Vol Complejometría EjjerciciDocument6 pagesVol Complejometría EjjerciciPiter Ortega MuñozPas encore d'évaluation
- Aplicaciones de Las Leyes de Roult y Henry y MasDocument12 pagesAplicaciones de Las Leyes de Roult y Henry y MasJuan Pablo Galindo Beltran100% (1)
- Vol - Redox P.propuestosDocument5 pagesVol - Redox P.propuestosOver Core0% (2)
- 2014guia de Problemas Nº1Document3 pages2014guia de Problemas Nº1jagus21100% (1)
- Guia Volumetria RedoxDocument3 pagesGuia Volumetria RedoxAlexander Gonzalez Barra0% (1)
- 1 Bloque de Ejercicios 2020-2Document4 pages1 Bloque de Ejercicios 2020-2Isabella Vargas Marin0% (1)
- Ejercicios 4. Complejometría PDFDocument2 pagesEjercicios 4. Complejometría PDFJuliana PNPas encore d'évaluation
- Problemas de GravimetriaDocument1 pageProblemas de GravimetriaLeidy Karen Canaza100% (1)
- Carbonatos y BicarbonatosDocument3 pagesCarbonatos y BicarbonatosAlejandro Ramirez AlpizarPas encore d'évaluation
- Determinacion de Carbonatos y BicarbonatosDocument4 pagesDeterminacion de Carbonatos y BicarbonatosEstebanPas encore d'évaluation
- Ácidos Polipróticos..Document9 pagesÁcidos Polipróticos..CARINAPas encore d'évaluation
- Mezclas AlcalinasDocument5 pagesMezclas AlcalinasTiffany Bernard100% (1)
- La Pureza Del Carbonato de SodioDocument2 pagesLa Pureza Del Carbonato de SodioRichardAngelCuencaPacheco100% (1)
- Mezclas AlcalinasDocument5 pagesMezclas AlcalinasZeballosNati100% (3)
- Unidad 3 Parte 3 ExtracciónDocument43 pagesUnidad 3 Parte 3 ExtracciónbessieolivaPas encore d'évaluation
- Tabla de Pesos Fórmula 2021Document2 pagesTabla de Pesos Fórmula 2021bessieoliva100% (1)
- Documento de Apoyo 2 MCD 2021Document6 pagesDocumento de Apoyo 2 MCD 2021bessieolivaPas encore d'évaluation
- Documento de Apoyo 3 MTC J Precisión y Exactitud 2021Document8 pagesDocumento de Apoyo 3 MTC J Precisión y Exactitud 2021bessieolivaPas encore d'évaluation
- Curva Nh4oh - HCLDocument1 pageCurva Nh4oh - HCLbessieolivaPas encore d'évaluation
- Documento de Apoyo 1 Cs 2021Document6 pagesDocumento de Apoyo 1 Cs 2021bessieolivaPas encore d'évaluation
- Tabla de Pesos FórmulaDocument2 pagesTabla de Pesos FórmulaFiorePGPas encore d'évaluation
- UNIDAD I Parte 1 2017 (Equilibrio Químico Homogéneo Parte II)Document20 pagesUNIDAD I Parte 1 2017 (Equilibrio Químico Homogéneo Parte II)bessieolivaPas encore d'évaluation
- UNIDAD II Parte 6 Métodos Con YodoDocument19 pagesUNIDAD II Parte 6 Métodos Con Yodobessieoliva100% (1)
- Calculo de PH AF-BFDocument6 pagesCalculo de PH AF-BFbessieolivaPas encore d'évaluation
- UNIDAD II, Parte 1 2017 Análisis TitrimétricoDocument14 pagesUNIDAD II, Parte 1 2017 Análisis TitrimétricobessieolivaPas encore d'évaluation
- Hoja de Trabajo No. 2Document1 pageHoja de Trabajo No. 2bessieolivaPas encore d'évaluation
- Tablas de IonizaciónDocument2 pagesTablas de IonizaciónbessieolivaPas encore d'évaluation
- Tablas de IonizaciónDocument2 pagesTablas de IonizaciónbessieolivaPas encore d'évaluation
- HT5Document4 pagesHT5bessieoliva67% (3)
- Equilibrio Químico HeterogéneoDocument31 pagesEquilibrio Químico HeterogéneobessieolivaPas encore d'évaluation
- Volumetría de PrecipitaciónDocument6 pagesVolumetría de Precipitaciónbessieoliva0% (3)
- Tabla de Pesos FórmulaDocument2 pagesTabla de Pesos FórmulabessieolivaPas encore d'évaluation
- Ejercicio 9, Guía Estudio PermanganimetríaDocument1 pageEjercicio 9, Guía Estudio Permanganimetríabessieoliva100% (3)
- Equilibrio Homogéneo en Disolución AcuosaDocument29 pagesEquilibrio Homogéneo en Disolución AcuosabessieolivaPas encore d'évaluation
- Hoja de Trabajo No. 3Document2 pagesHoja de Trabajo No. 3bessieoliva75% (4)
- Hoja de Trabajo No. 1: Escuela de Química Departamento de Análisis InorgánicoDocument1 pageHoja de Trabajo No. 1: Escuela de Química Departamento de Análisis InorgánicobessieolivaPas encore d'évaluation
- Escuela de Química Departamento de Análisis InorgánicoDocument2 pagesEscuela de Química Departamento de Análisis Inorgánicobessieoliva0% (1)
- Manual Procesos de Manufactura IIDocument159 pagesManual Procesos de Manufactura IIALEJANDRO CALVOPas encore d'évaluation
- Bases Del Concurso de Reconocimiento de MineralesDocument6 pagesBases Del Concurso de Reconocimiento de MineralesWelser Michael CarrascoPas encore d'évaluation
- Navec Ing Fabricacion CASTDocument16 pagesNavec Ing Fabricacion CASTEscalante Vargas WillinthonPas encore d'évaluation
- Grados de Los PernosDocument4 pagesGrados de Los PernosMiguelQuishpePas encore d'évaluation
- CaletonesDocument31 pagesCaletonesPerico Palotes100% (1)
- Diapositiva de InorganicaDocument52 pagesDiapositiva de InorganicarocioPas encore d'évaluation
- Usos y Aplicaciones Del Óxido de MagnesioDocument2 pagesUsos y Aplicaciones Del Óxido de MagnesioFlor Alba Villa Londoño29% (7)
- BoraxDocument9 pagesBoraxCristian Leonardo Galaz NavarroPas encore d'évaluation
- Arq 1 BateriaDocument1 pageArq 1 BateriaAlejandro Aya MendezPas encore d'évaluation
- Actividad Precios Unitarios Por ActividadDocument1 pageActividad Precios Unitarios Por ActividadJORGE EDUARDO ROMERO ZARTAPas encore d'évaluation
- ComplejosDocument6 pagesComplejosCatalina Alarcon NavarroPas encore d'évaluation
- Contrapisos Con BaritinaDocument3 pagesContrapisos Con BaritinaCarlos Mayhuiri0% (1)
- Evaluacion Del Curso III SOLDADURADocument40 pagesEvaluacion Del Curso III SOLDADURAisbass123Pas encore d'évaluation
- Reconocimiento de Acidos y BasesDocument10 pagesReconocimiento de Acidos y BasesmanuelaPas encore d'évaluation
- Constantes Elástoplásticas de Diferentes MaterialesDocument4 pagesConstantes Elástoplásticas de Diferentes MaterialesHenry ValenciaPas encore d'évaluation
- Compuestos QuimicosDocument42 pagesCompuestos QuimicosVeronicaGonzalezPas encore d'évaluation
- Datos de LaboratorioDocument6 pagesDatos de LaboratorioB ERPas encore d'évaluation
- Como Evitar La Corrosion en Ambientes HumedosDocument8 pagesComo Evitar La Corrosion en Ambientes HumedosniezchenPas encore d'évaluation
- Cajas Halado SB6ADocument10 pagesCajas Halado SB6AANDYAFANADORPas encore d'évaluation
- 6 Interpretación de Planos TuberiasDocument12 pages6 Interpretación de Planos TuberiasantonyPas encore d'évaluation
- Informe Colecbi 1 A 2Document2 pagesInforme Colecbi 1 A 2Wilson IzaguirrePas encore d'évaluation
- Tuberías de CobreDocument2 pagesTuberías de CobreRonald AstucuriPas encore d'évaluation
- ACU Cerco PerimétricoDocument12 pagesACU Cerco PerimétricoRoberto Chavez OjedaPas encore d'évaluation
- Pernos Molino Sag Mantos de OroDocument49 pagesPernos Molino Sag Mantos de OroMiguel Lamas ChacanaPas encore d'évaluation
- Marcha SistematicaDocument6 pagesMarcha SistematicaLaura Castaño GarridoPas encore d'évaluation
- Análisis de Riesgos de Los Metales AlcalinosDocument22 pagesAnálisis de Riesgos de Los Metales AlcalinosAntonio Anzures0% (1)
- Apunte Química Inórganica-2017-Leonardo CDocument118 pagesApunte Química Inórganica-2017-Leonardo CAdalid Leonela AdalidPas encore d'évaluation
- PeletizacionDocument36 pagesPeletizacionDani ElPas encore d'évaluation
- Pila SecaDocument1 pagePila SecaManuel ZambranoPas encore d'évaluation
- CvhjkuytfDocument4 pagesCvhjkuytfmarcos villagraPas encore d'évaluation