Académique Documents
Professionnel Documents
Culture Documents
Ley de Charles
Transféré par
Yessenia NathyCopyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Ley de Charles
Transféré par
Yessenia NathyDroits d'auteur :
Formats disponibles
Es una de las leyes de los gases ideales Relaciona el volumen y la temperatura de una cierta cantidad de gas ideal, mantenido
a una presin constante, mediante una constante de proporcionalidad directa.
En esta ley, Jacques Charles dice que para una cierta cantidad de gas a una presin constante, al aumentar la temperatura, el volumen del gas aumenta y al disminuir la temperatura el volumen del gas disminuye. Esto se debe a que la temperatura est directamente relacionada con la energa cintica (debido al movimiento) de las molculas del gas. As que, para cierta cantidad de gas a una presin dada, a mayor velocidad de las molculas (temperatura), mayor volumen del gas.
Despejando T1 se obtiene:
Despejando T2 se obtiene:
FORMULA GENERAL DE LA LEY DE CHARLES
Despejando V1 es igual a: :
Despejando V2 se obtiene
Un
gas ocupa un volumen de 3.5 litros a una temperatura de 60K. Si la presin permanece constante a que temperatura en volumen seria de 6.5 litros. V1= 3.5 Lt T1= 60 K V2= 6.5 Lt T2= ???? V1/T1 =V2/T2 T2= V2 x T1/V1 T2= 6.5 Lt x 60 K/3.5 Lt= 111.42 K
Vous aimerez peut-être aussi
- Gases Ideales y RealesDocument18 pagesGases Ideales y RealesAlexter 1601100% (1)
- Ecuación de Hazen-Williams para flujo de aguaDocument8 pagesEcuación de Hazen-Williams para flujo de aguaJf Leonardo100% (1)
- Termo Resistencia-40Document9 pagesTermo Resistencia-40David CasimiroPas encore d'évaluation
- Manual de prácticas de TermodinámicaDocument101 pagesManual de prácticas de TermodinámicaKevin Rivera GarciaPas encore d'évaluation
- Identificacion de Sistemas Cerrados y Abiertos TermodinamicaDocument8 pagesIdentificacion de Sistemas Cerrados y Abiertos TermodinamicaCristian Paúl Torres DíazPas encore d'évaluation
- Practica 3 Determinacion Del Peso MolecularDocument12 pagesPractica 3 Determinacion Del Peso MolecularAbner MartinezPas encore d'évaluation
- Termodinamica Trabajo IDocument30 pagesTermodinamica Trabajo IYexibel AguilarPas encore d'évaluation
- 2.4 Correlaciones Conveccion NaturalDocument17 pages2.4 Correlaciones Conveccion NaturalDanEstradaPas encore d'évaluation
- Primera Ley de La TermodinámicaDocument8 pagesPrimera Ley de La TermodinámicaAriana AlarcoPas encore d'évaluation
- Ecuaciones de EstadoDocument10 pagesEcuaciones de EstadoMiguel Angel PalominoPas encore d'évaluation
- Combustion GaseosaDocument25 pagesCombustion GaseosaNel Gutiérrez SalasPas encore d'évaluation
- Estudio IsocinéticoDocument19 pagesEstudio IsocinéticoRebeca AlvarePas encore d'évaluation
- Ley de CharlesDocument4 pagesLey de CharlesHenry Giampiere Reyna RamosPas encore d'évaluation
- Ley de Presión Parcial deDocument4 pagesLey de Presión Parcial deAntonio Torres SanchezPas encore d'évaluation
- Leyes de los gases ideales de Gay-Lussac y CharlesDocument15 pagesLeyes de los gases ideales de Gay-Lussac y CharlesAngie CalderonPas encore d'évaluation
- Resumen PirometrosDocument20 pagesResumen PirometrosJunior MazónPas encore d'évaluation
- Conceptos TermodinamicaDocument39 pagesConceptos TermodinamicaJuan ChoquePas encore d'évaluation
- Folleto2-Ley de Los Gases IdealesDocument14 pagesFolleto2-Ley de Los Gases IdealesNesly LagunaPas encore d'évaluation
- Gases RealesDocument16 pagesGases Realesnorman12normanPas encore d'évaluation
- Numero de ReynoldDocument20 pagesNumero de ReynoldMarco Antonio EscalantePas encore d'évaluation
- CentrifugacionDocument43 pagesCentrifugacioncarlos-roPas encore d'évaluation
- Ecuaciones de estado para gases realesDocument6 pagesEcuaciones de estado para gases realesJüan Prz100% (1)
- Aplicaciones de Flujo de Calor TransitorioDocument23 pagesAplicaciones de Flujo de Calor TransitorioJose Ricardo DuranPas encore d'évaluation
- Mecanismos de transferencia de calor: conducción, convección y radiaciónDocument3 pagesMecanismos de transferencia de calor: conducción, convección y radiaciónCesar GonzalezPas encore d'évaluation
- Termodinámica SistemasDocument33 pagesTermodinámica SistemasAdriana UsmaPas encore d'évaluation
- Medicion de PresionDocument49 pagesMedicion de PresionEver ContrerasPas encore d'évaluation
- Analisis de Un Sistema de Intercambio de CalorDocument19 pagesAnalisis de Un Sistema de Intercambio de CalorNora PeláezPas encore d'évaluation
- Series de FourierDocument12 pagesSeries de FourierVictor Timana SilvaPas encore d'évaluation
- Presión de vapor: definición y métodos de determinaciónDocument19 pagesPresión de vapor: definición y métodos de determinaciónJuan LuixPas encore d'évaluation
- CALORIMETRIADocument7 pagesCALORIMETRIAerick jhonatanPas encore d'évaluation
- Gravedad EspecificaDocument19 pagesGravedad Especificaivantorres24Pas encore d'évaluation
- Diagramas de Propiedades para Procesos de Cambio de FaseDocument9 pagesDiagramas de Propiedades para Procesos de Cambio de FaseDenni de LeónPas encore d'évaluation
- Leyes de Termodinamica e Instrumentos de MedidaDocument13 pagesLeyes de Termodinamica e Instrumentos de Medidabyron hernan paredes mirandaPas encore d'évaluation
- ClausDocument19 pagesClausArmandocr93100% (1)
- Qué Es Presión de VaporDocument8 pagesQué Es Presión de VaporVanessa HernandezPas encore d'évaluation
- 1er Labo FisicoquimicaDocument34 pages1er Labo Fisicoquimicaanthony de la cruz villanueva100% (1)
- Resumen Ciclo CombinadoDocument18 pagesResumen Ciclo Combinadoperryetrejo100% (1)
- Primera Ley de La TermodinamicaDocument13 pagesPrimera Ley de La TermodinamicaMiguelPas encore d'évaluation
- Procesos TermodinámicosDocument13 pagesProcesos TermodinámicosJosé Luis García VegaPas encore d'évaluation
- Ley Boyle-Mariotte, Charles, Gay-LussacDocument3 pagesLey Boyle-Mariotte, Charles, Gay-LussacWoper GdaPas encore d'évaluation
- Presion de VaporDocument29 pagesPresion de VaporJhonatan Angeles Santa Cruz100% (1)
- Trabajo Instrumentacion - Medicion TemperaturaDocument38 pagesTrabajo Instrumentacion - Medicion TemperaturaMarvin PughPas encore d'évaluation
- Trabajo de Investigación Medición de TemperaturaDocument13 pagesTrabajo de Investigación Medición de TemperaturaGabriel Yucra OquendoPas encore d'évaluation
- Procesos AdiabaticosDocument13 pagesProcesos AdiabaticosMarcelo Davila Carrasco100% (1)
- Gases reales y su aplicación en la industriaDocument20 pagesGases reales y su aplicación en la industriarobertPas encore d'évaluation
- Aire HumedoDocument14 pagesAire HumedoleandroPas encore d'évaluation
- Capacidad Calorifica y Calor EspecificoDocument4 pagesCapacidad Calorifica y Calor Especificosandry montielPas encore d'évaluation
- Ejercicios Resueltos Uso Carta Psicrometrica Nivel II Junio 2020Document15 pagesEjercicios Resueltos Uso Carta Psicrometrica Nivel II Junio 2020Rico Lopez Esperanza100% (1)
- Distribucion BarometricaDocument4 pagesDistribucion BarometricaMaryLuzLimaFloresPas encore d'évaluation
- Gases ideales y realesDocument31 pagesGases ideales y realesLuisa M PadovaniPas encore d'évaluation
- Syllabus Del Curso Fisicoquímica AmbientalDocument8 pagesSyllabus Del Curso Fisicoquímica AmbientalLORENA RAMIREZPas encore d'évaluation
- Perdidas Por FricciónDocument11 pagesPerdidas Por FricciónErick FernandezPas encore d'évaluation
- Entropia y EntalpiaDocument2 pagesEntropia y EntalpiaKsPas encore d'évaluation
- Práctica de laboratorio sobre pérdida por fricciónDocument12 pagesPráctica de laboratorio sobre pérdida por fricciónMIGUEL ANGEL SUAREZ MONTOYAPas encore d'évaluation
- Un Sistema TermodinámicoDocument13 pagesUn Sistema TermodinámicoMax Guzman100% (1)
- Flujo laminar vs turbulento: característicasDocument8 pagesFlujo laminar vs turbulento: característicasRamses RodriguezPas encore d'évaluation
- Conducción Bidimensional Diferencias FinitasDocument18 pagesConducción Bidimensional Diferencias FinitasPaola GarciaPas encore d'évaluation
- Ley de CharlesDocument2 pagesLey de CharlesKelo CastestPas encore d'évaluation
- Ley de BoyleDocument13 pagesLey de BoyleedwtrimoPas encore d'évaluation
- Teoría Del Gas Real: La Relación Exacta Para Gases RealesD'EverandTeoría Del Gas Real: La Relación Exacta Para Gases RealesPas encore d'évaluation
- Protocolo-En-Parkinson FinalDocument22 pagesProtocolo-En-Parkinson FinalYessenia NathyPas encore d'évaluation
- Protocolo Problemas Pies Completo ..Document40 pagesProtocolo Problemas Pies Completo ..Yessenia NathyPas encore d'évaluation
- Audit AdiccionesDocument4 pagesAudit AdiccionesYessenia NathyPas encore d'évaluation
- AHOGAMIENTODocument53 pagesAHOGAMIENTOYessenia Nathy100% (1)
- TRASTORNO-POST-TRAUMATICO CompletoDocument17 pagesTRASTORNO-POST-TRAUMATICO CompletoYessenia NathyPas encore d'évaluation
- El JuegoDocument15 pagesEl JuegoYessenia NathyPas encore d'évaluation
- Terapia ocupacional para trastornos postraumáticosDocument17 pagesTerapia ocupacional para trastornos postraumáticosYessenia NathyPas encore d'évaluation
- TRASTORNO-POST-TRAUMATICO CompletoDocument18 pagesTRASTORNO-POST-TRAUMATICO CompletoYessenia NathyPas encore d'évaluation
- Programas de Intervencion AspergerDocument25 pagesProgramas de Intervencion AspergerJaclyn OlsenPas encore d'évaluation
- Conductismo, Gestal, ReflexologiaDocument62 pagesConductismo, Gestal, ReflexologiaYessenia NathyPas encore d'évaluation
- Caso ClinicoDocument6 pagesCaso ClinicoYessenia NathyPas encore d'évaluation
- EgresosDocument21 pagesEgresosYessenia NathyPas encore d'évaluation
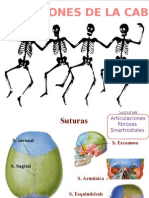
- Imágenes de Articulaciones de La Cabeza.Document13 pagesImágenes de Articulaciones de La Cabeza.Yessenia NathyPas encore d'évaluation
- Articulaciones de La Cabeza y CaraDocument13 pagesArticulaciones de La Cabeza y CaraYessenia NathyPas encore d'évaluation
- Dolor Fisiologia (Autoguardado)Document13 pagesDolor Fisiologia (Autoguardado)Yessenia NathyPas encore d'évaluation
- Necesidad de Contar Con Un Sistema Cardiaco FisiologiaDocument3 pagesNecesidad de Contar Con Un Sistema Cardiaco FisiologiaYessenia NathyPas encore d'évaluation
- Dolor Fisiologia (Autoguardado)Document13 pagesDolor Fisiologia (Autoguardado)Yessenia NathyPas encore d'évaluation
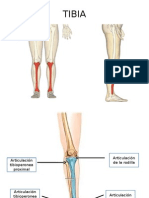
- Tibia (Cuerpo, Extremidad Superior e Inferior)Document14 pagesTibia (Cuerpo, Extremidad Superior e Inferior)Yessenia NathyPas encore d'évaluation
- Dolor FisiologiaDocument8 pagesDolor FisiologiaYessenia NathyPas encore d'évaluation
- Planificacion EstrategicaDocument28 pagesPlanificacion EstrategicaYessenia NathyPas encore d'évaluation
- Borrador Grupo 6Document15 pagesBorrador Grupo 6Yessenia NathyPas encore d'évaluation
- LenguajeDocument2 pagesLenguajeYessenia NathyPas encore d'évaluation
- Aparato RespiratorioDocument35 pagesAparato RespiratorioYessenia NathyPas encore d'évaluation
- Dolor Fisiologia (Autoguardado)Document14 pagesDolor Fisiologia (Autoguardado)Yessenia NathyPas encore d'évaluation
- Teoria Egologica Del Derecho FinalDocument29 pagesTeoria Egologica Del Derecho FinalCarlos Fernando RosalesPas encore d'évaluation
- ITCM Celaya: Potencia de prueba estadística, factores que influyen y cómo aumentarlaDocument4 pagesITCM Celaya: Potencia de prueba estadística, factores que influyen y cómo aumentarlaAraceli AbarcaPas encore d'évaluation
- Tecnicas para El Desarrollo de La CreatividadDocument16 pagesTecnicas para El Desarrollo de La CreatividadFrancisca JavierPas encore d'évaluation
- Cummins Ism Cm876 Codigo de Falla 115Document5 pagesCummins Ism Cm876 Codigo de Falla 115mauricio gomezPas encore d'évaluation
- Monografía Lomas de LúcumoDocument11 pagesMonografía Lomas de LúcumoAnonymous UvY4AtPas encore d'évaluation
- Articulo de Hamburguesa, TerminadoDocument8 pagesArticulo de Hamburguesa, TerminadoAdix Adelia BernillaPas encore d'évaluation
- Proyecto Interdisciplinario 1° TrimestreDocument6 pagesProyecto Interdisciplinario 1° TrimestreJANETH MAGDALENA ROSARIO RIOFRIOPas encore d'évaluation
- Inyectores DieselDocument12 pagesInyectores DieselAlvaro Alexander Aliaga AvilaPas encore d'évaluation
- Tarea OrganizacionalDocument4 pagesTarea Organizacionaljulio diazPas encore d'évaluation
- Oratoria JuridicaDocument1 pageOratoria JuridicaJean Carlos FerraraPas encore d'évaluation
- Unidad 2Document29 pagesUnidad 2David AcostaPas encore d'évaluation
- La Ética en La Toma de Decisiones, Construyendo ConfianzaDocument26 pagesLa Ética en La Toma de Decisiones, Construyendo ConfianzaMaribel OtoyaPas encore d'évaluation
- Formulario queja acoso laboralDocument2 pagesFormulario queja acoso laboraltatiana guevaraPas encore d'évaluation
- FASE 1 Tatiana Puerta Grupo 104Document22 pagesFASE 1 Tatiana Puerta Grupo 104TatisPuertaPas encore d'évaluation
- Cables Con Cargas DistribuidasDocument25 pagesCables Con Cargas DistribuidasYTll Gian llPas encore d'évaluation
- Enfoque de Auditoria ModernaDocument52 pagesEnfoque de Auditoria ModernaYohanita Perez GarciaPas encore d'évaluation
- Derecho de Peticion 3542992022 OkDocument9 pagesDerecho de Peticion 3542992022 OkFelix Armando Celis ValenciaPas encore d'évaluation
- Crónica de Una Izquierda SingularDocument87 pagesCrónica de Una Izquierda SingularPedro ValchsPas encore d'évaluation
- Cómo elaborar y compartir un díptico sobre prevención de enfermedadesDocument4 pagesCómo elaborar y compartir un díptico sobre prevención de enfermedadesMax Carlos MaChPas encore d'évaluation
- Principios de ElectromagnetismoDocument7 pagesPrincipios de ElectromagnetismoAlcantara Ordoñez CitlalliPas encore d'évaluation
- OS136Document2 pagesOS136komodiemoPas encore d'évaluation
- Pronósticos cuantitativos modelosDocument13 pagesPronósticos cuantitativos modelosFlor GonzalezPas encore d'évaluation
- Liderazgo y FlexibilidadDocument6 pagesLiderazgo y FlexibilidadPedroPas encore d'évaluation
- Orden de Entrada o InspeccionDocument1 pageOrden de Entrada o InspeccionEstefanía de FagundezPas encore d'évaluation
- Guia de Prac 2 Inst Electricas 1Document9 pagesGuia de Prac 2 Inst Electricas 1Jose Luis RiveraPas encore d'évaluation
- Teorias Act 3 Cuadro Comparativo JuanDocument20 pagesTeorias Act 3 Cuadro Comparativo JuanJuan Pablo RiverosPas encore d'évaluation
- 3°? Examen Mensual Febrero (2022-2023)Document10 pages3°? Examen Mensual Febrero (2022-2023)Grettel EspinosaPas encore d'évaluation
- Los Siete Puntos Del Entrenamiento de La Mente - AtishaDocument8 pagesLos Siete Puntos Del Entrenamiento de La Mente - AtishahuntedshotPas encore d'évaluation