Académique Documents
Professionnel Documents
Culture Documents
Copia de Regla de Markownikoff
Transféré par
Kampos GtzDescription originale:
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Copia de Regla de Markownikoff
Transféré par
Kampos GtzDroits d'auteur :
Formats disponibles
Regla de Markownikoff
En qumica, la regla de Markovnikov o regla de Markownikoff es una observacin respecto a la reaccin de adicin electrfilica. Fue formulada por el qumico ruso Vladimir Vasilevich Markovnikov en 18701 2 . En una reaccin qumica encontrada particularmente en qumica orgnica, la regla establece que, con la adicin de un reactivo asimtrico del tipo H-X a un alqueno o alquino, el tomo de hidrgeno lbil se une al tomo de carbono del doble o triple enlace con el mayor nmero de tomos de hidrgeno, y el grupo halogenuro (X) se une al tomo de carbono del doble o triple enlace con el menor nmero de tomos de hidrgeno.3 La regla de Markovnikov est ilustrada por la reaccin del propeno con HBr, se indica el mayor producto obtenido Lo mismo es verdad cuando un alqueno reacciona con agua en una reaccin catalizada por cidos minerales, para producir alcoholes. El grupo hidroxilo (OH) se une al tomo de carbono que tiene el mayor nmero de enlaces carbono-carbono, mientras que el tomo de hidrgeno se une al tomo de carbono en el otro extremo del enlace doble, el que tiene el mayor nmero de enlaces carbono-hidrgeno. La base qumica para la regla de Markovnikov es la formacin del carbocatin ms estable, durante el proceso de adicin. La adicin del tomo de hidrgeno a uno de los tomos de carbono origina una carga formal positiva en el otro tomo de carbono, formando un carbocatin intermediario. Mientras ms sustituido est un carbocatin (ms enlaces tiene a otro tomos de carbono u otros sustituyentes electrodonantes), ms estable es, debido al efecto inductivo, hiperconjugacin e impedimento estrico. El producto principal de la reaccin de adicin ser el que tenga el intermediario ms estable. En consecuencia, el producto principal de la adicin del HX (donde X es algn tomo o grupo ms electronegativo que el tomo de hidrgeno) a un alqueno tiene el tomo de hidrgeno en la posicin menos sustituida y el grupo X en la posicin ms sustituidas. Es importante notar que, sin embargo, tambin se formar el carbocatin menos estable, aunque en menor grado, y proceder a formar el producto minoritario con la disposicin de tomos en forma opuesta. Como una mnemotcnica, se puede sumarizar en "el rico se hace ms rico y el pobre se hace ms pobre": un tomo de carbono rico en sustituyentes ganar ms sustituyentes, y el tomo de carbono con ms tomos de hidrgeno unidos ganar ms tomos de hidrgeno.
Contexto histrico
Una de las reacciones orgnicas en las que Markovnikov bas su regla fue la que se da entre el yoduro de hidrgeno con el bromuro de vinilo (efectuada por primera vez en 1865). En otra manifestacin de su regla, observ que el tomo de halgeno se uni al tomo de carbono que ya llevaba un tomo de halgeno. La hidrlisis de halogenuros geminales del
producto inicial de reaccin con xido de plata hmedo o hidrogenado a etanal prob que la sustitucin era 1,1.
Se ha observado2 que la publicacin original de Markovnikov de 1869 era superficial y que no hizo mucho trabajo experimental por l mismo. La regla en s apareci slo como una nota al pie de cuatro pginas en un artculo de 26 pginas,lo que puede ayudar a explicar por qu tmo 60 aos que su regla sea aceptada.
Regla de Anti Markovnikov
Cuando el mecanismo seguido por la reaccin impide la formacin de un intermediario carbocatin, la reaccin puede seguir otros mecanismos que tambin son regioselectivos, pero en contra de las predicciones de la regla de Markovnikov, como la adicin radicalaria. Se dice que tales reacciones son anti-Markovnikov, dado que el tomo de halgeno se une al tomo de carbono menos sustituido. Esta reaccin es exactamente opuesta a la reaccin de Markovnikov en cuanto a sus resultados, y de ah el nombre. Nuevamente, del mismo modo que con la carga positiva, el radical es ms estable cuando est en la posicin ms sustituida. El comportamiento anti-Markovnikov se extiende a otras reacciones qumicas distintas a las simples adiciones a los alquenos. Una manifestacin anti-Markovnikov se observa en la hidratacin del fenilacetileno que, catalizado con oro, produce la acetofenona esperada, pero con un catalizador especial de rutenio4 el otro regioismero 2-fenilacetaldehdo:5
El comportamiento anti-Markovnikov tambin se puede manifestar en ciertas reacciones de transposicin. En una sustitucin nucleoflica formal catalizada por cloruro de titanio (IV) en el compuesto 1 enantiopuro en el esquema seguido, se forman los dos productos racmicos 2a y 2b:6
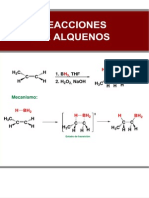
Esta distribucin del producto puede ser racionalizada asumiendo que la prdida del grupo hidroxilo en 1 produce el carbocatin terciario A, que se rearregla al aparentemente menos estable carbocatin secundario B. El cloro puede aproximarse a este centro desde las dos caras, conduciendo a la mezcla observada de ismeros Sin embargo, tal vez el ejemplo ms conocido de adicin anti-Markovnikov es la hidroboracin.
Regla de Hofmann
En qumica orgnica, la regla de Hofmann establece que en una reaccin de eliminacin (-eliminacin) en la que pueda ser formado ms de un alqueno ser mayoritario aquel con el doble enlace menos sustituido. Esta regla es vlida para las reacciones E2 en las que exista un importante impedimento estrico, sustrato ramificado y/o base voluminosa, y sin posibilidad de conjugacin.1 En el resto de situaciones se aplica la regla de Saytzeff.
En qumica orgnica, la regla de Saytzeff, Saytzev o Zaitsev establece que en una reaccin de eliminacin (-eliminacin) en la que pueda ser formado ms de un alqueno ser mayoritario el ms estable termodinmicamente.1 En general, el alqueno ms sustituido es el ms estable, debido a las propiedades de comparticin electrnica de los grupos alquilo con el doble enlace C=C (hiperconjugacin). Tambin, en algunos casos, puede incurrir otro efecto estabilizante a la hora de establecer la regioselectividad como es la conjugacin del doble enlace con otros grupos.
Esta regla es vlida salvo en reacciones de eliminacin bimolecular (E2) en las que exista un impedimento estrico importante, sustrato ramificado y/o base voluminosa, y sin posibilidad de conjugacin, aplicndose entonces la regla de Hofmann. La eliminacin de Hofmann se basa en que las sales de amonio cuaternarias son inestables frente a bases fuertes, las cuales provocan una eliminacin bimolecular (E2) que conduce a alqueno, actuando la trialquilamina como grupo saliente.
En el procedimiento habitual de la eliminacin o degradacin de Hofmann tiene lugar la metilacin exhaustiva de una amina, los grupos metilo unidos al tomo de nitrgeno no podrn sufrir -eliminacin evitndose ambigedades, mediante el empleo de un exceso de yodometano, llegando a la sal de amonio cuaternaria, que es tratada con Ag2O hmedo, fuente de OH-, y calor, teniendo lugar una E2 al ser la trimetilamina un buen grupo saliente.
Por motivos estricos en la eliminacin de Hofmann se forma mayoritariamente la olefina menos sustituida, se puede deducir empleando proyecciones de Newman.
En el confrmero ms abundante, a travs del cual transcurre de forma mayoritaria la reaccin, la E2 estereoespecfica anti slo puede producirse por un sitio. En general, en la eliminacin de Hofmann, la eliminacin bimolecular se produce por la posicin menos sustituida, conduciendo por tanto al alqueno menos sustituido, aunque si es posible la formacin de un sistema conjugado ste primar en la regioselectividad. La eliminacin de Hofmann dio origen, en su primera definicin, a la regla de Hofmann. Antes de la aparicin de los metdos instrumentales de determinacin estructural, la degradacin de Hofmann se empleaba para elucidar la estructura de aminas.
Vous aimerez peut-être aussi
- Ata 32 PDFDocument308 pagesAta 32 PDFArnold CruzadoPas encore d'évaluation
- Resumen de AlquenosDocument9 pagesResumen de AlquenosMariana SalazarPas encore d'évaluation
- Regla de MarkovnikovDocument4 pagesRegla de MarkovnikovDanielPovedaPas encore d'évaluation
- ALQUENOSDocument16 pagesALQUENOSSinuhé JrzPas encore d'évaluation
- Vladímir MarkóvnikovDocument9 pagesVladímir MarkóvnikovLuisAlejandroMorenoBarrigaPas encore d'évaluation
- Mecanismo de Reacción.Document21 pagesMecanismo de Reacción.carlitosvelasquezPas encore d'évaluation
- ALQUENOS y ALquinosDocument18 pagesALQUENOS y ALquinosValentina González100% (1)
- Enunciado de La Regla de MarkovnikovDocument6 pagesEnunciado de La Regla de MarkovnikovGago_880% (1)
- Adición A AlquenosDocument8 pagesAdición A AlquenoscarloschaverriPas encore d'évaluation
- Reacciones de Los AlquenosDocument10 pagesReacciones de Los AlquenosMilagros Valinotti GaunaPas encore d'évaluation
- Alquenos y AlquinosDocument24 pagesAlquenos y AlquinosAngeles AngellsPas encore d'évaluation
- Tema Quimica Organica 1Document15 pagesTema Quimica Organica 1Francisco José Pardo JusticiaPas encore d'évaluation
- Guía de Estudio OrganicaDocument8 pagesGuía de Estudio OrganicaUlises EstigarribiaPas encore d'évaluation
- 9 Reacciones de Adición Alquenos y AlquinosDocument51 pages9 Reacciones de Adición Alquenos y AlquinosMarianoIbañezPas encore d'évaluation
- Alquenos. Métodos de ObtenciónDocument8 pagesAlquenos. Métodos de ObtenciónDouglas RamirezPas encore d'évaluation
- Reacciones Alcanos, Alquenos y Alquinos 2023-2Document76 pagesReacciones Alcanos, Alquenos y Alquinos 2023-2kenlli23gomezPas encore d'évaluation
- Tarea Clase 13 - 10 - 2021Document6 pagesTarea Clase 13 - 10 - 2021Romel Esteban ReyesPas encore d'évaluation
- Cap7Parte3 Reactividad Alquenos Alquinos DienosDocument50 pagesCap7Parte3 Reactividad Alquenos Alquinos DienosSamuel Espinoza GarciaPas encore d'évaluation
- ALQUENOSDocument50 pagesALQUENOSSantiago Ortiz PérezPas encore d'évaluation
- Hidrogenación (Reducción) de AlquinosDocument8 pagesHidrogenación (Reducción) de AlquinosRicardo SierraPas encore d'évaluation
- Arenos y Halogenuros de AriloDocument6 pagesArenos y Halogenuros de ArilosabiPas encore d'évaluation
- 13 Alquenos ReaccDocument40 pages13 Alquenos ReaccRoberto Andres Delgado MillanPas encore d'évaluation
- Regla de MarkovnikovDocument7 pagesRegla de MarkovnikovFLORES05Pas encore d'évaluation
- Alquenos y AlquinosDocument70 pagesAlquenos y AlquinosMaleja Perpiñan BarriosPas encore d'évaluation
- Unidad 2 Reacciones de AdiciónDocument24 pagesUnidad 2 Reacciones de AdiciónRocío Sin Remedio50% (2)
- QMC 302 - Mecanismos de AdiciónDocument67 pagesQMC 302 - Mecanismos de AdiciónAnonymous yEGP9hn0% (1)
- Reacciones de EliminaciónDocument18 pagesReacciones de EliminaciónAcostaHernándezNarda33% (3)
- OXIMERCURACIONDocument4 pagesOXIMERCURACIONNalleli JaimePas encore d'évaluation
- Cap 6 2022Document92 pagesCap 6 2022Fabi AguilarPas encore d'évaluation
- Muchas de Las Reacciones de Los Alquinos SonDocument13 pagesMuchas de Las Reacciones de Los Alquinos SonFrank Pitalua BarbosaPas encore d'évaluation
- Reacciones de AlquenosDocument11 pagesReacciones de AlquenosDarwin MéndezPas encore d'évaluation
- Hidrocarburos AromáticosDocument15 pagesHidrocarburos AromáticosElvis Leonel Temoche SandovalPas encore d'évaluation
- Ozonòlisis de AlquenosDocument26 pagesOzonòlisis de AlquenosLorenzo MinayaPas encore d'évaluation
- Unidad 4 Alquenos U OlefinasDocument13 pagesUnidad 4 Alquenos U OlefinasYulibeth MoraPas encore d'évaluation
- Regla de MarkovnikovDocument3 pagesRegla de MarkovnikovJuan Carlos100% (1)
- Reacciones de AlquenosDocument16 pagesReacciones de AlquenosGabyy ReyesPas encore d'évaluation
- Reactividad de Aldehídos y CetonasDocument19 pagesReactividad de Aldehídos y CetonasDaniel GámezPas encore d'évaluation
- RESUMENDocument7 pagesRESUMENSalma MedinaPas encore d'évaluation
- Tema 2. AlquenosDocument21 pagesTema 2. AlquenosnereaPas encore d'évaluation
- DIENOSDocument12 pagesDIENOSAnaid DianaPas encore d'évaluation
- Estereoselectividad RegioselectividadDocument11 pagesEstereoselectividad RegioselectividadMau OrtegaPas encore d'évaluation
- HalogenacionDocument57 pagesHalogenacionleslie torres riveraPas encore d'évaluation
- Reacciones QuímicasDocument6 pagesReacciones QuímicasJavier GarciaPas encore d'évaluation
- 8 Reacciones de Adición Electrofílica IDocument63 pages8 Reacciones de Adición Electrofílica Isofia garcia moralesPas encore d'évaluation
- ALQUENOS y ALQUINOSDocument13 pagesALQUENOS y ALQUINOSFranco BorgatelloPas encore d'évaluation
- Nomenclatura de Los AnillosDocument2 pagesNomenclatura de Los AnillosAngie OrtizPas encore d'évaluation
- Adicion Electrofilica de AlquinosDocument25 pagesAdicion Electrofilica de AlquinosKimberly TorresPas encore d'évaluation
- ACO Guía de Reacciones OrgánicasDocument5 pagesACO Guía de Reacciones OrgánicasGianni D'Agostini SilvaPas encore d'évaluation
- Mecanismos de ReacciónDocument2 pagesMecanismos de ReacciónPamelaAltamiranoPas encore d'évaluation
- D08 - Bio - Material de Apoyo - 06 - Reacciones de Polimerización de AlquenosDocument30 pagesD08 - Bio - Material de Apoyo - 06 - Reacciones de Polimerización de AlquenosARIANNA MICAELA VELASTEGUI GUERREROPas encore d'évaluation
- S04 - Material PDFDocument49 pagesS04 - Material PDFAlejandro Renato Rengifo LedesmaPas encore d'évaluation
- Reacciones de AlquenosDocument18 pagesReacciones de AlquenosRoger ManzanarezPas encore d'évaluation
- Reacciones de AlquinosDocument8 pagesReacciones de AlquinoskarinaPas encore d'évaluation
- Reacciones de Los AlquenosDocument7 pagesReacciones de Los AlquenosRosario UbieraPas encore d'évaluation
- Compuestos Orgánicos, Química OrgánicaDocument58 pagesCompuestos Orgánicos, Química OrgánicaBea Paola ValenzuelaPas encore d'évaluation
- Manual TeóricoDocument119 pagesManual TeóricoAngel BlancoPas encore d'évaluation
- AlquenosDocument7 pagesAlquenosJorge Luis OsorioPas encore d'évaluation
- Trampas Quimicas. ExposicionDocument27 pagesTrampas Quimicas. ExposicionRaúl FloresPas encore d'évaluation
- Planta de de Hidrocarburos AromaticosDocument3 pagesPlanta de de Hidrocarburos Aromaticosnoelia cossioPas encore d'évaluation
- Cap 1 A Conc BasDocument19 pagesCap 1 A Conc Basjulian51Pas encore d'évaluation
- Practica 4 LabDocument2 pagesPractica 4 Labvictor emanuelPas encore d'évaluation
- INFOGRAFIA BiologiaDocument22 pagesINFOGRAFIA BiologiaNaysha CamavilcaPas encore d'évaluation
- Descomposicion Peroxido de HidrogenoDocument8 pagesDescomposicion Peroxido de HidrogenoDaniel PadillaPas encore d'évaluation
- Macromoléculas InorgánicasDocument371 pagesMacromoléculas InorgánicasCesar VegaPas encore d'évaluation
- EFT Klueberquiet BQH 72 102 ES EsDocument4 pagesEFT Klueberquiet BQH 72 102 ES EsAlejo FlorezPas encore d'évaluation
- Pliego 1398195079119Document229 pagesPliego 1398195079119mashulPas encore d'évaluation
- Penetrómetro PeruDocument12 pagesPenetrómetro PerudeehessePas encore d'évaluation
- Andre EeeeDocument6 pagesAndre EeeeMaribel Valero RamosPas encore d'évaluation
- Formato de Datos de SeguridadDocument14 pagesFormato de Datos de SeguridadBritany Jeanne Aguilar ViverosPas encore d'évaluation
- Previo 2 Analitica 3. PolarografíaDocument4 pagesPrevio 2 Analitica 3. Polarografíagancho2010Pas encore d'évaluation
- Calculos Nitritos y AlmidonDocument6 pagesCalculos Nitritos y AlmidonJarin SaaPas encore d'évaluation
- Guia Ejercicio ConcentracionDocument16 pagesGuia Ejercicio Concentraciondilmar86Pas encore d'évaluation
- Capitulo 10. Formulas MagistralesDocument36 pagesCapitulo 10. Formulas MagistralesKeni Guerra Huaman0% (1)
- FideosDocument13 pagesFideosGabriela De La Cruz PayanoPas encore d'évaluation
- Lubricación Adecuada para El Torno CNCDocument5 pagesLubricación Adecuada para El Torno CNCGerardo Arreola GalvanPas encore d'évaluation
- Tarea 5-Transformacion de La MateriaDocument2 pagesTarea 5-Transformacion de La MateriaYol EnríquezPas encore d'évaluation
- 27 100 Msds Sellador PvaDocument5 pages27 100 Msds Sellador PvaDAvid Alvarez CastilloPas encore d'évaluation
- Informe Cresta DelgadaDocument4 pagesInforme Cresta DelgadaAndres Escorcia100% (1)
- Destilacion Simple y FraccionadaDocument6 pagesDestilacion Simple y FraccionadaSthefanía Elizabeth TisalemaPas encore d'évaluation
- Matriz Batelle Columbus 2023Document8 pagesMatriz Batelle Columbus 2023Efrain Rondon MondalgoPas encore d'évaluation
- Cementación de CarillasDocument2 pagesCementación de CarillasJessica Ninoska Ramos HerradaPas encore d'évaluation
- Reg 89E GNCDocument12 pagesReg 89E GNCfabiostefania100% (1)
- Lodos ActivosDocument27 pagesLodos ActivosRut RomeroPas encore d'évaluation
- SuperficiesDocument22 pagesSuperficiesGuevara ManuelPas encore d'évaluation
- Guia Practica Quimica - 2023-1 (WORD)Document100 pagesGuia Practica Quimica - 2023-1 (WORD)Lipsa Magaly Amasifuen MacahuachiPas encore d'évaluation
- Gas en TanquesDocument9 pagesGas en TanquesRicardo ÁlvarezPas encore d'évaluation
- Practica 1 Circuitos EléctronicosDocument13 pagesPractica 1 Circuitos EléctronicosFredy Copa VillalbaPas encore d'évaluation