Académique Documents
Professionnel Documents
Culture Documents
Koloid
Transféré par
-hany Ukhibbu Umi-0 évaluation0% ont trouvé ce document utile (0 vote)
119 vues34 pagesSistem koloid merupakan campuran dua fase di mana fase terdispersi berukuran antara 1-1000 nm tersebar dalam fase kontinu. Terdapat tiga jenis sistem koloid berdasarkan ukuran partikelnya yaitu dispersi molekuler, koloid, dan dispersi kasar. Sistem koloid dapat distabilisasi menggunakan surfaktan dan memiliki berbagai penerapan di bidang farmasi seperti meningkatkan kelarutan dan absorpsi obat.
Description originale:
Titre original
3._Koloid
Copyright
© © All Rights Reserved
Formats disponibles
PPT, PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentSistem koloid merupakan campuran dua fase di mana fase terdispersi berukuran antara 1-1000 nm tersebar dalam fase kontinu. Terdapat tiga jenis sistem koloid berdasarkan ukuran partikelnya yaitu dispersi molekuler, koloid, dan dispersi kasar. Sistem koloid dapat distabilisasi menggunakan surfaktan dan memiliki berbagai penerapan di bidang farmasi seperti meningkatkan kelarutan dan absorpsi obat.
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PPT, PDF, TXT ou lisez en ligne sur Scribd
0 évaluation0% ont trouvé ce document utile (0 vote)
119 vues34 pagesKoloid
Transféré par
-hany Ukhibbu Umi-Sistem koloid merupakan campuran dua fase di mana fase terdispersi berukuran antara 1-1000 nm tersebar dalam fase kontinu. Terdapat tiga jenis sistem koloid berdasarkan ukuran partikelnya yaitu dispersi molekuler, koloid, dan dispersi kasar. Sistem koloid dapat distabilisasi menggunakan surfaktan dan memiliki berbagai penerapan di bidang farmasi seperti meningkatkan kelarutan dan absorpsi obat.
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PPT, PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 34
Penggolongan Koloid
Type sistem koloid
Type surfaktan
Sifat koloid
Aplikasi di bidang farmasi
Kesetimbangan Membran Donnan
Bila 2 substansi berbeda dicampur bersama sehingga
bercampur maka akan membentuk system 2 komponen
Bila satu komponen didistribusikan secara menyeluruh
kadalam koponen kedua maka :
fase pertama disebut fase terdispersi
komponen kedua disebut medium dispersi atau fase kontinue
Jadi system dispersi merupakan adanya fase terdispersi
dalam medium dispersi
Penggolongan system terdispers berdasarkan ukuran partikel.
Golongan Sifat Sistem Contoh
Dispersi
Molecular
(< 1 nm)
Partikel tidak terlihat dalam mikroskop
electron, dapat melewati ultrafiltrasi dan
membran semipermeabel, bersifat homogen
Molekul
oksigen, ion-
ion umumnya,
glukosa
Dispersi
Koloid
(0,5 1 nm)
Partikel tidak dilihat oleh mikroskop biasa
tapi bisa dengan mikroskop elektron, dapat
melewati kertas saring tapi tidak dapat
melewati membran semipermeabel, bersifat
heterogen
Sol perak
koloidal,
polimer alam
dan polimer
sisntetis
Dispersi
Kasar
(> 0,5 nm)
Partikel terlihat dibawah mikroskop, tidak
dapat melewati kertas saring normal,
bersifat heterogen
Butir-butir
pasir, emulsi
dan suspensi
farmasetik
CHEM1405 5
Properties of Solutions, Colloids, and
Suspensions
Property Solution Colloid Suspension
Particle Size 0.1-1.0 nm 1-1000 nm >1000 nm
Settles on
Standing?
No No Yes
Filter with
Paper?
No No Yes
Separate by
Dialysis?
No Yes Yes
Homogeneous? Yes Borderline No
CHEM1405 6
Colloids
red colloidal hydrous
iron (III) oxide
Addition of Al
2
(SO
4
)
3
soln
causing Coagulation of the
colloidal iron oxide
Partikel yang terletak dalam jangkauan ukuran koloid
mempunyai luas permukaan yang sangat besar
dibandingkan dengan luas permukaan partikel-partikel
besar dengan volume yang sama
Penerapan dalam bidang farmasi adalah untuk
mempertinggi efektifitas obat, contohnya :
Kalomel koloidal, daya antiseptiknya lebih tinggi
Serbuk sulfur absorpsinya lebih baik
Polimer sintetis digunakan sebagai bahan penyalut pada bentuk
sediaan padat
Elektrolit kololidal (zat aktif permukaan) digunakan untuk
mempertinggi kelarutan, stabilitas dan rasa dari senyawa
tertentu
CHEM1405 8
Types of Colloidal Dispersions
Type Particle Phase Medium Phase Example
Foam Gas Liquid Whipped Cream
Solid Foam Gas Solid Floating Soap
Aerosol Liquid Gas Fog, hairspray
Liquid Emulsion Liquid Liquid Milk, Mayonnaise
Solid Emulsion Liquid Solid Butter
Smoke Solid Gas Fine dust or soot
in air
Sol Solid Liquid Starch Solutions,
Jellies
Solid Sol Solid Solid Pearl
CHEM1405 9
Dialysis
Dialysis is a process that separates
solvent and small molecules and ions
from large ones by allowing the smaller
particles to pass through a membrane
that blocks the larger ones.
Uses a different type of membrane than
osmosis
CHEM1405 10
Dialysis
In dialysis, molecules
and ions always diffuse
from areas of higher
concentration to areas
of lower concentration.
Dialysis
Blood cells & plasma proteins fall in the
colloidal size range and will be retained,
while impurities pass through the dialysis
membrane
Artificial Kidney
Hemodialysis Device
Hemodialysis
Counter Current
(Shell&Tube) Membrane
Blood
DI Water
Series of Resistances
Mass Transfer
Blook
Water
Diffusion in Membrane
Urea
Byproducts
CHEM1405 14
Kidneys
Kidneys Eliminate certain
wastes by Dialysis
Smaller molecules pass
through dialysis
membrane, larger colloids
(Blood cells) do not
CHEM1405 15
Kidney Dialysis Machine
Kidney functions
can be replaced
by a dialysis
machine
Smaller molecules
pass through
dialysis
membrane, larger
colloids (Blood
cells) do not
Tipe Sistem Koloid
1. Koloid Liofilik (suka solvent)
Pada koloid tipe ini, partikel fase dispers
berinteraksi dengan medium dispers) dan
membentuk dispersi koloid atau sol dengan mudah,
contohnya :
gelatin, gom, insulin, albumin (media air ; sol hidrofilik)
Karet, polistiren (media pelarut organic)
Karena partikel fase dispers tersolvatasi dalam
medium dispers maka koloid ini stabil.
2. Koloid Liofobik (benci solvent)
Partikel fase dispers tidak berinteraksi (ikatan sangat
lemah) dengan medium dispers karena partikel fase
dispers tidak tersolvatasi.
Koloid liofobik umumnya tersusun dari partikel-
partikel anorganik yang terdispers dalam air, missal
emas, perak, belerang, arsen, sulfida dan perak
iodida
Pembentukan sol relatif susah
Untuk menyiapkan koloid liofob dari kolid liofilik
dapat dilakukan dengan metode dispersi dan metode
kondensasi.
3. Koloid Assosiasi (gabungan)
Koloid ini bersifat ampifil.. Membentuk koloid jika
kadar partikel fase dispers (dalam hal ini berupa
surfaktan) melebihi critical micelle concentration
(CMC).
Jika kadar fase disper masih dibawah CMC, ampifil
berada terpisah dan mempunyai ukuran subkoloid.
Jika konsentrasi ditingkatkan, terjadi agregasi pada
suatu jangkauan konsentrasi yang sempit. Agregat
ini disebut misel yang berada dalam daerah ukuran
koloid.
Koloid Assosiasi (cont)
Fenomena pembentukan misel adalah sebagai berikut :
Jika kadar fase dispers masih dibawah CMC maka fase dispers
diadsorpsi pada antarmuka terus menerus
Suatu saat antarmuka jenuh dengan fase dispers, penambahan
fase dispers berikutnya akan beragregasi membentuk misel
(yang ukurannya termasuk dimensi koloid).
Surfactants decrease surface tension
Critical micelle concentration (CMC)
-Surface tension decreases with increasing surfactant concentration untill
the surface is fully occupied
-Thus is valid until the surface is fully occupied
-Further increase of surfactant concentration: surfactant molecules are
forced to enter the bulk of the solution
- In the bulk of the solution, surfactant molecules form micelles
Micelle in hydrophilic liquid
+
+
Micelle in hydrophobic liquid
Also other morphologies are possible
a ln d RT d
CMC and aggregation # of some surfactants
Factors affecting CMC and micelle size
Structure of hydrophobic
group
Nature of hydrophilic
group
Nature of counter ions
Addition of electrolytes to
ionic surfactants
decreases CMC and
increase size
Effect of temperature
Solubilization
The ability of the micelles to increase the solubility of
materials that are normally insoluble or only slight soluble
in the dispersion medium.
Properties of Colloids
Optical Properties
The Faraday-Tyndall Effect
Electron Microscope
Light Scattering
Kinetic Properties
Brownian Motion
Diffusion
Sedimentation
Electrical Properties
Electrokinetic Phenomena
CHEM1405 26
Tyndall Effect
Light is scattered by Colloid
Colloidal
Iron(III) Oxide
Scatters light
A Solution
Does not
Scatter light
CHEM1405 27
Stabilization of Colloids
Colloids can
be stabilized
by surface
interactions
Colloids: Applications
Increased therapeutic properties
Proteins natural colloids
Polymers blood substitutes, coating agents
Association colloids - solubilization
Kesetimbangan Membran Donnan
Pada membran semipermeabel ion-ion kecil (seperti
Na+ Cl-) dapat berpindah (diffusible ion) sedang ion-ion
koloid tidak dapat melewati membran (non-diffusible
ion).
Sistem dalam kesetimbangan dinyatakan dalam diagram
berikut, dimana R- adalah anion koloid yang tidak dapat
berdifusi dan garis tegak yang memisahkan berbagai
jenis zat mewakili membran semipermeabel
Volume larutan pada kedua sisi dianggap sama.
Di luar (o) Di dalam (i)
R-
Na+ Na+
Cl- Cl-
Setelah tercapai kesetimbangan, konsentrasi natrium
klorida dalam larutan encer harus sama pada kedua sisi
membran
[Na+]o [Cl-]o = [Na+]i [Cl-]I (1)
Kondisi elektronetralitas harus pula diterapkan, jadi
kinsentrasi ion-ion bermuatan positif dalam larutan pada
kedua sisi membran harus seimbang dengan
konsentrasi ion-ion yang bermuatan negatif
Di luar : [Na+]o = [Cl-]o (2)
Di dalam : [Na+]i = [R-]i + [Cl-]i (3)
Bila persamaan disederhanakan dan persamaan (2) dan (3)
disubstitusikan kedalam persamaan (1) maka :
[Cl-]o [R-]i
= 1 + (4)
[Cl-]I [Cl-]I
Persamaan (4) merupakan perbandingan konsentrasi anion yang
berdifusi diluar dan di dalam membran pada kesetimbangan
Adanya non diffusible ion pada sisi membran dalam akan
mempengaruhi kecepatan masuknya anion
Hal ini disebabkan muatan yang sama akan saling tolak, sehingga
non diffusible ion akan mengusir anion keluar membran.
Higuchi, dkk. menggunakan rumus diatas untuk melihat kegunaan
polielektrolit Na CMC untuk menambah absorpsi obat seperti Na
Salisilat dan kalium benzil penisilin.
Jika [D-]o anion obat diluar membran
[D-]i anion di dalam membran
[R-]o digunakan untuk menyatakan konsentrasi Na CMC pada
kesetimbangan sehingga didapatkan :
[D-]o [R-]i
= 1 + (5)
[D-]I [D-]i
Jika [R-] i / [D-]i = 8 maka [D-]o / [D-]i = 3
Jika [R-] i / [D-]i = 99 maka [D-]o / [D-]i = 10
Jadi jika kadar [R-] meningkat maka absorpsi dapat ditingkatkan
Contoh Soal :
Suatu larutan karboksimetilseluloa disetimbangkan
menyeberangi suatu lmembran semipermeabel dengan
larutan natrium salisilat. Hitung perbandingan salisilat
pada kedua sisi membran pada kesetimbangan dengan
menganggap bahwa konsentrasi karboksimetilselulosa
pada kesetimbangan adalah 1,2 x 10
-2
gram
ekivalen/liter dan konsentrasi natrium salisilat pada
kesetimbangan 6,0 x 10
-3
.
Vous aimerez peut-être aussi
- Sistem Dispersi BCM 2017Document68 pagesSistem Dispersi BCM 2017poppy0% (1)
- Koloid dan Sistem DispersiDocument38 pagesKoloid dan Sistem DispersiKoming SukawatiPas encore d'évaluation
- KOLOIDDocument55 pagesKOLOIDMarLeniRNPas encore d'évaluation
- OPTIMALKOLOIDDocument27 pagesOPTIMALKOLOIDDoris PuspitasariPas encore d'évaluation
- KOLOIDDocument7 pagesKOLOIDAulia FebriantyPas encore d'évaluation
- Koloid 1Document38 pagesKoloid 1SriWahyuningsihPas encore d'évaluation
- KOLOIDDocument41 pagesKOLOIDLany Nila100% (1)
- KOLOID FarfisDocument45 pagesKOLOID Farfishera joesandyPas encore d'évaluation
- Makalah Sistem KoloidDocument6 pagesMakalah Sistem KoloidFifin FinCifer Finida100% (1)
- KOLOID OPTIMALDocument36 pagesKOLOID OPTIMALAnnisa'u Warosatul AnbiyaPas encore d'évaluation
- dispersiDocument53 pagesdispersiCharina AnatacyaPas encore d'évaluation
- Ringkasan KoloidDocument6 pagesRingkasan KoloidYakoeza HanZouPas encore d'évaluation
- Ringkasan Koloid (Kimia SMA Kelas 11)Document11 pagesRingkasan Koloid (Kimia SMA Kelas 11)akusukamakantelur100% (4)
- OPTIMIZED TITLEDocument30 pagesOPTIMIZED TITLEFeri MustafaPas encore d'évaluation
- Koloid AnalisisDocument13 pagesKoloid AnalisisWilly Prayoga NugrahaPas encore d'évaluation
- Sistem KoloidDocument27 pagesSistem KoloidVianindyPas encore d'évaluation
- Bagi 'KOLOID-WPS Office - Doc'Document7 pagesBagi 'KOLOID-WPS Office - Doc'Nur Afifah RizkiPas encore d'évaluation
- KoloidDocument23 pagesKoloidDyah Putri Ayu DinastyarPas encore d'évaluation
- KoloidDocument7 pagesKoloidshintaPas encore d'évaluation
- Dispersi Cair EmulsiDocument45 pagesDispersi Cair EmulsiSiti MasitoPas encore d'évaluation
- KFT Kel 6 KoloidDocument24 pagesKFT Kel 6 KoloidEster naully Sansalia FlorensisPas encore d'évaluation
- 2 KoloidDocument29 pages2 KoloidSherlyPas encore d'évaluation
- KoloidDocument35 pagesKoloidYakoeza HanZouPas encore d'évaluation
- Koloid Sistem DispersiDocument20 pagesKoloid Sistem DispersiBaim Black RushPas encore d'évaluation
- Soal KoloidDocument36 pagesSoal KoloidHilda SusantiPas encore d'évaluation
- KOLOIDA KOLOIDDocument18 pagesKOLOIDA KOLOIDSeptina AzridaPas encore d'évaluation
- Laporan Kimia KoloidDocument16 pagesLaporan Kimia KoloidSugiarto Restu JefryPas encore d'évaluation
- PENGERTIAN DAN JENIS KOLOIDDocument22 pagesPENGERTIAN DAN JENIS KOLOIDSiti Nur HalizaPas encore d'évaluation
- Ringkasan Materi Koloid PDF FreeDocument11 pagesRingkasan Materi Koloid PDF FreeAyaPas encore d'évaluation
- Bank Soal Kelas XI - KoloidDocument16 pagesBank Soal Kelas XI - KoloiddhinaranidhPas encore d'évaluation
- Farmasi Fisika PPT Farfis FixDocument15 pagesFarmasi Fisika PPT Farfis FixSuratiPas encore d'évaluation
- Sistem KoloidDocument8 pagesSistem Koloidcamelia nurasifaPas encore d'évaluation
- Makalah KoloidDocument15 pagesMakalah Koloidisminurfaizah60% (5)
- Sifat-Sifat Koloid SelDocument33 pagesSifat-Sifat Koloid SelSusy Hilza FatwaPas encore d'évaluation
- Sistem KoloidDocument54 pagesSistem KoloidFitriPas encore d'évaluation
- Review KoloidDocument4 pagesReview Koloidintania111Pas encore d'évaluation
- KoloidDocument42 pagesKoloidYanuarPas encore d'évaluation
- Dispersi KoloidDocument30 pagesDispersi KoloidSilvi PrisayulilahPas encore d'évaluation
- Laporan Praktikum Kimia Mengenal Sistem KoloidDocument10 pagesLaporan Praktikum Kimia Mengenal Sistem KoloidSatrio Ras SwastaPas encore d'évaluation
- Koloid dan SifatnyaDocument3 pagesKoloid dan SifatnyaAffanPas encore d'évaluation
- Pengertian Dan Jenis KoloidDocument13 pagesPengertian Dan Jenis KoloidMazboymentcankcLiquerzdjourney Menggapaisenjaygpernahiamliki FromguembowcwoxzupernguaLemzPas encore d'évaluation
- DISPERSI KOLOIDDocument31 pagesDISPERSI KOLOIDtutiPas encore d'évaluation
- koloid-PERTEMUAN 10Document31 pageskoloid-PERTEMUAN 10shadamPas encore d'évaluation
- Makalah KoloidDocument11 pagesMakalah KoloidAsdar Daeng BacoPas encore d'évaluation
- Koloid FarfisDocument6 pagesKoloid FarfisJunaedi JunaediPas encore d'évaluation
- Sistem KoloidDocument11 pagesSistem KoloidNico DarmawanPas encore d'évaluation
- Sifat Fisika Kimia KosmetikDocument43 pagesSifat Fisika Kimia KosmetikRanti Wahyuningtiyas100% (1)
- SINGKAT KOLOIDDocument8 pagesSINGKAT KOLOIDAyu Aprida IIPas encore d'évaluation
- KoloidDocument42 pagesKoloidFadeliPas encore d'évaluation
- Farfis Makalah KoloidDocument7 pagesFarfis Makalah KoloidLukluil maknunPas encore d'évaluation
- Aplication JobstreetDocument8 pagesAplication JobstreetHiranda WildayaniPas encore d'évaluation
- Pembuatan EskrimDocument7 pagesPembuatan EskrimbintisyarifPas encore d'évaluation
- KoloidDocument16 pagesKoloidNurul HumairahPas encore d'évaluation
- Laporan Kimia Dasar II Pembuatan Dan Sifat Koloid (Dimas)Document14 pagesLaporan Kimia Dasar II Pembuatan Dan Sifat Koloid (Dimas)Laila Majnun Hutagaol100% (5)
- Materi DispersiDocument49 pagesMateri DispersiNur QomariyahPas encore d'évaluation
- Kelompok 2 KoloidDocument54 pagesKelompok 2 KoloidAL SwendoPas encore d'évaluation
- EFEK TYNDALL PADA KOLIODDocument9 pagesEFEK TYNDALL PADA KOLIODAgung Dwi RahmawanPas encore d'évaluation
- MAKALAH KIMIA KoloidDocument10 pagesMAKALAH KIMIA KoloidAhkamPas encore d'évaluation
- GCDocument97 pagesGC-hany Ukhibbu Umi-Pas encore d'évaluation
- Resep Dan Cara Membuat Batagor Enak Dan Gurih Khas BandungDocument2 pagesResep Dan Cara Membuat Batagor Enak Dan Gurih Khas Bandung-hany Ukhibbu Umi-Pas encore d'évaluation
- Patin Asam PedasDocument11 pagesPatin Asam Pedas-hany Ukhibbu Umi-Pas encore d'évaluation
- Sumber Energi Untuk Kontraksi OtotDocument3 pagesSumber Energi Untuk Kontraksi Otot-hany Ukhibbu Umi-100% (1)
- Bab12 SistemendogrinDocument9 pagesBab12 SistemendogrinNovi LisnawatiPas encore d'évaluation
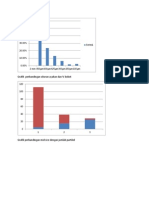
- Grafik Perbandingan Ukuran Ayakan DanDocument1 pageGrafik Perbandingan Ukuran Ayakan Dan-hany Ukhibbu Umi-Pas encore d'évaluation
- IbuDocument1 pageIbu-hany Ukhibbu Umi-Pas encore d'évaluation
- Alkaloid Rev 2Document2 pagesAlkaloid Rev 2-hany Ukhibbu Umi-Pas encore d'évaluation
- Nilai Bahan AlamiDocument16 pagesNilai Bahan Alami-hany Ukhibbu Umi-Pas encore d'évaluation
- Steroid 130629202514 Phpapp01Document16 pagesSteroid 130629202514 Phpapp01-hany Ukhibbu Umi-Pas encore d'évaluation
- Makalah Tentang RosellaDocument6 pagesMakalah Tentang RosellaAgus SantosoPas encore d'évaluation
- Simplisia Tanaman ObatDocument15 pagesSimplisia Tanaman Obat-hany Ukhibbu Umi-Pas encore d'évaluation
- Tugas Farmakologi TambahanDocument6 pagesTugas Farmakologi Tambahan-hany Ukhibbu Umi-Pas encore d'évaluation
- Kelompok Vi BiokimiaDocument9 pagesKelompok Vi Biokimia-hany Ukhibbu Umi-Pas encore d'évaluation
- Pedoman Karya TulisDocument4 pagesPedoman Karya TulisDhanie Ardhan Alvar PosposPas encore d'évaluation
- Aspirin Dari Asam AnhidridaDocument2 pagesAspirin Dari Asam Anhidrida-hany Ukhibbu Umi-Pas encore d'évaluation
- Gula CantikDocument1 pageGula Cantik-hany Ukhibbu Umi-Pas encore d'évaluation
- Cara Buat Omelet SederhanaDocument1 pageCara Buat Omelet Sederhana-hany Ukhibbu Umi-Pas encore d'évaluation
- Ciri Fisik Dari Madu AsliDocument1 pageCiri Fisik Dari Madu Asli-hany Ukhibbu Umi-Pas encore d'évaluation
- Nilai Bahan AlamiDocument16 pagesNilai Bahan Alami-hany Ukhibbu Umi-Pas encore d'évaluation