Académique Documents
Professionnel Documents
Culture Documents
Medición de La Acidez
Transféré par
Jesus_Emilio_M_3632Description originale:
Titre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Medición de La Acidez
Transféré par
Jesus_Emilio_M_3632Droits d'auteur :
Formats disponibles
1.
Medicin de la acidez
Un cido carboxlico se puede disociar en agua para dar un protn y un in carboxilato. La constante de equilibrio Ka para esta reaccin se llama constante de acidez. El pKa de un cido es el logaritmo negativo de Ka, y normalmente se usa al pKa como indicacin de la acidez relativa de diferente cidos. 2. Efectos de los sustituyentes sobre la acidez.
Un sustituyente que estabilice al in carboxilato, con carga negativa, aumenta la disociacin y produce un cido ms fuerte. De este modo los tomos electronegativos aumentan la fuerza de un cido. Este efecto inductivo puede ser muy grande si estn presentes uno o ms grupos que atraen electrones en el tomo de carbono alfa. La magnitud del efecto de un sustituyente depende de su distancia al grupo carboxilo. Los sustituyentes en el tomo de carbono alfa son los ms eficaces para aumentar la fuerza de un cido. Los sustituyentes ms distantes tienen efectos mucho ms pequeos sobre la acidez, mostrando que los efectos inductivos decrecen rpidamente con la distancia. 4- Sales de acidos carboxilicos. Una base fuerte puede desprotonar completamente en un cido carboxlico. Los productos son el in carboxilato, el catin que queda de la base, y agua. La combinacin de un in carboxilato y un catin constituyen la sal de un cido carboxlico.
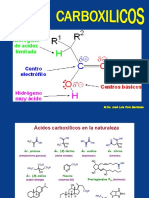
Comportamiento cido
Comportamiento cido: el hidrgeno del grupo hidroxilo de los cidos carboxlicos presenta un pKa comprendido entre 4 y 5, valores relativamente bajos que tienen su explicacin en la importante electronegatividad del grupo carbonilo al que est unido y a la estabilizacin por resonancia de la base conjugada. Nomenclatura
cidos carboxlicos. Cuando el grupo carboxilo es la funcin principal se antepone la palabra cido al nombre del hidrocarburo correspondiente acabado en -oico.
Cuando en un compuesto hay tres o ms grupos COOH y en caso de cidos cclicos se utiliza el sufijo -carboxlico.
Cuando el grupo COOH se considera como sustituyente se utiliza el prefijo carboxi. Sales. Se sustituye la terminacin -ico del cido por la terminacin -ato.En caso de que se haya utilizado el sufijo -carboxlico para nombrar el cido se sustituye por -carboxilato.A continuacin el nombre del metal correspondiente.
Acidez y grupos electronegativos
Los grupos electronegativos aumentan la acidez del los cidos carboxlicos ya que roban carga por efecto inductivo, estabilizando la base conjugada (ion carboxilato). En la siguiente tabla puede observarse la disminucin de pKa que se produce al introducir halgenos en la cadena carbonada, llegndose incluso a valores cercanos a cero. Compuesto pKa CH3COOH ClCH2COOH 4,75 2,86
Cl2CHCOOH Cl3CCOOH
1,26 0,64
F3CCOOH 0,23 Los cidos carboxlicos ocupan un lugar importante dentro de la qumica orgnica, dado que sirven para la construccin de derivados relacionados, como steres y amidas. Tambin son importantes en la sntesis orgnica de muchas otras molculas. Algunos ejemplos importantes son el cido clico, uno de los principales componentes de la bilis humana, y los cidos alifticos de cadena larga como el cido oleico y el cido linoleico, precursores biolgicos de grasas y otros lpidos. Tambin se encuentran en la naturaleza muchos cidos carboxlicos saturados simples. Por ejemplo, el cido actico, CH3CO2H, es el principal componente orgnico del vinagre; el cido butanoico, CH3CH2CH2CO2H, es el que da el olor a la mantequilla rancia, y el cido hexanoico (cido caproico), CH3(CH2)4CO2H, es la causa del inconfundible olor de las cabras y de los calcetines deportivos despus de hacer ejercicios. Los cidos carboxlicos tienen un pKa bajo (pH menor que 7.0) es decir son compuestos cidos. Por lo tanto la desprotonacin para dar carboxilato es relativamente fcil, mientras que la protonacin es ms difcil. Suelen reaccionar con bases como el hidrxido de sodio y bicarbonato de sodio para formar las sales correspondientes.
Un cido carboxlico (insoluble en agua)
Una sal de cido carboxlico (soluble en agua)
Los cidos carboxlicos suelen disociarse ligeramente en soluciones acuosas para formar H3O+ y el anin carboxilato, RCOO-. Como en todo cido, es posible definir una constante de acidez, Ka.
Casi en la mayora de los cidos carboxlicos, la constante de acidez Ka es del orden de 10-5, que corresponde a un pKa de 4.72. la acidez de los acidos carboxlicos es la mas fuerte de los acidos orgnicos pero no tanto como los inorgnicos. Estos presentan propiedades acidez fuertes en comparacin con otros acidos organicos debido a la estabilidad relativa de la base conjugada que es el ion carboxilato COO-. La estabilidad de esta especie en solucin acuosa se debe a que en este estado se distribuye mejor la carga negativa, esta es resonante(de resonancia) entre los dos oxigenos, el del doble enlace con carbono y el desprotonado.
Vous aimerez peut-être aussi
- Estatus ácido-base: Conceptos, desequilibrios e interpretaciónD'EverandEstatus ácido-base: Conceptos, desequilibrios e interpretaciónPas encore d'évaluation
- Unidades de AprendizajeDocument12 pagesUnidades de AprendizajeKristel Banda showPas encore d'évaluation
- Mecanismo Del Proceso de Saponificación de ÉsteresDocument31 pagesMecanismo Del Proceso de Saponificación de ÉsteresPedro Gerardo Trejo Flores50% (2)
- Acidos CarboxilosDocument22 pagesAcidos CarboxilosFERNANDO MENDEZ GONZALEZPas encore d'évaluation
- Quim310 - Tema 5 - Ácidos Carboxílicos y Derivados-Quim310-202320Document40 pagesQuim310 - Tema 5 - Ácidos Carboxílicos y Derivados-Quim310-202320121150unPas encore d'évaluation
- ÁCIDOS CARBOXILICOS EnviarDocument29 pagesÁCIDOS CARBOXILICOS EnviarNicole95gmail.com 101295Pas encore d'évaluation
- Ácidos Carboxílicos. Teoría Final 2021Document20 pagesÁcidos Carboxílicos. Teoría Final 2021Rosa Angela GarciaPas encore d'évaluation
- De Acidos CarboxilicosDocument7 pagesDe Acidos CarboxilicosEdwin Loza CoaquiraPas encore d'évaluation
- Clase 1 A PDFDocument20 pagesClase 1 A PDFBarbara Belen Mejia ConformePas encore d'évaluation
- Acidos CarboxilicosDocument32 pagesAcidos CarboxilicosjoglijobPas encore d'évaluation
- Informe de Acidos CarboxilicosDocument16 pagesInforme de Acidos CarboxilicosGermanAvellaPas encore d'évaluation
- Ácidos Carboxílicos y DerivadosDocument31 pagesÁcidos Carboxílicos y DerivadosEliana GuardaPas encore d'évaluation
- Acidos CarboxilicosDocument21 pagesAcidos CarboxilicosGabriela Gonzalez100% (1)
- Acidos Carboxilicos. InfDocument37 pagesAcidos Carboxilicos. InfIvanov100% (1)
- Exo QuimicaDocument26 pagesExo Quimicayuribel rodriguezPas encore d'évaluation
- ACIDEZ DE ACIDOS CARBOXILICOS Jairo Perez PDFDocument7 pagesACIDEZ DE ACIDOS CARBOXILICOS Jairo Perez PDFAntonio MalavePas encore d'évaluation
- Guia 1 Quimica Once 3PDocument3 pagesGuia 1 Quimica Once 3PArmandoMartinezPas encore d'évaluation
- Acidos Carboxilicos AromaticosDocument29 pagesAcidos Carboxilicos AromaticosEsteban MendezPas encore d'évaluation
- Ácidos Carboxílicos.Document26 pagesÁcidos Carboxílicos.Jonathan BalancanPas encore d'évaluation
- Acidez 3 y Mec. BuenoDocument138 pagesAcidez 3 y Mec. BuenoasdafadPas encore d'évaluation
- Acidez en Moléculas OrganicasDocument109 pagesAcidez en Moléculas OrganicasAlicia SanchezPas encore d'évaluation
- Ácidos y BasesDocument24 pagesÁcidos y BasesomarguerrawarPas encore d'évaluation
- Ácidos Carboxílicos y Sus DerivadosDocument3 pagesÁcidos Carboxílicos y Sus DerivadosIbed VargasPas encore d'évaluation
- Resumen de Sintesis de ÁcidosDocument8 pagesResumen de Sintesis de ÁcidosDíaz Centellas Luis AdriánPas encore d'évaluation
- Acidos Carboxilicos - y Derivados Universidad Nacional de TrujilloDocument54 pagesAcidos Carboxilicos - y Derivados Universidad Nacional de TrujilloUsuario1234Pas encore d'évaluation
- Unidad IV D Ácidos y BasesDocument16 pagesUnidad IV D Ácidos y BasesJORGE SALOMONPas encore d'évaluation
- Acidos CarboxilicosDocument19 pagesAcidos CarboxilicosYvetNadiaPas encore d'évaluation
- QFOII - 5.ácidos CarboxílicosDocument40 pagesQFOII - 5.ácidos CarboxílicosTifoneitorPas encore d'évaluation
- Acidos Carboxilicos LDocument10 pagesAcidos Carboxilicos LAlexi Cristel Aguilar AliPas encore d'évaluation
- Capitulo 12 - Acidos CarboxilicosDocument40 pagesCapitulo 12 - Acidos CarboxilicosAngel SolanoPas encore d'évaluation
- Expoac03 Terminada2 1212261856476596 9Document26 pagesExpoac03 Terminada2 1212261856476596 9santiago castro gonzalesPas encore d'évaluation
- P6 Propiedades Químicas Ácidos CarboxílicosDocument15 pagesP6 Propiedades Químicas Ácidos Carboxílicosyuliana pavasPas encore d'évaluation
- Cidos Carbox Licos2 PDFDocument62 pagesCidos Carbox Licos2 PDFCristian Nacianceno Parra GonzálezPas encore d'évaluation
- Ácidos CarboxílicosDocument36 pagesÁcidos Carboxílicosreyes.sammyPas encore d'évaluation
- Acidez y BasicidadDocument39 pagesAcidez y BasicidadGise VacarezzaPas encore d'évaluation
- Ácidos CarboxílicosDocument22 pagesÁcidos CarboxílicosElisa floresPas encore d'évaluation
- Qu - Lab 6Document19 pagesQu - Lab 6Edith León HuamaniPas encore d'évaluation
- Acidos CarboxilicosDocument9 pagesAcidos CarboxilicosStefaniGarcesPas encore d'évaluation
- Diapositiva de La Sintesis Del Acido BenzoicoDocument14 pagesDiapositiva de La Sintesis Del Acido BenzoicoNick777Pas encore d'évaluation
- Ácidos CarboxílicosDocument8 pagesÁcidos CarboxílicosMaKa RosadoPas encore d'évaluation
- Ácido CarboxílicoDocument10 pagesÁcido Carboxílicoroy rosarioPas encore d'évaluation
- Presentación Semana 10 Primera Parte (-)Document27 pagesPresentación Semana 10 Primera Parte (-)Katherin GarciaPas encore d'évaluation
- Desarrollo Tarea 4Document4 pagesDesarrollo Tarea 4Lucía MoralesPas encore d'évaluation
- Ácido CarboxílicoDocument9 pagesÁcido Carboxílico'Fer Chópite UrbinaPas encore d'évaluation
- Acido CarboxilicosDocument20 pagesAcido CarboxilicosTito SolisPas encore d'évaluation
- Material de Estudio Semana 11Document8 pagesMaterial de Estudio Semana 11MarPas encore d'évaluation
- Reacciones de Los Ácidos Carboxílicos y Sus DerivadosDocument28 pagesReacciones de Los Ácidos Carboxílicos y Sus DerivadosAlexandra OrtegaPas encore d'évaluation
- Acidos Carboxilicos ReaccionesDocument13 pagesAcidos Carboxilicos ReaccionesKevinFernandez100% (1)
- Acidez de Los Acidos CarboxilicosDocument5 pagesAcidez de Los Acidos CarboxilicosChayito Sánchez RomeroPas encore d'évaluation
- Ácidos Carboxilicos Química 1Document5 pagesÁcidos Carboxilicos Química 1leidy hernandezPas encore d'évaluation
- Acidos Carboxilicos - WordDocument21 pagesAcidos Carboxilicos - WordEdwar CelonPas encore d'évaluation
- Acidos CarboxilicosDocument10 pagesAcidos CarboxilicosLucy HuanacuniPas encore d'évaluation
- Acidos CarboxilicosDocument28 pagesAcidos CarboxilicosIvanovPas encore d'évaluation
- Clase 7 WADE7 - Lecture - 20 Ac CarboxDocument17 pagesClase 7 WADE7 - Lecture - 20 Ac CarboxAlejandro Cortes GonzalezPas encore d'évaluation
- El Manual Del Jabón Líquido Hecho a Mano: Guía completa para Crear Champú, Gel de Ducha, Perfumes y Mucho MásD'EverandEl Manual Del Jabón Líquido Hecho a Mano: Guía completa para Crear Champú, Gel de Ducha, Perfumes y Mucho MásPas encore d'évaluation
- Upstream DownstreamDocument7 pagesUpstream DownstreamCHANFLEPas encore d'évaluation
- Tipos de Compuestos Químicos para Controlar EnfermedadesDocument11 pagesTipos de Compuestos Químicos para Controlar EnfermedadesGerman ColmenaresPas encore d'évaluation
- El Yodo Es Un Oxidante Medio y Permite Valorar Los TiosulfatosDocument2 pagesEl Yodo Es Un Oxidante Medio y Permite Valorar Los TiosulfatosRosalia Pacheco CastroPas encore d'évaluation
- Clase 8 Regulacion de La Expresion GenicaDocument2 pagesClase 8 Regulacion de La Expresion GenicaAnais AyleenPas encore d'évaluation
- Sintesis de Lactato de Metilo Lactato Laurico Laureato de PropiloDocument6 pagesSintesis de Lactato de Metilo Lactato Laurico Laureato de PropiloConsiito MuñozPas encore d'évaluation
- Practicas QoiiDocument39 pagesPracticas Qoiijuan islas100% (1)
- Diseño Experimental 3x3x3 Temperatura, Tiempo, Porcentaje de Tierras. Respuesta de Superficies Aplicando Statistica.Document1 pageDiseño Experimental 3x3x3 Temperatura, Tiempo, Porcentaje de Tierras. Respuesta de Superficies Aplicando Statistica.Jorgeh SantozPas encore d'évaluation
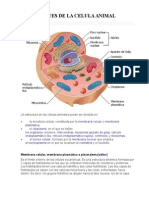
- Partes de La Celula AnimalDocument7 pagesPartes de La Celula AnimalDanilo Daniel López PérezPas encore d'évaluation
- Grupos FuncionalesDocument6 pagesGrupos FuncionalesAngela MonguiPas encore d'évaluation
- Reporte Fenolftaleína y FluoresceínaDocument4 pagesReporte Fenolftaleína y FluoresceínaFrancisco RosalesPas encore d'évaluation
- Taller de Quimica Orgánica EstereoquimicaDocument3 pagesTaller de Quimica Orgánica EstereoquimicaDanny BalantaPas encore d'évaluation
- Nomenclatura de Compuestos InorgánicosDocument15 pagesNomenclatura de Compuestos InorgánicosDaniel Camilo CeraPas encore d'évaluation
- NEO-43 Eslingas de Fibra Sintética para Elevacióny Movimiento de Cargas en Altura - Eslingas PlanDocument32 pagesNEO-43 Eslingas de Fibra Sintética para Elevacióny Movimiento de Cargas en Altura - Eslingas PlanPaulo Diego Aguilera100% (4)
- XenobioticosDocument23 pagesXenobioticosManuel CuevaPas encore d'évaluation
- Diapositivas Bebidas Alcoholicas PDFDocument36 pagesDiapositivas Bebidas Alcoholicas PDFAnabel HernándezPas encore d'évaluation
- HIBRIDACIONDocument4 pagesHIBRIDACIONSalus LagunasPas encore d'évaluation
- Agentes para El Control de MicroorganismosDocument9 pagesAgentes para El Control de MicroorganismosPaula Emery100% (1)
- 1 Benceno 001Document42 pages1 Benceno 001Donovan Gonzalez BureosPas encore d'évaluation
- 01 - Presentación Felipe Kaiser - 20190613Document86 pages01 - Presentación Felipe Kaiser - 20190613LUISA ARIASPas encore d'évaluation
- Identificacion para CarbohidratosDocument13 pagesIdentificacion para CarbohidratosAntonio Castillo Galindo100% (2)
- Los Aceites Son Liquidos A Temperatura AmbienteDocument11 pagesLos Aceites Son Liquidos A Temperatura Ambientemary_6685Pas encore d'évaluation
- Elaboración de Abonos OrgánicosDocument1 pageElaboración de Abonos OrgánicosLuis ArmandoPas encore d'évaluation
- Curso LC Ms Ms IparteDocument94 pagesCurso LC Ms Ms Iparteandrea nettle bareaPas encore d'évaluation
- Los Principales Procesos Energéticos de Los Seres VivosDocument3 pagesLos Principales Procesos Energéticos de Los Seres VivosPedro fuenmayor100% (1)
- Proyecto de Investigacion BiodigestorDocument60 pagesProyecto de Investigacion BiodigestorJean Carlo Mendez R100% (1)
- Bioquimica Práctica No. 3 2022 ADocument15 pagesBioquimica Práctica No. 3 2022 ALUIS GUILLERMO RODRIGUEZ CASILLASPas encore d'évaluation
- ALGAS OkDocument26 pagesALGAS OkaaroncillaPas encore d'évaluation
- Hidrólisis Enzimática de CelulosaDocument5 pagesHidrólisis Enzimática de Celulosafernando maldonadoPas encore d'évaluation
- Evolución de La Celula Procariota y EucariotaDocument7 pagesEvolución de La Celula Procariota y EucariotaAngely Rojas ContrerasPas encore d'évaluation
- Elaboración Del Polímero SlimeDocument6 pagesElaboración Del Polímero SlimeJosué Monterroso100% (1)