Académique Documents
Professionnel Documents
Culture Documents
2007 Sept PDF
Transféré par
Jorge BáezTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
2007 Sept PDF
Transféré par
Jorge BáezDroits d'auteur :
Formats disponibles
PRUEBAS DE ACCESO A LA UNIVERSIDAD L.O.G.S.E.
CURSO 2006-2007 - CONVOCATORIA: SEPTIEMBRE QUMICA
Se ha de elegir UNA de las dos PROPUESTAS presentadas. Cada propuesta consta de cinco preguntas. Cada pregunta ser calificada con un mximo de dos puntos. El tiempo disponible para la realizacin de la prueba es de 1,5 horas.
PROPUESTA I 1.- Dados los elementos A, B y C de nmeros atmicos 19, 17 y 12, respectivamente, indica razonando las respuestas: a) Estructura electrnica de sus respectivos estados fundamentales y el grupo de la tabla peridica al que pertenece cada uno de ellos (1,2 puntos) b) Tipo de enlace formado cuando se unen A y B (0,8 puntos) 2.-a) Escribir todos los ismeros posibles de la propanona (H3C CO CH3) (1,0 puntos) b) Indica la hibridacin que cabe esperar de cada uno de los tomos de carbono que participan en los siguientes compuestos: b1) Propanona (H3C CO CH3);b2) Propino (H3C C CH) (1,0 puntos) 3.- a) Formular las siguientes especies qumicas: (0,125 puntos c/u)
cido crmico [(Tetraoxocromato (VI) de hidrgeno)] Sufuro frrico (Trisulfuro de dihierro) 1-Hexen-5-ino (Hex-1-en-5-ino) 6-metil-3-heptanol (6-Metilheptan-3-ol) Fe(ClO)2 H2SO3 H3C CH = CH CH = CH CH2OH H2C(Cl) CH(Cl) CH2 CH2OH Hidrxido de calcio (Dihidrxido de calcio) Bromato frrico [(Trioxobromato (V) de hierro (III)] 3-Hidroxipentanal cido 3-pentinoico (cido pent-3-inoico) FeCl2 H 2O 2 H3C COO CH2 CH3 H3C CH2 CH2 CONH2
b) Nombrar (de una sola forma), las siguientes especies qumicas: (0,125 puntos c/u)
4.- La reaccin: CO(g) + H2O(g) H2(g) + CO2(g), tiene una constante KC de 8,25 a 900 C. En un recipiente de 25 litros se mezclan 10 moles de CO y 5 moles de H2O a 900 C. Calcule en el equilibrio a) Las concentraciones de todos los compuestos (1,2 puntos) b) La presin total de la mezcla. (0,8 puntos) Datos: R=0,082 atmlmol1K1 5.- Deduce razonadamente y escribiendo la ecuacin ajustada: a) Si el hierro en su estado elemental puede ser oxidado a hierro(II) con MoO42 (1,0 puntos) b) Si el hierro(II) puede ser oxidado a hierro(III) con NO3 (1,0 puntos) Datos: Eo(MoO42/Mo3+) = 0,51 V; Eo(NO3/NO) = 0,96 V; Eo(Fe3+/Fe2+) = 0,77 V; Eo(Fe2+/Fe0) = 0,44 V.
PROPUESTA II
1- Dada la siguiente reaccin: N2(g) + O2 (g) 2 NO (g); H = 90,4 kJ/mol, G = 86,7kJ/mol. Justifica cules de las siguientes afirmaciones son ciertas: (0,5 puntos c/u) a) La reaccin es espontnea de izquierda a derecha. b) La reaccin es exotrmica de derecha a izquierda y un aumento de temperatura desplaza el equilibrio a la derecha. c) El equilibrio se desplaza a la izquierda aumentando su presin. d) Kp = pNO/pN2 pO2 2.- Ajustar las siguientes reacciones e indicar en cada caso las semirreacciones redox y cules son los agentes oxidantes y reductores. a) K2Cr2O7 + HI + HClO4 Cr(ClO4)3 + KClO4 + I2 + H2O (1,0 puntos) b) KIO3 + KI + H2SO4 I2 + K2SO4 + H2O (1,0 puntos) 3.- a) Formular las siguientes especies qumicas: (0,125 puntos c/u)
Hidrxido frrico (Trihidrxido de hierro) Yodato niqueloso (Trioxoyodato (V) de niquel (II)) 2-Fenil butanal 2,4-Hexanodiona (Hexano-2,4-diona) Cloruro plumboso [(Cloruro de plomo (II)] cido perclrico [(cido tetraoxoclrico (VII)] Etil propil ter 3 metil pentanamida
b) Nombrar (de una sola forma), las siguientes especies qumicas: (0,125 puntos c/u)
H2SeO4 Na2SO4 HC C CH = CH CH = CH2 H3C CH2 CH2 CH2 COO CH2 CH3 Ni2O3 ZnBr2 CH2OH CH2 CH2 CH2OH H3C CHOH CH2 CH2 - COOH
4.- Se prepara una disolucin acuosa de cido actico (CH3-COOH ) 0,1M. Calcular: a) el pH de la disolucin. (1,3 puntos) b) el grado de disociacin del cido actico en dicha disolucin (0,7 puntos) Datos: Ka (cido ctico) = 1,85. 10 -5 5.-a) Calcula el calor de formacin a presin constante del metano gaseoso (CH4) a partir de los calores de combustin del C (s), H2 (g) y CH4 (g) cuyos valores son respectivamente -393,5, -285,9 y -890,4 kJ/mol. (1,5 puntos) b) Qu cantidad de calor se desprende en la combustin de 1 Kg de metano gaseoso. (0,5 puntos) Datos: mas. Atm. (C) = 12 ; mas. Atm. (H) = 1.
PRUEBAS DE ACCESO A LA UNIVERSIDAD L.O.G.S.E.
CURSO 2006-2007 - CONVOCATORIA: SEPTIEMBRE QUMICA CRITERIOS ESPECFICOS DE CORRECCIN
PROPUESTA I.
1.-a ) Configuracin electrnica correcta y grupo correcto para cada elemento (0,4 puntos c/u) b) Tipo de enlace entre A y B 0,8 puntos. 2) a) Apartado a) b) Cada subapartado . . 1,0 puntos. 0,5 puntos 0,125 puntos. 1,2 puntos. 0,8 puntos. 0,2 puntos 1,0 puntos 1,0 puntos
3.- Cada especie correcta .. 4.- Apartado a) ...... Apartado b) 5.- Apartado a) o b) sin razonar mediante la reaccin Apartado a) razonado Apartado b) razonado
--------- ooo0ooo ---------
PROPUESTA II.
1.- a) Cada apartado acertado pero mal razonado 0,1 puntos. b) Cada apartado bien razonado pero no acertado 0,2 puntos c) Cada apartado acertado y bien razonado 0,5 puntos. 2.- Apartado a) Semireeacciones redox correctas ................ Reaccin global bien ajustada . Oxidante y reductor correctos.. Apartado b) Semireeacciones redox correctas ................ Reaccin global bien ajustada.. Oxidante y reductor correctos..
0,3 puntos. 0,5puntos. 0,2 puntos. 0,3 puntos. 0,5puntos. 0,2 puntos.
3.- Cada especie correcta ..... 0,125 puntos. 4.- Apartado a) Apartado b) 5.- Apartado a) .... Apartado b) --------- ooo0ooo --------1,3 puntos. 0,7 puntos. 1,5 puntos. 0,5 puntos.
Vous aimerez peut-être aussi
- Analisis de FuncionesDocument59 pagesAnalisis de FuncionescamperacPas encore d'évaluation
- Exámenes de Primero de BachilleratoDocument10 pagesExámenes de Primero de BachilleratoJorge BáezPas encore d'évaluation
- UR28M OperationManual EsDocument40 pagesUR28M OperationManual EsJorge BáezPas encore d'évaluation
- Sol Hoja Ejercicios Dinamica 01 PDFDocument1 pageSol Hoja Ejercicios Dinamica 01 PDFJorge BáezPas encore d'évaluation
- Examen 1 Final PDFDocument2 pagesExamen 1 Final PDFJorge BáezPas encore d'évaluation
- Examen CTM PAU Canarias 2004-JunioDocument4 pagesExamen CTM PAU Canarias 2004-JunioJorge BáezPas encore d'évaluation
- Unidad 14Document26 pagesUnidad 14Hector Vino MamaniPas encore d'évaluation
- Problemas Ecuaciones PrimergradoDocument3 pagesProblemas Ecuaciones PrimergradomadomisaPas encore d'évaluation
- Analiza Sintácticamente Las Siguientes Oraciones CompuestasDocument11 pagesAnaliza Sintácticamente Las Siguientes Oraciones CompuestasJorge BáezPas encore d'évaluation
- 2014 Junio PDFDocument2 pages2014 Junio PDFJorge BáezPas encore d'évaluation
- Sept 2003Document1 pageSept 2003Jorge BáezPas encore d'évaluation
- Hoja Ejercicios Dinamica 01-1 PDFDocument1 pageHoja Ejercicios Dinamica 01-1 PDFJorge BáezPas encore d'évaluation
- Esquemas Formulación InorganicaDocument1 pageEsquemas Formulación InorganicaCarPas encore d'évaluation
- 01-Ejercicios Formulacion InorganicaDocument4 pages01-Ejercicios Formulacion InorganicaPaula Sánchez Rueda0% (1)
- 2008 Junio PDFDocument2 pages2008 Junio PDFJorge BáezPas encore d'évaluation
- 2000 Junio Corrección PDFDocument3 pages2000 Junio Corrección PDFJorge BáezPas encore d'évaluation
- Apuntes de Formulación Inorgánica PDFDocument12 pagesApuntes de Formulación Inorgánica PDFJorge BáezPas encore d'évaluation
- Ejer FormulacionDocument5 pagesEjer FormulacionJorge BáezPas encore d'évaluation
- Tabla de Preferencia de Grupos Funcionales de Química OrgánicaDocument1 pageTabla de Preferencia de Grupos Funcionales de Química OrgánicaPablo Daniel Alvares Hernandez100% (2)
- Julio 2013Document4 pagesJulio 2013mvillaconejosPas encore d'évaluation
- Ejercicio de Formulación Orgánica 1Document2 pagesEjercicio de Formulación Orgánica 1Jorge BáezPas encore d'évaluation
- 2013 JunioDocument2 pages2013 JunioJorge BáezPas encore d'évaluation
- Biología Junio 2013Document4 pagesBiología Junio 2013Jorge BáezPas encore d'évaluation
- 2001 JunioDocument1 page2001 JunioJorge BáezPas encore d'évaluation
- Pau Canarias Fisica 2bac Sep 09Document2 pagesPau Canarias Fisica 2bac Sep 09ALBPERMONPas encore d'évaluation
- PAU Junio 2013Document3 pagesPAU Junio 2013Jorge BáezPas encore d'évaluation
- Sept 2002 PDFDocument1 pageSept 2002 PDFJorge BáezPas encore d'évaluation
- Sept 2012 PDFDocument2 pagesSept 2012 PDFJorge BáezPas encore d'évaluation
- Junio 2006 PDFDocument2 pagesJunio 2006 PDFJorge BáezPas encore d'évaluation
- Starbucks, InternacionalizacionDocument10 pagesStarbucks, InternacionalizacionJulio GarzaPas encore d'évaluation
- Aplicaciones Clinicas de Las EnzimasDocument5 pagesAplicaciones Clinicas de Las EnzimasElias Charcape OtinianoPas encore d'évaluation
- Griffin,: ElviraDocument46 pagesGriffin,: ElviraMagdalena Diani WilkePas encore d'évaluation
- Aprendamos a leer y escribir con ejercicios de maduración y vocalesDocument101 pagesAprendamos a leer y escribir con ejercicios de maduración y vocalesAmiret Martinez100% (2)
- RRSS PIGARS GALS y MEFDocument83 pagesRRSS PIGARS GALS y MEFKaren ChasiPas encore d'évaluation
- Ecualizadores Graficos HPF y LPFDocument7 pagesEcualizadores Graficos HPF y LPFGöestaf ZarPas encore d'évaluation
- Caso para Estudio de Auditoria InternaDocument42 pagesCaso para Estudio de Auditoria InternaMiguel Angel Suero HerreraPas encore d'évaluation
- Demencias - Evaluación y TratamientosDocument110 pagesDemencias - Evaluación y Tratamientosjuan camilo andres navarretePas encore d'évaluation
- Respuesta en Frecuencia de Un Sistema DiscretoDocument5 pagesRespuesta en Frecuencia de Un Sistema DiscretoKarlitosmanPas encore d'évaluation
- Desagües Pluviales DomiciliariosDocument34 pagesDesagües Pluviales DomiciliariosGustavo GioiosaPas encore d'évaluation
- Harvey Cap 15 y 16Document6 pagesHarvey Cap 15 y 16MicaelaPoncePas encore d'évaluation
- Fase 2 Estructura AbanicoDocument10 pagesFase 2 Estructura Abanicoconstain1989Pas encore d'évaluation
- MANTEQUILLA CLARIFICADA - Tecnicas de Cocina en PlanetaGastronomico" PDFDocument3 pagesMANTEQUILLA CLARIFICADA - Tecnicas de Cocina en PlanetaGastronomico" PDFPancho Sagrera AlmuzaraPas encore d'évaluation
- Introducción A La Investigación AplicadaDocument50 pagesIntroducción A La Investigación Aplicadamargarita ascencioPas encore d'évaluation
- Warhammer Ancient Battles - SHIELDWALLDocument27 pagesWarhammer Ancient Battles - SHIELDWALLblackbird413Pas encore d'évaluation
- Annotated TAREA20ACTIVIDAD20II2029Document7 pagesAnnotated TAREA20ACTIVIDAD20II2029Valeria CastroPas encore d'évaluation
- 9 Indicadores Del Nivel de SaludDocument16 pages9 Indicadores Del Nivel de SaludAndrea HernandezPas encore d'évaluation
- Hard To Love 03 - Bulldozer - P. DangelicoDocument311 pagesHard To Love 03 - Bulldozer - P. DangelicoKarina VillegasPas encore d'évaluation
- VP Reinos de Italia Napoles Feb2023Document3 pagesVP Reinos de Italia Napoles Feb2023pepemikel2009Pas encore d'évaluation
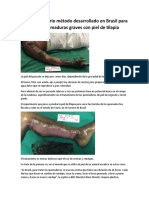
- Método Desarrollado en Brasil para Tratar Quemaduras Graves Con Piel de TilapiaDocument3 pagesMétodo Desarrollado en Brasil para Tratar Quemaduras Graves Con Piel de TilapiaJose Maria VargasPas encore d'évaluation
- Leyes de NewtonDocument9 pagesLeyes de NewtonAmador BolivarPas encore d'évaluation
- Prueba Hyundai Ioniq 5Document11 pagesPrueba Hyundai Ioniq 5Francisco Javier Mendoza Patiño100% (1)
- 3° Sem11 Word Planeación Proyectos Darukel 23-24Document12 pages3° Sem11 Word Planeación Proyectos Darukel 23-24barcenasgonzalezdiana325Pas encore d'évaluation
- LIS Logistics Information SystemsDocument33 pagesLIS Logistics Information SystemsEnrique ValenzuelaPas encore d'évaluation
- Informe de Labo 2012 FINAL!!!Document16 pagesInforme de Labo 2012 FINAL!!!JorgeLuisGarcíaBerrocalPas encore d'évaluation
- Referente Centro Cultural Alto Hospicio - Diseño y Metodologia 3 - Valeria OsorioDocument2 pagesReferente Centro Cultural Alto Hospicio - Diseño y Metodologia 3 - Valeria OsorioNizzPas encore d'évaluation
- Asis Nuevo Pucará 2017Document78 pagesAsis Nuevo Pucará 2017Laura VillafuertePas encore d'évaluation
- Cap II. Importancia de La FlexibilidadDocument54 pagesCap II. Importancia de La Flexibilidadivancattoni98Pas encore d'évaluation
- Mejoramiento Genetico en Bufalos de AguaDocument14 pagesMejoramiento Genetico en Bufalos de AguaJhoanAvellanedaPas encore d'évaluation
- Comentario Paisajes NaturalesDocument3 pagesComentario Paisajes NaturalesVanessa Gomez AlonsoPas encore d'évaluation