Académique Documents
Professionnel Documents
Culture Documents
Actividad de Aprendizaje en Clases Repaso Concentracion de Soluciones
Transféré par
Diego Ignacio Parra ZentenoCopyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Actividad de Aprendizaje en Clases Repaso Concentracion de Soluciones
Transféré par
Diego Ignacio Parra ZentenoDroits d'auteur :
Formats disponibles
Actividad de aprendizaje en clases SOLUCIONES (Unidades de concentracin) Nombre: ... curso: Fecha: Asignatura:..Qumica...
SOLUCIONES (Unidades de concentracin) Desarrolla en tu cuaderno los siguientes ejercicios utilizando las formulas analizadas durante las clases. 1. Determine la molaridad de una solucin que contiene 2,4 moles de NaCl cuyo volumen es de 2 L. (Respuesta: 1,2 mol/L) 2. Determine la molaridad de una solucin que contiene 0,045 moles de KNO3 cuyo volumen es de 0,01 L. (Respuesta: 4,5 mol/L). 3. Determine la molaridad de una solucin que contiene 25 g de NaOH (PM = 40 g/mol), cuyo volumen es de 0,250 L. (Respuesta: 2,5 mol/L). 4. Determine la molaridad de una solucin que contiene 12 g de NaCl (MM = 58,46 g/mol), cuyo volumen es de 0,100 L. (Respuesta: 0,2 mol/L). 5. Determine la molaridad de una solucin que contiene 0,4 g de NaOH (MM = 40 g/mol), cuyo volumen es de 10 mL. (Respuesta: 1,0 mol/L). 6. Determine la molaridad de una solucin que contiene 5,4 g de glucosa (MM = 180 g/mol), cuyo volumen es de 250 mL (Respuesta: 0,12 mol/L). 7. Determine la molaridad de una solucin obtenida al mezclar 30 g de glucosa (PM= 180 g/mol) con 150 g de agua. Considere que la solucin resultante tiene un volumen de 178 mL. (Respuesta: 0,94 mol/L). 8. Determine la molaridad de una solucin obtenida al mezclar 10 g de NaCl (MM = 58,46 g/mol) con 200 g de agua. Considere que la solucin resultante tiene un volumen de 195 mL. (Respuesta: 0,88 mol/L). 9. Determine la molaridad de una solucin de HCl 37 % m/m. Cuya densidad es de 1,19 g/mL. (MMHCl = 36,46 g/mol). (Respuesta: 12,08 mol/L). 10. Determine la molaridad de una solucin de HCOOH 88 % m/m. Cuya densidad es de 1,201 g/mL. (MMHCOOH = 46,03 g/mol). (Respuesta: 23 mol/L). 11. Determine la molaridad de una solucin de HNO3 65,0 % m/m. Cuya densidad es de 1,40 g/mL. (MMHNO3 = 63,0 g/mol).(Respuesta: 14,4 mol/L). 12. Determine la molaridad de una solucin de H3PO4 85,0 % m/m. Cuya densidad es de 1,689 g/mL. (MMH3PO4 = 97,99 g/mol). (Respuesta: 14,7 mol/L). 13. Determine la molalidad de una solucin obtenida al mezclar 30 g de glucosa (MM = 180 g/mol) con 150 g de agua. Considere que la solucin resultante tiene un volumen de 178 mL. (Respuesta: 1,11 molal) 14. Determine la molalidad de una solucin obtenida al mezclar 10 g de NaCl (MM = 58,46 g/mol) con 200 g de agua. Considere que la solucin resultante tiene un volumen de 195 mL.(Respuesta: 0,86 molal). 15. Determine la molalidad de una solucin obtenida al mezclar 48,5 g de benceno (MM = 78,11 g/mol) con 300 g de tolueno. Considere que la solucin resultante tiene un volumen de 396 mL. (Respuesta: 2,07 molal).
16. Determine la molalidad de una solucin de HCl 37 % m/m. Cuya densidad es de 1,19 g/mL. (MMHCl = 36,46 g/mol). (Respuesta: 16,1 molal). 17. Determine la molalidad de una solucin de HCOOH 88 % m/m. Cuya densidad es de 1,201 g/mL. (MMHCOOH = 46,03 g/mol). (Respuesta: 159 molal). 18. Determine la molalidad de una solucin de H3PO4 85,0 %m/m. Cuya densidad es de 1,689 g/mL. (MMH3PO4 = 97,99 g/mol). (Respuesta: 57,8 molal). 19. Determine la molalidad de una solucin de HNO3 65,0 % m/m. Cuya densidad es de 1,40 g/mL. (MMHNO3 = 63,0 g/mol).(Respuesta: 29,5 molal) 20. Considere una solucin que se obtiene mezclando 30,0 g de NaCl (MMNaCl = 58.46 g/mol) y 750 g de agua. Si el volumen de solucin es de 765 mL. Calcular: Porcentaje masamasa (% m/m) a) Porcentaje masavolumen (%m/v) b) Molaridad (M) c) Molalidad (m) d) Densidad de la solucin en g/mL (Respuestas: a) 3,85 % m/m; b) 3,92 % m/v; c) 0,67 mol/L; d) 0,68 molal; e) 1,02 g/mL). 21. Considere una solucin que se obtiene mezclando 4,00 g de NaCl (MMNaOH = 40 g/mol) y 150 g de agua. Si el volumen de solucin es de 158 mL. Calcular: e) Porcentaje masamasa (% m/m) f) Porcentaje masavolumen (% m/v) g) Molaridad (M) h) Molalidad (m) i) Densidad de la solucin en g/mL (Respuestas: a) 2,60 % m/m; b) 2,53 % m/v; c) 0,63 mol/L; d) 0,67 molal; 0.974 g/mL) 22. Considere una solucin que se obtiene mezclando 10,0 g de sacarosa (MM = 342g/mol) y 200 g de agua. Si el volumen de la solucin es de 202 mL. Calcular: a. Porcentaje masamasa (% m/m) b. Porcentaje masavolumen (% m/v) c. Molaridad (M) d. Molalidad (m) e. Densidad de la solucin en g/mL (Respuestas: a) 4,76 % m/m; b) 4,95 % m/v; c) 0,14 mol/L; d) 0,15 molal; e) 1,04 g/mL). 23. Considere una solucin que se obtiene mezclando 15,0 g de CuSO45H2O (MM = 249,55 g/mol) y 200 g de agua. Si el volumen de la solucin es de 203 mL.* Calcular: a. Porcentaje masamasa (% m/m) b. Porcentaje masavolumen (% m/v) c. Molaridad (M) d. Molalidad (m) e. Densidad de la solucin en g/mL (Respuestas: a) 6,98 % m/m; b) 7,39 % m/v; c) 0,30 mol/L; d) 0,30 molal; e) 1,06 g/mL)
24. . Considere una solucin que se obtiene mezclando 15 mL de etanol CH3CH2OH (densidad = 0,791 g/mL) y 85 mL de 2propanol (CH3)2CHOH (densidad = 0,785 g/mL). Si el volumen final de la solucin es 100 mL. (Masas: C = 12; H = 1,0; O = 16). Calcular: a. Porcentaje masamasa (% m/m) b. Porcentaje masavolumen (% m/v) c. Molaridad (M) d. Molalidad (m) e. Densidad de la solucin en g/mL (Respuestas: a) 15,1 % m/m; b) 11,9 % m/v; c) 2,58 mol/L; d) 3,87 molal; e) 0,789 g/mL). 25. Considere una solucin que se obtiene mezclando 10 mL de nhexano CH3CH2CH2CH2CH2CH3 (densidad = 0,659 g/mL) y 90 mL de n pentanoCH3CH2CH2CH2CH3 (densidad = 0,626 g/mL). Si el volumen final de la solucin es 100 mL. (Masas: C = 12; H = 1,0). Calcular: a. Porcentaje masamasa (% m/m) b. Porcentaje masavolumen (% m/v) c. Molaridad (M) d. Molalidad (m) e. Densidad de la solucin en g/mL (Respuestas: a) 10,5 % m/m; b) 6,59 % m/v; c) 0,76 mol/L; d) 1,36 molal; e) 0,629 g/mL). 26. Considere una solucin que se obtiene mezclando 40 mL de acetato de etilo C4H8O2 (densidad = 0,901 g/mL) y 80 mL de npentano CH3CH2CH2CH2CH3 (densidad = 0,626 g/mL). Si el volumen final de la solucin es 120 mL. (Masas: C = 12; H = 1,0; O = 16). Calcular: a. Porcentaje masamasa (% m/m) b. Porcentaje masavolumen (% m/v) c. Molaridad (M) d. Molalidad (m) e. Densidad de la solucin g/mL (Respuestas: a) 41,8 % m/m; b) 30,0 % m/v; c) 3,41 mol/L; d) 8,18 molal; e) 0,718 g/mL).
Vous aimerez peut-être aussi
- Prueba Celula y Digestivo - DocxDocument5 pagesPrueba Celula y Digestivo - DocxDiego Ignacio Parra ZentenoPas encore d'évaluation
- Prueba Celula y Digestivo - DocxDocument5 pagesPrueba Celula y Digestivo - DocxDiego Ignacio Parra ZentenoPas encore d'évaluation
- Prueba Ciencias Naturales Higiene y Drogas .Document5 pagesPrueba Ciencias Naturales Higiene y Drogas .Diego Ignacio Parra ZentenoPas encore d'évaluation
- Clase Intro A REDOXDocument1 pageClase Intro A REDOXDiego Ignacio Parra ZentenoPas encore d'évaluation
- Soluciones Porcentuales GuiaDocument2 pagesSoluciones Porcentuales GuiaDiego Ignacio Parra ZentenoPas encore d'évaluation
- Guía de Actividades Ciencias para La Ciudadanía IV MedioDocument1 pageGuía de Actividades Ciencias para La Ciudadanía IV MedioDiego Ignacio Parra ZentenoPas encore d'évaluation
- Prueba Concentracion de Soluciones Molaridad y MolalidadDocument6 pagesPrueba Concentracion de Soluciones Molaridad y MolalidadDiego Ignacio Parra ZentenoPas encore d'évaluation
- Prueba 5º Basico Celula y Digestivo AtrasadosDocument3 pagesPrueba 5º Basico Celula y Digestivo AtrasadosDiego Ignacio Parra ZentenoPas encore d'évaluation
- Oa 1 Quinto Ciencias Unidad 2Document4 pagesOa 1 Quinto Ciencias Unidad 2Tanya Fuentealba NegrónPas encore d'évaluation
- Guia Estequiometria Calculos de Mol Balance de EcuacionDocument3 pagesGuia Estequiometria Calculos de Mol Balance de EcuacionMatias FigueroaPas encore d'évaluation
- Prueba Química REDOX 2020alternDocument4 pagesPrueba Química REDOX 2020alternDiego Ignacio Parra Zenteno100% (1)
- Energía en la naturalezaDocument4 pagesEnergía en la naturalezaDiego Ignacio Parra ZentenoPas encore d'évaluation
- Ejercicios RedoxDocument1 pageEjercicios RedoxDiego Ignacio Parra ZentenoPas encore d'évaluation
- Calculo de Agente Oxidante, Agente Reductor y Balance de Ecuaciones RedoxDocument1 pageCalculo de Agente Oxidante, Agente Reductor y Balance de Ecuaciones RedoxDiego Ignacio Parra ZentenoPas encore d'évaluation
- Características del agua en sus distintos estadosDocument1 pageCaracterísticas del agua en sus distintos estadosDiego Ignacio Parra ZentenoPas encore d'évaluation
- Trabajo Consumo de Agua 12 de JunioDocument2 pagesTrabajo Consumo de Agua 12 de JunioDiego Ignacio Parra ZentenoPas encore d'évaluation
- Clase N 1 El Ciclo Del AguaDocument1 pageClase N 1 El Ciclo Del AguaDiego Ignacio Parra ZentenoPas encore d'évaluation
- Usos Del Agua DulceDocument6 pagesUsos Del Agua DulceDiego Ignacio Parra ZentenoPas encore d'évaluation
- Cómo se distribuye el agua en la TierraDocument1 pageCómo se distribuye el agua en la TierraDiego Ignacio Parra ZentenoPas encore d'évaluation
- Usos Domesticos Del AguaDocument1 pageUsos Domesticos Del AguaDiego Ignacio Parra ZentenoPas encore d'évaluation
- Cómo se distribuye el agua en la TierraDocument1 pageCómo se distribuye el agua en la TierraDiego Ignacio Parra ZentenoPas encore d'évaluation
- Usos Del Agua DulceDocument6 pagesUsos Del Agua DulceDiego Ignacio Parra ZentenoPas encore d'évaluation
- Construccion de GraficoDocument2 pagesConstruccion de GraficoDiego Ignacio Parra ZentenoPas encore d'évaluation
- Características del agua en sus distintos estadosDocument1 pageCaracterísticas del agua en sus distintos estadosDiego Ignacio Parra ZentenoPas encore d'évaluation
- Usos Domesticos Del AguaDocument1 pageUsos Domesticos Del AguaDiego Ignacio Parra ZentenoPas encore d'évaluation
- La hidrosfera y su cicloDocument24 pagesLa hidrosfera y su cicloVicente MalerbaPas encore d'évaluation
- Trabajo Consumo de Agua 12 de JunioDocument2 pagesTrabajo Consumo de Agua 12 de JunioDiego Ignacio Parra ZentenoPas encore d'évaluation
- Clase N 1 El Ciclo Del AguaDocument1 pageClase N 1 El Ciclo Del AguaDiego Ignacio Parra ZentenoPas encore d'évaluation
- Prueba Ciencias Naturales El Agua y Sus CaracteristicasDocument4 pagesPrueba Ciencias Naturales El Agua y Sus CaracteristicasDiego Ignacio Parra Zenteno100% (1)
- Prueba 5º Basico CelulaDocument1 pagePrueba 5º Basico CelulaDiego Ignacio Parra ZentenoPas encore d'évaluation
- Diagnostico AutomotrizDocument44 pagesDiagnostico AutomotrizhellfishPas encore d'évaluation
- Campo eléctrico protónDocument6 pagesCampo eléctrico protóncarla1gutierrez-1Pas encore d'évaluation
- Cuadro Comparativo de PotenciasDocument8 pagesCuadro Comparativo de PotenciasJuan Manuel Bedoya AcevedoPas encore d'évaluation
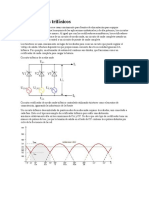
- Rectificadores TrifásicosDocument6 pagesRectificadores TrifásicosDavid SosaPas encore d'évaluation
- Examen Final FísicaDocument1 pageExamen Final FísicaSTEFANIA CAMACHO DAZAPas encore d'évaluation
- Factor de PotenciaDocument5 pagesFactor de PotenciaCristian JoséPas encore d'évaluation
- Semana 9 y 10 - Motores Eléctricos AC PDFDocument77 pagesSemana 9 y 10 - Motores Eléctricos AC PDFJOE BALVIN MONTALVOPas encore d'évaluation
- Lab 5 Fuerza de Arrastre y Sustentacion PDFDocument16 pagesLab 5 Fuerza de Arrastre y Sustentacion PDFWendy Vásquez QuirozPas encore d'évaluation
- Apuntes Tema 1 y 2 Fis 200 Par B PDFDocument30 pagesApuntes Tema 1 y 2 Fis 200 Par B PDFElias V. Gomez MamaniPas encore d'évaluation
- Reporte Ejemplo de Termografía InfrarrojaDocument37 pagesReporte Ejemplo de Termografía InfrarrojaJuan Mar100% (1)
- Instalaciones ElectricasDocument21 pagesInstalaciones Electricasricardo martinez albertoPas encore d'évaluation
- Convertidores CCDocument14 pagesConvertidores CCOmer MarquezPas encore d'évaluation
- Seminario Del Tema 1 Circuitos EléctricosDocument2 pagesSeminario Del Tema 1 Circuitos Eléctricosmatixpro 10Pas encore d'évaluation
- GianProFísica 1 Principios Con Aplicaciones - Douglas Giancoli - 6ta EdiciónDocument8 pagesGianProFísica 1 Principios Con Aplicaciones - Douglas Giancoli - 6ta EdiciónDiego Alejandro33% (3)
- Primer Trabajo de DinamicaDocument19 pagesPrimer Trabajo de DinamicaRUDEMIX NAJARRO ACOSTAPas encore d'évaluation
- PresionDocument34 pagesPresionJulio DíazPas encore d'évaluation
- Kaleidos Catalogo Web 2022 V1 7Document32 pagesKaleidos Catalogo Web 2022 V1 7alejandroPas encore d'évaluation
- Capacitores y DielectricosDocument11 pagesCapacitores y Dielectricosrocio blancoPas encore d'évaluation
- Magnetismo: Campos, Inductancia y CircuitosDocument19 pagesMagnetismo: Campos, Inductancia y CircuitosEusebio Gutierrez MuñozPas encore d'évaluation
- GARCÍA - Diseño de Un Microinversor Tipo Flyback Conectado A Red para Aplicaciones Fotovoltaicas.Document108 pagesGARCÍA - Diseño de Un Microinversor Tipo Flyback Conectado A Red para Aplicaciones Fotovoltaicas.BastianHerreraBugueñoPas encore d'évaluation
- Deducción Algebraica de Las Ecuaciones Utilizados para Determinar La Magnitud de Los Conceptos de ElectroestáticaDocument5 pagesDeducción Algebraica de Las Ecuaciones Utilizados para Determinar La Magnitud de Los Conceptos de ElectroestáticaPatrizziaMoratyPas encore d'évaluation
- Solucion Practica s1 FluidosDocument6 pagesSolucion Practica s1 FluidosKEYLA YASMĂN DE LEĂ“N CALDERĂ“NPas encore d'évaluation
- Mediciones y Calculos de Incertidumbres ExperimentalesDocument50 pagesMediciones y Calculos de Incertidumbres ExperimentalesNataly Urrutia VegaPas encore d'évaluation
- INGEMETA - Ficha TécnicaDocument4 pagesINGEMETA - Ficha Técnicacristian velizPas encore d'évaluation
- Unidad 12 + Técnicas de VacíoDocument10 pagesUnidad 12 + Técnicas de VacíoGH BemjPas encore d'évaluation
- Sensores y Acondicionadores de Señal - Unidad 2-3Document58 pagesSensores y Acondicionadores de Señal - Unidad 2-3Gloria Esmeralda Sandoval Martinez100% (1)
- Análisis DimensionalDocument10 pagesAnálisis DimensionalFrark29Pas encore d'évaluation
- Prueba BiofisicaDocument7 pagesPrueba Biofisicapablo olmedoPas encore d'évaluation
- Mathcad - Compresor Alt. OruroDocument5 pagesMathcad - Compresor Alt. OruroAndrei A. TicoNaPas encore d'évaluation
- Rectificadores de 6 Pulsos Con Transformador DeltaDocument20 pagesRectificadores de 6 Pulsos Con Transformador DeltaLuis Fernando Merma Durand100% (1)
- Cómo hacer que te pasen cosas buenas: Entiende tu cerebro, gestiona tus emociones, mejora tu vidaD'EverandCómo hacer que te pasen cosas buenas: Entiende tu cerebro, gestiona tus emociones, mejora tu vidaÉvaluation : 5 sur 5 étoiles5/5 (1866)
- El lenguaje del cuerpo: Una guía para conocer los sentimientos y las emociones de quienes nos rodeanD'EverandEl lenguaje del cuerpo: Una guía para conocer los sentimientos y las emociones de quienes nos rodeanÉvaluation : 4 sur 5 étoiles4/5 (49)
- No desperdicies tus emociones: Cómo lo que sientes te acerca a Dios y le da gloriaD'EverandNo desperdicies tus emociones: Cómo lo que sientes te acerca a Dios y le da gloriaÉvaluation : 4.5 sur 5 étoiles4.5/5 (11)
- La revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaD'EverandLa revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaÉvaluation : 5 sur 5 étoiles5/5 (200)
- Resetea tu mente. Descubre de lo que eres capazD'EverandResetea tu mente. Descubre de lo que eres capazÉvaluation : 5 sur 5 étoiles5/5 (196)
- Tu cerebro emocional: Saca partido de lo que sientes y transforma tu vidaD'EverandTu cerebro emocional: Saca partido de lo que sientes y transforma tu vidaÉvaluation : 5 sur 5 étoiles5/5 (2)
- Terapia cognitivo-conductual (TCC) y terapia dialéctico-conductual (TDC): Cómo la TCC, la TDC y la ACT pueden ayudarle a superar la ansiedad, la depresión, y los TOCSD'EverandTerapia cognitivo-conductual (TCC) y terapia dialéctico-conductual (TDC): Cómo la TCC, la TDC y la ACT pueden ayudarle a superar la ansiedad, la depresión, y los TOCSÉvaluation : 5 sur 5 étoiles5/5 (1)
- Disciplina con amor para adolescentes (Discipline With Love for Adolescents): Guía para llevarte bien con tu adolescente (A Guide for Getting Along Well With Your Adolescent)D'EverandDisciplina con amor para adolescentes (Discipline With Love for Adolescents): Guía para llevarte bien con tu adolescente (A Guide for Getting Along Well With Your Adolescent)Évaluation : 5 sur 5 étoiles5/5 (10)
- El poder del optimismo: Herramientas para vivir de forma más positivaD'EverandEl poder del optimismo: Herramientas para vivir de forma más positivaÉvaluation : 4.5 sur 5 étoiles4.5/5 (15)
- Psiconeuroinmunología para la práctica clínicaD'EverandPsiconeuroinmunología para la práctica clínicaÉvaluation : 5 sur 5 étoiles5/5 (4)
- Psicogenealogía: Sanar las heridas del alma y encontrarse a uno mismoD'EverandPsicogenealogía: Sanar las heridas del alma y encontrarse a uno mismoÉvaluation : 5 sur 5 étoiles5/5 (5)
- Influencia. La psicología de la persuasiónD'EverandInfluencia. La psicología de la persuasiónÉvaluation : 4.5 sur 5 étoiles4.5/5 (14)
- Pensamiento Crítico: Utiliza modelos mentales para desarrollar tomas de decisiones efectivas y habilidades de resolución de problemas. Supera los obstáculos cognitivos y las falacias en los sistemas para pensar con claridad en tu vida cotidiana.D'EverandPensamiento Crítico: Utiliza modelos mentales para desarrollar tomas de decisiones efectivas y habilidades de resolución de problemas. Supera los obstáculos cognitivos y las falacias en los sistemas para pensar con claridad en tu vida cotidiana.Évaluation : 4.5 sur 5 étoiles4.5/5 (33)
- ¿Por qué mis padres no me aman?: Empezando a sanarD'Everand¿Por qué mis padres no me aman?: Empezando a sanarÉvaluation : 4.5 sur 5 étoiles4.5/5 (33)
- Maneja tus emociones: Curso intensivo de mindfulness y regulación emocionalD'EverandManeja tus emociones: Curso intensivo de mindfulness y regulación emocionalÉvaluation : 4.5 sur 5 étoiles4.5/5 (140)
- Después de la infidelidad: Sanando el dolor y restableciendo la conD'EverandDespués de la infidelidad: Sanando el dolor y restableciendo la conÉvaluation : 4 sur 5 étoiles4/5 (15)
- Cómo Conversar Con Cualquier Persona: Mejora tus habilidades sociales, desarrolla tu carisma, domina las conversaciones triviales y conviértete en una persona sociable para hacer verdaderos amigos y construir relaciones significativas.D'EverandCómo Conversar Con Cualquier Persona: Mejora tus habilidades sociales, desarrolla tu carisma, domina las conversaciones triviales y conviértete en una persona sociable para hacer verdaderos amigos y construir relaciones significativas.Évaluation : 5 sur 5 étoiles5/5 (54)
- La metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceD'EverandLa metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceÉvaluation : 5 sur 5 étoiles5/5 (8)
- Ansiedad infantil. Los trastornos explicados a los padresD'EverandAnsiedad infantil. Los trastornos explicados a los padresÉvaluation : 4.5 sur 5 étoiles4.5/5 (25)
- Contra la ansiedad: Una guía completa para manejar emociones difícilesD'EverandContra la ansiedad: Una guía completa para manejar emociones difícilesÉvaluation : 5 sur 5 étoiles5/5 (58)
- Resumen de El Sutil Arte de que te Importe un Carajo, de Mark MansonD'EverandResumen de El Sutil Arte de que te Importe un Carajo, de Mark MansonÉvaluation : 4.5 sur 5 étoiles4.5/5 (15)
- Te odio - no me abandones: Comprender el trastorno límite de personalidadD'EverandTe odio - no me abandones: Comprender el trastorno límite de personalidadÉvaluation : 5 sur 5 étoiles5/5 (3)
- Libro de Trabajo DE LA TERAPIA DE ACEPTACIÓN Y COMPROMISO (ACT). UNA GUÍA COMPLETA PARA CAMBIAR EL MINDFULNESS Y RECUPERARSE DE LA ANSIEDAD, LA DEPRESIÓN, LOS ATAQUES DE PÁNICO Y LA IRAD'EverandLibro de Trabajo DE LA TERAPIA DE ACEPTACIÓN Y COMPROMISO (ACT). UNA GUÍA COMPLETA PARA CAMBIAR EL MINDFULNESS Y RECUPERARSE DE LA ANSIEDAD, LA DEPRESIÓN, LOS ATAQUES DE PÁNICO Y LA IRAÉvaluation : 4 sur 5 étoiles4/5 (26)
- Batidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoD'EverandBatidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoÉvaluation : 5 sur 5 étoiles5/5 (2)