Académique Documents
Professionnel Documents
Culture Documents
Fisiopatologia Da Doença Hepática Alcoolica - Tese PDF
Transféré par
Monique Lopes da SilvaTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Fisiopatologia Da Doença Hepática Alcoolica - Tese PDF
Transféré par
Monique Lopes da SilvaDroits d'auteur :
Formats disponibles
Maria Sofia Correia Ribeiro da Cruz Bucho
Fisiopatologia da Doena Heptica Alcolica
Universidade Fernando Pessoa
Faculdade de Cincias da Sade
Porto, 2012
Maria Sofia Correia Ribeiro da Cruz Bucho
Fisiopatologia da Doena Heptica Alcolica
Universidade Fernando Pessoa
Faculdade de Cincias da Sade
Porto, 2012
Maria Sofia Correia Ribeiro da Cruz Bucho
Fisiopatologia da Doena Heptica Alcolica
Trabalho apresentado Universidade Fernando Pessoa como parte dos requisitos para obteno do grau Mestre em Cincias Farmacuticas.
_________________________________ Maria Sofia Correia Ribeiro da Cruz Bucho
Fisiopatologia da Doena Heptica Alcolica
Sumrio O alcoolismo um problema de sade pblica de escala mundial. A doena heptica alcolica uma consequncia primria do uso excessivo e prolongado do lcool, sendo um problema de sade pblica em Portugal, uma vez que o lcool a droga de abuso mais comum do pas. Esta reviso de literatura aborda a fisiopatologia da doena heptica alcolica, incluindo a hepatoxicidade do etanol sobre o fgado, o espectro da doena heptica alcolica e as suas principais manifestaes. A fisiopatologia da doena heptica alcolica envolve as consequncias do metabolismo do lcool e mecanismos secundrios, tais como o stress oxidativo, a depleo da glutationa, a produo de endotoxinas, citocinas e reguladores imunolgicos. O desenvolvimento da doena heptica alcolica um processo multifatorial e de vrias etapas, que compreende muitos fatores de risco e o seu espectro inclui: esteatose, hepatite alcolica, fibrose, cirrose e carcinoma hepatocelular. Cada uma destas condies patolgicas produz uma diversidade de manifestaes clnicas muito importantes, podendo algumas ser fatais.
Fisiopatologia da Doena Heptica Alcolica
Abstract Alcoholism is a world scale health problem. Alcoholic liver disease is a primary consequence of prolonged and excessive use of alcohol being a public health problem in Portugal, since alcohol is the most common drug of abuse in the country. This literature review discusses the pathophysiology of alcoholic liver disease, including the hepatotoxicity of ethanol on the liver, the spectrum of alcoholic liver disease and its main manifestations. The pathophysiology of alcoholic liver disease involves the consequences of the metabolism of alcohol and secondary mechanisms such as oxidative stress, depletion of glutathione, production of endotoxins, cytokines and immune regulators. The development of alcoholic liver disease is a multifactorial and multistep process that includes many risk factors and its spectrum includes: simple steatosis, alcoholic hepatitis, fibrosis, cirrhosis, and hepatocellular carcinoma. Each one of this pathological conditions produces a variety of clinical manifestations very importante, some may be fatal.
ii
Fisiopatologia da Doena Heptica Alcolica
Agradecimentos
Agradeo Professora Doutora Ftima Guedes, minha orientadora, pela competncia cientfica e acompanhamento do trabalho, pela disponibilidade e generosidade reveladas, assim como pelas crticas, correes e sugestes relevantes, feitas durante a orientao. Agradeo Universidade Fernando Pessoa e a todos os profissionais que a constituem pela formao que me proporcionaram. Agradeo minha famlia, em particular, aos meus pais por todo o apoio incondicional ao longo da minha carreira acadmica e pela sensatez com que sempre me aconselharam. Agradeo aos meus amigos pelo incentivo e companheirismo demonstrados ao longo do meu percurso acadmico.
iii
Fisiopatologia da Doena Heptica Alcolica
ndice
Sumrio...i Abstract.....ii Agradecimentos....iii ndice de figurasv Lista de abreviaturas....vii 1-Introduo...1 2- A doena heptica alcolica..3 2.1- Consideraes gerais.....3 2.2- Hepatotoxicidade do etanol .....4 2.3 - Espectro da doena heptica alcolica.. 18 2.3.1- Esteatose heptica.19 2.3.2- Hepatite alcolica..21 2.3.3- Fibrose heptica.24 2.3.4 - Cirrose heptica...27 2.3.5- Carcinoma hepatocelular...34
3- Consideraes finais....39 4- Bibliografia......................................40
iv
Fisiopatologia da Doena Heptica Alcolica
ndice de figuras Figura 1- Metabolismo heptico do etanol...4 Figura 2- Reao de oxidao do etanol pela ADH.5 Figura 3- Classificao dos genes da enzima lcool desidrogenase.5 Figura 4- Reao da oxidao do etanol pelo MEOS...8 Figura 5- Reao da metabolizao do lcool pela catlase.8 Figura 6- Oxidao do acetaldedo pela ALDH..9 Figura 7- Converso do acetato a acetil-Coenzima A....10 Figura 8- Funo das citocinas envolvidas na doena heptica alcolica..12 Figura 9- Ativao da clula de Kupffer....13 Figura 10- Ativao do NFkb pelo TNF-.14 Figura 11- Ativao das clulas estreladas hepticas.....15 Figura 12- Diversos mecanismos da hepatotoxicidade do etanol no fgado.17 Figura 13- Fatores de risco da doena heptica alcolica..18 Figura 14- Alteraes morfolgicas e histolgicas da esteatose....20 Figura 15- Inter-relaes entre as manifestaes da doena heptica alcolica.20 Figura 16- Mecanismos pelos quais o etanol causa inflamao na doena heptica alcolica ..22 Figura 17- Alteraes histolgicas da hepatite alcolica...23 Figura 18- Vias de ativao das clulas hepticas estreladas aps leso heptica.25 Figura 19- Lbulo heptico....26
v
Fisiopatologia da Doena Heptica Alcolica
Figura 20 - Cirrose micronodular e macronodular....28 Figura 21- Circulao portal: A: sistema de portal normal. B: fgado cirrtico: formao de varizes e esplenomegalia30 Figura 22- Ascite...30 Figura 23- Lquido acumulado na cavidade peritoneal..31 Figura 24- Mecanismos de ascite na cirrose heptica...32 Figura 25- Fisiopatologia da SHR.33 Figura 26- Hepatocarcinognese35 Figura 27- Carcinoma hepatocelular difuso num fgado cirrtico.36 Figura 28- Carcinoma hepatocelular unifocal num fgado cirrtico..37 Figura 29- Carcinoma hepatocelular multifocal....37 Figura 30- Carcinoma hepatocelular infiltrante.37
vi
Fisiopatologia da Doena Heptica Alcolica
Lista de Abreviaturas
ADH- lcool Desidrogenase ALDH- Acetaldedo Desidrogenase ATP- Adenosina Trifosfato CHC- Carcinoma Hepatocelular CYP2E1- Citocromo P450 2E1 DHA- Doena Heptica Alcolica GSH- Glutationa HSCs- Clulas Estreladas Hepticas IL- Interleucina LBP- Protena de Ligao a Lipopolissacardeos LPS- Lipopolissacardeos MEOS- Sistema Microssomal de Oxidao do Etanol MMPS- Metaloprotenases NAD- Dinucletido de Nicotinamida e Adenina NADH- Dinucletido de Nicotinamida e Adenina na forma reduzida NADP- Dinucletido de Nicotinamida e Adenina Fosfato NADPH- Dinucletido de Nicotinamida e Adenina Fosfato na forma reduzida NFkB - Factor Nuclear Kappa B OMS- Organizao Mundial de Sade ROS- Espcies Reativas de Oxignio SHR- Sndrome Hepato-Renal TGF-- Fator de Transformao de Crescimento Beta TIMPs- Inibidores Tissulares de Metaloprotenases TLR4- Recetor Toll do Tipo 4 TNF-- Fator de Necrose Tumoral Alfa
vii
Fisiopatologia da Doena Heptica Alcolica
1-Introduo A Organizao Mundial de Sade (OMS) estima que 2 bilies de pessoas de todo o mundo consumem bebidas alcolicas, e que 76,3 milhes apresentam doenas associadas ao consumo de lcool, visto que este constitui uma das drogas mais acessveis e com mais consumo imprprio de todas as drogas de abuso (World Health Organization, 2011). Segundo dados apurados pela OMS o consumo excessivo e descontrolado de lcool responsvel pela morte de 2,5 milhes de pessoas por ano, um nmero mais elevado do que as mortes causadas pelo vrus da imunodeficincia humana, sendo um fator causal em 60 tipos de patologias (World Health Organization, 2011). O uso prejudicial do lcool uma ameaa particularmente grave para os homens, sendo o principal fator de risco de morte em homens com idades compreendidas entre 15-59 anos, principalmente devido a leses, violncia e doenas cardiovasculares e, ainda, globalmente, 6,2% de todas as mortes de homens so atribuveis ao lcool, em comparao a 1,1% das mortes femininas (World Health Organization, 2011). O relatrio da OMS, mais recente, sobre o consumo alcolico (World Health Organization, 2011) revela o padro Europeu relativamente ao consumo de lcool: "Os adultos na Europa consomem trs bebidas alcolicas por dia", o que equivale a 12,5 litros de lcool puro por ano, ou seja 27 gramas por dia. Numa lista de 34 pases da Europa, Portugal surge no nono lugar no que se refere mdia anual de consumo de lcool puro per capita, com 13,43 litros (World Health Organization, 2011). Neste contexto, dentro das vrias patologias associadas ao consumo excessivo e crnico do lcool, uma das doenas mais relevante a doena heptica alcolica (DHA), que considerada uma das principais causas de morbilidade e mortalidade em todo o mundo (Seth et al., 2011).
Fisiopatologia da Doena Heptica Alcolica
A elaborao deste trabalho surge no sentido de dar cumprimento a uma exigncia curricular para a finalizao do Mestrado integrado em Cincias Farmacuticas da Universidade Fernando Pessoa, tratando-se de uma reviso bibliogrfica sobre o tema Doena heptica Alcolica, em que a metodologia utilizada foi de cariz terico, tendo por base publicaes cientficas na rea do tema proposto. Porm, para alm disso, atendendo ao crescente consumo de lcool em todo o mundo, particularmente em Portugal, assim como o aumento das suas consequncias na sade pblica, esta monografia pretende atingir uma maior e melhor qualificao profissional, entendendo-se que o farmacutico deve assumir um papel preponderante no que diz respeito orientao do doente, nomeadamente a nvel da preveno, assim como do tratamento da doena heptica alcolica.
Fisiopatologia da Doena Heptica Alcolica
2- A doena heptica alcolica
2.1-Consideraes gerais A doena heptica mais frequente em Portugal, que causa maior morbilidade e mortalidade, a doena heptica alcolica. Dois teros dos doentes com doena heptica apresentam como causa o lcool (Mello et al., 2011). A considerar que o lcool representa a droga de abuso mais consumida no pas, a doena heptica alcolica traduz-se num grave problema no contexto da sade pblica portuguesa (Mello et al.,2011). A doena heptica alcolica a leso do fgado que diz respeito a uma variedade de alteraes hepticas que surgem aps anos de consumo excessivo de lcool (Lieber,2000). Trata-se de uma doena multifactorial, complexa e representa um espectro de doenas e alteraes morfolgicas que variam desde a esteatose, inflamao e necrose heptica (hepatite alcolica) fibrose progressiva e cirrose. Alm disso, o consumo excessivo de lcool favorece a progresso de outras patologias hepticas, tais como a hepatite pelo vrus C , a hepatite pelo vrus B e o carcinoma hepatocelular (CHC) (Lieber , 2000). A progresso da doena heptica alcolica implica vrios mecanismos decorrentes da hepatoxicidade do etanol no fgado, alm de outros fatores, entre eles a dose, a durao e tipo de consumo de lcool, sexo, etnia e ainda a obesidade, desnutrio, infeo concomitante com hepatite viral B e C e, ainda, fatores genticos (Gao e Bataller,2011; OShea et al., 2010). No que concerne quantidade do consumo de lcool, de referir que em alguns alcolicos pesados (geralmente definidos como homens que habitualmente consomem mais de 80 g de etanol por dia ou mulheres que bebem regularmente mais de 20 g de etanol por dia, durante 10 anos), verifica-se que h o desenvolvimento de vrios estdios da doena heptica alcolica (Diehl, 2002).
Fisiopatologia da Doena Heptica Alcolica
2.2 Hepatotoxicidade do etanol O fgado o maior rgo interno do corpo, sendo responsvel por vrias funes como: metabolizao de substncias, sntese de protenas, detoxificao, secreo biliar, entre outras. Tais funes so vitais e a preservao destas indispensvel sobrevivncia do ser humano (Seeley et al., 2005). Neste contexto, o fgado metaboliza aproximadamente 90% do lcool ingerido, envolvendo vias metablicas: oxidativa e no oxidativa (Laposata e Lange, 1986). A via oxidativa a que desempenha o papel mais importante no metabolismo do lcool, em que este metabolizado nos hepatcitos, sobretudo por dois sistemas: pela enzima lcool desidrogenase (ADH) e pelo sistema microssomal de oxidao do etanol (MEOS), sendo que cada um destes sistemas metablicos causa alteraes metablicas e txicas especficas levando produo de acetaldedo como demonstrado na figura 1 (Caballera,2003; Lieber, 1997).
Figura 1 Metabolismo heptico do etanol (Adaptado de Caballera,2003).
Fisiopatologia da Doena Heptica Alcolica
A lcool desidrogenase a principal enzima que oxida o lcool a acetaldedo, envolvendo os cofatores dinucletido de nicotinamida e adenina (NAD) e dinucletido de nicotinamida e adenina na forma reduzida (NADH) (Cabellera, 2003). A reao esquematizada na figura 2:
Figura 2 Reao de oxidao do etanol pela ADH (Adaptado Gramenzi et al., 2006).
A ADH uma metaloenzima dimrica que se encontra no citoplasma celular e codificada por sete genes localizados no cromossoma 4. Esta enzima exibe vrios polimorfismos genticos, existindo em humanos aproximadamente 20 isoenzimas que possuem diferenas a nvel estrutural e funcional, em termos de propriedades cinticas e de distribuio no organismo, dividindo-se em cinco classes, conforme apresentado na figura 3 (Rebello e Carvalho, 2008). Os polimorfismos genticos da ADH concedem uma maior suscetibilidade individual ao alcoolismo e sua toxicidade e, consequentemente doena heptica alcolica ( Cabellera, 2003).
Figura 3- Classificao dos genes da enzima lcool desidrogenase (Rebello e Carvalho, 2008).
Fisiopatologia da Doena Heptica Alcolica
Das vrias isoenzimas da ADH, as mais importantes, envolvidas no metabolismo do lcool, so as pertencentes s classes I,II,IV. A classe I de isoenzimas, encontrada no fgado, localiza-se em trs loci de genes: ADH1, ADH2, ADH3 os quais originam as subunidades , e , respetivamente. A classe II comporta o gene ADH4, estando presente no fgado e a classe IV o gene ADH7, que encontrada no estmago (Caballera, 2003). Contudo, os polimorfismos apenas ocorrem nos genes pertencentes classe I, ADH2 e ADH3, que possuem diferentes alelos. Os alelos ADH2*1, ADH2*2 e ADH2*3 possuem subunidades 1,2 e 3 respetivamente e os alelos ADH3*1 e ADH3*2 possuem as subunidades 1 e 2, respetivamente. Neste sentido, as isoenzimas de subunidade 2 e 1 codificadas pelos alelos ADH2*2 e ADH3*1, respetivamente, diferem na capacidade de oxidao do etanol e apresentam uma maior atividade enzimtica, oxidando o etanol de forma rpida, originando nveis elevados de acetaldedo (Matsuo et al., 2006). Assim, indivduos portadores do alelo ADH2*2 encontram-se mais sujeitos a apresentar reaes adversas ao consumo de etanol, o que em ltima anlise, reduz a probabilidade dos indivduos se tornarem alcolicos e desenvolverem doenas consequentes (Matsuo et al., 2006). Neste contexto, um aspeto a considerar o que se refere s diferenas da suscetibilidade por parte das diferentes etnias relativamente toxicidade do lcool e doena heptica alcolica. Esta diferena entre as populaes particularmente devida ao gene ADH2, em que o alelo ADH2*1 comumente expresso em caucasianos e afro-americanos e o alelo ADH2*2 predomina entre japoneses e chineses (Caballera, 2003). Consequentemente, este polimorfismo responsvel por uma converso rpida do etanol a acetaldedo em 90% da populao asitica e cerca de 50% desta, denuncia uma resposta desagradvel ao lcool, visto que nveis altos de acetaldedo originam a manifestao de sinais como: rubor, taquicardia, dor de cabea, nuseas, entre outros (Caballera, 2003). Por outro lado, a ADH encontrada no estmago (ADH7), de extrema importncia, uma vez que em comparao com a ADH heptica, apresenta uma menor afinidade mas uma maior capacidade de oxidao do etanol. Ainda, esta ADH7 pode limitar a
6
Fisiopatologia da Doena Heptica Alcolica
biodisponibilidade do etanol, dependendo da forma como este ingerido, de modo que, no consumo de elevadas quantidades de etanol em curtos perodos de tempo, origina-se uma elevada concentrao desta molcula no estmago (Matsuo et al., 2006). , ainda, de referir que o aumento do consumo de lcool inibe, por si s, a atividade da ADH. A sua atividade v-se tambm reduzida durante o jejum, o que explica o facto de o etanol ser mais txico quando consumido com o estmago vazio, concluindo-se que a presena de alimentos no estmago no s diminui a velocidade de absoro de etanol como tambm aumenta a atividade da ADH7 gstrica (Matsuo et al., 2006). Outro aspeto a ter em conta o que concerne ao gnero, a ADH7 gstrica tem a sua atividade diminuda nas mulheres, em comparao com os homens, constituindo um fator de suscetibilidade individual DHA. Tradicionalmente, as mulheres bebem menos do que os homens, mas para uma determinada quantidade de lcool consumida, os nveis de sangue so mais elevados em mulheres do que em homens principalmente devido a duas razes farmacocinticas (Lieber , 1995). Uma razo que as mulheres apresentam maior proporo de gordura corporal, logo menor quantidade de gua e consequentemente menor volume de distribuio; e a outra razo traduzida pelo facto das mulheres exibirem menor capacidade de metabolizao da enzima lcool desidrogenase gstrica, o que leva ao aumento da absoro do etanol e dos seus nveis sanguneos (Mello et al.,2001). Alm disso, outro fator a referir o atraso no esvaziamento gstrico durante a fase ltea do ciclo menstrual das mulheres, que faz com que haja uma maior absoro do etanol sem que ocorra uma prvia metabolizao (Lieber, 1995). Cabe ressaltar que, quando se atingem elevados nveis de etanol na corrente sangunea, a oxidao do etanol passa a ser efetuada pelo sistema microssomal de oxidao do etanol, localizado no reticulo endoplasmtico. Este sistema inclui algumas enzimas envolvidas na metabolizao geral de substncias como, por exemplo, o Citocromo P450 e sob condies de ingesto crnica e/ou excessiva de lcool (quando a concentrao superior a 10mM (50 mg/dl)), a metabolizao do lcool origina Citocromo P-450 2E1, uma variante do citocromo P-450 induzida pelo etanol (Gramenzi et al., 2006; Suddendorf, 1989).
Fisiopatologia da Doena Heptica Alcolica
A reao da oxidao do etanol pelo MEOS envolve o cofator NADP (nicotinamida adenina dinucletido fosfato) e oxignio, e tem a seguinte representao (figura 4):
Figura 4- Reao da oxidao do etanol pelo MEOS (Adaptado de Suddendorf, 1989).
A induo do citocromo P-4502E1 origina desequilbrios metablicos importantes, produzindo espcies reativas de oxignio (ROS), como por exemplo, perxido e superxido de hidrognio, causando leso tecidual do rgo. As espcies reativas de oxignio so responsveis pela ativao de fatores de transcrio redox-sensveis, como o fator nuclear kappa B (NFkB), promovendo um perfil pr-inflamatrio (Lieber 1997; Gramenzi et al., 2006). Assim, o stress oxidativo sem dvida uma fora motriz na doena heptica alcolica, pois d incio peroxidao lipdica que danifica diretamente o plasma e as membranas intracelulares e induz a produo de grupos aldedos reativos com potentes propriedades pr-inflamatrias e pr-fibrticas (Stewart et al., 2004). Por fim, o metabolismo do etanol pode ainda ser mediado pela catalase, uma enzima peroxissomal. De acordo com Seth e os seus colaboradores (2011) este processo ainda no foi devidamente esclarecido e tem por base a pequena produo do perxido de hidrognio, um pr-requisito para oxidao do etanol por esta via. Assim, no processo oxidativo do etanol via catalase, ocorre, inicialmente, a oxidao do NADPH atravs da NADPH-oxidase, com a formao da gua oxigenada, a qual, sob a influncia da catalase, promove a oxidao do etanol (Jnior, 1998). A reao esquematizada da seguinte forma (figura 5) :
Figura 5- Reao da metabolizao do lcool pela catalase (Adaptado de Suddendorf,1989).
Fisiopatologia da Doena Heptica Alcolica
Finalmente, relativamente via no-oxidativa do metabolismo do etanol, cabe dizer que esta caracterizada pela formao de til-esteres de cidos gordos, atravs da reao do etanol com cidos gordos (Laposata e Lange, 1986). Estudos apontam que esta via, embora possa ter um algum efeito em leses do fgado causadas pelo consumo excessivo de lcool, no apresenta evidncias no desenvolvimento da doena heptica alcolica, no sendo preponderante, adquirindo dessa forma um papel minoritrio (Laposata e Lange, 1986). Cada uma destas vias referidas, produz uma perturbao metablica especfica e txica e todos as trs resultam na produo de acetaldedo, um metabolito cuja hepatoxicidade elevada (Bruha et al., 2012). Neste sentido, o acetaldedo considerado a toxina chave na doena heptica alcolica, provocando danos celulares, inflamao, remodelao da matriz extracelular e fibrinognese dos hepatcitos (Lieber, 1997). Desta forma, o acetaldedo induz uma resposta de fase tardia nas clulas hepticas estreladas envolvendo o fator de transformao de crescimento beta (TGF-), para manter um perfil pro-fibrinognico e pr-inflamatrio. Alm disso, o acetaldedo liga-se covalentemente a protenas e ao DNA, formando aductos imunognicos, tais como, o malondialdedo e hidroxinonenal, que podem afetar diretamente as funes celulares, contribuindo para a leso heptica (Casini et al., 1991). Por outro lado, seguindo-se a metabolizao completa do etanol, o acetaldedo resultante da ao da ADH sobre o etanol, oxidado a acetato pela enzima mitocondrial lcool desidrogenase (ALDH), como esquematizado na figura 6 (Suddendorf, 1989).
Figura 6- Oxidao do acetaldedo pela ALDH (Adaptado de Suddendorf,1989).
Fisiopatologia da Doena Heptica Alcolica
Assim sendo, o metabolismo do etanol, requer basicamente o envolvimento de duas etapas oxidativas dependentes de NAD, a primeira catalisada pela ADH e a segunda pela ALDH (Suddendorf, 1989). Relativamente aldedo desidrogenase, existem duas classes, a ALDH1 localizada no citoplasma e a ALDH2 localizada na mitocndria. Esta ltima representa a classe mais importante no que concerne ao metabolismo do acetaldedo e como acontece na enzima ADH, a ADH2 tambm polimrfica, apresentando os alelos ALDH2*1 e ALDH2*2 (Cabellera ,2003). Segundo Crabb e colaboradores (1989) a prevalncia das diferenas genticas da ALDH varia de acordo com a etnia, em que os polimorfismos de ALDH2 esto presentes entre 10% a 44% na populao asitica, enquanto que em caucasianos, praticamente no detetada (Cabellera ,2003). Conforme os estudos de Cabellera (2003), esta mutao,ALDH2*2, tal como o polimorfismo anteriormente referido da enzima ADH, d origem a elevados nveis de acetaldedo e consequentemente aos seus efeitos txicos, conduzindo averso do lcool, sendo um fator de proteo ao alcoolismo por parte da populao asitica. sabido que a metabolizao do acetaldedo resulta na produo de acetato livre, o que tambm pode afetar outras vias metablicas, incluindo a gerao de acetil-coenzima-A em diferentes partes do organismo (figura 7) (Suddendorf, 1989).
Figura 7- Converso do acetato a acetil- coenzima A ( Adaptado de Suddendorf, 1989).
10
Fisiopatologia da Doena Heptica Alcolica
Tem sido referido que a converso de lcool para acetato, e ainda mais a acetilcoenzima A, aumenta a acetilao das histonas, proporcionando um mecanismo de inflamao acrescido em determinadas leses do fgado como a hepatite alcolica aguda. A acetilao da histona em promotores de genes especficos crtica na regulao da sntese de citocinas inflamatrias de macrfagos, tais como, interleucina-6 (IL-6), IL-8 e o fator de necrose tumoral alfa (TNF-) ( Seth et al., 2001). Para alm das alteraes metablicas, o etanol tambm induz alteraes noutras molculas, entre as quais a glutationa (GSH) (Townsend et al., 2003). A glutationa um tripeptdeo solvel em gua, que possui caractersticas antioxidantes, sendo um importante fator contra a formao e manuteno de radicais livres, desempenhando um papel na desintoxicao de uma variedade de compostos via catlise pela glutationa S-transferase e pelas glutationa- peroxidases (Townsend et al.,2003). A glutationa encontrada tanto no citoplasma como nas mitocndrias, em que a maior parte da produo de energia da clula ocorre, e para a clula funcionar normalmente, importante que a quantidade de GSH presente na mitocndria seja suficiente, visto que a maior parte dos ROS so formados nesse local (Neuman, 2004). importante mencionar que, se os ROS no forem rapidamente eliminados pela GSH, estes podem danificar a mitocndria, permitindo que a molcula de citocromo se liberte da mitocndria para o citoplasma, e consequentemente o citocromo c vai ativar vrias molculas mediadoras qumicas, contribuindo para a apoptose celular heptica (Fernandez-Checa et al., 1998) . de referir, que diminuies deste antioxidante indispensvel, so relatadas na associao com a doena alcolica heptica, uma vez que o etanol reduz os nveis dessa molcula nas clulas (Lieber, 1997). No que concerne s citocinas, cabe ressaltar que tratam-se de mensageiros qumicos que desempenham um papel importante durante a primeira resposta do organismo infeo pois atraem e ativam componentes do sistema imunolgico. De acordo com McClain e colaboradores (1997) o consumo de lcool causa a produo acentuada de citocinas no fgado, conduzindo hepatoxicidade .
11
Fisiopatologia da Doena Heptica Alcolica
Com base nas suas funes especficas de combate inflamao, neste caso em relao doena heptica alcolica, as citocinas podem ser agrupadas em diferentes grupos, conforme apresentando na figura 8 (Neuman, 2004).
Citocinas
Funo Citocinas proinflamatrias
Interleucina1 (IL1)
Produz respostas inflamatrias; induz febre, estimula o crescimento e diferenciao do sistema imunitrio Promove a maturao de clulas B secretoras de anticorpos, atua com outras citoquinas para estimular outras clulas do sistema imunitrio; estimula a produo de mediadores de resposta inflamatria e a regenerao heptica Promove respostas inflamatrias; estimula neutrfilos e macrfagos; induz febre, induz macrfagos a produzirem citocinas, induz a apoptose e necrose Promove a sntese de colagnio
Interleucina6 (IL6)
Fator de necrose tumoral alfa (TNF) Fator de transformao de crescimento beta (TGF)
Interleucina10 (IL10)
Citocinas Imuno-reguladoras Inibe a proliferao de certas clulas do sistema imunolgico e promove a proliferao de outras; reduz a produo de citocinas inflamatrias; promove a secreo de anticorpos Quimiocinas
Interleucina8 (IL8)
Atrai neutrfilos para o local de uma infeo.
Figura 8 Funo das citocinas envolvidas na doena heptica alcolica ( Adaptado de Neuman,2004).
Estudos reportam que concentraes de soro/plasma de interleucinas: IL-1, IL-6 e IL-8 , esto aumentados em pacientes inicialmente hospitalizados com esteato-hepatite
alcolica e que estas diminuem durante a sua recuperao. A atividade destas citocinas pr-inflamatrias est extremamente relacionada com o grau da inflamao heptica (Dominguez et al., 2011). Tem sido referido que, entre as vrias citocinas, o fator de necrose tumoral alfa e o fator de transformao de crescimento beta so as citocinas que representam fatores-chave e que influenciam fortemente os processos de disfuno heptica (Neuman, 2004).
12
Fisiopatologia da Doena Heptica Alcolica
Outro aspeto importante, que a produo destas citocinas envolvidas na leso do fgado desencadeada pela estimulao das clulas de Kupffer (Hritz et al., 2008). Neste sentido, de acordo com Hritz e colaboradores (2008), o consumo de lcool aumenta a permeabilidade do intestino, permitindo a libertao para a circulao sangunea de certos produtos bacterianos txicos- as endotoxinas, nomeadamente os lipopolissacardeos (LPS) que so componentes das bactrias gram-negativas no intestino, e que estimulam e sensibilizam as clulas de Kupffer. Ainda, segundo Hritz e colaboradores (2008) e Tilg e Diehl (2000), este efeito sobre as clulas de Kupffer resulta do facto dos LPS complexarem com a protena de ligao, a LPS (LBP), que se liga superfcie do recetor CD14 nas clulas de Kupffer hepticas e este complexo CD14-LPBLPS interage com recetor do tipo toll-4 (TLR4) para acionar uma cascata de sinalizao que ativa o fator nuclear kappa B (NFkB) e libertar citocinas pr-inflamatrias, TNF-, TGF- e outras citocinas que contribuem para a disfuno do hepatcito, necrose e apoptose e a formao de protenas de matriz extracelular levando fibrose / cirrose, como representado no esquema seguinte (figura 9):
Figura 9 Ativao da clula de Kupffer.
13
Fisiopatologia da Doena Heptica Alcolica
Alm disso, o TNF- pode aumentar o metabolismo dos hepatcitos, em especial a produo de energia na sua mitocndria, o que pode levar a um aumento da produo de ROS nas mitocndrias que, por sua vez, pode ativar o fator nuclear kappa B, que controla a atividade de vrios genes, incluindo aqueles que codificam o TNF- e, assim como os genes que codificam protenas que promovem a apoptose ( Neuman, 2004) . Desta forma, um ciclo vicioso estabelecido nos hepatcitos: o TNF- promove a produo de ROS, a produo de ROS ativa o NFkB, e o NFkB conduz produo de TNF- adicional, assim como a produo de fatores que promovem a apoptose, e este ciclo, eventualmente altera a estrutura dos hepatcitos, prejudicando a sua funo, e pode levar apoptose dos hepatcitos (figura 10) (Parlesak et al., 2000).
Figura 10 Ativao do NFkb pelo TNF-.
Relativamente ao TGF-, estudos revelaram que a quantidade de TGF- produzida maior no fgado de pacientes com cirrose alcolica do que nos fgados de pessoas saudveis, o que sugere que o TGF- pode estar envolvido no desenvolvimento da fibrose induzida por lcool no fgado (Neuman et al., 2002).
14
Fisiopatologia da Doena Heptica Alcolica
Assim, o TGF- tambm pode contribuir para a leso heptica atravs da ativao das clulas estreladas hepticas, as quais desempenham um papel-chave no processo de regenerao e fibrinognese heptica (figura 11) (Neuman et al., 2002). Deste modo, a fibrinognese, uma resposta de cura da ferida tpica de leso, envolve regenerao heptica, remodelao da matriz extracelular e estabelece uma cicatriz tecidual ( Diehl, 1998).
Figura 11 Ativao das clulas estreladas hepticas (Adaptado de Mann e Mann, 2009).
Conforme os postulados de Friedman (1999) estas clulas, em estado de repouso, servem essencialmente para armazenar gordura e vitamina A no fgado. Contudo, quando ativadas as clulas estreladas hepticas podem produzir colagnio, o principal componente do tecido cicatricial, sendo que essa produo de colagnio representa um passo crucial no desenvolvimento de fibrose em pacientes com hepatite alcolica e, desta forma, como o TGF-, como ativa as clulas estreladas hepticas, pode ser um ator importante neste processo. Tal como com o TNF-, os hepatcitos normalmente produzem pouco ou nenhum TGF. Entretanto, sob certas condies, os hepatcitos podem produzir TGF- em maior escala. Neste contexto, o lcool pode desencadear a ativao do TGF- e, assim, contribuir para a iniciao de apoptose, se esta molcula entrar na corrente sangunea em concentraes mais elevadas (Neuman, 2001; Katz et al., 2001).
15
Fisiopatologia da Doena Heptica Alcolica
Alm disso, esta citoquina pode fazer com que os hepatcitos aumentem a produo de certas molculas, como a transglutaminase e citoqueratinas, que normalmente so responsveis pela estrutura e forma das clulas. Quando os nveis dessas molculas esto aumentados, h a formao de estruturas denominadas corpos de Mallory, que so indicadores de leso heptica, nomeadamente de hepatite alcolica (Cameron e Neuman,1999). Em suma, o fgado o rgo mais severamente afetado pelo alcoolismo sendo que o consumo excessivo de lcool provoca danos que envolvem uma sria de alteraes fisiolgicas e bioqumicas (Lieber, 1997) (figura 12). Dentro dos vrios efeitos txicos do lcool no fgado, destacam-se aqueles ligados ao seu metabolismo, demonstrando que o lcool exerce hepatotoxicidade intrnseca independente de deficincias nutricionais como estudos iniciais referiam (Lieber, 1997). Contudo, a hepatoxicidade do etanol no fgado para alm de envolver o metabolismo do lcool, tambm compreende mecanismos secundrios (Seth et al., 2011). Estudos recentes indicaram que a etopatogenia da DHA est profundamente ligada no s com o metabolismo do etanol mas tambm com o stress oxidativo, a depleo de glutationa, induo mediada pelo etanol da libertao de endotoxinas do intestino e consequente ativao das clulas de Kupffer e as clulas estreladas hepticas (Gao e Bataller, 2011).
16
Fisiopatologia da Doena Heptica Alcolica
Figura 12 - Diversos mecanismos da hepatotoxicidade do etanol no fgado ( Adaptado de Neuman,2004).
17
Fisiopatologia da Doena Heptica Alcolica
2.3 - Espectro da doena heptica alcolica A doena heptica alcolica engloba vrios estdios, assim o seu espectro diverso e inclui: a esteatose heptica alcolica, hepatite alcolica, fibrose alcolica, cirrose alcolica e hepatocarcionoma. Estes estdios no so necessariamente fases distintas da evoluo da doena, mas sim, vrias etapas que podem estar presentes simultaneamente num dado indivduo, sob a influncia de inmeros fatores de risco (figura 13) (Lieber,2000).
Figura 13 Fatores de risco da doena heptica alcolica ( Gao e Bataller, 2011).
18
Fisiopatologia da Doena Heptica Alcolica
2.3.1- Esteatose heptica A esteatose a manifestao mais precoce, mais frequente e menos grave da doena alcolica heptica, que compromete o parnquima heptico e caracteriza-se pela acumulao de gordura nos hepatcitos, decorrente do consumo crnico do etanol (figura 14) (Breitkopf et al., 2009; Arteel et al., 2009). Como j referido anteriormente, o etanol e os efeitos txicos do seu metabolismo originam vrias alteraes na funo normal do fgado. Desta forma, cabe ressaltar que a formao de acetaldedo e acetato, tanto pela via da enzima lcool desidrogenase assim como pela via do citocromo P450 2E1, causa disfunes mitocondriais (Yang,2008). Estudos prvios postulam que o consumo de lcool crnico e excessivo altera a relao NADH/NAD, aumentando a proporo de dinucletido de nicotinamida e adenina na forma reduzida/dinucletido de nicotinamida e adenina na forma oxidada nos hepatcitos, alterando, em consequncia, a - oxidao mitocondrial dos cidos gordos e resultando na acumulao dos mesmos nos hepatcitos, o que leva ao desenvolvimento da esteatose (Gao e Bataller,2011). Neste contexto, em condies normais os lpidos so transportados para o fgado na forma de cidos gordos livres, cuja maioria penetra o hepatcito e esterificada em triglicerdeos, ou oxidada produzindo energia sob forma de ATP e corpos cetnicos, existindo assim um ciclo constante de cidos gordos entre o fgado e o tecido adiposo, que est sob um delicado equilbrio (Lieber, 2004). No entanto, como j referido, o lcool altera as funes mitocondriais, aumentando a sntese e absoro dos cidos gordos e diminuindo a sua oxidao. Consequentemente, a no-utilizao destes cidos gordos resulta na acumulao excessiva de lpidos no interior dos hepatcitos e o desenvolvimento de esteatose heptica ( Lieber, 2004). No que diz respeito s manifestaes clnicas da esteatose, observa-se uma estreita relao com o grau da infiltrao de gordura, causa subjacente e ao tempo de exposio. De um modo geral, os indivduos mostram-se geralmente assintomticos, porm quando a infiltrao da gordura mais pronunciada pode ocorrer hepatomegalia, cujo aumento do volume heptico pode atingir at seis vezes o seu volume normal, dor
19
Fisiopatologia da Doena Heptica Alcolica
no hipocndrio direito e pode ocorrer a evoluo para um quadro de insuficincia heptica (Donohue,2007).
Figura 14 - Alteraes morfolgicas e histolgicas da esteatose ( Fonte: http://www.mayoclinic.com/health/medical/IM03725).
No que concerne s complicaes hepticas resultantes da esteatose, cabe salientar que esta uma condio patolgica benigna e reversvel, visto que a interrupo de
ingesto alcolica leva normalizao da arquitetura heptica, e que esta manifestao constitui uma alterao relevante e um fator de risco para o desenvolvimento de manifestaes hepticas avanadas, nomeadamente esteato-hepatite, fibrose, e cirrose heptica (figura 15 ) (Donohue,2007) .
Figura 15 - Inter-relaes entre as manifestaes da doena heptica alcolica (Adaptado de Shrestha e Shakya, 2011). 20
Fisiopatologia da Doena Heptica Alcolica
2.3.2- Hepatite alcolica A hepatite alcolica um processo inflamatrio associado necrose hepatocitria, resultante do consumo excessivo de lcool e considerada como uma leso pr-cirrtica (Trabut et al., 2012). Desta forma, a hepatite alcolica caracterizada pela infiltrao do fgado por clulas inflamatrias e leses hepatocelulares, podendo-se desenvolver em pacientes com esteatose e sendo associada fibrose progressiva (Trabut et al., 2012). No que diz respeitos aos mecanismos atravs dos quais o uso abusivo do etanol produz as leses mais caractersticas da hepatite alcolica, cabe salientar que a ao lesiva do etanol pode estar relacionada ao direta do seu metabolismo ou absoro de endotoxinas do intestino, decorrente da reduo da barreira intestinal induzida pelo etanol (Stickel e Seitz, 2010). Neste contexto, alm da agresso direta causada pelo stress oxidativo, todos os metabolitos originados pela oxidao do etanol podem interagir com aminocidos, provocando uma srie de alteraes funcionais e morfolgicas, nomeadamente, alteraes na tubulina importante elemento da constituio dos microtbulos- o que prejudica o transporte citoplasmtico (Gao e Bataller,2011). Alm disso, tambm, so observadas as alteraes nas protenas do citoesqueleto, como as citoqueratinas, resultando em depsitos hialinos no citoplasma, denominados corpsculos de Mallory ( Gao e Bataller ,2011). Por outro lado, como j citado anteriormente, o etanol favorece a absoro de endotoxinas e de outros produtos da flora intestinal, que atuam sobre as clulas de Kupffer promovendo a produo de citocinas, especialmente TNF-, mas tambm IL-1, IL- 6 e IL-8, favorecendo a inflamao, a agresso hepatocitria e a estimulao das clulas estreladas hepticas, com induo de fibrose (Trabut et al., 2012). A infiltrao neutroflica na hepatite alcolica deve-se produo de grande quantidade das quimiocinas CxCL 8 (IL-8) por parte das clulas de Kupffer, ativadas no s pelos metabolitos do etanol (acetaldedo e radicais livres), como pelos produtos bacterianos absorvidos do intestino ( Trabut et al., 2012).
21
Fisiopatologia da Doena Heptica Alcolica
Todos estes processos acabam por induzir o sistema imune a produzir anticorpos, clulas T auxiliares e citotxicas, capazes de agredir hepatcitos, contribuindo, desta forma, para a necrose e a inflamao ( figura 16) ( Gao e Bataller,2011). Neste contexto, ocorre a ativao da imunidade adaptativa, com consequentes nveis aumentados de anticorpos circulantes, originados para combater os aductos de peroxidao lipdica, e nmeros elevados de clulas T no fgado, o que indica que a ativao da imunidade adaptativa, est envolvida na patognese da doena heptica alcolica, inclusivamente na hepatite alcolica. Coletivamente com a ativao de componentes da imunidade inata no s se inicia a leso heptica alcolica, mas tambm se aciona a resposta hepato-protetora, regenerativa, e anti-inflamatria (figura16 ) ( Gao e Bataller, 2011).
Figura 16 - Mecanismos pelos quais o etanol causa inflamao na doena heptica alcolica ( Gao e Bataller ,2011).
de referir que, o quadro histolgico muito mais evidente do que a expresso clnica da doena. As caractersticas histolgicas da hepatite alcolica incluem: infiltrao neutroflica, balonizao centrolobular dos hepatcitos, necrose irregular, fibrose perivenular e ocorrncia de corpsculos de Mallory (figura 17) (Trabut et al., 2012).
22
Fisiopatologia da Doena Heptica Alcolica
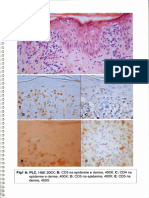
Figura 17 Alteraes histolgicas da hepatite alcolica ( Adaptado de http://www.kmle.co.kr/search.php?Search=alcoholic+hepatitis&Page=3).
No que concerne ao quadro clnico da hepatite alcolica, este apresenta um amplo espectro, variando de formas totalmente assintomticas a quadros fulminantes, sendo que, os casos assintomticos e as formas brandas so muito mais frequentes do que os casos graves. Por outro lado, as formas graves geralmente esto associadas a quadros fulminantes devido a surtos de hepatite alcolica em fgados j cirrticos (Gonalves et al., 2006). Assim, o incio da sintomatologia geralmente insidioso, com manifestaes inespecficas como a anorexia, nuseas e vmitos, mas quando o quadro clnico se agrava, surgem manifestaes como hepatomegalia dolorosa, febre, leucocitose, ictercia, podendo ou no ter outros sinais de insuficincia heptica e/ou hipertenso portal (esplenomegalia, ascite, varizes vasculares, etc.). Ao contrrio da esteatose, a hepatite alcolica aps curada, deixa cicatrizes permanentes no fgado, podendo levar ao aparecimento de fibrose (Gonalves et al., 2006).
23
Fisiopatologia da Doena Heptica Alcolica
2.3.3- Fibrose heptica A fibrose heptica alcolica pode ser definida como uma resposta de cicatrizao s leses hepticas desencadeadas pelo abuso crnico de etanol e caracterizada por uma deposio excessiva de matriz extracelular , que inclui trs grandes famlias de protenas: glicoprotenas colagnios e proteoglicanos ( Tsukada et al., 2006) . Como anteriormente referido, o etanol promove a fibrinognese tanto atravs do seu metabolito primrio, o acetaldedo, assim como pelo desenvolvimento de ROS, que ao originar stress oxidativo ativa as clulas de Kupffer, aumentando a produo de citocinas pr-inflamatrias e consequente ocorre a ativao das clulas estreladas hepticas. Nesta sequncia, as clulas hepticas estreladas, localizadas no espao de Disse, e aquando ativadas, proliferam-se e adquirem as caractersticas de miofibroblastos (Tsukada et al., 2006; Bataller e Brenner, 2005). Neste contexto, a deposio excessiva da matriz extracelular resultante do desequilbrio entre a fibrinognese e a fibrlise no fgado, sendo que a deposio de matriz extracelular passa a ser maior que a sua remoo, principalmente a nvel de colagnio tipo I e II, mas tambm proteoglicanos e glicoprotenas (Pinzani e Rombouts,2004).
Em condies normais, o metabolismo da matriz extracelular realizado por enzimas designadas por metaloprotenases (MMPS), que so produzidas pelas clulas estreladas hepticas e clulas de Kupffer. Estas enzimas e os seus inibidores especficos (TIMPsinibidores tissulares de metaloprotenases), garantem o equilbrio na remodelao da matriz extracelular, uma vez que esto envolvidas na degradao das protenas da matriz, nomeadamente o colagnio I, o principal tipo presente no fgado fibrtico (Guedes, 2004). Porm, estas enzimas so reguladas por inibidores fisiolgicos, que esto atuantes no processo fibrtico e impedem a atividade dessas enzimas sobre o excesso de matriz, que por sua vez no degradada e se acumula, resultando em fibrose heptica (Friedman,2008).
24
Fisiopatologia da Doena Heptica Alcolica
Deste modo, a ativao de clulas estreladas hepticas em resposta leso heptica, ocorre em duas etapas: a iniciao e a perpetuao ( figura 18 ) ( Friedman, 2008) . A iniciao provocada por estmulos solveis, que incluem ROS, resultante do stress oxidativo, assim como por lipopolissacardeos, clulas de Kupffer, hepatcitos, clulas endoteliais sinusoidais, leuccitos, plaquetas e corpos apoptticos circulantes (Guedes,2004). A perpetuao que se segue caracterizada por um certo nmero de alteraes fenotpicas especficas, incluindo proliferao, fibrinognese, contratilidade, degradao da matriz extracelular, quimiotaxia e sinalizao inflamatria (Friedman, 2008).
Figura 18- Vias de ativao das clulas hepticas estreladas aps leso heptica ( Friedman, 2008).
25
Fisiopatologia da Doena Heptica Alcolica
Cabe ressaltar que inicialmente na doena heptica alcolica, o excesso de matriz extracelular, isto , a leso fibrtica inicia-se na zona III do lbulo heptico com fibrose perivenular que acomete a veia centrolobular (figura 19). No entanto, posteriormente ocorre a evoluo para fibrose septal, ocorrendo ligao entre as veias centrolobulares e os espaos portais, com consequente formao de septos fibrosos (Guedes, 2004) .
Figura 19- Lbulo heptico (Micheu e Hoa, 2012).
Alm disso, a transformao das clulas estreladas em miofibroblastos e consequente desorganizao da arquitetura parenquimatosa, tambm origina o aumento da resistncia vascular, pois ocorre a ativao de substncias vasoconstritoras, o que constringe os canais vasculares, resultando na resistncia portal aumentada (Friedman, 2008). A progresso d fibrose heptica leva cirrose, podendo ocorrer descompensao desta, com consequente hipertenso portal, e em ltima anlise, insuficincia heptica (Mormone et al., 2011).
26
Fisiopatologia da Doena Heptica Alcolica
2.3.4 - Cirrose heptica Com j referido anteriormente, o principal agente etiolgico entre os pacientes com cirrose o lcool, ressaltando que a cirrose heptica alcolica, designada em termos histricos como cirrose de Laennec, responsvel por cerca de 90% do total de cirroses em Portugal (Matos, 2006). Existem evidncias que a cirrose heptica alcolica ocorre quando h consumo significativo de lcool por perodos de mais de 10 anos, nomeadamente 60 a 80 g etanol/dia em homens e 20g etanol/dia em mulheres. Contudo, se houver associao com outros fatores agressores do fgado, tais como hepatites virais, sndrome metablica, depsitos de ferro ou uso de medicamentos hepatotxicos, o perodo e a quantidade de lcool necessrios podem ser menores (Diehl, 2001). A cirrose heptica uma leso crnica do fgado, consequente de todas as doenas hepticas crnicas e ocorre por um processo difuso, caracterizado por fibrose tecidual e pela converso da arquitetura normal em ndulos estruturalmente anormais, sendo tradicionalmente considerada como uma leso irreversvel, muito embora estudos recentes questionem a sua irreversibilidade (Pinzani et al., 2011). A forma como o acetaldedo, resultante do consumo excessivo do lcool, lesa a clula heptica j foi amplamente debatida. Cabe ressaltar, que a instalao da fibrose e da regenerao nodular do fgado determina alteraes na funo dos hepatcitos e o aparecimento de diversas complicaes (Pinzani et al., 2011). Do ponto de vista morfolgico, as caractersticas da cirrose incluem: fibrose difusa, ndulos regenerativos, arquitetura lobular alterada e estabelecimento de shunts vasculares intra-hepticos entre a veia porta e a artria heptica, bem como a veia supraheptica do fgado (Millward-Sadler et al., 1985). Por outro lado a nvel macroscpico, estabelecido que existem dois padres de regenerao nodular: cirrose micronodular e macronodular, sendo que a cirrose causada pelo lcool , predominantemente, do tipo micronodular. Desta forma o fgado cirrtico pode-se apresentar com um tamanho inicialmente aumentado e posteriormente reduzido, com o lobo caudado, via de regra, hipertrfico e com contorno nodular irregular (figura 20) (Robbins et al., 1996).
27
Fisiopatologia da Doena Heptica Alcolica
Figura 20- Cirrose micronodular e macronodular ( Castro, 2012 ).
Relativamente s manifestaes clnicas da cirrose, estas so amplas e variam muito desde a ausncia de sintomas at ao desenvolvimento de complicaes, muitas delas fatais, sendo as principais: hipertenso portal (manifestada por varizes esofgicas e gstricas e esplenomegalia), ascite, peritonite bacteriana espontnea, encefalopatia heptica, sndrome hepato-renal e carcinoma hepatocelular (Pinzani et al., 2011). Do ponto de vista fisiolgico, a veia porta resultante da confluncia da veia esplnica e das veias mesentricas superior e inferior, sendo responsvel pela drenagem da circulao esplncnica para o fgado. Assim, o fgado o principal stio de resistncia ao fluxo venoso portal e age como uma rede vascular distensvel de baixa resistncia. Deste modo, a presso venosa portal normalmente baixa (5-10 mmHg), sendo a hipertenso portal definida como uma presso anormalmente elevada na veia porta (superior a 10 mmHg) (Garcia-Pagan et al., 2005). Assim, a hipertenso portal ocorre como consequncia de mudanas estruturais da arquitetura heptica decorrente da cirrose e pode resultar do aumento da resistncia ao fluxo portal ou do aumento do fluxo sanguneo portal, ou, ainda, de ambos (Pinzani et al., 2011). Neste contexto, por um lado o aumento de fluxo sanguneo portal pode ocorrer como causa primria de hipertenso portal, mas um evento raro. Ao contrrio, o aumento da
28
Fisiopatologia da Doena Heptica Alcolica
resistncia o evento mais comum e pode ocorrer em qualquer ponto ao longo do sistema venoso, na veia porta, nos espaos vasculares dentro do fgado e nas veias e compartimentos vasculares que recebem o fluxo portal aps sair do fgado (Martinelli,2004). Cabe ressaltar que a hipertenso portal a consequncia mais antiga e mais importante da cirrose e subjaz a maioria das complicaes clnicas da doena, sendo de facto o principal mecanismo que leva morte de pacientes cirrticos (Martinelli,2004). De acordo com a localizao anatmica do obstculo ao fluxo sanguneo, a hipertenso portal pode ser classificada em: pr-heptica, ps-heptica e intra-heptica, sendo que, na cirrose heptica, o aumento da resistncia ao fluxo portal principalmente do tipo pr-heptico sinusoidal e ps- sinusoidal (Martinelli,2004). A ocorrncia da hipertenso portal adquire muita relevncia, devido frequncia e gravidade das suas complicaes, que representam a primeira causa de internamento hospitalar, transplante de fgado e morte em pacientes com cirrose, uma vez que a hipertenso portal cirrtica uma doena vascular que envolve vrios sistemas e rgos cujas principais manifestaes clnicas so: hemorragia por varizes gastro-esofgicas, esplenomegalia, ascite, circulao colateral superficial (veias abdominais e periumbilicais) e varizes de reto (Costaguta e Alvarez,2010). No que refere s varizes esofgicas, estas so veias anormalmente dilatadas, geralmente localizadas no tero distal do esfago, podendo tambm ocorrer na parede gstrica, que surgem como resultado da tenso elevada nas paredes dos vasos que leva sua dilatao e rutura, uma consequncia do aumento da presso do sangue na veia porta (Costaguta e Alvarez,2010). A rutura das varizes esofgicas e/ou gstricas a causa mais comum de hemorragia digestiva na hipertenso portal e est geralmente acompanhada por esplenomegalia (aumento do bao) e hiperesplenismo, o que faz com que o bao aumente a sua funo e consequentemente ocorra o aumento da destruio de clulas sanguneas,
nomeadamente as plaquetas (figura 21) (Costaguta e Alvarez, 2010).
29
Fisiopatologia da Doena Heptica Alcolica
Figura 21 Circulao portal: A: sistema de portal normal. B: fgado cirrtico: formao de varizes e esplenomegalia (Costaguta e Alvarez, 2010).
No que diz respeito ascite, outra das complicaes da hipertenso portal, esta definida por um acmulo anormal de lquido na cavidade peritoneal, em torno do intestino e outros rgos abdominais e notada pelo aumento do volume abdominal (figura 22) (Bernardi et al., 2004).
Figura 22 Ascite (Fonte: http://www.hepcentro.com.br/ascite.htm).
30
Fisiopatologia da Doena Heptica Alcolica
Neste contexto, a hipertenso portal aumenta a presso hidrosttica dentro dos sinusoides hepticos e favorece a transudao de fluido para a cavidade peritoneal (Moore e Aithal, 2006). Desta forma, as alteraes vasculares hepticas e a consequente hipertenso portal ativam a vasodilatao esplncnica (sequestro lquido no terceiro espao),que posteriormente origina um deficit no volume sanguneo efetivo e a queda na presso arterial, que tem como consequncia a ativao de fatores neuro humorais, que por sua vez, ativam sistemas endgenos como: sistema renina angiotensina aldosterona, sistema nervoso simptico e libertao de hormona antidiurtica, como tentativa de restaurar a homeostasia sangunea (figura 24) (Moore e Aithal, 2006). Assim, como consequncia ocorre a reteno de sdio e gua no organismo, que juntamente com o aumento da permeabilidade vascular esplncnica e acumulao de linfa na cavidade peritoneal origina a formao da ascite (figura 23) (Bernardi et al., 2004).
Figura 23 - Lquido acumulado na cavidade peritoneal ( Adaptado de http://www.medicalook.com/Digestive_system/Ascites.html).
31
Fisiopatologia da Doena Heptica Alcolica
Cirrose Aumento da resistncia vascular intra-heptica Hipertenso portal Vasodilatao esplncnica Aumento do volume plasmtico Hipotenso arterial Aumento fatores neuro-humorais Reteno de sdio e gua ASCITE
Figura 24 - Mecanismos de ascite na cirrose heptica.
Os pacientes com cirrose e ascite podem desenvolver infeo bacteriana aguda no lquido peritoneal, denominada de peritonite bacteriana espontnea. Atualmente sugere-se que a maioria dos episdios de peritonite bacteriana resultante da translocao bacteriana de origem intestinal, em que ocorre a migrao de bactrias do lmen intestinal para os linfonodos mesentricos ou outros stios extraintestinais, representando a rutura do equilbrio da flora intestinal normal do hospedeiro, causando uma resposta inflamatria sustentada podendo, finalmente, acarretar infeo (Strauss e Caly , 2003) . No que concerne a outra manifestao clnica, a encefalopatia heptica definida como um sndrome neuropsiquitrico complexo, caracterizada por distrbios da conscincia e do comportamento com alteraes de personalidade (Albrecht e Jones , 1999) . Acredita-se que a encefalopatia heptica seja desencadeada por substncias txicas que atingem o crebro. Essas substncias no so eliminadas na detoxificao realizada pelo fgado devido funo heptica comprometida, ou pela presena de shunts portosistmicos que impedem a detoxificao heptica. A principal substncia envolvida nesse processo a amnia, sendo considerada um composto altamente neurotxico (Wright e Jalan, 2007).
32
Fisiopatologia da Doena Heptica Alcolica
Por fim, outra complicao da hipertenso portal que pode surgir o sndrome hepatorenal (SHR), que ocorre em pacientes com doena heptica crnica, sendo caracterizado pela alterao da funo renal, sem leso morfolgica (Arroyo et al.,2002). Desta forma o SHR responsvel por diversas alteraes da funo renal, nomeadamente pela reteno de sdio, alterao da excreo de gua, diminuio da perfuso renal e da taxa de filtrao glomerular, sendo o seu mecanismo de patologia esquematizado na figura 25 (Gins et al., 2003). Como resultado o SHR origina vrias manifestaes clinicas como azotemia progressiva, hipotenso, hiponatremia, insuficincia heptica e insuficincia renal (Arroyo et al., 2002).
Cirrose heptica Hipertenso portal Vasodilatao esplncnica acentuada Estimulao dos sistemas vasoconstritores Vasoconstrio renal SHR
Figura 25 - Fisiopatologia da SHR.
33
Fisiopatologia da Doena Heptica Alcolica
2.3.5- Carcinoma hepatocelular O carcinoma hepatocelular a sexta neoplasia mais comum no mundo e a terceira causa mais frequente de morte por tumor maligno, sendo que na maioria dos casos, o carcinoma hepatocelular surge como uma das complicaes da cirrose, representando o estado final da doena, sendo considerado uma das principais causas de morte entre os pacientes com cirrose (Forner et al., 2012). Neste contexto, bem estabelecida a associao entre o abuso crnico de lcool e o desenvolvimento de cirrose, assim como entre o desenvolvimento de cirrose e consequente CHC. No entanto, a relao direta entre o consumo de lcool e o desenvolvimento de CHC, ainda no est bem esclarecida (El-Serag, 2011). Alm disso, estudos evidenciaram que a presena de hepatite viral, outra condio frequente em pacientes alcolicos, aumenta significativamente o risco de
desenvolvimento do cancro do fgado (Tinkle e Haas-Kogan, 2012 ). No que concerne patognese molecular do carcinoma hepatocelular, um processo complexo, de mltiplos passos e a maioria dos investigadores concorda que os efeitos do metabolismo do etanol sobre a integridade do DNA e mecanismos de reparao desempenham um papel significativo na processo de transformao (Mckillop et al., 2006). No entanto, torna-se cada vez mais evidente que o etanol, o metabolismo do etanol, ou ambos tambm podem afetar as vias de sinalizao de clulas que regulam a funo normal dos hepatcitos, a sua proliferao e apoptose (Mckillop et al., 2006). Assim, o metabolismo do etanol contribui para o desenvolvimento de carcinoma hepatocelular especificamente em doentes com doena alcolica heptica,
nomeadamente devido formao de acetaldedo, que uma substncia cancergena com propriedades mutagnicas, induo de CYP2E1, que aumenta a produo de ROS, e ao efeito imunossupressor do lcool (Gao e Bataller ,2011). Por outro lado, as mutaes no DNA e na proliferao dos hepatcitos so causadas por vrios mecanismos que incluem: encurtamento dos telmeros (que induz a instabilidade genmica), alteraes no microambiente e macroambiente, que promovem a sobrevivncia e proliferao de clulas tumorais, perda de postos de controlo do ciclo
34
Fisiopatologia da Doena Heptica Alcolica
celular, nomeadamente supressores tumorais e ativao de vias oncognicas (Gao e Bataller ,2011) . De acordo com os estudos de Gao e Bataller (2011) e Conte (2000), num primeiro momento ocorre hiperplasia (proliferao anormal de clulas) e com o agravamento da doena, ocorre a displasia, j com instabilidade genmica. Posteriormente, esta instabilidade genmica agrava-se e somada perda do gene supressor de tumores (p53) e reativao da telomerase, forma-se ento o carcinoma hepatocelular (figura 26).
Figura 26 Hepatocarcinognese ( Paraskevi et al., 2006 ).
Relativamente s manifestaes clnicas, cabe ressaltar que os sintomas atribuveis ao carcinoma hepatocelular, numa fase inicial so geralmente ausentes, sendo este, portanto, assintomtico (Tinkle e Haas-Kogan, 2012). Porm, quando existe a presena de sintomas, estes podem estar relacionados com a cirrose subjacente na maior parte dos casos. Entretanto, a maioria dos pacientes apresenta dor abdominal superior mal definida, perda de peso acentuada e progressiva, massa ou irregularidades palpveis e, com a descompensao heptica, esplenomegalia, com aumento da ascite, hemorragia digestiva, encefalopatia (Tinkle e Haas-Kogan, 2012 ).
35
Fisiopatologia da Doena Heptica Alcolica
de referir que, o carcinoma hepatocelular pode estar associado a um nmero de sndromes para-neoplsicos resultando em: hipoglicemia, hipercolesterolemia,
eritrocitose, hipercalcemia, trombocitose, manifestaes cutneas (Tinkle e HaasKogan, 2012 ). Cabe ressaltar, ainda, que macroscopicamente o CHC pode ser classificado conforme dois padres distintos: quanto sua forma e tamanho e quanto ao padro de crescimento (Kojiro, 1998) No que respeita forma e tamanho, distingue-se o tipo nodular, indicando uma massa arredondada com limites ntidos em relao ao parnquima circundante; o tipo macio, no qual uma grande massa aparenta invadir o parnquima adjacente; e o tipo difuso, no qual mltiplos ndulos semelhantes a ndulos cirrticos so encontrados por todo o fgado (Kojiro, 1998). Quanto ao padro de crescimento, so referidos o crescimento unifocal, multifocal e infiltrante. O tumor unifocal tem uma ntida demarcao entre os limites da massa tumoral e do parnquima circundante, sendo uma massa unifocal geralmente grande (figura 28). O tumor multifocal (figura 29) geralmente representado por mltiplos ndulos em diversos segmentos hepticos, e o tumor infiltrante, (figura 30) o mais comum em fgados cirrticos, possui os seus limites mal definidos e irregulares e com frequente invaso vascular (figura 27) (Kojiro, 1998).
Figura 27 Carcinoma hepatocelular difuso num fgado cirrtico (Ficher, 2010).
36
Fisiopatologia da Doena Heptica Alcolica
Figura 28 Carcinoma hepatocelular unifocal num fgado cirrtico ( Peterson et al., 2000).
Figura 29 Carcinoma hepatocelular multifocal (Fonte: http://escuela.med.puc.cl/paginas/cursos/tercero/anatomiapatologica/imagenes_ap/fotos588-596/589.jpg).
Figura 30- Carcinoma hepatocelular infiltrante (http://galeria.sld.cu/main.php?g2_itemId=28246).
37
Fisiopatologia da Doena Heptica Alcolica
Assim, de uma forma geral, a apresentao clnica do carcinoma hepatocelular depende, principalmente, da extenso da neoplasia e do nvel de comprometimento da funo heptica pela doena de base, sendo que a evoluo natural consiste no aumento progressivo da massa primria at que esta comprometa a funo heptica e / ou evolua para metstases, nomeadamente para os pulmes em primeiro lugar e posteriormente para outros locais como a glndula adrenal, linfonodos, ossos e crebro (Tinkle e HaasKogan, 2012 ). Num estdio final da doena, a morte ocorre mais comumente por: caquexia, hemorragia gastrintestinal ou de varizes esofgicas, insuficincia heptica ou coma heptico e mais raramente, por rutura do tumor com hemorragia fatal (Tinkle e HaasKogan, 2012 )
38
Fisiopatologia da Doena Heptica Alcolica
3- Consideraes finais O consumo excessivo e crnico de etanol representa uma das maiores causas de mortalidade e morbilidade de todo o mundo, ressaltando-se a doena heptica alcolica, cujo espectro envolve: esteatose, hepatite alcolica, fibrose heptica, cirrose e carcinoma hepatocelular. No que concerne fisiopatologia da doena heptica alcolica, verifica-se uma relao estreita entre a hepatoxicidade direta do etanol, as consequncias advindas do processo metablico, a produo de metabolitos txicos e a participao de citocinas, com as leses hepticas decorrentes Dada prevalncia e gravidade da doena heptica alcolica, bem como seu elevado custo mdico-social, torna-se imperativa a necessidade da implementao de programas que envolvam a preveno da doena alcolica e a assistncia do doente alcolico. A considerar o importante papel dos profissionais de Cincias Farmacuticas, enquanto profissionais de sade, a abordagem da temtica reveste-se de enorme relevncia, possibilitando maior e melhor qualificao para a orientao adequada dos doentes alcolicos.
39
Fisiopatologia da Doena Heptica Alcolica
4- Bibliografia 1. Albrecht, J. e Jones, E. A. (1999). Hepatic encephalopathy: molecular
mechanisms underlying the clinical syndrome, Journal of the Neurological Sciences, 170, pp. 138-146. 2. Arroyo, V., et al. (2002). Hepatorenal syndrome in cirrhosis: Pathogenesis and
treatment, Gastroenterology, 122, pp. 1658-1676. 3. Arteel, G. (2003). Advances in alcoholic liver disease, Best Practice &
Research Clinical Gastroenterology, 17, pp. 625-647. 4. Bataller, R. e Brenner, D. A. (2005). Liver fibrosis, The Journal of Clinical
Investigation, 115, pp. 209-218. 5. Bedossa, P. e Paradis, V. (1995). Transforming growth factor-beta (TGF-beta): a
key role in liver fibrogenesis, Journal of Hepatoly, 22(2), pp. 37-42. 6. Bernardi, M., et al. (1994). Renal sodium handling in cirrhosis with ascites:
mechanisms of impaired natriuretic response to reclining, Journal of Hepatology, 21, pp. 1116-1122. 7. Breitkopf, K., et al. (2009). Current Experimental Perspectives on the Clinical
Progression of Alcoholic Liver Disease, Alcoholism: Clinical and Experimental Research, 33, pp. 1647-1655. 8. Bruha, R., et al. (2012). Alcoholic liver disease, World Journal of Hepatology,
4, pp. 81-90. 9. Caballera, J. (2003). Current concepts in alcohol metabolismo, Annals of
Hepatology, 2, pp. 60-68. 10. Cameron, R.G., e Neuman, M.G. (1999). Novel morphologic findings in
alcoholic liver disease, Clinical Biochemistry, 32, pp. 579584. 11. Casini, A., et al. (1991). Acetaldehyde increases procollagen type I and
fibronectin gene transcription in cultured rat fat-storing cells through a protein synthesis-dependent mechanism, Hepatology, 13, 758-65.
40
Fisiopatologia da Doena Heptica Alcolica
12.
Castro, J.M. (2012). Hepatites Cronicas e Cirrose. [Em linha] Disponvel em
<http://dc356.4shared.com/doc/ZBQP0eJb/preview.html> [Consultado em 22/06/2012]. 13. Conte, V. P. (2000). Carcinoma hepatocelular. Parte 1: consideraes gerais e
diagnstico, Arquivos de Gastroenterologia, 37, pp. 58-67. 14. Costaguta, A. e Alvarez, F. (2010) Hipertensin portal en pediatra. I: Aspectos
fisiopatolgicosy clnicos, Arch. argent. pediatr, 108(3), pp. 239-249 . 15. Diehl, A. M. (2002). Liver disease in alcohol abusers: clinical perspective, Alcohol, 27, pp. 7-11. 16. Donohue, T.M. (2007). Alcohol-induced steatosis in liver cell, World Jounal
Gastroenteroly. 2007, 13(37), pp.4974-4978. 17. Dominguez M., et al. ( 2009) Hepatic expression of CXC chemokines predicts
portal hypertension and survival in patients with alcoholic hepatitis, Gastroenterology, 136, pp. 16391650. 18. ElSerag, H. B. (2011). Hepatocellular carcinoma, New England Journal of
Medicine, 365, pp. 1118-1127. 19. Escuela de Medicina Home Page. [Em linha]. Disponvel em
<http://escuela.med.puc.cl/paginas/cursos/tercero/anatomiapatologica/imagenes_ap/foto s588-596/589.jpg> [Consultado em 22/08/2012]. 20. FernandezCheca, J.C., et al. (1996) Plasma membrane and mitochondrial
transport of hepatic reduced glutathione, Seminars in Liver Disease, 16, pp. 147158. 21. Fischer, K.G. ( 2010) . Carcinoma hepatocelular, Revista Dolor, Foro Nacional
de Investigacin y Clnica Mdica, 7, pp. 4-7 22. 1255. 23. Friedman, S. (1999). Liver fibrogenesis and the role of hepatic stellate cells: new Forner E. R., et al., (2012) Hepatocellular carcinoma, The Lancet, 379, pp. 1245-
insights and prospects for therapy, Jounal Gastroenteroly Hepatoly. 14,pp. 618633.
41
Fisiopatologia da Doena Heptica Alcolica
24.
Friedman, S. L. (2008). Mechanisms of Hepatic Fibrogenesis, Gastroenterology,
134, pp. 1655-1669. 25. Gao, B. e Bataller, R. (2011). Alcoholic liver disease: pathogenesis and new
therapeutic targets, Gastroenterology 141(5), pp. 1572-85. 26. 27. 68. 28. Gramenzi, A., et al. (2006). Review article: alcoholic liver disease-Gins, P., et al . (2003). Hepatorenal syndrome, The Lancet, 362, pp. 1819-1827. Gonalves C. J. et al. (2006). Hepatite alcolica, Gastroenterologia, 6(2), pp.59-
pathophysiological aspects and risk factos, Aliment Pharmacol Ther, 24,pp. 1151-1161.
29.
Guedes, A. (2004). Estudo dos marcadores sricos de fibrose hepatica crnica
pelo alcol e/ou infeco pelo VHC. Dissertao apresentada ao Instituto de Cincias Biomdicas de Abel Salazar.
30.
Hepcentro
Home
page.
[Em
linha]
Disponvel
em
<http://www.hepcentro.com.br/ascite.htm> [Consultado em 6/6/2012]. 31. Hritz, I. et al. (2008) The critical role of toll-like receptor (TLR) 4 in alcoholic
liver disease is independent of the common TLR adapter MyD88, Hepatology, 48, pp. 1224 1231. 32. Infomed Galeria Home page [Em linha]. Disponvel em
http://galeria.sld.cu/main.php?g2_itemId=28246 [Consultado em 22/08/2012]. 33. Katz, G., et al.(2001) Signaling for ethanolinduced apoptosis and repair in
vitro, Clinical Biochemistry 34, pp.219227. 34. Kojiro M. (1998). Pathology of early hepatocellular carcinoma: progression
from early to advanced, Hepatogastroenterology, 45(3), pp. 1203-1205. 35. Korean Medical Library Engine Home Page. [Em linha]. Disponvel em
<http://www.kmle.co.kr/search.php?Search=alcoholic+hepatitis&Page=3> [Consultado em 1/08/2012].
42
Fisiopatologia da Doena Heptica Alcolica
36.
Laposata, E.A e Lange, L.G. (1986). Presence of nonoxidative ethanol
metabolism in human organs commonly damaged by ethanol abuse, Science, 231, pp. 497-499. 37. Lieber, C.S. (1995) Medical disorders of alcoholism, The New England Journal
of Medicine, 333(16) pp. 1058-1065. 38. Lieber, C. S. (1997b). Ethanol metabolism, cirrhosis and alcoholism, Clinica
Chimica Acta, 257, pp. 59-84. 39. Lieber, C. S., (2000). Alcohol and the Liver: metabolism of alcohol and its role
in hepatic and extrahepatic diseases, The Mount Sinai Journal of Medicin, 67 (1), pp. 84-94. 40. Lieber, C. S. (2004). Alcoholic fatty liver: its pathogenesis and mechanism of
progression to inflammation and fibrosis, Alcohol, 34,pp. 9-19. 41. Mann, J. e Mann, D. A. (2009). Transcriptional regulation of hepatic stellate cells, Advanced Drug Delivery Reviews, 61, pp. 497-512. 42. Martinelli A.L. (2004) Hipertenso portal, Medicina, Ribeiro Preto, 37, pp.
253-261. 43. Matsuo, K., et al. (2006). Alcohol dehydrogenase 2 His47Arg polymorphism
influences drinking habit independently of aldehyde dehydrogenase 2 Glu487Lys polymorphism: analysis of 2,299 Japanese subjects, Cancer Epidemiol Biomarkers Prev, 15, pp. 1009-1013 44. Mayo Clinic Home Page. [Em linha]. Disponvel em
<http://www.mayoclinic.com/health/medical/IM03725> [Consultado em 05/07/2012]. 45. McClain, C., et al. (1997). Cytokines and Alcoholic Liver Disease, Alcohol
Health & Research World, 21(4) pp. 317-320. 46. Mckillop I. H., et al. (2006). Molecular Pathogenesis of Hepatocellular
Carcinoma, Journal of Surgical Research, 136, pp. 125-135.
43
Fisiopatologia da Doena Heptica Alcolica
47.
Medicalook
Home
Page.
[Em
linha].
<Disponivel [Consultado
em em
<http://www.medicalook.com/Digestive_system/Ascites.html> 25/07/2012]. 48.
Mello, M.L., et al. (2001). lcool e problemas ligados ao lcool em Portugal:
Direco Geral de Sade. 49. Micheu, A. E Hoa D. (2012) Anatomia do sistema digestivo e abdmen:
ilustraes. [Em linha]. Disponvel em http://www.imaios.com/br/e-Anatomy/ToraxAbdome-Pelve/Sistema-digestorio-Ilustracoes [Consultado em 20/06/2012]. 50. Millward-Sadler, G.H., et al. (1985). Cirrhosis: an appraisal. In: Wright R,
Millward-Sadler GH, Alberti KGMM, Karran S, editors. Liver and biliary disease. 2nd ed. London, pp. 82160. 51. Moore K. P. e Aithal G.P. (2006). Guidelines on the management of ascites in
cirrhosis,Gut, 55 (6), pp.1-12 . 52. Mormone, E., et al. (2011). Molecular pathogenesis of hepatic fibrosis and
current therapeutic approaches, Chemico-Biological Interactions, 193, pp. 225-231. 53. Neuman, M.G. (2001) Apoptosis in diseases of the liver. Critical Reviews in
Clinical and Laboratory Science 38, pp. 109166. 54. Neuman, M.G. (2003). Cytokines central factors in alcoholic liver
disease, Alcohol Res. & Health , 27 (4), pp. 307315. 55. Neuman, M.G., et al. (2001) Alcoholic liver injury and apoptosissynopsis of
the symposium held at ESBRA 2001: 8th Congress of the European Society for Biomedical Research on Alcoholism, Alcohol, 28, pp. 117128. 56. OShea, R.S., et al. (2010). Alcoholic Liver Disease, Hepatology, 51 (1), pp.
307-28. 57. Paraskevi, A., et al. (2006) Hepatocellular carcinoma pathogenesis: from genes
to environment, Nature Reviews Cancer, 6,pp. 674-687.
44
Fisiopatologia da Doena Heptica Alcolica
58.
Parlesak A, et al. (2000). Increased intestinal permeability to macromolecules
and endotoxemia in patients with chronic alcohol abuse in different stages of alcoholinduced liver disease, Journal of Hepatology, 32(5) pp. 742-747. 59. Peterson, M. S., et al. (2000). Pretransplantation Surveillance for Possible
Hepatocellular Carcinoma in Patients with Cirrhosis: Epidemiology and CT-based Tumor Detection Rate in 430 Cases with Surgical Pathologic Correlation1, Radiology, 217, pp. 743-749. 60. Pinzani, M., et al. (2011). Liver cirrhosis. Best Practice & Research
Clinical Gastroenterology , 29(2), pp. 243-148. 61. Pinzani, M. e Rombouts, K. (2004). Liver fibrosis: from the bench to clinical
targets. Digestive and Liver Disease, 36, pp. 231-242. 62. Rebello, S.A e Carvalho M.C. (2008). Metodologia para estudo do polimorfismo
do gene da enzima lcool desidrogenase. Revista de Cincias Mdicas e Biolgicas, 7(2), pp.163-168. 63. Suddendorf, R. F. (1989) Research on alcohol metabolism among Asians and its
implications for understanding causes of alcoholism, Public Health Rep, 104 (6), pp. 615620. 64. Seeley,et al. (2003). Aparelho digestivo. In: Anatomia & Fisiologia. 6 Ed.
Loures , Lusocincia, 23, pp. 898-903. 65. Sherlock, S. e Dooley, J. (2002). Alcohol and the Liver. In: Sherlock, S. e
Dooley, J. Diseases of the Liver and Billiary System. 11 Ed. Oxford Blackwell Science, pp . 381-98. 66. Shrestha, S e Shakya, S. (2011). Morphology of alcoholic liver disease. [Em
linha]. Disponvel em <http://medchrome.com/basic-science/pathology/morphologyalcoholic-liver-disease/> [Consultado em 22/08/2012] 67. Stewart, S. F., et al. (2004). Oxidative stress as a trigger for cellular immune
responses in patients with alcoholic liver disease, Hepatology, 39, pp. 197-203.
45
Fisiopatologia da Doena Heptica Alcolica
68.
Seth, D., et al. (2011), Pathogenesis of Alcohol-induced Liver Disease
classical concepts and recent advances, Journal of gastroenterology and hepatology. 26(7), pp. 1089-105. 69. Stickle, F. e Seitz , H. K. (2010). Alcoholic steatohepatitis. Best Practice &
Research Clinical Gastroenterology, 24, pp. 683-93. 70. Strauss, E. e Caly, W. R. (2003). Peritonite bacteriana espontnea. Revista da
Sociedade Brasileira de Medicina Tropical, 36, pp. 711-717. 71. Tilg H. e Diehl, A. M.(2000). Cytokines in alcoholic and nonalcoholic
steatohepatitis, New England Journal of Medicine, 343, pp. 14671476. 72. Tinkle, C. L. e Haas-Kogan, D. (2012). Hepatocellular carcinoma: natural
history, current management, and emerging tools, Biologics, 6,pp.207-219. 73. Townsend, D. M., et al. (2003). The importance of glutathione in human disease.
Biomedicine & Pharmacotherapy, 57, pp. 145-155. 74. Trabut, J.B et al., 2012. Hpatite alcoolique aigu, La Revue de Mdecine
Interne, 33, pp. 311-317. 75. Tsukada, S., et al. ( 2006). Mechanisms of liver fibrosis, Clinica Chimica Acta,
364, pp. 33-60. 76. Wright, G. e Jalan, R. (2007). Management of hepatic encephalopathy in
patients with cirrhosis, Best Practice & Research Clinical Gastroenterology, 21, pp. 95-110. 77. Yang, S. (2008). Alcoholic Liver Disease: Clinical and Sonographic Features,
Journal of Medical Ultrasound, 16, pp. 140-149. 78. World Health Organization(2011) . Global status report on alcoholic and health.
Geneva. Department of Mental Health and Substance Abuse.
46
Vous aimerez peut-être aussi
- Microbiologia - Tortora 10a Edição - 2 527 PDFDocument1 pageMicrobiologia - Tortora 10a Edição - 2 527 PDFCarlos Eduardo Barbosa100% (1)
- Farmacologia AnotaçõesDocument34 pagesFarmacologia AnotaçõesMonique Lopes da SilvaPas encore d'évaluation
- Lista-7 SN PDFDocument8 pagesLista-7 SN PDFMonique Lopes da SilvaPas encore d'évaluation
- Aula Concurso SusDocument55 pagesAula Concurso SusMonique Lopes da SilvaPas encore d'évaluation
- Relatório Resistividade e Leis de Ohm PDFDocument11 pagesRelatório Resistividade e Leis de Ohm PDFMonique Lopes da SilvaPas encore d'évaluation
- Relatório 2 - Análise de Gordura - Método Soxhlet.Document3 pagesRelatório 2 - Análise de Gordura - Método Soxhlet.Monique Lopes da SilvaPas encore d'évaluation
- Apostila Parasitologia-LIVROPARDocument106 pagesApostila Parasitologia-LIVROPARLuiz Ricardo RottaPas encore d'évaluation
- Materiais para Fabricação MecânicaDocument111 pagesMateriais para Fabricação MecânicaMonique Lopes da SilvaPas encore d'évaluation
- Amaroli-Agua Da VidaDocument7 pagesAmaroli-Agua Da VidaMário FonsecaPas encore d'évaluation
- TCC Jaqueline - VERSÃO FINALDocument35 pagesTCC Jaqueline - VERSÃO FINALBruno AguiarPas encore d'évaluation
- Imuno Alergia PDFDocument4 pagesImuno Alergia PDFJosefa MoreiraPas encore d'évaluation
- CandidiaseDocument9 pagesCandidiaseTamiris PupoPas encore d'évaluation
- Secretaria de Estado de Saúde Do DF - Impressão de Resultados - Cristiane Silva Da Conceicao PereiraDocument6 pagesSecretaria de Estado de Saúde Do DF - Impressão de Resultados - Cristiane Silva Da Conceicao Pereiracristian Silva da conceição pereiraPas encore d'évaluation
- A História Da Doença - PotterDocument18 pagesA História Da Doença - PotterBruna MottaPas encore d'évaluation
- Prova Imunologia 32 2Document7 pagesProva Imunologia 32 2HASFTAGPas encore d'évaluation
- 27164Document121 pages27164Giovani AngeloPas encore d'évaluation
- A Post I La BacteriasDocument82 pagesA Post I La BacteriaspedroPas encore d'évaluation
- Apostila de Fermentados Telma PiccirilloDocument10 pagesApostila de Fermentados Telma Piccirilloero w bbs100% (1)
- Texto - Complementar - EstresseDocument34 pagesTexto - Complementar - EstresseLarissa OttoniPas encore d'évaluation
- Antivirais - q.f.2.Document97 pagesAntivirais - q.f.2.Lucas WeslleyPas encore d'évaluation
- Tratamento AlergiasDocument16 pagesTratamento Alergiaswwsom50% (2)
- Ebook Imunologia: Conceitos, Regulação e DoençasDocument45 pagesEbook Imunologia: Conceitos, Regulação e DoençasRebeca Figueredo LimaPas encore d'évaluation
- GabaritoDocument22 pagesGabaritoTais LopesPas encore d'évaluation
- Atividade-1 - Imunologia Pergunta e Resposta Gabriela VerissimoDocument5 pagesAtividade-1 - Imunologia Pergunta e Resposta Gabriela VerissimoGabriela Verissimo GabyPas encore d'évaluation
- Dermatite AtopicaDocument11 pagesDermatite AtopicaJosé Augusto CeronPas encore d'évaluation
- Ebmsp DC 2020 1Document18 pagesEbmsp DC 2020 1Bruna SabaPas encore d'évaluation
- Anais 2019 (1) 2Document132 pagesAnais 2019 (1) 2Orlando JuniorPas encore d'évaluation
- Resposta Imune Aos FungosDocument1 pageResposta Imune Aos Fungoscintiademartini9Pas encore d'évaluation
- Curso de Biomedicina Artigo de Revisão: LKLKLKDocument7 pagesCurso de Biomedicina Artigo de Revisão: LKLKLKErika SantiagoPas encore d'évaluation
- Aula Imunologia Clínica - Imunidade Às Bactérias IntracelularesDocument13 pagesAula Imunologia Clínica - Imunidade Às Bactérias IntracelularesTamires RodriguesPas encore d'évaluation
- Ix Comunicacao Cientifica em Saude e Meio Ambiente 26032018 PDFDocument438 pagesIx Comunicacao Cientifica em Saude e Meio Ambiente 26032018 PDFJozzy FerreiraPas encore d'évaluation
- Simulado QuarentenaMED - Parte 1Document13 pagesSimulado QuarentenaMED - Parte 1Marcos Junior MimosoPas encore d'évaluation
- Manual Diagnostico Laboratorial RaivaDocument108 pagesManual Diagnostico Laboratorial RaivaFrancisco Altemar DutraPas encore d'évaluation
- Cervicite FolicularDocument1 pageCervicite FolicularKetlyn OliveiraPas encore d'évaluation
- Hemograma CompletoDocument9 pagesHemograma CompletoDelcio ChambulePas encore d'évaluation
- Resumo Da Imunologia Dos TransplantesDocument5 pagesResumo Da Imunologia Dos TransplantesCristovão MarcondesPas encore d'évaluation
- Benefícios Dos Probióticos À Saúde Humana - Acadêmica Laise RochaDocument31 pagesBenefícios Dos Probióticos À Saúde Humana - Acadêmica Laise RochaTalita DezidérioPas encore d'évaluation