Académique Documents
Professionnel Documents
Culture Documents
Guia Modelos Atomicos
Transféré par
Maria Eugenia Martinez CabezasCopyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Guia Modelos Atomicos
Transféré par
Maria Eugenia Martinez CabezasDroits d'auteur :
Formats disponibles
LICEO BICENTENARIO ORIENTE DEPTO.
DE CIENCIAS
Mara Eugenia Martnez
Unidad N 1:"Modelo mecnico cuntico y enlace qumico" Gua Modelos Atmicos
..Naturaleza Elctrica de la Materia La electricidad fue por primera vez observada por Thales de Mileto en el siglo VI a.C. Frot un trozo de mbar con un pao y vio como las briznas (pastos secos, plumas, etc.) se adheran al mbar una vez frotado. El trmino electricidad deriva de la palabra griega elektrn nombre que designaba al mbar. La electricidad est presente en algunas partculas subatmicas. La partcula ms ligera que lleva carga elctrica es el electrn, que transporta una unidad de carga. ORGENES DE LA TEORA ATMICA Las primeras teoras atmicas, remontan al siglo V a.C. Cuando Leucipo y Demcrito, sugeran que el Universo (as como toda la materia) estaba formada por partculas indivisibles, a las que llamaron tomos (a: sin; tomos: divisin). Demcrito crea que estas partculas se hallaban en constante movimiento, que podan unirse entre s en combinaciones estables. Propuso que: Las diversas sustancias resultan de los diversos tamaos, formas y arreglos de estos tomos MODELO ATMICO DE DALTON
a las dos leyes fundamentales de las combinaciones qumicas, es decir: la "Ley de conservacin de la masa" elaborada por Antoine Lavoiser en 1789 (La masa total de las sustancias presentes despus de una reaccin qumica es la misma que la masa total de las sustancias antes de la reaccin) y la "Ley de composicin constante" enunciada por el qumico francs Joseph Louis Proust en 1799 (Todas las muestras de un compuesto tienen la misma composicin, es decir las mismas proporciones en masa de los elementos constituyentes.) como base de una teora atmica. En base a esto, la teora atmica de la materia de Dalton se resume en los siguientes postulados:
En 1808, de acuerdo a Leucipo y Demcrito y, en base 1. Toda la Materia est formada por tomos. 2. Los tomos son partculas indivisibles e invisibles. 3. Los tomos de un elemento son iguales entre si. (Es decir presentan igual masa e iguales propiedades) 4. Los cambios qumicos corresponden a una reordenacin, combinacin o separacin de tomos 5. Los tomos que forman los compuestos son de dos o ms clases diferentes. Los compuestos son el resultado de la combinacin o, asociacin de tomos y estas asociaciones de tomos pueden volver a separarse. Los tomos al combinarse o al volver a separarse no pierden su identidad, es decir no experimentan transformaciones.
6. Los tomos que forman los compuestos estn en una relacin de nmeros enteros y sencillos.
DESCUBRIMIENTO DE LAS CARGAS NEGATIVAS Crookes diseo un aparato llamado Tubo de Rayos Catdicos, tambin conocido como Tubo de Crookes. Es un hecho experimental: Cuando en un tubo de vidrio que contiene un gas, a baja presin y, se aplica un alto voltaje, fluye una corriente elctrica a travs de l. Asociado a este flujo elctrico, el gas encerrado en el tubo emite unos rayos de luz de colores, denominados Rayos Catdicos, que son desviados por la accin de campos elctricos y magnticos. En 1874 Stoney sugiri por primera vez la existencia de una unidad natural de electricidad a la cual llam electrn, pero no pudo demostrar la existencia de estas partculas. Luego, mediante un estudio cuidadoso de esta desviacin. Sir Joseph John Thompson demostr en 1897 que los rayos estaban formados por una corriente de partculas cargadas negativamente, que llam electrones.
Tubo de Rayos Catdicos, Thompson.
Thompson determin para el electrn, la relacin carga/masa = -1,76x10 C/g. Por otra parte Millikan determin la carga del electrn mediante su experimento de gotas -19 suspendidas en aceite. Obtuvo un valor de 1,6x10 C. Ambos trabajos permitieron determinar la masa del electrn:
Masa del Electrn
Modelo Atmico de Thompson
A partir de las observaciones realizadas por J.J. Thompson al tubo de rayos catdicos, nace una interrogante: La materia en estado normal es neutra, es decir no posee carga elctrica, pero se conocen en ella partculas cargadas negativamente Entonces como se mantiene la neutralidad de carga?... Thompson a partir de sus estudios de los rayos catdicos. Considera al tomo como una gran esfera con carga elctrica positiva, sobre la que se distribuyen los electrones, Ordenadamente y separados entre s. El principal aporte de Thompson, fue introducir la idea de que el tomo puede dividirse en partculas subatmicas PROTONES En 1886, Eugene Goldstein observ que al trabajar con un tubo de descarga de ctodo perforado, en direccin opuesta a los rayos Catdicos, se desprenda una radiacin. Estos rayos se denominaron Rayos Canales y resultaron ser partculas con carga positiva producto del choque de los rayos catdicos con los tomos de los gases residuales en el tubo. Al utilizar Hidrgeno de gas residual, se 4 logr determinar la relacin carga/masa para el protn 9,58x10 C/g, de lo cual se desprende que la 24 masa del protn es 1,67x10 g
EXPERIMENTO DE RUTHERFORD
En 1911 Ernest Rutherford y sus colaboradores Geiger y Marsden disearon un experimento que modific las ideas existentes sobre la naturaleza del tomo: Bombardearon una fina lmina de oro con partculas alfa (ncleos de helio He+2). Observ en una pantalla fluorescente, en qu medida eran dispersadas las partculas: La mayora de ellas atravesaba la lmina metlica sin cambiar de direccin, ya que los tomos no son macizos, sino principalmente vacos. Algunas partculas (las positivas), se desviaron porque pasaron por las proximidades de un ncleo cargado positivamente, situado en el centro del tomo de oro. De esto se desprende que: En el interior del tomo, las partculas positivas, estn separadas de las negativas. Y otras partculas no atraviesan la lamina (rebotaban), eran reflejadas hacia atrs con ngulos muy pequeos. Se dedujo que chocaban con algn corpsculo de mayor masa que la radiacin incidente
De sus experimentos, Rutherford, demostr que el tomo est formado por dos partes: 1. Ncleo Parte central, de tamao muy pequeo, donde se encuentra toda la carga positiva y, prcticamente, toda la masa del tomo. La carga positiva del ncleo, en su experimento es la responsable de la desviacin de las partculas alfa (tambin con carga positiva).
Posteriormente se descubri que el ncleo atmico tambin contena los neutrones. El neutrn fue descubierto experimentalmente en 1932 por Chadwick, quien, al bombardear el berilio con partculas , observ que se producan unas partculas que identific con los neutrones predichos por Rutherford.
2. Corteza Es casi un inmenso vaco, comparado con el ncleo. Aqu se encuentran los electrones con masa muy pequea y carga negativa. Como en un sistema solar, los electrones giran alrededor del ncleo. Los electrones estn ligados al ncleo por la atraccin elctrica entre cargas de signo contrario. Esto explica que la mayor parte de las partculas alfa atraviesan la lmina de oro sin desviarse. Con sus experimentos, Rutherford demostr que: los tomos no eran macizos, sino que estn vacos en su mayor parte y en su centro hay un diminuto ncleo. Ao Cientfico Modelo atmico La imagen del tomo expuesta por Durante el s.XVIII y principios del Dalton en su teora atmica, para XIX algunos cientficos haban explicar estas leyes, es la de minsculas investigado distintos aspectos de las partculas esfricas, indivisibles e reacciones qumicas, obteniendo las inmutables, llamadas leyes clsicas de la iguales entre s en qumica cada elemento qumico. Demostr que dentro de los tomos hay unas partculas diminutas, con carga elctrica negativa, a las que se llam electrones De este descubrimiento dedujo que el tomo deba de ser una esfera de materia cargada positivamente, en cuyo interior estaban incrustados los electrones. Descubrimientos experimentales
1808
John Dalton
1897
Modelo atmico de Thompson
J.J. Thomson Demostr que los tomos no eran macizos, como se crea, sino que estn vacos en su mayor parte y en su centro hay un diminuto ncleo. Dedujo que el tomo deba estar formado por una corteza con los electrones girando alrededor de un ncleo central cargado positivamente. (Modelo atmico de Rutherford) E. Rutherford Espectros atmicos discontinuos originados por la radiacin emitida por los tomos excitados de los elementos en estado gaseoso. Propuso un nuevo modelo atmico, segn el cual los electrones giran alrededor del ncleo en unos niveles bien definidos.
1911
1913
( modelo atmico de Bohr)
Niels Bohr
Resuelve las siguientes preguntas: 1. 2. 3. 4. Qu diferencias existen entre el modelo planteado por Bohr y el modelo de Thomson? Cul fue la contribucin de Dalton a la teora atmica de la materia? Cul es la importancia de Rutherford en el descubrimiento de las propiedades del tomo? Describe cules son las leyes que utiliz Dalton para postular su teora.
Vous aimerez peut-être aussi
- Guia de Descomposicion de El Agua OxigenadaDocument2 pagesGuia de Descomposicion de El Agua OxigenadaMaria Eugenia Martinez CabezasPas encore d'évaluation
- Conociendo El MicroscopioDocument26 pagesConociendo El MicroscopioMaria Eugenia Martinez CabezasPas encore d'évaluation
- Laboratorio Hidratos de CarbonoDocument3 pagesLaboratorio Hidratos de CarbonoMaria Eugenia Martinez CabezasPas encore d'évaluation
- Guia de Acle PHDocument2 pagesGuia de Acle PHMaria Eugenia Martinez CabezasPas encore d'évaluation
- Efectos Del SonidoDocument11 pagesEfectos Del SonidoMaria Eugenia Martinez Cabezas100% (1)
- Rio Ideas Previas MKDocument15 pagesRio Ideas Previas MKMaria Eugenia Martinez CabezasPas encore d'évaluation
- Guia de Aparato DigestivoDocument4 pagesGuia de Aparato DigestivoMaria Eugenia Martinez CabezasPas encore d'évaluation
- Estructura Atomica Del AtomoDocument32 pagesEstructura Atomica Del Atomomauricio duranPas encore d'évaluation
- Manual Practico Protección RadiológicaDocument65 pagesManual Practico Protección Radiológica7alejandro7Pas encore d'évaluation
- Ejercicios ATOMO y MATERIA (Test y Desarrollo) - 3FyQDocument9 pagesEjercicios ATOMO y MATERIA (Test y Desarrollo) - 3FyQRodolfo PozoPas encore d'évaluation
- Resumen - Estructura Del ÁtomoDocument5 pagesResumen - Estructura Del ÁtomoAntony Yupanqui TorpocoPas encore d'évaluation
- Modulo - Galois - 1 - 2Document15 pagesModulo - Galois - 1 - 2César Hilton Aguilar RamosPas encore d'évaluation
- 01 Estructura Atomica 2020 IfddcDocument51 pages01 Estructura Atomica 2020 IfddcAlberto Moreno GarrigaPas encore d'évaluation
- 01 Simulacro Ciencias - 02 - 09Document6 pages01 Simulacro Ciencias - 02 - 09oscar sebastian vela reateguiPas encore d'évaluation
- Guia 02 y 03 Atomos, Moleculas e Iones. Nomenclatura Inorganica QUI080Document13 pagesGuia 02 y 03 Atomos, Moleculas e Iones. Nomenclatura Inorganica QUI080Alan John Andrades100% (2)
- Quimica 3°año IDocument43 pagesQuimica 3°año IOscar Rodríguez Gómez100% (1)
- Elementos Químicos Ordenados Por Su Número AtómicoDocument12 pagesElementos Químicos Ordenados Por Su Número AtómicoRichard RojasPas encore d'évaluation
- Practica Numero Cuantico DannyDocument7 pagesPractica Numero Cuantico DannyDanny Alain Mullisaca Perez0% (1)
- BiocelularDocument4 pagesBiocelularMercedes Narvaez ArguellesPas encore d'évaluation
- ChemistryLab Journal SPADocument12 pagesChemistryLab Journal SPAcgg88% (24)
- Notas de FISICOQUÍMICA 2003 Jimenez Vargas MacarullaDocument71 pagesNotas de FISICOQUÍMICA 2003 Jimenez Vargas MacarullaALeejaandra Ordaaz0% (1)
- Problemario 1-ResueltoDocument6 pagesProblemario 1-ResueltoJonathan Alejandro100% (1)
- ÁTOMOS Y MOLÉCULAS Composicion de Porcentaje Por Peso (Consulta de Quimica)Document15 pagesÁTOMOS Y MOLÉCULAS Composicion de Porcentaje Por Peso (Consulta de Quimica)Paul VillacresesPas encore d'évaluation
- Cuadernillo Nro 2 Química Fat 2023Document24 pagesCuadernillo Nro 2 Química Fat 2023Ximena MaierPas encore d'évaluation
- Evaluación de QuímicaDocument2 pagesEvaluación de QuímicabeamPas encore d'évaluation
- Taller #3 Masa Atómica y Masa MolecularDocument7 pagesTaller #3 Masa Atómica y Masa MolecularJosé MorenoPas encore d'évaluation
- 620 Preguntas Resueltas de Quimica 01Document98 pages620 Preguntas Resueltas de Quimica 01Luis AdrianPas encore d'évaluation
- Geomorfología Estructual PDFDocument67 pagesGeomorfología Estructual PDFAntonio LópezPas encore d'évaluation
- El Cuento en VenezuelaDocument21 pagesEl Cuento en VenezuelaYsmar Laisney Lucena PerdomoPas encore d'évaluation
- 1ero Bgu Texto QuimicaDocument17 pages1ero Bgu Texto Quimicajedaymc27Pas encore d'évaluation
- MAYO - QUIMICA - 3ROjbDocument26 pagesMAYO - QUIMICA - 3ROjbLuis A Villanueva VPas encore d'évaluation
- Ejercicios Unidad 2Document3 pagesEjercicios Unidad 2gatito021205Pas encore d'évaluation
- Evaluación Formativa 1º MediosDocument3 pagesEvaluación Formativa 1º MediosPatricio Andres Figueroa SalinasPas encore d'évaluation
- Unidad 1 - Fase 2 - Fuentes de RadiaciónDocument21 pagesUnidad 1 - Fase 2 - Fuentes de RadiaciónEsneider Ramirez FrancoPas encore d'évaluation
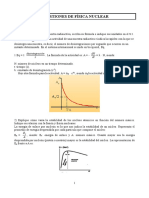
- F2Bto. 7. Cuestiones Resueltas. Fisica NuclearDocument14 pagesF2Bto. 7. Cuestiones Resueltas. Fisica Nuclearfermin100% (1)
- EjerciciosDocument2 pagesEjerciciosPabloPas encore d'évaluation
- Practica de ElectricidadDocument7 pagesPractica de ElectricidadAldo FacundoPas encore d'évaluation