Académique Documents
Professionnel Documents
Culture Documents
Practica 4 Equilibrio!!!
Transféré par
Iván Esquer0 évaluation0% ont trouvé ce document utile (0 vote)
50 vues7 pagesEste documento describe un experimento de laboratorio para estudiar el efecto de la concentración en el equilibrio químico de la reacción entre los iones Fe3+ y SCN- formando el ión complejo FeSCN2+. Se midió la absorbancia de varias soluciones con diferentes concentraciones iniciales de Fe3+ manteniendo fija la concentración de SCN-. Los cálculos realizados no demostraron que la constante de equilibrio es independiente de la concentración inicial como era el objetivo, ya que las constantes calculadas aumentaron a medida que las dis
Description originale:
Copyright
© © All Rights Reserved
Formats disponibles
DOCX, PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentEste documento describe un experimento de laboratorio para estudiar el efecto de la concentración en el equilibrio químico de la reacción entre los iones Fe3+ y SCN- formando el ión complejo FeSCN2+. Se midió la absorbancia de varias soluciones con diferentes concentraciones iniciales de Fe3+ manteniendo fija la concentración de SCN-. Los cálculos realizados no demostraron que la constante de equilibrio es independiente de la concentración inicial como era el objetivo, ya que las constantes calculadas aumentaron a medida que las dis
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme DOCX, PDF, TXT ou lisez en ligne sur Scribd
0 évaluation0% ont trouvé ce document utile (0 vote)
50 vues7 pagesPractica 4 Equilibrio!!!
Transféré par
Iván EsquerEste documento describe un experimento de laboratorio para estudiar el efecto de la concentración en el equilibrio químico de la reacción entre los iones Fe3+ y SCN- formando el ión complejo FeSCN2+. Se midió la absorbancia de varias soluciones con diferentes concentraciones iniciales de Fe3+ manteniendo fija la concentración de SCN-. Los cálculos realizados no demostraron que la constante de equilibrio es independiente de la concentración inicial como era el objetivo, ya que las constantes calculadas aumentaron a medida que las dis
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme DOCX, PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 7
UNIVERSIDAD DE SONORA
Depto. De Ciencias Qumico Biolgicas
Laboratorio de Equilibrio Qumico
Practica #2
Estudio del equilibrio en una reaccin homognea y clculo de la
constante
Integrantes:
Andrea Moreno Roldan
Karla Guadalupe Serna del Real
Andrs Gerardo Evans Villegas
Hermosillo, Sonora 3 de octubre del 2013
EFECTO DE LA CONCENTRACIN EN LA CONSTANTE DE
EQUILIBRO DE UNA REACCIN COLORIDA
Objetivo
Evaluar el efecto de la concentracin en una reaccin, mediante la
deteccin espectrofotomtrica de un compuesto formador de color para
demostrar que la constante de equilibrio es independiente de la
concentracin inicial.
Introduccin
La influencia de variaciones en la concentracin sobre un sistema en
equilibrio est regida por la ley de accin de masas: La velocidad de
una reaccin qumica es proporcional al producto de las concentraciones
molares de las sustancias reaccionantes.
El aumento de la concentracin de una sustancia presente en el
equilibrio hace que el mismo se traslada en el sentido de consumir la
sustancia adicionada, esto es, el equilibrio se traslada para el lado
contrario al aumento. Ya la disminucin de una sustancia retirada, esto
es, el equilibrio se traslada para el mismo lado de la disminucin.
Si en una reaccin N
2
+ 3H
2
2 NH
3
aumenta la concentracin del
N
2
, el equilibrio se desplaza hacia la derecha para favorecer los
productos. Lo mismo ocurre si se incrementa la concentracin de H
2
.
Despus de cierto tiempo se alcanza un nuevo estado de equilibrio de
acuerdo a las nuevas concentraciones.
En esta prctica se estudiar el equilibrio existente entre los iones Fe
+3
y
SCN
-1
, con el in complejo FeSCN
+2
, de acuerdo a la siguiente reaccin:
Fe
+3
+ SCN
-1
FeSCN
+2
Dado que el in FeSCN
+2
es de color rojo, su concentracin puede
determinarse en un espectrofotmetro, en donde la intensidad del color
(que es directamente proporcional a la concentracin de la sustancia
colorida), se calcular en funcin de la absorbancia.
A= K [FeSCN
+2
]
Materiales:
6 tubos de ensaye de 16 x 150 mm
1 gradilla para tubos de ensaye
5 celdas para espectrofotmetro
6 pipetas volumtricas de 5 mL
Reactivos:
Solucin de SCN
-1
4x10
-4
M.
5 soluciones de Fe(NO3)3 : 0.2M , 0.04 M, 0.02M, 0.01M y 0.05M.
Equipo: 1 espectrofotmetro.
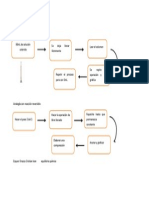
Procedimiento:
1. Enumere 5 tubos de ensaye limpios y secos. Adicione a cada tubo
5 mL de NaSCN 4x10
-4
M.
2. Agregar al tubo 1, 5 mL de Fe(NO3)3 0.2M.
3. A los tubos del 2 al 5 agregar las siguientes cantidades:
Tubo Fe(NO3)3 a
adicionar
Fe
+3
inicial(a)
2 0.04 M 0.02
3 0.02 M 0.01
4 0.01 M 0.005
5 0.005 M 0.0025
4. Leer la absorbancia de cada tubo a 340 nm.
Con el valor de la absorbancia del tubo 1 y la concentracin
de FeSCN
+2
, calcular la constante con la siguiente frmula:
A= K [FeSCN
+2
].
Con el valor de K y la absorbancia de los tubos de 2 al 5
determinar la concentracin de FeSCN
+2
en cada reaccin.
5. Con [FeSCN
+2
] determinar [Fe
+3
]y [SCN
-1
] en el equilibrio y la
constante de equilibrio para cada reaccin.
Resultados
Registro de datos:
Tubo Absorbancia
1 2.258
2 0.764
3 0.523
4 0.420
5 0.357
Con el valor de la absorbancia del tubo 1 y la concentracin de
FeSCN
+2.
A= K [FeSCN
+2
].
A/[FeSCN
+2
]=K
2.258/ 2x10
-4
M
= 11 290 M
-1
K=11 290 M
-1
Con el valor de K y la absorbancia de los tubos de 2 al 5
determinar la concentracin de FeSCN
+2
en cada reaccin
A/K =[FeSCN
+2
].
Tubo 2: 0.764/11 290 M
-1
= 6.7670 x10
-5
M
Tubo 3: 0.523/11 290 M
-1
= 4.6324 x10
-5
M
Tubo 4: 0.420/11 290 M
-1
= 3.7201 x10
-5
M
Tubo 5: 0.357/11 290 M
-1
= 3.1620 x10
-5
M
Con [FeSCN
+2
] determinar [Fe
+3
] y [SCN
-1
] en el equilibrio y la
constante de equilibrio para cada reaccin. De acuerdo con:
[Fe
+3
] + [SCN
-1
] [FeSCN
+2
]
Inicio aM 2x10
-4
M
0
Equilibrio a-x (2x10
-4
M- x) xM
Sustituyendo en K= [FeSCN
+2
] / [Fe
+3
][SCN
-1
]
Tubo 2
K= [FeSCN
+2
] / [Fe
+3
][SCN
-1
]
K= xM / (a-x ) (2x10
-4
M- x)
K= xM / (a-x ) (2x10
-4
M- x)
K= 6.7670 x10
-5
M / 0.02 M -6.7670 x10
-5
M)( 2x10
-4
M-6.7670 x10
-5
M)
K= 25.6554
Tubo 3
K= [FeSCN
+2
] / [Fe
+3
][SCN
-1
]
K= xM / (a-x ) (2x10
-4
M- x)
K= xM / (a-x ) (2x10
-4
M- x)
K= 4.6324 x10
-5
M /(0.01 M -4.6324 x10
-5
M)( 2x10
-4
M-4.6324 x10
-5
M)
K= 30.2842
Tubo 4
K= [FeSCN
+2
] / [Fe
+3
][SCN
-1
]
K= xM / (a-x ) (2x10
-4
M- x)
K= xM / (a-x ) (2x10
-4
M- x)
K=3.7201x10
-5
M/(0.005 M - 3.7201 x10
-5
M)( 2x10
-4
M-3.7201 x10
-5
M)
K= 46.0443
Tubo 5
K= [FeSCN
+2
] / [Fe
+3
][SCN
-1
]
K= xM / (a-x ) (2x10
-4
M- x)
K= xM / (a-x ) (2x10
-4
M- x)
K=3.1620x10
-5
M/(0.0025 M-3.1620 x10
-5
M)( 2x10
-4
M-3.1620 x10
-5
M )
K= 76.0780
Cuestionario
1. Escriba en enunciado de la ley de Lamber & Beer:
La Ley Lambert Beer es un medio matemtico de expresar cmo la
materia absorbe la luz. Esta relacin puede ser expresada como:
A = dc
Donde
A = Absorbencia
= Coeficiente molar de extincin
d = Distancia en cm
c = Concentracin molar
2. Qu es la absorbancia de una solucin?
En espectrofotometra, la absorbancia ( ) es definida como:
, donde:
= es la intensidad de la luz con una longitud de onda especfica y
que es pasada por una muestra (intensidad de la luz transmitida)
= es la intensidad de la luz antes de que entre a la muestra
(intensidad de la luz incidente)
3. Cmo explica el efecto de un cambio de concentracin en
una reaccin que se encuentra en equilibrio? (por ejemplo:
Qu pasa si aade ms de alguno de los reactivos?
El aumento de la concentracin de una sustancia presente en el
equilibrio hace que el mismo se traslada en el sentido de consumir la
sustancia adicionada, esto es, el equilibrio se traslada para el lado
contrario al aumento.
Observaciones
Se observ en la prctica que, al medir las absorbancias de las
disoluciones preparadas, el resultado de emisin aumentaba segn la
concentracin que presentaba. Dando as, la ms concentrada la mayor
emisin. Adems, de el cambio de color en soluciones disminuyendo de
la ms concentrada a la menos concentrada.
Conclusiones
No se logr con el objetivo de demostrar que la constante de
equilibrio es independiente de la concentracin inicial, ya que al realizar
los clculos correspondientes segn el mtodo utilizado, las constantes
van en aumento segn las disoluciones estn ms diluidas.
Bibliografas:
Manuel de prcticas Parte II, Equilibrio Qumico. Laboratorio de
Fisicoqumica. Autores: Moreno Salazar Sergio et al.
http://www.optek.com/es/Lambert_Beer_Law.asp
http://es.wikipedia.org/wiki/Absorbancia
Vous aimerez peut-être aussi
- Lab III Equilibrio QuímicoDocument12 pagesLab III Equilibrio QuímicoSofía Flores SantilliPas encore d'évaluation
- Cinetica - No.3Document11 pagesCinetica - No.3Isabel RinconPas encore d'évaluation
- Guia 3Document11 pagesGuia 3SharaPas encore d'évaluation
- Equilibrio Químico y Constante KeqDocument12 pagesEquilibrio Químico y Constante KeqCésar JiménezPas encore d'évaluation
- Equilibrio Quimico y CineticaDocument16 pagesEquilibrio Quimico y CineticaYAMILEX DURAN SALAZARPas encore d'évaluation
- Calibracion Del ColorimetroDocument5 pagesCalibracion Del ColorimetroMarlon Riascos VallejoPas encore d'évaluation
- Informe de Equilibrio Quimico 1Document8 pagesInforme de Equilibrio Quimico 1ana maria gonzalez moralesPas encore d'évaluation
- Informe Química IIDocument5 pagesInforme Química IIbenjaminPas encore d'évaluation
- Quimica 2Document8 pagesQuimica 2Manuel DGcPas encore d'évaluation
- Practicas de Laboratorio de Termoquimica 2Document24 pagesPracticas de Laboratorio de Termoquimica 2acte9050% (2)
- Equilibrio Quimico IonicoDocument15 pagesEquilibrio Quimico IonicoNUMBASD100% (2)
- Informe de Lab. de Química Nro. 7-EncisoDocument11 pagesInforme de Lab. de Química Nro. 7-EncisoJosePas encore d'évaluation
- Informe de Laboratorio 2Document10 pagesInforme de Laboratorio 2mariaPas encore d'évaluation
- Equilibrio Quimico Lab Ciencias Proyecto 1Document9 pagesEquilibrio Quimico Lab Ciencias Proyecto 1Magda CervantesPas encore d'évaluation
- Reporte de Fisicoquimica AbsorbanciaDocument11 pagesReporte de Fisicoquimica AbsorbanciakarensitogordisPas encore d'évaluation
- Equilibrio QuimicoDocument9 pagesEquilibrio QuimicoLyann Yesenia Gorena VacaPas encore d'évaluation
- Guía de Laboratorio Práctico 2019Document45 pagesGuía de Laboratorio Práctico 2019Axel EguizabalPas encore d'évaluation
- Informe N° 3 Equilibrio QuimicoDocument11 pagesInforme N° 3 Equilibrio Quimicoiaraneda30Pas encore d'évaluation
- Le Chatelier MPRMRDocument16 pagesLe Chatelier MPRMRVivi Mar CSiPas encore d'évaluation
- Practica 8 Quimica 2Document9 pagesPractica 8 Quimica 2Gabriel Ricardo Gutierrez VivancoPas encore d'évaluation
- Equipo 2 Practica2 TEQ 2IV45Document16 pagesEquipo 2 Practica2 TEQ 2IV45Monroy Sotomayor Alberto ArturoPas encore d'évaluation
- Estequiometría experimental en el IPNDocument17 pagesEstequiometría experimental en el IPNVale ChavezPas encore d'évaluation
- INFORME DE LABORATORIO DE FISICOQUIMICA Practica 5..Document13 pagesINFORME DE LABORATORIO DE FISICOQUIMICA Practica 5..miguelPas encore d'évaluation
- Espectrofometria PDFDocument6 pagesEspectrofometria PDFaurora_9152Pas encore d'évaluation
- Determinación de la constante de equilibrio KcDocument4 pagesDeterminación de la constante de equilibrio KcDanilo Arias RojasPas encore d'évaluation
- Trabajo Práctico #09, Equilibrio QuímicoDocument8 pagesTrabajo Práctico #09, Equilibrio QuímicoMauro GardinettiPas encore d'évaluation
- Determinación Kc Fe(SCN)+2 espectrofotometríaDocument7 pagesDeterminación Kc Fe(SCN)+2 espectrofotometríaEugenia GuilliodPas encore d'évaluation
- Informe 03 de Analisis InstrumentalDocument13 pagesInforme 03 de Analisis InstrumentalAnabel Victoria Mallqui BerrocalPas encore d'évaluation
- Práctica Fisicoquímica (Constante de Equilibrio)Document6 pagesPráctica Fisicoquímica (Constante de Equilibrio)yazsancer10Pas encore d'évaluation
- RP Labfqii 02Document6 pagesRP Labfqii 02Abraham Joel Mendoza FloresPas encore d'évaluation
- Informe 4 Analítica IIIDocument9 pagesInforme 4 Analítica IIIJACKELINE SALGADO PALACIOPas encore d'évaluation
- Práctica #3: Equilibrio Químico: Cálculo de La Constante, K: IntroducciónDocument11 pagesPráctica #3: Equilibrio Químico: Cálculo de La Constante, K: IntroducciónLuis Mario HernandezPas encore d'évaluation
- 2008-TP-04-Determinacion Espectrofotometrica de PkaDocument4 pages2008-TP-04-Determinacion Espectrofotometrica de PkaPedro Pablo BossioPas encore d'évaluation
- RP Labfqii 02Document6 pagesRP Labfqii 02Subaro SanchezPas encore d'évaluation
- CCQ G1 E1 PrácticaDocument10 pagesCCQ G1 E1 PrácticaCamilo PerezPas encore d'évaluation
- Guia de Laboratorio #8Document8 pagesGuia de Laboratorio #8PabloPas encore d'évaluation
- Informe #2-Oxidación del Yoduro con PersulfatoDocument16 pagesInforme #2-Oxidación del Yoduro con PersulfatoJuniorRomeroPas encore d'évaluation
- Práctica2 Equilibrio Químico IónicoDocument17 pagesPráctica2 Equilibrio Químico IónicoJavier Rodriguez50% (2)
- Informe de Laboratorio N 3 Equilibrio Quimico PDFDocument24 pagesInforme de Laboratorio N 3 Equilibrio Quimico PDFValdez LuisPas encore d'évaluation
- Laboratorio Número 7Document16 pagesLaboratorio Número 7YOSVIN KEVIN GONZALES ANTICONAPas encore d'évaluation
- Antología de QuímicaDocument63 pagesAntología de QuímicaArturo ChavezPas encore d'évaluation
- Reporte 8 .-Valoración EspectrofotométricaDocument13 pagesReporte 8 .-Valoración EspectrofotométricaJorge Adrian Pérez TrejoPas encore d'évaluation
- Equilibrio Quimico INFORMEDocument5 pagesEquilibrio Quimico INFORMEMaryorisPas encore d'évaluation
- Taller5 Equilibrio Químico 2019Document7 pagesTaller5 Equilibrio Químico 2019Vale PinedaPas encore d'évaluation
- Informe FinalDocument15 pagesInforme FinalAnonymous 1biQkQ7EV3Pas encore d'évaluation
- Obtención de sulfato de cobreDocument8 pagesObtención de sulfato de cobreCitlally Ortiz100% (1)
- Equilibrio QuimicoDocument11 pagesEquilibrio QuimicoDUANE MADELEINE MONTERO MENDEZPas encore d'évaluation
- Laboratorio EquilibrioDocument9 pagesLaboratorio EquilibrioLuis Angel Trujillo MendozaPas encore d'évaluation
- Informe Le-Chatelier PDFDocument8 pagesInforme Le-Chatelier PDFCindy Paola GarciaPas encore d'évaluation
- Reporte de PrácticaDocument5 pagesReporte de PrácticaSANTIAGO ROMERO GARCIAPas encore d'évaluation
- Universidad Nacional de San Cristóbal de HuamangaDocument7 pagesUniversidad Nacional de San Cristóbal de HuamangaRONALDIÑOPas encore d'évaluation
- Informe#4 Espectrofotometría Uv-VisDocument7 pagesInforme#4 Espectrofotometría Uv-VisJULIAN ALEJANDRO ARAUJO TUTALCHAPas encore d'évaluation
- Cinética Química IiDocument13 pagesCinética Química IiJoel Yupanqui CastroPas encore d'évaluation
- Informe de MezclasDocument15 pagesInforme de MezclasAndrés SuárezPas encore d'évaluation
- ANÁLISIS1Document235 pagesANÁLISIS1Elizabeth EscalantePas encore d'évaluation
- Informe 1 Laboratorio PPQDocument11 pagesInforme 1 Laboratorio PPQConstanzaPérezMoralesPas encore d'évaluation
- Universidad de SonoraDocument2 pagesUniversidad de SonoraIván EsquerPas encore d'évaluation
- Control de InfeccionesDocument5 pagesControl de InfeccionesIván EsquerPas encore d'évaluation
- InmunoC - Práctica1Document1 pageInmunoC - Práctica1Iván EsquerPas encore d'évaluation
- Diagrama EqulibrioDocument1 pageDiagrama EqulibrioIván EsquerPas encore d'évaluation
- Control de InfeccionesDocument5 pagesControl de InfeccionesIván EsquerPas encore d'évaluation
- Far MacoDocument4 pagesFar MacoIván EsquerPas encore d'évaluation
- ColesterolDocument2 pagesColesterolIván EsquerPas encore d'évaluation
- Intro Ducci OnDocument1 pageIntro Ducci OnIván EsquerPas encore d'évaluation
- Diagrama de FlujoDocument1 pageDiagrama de FlujoIván EsquerPas encore d'évaluation
- Diagrama de FlujoDocument1 pageDiagrama de FlujoIván EsquerPas encore d'évaluation
- Plímeros Exposicion OrganicaDocument12 pagesPlímeros Exposicion OrganicaIván EsquerPas encore d'évaluation
- Formato OR 2011Document6 pagesFormato OR 2011dj danielilloPas encore d'évaluation
- Lineamiento de Construcción de Santa Cruz de La SierraDocument10 pagesLineamiento de Construcción de Santa Cruz de La SierraHugo Angel Gomez Callejas100% (1)
- Tercera Práctica Calificada: Pregunta (20 Puntos) : Agregar Las Opciones Al ProgramaDocument6 pagesTercera Práctica Calificada: Pregunta (20 Puntos) : Agregar Las Opciones Al ProgramaCristhian David ContrerasPas encore d'évaluation
- SECADO DE SEMILLAS DE GIRASOL: EVALUACIÓN DE TEMPERATURA Y TIEMPODocument12 pagesSECADO DE SEMILLAS DE GIRASOL: EVALUACIÓN DE TEMPERATURA Y TIEMPODAHANA CAROLINA VARGAS AGROTAPas encore d'évaluation
- Informe N°03Document33 pagesInforme N°03brayan garciaPas encore d'évaluation
- Actividad de ANALISIS ANOVA Y RLSDocument3 pagesActividad de ANALISIS ANOVA Y RLSJosé Ramos EscorciaPas encore d'évaluation
- T1 Sistemas de Ecuaciones 2x2 MAT 3 ALG LINEAL 15082021Document2 pagesT1 Sistemas de Ecuaciones 2x2 MAT 3 ALG LINEAL 15082021CARLOS CABEZASPas encore d'évaluation
- Actividad 2Document3 pagesActividad 2alexander muñozPas encore d'évaluation
- Unidad VI. SolucionesDocument9 pagesUnidad VI. SolucionesJulio César Matute CorderoPas encore d'évaluation
- FT Ficha Tecnica 385 410 WattsDocument1 pageFT Ficha Tecnica 385 410 WattsFrancescoPas encore d'évaluation
- El Micrometro y El VernierDocument13 pagesEl Micrometro y El VernierAbundis Martinez Ismael 1FPas encore d'évaluation
- Taller de QuimicaDocument5 pagesTaller de Quimicaml_sanchezcruz787533% (24)
- Acumulativo - 10 - Periodo IDocument2 pagesAcumulativo - 10 - Periodo ISANDRA MILENA RIOS MALDONADOPas encore d'évaluation
- Prueba Piloto 2 Estadistica IIDocument1 pagePrueba Piloto 2 Estadistica IIHenry CamposPas encore d'évaluation
- Enteros CombinadosDocument57 pagesEnteros Combinadossandra100% (1)
- Lubricación de ChumacerasDocument35 pagesLubricación de ChumacerasRamón RocaPas encore d'évaluation
- Reologia Aplicada A Procesos de Fundición y Propiedades Del Metal LíquidoDocument9 pagesReologia Aplicada A Procesos de Fundición y Propiedades Del Metal LíquidoIsmael Saidi Naranjo100% (1)
- Guía 1 ElectrostáticaDocument9 pagesGuía 1 ElectrostáticaJavier AlvarezPas encore d'évaluation
- Métodos de Separación de MezclasDocument16 pagesMétodos de Separación de Mezclasjuan carlos lazoPas encore d'évaluation
- Trabajo Practico MiguelDocument3 pagesTrabajo Practico MiguelMiguel OrtizPas encore d'évaluation
- P.sugarpress BR 1000.c.membreteDocument2 pagesP.sugarpress BR 1000.c.membreteRED DRAGOPas encore d'évaluation
- Plano de RiesgosDocument1 pagePlano de RiesgosElias Han Cuba CorzoPas encore d'évaluation
- Impresoras DeskjetDocument3 pagesImpresoras DeskjetemesticaPas encore d'évaluation
- Practica FisicoquimciaDocument6 pagesPractica FisicoquimciaDAYANA MICHELL SANTANA PINTOPas encore d'évaluation
- Actividad Semanal Del Curso Resitencia de MaterialesDocument24 pagesActividad Semanal Del Curso Resitencia de MaterialesHECTOR ALBERTO PASCO GARFIASPas encore d'évaluation
- GuiadeEjercicioyProblemas Sistemas 2007 PDFDocument41 pagesGuiadeEjercicioyProblemas Sistemas 2007 PDFOsbel Elver Campos SandovalPas encore d'évaluation
- Ventiladores centrífugos robustos CMRDocument5 pagesVentiladores centrífugos robustos CMRWilfredo Salas MarcosPas encore d'évaluation
- Termodinámica QuímicaDocument7 pagesTermodinámica QuímicaJimmyRiveraPas encore d'évaluation
- RM BECA 18 Miscelánea 5Document8 pagesRM BECA 18 Miscelánea 5Diluc quetiPas encore d'évaluation