Académique Documents
Professionnel Documents
Culture Documents
Biodisponibilidad y Su Proceso Farmacológico
Transféré par
Cathy Díaz Pérez0 évaluation0% ont trouvé ce document utile (0 vote)
83 vues6 pagesCopyright
© © All Rights Reserved
Formats disponibles
DOCX, PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme DOCX, PDF, TXT ou lisez en ligne sur Scribd
0 évaluation0% ont trouvé ce document utile (0 vote)
83 vues6 pagesBiodisponibilidad y Su Proceso Farmacológico
Transféré par
Cathy Díaz PérezDroits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme DOCX, PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 6
BIODISPONIBILIDAD Y SU PROCESO FARMACOLGICO
La Biodisponibilidad de un medicamento es un concepto que ha ido cobrando
importancia en las ltimas dcadas tras haberse demostrado en innumerables
trabajos que formas farmacuticas slidas de administracin oral (tabletas,
cpsulas, entre otras) si bien eran equivalentes desde el punto de vista de
cantidad del frmaco, no lo eran desde el punto de vista fisiolgico.
La biodisponibilidad se define como la cantidad y la velocidad a la que el principio
activo se absorbe a partir de una forma farmacutica y llega al lugar de accin
(biofase). Teniendo en cuenta que el principio activo se encuentra en equilibrio
entre el sitio de accin y la circulacin general, se asume que los parmetros del
medicamento medidos en sangre son representativos de la biodisponibilidad del
mismo.
Por ejemplo, cuando se administra un medicamento por va oral, antes de llegar a
la circulacin sangunea y por ende al sitio de accin, el ingrediente activo
presente en el preparado farmacutico debe franquear diversas barreras,
pudiendo presentar perdidas de la dosis original en cada una de ellas. Las
cuales se mencionan a continuacin:
1. Estmago
2. Mucosa intestinal
3. Hgado
4. Corazn
5. Pulmones
Pueden existir diferencias significativas entre medicamentos con diferentes
ingredientes activos, esta diferencia depende directamente de las propiedades
inherentes al frmaco como la facilidad de solubilizarse en los fluidos biolgicos ya
sea de carcter acuoso o lpidico, as como la forma en la que el organismo la
asimila; es decir como la absorbe, la distribuye, metaboliza y elimina del
organismo. El siguiente esquema representa el proceso de absorcin de 2
diferentes frmacos, los cuales se administran a la misma dosis (100 mg), pero
durante su trayecto a la circulacin general se van retirando del organismo
cantidades diferentes del frmaco en cada uno de los rganos, aprecindose que
al final el frmaco A cuenta con una biodisponibilidad del 72% mientras que el
frmaco B tiene una biodisponibilidad del 16%.
Por ello, se acepta como definicin operativa que la biodisponibilidad es la
propiedad de una forma farmacutica que determina cunto y cmo llega el
frmaco contenida en ella hasta la circulacin sistmica. La biodisponibilidad de un
medicamento se determina caracterizando su perfil farmacocintico, para ello se
administra el medicamento en evaluacin y posteriormente se toman muestras
sanguneas a diferentes tiempos, estas muestras sanguneas se someten a un
tratamiento para determinar las concentraciones. Con estos resultados se
construye la grfica de concentracin respecto al tiempo, aprecindose un
comportamiento similar a la siguiente figura. A partir de ella se determinan los 3
parmetros representativos de la Biodisponibilidad:
a) La concentracin mxima obtenida (Cmax).
Como su nombre lo indica, representa la concentracin ms alta del frmaco en la
sangre o en plasma despus de su administracin oral. Este parmetro es
directamente proporcional a la fraccin del frmaco absorbido.
b) El tiempo al cual se aprecia la concentracin mxima (Tmax).
Junto con el Cmax, este parmetro est estrechamente relacionado con la
velocidad de absorcin. Frmacos con valores de Tmax ms pequeo presentarn
respuesta farmacolgica en tiempo ms cortos.
c) El rea bajo la curva de la concentracin plasmtica respecto al tiempo (ABC).
Este parmetro representa la cantidad de frmaco absorbido. El ABC es
directamente proporcional a la cantidad de frmaco que ingresa a la circulacin y
es independiente de la velocidad de absorcin.
BIOEQUIVALENCIA Y SU PROCESO FARMACOLGICO
En el campo de los medicamentos genricos, es fundamental tener en cuenta el
concepto de bioequivalencia. La bioequivalencia es la cualidad que demuestra que
un medicamento genrico y uno de marca con el mismo principio activo son
equivalentes e intercambiables desde el punto de vista de la calidad, la seguridad
y la eficacia.
Para demostrar la bioequivalencia de los medicamentos genricos se realizan
exhaustivos y rigurosos estudios. Cuando dos medicamentos son equivalentes en
la velocidad y cantidad del frmaco activo que se absorbe y llega al tejido o rea
donde se produce su efecto, los dos frmacos son teraputicamente equivalentes
y pueden usarse indistintamente. As se demuestra la bioequivalencia de un
medicamento genrico, que cuenta con las mismas garantas de calidad,
seguridad y eficacia que su correspondiente frmaco de marca.
Existe un falso mito segn el cual hay una diferencia del 20% en la concentracin
o principio activo del frmaco genrico respecto del original. Este 20% no se
refiere a una variabilidad en la eficacia del medicamento, ni tampoco al contenido
real de principio activo, sino a la variabilidad en la absorcin del frmaco. Este
20% de variabilidad en la absorcin se da de igual modo en los medicamentos
genricos y en los de marca. La realidad es que la biodisponibilidad (tiempo que
tarda una cantidad de un principio activo en alcanzar su diana teraputica) de
cualquier principio activo vara entre los diferentes individuos e incluso entre los
diferentes lotes de un medicamento, incluidos los de marca.
En una reciente declaracin de la Agencia Espaola del Medicamento, la
institucin encargada de la aprobacin y la supervisin de todos los
medicamentos, se afirmaba que genricos e innovadores no difieren en cuanto a
las garantas de calidad que tienen que elevar a los organismos reguladores.
Qu frmacos requieren estudios de bioequivalencia?
La variabilidad de hasta un 20% entre genricos y marca de referencia carece de
relevancia clnico-teraputica para medicamentos cuyos principios activos poseen
una amplia ventana teraputica, por ejemplo, muchos antibiticos, anticidos,
algunos antihistamnicos H1, vitaminas y algunos analgsicos. Las dosis de estos
frmacos suelen ser elevadas, por lo que las posibles diferencias de absorcin
enteral no es esperable que ocasionen cambios relevantes en su eficacia
teraputica o txica. Sin embargo, en el caso de otros frmacos que poseen un
margen teraputico reducido, o que sufren un metabolismo presistmico
importante, o que necesitan un ajuste de dosis frecuente, la demostracin rigurosa
de que existe bioequivalencia entre el preparado de referencia y el genrico
reviste la mxima importancia clnica. Tal ocurre con algunos frmacos de las
reas cardiovascular, de los sistemas nervioso y endocrino, y tambin con algunos
bronco-dilatadores, diurticos y anticoagulantes orales
Cuando existen dificultades para medir las concentraciones en sagre u orina de un
frmaco, o cuando la concentracin srica no es un buen indicador de eficacia,
como ocurre con las formulaciones tpicas, se requieren estudios
farmacodinmicos en voluntarios sanos o en pacientes, a fin de establecer la
bioequivalencia de dos formulaciones farmacuticas. Los frmacos que se
administran ya disueltos, o los que se administran por va parenteral (excepto las
formas intramusculares depot) no requieren, en general, estudios de
bioequivalencia.
Se dice quedos medicamentos son bioequivalentes si presentan:
La misma cantidad de principio activo
La misma forma de dosificacin
La misma biodisponibilidad tras la administracin de las mismas dosis en id
nticas condiciones.
Los efectos farmacolgicos de ambos medicamentos sern iguales.
TRABAJO DE FARMACOLOGA
PRESENTADO POR:
DEISY CORREA
MAYERLY MURILLO
MARELIS
ACADEMIA FREDERICK FLORET
MONTERIA
2014
Vous aimerez peut-être aussi
- Wa0002.Document13 pagesWa0002.egonzalezPas encore d'évaluation
- Biodisponibilidad y BioequivalenciaDocument8 pagesBiodisponibilidad y BioequivalenciaWesResPas encore d'évaluation
- BIOQUIVALENCIADocument10 pagesBIOQUIVALENCIAIsabel CristinaPas encore d'évaluation
- BIOEQUIVALENCIADocument7 pagesBIOEQUIVALENCIAWesResPas encore d'évaluation
- BiodisponibilidadDocument7 pagesBiodisponibilidadKarina StradinoffPas encore d'évaluation
- Biodisponibilidad y Bioequivalencia-Exposicion - Biofarmacia.Document37 pagesBiodisponibilidad y Bioequivalencia-Exposicion - Biofarmacia.leisyPas encore d'évaluation
- Tema 7 BiodisponibilidadDocument17 pagesTema 7 BiodisponibilidadCecilia Gladys Cohaila AcevedoPas encore d'évaluation
- BioequivalenciaDocument28 pagesBioequivalenciaDk-AngelPas encore d'évaluation
- Bio FarmaciaDocument6 pagesBio FarmaciaFranco PortalPas encore d'évaluation
- Clase #5Document15 pagesClase #5Luis Raymundo flores floresPas encore d'évaluation
- Biodisponibilidad y BioequivalenciaDocument28 pagesBiodisponibilidad y BioequivalenciaEddy CarbajalPas encore d'évaluation
- Biod Is Poni Bili DadDocument3 pagesBiod Is Poni Bili DadFrancisco PinheiroPas encore d'évaluation
- Biodisponibilidad de Los Fármacos - Farmacología Clínica - Manual MSD Versión para Profesionales PDFDocument2 pagesBiodisponibilidad de Los Fármacos - Farmacología Clínica - Manual MSD Versión para Profesionales PDFDoris AbadPas encore d'évaluation
- Conceptos Fundamentales de Biofarmacia.Document37 pagesConceptos Fundamentales de Biofarmacia.raziel boxPas encore d'évaluation
- Biodisponibilidad y Bioequivalencia Exposicion BiofarmaciaDocument35 pagesBiodisponibilidad y Bioequivalencia Exposicion BiofarmaciaAaron Garcia SanchezPas encore d'évaluation
- Biodisponibilidad FarmacéuticaDocument3 pagesBiodisponibilidad FarmacéuticaFavio Zuñiga100% (1)
- Practica Biodisponibilidad-Bioequivalencia-ToxicidadDocument11 pagesPractica Biodisponibilidad-Bioequivalencia-ToxicidadLILIANA CASTILLOPas encore d'évaluation
- Biofarmacia I. Tema IDocument7 pagesBiofarmacia I. Tema IXiomara Ortega BetancoPas encore d'évaluation
- Estudio de BioequivalenciaDocument14 pagesEstudio de BioequivalenciaVladimir Condori Melgar0% (1)
- Parámetros FarmacocinéticosDocument27 pagesParámetros FarmacocinéticosLuis Cordova50% (2)
- BiodisponibilidadDocument17 pagesBiodisponibilidadLuis DuartePas encore d'évaluation
- BiodisponibilidadDocument24 pagesBiodisponibilidadquintanilla_asesorPas encore d'évaluation
- Regimenes de Dosificacion y Farmacocinetica ClinicaDocument4 pagesRegimenes de Dosificacion y Farmacocinetica ClinicaDe León100% (1)
- 5pm2 - Franco Martinez Candy Scarlet - Med Genéricos y BiodisponibilidadDocument1 page5pm2 - Franco Martinez Candy Scarlet - Med Genéricos y BiodisponibilidadDulce MartínezPas encore d'évaluation
- Repaso Conceptos Generales + Farmacocinética CON RESPUESTASDocument8 pagesRepaso Conceptos Generales + Farmacocinética CON RESPUESTASAracelly JofrePas encore d'évaluation
- Estudios de Bioequivalencia - Enfoque Metodológico y Aplicaciones Prácticas en La Evaluación de Medicamentos GenéricosDocument11 pagesEstudios de Bioequivalencia - Enfoque Metodológico y Aplicaciones Prácticas en La Evaluación de Medicamentos GenéricosCarlos Alberto Bayona LópezPas encore d'évaluation
- BiodisponibilidadDocument4 pagesBiodisponibilidadMargot Mendoza SalasPas encore d'évaluation
- Modulo 1 BioequivalenciaDocument27 pagesModulo 1 BioequivalenciaDEICYPas encore d'évaluation
- Biodisponibilidad y BioequivalenciaDocument4 pagesBiodisponibilidad y BioequivalenciaJosé Antonio ARPas encore d'évaluation
- Importancia de La Biodisponibilidad en Medicamentos GenéricosDocument1 pageImportancia de La Biodisponibilidad en Medicamentos GenéricosAlondra CoroyPas encore d'évaluation
- Practica FarmaDocument9 pagesPractica FarmaBriseidaPas encore d'évaluation
- 1 Farmacia HospitalariaDocument74 pages1 Farmacia HospitalariaJennyCortez67% (3)
- Semana 1 Introduccion A La Biof-Fcocin. BF - FKDocument30 pagesSemana 1 Introduccion A La Biof-Fcocin. BF - FKricardo100% (1)
- BIOEQUIVALENCIA-Y-REGLAMENTO-DE-INTERCAMBIABILIDAD UltimoDocument10 pagesBIOEQUIVALENCIA-Y-REGLAMENTO-DE-INTERCAMBIABILIDAD UltimoCieloPas encore d'évaluation
- Regimenes PosológicosDocument6 pagesRegimenes PosológicosKaren Calixto100% (1)
- Biofarmacia Tarea #1Document3 pagesBiofarmacia Tarea #1roberth panchanaPas encore d'évaluation
- Medicamentos GenéricosDocument37 pagesMedicamentos GenéricosPamelaHuancaQPas encore d'évaluation
- Doc2 DoralinDocument32 pagesDoc2 Doralinalfreulis rodriguezPas encore d'évaluation
- BiofarmaciaDocument10 pagesBiofarmaciaDaysi LombardoPas encore d'évaluation
- Mapas Mentales de Principios FarmacologicosDocument5 pagesMapas Mentales de Principios FarmacologicosjuanflorarcsaPas encore d'évaluation
- Estudio de BioequivalenciaDocument33 pagesEstudio de BioequivalenciaFernanda MartinezPas encore d'évaluation
- Biodisponibilidad y Bioequivalencia+MakDocument41 pagesBiodisponibilidad y Bioequivalencia+MakJessica Benavides BermudezPas encore d'évaluation
- ABC BioequiDocument30 pagesABC BioequiAdriana Soto MijaresPas encore d'évaluation
- Biodisponibilidad y Bioequivalencia Upch 2020 - IDocument56 pagesBiodisponibilidad y Bioequivalencia Upch 2020 - IBERNI ABEL CONDORI FLORES100% (1)
- Eliminacion SalivalDocument4 pagesEliminacion SalivaleduPas encore d'évaluation
- Cuestionario Farmacocinética Clínica Esli OropezaDocument4 pagesCuestionario Farmacocinética Clínica Esli OropezaEsli OropezaPas encore d'évaluation
- Gomez Martinez Briseida Itzel 5PM2 Practica2Document6 pagesGomez Martinez Briseida Itzel 5PM2 Practica2BriseidaPas encore d'évaluation
- Temas 1 Y 2.-Introducción A La Biofarmacia Y FarmacocinéticaDocument142 pagesTemas 1 Y 2.-Introducción A La Biofarmacia Y FarmacocinéticaDaniela Ruth Herbas Del VillarPas encore d'évaluation
- Biodisponibilidad y BioequivalenciaDocument2 pagesBiodisponibilidad y BioequivalenciaGaBys Gabuchx's BabuchasPas encore d'évaluation
- Conceptos Basicosde Farmacocinetica ClinDocument36 pagesConceptos Basicosde Farmacocinetica ClinValeria SerranoPas encore d'évaluation
- 01biofarmacia y FarmacocineticaDocument28 pages01biofarmacia y FarmacocineticaLizeth Rodriguez MamaniPas encore d'évaluation
- 1998 134 4 491 494 PDFDocument4 pages1998 134 4 491 494 PDFAna Cecilia Huaman RojasPas encore d'évaluation
- Wikinski Cap1 PDFDocument21 pagesWikinski Cap1 PDFResidencia Psiquiatría CochabambaPas encore d'évaluation
- FARMACOLOGIADocument16 pagesFARMACOLOGIAarturo partida silvaPas encore d'évaluation
- BIOFARMACIADocument5 pagesBIOFARMACIAPRISCILA YAMILET JIMENEZ MANZOPas encore d'évaluation
- P5.-Estudio Piloto de Bioequivalencia de Metronidazol FinalDocument33 pagesP5.-Estudio Piloto de Bioequivalencia de Metronidazol FinalMiriam AlcaidePas encore d'évaluation
- Biodisponibilidad y Bioequivalencia - Parte 1Document28 pagesBiodisponibilidad y Bioequivalencia - Parte 1GUICELASAIGUAPas encore d'évaluation
- Practica LLL BiodisponibilidadDocument3 pagesPractica LLL BiodisponibilidadKarina ZavalaPas encore d'évaluation
- Ensayo de Los Temas de FarmacocinéticaDocument3 pagesEnsayo de Los Temas de FarmacocinéticaEloy L. Eufracio100% (1)
- Ciencia regulatoria: Medicamentos bio y su relevancia para la saludD'EverandCiencia regulatoria: Medicamentos bio y su relevancia para la saludPas encore d'évaluation
- Imperio CarolingioDocument1 pageImperio CarolingioCathy Díaz PérezPas encore d'évaluation
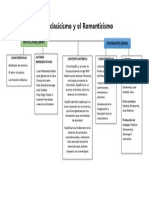
- El Neoclasicismo y El RomanticismoDocument1 pageEl Neoclasicismo y El RomanticismoCathy Díaz Pérez100% (1)
- Ley 640 de 2001Document9 pagesLey 640 de 2001Cathy Díaz PérezPas encore d'évaluation
- Bibliografía de DanielDocument9 pagesBibliografía de DanielCathy Díaz PérezPas encore d'évaluation
- Leyes AmbientalesDocument3 pagesLeyes AmbientalesCathy Díaz Pérez100% (1)
- Que Busca La Ley 1237 Del 2009Document2 pagesQue Busca La Ley 1237 Del 2009Cathy Díaz PérezPas encore d'évaluation
- Análisis Artículo 45 de La Constitución Política de ColombiaDocument10 pagesAnálisis Artículo 45 de La Constitución Política de ColombiaCathy Díaz Pérez100% (2)
- Exposicion ReligionDocument6 pagesExposicion ReligionCathy Díaz PérezPas encore d'évaluation
- Metodología de La InvestigaciónDocument1 pageMetodología de La InvestigaciónCathy Díaz PérezPas encore d'évaluation
- Trabajo de Práctica de LaboratorioDocument11 pagesTrabajo de Práctica de LaboratorioCathy Díaz PérezPas encore d'évaluation
- Filosofia en La Edad AntiguaDocument30 pagesFilosofia en La Edad AntiguaCathy Díaz PérezPas encore d'évaluation
- Las Fiestas JudiasDocument14 pagesLas Fiestas JudiasCathy Díaz PérezPas encore d'évaluation
- Enfermedades NeuromuscularesDocument13 pagesEnfermedades NeuromuscularesLuis AlvarezPas encore d'évaluation
- Presentación2 Campos de Aplicacion de La PsicologiaDocument20 pagesPresentación2 Campos de Aplicacion de La PsicologiaKarla RPas encore d'évaluation
- Susan Sherwin: "Feminismo y Bioética"Document25 pagesSusan Sherwin: "Feminismo y Bioética"MijuPas encore d'évaluation
- MANUAL DE PROTECCIÓN RADIOLÓGICA SCAN 20017SEPfin2Document2 pagesMANUAL DE PROTECCIÓN RADIOLÓGICA SCAN 20017SEPfin2Luis CastilloPas encore d'évaluation
- Terapia Neural MADocument38 pagesTerapia Neural MAAnibal Monge100% (2)
- L 10 VendajesDocument3 pagesL 10 VendajesMatías N. DíazPas encore d'évaluation
- Oxime TriaDocument7 pagesOxime Triazenith4499Pas encore d'évaluation
- 2005 GuiaNacionaldeneonatologia PDFDocument475 pages2005 GuiaNacionaldeneonatologia PDFCecilia BerenicePas encore d'évaluation
- Guia de Laringectomizado Final para España PDFDocument191 pagesGuia de Laringectomizado Final para España PDFprueba12345Pas encore d'évaluation
- ApuntesENARM PDFDocument43 pagesApuntesENARM PDFsupergasper11Pas encore d'évaluation
- Cuestionario D EparaDocument3 pagesCuestionario D EparaShaden Dionicio50% (2)
- Evaluación - Módulo 4Document3 pagesEvaluación - Módulo 4Luis H Velasco H100% (1)
- Ebb1 34B S LP 1Document1 pageEbb1 34B S LP 1Lg SlkPas encore d'évaluation
- Okana IworiDocument10 pagesOkana Iwori3al33% (3)
- Anti ComercialesDocument1 pageAnti ComercialesRoberto PeñaPas encore d'évaluation
- Ortopedia y TraumatologiaDocument24 pagesOrtopedia y TraumatologiaEdgar EstradaPas encore d'évaluation
- MANEJO DE pROLApSO pELVICODocument54 pagesMANEJO DE pROLApSO pELVICOAna Rocio del Pilar100% (1)
- Actividad Antimicrobiana Del Cafe Con Penicilina y AmpicilinaDocument4 pagesActividad Antimicrobiana Del Cafe Con Penicilina y AmpicilinaDago OrtizPas encore d'évaluation
- Test de Posiciones CorporalesDocument17 pagesTest de Posiciones CorporalesinesPas encore d'évaluation
- Firma PersonalDocument2 pagesFirma PersonalLuis BlancoPas encore d'évaluation
- Nom 010 Ssa2 2010Document16 pagesNom 010 Ssa2 2010Abdiel RodriguezPas encore d'évaluation
- WU WEI XIAO DU WAN Eliminar El Calor Tóxico y Viento-Calor FitokiDocument5 pagesWU WEI XIAO DU WAN Eliminar El Calor Tóxico y Viento-Calor FitokiJuan Carlos HernandezPas encore d'évaluation
- Esporotricosis Sporothrix SchenckiiDocument22 pagesEsporotricosis Sporothrix SchenckiiCarolina Cabrera CernaPas encore d'évaluation
- Finanzas Practica Punto de EquilibrioDocument2 pagesFinanzas Practica Punto de Equilibrionico-1593Pas encore d'évaluation
- Validación Procesos Térmicos-Calor Seco PDFDocument83 pagesValidación Procesos Térmicos-Calor Seco PDFSandro Sotomayor100% (2)
- DispensarizacionDocument10 pagesDispensarizacionGarcíaVentuarysPas encore d'évaluation
- Equipos USAR Nivel MedianoDocument16 pagesEquipos USAR Nivel MedianoPablo VásquezPas encore d'évaluation
- Sika AceleranteDocument8 pagesSika AceleranteraarquitecturaPas encore d'évaluation
- AfasiasDocument7 pagesAfasiasStefania Galvan BaezPas encore d'évaluation
- VibracionesDocument4 pagesVibracionesDIANA YULEI CASANOVA MARROQUINPas encore d'évaluation