Académique Documents
Professionnel Documents
Culture Documents
Lista de Cinética - 2 PDF
Transféré par
Marcelo Satorres0 évaluation0% ont trouvé ce document utile (0 vote)
279 vues2 pagesTitre original
LISTA DE CINÉTICA - 2.pdf
Copyright
© © All Rights Reserved
Formats disponibles
PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PDF, TXT ou lisez en ligne sur Scribd
0 évaluation0% ont trouvé ce document utile (0 vote)
279 vues2 pagesLista de Cinética - 2 PDF
Transféré par
Marcelo SatorresDroits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 2
Prof.
Murilo Chales Pereira (PINK)
Lista de Exerccios CINTICA QUMICA
CINTICA - 2
01. Durante a decomposio da gua oxigenada,
ocorre a formao de gua e oxignio, de acordo
com a equao:
2H
2
O
2
(aq) 2H
2
O(l) + O
2
(g)
Se a velocidade de liberao de oxignio 1 10
-4
mol.s
-1
, a velocidade de consumo da gua
oxigenada em mol.s
-1
:
a) 0,5 10
-4
b) 1 10
-4
c) 2 10
-4
d) 3 10
-4
02. A penicilina, antibitico natural derivado de um
fungo e descoberto por Alexander Fleming, est
disponvel como frmaco desde a dcada de 40,
quando foi desenvolvida tcnica de congelamento
e preparao industrial. Este antibitico sofre uma
deteriorao com o tempo, conforme o grfico
apresentado a seguir:
Com base nas informaes apresentadas, conclui-
se que a velocidade de deteriorao da penicilina
nas primeiras dez semanas , em mol.L
-1
/semana,
aproximadamente:
a) 0,0025
b) 0,01
c) 0,025
d) 0,125
e) 0,166
03. Os dados experimentais para a velocidade de
reao, v, indicados no quadro a seguir, foram
obtidos a partir dos resultados em diferentes
concentraes de reagentes iniciais para a
combusto do monxido de carbono, em
temperatura constante.
A equao de velocidade para essa reao pode
ser escrita como v = k [CO]
a
[O
2
]
b
, onde a e b so,
respectivamente, as ordens de reao em relao
aos componentes CO e O
2
.
De acordo com os dados experimentais, correto
afirmar que respectivamente os valores de a e b
so:
a) 1 e 2
b) 2 e 1
c) 3 e 2
d) 0 e 1
e) 1 e 1
04. Analise este grfico, em que est representada
a variao da concentrao de um reagente em
funo do tempo em uma reao qumica:
Considerando-se as informaes desse grfico,
CORRETO afirmar que, no intervalo entre 1 e 5
minutos, a velocidade mdia de consumo desse
reagente de
a) 0,200 (mol/L)/min .
b) 0,167 (mol/L)/min .
c) 0,225 (mol/L)/min .
d) 0,180 (mol/L)/min .
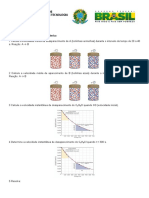
05. O aspartame um adoante usado em bebidas
lcteas dietticas. A reao de degradao do
aspartame nessas bebidas apresenta cintica de
primeira ordem em relao a sua concentrao. O
grfico a seguir relaciona a velocidade de
degradao do aspartame com a concentrao,
nas temperaturas de 4C e 20C.
Dois frascos A e B tm a mesma concentrao
inicial de aspartame, 200 mg/L, mas o primeiro
est armazenado a 20C e o segundo a 4C. Qual
reao mais veloz? Justifique sem clculos.
06. O grfico a seguir representa a variao, em
funo do tempo, da concentrao, em quantidade
de matria, do hidrognio gasoso formado em
duas reaes qumicas de alumnio metlico com
soluo concentrada de cido clordrico. Estas
reaes so realizadas sob as mesmas condies,
diferindo, somente, quanto s formas de
apresentao do alumnio: placas metlicas e p
metlico.
Calcule a razo entre a maior e a menor
velocidade mdia da reao.
07. Considere a reao elementar representada
pela equao
3 O
2
(g) 2 O
3
(g)
Ao triplicarmos a concentrao do oxignio, a
velocidade da reao, em relao velocidade
inicial, torna-se
a) duas vezes menor.
b) trs vezes maior.
c) oito vezes menor.
d) nove vezes maior.
e) vinte e sete vezes maior.
08. No incio do sculo XX, a expectativa da
Primeira Guerra Mundial gerou uma grande
necessidade de compostos nitrogenados. Haber foi
o pioneiro na produo de amnia, a partir do
nitrognio do ar. Se a amnia for colocada num
recipiente fechado, sua decomposio ocorre de
acordo com a seguinte equao qumica no
balanceada:
NH
3
(g) N
2
(g) + H
2
(g).
As variaes das concentraes com o tempo
esto ilustradas na figura a seguir:
A partir da anlise da figura acima, podemos
afirmar que as curvas A, B e C representam a
variao temporal das concentraes dos
seguintes componentes da reao,
respectivamente:
a) H
2
, N
2
e NH
3
b) NH
3
, H
2
e N
2
c) NH
3
, N
2
e H
2
d) N
2
, H
2
e NH
3
e) H
2
, NH
3
e N
2
09. A reao 2NO(g) + 2H
2
(g) N
2
(g) + 2H
2
O(g)
foi estudada a 904 C. Os dados da tabela
seguinte referem-se a essa reao.
A respeito dessa reao correto afirmar que sua
expresso da velocidade
a) v = k[NO] [H
2
].
b) v = k[NO]
2
[H
2
].
c) v = k[H
2
].
d) v = k[NO]
4
[H
2
]
2
.
e) v = k[NO]
2
[H
2
]
2
.
Gabarito
01. c
02. b
03. a
04. a
05. a 20
o
C
06. 3
07. e
08. d
09. b
Vous aimerez peut-être aussi
- Lista de Cinética - 1 PDFDocument3 pagesLista de Cinética - 1 PDFMarcelo Satorres0% (1)
- Cinética Química - Expressão e Cálculo Da Velocidade - 130 QuestõesDocument72 pagesCinética Química - Expressão e Cálculo Da Velocidade - 130 QuestõesrafelPas encore d'évaluation
- Cinética da reação entre NO e O2Document72 pagesCinética da reação entre NO e O2ani_matrixx4733100% (1)
- Alfa - Módulo 37Document23 pagesAlfa - Módulo 37Jackson Rodrigo Sousa PintoPas encore d'évaluation
- Alex 3 Série e Curso Cinética Química Lista 1 15 01 15 PDFDocument2 pagesAlex 3 Série e Curso Cinética Química Lista 1 15 01 15 PDFElysangela RavaniPas encore d'évaluation
- Lista Cinética QuímicaDocument6 pagesLista Cinética QuímicavfmgarciaPas encore d'évaluation
- Cinética QuímicaDocument6 pagesCinética QuímicaSirlei Gonçalves PoffoPas encore d'évaluation
- Cinetica CompletaDocument5 pagesCinetica CompletaConta ReservaPas encore d'évaluation
- Lista de apoio química trimestralDocument5 pagesLista de apoio química trimestralThaayna BarroosPas encore d'évaluation
- Lista CinéticaDocument18 pagesLista Cinéticamoitinhamhsp2Pas encore d'évaluation
- Equilibrios ConstantesDocument6 pagesEquilibrios ConstantesFred DiasPas encore d'évaluation
- Cinética QuímicaDocument5 pagesCinética QuímicaJames OliverPas encore d'évaluation
- Cinetica Quimica If ExercDocument5 pagesCinetica Quimica If ExercRaquel Andreola ValentePas encore d'évaluation
- Formação de estalactites em cavernasDocument9 pagesFormação de estalactites em cavernasfernandaveredianoPas encore d'évaluation
- Lista de Equilíbrio Químico PDFDocument3 pagesLista de Equilíbrio Químico PDFMarcelo SatorresPas encore d'évaluation
- Lista 1.cinética QuímicaDocument6 pagesLista 1.cinética Químicagiovannaluiza1323Pas encore d'évaluation
- Lista de Exercícios Cinética QuímicaDocument6 pagesLista de Exercícios Cinética QuímicagabezmirandaPas encore d'évaluation
- CNPJDocument5 pagesCNPJDavi AraújoPas encore d'évaluation
- Química - Prof. Rafael - Equilíbrio Químico e Deslocamento de EquilíbrioDocument12 pagesQuímica - Prof. Rafael - Equilíbrio Químico e Deslocamento de EquilíbrioRafael VaristeloPas encore d'évaluation
- Química: Raio atômico, reatividade e pares galvânicosDocument9 pagesQuímica: Raio atômico, reatividade e pares galvânicosKelita CoimbraPas encore d'évaluation
- Cinética da reação entre NO e Br2Document2 pagesCinética da reação entre NO e Br2Alexander OrtizPas encore d'évaluation
- Matéria e Suas PropriedadesDocument28 pagesMatéria e Suas PropriedadesGleisonPas encore d'évaluation
- Lista de Termoquímica GeraisDocument3 pagesLista de Termoquímica GeraisMarcelo SatorresPas encore d'évaluation
- 6 Lista de Exercícios - 2019 1Document3 pages6 Lista de Exercícios - 2019 1Pedro FelipePas encore d'évaluation
- Lista de QuimicaDocument9 pagesLista de QuimicaBeatriz Miranda MoreiraPas encore d'évaluation
- Extensivoenem Química Equilíbrio Químico - KC e KP 12-07-2019Document9 pagesExtensivoenem Química Equilíbrio Químico - KC e KP 12-07-2019Pedro ManoelPas encore d'évaluation
- Lista de Exercícios sobre Equilíbrio QuímicoDocument5 pagesLista de Exercícios sobre Equilíbrio Químicoricharlesalves2013Pas encore d'évaluation
- 3 Lista de Exercicios - Cinética Química e Equilíbrio Químico (Gabarito)Document3 pages3 Lista de Exercicios - Cinética Química e Equilíbrio Químico (Gabarito)Dvmr AnapPas encore d'évaluation
- Alfa - Módulo 40Document28 pagesAlfa - Módulo 40Luiza FreitasPas encore d'évaluation
- 21Document5 pages21gabezmirandaPas encore d'évaluation
- Ae rq11 Ficha 1Document9 pagesAe rq11 Ficha 1Juliana SáPas encore d'évaluation
- Cinética e Equilíbrio QuímicoDocument8 pagesCinética e Equilíbrio QuímicoBruna FerreiraPas encore d'évaluation
- DF Quimica Welson 5e790a5ce82acDocument28 pagesDF Quimica Welson 5e790a5ce82acPedro HenriquePas encore d'évaluation
- Química Fundamental: Cinética e Equilíbrio QuímicoDocument5 pagesQuímica Fundamental: Cinética e Equilíbrio QuímicoHugo ChavesPas encore d'évaluation
- Lista de Exercicios Cinetica Quimica EQM061Document13 pagesLista de Exercicios Cinetica Quimica EQM061Mariana DomicianoPas encore d'évaluation
- Balanceamento de equações químicas de oxirreduçãoDocument2 pagesBalanceamento de equações químicas de oxirreduçãoMarineide Resende Medeiros0% (1)
- Termoquímica - ExercíciosDocument39 pagesTermoquímica - ExercíciosGleisonPas encore d'évaluation
- Quím CinéticaDocument8 pagesQuím CinéticaJoão Ribeiro Franco NetoPas encore d'évaluation
- Cinética Química: Velocidade de ReaçõesDocument166 pagesCinética Química: Velocidade de Reaçõesandrevini890% (1)
- Balanceamento por Números de OxidaçãoDocument3 pagesBalanceamento por Números de OxidaçãoalarinhoPas encore d'évaluation
- Exercícios termoquímicaDocument22 pagesExercícios termoquímicaSérgio ViroliPas encore d'évaluation
- Simulado de QuímicaDocument7 pagesSimulado de QuímicaTalles FelipePas encore d'évaluation
- Velocidade Das Reações - ÍtaloDocument8 pagesVelocidade Das Reações - ÍtaloItalo PiresPas encore d'évaluation
- 51 20equil C3 ADbrio 20qu C3 ADmico 20ADocument87 pages51 20equil C3 ADbrio 20qu C3 ADmico 20AJhonny WalkerPas encore d'évaluation
- Cinética Química: Vm e Teoria das ColisõesDocument4 pagesCinética Química: Vm e Teoria das ColisõesEduardo KüllPas encore d'évaluation
- Termoquímica FundamentosDocument6 pagesTermoquímica FundamentosEduardo KüllPas encore d'évaluation
- TermoquimicaDocument8 pagesTermoquimicaBruno Bonafé100% (1)
- Lista I - Reatores IDocument13 pagesLista I - Reatores IVilmar Bertotti JuniorPas encore d'évaluation
- Exercícios de Cinética Química (Lista 1) (1)Document7 pagesExercícios de Cinética Química (Lista 1) (1)gabriel.kenzo18Pas encore d'évaluation
- LISTA9Document12 pagesLISTA9Amanda Tenório BatistaPas encore d'évaluation
- Cinetica Quimica Questoes SubjetivasDocument18 pagesCinetica Quimica Questoes SubjetivasJosue Dos Santos NascimentoPas encore d'évaluation
- Lista de exercícios equilíbrio químicoDocument6 pagesLista de exercícios equilíbrio químicoJoice BeatrizPas encore d'évaluation
- Cinetica Quimica Com GabaritoDocument7 pagesCinetica Quimica Com GabaritoCésar Augusto100% (4)
- Lista Cinética PDFDocument9 pagesLista Cinética PDFLeydiane Araujo BrandaoPas encore d'évaluation
- Reação química: cinética e fatores que influenciam a velocidadeDocument10 pagesReação química: cinética e fatores que influenciam a velocidadeErick Teckio100% (1)
- Velocidade de reações químicasDocument4 pagesVelocidade de reações químicasaguiartePas encore d'évaluation
- Apostila Química Orgânica: Carbono, Dienos E AromáticosD'EverandApostila Química Orgânica: Carbono, Dienos E AromáticosPas encore d'évaluation
- Apresentação FulerenoDocument12 pagesApresentação FulerenoMarcelo SatorresPas encore d'évaluation
- Apresentação NitrogênioDocument19 pagesApresentação NitrogênioMarcelo SatorresPas encore d'évaluation
- Substâncias e misturasDocument14 pagesSubstâncias e misturasAdryana SousaPas encore d'évaluation
- Lista de Equilíbrio Químico PDFDocument3 pagesLista de Equilíbrio Químico PDFMarcelo SatorresPas encore d'évaluation
- 04 Numeros QuanticosDocument27 pages04 Numeros QuanticosGabriel OliveiraPas encore d'évaluation
- 04 Numeros QuanticosDocument27 pages04 Numeros QuanticosGabriel OliveiraPas encore d'évaluation
- Classificação de cadeias carbônicas em compostos orgânicosDocument2 pagesClassificação de cadeias carbônicas em compostos orgânicosMarcelo SatorresPas encore d'évaluation
- Lista de Classificação Do Átomo de Carbono PDFDocument2 pagesLista de Classificação Do Átomo de Carbono PDFMarcelo SatorresPas encore d'évaluation
- Lista de Isomeria Plana PDFDocument3 pagesLista de Isomeria Plana PDFMarcelo SatorresPas encore d'évaluation
- Lista de Pilha PDFDocument4 pagesLista de Pilha PDFMarcelo SatorresPas encore d'évaluation
- Lista de Reação de Eliminação PDFDocument2 pagesLista de Reação de Eliminação PDFMarcelo SatorresPas encore d'évaluation
- Lista de Eletrólise PDFDocument3 pagesLista de Eletrólise PDFMarcelo Satorres0% (1)
- Reações de adição em química orgânicaDocument2 pagesReações de adição em química orgânicaMarcelo SatorresPas encore d'évaluation
- Energia de ligação em exercícios de termoquímicaDocument2 pagesEnergia de ligação em exercícios de termoquímicaMarcelo SatorresPas encore d'évaluation
- Lista de Esterificação e Hidrólise PDFDocument3 pagesLista de Esterificação e Hidrólise PDFMarcelo SatorresPas encore d'évaluation
- Estrutura AtômicaDocument7 pagesEstrutura AtômicaMarcelo SatorresPas encore d'évaluation
- Estrutura AtômicaDocument7 pagesEstrutura AtômicaMarcelo SatorresPas encore d'évaluation
- Estágio Institucional M InêsDocument22 pagesEstágio Institucional M InêsMarcelo SatorresPas encore d'évaluation
- Lista de Termoquímica GeraisDocument3 pagesLista de Termoquímica GeraisMarcelo SatorresPas encore d'évaluation
- Propriedades ColigativasDocument3 pagesPropriedades ColigativasMarcelo SatorresPas encore d'évaluation
- Volume Molar e Equação de EstadoDocument1 pageVolume Molar e Equação de EstadoMarcelo SatorresPas encore d'évaluation
- 6 - de GasDocument18 pages6 - de GasClaudia Marcia Ferreira DiasPas encore d'évaluation
- Armazenamento Seguro Produtos QuímicosDocument4 pagesArmazenamento Seguro Produtos QuímicosJorge Ferreira Junior100% (1)
- Lista de Exercicios Aulas 1 e 2Document6 pagesLista de Exercicios Aulas 1 e 2Nathalia KarinePas encore d'évaluation
- Corrosão por cloreto acelera falha prematura de tubos de aço inoxidável em pré-aquecedor de caldeiraDocument6 pagesCorrosão por cloreto acelera falha prematura de tubos de aço inoxidável em pré-aquecedor de caldeirabiancogallazziPas encore d'évaluation
- 2007 Organ Iza Mercado 1Document93 pages2007 Organ Iza Mercado 1FelipePas encore d'évaluation
- Deslocamento de Equilibrio Quimica Exercicios GabaritoDocument29 pagesDeslocamento de Equilibrio Quimica Exercicios GabaritoAdolfo GomesPas encore d'évaluation
- Trad. A Recuperação Do Cobre Através Da LixiviaçãoDocument15 pagesTrad. A Recuperação Do Cobre Através Da LixiviaçãoRahmanRachideAliBacarPas encore d'évaluation
- Conversão Caldeiras GN OCDocument152 pagesConversão Caldeiras GN OCLuis Antonio BassoPas encore d'évaluation
- LubrificantesDocument21 pagesLubrificantesrmsabreuPas encore d'évaluation
- CAP 3 - Tabela PeriódicaDocument11 pagesCAP 3 - Tabela PeriódicaGiovan LautenschlagerPas encore d'évaluation
- Fogão 5 Bocas EletroluxDocument32 pagesFogão 5 Bocas EletroluxclaytonPas encore d'évaluation
- Manual Dispenser GNVDocument18 pagesManual Dispenser GNVWelenadja de SáPas encore d'évaluation
- Parte 2 - Energias RenováveisDocument46 pagesParte 2 - Energias RenováveisAndressa SoaresPas encore d'évaluation
- Exercicio de Massa Molar, Atomica e MolDocument4 pagesExercicio de Massa Molar, Atomica e Molyvy_gayaPas encore d'évaluation
- UFES-Corrosão MateriaisDocument41 pagesUFES-Corrosão MateriaisBruno VazPas encore d'évaluation
- Parecer Técnico Lo Metanauto Posto de Combustivel LtdaDocument10 pagesParecer Técnico Lo Metanauto Posto de Combustivel LtdaMARCELO MANHÃES DE AMORIMPas encore d'évaluation
- Producao de Biodiesel-2Document29 pagesProducao de Biodiesel-2Mariana FerreiraPas encore d'évaluation
- Mapa - Gamb - Estatística - 51/2024Document3 pagesMapa - Gamb - Estatística - 51/2024Sara CristinaPas encore d'évaluation
- Sistemas Fixos de Combate A Incêndio Por GasesDocument28 pagesSistemas Fixos de Combate A Incêndio Por GasesCleiton Viera Dos Santos100% (1)
- Lista de GeradoresDocument22 pagesLista de GeradoresScarlett Neves100% (1)
- Aquecimento de tubos e béquer com bico de BunsenDocument4 pagesAquecimento de tubos e béquer com bico de BunsenClaudia MetanoiaPas encore d'évaluation
- Tabela CESTDocument33 pagesTabela CESTtressoPas encore d'évaluation
- Kombucha Receita e CuidadosDocument5 pagesKombucha Receita e CuidadosLéo BritoPas encore d'évaluation
- Porque As Unhas de Gel Se CaenDocument2 pagesPorque As Unhas de Gel Se CaenEasy Nails BrasilPas encore d'évaluation
- NBR 17505-3 - Líquidos Inflamáveis e Combustíveis - TubulaçõDocument12 pagesNBR 17505-3 - Líquidos Inflamáveis e Combustíveis - TubulaçõGuilherme AugustoPas encore d'évaluation
- Obqne 1999Document4 pagesObqne 1999Nicole OliveiraPas encore d'évaluation
- NBR-7094-Motores de InduçãoDocument61 pagesNBR-7094-Motores de InduçãoWanderson SantosPas encore d'évaluation
- Aplicações Do Bicarbonato de SódioDocument14 pagesAplicações Do Bicarbonato de SódiomarsjommPas encore d'évaluation
- Instalação e operação de forno de panificaçãoDocument19 pagesInstalação e operação de forno de panificaçãoDiego MiramontesPas encore d'évaluation