Académique Documents
Professionnel Documents
Culture Documents
Guía 8 de Balance de Masa y Energía
Transféré par
JUAN ANDRÉS SANDOVAL HERRERADescription originale:
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Guía 8 de Balance de Masa y Energía
Transféré par
JUAN ANDRÉS SANDOVAL HERRERADroits d'auteur :
Formats disponibles
GUA 8 DE BALANCE DE MASA Y ENERGA Curso Intersemestral
Profesor JUAN ANDRS SANDOVAL HERRERA
F.U.A. 2014
Introduccin a los Balances de energa sin reaccin qumica
Problemas resueltos y propuestos
PROBLEMAS RESUELTOS
1. Un kilogramo de vapor a una presin de 1 bar, que est
contenido en un recipiente cilndrico de rea transversal 1,69
m
2
, soporta una cubierta mvil hermtica, de un
determinado peso. Se calienta externamente el cilindro para
elevar la temperatura del vapor de 100 C hasta 300 C.
Suponiendo que no hay prdidas de calor hacia los
alrededores, calcule la cantidad de calor que requiere el
proceso y el trabajo realizado.
SOLUCIN:
El sistema es el vapor de agua encerrado. No hay entradas ni salidas,
luego es un sistema cerrado. Al calentarse el vapor, se expande y
sube la cubierta mvil, as la presin se mantiene constante. El gas se
puede considerar en reposo, porque su velocidad es mnima.
Entonces, la ecuacin de energa en trminos de entalpa ser:
[( )]
O en otra forma:
)
En la tabla de vapor sobre calentado, a 1 bar y 100 C, la entalpa
especfica del vapor es 2676 kJ/kg y el volumen especfico es 1,69
m
3
/kg. A 300C y 1 bar, los valores correspondientes, en la misma
tabla, son 3074 kJ/kg y 2,64 m
3
/kg. Se aplica la ecuacin de energa
entre los dos puntos y da:
) El
volumen dividido entre el rea, da la altura. Pero el centro de masa
est en la mitad de esa altura, de forma que (
) =
(2,64-1,69)/2*1,69 = 0,281 m
Entonces, Q = 1 kg (3074-2676) kJ/kg + (1 kg*9,8 m/s
2
*0,281 m)
Q = 400 kJ
Ahora, el trabajo realizado por el vapor al expandirse:
W = pV2- pV1 = 100000 N/m
2
* (2,74-1,69) m
3
/kg =95 kJ/kg
2. La energa interna especfica del helio a 300 K y 1 atm es
3800 J/mol y su volumen especfico a la misma temperatura y
presin es 24,63 L/mol. Calcule la entalpa especfica del helio
a esas condiciones y la velocidad a la cual transporta entalpa
si la velocidad de flujo molar del helio es 250 kmol/h.
SOLUCIN:
La entalpa especfica es:
Se conoce la energa interna
especfica (molar), la presin y el volumen especfico (molar).
Entonces, reemplazando:
3800 J/mol + (1 atm * 24,63 L/mol * 101,3 J /(L*atm) = 6295 J
/mol
*El factor de conversin resulta de dividir las constantes de
los gases en unidades J/mol*K entre las unidades
atm*L/(mol*K)
Ahora la velocidad de transporte (o de flujo) de entalpa, es:
1,57*10
9
J/h
3. Calcule la cantidad de calor necesario para elevar la
temperatura de 1 kg de vapor a 1 bar, desde 100 hasta 300
C, y la presin final del vapor.
SOLUCIN:
El sistema es el vapor de agua encerrado. No hay entradas ni salidas,
luego es un sistema cerrado. Entonces la ecuacin de energa se
reduce a: Dado que el recipiente est a presin y dice
que se eleva la presin, por el calentamiento, entonces el volumen
es constante (a diferencia del primer ejercicio). Esto significa que: W
= 0
Porque W = pV. De esta manera,
Entonces, se mira en las tablas a 1 bar y 100C, la
= 2507 kJ/kg. Y
se mira el volumen especfico,
= 1,69 m
3
/kg, porque este volumen
no debe cambiar, ya que el sistema es cerrado (no entra ni sale
masa) y el volumen se mantiene constante, como se haba analizado
arriba.
Ahora, a 300C, se busca tambin en las tablas de vapor
sobrecalentado. Se entra por temperatura (Tabla B7) Y se mira
primero a 1 bar y luego a una presin mayor. Entonces, a 1 bar el
volumen especfico es 2,64 m
3
/kg, mientras que a 5 bar es 0,522
m
3
/kg. De forma que la presin final del vapor debe estar entre estos
dos valores 1 o 5 bar. Entonces, se interpola, de la siguiente manera:
( ) ( )
( )
Esa es la presin final del vapor. Ahora, hay que interpolar tambin
para saber la energa interna especfica del vapor en esa condicin
final, tomando como referencias las energas internas a 1 bar y a 5
bar, tambin.
( ) ( )
( )
Y ahora s, con los dos valores de energas internas especficas, final e
inicial, se calcula el calor necesario para calentar el vapor:
Q = 1 kg (2807,4 2507) kJ/kg = 300,4 kJ
4. Se alimenta vapor a 10 bar absolutos con 190 C de
sobrecalentamiento a una turbina a razn de 2000 kg/h. La
operacin de la turbina es adiabtica y el efluente es vapor
saturado a 1 bar. Calcule el trabajo producido por la turbina
en kW, despreciando los cambios de energas cintica y
potencial.
SOLUCIN:
La turbina es el sistema, no el vapor. Sin embargo, se requieren las
propiedades del vapor para caracterizar las corrientes de entrada y
de salida (que son iguales en su flujo). Y a propsito, ste es un
sistema abierto (por las corrientes). Dice que la operacin esa
adiabtica (idealmente), entonces Q = 0. Y se supone, que trabaja en
estado estacionario, a diferencia del ejercicio anterior. Entonces, la
ecuacin de energa quedara as, despus de despejar:
)
Ahora, se buscan en la Tabla de Vapor sobrecalentado (B7) a 10 bar.
Se lee la temperatura de saturacin correspondiente: 180C.
Entonces, como dice que tiene 190C de sobrecalentamiento, quiere
decir que la temperatura real del vapor a la que est, es 180 + 190 =
370 C.
No aparece esa temperatura en la Tabla. De modo que nuevamente
hay que interpolar, entre 350 y 400 C, que si aparecen, para saber el
verdadero valor de la entalpa especfica (kJ/kg). Interpolando da:
(Comprubelo)
Se busca la entalpa especfica para el vapor de salida. Sin embargo,
ste no es sobrecalentado, sino saturado, entonces se utiliza la Tabla
B6. Ah aparece que a 1 bar es: 2675 kJ/kg
De forma que:
( )
Es positivo, porque es la turbina la que lo produce sobre los
alrededores.
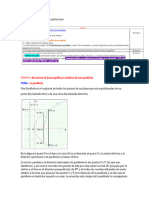
5. Una corriente de 100 kg/s de Nitrgeno a 1 bar se va a
calentar desde 25 hasta 200 C, en un intercambiador de
calor aislado, mediante la condensacin de vapor saturado
disponible a 1,5 bar. Determine el consumo de vapor.
SOLUCIN:
El intercambiador de calor es el sistema. Hay corrientes de entrada y
corrientes de salida (que son iguales en su flujo para cada sustancia).
El intercambiador puede visualizarse, para su mejor
entendimiento, como un dispositivo doble, una parte es el vapor y
la otra el nitrgeno. El vapor de agua, cede su calor al
condensarse, para que el nitrgeno se caliente. El proceso se
realiza en estado estacionario. El calor no se pierde a los
alrededores (idealmente), por lo cual Q = 0. Un intercambiador de
calor NO produce ni consume trabajo, W = 0 Por lo dems, no hay
cambios de velocidad ni de altura de las corrientes, entonces la
ecuacin de energa quedara as:
O en trminos matemticos:
( )
( )
( )
( )
Hay que tener en cuenta que los flujos de nitrgeno a la
entrada y a la salida son iguales. As mismo, los flujos de
vapor y de condensado son iguales. Entonces,
( )
( )]
[
( )
( )]
Pero como las entalpas del nitrgeno a 200C y del vapor
son mayores a las del nitrgeno a 25C y del condensado,
(porque un vapor tiene ms contenido energtico que un
lquido y un gas a mayor temperatura tiene mayor
contenido energtico que el mismo gas a menor
temperatura), entonces ambos trminos de esa expresin
darn negativos. Por lo cual, se suele expresar mejor como:
( )
( )]
[
( )
( )] (Ecuacin A)
Las entalpas del vapor y del lquido se toman de la Tabla B-
6 a 1,5 bar. Sus valores son: 2693,4 y 467,1 kJ7kg,
respectivamente. De forma que [
( )
( )]
Para el nitrgeno, se realiza la siguiente integral, que
relaciona al cambio de temperatura, con la entalpa.
Recordando que un cambio de temperatura corresponde a
un CALOR SENSIBLE; Mientras que un cambio de fase,
corresponde a un CALOR LATENTE.
Donde,
es la capacidad calorfica del nitrgeno a
presin constante. Y se evala la integral entre las
temperaturas inicial (25C = 298,15 K) y final (200C =
473,15 K), con las constantes del Cp, para el nitrgeno,
tomadas de la Tabla B-2. As:
a : 29*10
-3
; b : 0,2199*10
-5
; c : 0,5723*10
-8
; d : -2,871*10
-12
En unidades de kJ/mol*K
*29*10
-3
*(473,15-298,15) + 0,2199*10
-5
*[(498,15^2-298,15^2]/2 + 0,5723*10
-8
*[(498,15^3-
298,15^3]/3 - 2,871*10
-12
*[(498,15^4-298,15^4]/4} kJ/mol
*100 kg/s * (1 mol N
2
/0,028 kg) = 3571,43*(5,22 + 0,1484 +
0,1515 0,0303) kJ/s = 19605,72 kW
Ahora, en la Ecuacin A, se despeja flujo msico del vapor:
PROBLEMAS PROPUESTOS
1. Suponga que para un flujo de 100 kg/ s de oxgeno que
se va a calentar en un intercambiador de calor
alimentado con vapor saturado a 1,5 bar se fija el flujo
msico de vapor en 150 kg/h. A qu temperatura
saldr el oxgeno si entra al intercambiador a 25C?
(Rta: 410 K)
2. Dos corrientes de agua se mezclan para formar la
alimentacin a una caldera. La corriente, con un flujo
de 120 kg / min, entra a 30 C. Mientras que la
corriente 2, con un flujo de 175 kg/min, entra a 65C.
La caldera opera a 17 bar absolutos. Si el vapor
producido sale saturado a la presin de la caldera,
calcule la velocidad de transferencia de calor en kJ/
min, necesario para este proceso. (Rta: 7,6 kJ/min)
3. 20000 L/h de leche para fabricacin de queso se ha de
calentar desde 4C hasta 34C por medio de 3000 L/h
de agua caliente que entra a 50C. La densidad () y el
Cp de la leche son, aproximadamente, 1020 kg/m
3
y
3.95 KJ/kg.K Para el agua estos datos son: 990 kg/m
3
y
4.18 KJ/kg.K. Calcule la temperatura a la que sale el
agua del intercambiador. (Rta: 30,5 C)
4. 10 kmol de una mezcla de N
2
y H
2
, con una relacin
molar N
2
/H
2
= 1/ 3, se calientan desde 50C hasta
450C. Calclese el flujo de calor, en kJ, que es preciso
comunicar al gas a 1 atm para dicho calentamiento.
(Respuesta: 1,18*10
5
)
5. Se desea calentar desde 25C hasta 300C, a la presin
de 1 atm, una corriente que contiene un 10% en
volumen de CH
4
y un 90% de aire. Calclese la
velocidad de aporte de calor necesaria, expresada en
kW, para un flujo de gas de 2 m
3
/min medido en
condiciones normales. (Respuesta: 12.65)
6. Un gas natural que contiene un 95% en moles de
metano y el resto de etano se quema con un 25% de
aire en exceso. El gas de combustin sale del horno a
900C y 1 atm, enfrindose posteriormente en un
cambiador de calor hasta 500C. Tomando como base
de clculo 100 moles del gas natural que alimenta el
horno, calclese la cantidad de calor (kJ) que se debe
retirar del gas en el cambiador de calor para efectuar el
enfriamiento indicado. (Respuesta: 1.90.10
4
)
7. 10 kmol/h de una corriente gaseosa, cuya composicin
es 80 mol % de CO, 15 mol % de H
2
y 5 mol % de N
2
, se
calienta, a presin constante de 1 atm, desde 50C
hasta 275C mediante una resistencia elctrica situada
en el interior del tubo por el que circula el gas.
Calclese la potencia elctrica, en kW, que es preciso
comunicar a la resistencia. (Respuesta: 18,45)
BIBLIOGRAFA
Balances de materia y energa. Reklaitis, captulos
6 y 7.
Principios elementales de los procesos qumicos.
Felder, Captulos 7 y 8.
Vous aimerez peut-être aussi
- Procesosbio - AbsorciónDocument12 pagesProcesosbio - AbsorciónJazmin ZuñigaPas encore d'évaluation
- Introduccion Balance de Materia Y EnergiaDocument26 pagesIntroduccion Balance de Materia Y Energiamaii_toloza100% (1)
- KW P M H: Kpa KpaDocument5 pagesKW P M H: Kpa Kpaivan felipe erazo ceronPas encore d'évaluation
- Ejercicios Balance de MasaDocument8 pagesEjercicios Balance de MasaMelissa RPas encore d'évaluation
- Doc. BalancesDocument6 pagesDoc. BalancesOliver Moncada PinoPas encore d'évaluation
- Informe de FisicaDocument11 pagesInforme de FisicaJesus QuinteroPas encore d'évaluation
- AgroIndustrial EjercicioDocument7 pagesAgroIndustrial EjercicioAlex GomezPas encore d'évaluation
- Reacciones Monomoleculares Irreversibles de Primer OrdenDocument8 pagesReacciones Monomoleculares Irreversibles de Primer OrdenIvan CruzPas encore d'évaluation
- Ejercicios Sobre Aplicacion de La Ecuacion General de Energia-BernoulliDocument3 pagesEjercicios Sobre Aplicacion de La Ecuacion General de Energia-BernoulliGilberto Salas Colotta100% (2)
- Tarea 5 Balance de Materia en Procesos No EstacionariosDocument3 pagesTarea 5 Balance de Materia en Procesos No EstacionariosANETH TREYSI SAVINA SALHUAPas encore d'évaluation
- Practica Calificada 2109Document2 pagesPractica Calificada 2109Miguel Angel Moncca BernalPas encore d'évaluation
- Guia Tema 1 Unidades y DimensionesDocument5 pagesGuia Tema 1 Unidades y DimensionesReynel A. Lugo100% (2)
- Diapositivas II Par. Calidad EstudiantesDocument320 pagesDiapositivas II Par. Calidad EstudiantesByron Geovanny LlangaPas encore d'évaluation
- Serie de Ejercicios de Flujo de Fluidos.Document2 pagesSerie de Ejercicios de Flujo de Fluidos.Paula ArzatePas encore d'évaluation
- Balance 21Document11 pagesBalance 21FL Margiory100% (1)
- Balance de Materia LactosaDocument17 pagesBalance de Materia LactosaKaren NietoPas encore d'évaluation
- 5.1 Problemas de EvaporadoresDocument14 pages5.1 Problemas de EvaporadoresJulio Cesar Cuzcano GonzalesPas encore d'évaluation
- Balance de Materia y EnergiaDocument4 pagesBalance de Materia y EnergiaYeik DávilaPas encore d'évaluation
- Prob #3.1 Balance de Mat Con ReaccionDocument7 pagesProb #3.1 Balance de Mat Con ReaccionCarlos Bravo RPas encore d'évaluation
- Ejercicios de OPUDocument10 pagesEjercicios de OPUEstudiante INGPas encore d'évaluation
- OPE1 Formulas Transp FluidosDocument4 pagesOPE1 Formulas Transp FluidosAres Yosely Saavedra DelgadoPas encore d'évaluation
- Serie (9.2) - BeDocument8 pagesSerie (9.2) - BeBenyi Custodio VasquezPas encore d'évaluation
- Raul Fernadezbaca BarrientosDocument5 pagesRaul Fernadezbaca BarrientosLlim Alany AbregPas encore d'évaluation
- Lab.9 Flujo Atravez de Un OrificioDocument17 pagesLab.9 Flujo Atravez de Un OrificioJosé Dolores Gutiérrez100% (1)
- Tema BM Estado No Estacionario Con RX - OkDocument29 pagesTema BM Estado No Estacionario Con RX - OkSoledad PadillaPas encore d'évaluation
- 5 Taller - 1ra Ley SCDocument2 pages5 Taller - 1ra Ley SCNelson RamirezPas encore d'évaluation
- PROCESOS INDUSTRIALES I Practica IDocument2 pagesPROCESOS INDUSTRIALES I Practica ISalvattore RCPas encore d'évaluation
- Homework 4Document3 pagesHomework 4jacqueline milagros de la cruz palominoPas encore d'évaluation
- Grupo 3, TAREA IV0..2.2.Document6 pagesGrupo 3, TAREA IV0..2.2.Netflix ProductsPas encore d'évaluation
- Tarea Preparatoria #1Document2 pagesTarea Preparatoria #1Esdras Benjamin Cotto Revolorio0% (1)
- Artículo Cientifico YogurtDocument37 pagesArtículo Cientifico YogurtMayra Dayana100% (1)
- Taller de QuimicaDocument1 pageTaller de QuimicaSilvana Torres GallegosPas encore d'évaluation
- Balance de MasaDocument10 pagesBalance de Masaclarkentr100% (1)
- PSICROMETRIADocument8 pagesPSICROMETRIAJacky V. HerbasPas encore d'évaluation
- Informe EvaporadoresDocument22 pagesInforme EvaporadoresLiliana Herrera BallesterosPas encore d'évaluation
- EJERCICIOSDocument2 pagesEJERCICIOSLeonardo CamposPas encore d'évaluation
- Balance de MateriaDocument11 pagesBalance de MateriaPablo Orellana TapiaPas encore d'évaluation
- TP EtilbencenoDocument3 pagesTP EtilbencenoFlorencia CapurroPas encore d'évaluation
- Sesión 03-Ecuación Química y Estequiometría 2022 IDocument21 pagesSesión 03-Ecuación Química y Estequiometría 2022 ILuis FernandoPas encore d'évaluation
- Lama GJADocument125 pagesLama GJAAnonymous eHy4sNcra8Pas encore d'évaluation
- Mno4-+ 8H + 5E - Mn2+ + 8H2O?: Fuente (S)Document5 pagesMno4-+ 8H + 5E - Mn2+ + 8H2O?: Fuente (S)melocoton123Pas encore d'évaluation
- Diagrama PsicrométricoDocument18 pagesDiagrama PsicrométricoGian Franco Isquierdo VelaPas encore d'évaluation
- Taller Balances 4 - Balances de Materia Sobre Unidades de ProcesoDocument2 pagesTaller Balances 4 - Balances de Materia Sobre Unidades de ProcesoMar ValenciaPas encore d'évaluation
- A Un Dispositivo Que Funciona en Regimen Estacionario Entra Vapor de Agua A 160bar y 560Document7 pagesA Un Dispositivo Que Funciona en Regimen Estacionario Entra Vapor de Agua A 160bar y 560Vanny PedrinPas encore d'évaluation
- Procesos y Sistemas de Compresión y ExpansiónDocument8 pagesProcesos y Sistemas de Compresión y ExpansiónMiguel VenegasPas encore d'évaluation
- Aplicación de Los Evaporadores Al Vacío en La IndustriaDocument10 pagesAplicación de Los Evaporadores Al Vacío en La IndustriaDamian ReyesPas encore d'évaluation
- Destilación Fraccionada - Método de MC Cabe ThieleDocument13 pagesDestilación Fraccionada - Método de MC Cabe ThieleMiguel Castillo LeyvaPas encore d'évaluation
- Universidad de GuayaquilDocument22 pagesUniversidad de GuayaquilLeiver JoelPas encore d'évaluation
- 3 BTL Screening de CepasDocument10 pages3 BTL Screening de CepasAlejandro CuetoPas encore d'évaluation
- UT3 Balance de Materia y EnergiaDocument7 pagesUT3 Balance de Materia y Energiathortu100% (1)
- Ecuacion Diferencial de ContinuidadDocument12 pagesEcuacion Diferencial de ContinuidadCristian Gonzáles OlórteguiPas encore d'évaluation
- Examen de Ingeniería de Procesos AgroindustrialesDocument2 pagesExamen de Ingeniería de Procesos AgroindustrialesJV JhonnyPas encore d'évaluation
- Balance de Masa y Energía para El Concentrado de Piña)Document20 pagesBalance de Masa y Energía para El Concentrado de Piña)Mario LiosPas encore d'évaluation
- Ejercicios de Balance de Energia FluidosDocument2 pagesEjercicios de Balance de Energia FluidosDayana AlvarezPas encore d'évaluation
- Balance Tansitorio y de EnergiaDocument3 pagesBalance Tansitorio y de EnergiasteffanyPas encore d'évaluation
- Examen TermoDocument19 pagesExamen TermoDora A. ParraguezPas encore d'évaluation
- Física 2 - Guía 7 - 1er Principio TermoDocument4 pagesFísica 2 - Guía 7 - 1er Principio TermoTamara FigueroaPas encore d'évaluation
- Problemas Tema 2Document2 pagesProblemas Tema 2José Rafael GuillénPas encore d'évaluation
- GUIA 8 de BALANCE de Energia Sin ReaccioDocument2 pagesGUIA 8 de BALANCE de Energia Sin ReaccioYesenia Yubi CHancco100% (1)
- Soluciones Ejercicios Guía de AprendizajeDocument13 pagesSoluciones Ejercicios Guía de AprendizajeJUAN ANDRÉS SANDOVAL HERRERAPas encore d'évaluation
- Guía 4a de Fluidos (Estática de Fluidos)Document2 pagesGuía 4a de Fluidos (Estática de Fluidos)JUAN ANDRÉS SANDOVAL HERRERAPas encore d'évaluation
- Guía 3 Mecánica de FluidosDocument2 pagesGuía 3 Mecánica de FluidosJUAN ANDRÉS SANDOVAL HERRERAPas encore d'évaluation
- Guía 6a Ecuación General de EnergíaDocument7 pagesGuía 6a Ecuación General de EnergíaJUAN ANDRÉS SANDOVAL HERRERAPas encore d'évaluation
- Guía 2 Mecánica de Fluidos Juan Sandoval HerreraDocument2 pagesGuía 2 Mecánica de Fluidos Juan Sandoval HerreraJUAN ANDRÉS SANDOVAL HERRERAPas encore d'évaluation
- Guía 1 Mecánica de Fluidos Juan Sandoval HerreraDocument2 pagesGuía 1 Mecánica de Fluidos Juan Sandoval HerreraJUAN ANDRÉS SANDOVAL HERRERAPas encore d'évaluation
- Gato HidráulicoDocument8 pagesGato HidráulicoJUAN ANDRÉS SANDOVAL HERRERAPas encore d'évaluation
- Ejercicios Resueltos de PsicrometríaDocument9 pagesEjercicios Resueltos de PsicrometríaJUAN ANDRÉS SANDOVAL HERRERA100% (4)
- Guía 9 de Balance de Masa y EnergíaDocument1 pageGuía 9 de Balance de Masa y EnergíaJUAN ANDRÉS SANDOVAL HERRERAPas encore d'évaluation
- Tablas de Propiedades Termodinámicas para Balance de EnergíaDocument25 pagesTablas de Propiedades Termodinámicas para Balance de EnergíaJUAN ANDRÉS SANDOVAL HERRERAPas encore d'évaluation
- Guía 2 Balance de Masa Juan Sandoval HerreraDocument2 pagesGuía 2 Balance de Masa Juan Sandoval HerreraJUAN ANDRÉS SANDOVAL HERRERAPas encore d'évaluation
- Guía 6b Balance de Masa Juan Sandoval HerreraDocument2 pagesGuía 6b Balance de Masa Juan Sandoval HerreraJUAN ANDRÉS SANDOVAL HERRERAPas encore d'évaluation
- Guía 5b Balance de Masa Juan Sandoval HerreraDocument1 pageGuía 5b Balance de Masa Juan Sandoval HerreraJUAN ANDRÉS SANDOVAL HERRERAPas encore d'évaluation
- Guía 4 Balance de Masa Juan Sandoval HerreraDocument3 pagesGuía 4 Balance de Masa Juan Sandoval HerreraJUAN ANDRÉS SANDOVAL HERRERAPas encore d'évaluation
- Guia 7Document6 pagesGuia 7tufu4747Pas encore d'évaluation
- TRABAJO GRUPAL SensoresDocument5 pagesTRABAJO GRUPAL SensoresNieves Sihomara Mendoza LarreaPas encore d'évaluation
- ANEXO - CIENCIA - 15 y 17 Nov. Plano Inclin. y Palanca-FólderDocument3 pagesANEXO - CIENCIA - 15 y 17 Nov. Plano Inclin. y Palanca-FólderLeidy Chávez NarcisoPas encore d'évaluation
- Practica 1Document3 pagesPractica 1DnlUrgilesPas encore d'évaluation
- Marco Navarro Maldonado Control 3Document7 pagesMarco Navarro Maldonado Control 3alexPas encore d'évaluation
- Alternativas de Decisión Mediante Distribuciones de ProbabilidadDocument5 pagesAlternativas de Decisión Mediante Distribuciones de ProbabilidadEdgard Alberto Lugo SolorzanoPas encore d'évaluation
- Maquinas EmparalelamientoDocument5 pagesMaquinas EmparalelamientoDiego Velasquez AlbanPas encore d'évaluation
- Arrancador SuaveDocument13 pagesArrancador SuavelluchitoPas encore d'évaluation
- Avance InstrumentaciónDocument23 pagesAvance Instrumentaciónarmando palacinPas encore d'évaluation
- 2 Derivada de Producto y CocienteDocument9 pages2 Derivada de Producto y CocienteJosé Rafael Castro FernándezPas encore d'évaluation
- Lab-Informe N°5Document10 pagesLab-Informe N°5Alejandro Treneman20% (5)
- Guia Ejercicios FlotacionDocument12 pagesGuia Ejercicios Flotacionjvchique100% (2)
- Guía BUM Semana 7Document12 pagesGuía BUM Semana 7Derek Benigno Rojas GarciaPas encore d'évaluation
- 1.trabajo Individual T.C.MDocument5 pages1.trabajo Individual T.C.MChristian0% (1)
- PC01 - Mecanica de Fluidos 13990Document3 pagesPC01 - Mecanica de Fluidos 13990Harold AranaPas encore d'évaluation
- Códigos de Falla Sistemas Obd2Document57 pagesCódigos de Falla Sistemas Obd2Joel Sierra100% (3)
- Tarea (Unidades y Valores de Viscosidad)Document1 pageTarea (Unidades y Valores de Viscosidad)Jasso JassoPas encore d'évaluation
- Sem 5Document4 pagesSem 5RONALD VILCA CACERESPas encore d'évaluation
- Modelo EgliDocument14 pagesModelo EgliOscar OrtizPas encore d'évaluation
- Cotizacion de Purificacion400garrafonesDocument4 pagesCotizacion de Purificacion400garrafonesAche Hector HernándezPas encore d'évaluation
- Material Clase Grado 10 B MatematicaDocument10 pagesMaterial Clase Grado 10 B Matematicaluis miguel galarcio pachecoPas encore d'évaluation
- Mega Man X2Document39 pagesMega Man X2Af BrhoaPas encore d'évaluation
- TaxonomiaDocument17 pagesTaxonomiaJose Gabriel Hernandez Felix100% (2)
- ConicasDocument18 pagesConicasAniRiveroPas encore d'évaluation
- Segunda Práctica Grupal - Resistencia de Materiales ADocument29 pagesSegunda Práctica Grupal - Resistencia de Materiales AObed Delgado TorresPas encore d'évaluation
- Materiales Bituminosos 2011 PDFDocument24 pagesMateriales Bituminosos 2011 PDFAngelica QuimbitaPas encore d'évaluation
- Practica DinámicaDocument2 pagesPractica DinámicaDulman ChávezPas encore d'évaluation
- Trabajo de Investigación Generador SíncronoDocument16 pagesTrabajo de Investigación Generador SíncronoYshtar Ramirez BurgueñoPas encore d'évaluation
- Tarea 4Document16 pagesTarea 4Eder ReloPas encore d'évaluation
- Ficha Tecnica m10s SPIRAX SARCODocument4 pagesFicha Tecnica m10s SPIRAX SARCOLuis Enrique Torres Tone0% (1)