Académique Documents
Professionnel Documents
Culture Documents
T0709 PDF
Transféré par
davinccicodeTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
T0709 PDF
Transféré par
davinccicodeDroits d'auteur :
Formats disponibles
N d'ordre : 3483
THSE
prsente
L'UNIVERSIT BORDEAUX 1
COLE DOCTORALE DES SCIENCES CHIMIQUES
par Magali MACCARIO
Ingnieur de lEcole Nationale Suprieure dIngnieur de Caen (ENSICAEN)
POUR OBTENIR LE GRADE DE
DOCTEUR
SPCIALIT : PHYSICO-CHIMIE DE LA MATIERE CONDENSEE
*********************
Caractrisation de nanomatriaux C-LiFePO
4
optimiss pour matriaux
dlectrode positive pour batteries lithium ion. Dtermination du
mcanisme de dsintercalation / intercalation du lithium partir de ces
matriaux.
*********************
Soutenue le : 30 novembre 2007
Aprs avis de :
M. C. JULIEN Ingnieur de Recherche - INSP, Paris Rapporteur
M. D. GUYOMARD Directeur de Recherche IMN, Nantes Rapporteur
Devant la commission d'examen forme de :
M. C. MASQUELIER Professeur LCRS, Amiens Prsident
M. C. JULIEN Ingnieur de Recherche - INSP, Paris Rapporteur
M. D. GUYOMARD Directeur de Recherche IMN, Nantes Rapporteur
M
me
L. CROGUENNEC Charge de Recherche ICMCB, Bordeaux 1 Examinateur
M. C. DELMAS Directeur de Recherche ICMCB, Bordeaux 1 Examinateur
M. F. LE CRAS Ingnieur CEA CEA, Grenoble Examinateur
M. L. SERVANT Professeur ISM, Bordeaux 1 Examinateur
- 2007
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
A ma famille,
A tous ceux qui me sont chers.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Remerciements
Ce travail a t ralis au sein du Groupe "Energie : Matriaux pour Batteries" dans les
locaux de lInstitut de Chimie de la Matire Condense de Bordeaux, dirig successivement par
Monsieur le Professeur Jean Etourneau puis par Monsieur Claude Delmas, et dans ceux de
lEcole Nationale Suprieure de Chimie et de Physique de Bordeaux, dirige par Monsieur le
Professeur Bernard Clin puis par Monsieur le Professeur Franois Cansell, quils soient
remercis pour laccueil quils mont rserv.
Dans un premier temps, je tiens exprimer toute ma gratitude Monsieur le Professeur
Christian Masquelier du Laboratoire de Ractivit et Chimie des Solides dAmiens de mavoir
fait lhonneur de prsider mon jury de thse. Je tiens galement remercier Monsieur Dominique
Guyomard, Directeur de Recherche lInstitut des Matriaux de Nantes, ainsi que Monsieur
Christian Julien, Ingnieur de Recherche lInstitut des Nano-Sciences de Paris, de mavoir fait
lhonneur de juger ce travail en tant que rapporteurs. Je les remercie tout comme Monsieur le
Professeur Laurent Servant pour leur analyse dtaille et leurs questions pertinentes sur ce
travail.
Je remercie Monsieur Claude Delmas, Directeur de Recherche au CNRS, qui a dirig ce
travail de thse paralllement son statut de Directeur de lICMCB, pour les discussions trs
enrichissantes sur les phosphates et le mcanisme "Domino-cascade".
Comment ne pas exprimer toute ma gratitude Madame Laurence Croguennec, Charge
de Recherche au CNRS, qui a co-encadr cette thse. Merci elle pour son investissement dans
ces travaux car comme moi elle dcouvrait le monde merveilleux des phosphates. Quelle soit
remercie pour le grand intrt quelle a manifest pour ce travail et la rigueur dont elle a fait
preuve tout au long de ces annes.
Je remercie galement Monsieur Frdric Le Cras, Ingnieur au CEA Grenoble, co-
financeur de cette thse, pour les discussions et laccueil quil ma rserv au LITEN.
Mes remerciements sadressent galement Monsieur le Professeur Alain Levasseur pour
ses conseils aviss.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Je tiens galement remercier chaleureusement Monsieur Alain Wattiaux, Ingnieur de
Recherche au CNRS, pour son implication, sa disponibilit et sa gentillesse pour raliser les
analyses Mssbauer mais galement pour les discussions trs enrichissantes qui ont suivi.
Je remercie sincrement Monsieur Franois Weill, Charg de Recherche au CNRS, pour
les longues et fastidieuses journes passes au Microscope au CREMEM. Ca na pas t
toujours facile de trouver LA cristallite et de bien lorienter, car certaines dentre elles ny ont
pas mis du leur !!!! Malgr cela, merci encore pour les jolies photos et aussi les discussions
cristallo qui ont suivi.
Je tiens exprimer toute ma gratitude Messieurs Bernard Desbat, Michel Couzi,
Directeurs de Recherche au CNRS des laboratoires CBMN et ISM, et Monsieur le Professeur
Laurent Servant (ISM-Universit Bordeaux 1) pour leur collaboration en spectroscopie Infra
Rouge et Raman et les prcieuses discussions qui sen sont suivies. Je tiens galement leur
adresser mes sincres remerciements pour leur gentillesse et leur disponibilit de tous les instants.
Que Messieurs Jean-Luc Bruneel et David Talaga, Ingnieurs dtude lISM, ainsi que
Monsieur Thierry Tassaing, Charg de Recherche au CNRS soient vivement remercis pour la
formation la spectroscopie Raman et au lointain Infra Rouge quils mont prodigu.
Mes plus sincres remerciements sadressent galement Monsieur Rmi Ddryvre,
Matre de Confrences lUniversit de Pau et des Pays de lAdour, ainsi qu Madame
Danielle Gonbeau, Directeur de Recherche au CNRS, pour le temps pass pour raliser les
analyses de Spectroscopie XPS et les commentaires aviss qui ont suivi
Que Monsieur Sylvain Franger, Matre de Confrences lUniversit Paris XI, soit
vivement remerci pour sa collaboration en spectroscopie dimpdance lectrochimique.
Mes remerciements sadressent galement tous les membres de lICMCB qui mont aid
dans ce travail et plus particulirement Eric Lebraud, Stanislav Pechev, Pierre Graverau pour
leur gentillesse, leur collaboration pour la diffraction des Rayons X, Olivier NGuyen pour son
aide prcieuse pour les manipulations de SQUID, Rodolphe Decourt pour les mesures de
conductivits lectroniques, Bertrand Guillaume, Ludovic Pezat et Loc Le Goff de lAtelier de
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
lICMCB pour laide la conception et la ralisation de la cellule lectrochimique DRX
in-situ. Un grand Merci galement Stphane Toulin pour sa disponibilit et son aide prcieuse
en matire de bibliographie.
Je tiens galement adresser mes remerciements les plus sincres Madame Carole
Bourbon pour son aide permanente lors de mes diffrents sjours au CEA Grenoble. Je tiens
galement saluer amicalement les personnes que jai crois Grenoble ; Djamel, Hlne,
Sverine, Nelly, cette liste ntant pas exhaustive.
Ces remerciements seraient incomplets si jomettais de remercier tous les membres du
groupe Ionique du Solide (YoNick pour les intimes ) devenu maintenant le groupe
GEMBatt. Je remercie chaleureusement Cathy pour sa gentillesse, les conversations du mercredi
aprs-midi au MEB et son aide technique. Merci galement Sabine pour les discussions la
pause caf ou la pause dans le bureau microbatteries. Je tiens galement remercier
sincrement les permanents du groupe pour leur aide, leur soutien et leur gentillesse au cours de
ces annes, alors merci du fond du cur Laurence, Philippe V., Liliane, Franois, Lydie (ou
plutt LC, PV, LD, FW et LB (a vous voque quelque chose ?) moi oui, je noublierai pas
IMLB 2006 et les vnements divers et varis qui nous ont tant fait rire), Philippe D., Dany,
Michel, Alain et Nicole.
Merci galement aux diffrentes personnes qui ont particip la vie du groupe. Je tiens
donc remercier les plus anciens comme Frdric Tournadre, sans qui mon intgration dans le
groupe aurait t beaucoup plus difficile, Marie-Hlne et Christoph, pour sa gentillesse. Je
noublierai pas non plus nos amis japonais Shinichi et Kazuyuki (Merci pour les Origamis) ni
indiens Arya, Parvati et Gowda (il ne manquerait pas un indien, non je ne vois pas !!!).
Merci tous les stagiaires, doctorants et post doctorants qui ont partag la vie du
groupe : les MAV (vous tes des voisins de boite gants trs bruyants mais tellement sympa !!!),
Gal et Mickal (les stagiaires presque parfaits enfin surtout le premier!!!), Alexandrine, Pierre
et Emilie : les fameux nordistes, Mava (une super stagiaire qui est devenue une super thsarde),
Jessica, Khiem, Jrmy (promis je vais te rendre tes post-it), Adrien (ah la fameuse addition aux
Provinces !!), Nicolas (courage avec les phosphates, tu verras cest sympa au final !!!), Benot A
(ce fut un plaisir de partager le bureau avec toi, merci de ton aide et de ton soutien sans
faille), Alexandra (merci pour les potins, tas du lourd ? courage pour la suite ) & Benot F
(merci de ta confiance et bonne chance pour la suite ).
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Merci Maxime (pour ses visites instructives sur la vie lICMCB) et Romain.
Un grand mcerci (de Lalla) la MC (Maroc Connexion) : Ismal (le fameux Moulay), Chakir (le
Cheikh) & Nabil davoir partag et gay mcon bureau. Et oui je confirme la mcenthe a parfois
des feuilles roses Nest ce pas Mciskina ??
Comment ne pas voquer et remercier les plus anciens, mes amis :
Yohann, merci pour tes rcits de roller toute heure du jour et de la nuit,
Olivier, merci pour les discussions scientifiques ou pas et pour ton
aide,
Nicolas T, merci de nous avoir fait dcouvrir ce sport collectif individuel qui se
pratique en couple mixte avec un partenaire de mme sexe,
Cdric, merci pour ces parties mmorables de Trivial Pursuit et de Jungle Speed, pour les
Chazel Angels et pour tout ce que tu as fait pour moi,
Astrid, mon allemande prfre, merci pour ces deux annes au
labo inoubliables (mais aussi pour les annes qui ont suivi !!!),
pour tes rponses aux questions vertes au Trivial, pour les portes
ouvertes de Loupiac, pour les soires diverses et varies,
Graldine, toujours de bonne humeur et prte remonter le moral, merci pour les
pauses dans ton bureau, tes histoires (parisiennes !!!) du midi et le rsum des
programmes tls pas toujours trs intellectuels,
Myriam, merci pour tout, tu le sais je noublierai jamais nos derniers mois de
thse et tes visites dencouragement et de soutien. Je noublierai pas non plus
ton soutien sans faille un fameux jour doctobre et puis les jours (lanne) qui
ont suivi. MERCI.
MERCI tous davoir partag ces annes de thse !!!!
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Table des matires
Magali Maccario 30 novembre 2007
i
TABLE DES MATIERES
CHAPITRE I 1
INTRODUCTION GENERALE 1
I-1 Gnralits 1
I-2 Matriaux structure lamellaire 2
I-3 Matriaux charpente polyanionique 4
Bibliographie du Chapitre I 12
CHAPITRE II 19
METHODES ET TECHNIQUES EXPERIMENTALES 19
II-1 Dosages 19
II-1-1 Dosages chimiques 19
II-1-2 Analyses par Spectroscopie Mssbauer (en collaboration avec Alain
Wattiaux, ICMCB) 19
II-2 Caractrisations structurales 21
II-2-1 Diffraction des rayons X (DRX) 21
II-2-2 Diffraction des neutrons (DN) (en collaboration avec Emmanuelle
Suard, ILL - Grenoble) 22
II-2-3 Affinement structural par la mthode de Rietveld 23
II-2-3-a Full pattern matching (ou mthode de Le Bail) 23
II-2-3-b Mthode de Rietveld 24
II-3 Caractrisations lectrochimiques 25
II-3-1 Fonctionnement dune batterie lithium ion 25
II-3-2 Elaboration de batteries au lithium de laboratoire 27
II-4 Caractrisations physico-chimiques et texturales 29
II-4-1 Microscopie Electronique Balayage (MEB) 29
II-4-2 Mesures de surface spcifique par la mthode de B. E. T. 29
II-4-3 Mesures magntiques 29
II-4-4 Conductivit lectronique 30
II-4-5 Microscopie Electronique Transmission Haute Rsolution (MET-HR)
(en collaboration avec Franois Weill, ICMCB - CREMEM - Talence) 30
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Table des matires
Magali Maccario 30 novembre 2007
ii
II-4-6 Spectroscopie infrarouge (en collaboration avec Bernard Desbat,
CBMN - Pessac ; Laurent Servant et Thierry Tassaing, ISM - Talence) 30
II-4-7 Microspectroscopie Raman (en collaboration avec Bernard Desbat
CBMN - Pessac ; Laurent Servant et Michel Couzi, ISM - Talence) 32
II-4-8 Spectroscopie XPS (en collaboration avec Rmi Ddryvre et Danielle
Gonbeau, IPREM/ECP - Pau) 33
Bibliographie du Chapitre II 34
CHAPITRE III 35
ETUDE PRELIMINAIRE DE LA SYNTHESE DES MATERIAUX C-LIFEPO
4
: EFFET DU RAPPORT
NOMINAL LI/FE SUR LES PROPRIETES ELECTROCHIMIQUES EN BATTERIES AU LITHIUM
35
III-1 Synthse 36
III2 Analyses physico-chimiques 37
III-2-1 Caractrisation par Diffraction des Rayons X 37
III-2-2 Dosages chimiques 39
III2-3 Dosages redox par spectroscopie Mssbauer 40
III3 Mesures de conductivit lectronique 43
III4 Caractrisation lectrochimique 45
III5 Caractrisations morphologiques 47
III-6 Conclusions 49
Bibliographie du Chapitre III 50
CHAPITRE IV 51
INFLUENCE DES CONDITIONS DES SYNTHESE SUR LES PROPRIETES PHYSICO-CHIMIQUES,
MORPHOLOGIQUES ET ELECTROCHIMIQUES DE MATERIAUX DE STRUCTURE OLIVINE
LIFEPO
4
51
IV-1 Synthse des matriaux 52
IV-2 Caractrisations physico-chimiques 53
IV-2-1 Diffraction des rayons X 53
IV-2-2 Analyses chimiques 53
IV-2-3 Analyses par spectroscopie Mssbauer 55
IV-3 Caractrisations structurales : dtermination de la distribution cationique
58
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Table des matires
Magali Maccario 30 novembre 2007
iii
IV-3-1 Diffraction des rayons X 58
IV-3-2 Diffraction des neutrons 62
IV-3-2-a Prsence dions lithium dans le site du fer 62
IV-3-2-b Echange cationique entre les ions fer et lithium 62
IV-4 Caractrisations magntiques 64
IV-5 Mesures de conductivit lectronique 66
IV-6 Caractrisations par spectroscopie infrarouge 67
IV-7 Caractrisation par spectroscopie Raman 72
IV-8 Caractrisations texturales 80
IV-8-1 Microscopie Electronique Balayage 80
IV-8-2 Microscopie Electronique Transmission 80
IV-8-3 Mesure de surface spcifique 83
IV-9 Caractrisations lectrochimiques 83
IV-9-1 Cyclages continus rgime constant 83
IV-9-2 Cyclages lectrochimiques avec variation du rgime de cyclage
86
IV-9-2-a Cyclage en puissance n1 86
IV-9-2-b Cyclage en puissance n2 88
IV-10 Conclusions 90
Bibliographie du Chapitre IV 92
CHAPITRE V 95
CARACTERISATION DU MATERIAUX LIFEPO
4
AU COURS DU CYCLAGE ELECTROCHIMIQUE
EN BATTERIES AU LITHIUM 95
PARTIE A : Etude du mcanisme de dsintercalation / intercalation du lithium dans
LiFePO
4
au cours du cyclage lectrochimique en batteries au lithium 98
A-V-1 Etude par diffraction des rayons X dlectrodes rcupres au cours du
premier cycle lectrochimique des cellules LiFe
800-fast
98
A-V-1-1 Etude par diffraction des rayons X 98
A-V-1-2 Etude structurale des matriaux obtenus au cours du premier
cycle lectrochimique . 103
A-V-1-2-a Etude structurale des compositions Li
~0.39
FePO
4
et
Li
~0.38
FePO
4
obtenues respectivement en charge et en dcharge 104
A-V-1-2-b Etude structurale gnrale des diffrentes compositions obtenues
en charge ou en dcharge 107
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Table des matires
Magali Maccario 30 novembre 2007
iv
A-V-2 Etude par spectroscopie Mssbauer de matriaux C-Li
x
FePO
4
obtenus au cours de la premire charge lectrochimique des cellules
LiFe
800-fast
113
A-V-3 Etude par spectroscopie XPS dlectrodes enduites rcupres au cours
des premiers cycles lectrochimiques des cellules LiFe
575-fast
117
A-V-3-1 Etude des matriaux initiaux (poudre et lectrode enduite)
117
A-V-3-2 Etude des matriaux C-Li
x
FePO
4
120
A-V-3-3 Etude de linterface lectrode / lectrolyte par XPS 123
A-V-4 Etude par MET - HR de matriaux C-Li
x
FePO
4
rcuprs diffrents
tats de charge des cellules LiFe
800-fast
127
PARTIE B : tude de cyclages longue dure a temprature ambiante, 40C et 60C
134
B-V-1 Cyclages longue dure de cellules Li C LiFePO
4
(Fe
800-fast
)
diffrentes tempratures 134
B-V-1-1 Cyclages longue dure temprature ambiante (RT) 134
B-V-1-2 Cyclages longue dure 40C 138
B-V-1-3 Cyclages longue dure 60C 139
B-V-2 Etude par diffraction des rayons X des matriaux rcuprs aprs des
cyclages longue dure 141
B-V-2-1 Matriaux rcuprs aprs un cyclage temprature ambiante
(RT) 143
B-V-2-2 Matriaux rcuprs aprs un cyclage 40C 146
B-V-2-3 Matriaux rcuprs aprs un cyclage 60C 147
PARTIE C : Conclusions 150
Bibliographie du Chapitre VI 152
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Table des matires
Magali Maccario 30 novembre 2007
v
CHAPITRE VI 155
DESCRIPTION DU MECANISME DOMINO-CASCADE DE
DESINTERCALATION / INTERCALATION DU LITHIUM DANS LIFEPO
4
155
Bibliographie du Chapitre VI 163
CHAPITRE VII 165
CONCLUSION GENERALE 165
Bibliographie du Chapitre VII 168
Liste des figures 169
Liste des tableaux 175
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre I
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre I
Magali Maccario 30 novembre 2007 1
Chapitre I
Introduction gnrale
I-1 Gnralits.................................................................................................................... 1
I-2 Matriaux structure lamellaire.................................................................................. 2
I-3 Matriaux charpente polyanionique.......................................................................... 4
Bibliographie du Chapitre I ............................................................................................. 12
I-1 Gnralits
La matrise de lnergie, c'est--dire la production et le stockage dnergies nouvelles
et propres, est un des grands dfis futurs pour pallier dune part lpuisement des ressources
naturelles et dautre part lutilisation croissante de systmes sollicitant un apport dnergie
lectrique (appareils lectroniques portables : micro-ordinateurs, tlphones, camscopes,
vhicules lectriques et hybrides, ). Ces diffrents marchs ont ncessit le dveloppement
de diffrents systmes lectrochimiques comme les piles combustible, les super-
condensateurs et bien sr les batteries.
Depuis la dcouverte de la batterie acide - plomb par Gaston Plant (1859), dautres
batteries ont t dveloppes comme la batterie nickel cadmium fortement concurrence
depuis les annes 1990 par la batterie nickel mtal hydrure (Ni-MH) et la batterie
lithium - ion. Cette dernire prsente une capacit massique plus importante avec une toxicit
moindre. De plus, la batterie lithium ion prsente des nergies volumique et massique plus
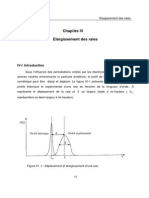
leves ainsi quun taux dautodcharge deux fois moindre que les batteries Ni-MH (cf.
Figure I-1) [1,2].
Les batteries lithium ion nous intressent particulirement, car elles dlivrent une
haute densit dnergie, permettant une autonomie suffisante, pour une masse et un
encombrement rduits, tout fait adapte aux attentes dun march en plein essor. La
premire batterie lithium ion (LiCoO
2
/ graphite) fut commercialise par SONY en 1992 [3]
et le march na cess de crotre depuis cette premire commercialisation. De quelques
centaines de milliers en 1995, la production mondiale de batteries lithium ion a atteint 500
millions en 2000 ( comparer avec les 1300 millions de batteries Ni-MH) puis 1700 millions
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre I
Magali Maccario 30 novembre 2007 2
en 2005 [4,5]. En 2006, le Japon, premier producteur mondial, a produit lui seul plus de
1200 millions de batteries lithium ion par an [6,7].
Avant de prsenter ltude de LiFePO
4
ralise dans le cadre de cette thse, ce premier
chapitre donne une prsentation gnrale et succincte des matriaux dlectrode positive pour
batteries lithium ion tudis depuis le dbut des annes 1980, en mettant laccent sur les
matriaux charpente polyanionique.
Figure I-1 : Comparaison des nergies volumiques et massiques de diffrents types de batteries
rechargeables.
I-2 Matriaux structure lamellaire
Depuis lmergence des batteries lithium et lithium-ion, plusieurs gnrations
dlectrodes positives ont successivement fait leur apparition. Les tudes des annes 80,
reprenant lide des matriaux lamellaires (TiS
2
) dvelopps par Whittingham [8] dans les
annes 70, se sont orientes vers les oxydes de type LiMO
2
(M = Co [9] et Ni [10]). LiCoO
2
est dailleurs commercialis depuis plus de 15 ans, bien que la dlithiation totale soit nfaste
la rversibilit du systme et la dure de vie. Il nest en effet possible de dsintercaler
rversiblement que 0.5 moles dions lithium de LiCoO
2
. Malgr des performances tout fait
satisfaisantes, les recherches se poursuivent dans le but de trouver un matriau dlectrode
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre I
Magali Maccario 30 novembre 2007 3
positive moins cher et moins toxique que LiCoO
2
et prsentant de meilleures performances
lectrochimiques.
Des tudes ont galement t menes sur dautres oxydes de mtaux de transition
lithis comme LiNiO
2
, LiMnO
2
, LiFeO
2
et LiMn
2
O
4
. LiNiO
2
a t tudi le plus
intensivement car il sest avr tre le plus adapt remplacer LiCoO
2
grce au faible cot du
nickel par rapport au cobalt, sa non toxicit, son potentiel de fonctionnement et sa
capacit rversible plus levs que ceux de LiCoO
2
. Plusieurs problmes ont nanmoins t
mis en vidence. Il est difficile de synthtiser le matriau LiNiO
2
stoechiomtrique : il y a en
effet la prsence systmatique dune faible quantit dions nickel dans le site du lithium
(Li
1-z
Ni
1+z
O
2
), ce qui est trs nfaste aux proprits lectrochimiques [10,11]. De plus, le
nickelate de lithium est trs instable ltat charg : laugmentation de la temprature induit
en effet une transformation de la phase lamellaire en phase spinelle, puis en phase de type
NaCl plus haute temprature, cette transformation structurale se produisant avec un
dgagement doxygne. Loxygne ainsi libr ragit exothermiquement avec les diffrents
composants de llectrolyte, provoquant une raction demballement au sein de la cellule
lectrochimique. Pour ces diffrentes raisons, LiNiO
2
na pas pu tre commercialis comme
matriau dlectrode positive pour batteries lithium ion [12,13].
Les composs lamellaires LiMnO
2
(deux varits structurales, lune de symtrie
orthorhombique et lautre lamellaire de symtrie monoclinique) et LiFeO
2
ont galement t
largement tudis du fait de leur faible cot. Mais, les trs faibles performances
lectrochimiques de LiFeO
2
et la transformation de LiMnO
2
en une phase de structure spinelle
au cours du cyclage lectrochimique [14-16], ont conduit un abandon de ces recherches.
Dautres matriaux de structure spinelle ont galement t tudis, comme LiMn
2
O
4
du fait de
son faible cot et de sa non toxicit, mais ce matriau prsente une dissolution du manganse
au cours du cyclage et donc une perte importante de capacit en cyclage [17-19]. Cependant,
ce matriau est commercialis pour de petites applications rechargeables.
Les recherches actuelles sur les oxydes lithis de mtaux de transition sorientent vers
des matriaux polysubstitus drivant de LiNiO
2
, de LiCoO
2
ou de LiMn
2
O
4
. Dans un premier
temps, les tudes se sont orientes vers la substitution partielle du cobalt au nickel dans
LiNiO
2
. Celle-ci a effectivement permis de renforcer le caractre lamellaire de la structure en
rduisant le taux dions nickel prsents dans lespace interfeuillet et damliorer les proprits
lectrochimiques [20,21]. Dautres co-substitutions par des cations tels que le magnsium, le
gallium ont t envisages afin de rduire notamment la perte de capacit au cours du
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre I
Magali Maccario 30 novembre 2007 4
cyclage lectrochimique [22-24]. La substitution de laluminium [25,26], du titane [27] ou du
manganse [28,29] au nickel a quant elle permis dobtenir une nette amlioration de la
stabilit thermique du matriau ltat charg. Ces rsultats ont encourag les bi-substitutions
du nickel par les lments prcdemment cits pour amliorer simultanment la stabilit
thermique ltat charg et les performances lectrochimiques du nickelate de lithium. Les
matriaux Li(Ni,Co,Al)O
2
[13,30-32] sont ceux qui ont finalement t retenus par lindustriel
Saft comme matriaux dlectrode positive dans leurs batteries pour toutes leurs applications
(spatiales, militaires, ). Les matriaux appartenant au systme ternaire NiO - Li
2
MnO
3
LiCoO
2
[33-37] font actuellement lobjet dintenses recherches. De la mme manire, pour
pallier la perte de capacit observe en cyclage pour LiMn
2
O
4
les spinelles substitues de type
LiMn
2-y
M
y
O
4
(M = Cr, Ni, Ti, Fe, ) sont largement tudies [38-42]. Ces matriaux
dlivrent des tensions leves et permettent ainsi dobtenir des nergies massiques et
volumiques trs intressantes. Cependant la ractivit haut potentiel avec llectrolyte
requiert un revtement de surface [43,44].
I-3 Matriaux charpente polyanionique
Les matriaux charpente polyanionique prsentent des structures tridimensionnelles
constitues de ttradres XO
4
n-
(X = P
5+
, Si
4+
, Mo
6+
, ) et de polydres MO
6
ou MO
4
(M = mtal de transition). Par comparaison aux oxydes lamellaires, on peut dire quun anion
O
2-
est remplac par un anion XO
4
n-
dans une structure charpente polyanionique.
Ces matriaux ont fait lobjet de plusieurs tudes grce leurs proprits remarquables
dchange et de conduction ionique. Dans un premier temps, ce type de structure
tridimensionnelle a t envisag pour des applications comme lectrolyte solide grce leur
capacit conduire rapidement les ions Na
+
, comme cela a t le cas pour Na
3
Zr
2
PSi
2
O
12
,
[45]. Ce matriau prsente une structure NASICON (NAtrium Super Ionic CONductor),
apparente celle du phosphate NaZr
2
(PO
4
)
3
[46]. Ce phosphate, dcrit dans les annes 60
par Hagman et al., cristallise dans la symtrie trigonale et sa structure consiste en un rseau
tridimensionnel de ttradres PO
4
et d'octadres ZrO
6
lis par les sommets. A lintrieur de ce
rseau 3D, de larges cavits, usuellement appeles sites M(1) et M(2), peuvent accueillir
dautres cations. Diverses proprits (cramiques faible coefficient de dilatation thermique,
luminescence, ) peuvent tre obtenues pour ce type de matriaux NASICON grce la fois
la souplesse des compositions envisages et la structure particulire de ces matriaux.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre I
Magali Maccario 30 novembre 2007 5
Lintercalation / dsintercalation rversible dun ion mobile dans ce type de composs
a t envisage, et par consquent leurs applications comme matriaux dlectrodes pour
batteries au lithium. Au milieu des annes 1980, les groupes de Delmas [47], Torardi [48] et
Goodenough [49] ont envisag lintercalation rversible, de manire chimique ou
lectrochimique, dun ion alcalin dans la structure polyanionique de Fe
2
(XO
4
)
3
(X = W ou
Mo) ; ces tudes ont montr une bonne rversibilit du processus
dintercalation / dsintercalation du lithium dans cette structure polyanionique, avec un
potentiel de 3 V vs. Li
+
/Li, intressant pour les applications lectrochimiques. A partir du
mme concept, Manthiram et al. ont tudi linsertion de lithium dans le compos Fe
2
(SO
4
)
3
de structure NASICON, celle-ci se fait selon une raction biphase un potentiel de 3.6 V vs.
Li
+
/Li [50]. Ces tudes ont permis de comprendre leffet inductif de lanion XO
4
n-
dans ce
type de structure polyanionique. En effet, dans ce type de matriaux structure
tridimensionnelle constitue doctadres MO
6
et de ttradres XO
4
lis par les sommets,
lenchanement X-O-M (M = mtal de transition) existe et la nature de llment X a une
influence sur le potentiel, via la covalence de la liaison X-O [50,51]. Lorsque la covalence de
la liaison X-O augmente celle de la liaison M-O diminue, entranant une diminution de la
densit lectronique autour du mtal de transition et donc une plus grande affinit pour les
lectrons. Cela a pour consquence une augmentation du potentiel du couple rdox du mtal
de transition. Une classification a pu tre tablie par J. B. Goodenough [52] : dans une
structure analogue, le potentiel du couple rdox du mtal de transition est, par exemple, plus
lev dans les matriaux phosphates que dans les matriaux sulfates. En effet, il existe un
dcalage de 0.8 V vs. Li
+
/Li entre le potentiel du couple redox Fe
3+
/Fe
2+
dans Li
3+x
Fe
2
(PO
4
)
3
et Li
3+x
Fe
2
(SO
4
)
3
[52].
Par la suite, de nombreuses tudes ont t menes sur les composs de structure
NASICON et plus particulirement, par les groupes de Goodenough, Delmas et Quarton [53-
57], sur lintercalation rversible de Li
+
ou Na
+
dans ces structures. Les premires tudes
lectrochimiques ont t menes au sein du laboratoire de Bordeaux sur les matriaux
A
1+x
Ti
2
(PO
4
)
3
(A = Li, Na) [53,54]. Elles ont montr lexistence dun plateau de potentiel, en
bon accord avec la raction biphase mise en vidence par diffraction des rayons X, et la
bonne rversibilit des ractions dintercalation / dsintercalation qui se produisent sans
rupture de liaisons Ti-O ou P-O.
Dautres tudes ont t menes plus rcemment pour obtenir des matriaux avec des
performances lectrochimiques plus attractives, on peut notamment citer le travail du groupe
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre I
Magali Maccario 30 novembre 2007 6
de Masquelier qui a tudi plus spcifiquement les compositions Li
3
Fe
2
(XO
4
)
3
(X = P, As)
[55,58,59], mais galement des compositions prsentant la coexistence du Ti et dun autre
lment de transition dans le site M (Fe ou Cr) [60]. Les travaux sur le matriau Li
3
Fe
2
(PO
4
)
3
ont surtout port sur loptimisation de la synthse (co-prcipitation, temps de broyage) en
relation avec les proprits lectrochimiques, sur le mme principe de ce qui est fait pour
LiFePO
4
; ils ont donn des rsultats intressants [58]. Bien que prsentant une bonne
rversibilit du processus dintercalation / dsintercalation du lithium, le potentiel moyen de
ce matriau nest cependant que de 2.7 V vs. Li
+
/Li. Pour des applications plus haut
potentiel (> 4 V vs. Li
+
/Li), dautres matriaux de structure NASICON ont t envisags par
les groupes de Masquelier et Nazar, comme Li
3
V
2
(PO
4
)
3
qui permet un fonctionnement entre
3.5 et 4.7 V vs. Li
+
/Li [59,61-63]. Son analogue monoclinique prsente de bonnes
performances lectrochimiques haut rgime [64]. Cependant leur faible conductivit
lectronique demeure pour ces matriaux un inconvnient majeur pour des applications en
batteries lithium-ion.
Depuis 1997 et les travaux de Goodenough et coll. [65], un nouveau matriau
dlectrode positive charpente polyanionique a montr de trs bonnes performances
lectrochimiques, il sagit du compos de structure olivine LiFePO
4
. A lorigine, le terme
olivine dsignait les minraux de la srie (Mg, Fe)
2
SiO
4
dont les deux compositions extrmes
sont Mg
2
SiO
4
et Fe
2
SiO
4
. Par extension ce terme dsigne aujourdhui les minraux de
structure identique, ce qui inclut les composs de type LiMPO
4
(M = Fe, Co, Mn, Ni).
La structure olivine de LiFePO
4
peut se dcrire par analogie avec la structure spinelle,
elles sont en effet toutes deux caractrises par la mme formule chimique gnrale AB
2
O
4
o
A et B occupent respectivement les sites ttradriques et octadriques dun empilement
datomes doxygne. La diffrence vient de lempilement : cubique faces centres pour la
structure spinelle mais hexagonal compact distordu pour la structure olivine. Contrairement
la structure spinelle, dans la structure olivine les sites octadriques sont occups par deux
types de cations (M
2+
et Li
+
), ce qui permet dtablir un ordre entre ces deux cations [65]. La
charpente est constitue par des octadres MO
6
et des ttradres PO
4
lis par des artes et des
sommets. Cet empilement tridimensionnel dlimite des tunnels dans les directions [010] et
[001] o se trouvent les ions lithium en sites octadriques. La structure orthorhombique de
LiFePO
4
est dcrite dans le groupe despace Pnma (cf. Figure I-2). Tous les ions sont situs
dans des positions particulires 4c sur le plan miroir, except le lithium qui est situ en
position 4a (sur un centre dinversion) et un des trois atomes doxygne qui est en position 8d.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre I
Magali Maccario 30 novembre 2007 7
Latome mtallique M est situ en site octadrique distordu doxygne. Un octadre MO
6
est
li quatre autres octadres MO
6
par partage de sommets, ce qui limite la conductivit
lectronique, mais galement cinq ttradres PO
4
dont un par une arte. Les couches
doctadres forment ainsi des damiers dans le plan bc. Ces couches sont relies par des
ttradres PO
4
, ces derniers jouent un rle de piliers dans la structure. Les polydres de
lithium LiO
6
forment des chanes selon laxe b par partage dartes dans le plan bc.
a
b
c
Figure I-2 : Vue en perspective de la structure olivine de LiFePO
4
dans le plan ac, les ions lithium tant
dans les tunnels parallles la direction b (octadres FeO
6
reprsents en marron, ttradres PO
4
reprsents en vert et atomes de lithium reprsents en bleu).
Diffrentes tudes ont montr que le mode de synthse, la morphologie des particules
ainsi que la conductivit de LiFePO
4
sont des facteurs trs importants pour lobtention de
bonnes performances lectrochimiques en batteries au lithium. Un matriau LiFePO
4
optimis
peut dlivrer une capacit rversible proche de la capacit thorique (~ 170 mAh/g) mme
des rgimes de cyclage lev temprature ambiante [66]. Pour obtenir de telles
performances, diffrentes tudes ont t entreprises et ont permis une amlioration simultane
du transport ionique et lectronique.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre I
Magali Maccario 30 novembre 2007 8
Lamlioration des proprits de conduction est obtenue en partie en diminuant la
taille des particules primaires (jusqu quelques dizaines de nanomtres) et en assurant une
distribution homogne de taille de particules [67-70]. Le contact entre les particules est donc
optimis et il y a ainsi une diminution du libre parcours moyen du lithium. Lextraction du
lithium mais galement la circulation des lectrons sont alors facilites. Le groupe de Armand
a le premier montr que lamlioration des proprits de transport lectronique pouvait
galement se faire par lajout dun agent conducteur la surface des particules [71]. Plusieurs
voies ont t envisages : ajout de particules mtalliques de cuivre ou dargent [72] ou
formation dun revtement de carbone [71,73-78]. Deux modes de synthse ont t explors
pour laborer le revtement carbon et former ainsi un matriau C-LiFePO
4
:
ajout et mlange intime du prcurseur carbon avec le matriau LiFePO
4
aprs la
synthse [65,73,79,80],
ajout dun prcurseur carbon par dcomposition dun compos organique : sucre
[70,80,81], rsorcinol [75,81] ou cellulose [66,82] ajouts comme additifs en dbut
de synthse ou actates / oxalates de fer ou de lithium utiliss comme prcurseurs
lors de la synthse de LiFePO
4
[67,70,83,84].
Les diffrents rsultats obtenus lors de ltude mene par Chen et al. [80] montrent que lajout
des prcurseurs de carbone avant la synthse et donc la formation du revtement carbon en
cours de synthse est plus efficace. Le carbone permet ainsi daugmenter les proprits
conductrices du matriau C-LiFePO
4
, mais galement dempcher la coalescence des grains et
dobtenir des nanoparticules de taille homogne. Cependant, la teneur en carbone doit tre
choisie de telle sorte favoriser une bonne capacit rversible tout en ne perdant pas en
densit dnergie volumique [75,80] ni en contact entre le matriau actif et llectrolyte.
La dsintercalation / intercalation du lithium se fait majoritairement selon un
mcanisme biphas entre la phase riche (LiFePO
4
) et la phase pauvre (FePO
4
) en lithium.
Nanmoins deux domaines de solution-solide ont t observs par Yamada et al. [85] en dbut
et fin de charge (dcharge). Ce rsultat est longtemps rest controvers, mais une tude
rcente mene par Meethong et al. [86] la confirm. Le mcanisme de dsintercalation du
lithium est souvent dcrit comme tant la croissance de FePO
4
au dtriment de LiFePO
4
selon
un procd cur-corce [65,83]. Cependant les groupes de recherche de Richardson et
Masquelier ont montr rcemment que le modle cur-corce ne permettait pas de dcrire la
raction de dsintercalation / intercalation du lithium de LiFePO
4
, ils ont propos un
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre I
Magali Maccario 30 novembre 2007 9
mcanisme impliquant la coexistence de domaines des deux phases dans une mme particule,
dont la proportion varie avec la composition de la phase dsintercale [87,88].
Dans la ligne de LiFePO
4
, dautres matriaux de structure olivine comme LiMnPO
4
et LiCoPO
4
ont t tudis, lintrt tant daugmenter le potentiel moyen du systme qui
serait respectivement de 4.1 et 4.8 V vs. Li
+
/Li. Les tudes de LiCoPO
4
sont trs limites
cause du manque de stabilit haut potentiel des lectrolytes utiliss classiquement [89-97].
Les tudes de LiMnPO
4
sont plus nombreuses mais malgr un potentiel intressant pour une
utilisation comme lectrode positive pour batteries lithium - ion, LiMnPO
4
prsente de fortes
diffrences avec LiFePO
4
qui lui sont ce jour trs prjudiciables [98-103]. En effet,
LiMnPO
4
est un isolant lectrique alors que LiFePO
4
est un semi-conducteur [102]. De plus,
ce compos au manganse prsente une cintique de raction trs lente mais aussi une forte
dformation du site octadrique des ions manganse due leffet Jahn-Teller [102] ainsi
quune plus forte variation de volume entre les phases extrmes (lithie et non lithie) par
rapport celle observe pour le compos au fer [100]. Nanmoins, des conditions de synthse
optimises (particules de 140 - 160 nm) permettent datteindre une capacit proche de la
valeur thorique rgime lent [99,100]. Un bon compromis entre les matriaux LiFePO
4
et
LiMnPO
4
serait les matriaux mixtes fer / manganse, c'est--dire LiFe
1-y
Mn
y
PO
4
. Ils
prsenteraient lavantage de combiner les bonnes proprits lectrochimiques (bonne
cyclabilit et capacit rversible leve) de LiFePO
4
avec un potentiel plus lev pour le
manganse (~ 4.1 V vs. Li
+
/Li) compar celui du fer (~ 3.5 V vs. Li
+
/Li) [100,104-114].
Yamada et al. ont montr que la composition LiFe
0.4
Mn
0.6
PO
4
est celle qui prsente les
proprits lectrochimiques les plus intressantes [106,107]. Durant cette thse, les matriaux
LiFe
1-y
Mn
y
PO
4
(0 y < 1) ont galement t tudis mais ne sont pas intgrs ce manuscrit,
ces rsultats feront lobjet dune publication [115].
Les bonnes performances obtenues pour les matriaux de type olivine et plus spcialement
pour LiFePO
4
ont suscit un engouement pour dautres matriaux polyanioniques de type
phosphates comme Fe
2-y
(PO
4
)(OH) (lipscombite) [116-118], FePO
4
.nH
2
O (0 n 2) avec
pour FePO
4
une structure diffrente de celle obtenue aprs dlithiation de LiFePO
4
[119-126],
LiMPO
4
F [12,83,127] ou LiVPO
4
F [128-130] ; les recherches sorientent galement vers les
silicates, arsniates, ... [58,131-136]. Tous ces matriaux prsentent lavantage dtre plus
srs que les matriaux dlectrode positive de type oxydes car ils mettent en jeu des couples
redox avec de plus faibles degrs doxydation et sont caractriss par des liaisons P-O trs
covalentes, ce qui prvient tout dgagement doxygne haut potentiel.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre I
Magali Maccario 30 novembre 2007 10
LiFePO
4
, qui prsente de nombreux avantages (faible cot, nocivit rduite pour
lenvironnement, stabilit thermique leve, capacit rversible leve, ), a fait lobjet de
nombreuses tudes et a aujourdhui atteint une optimisation telle que sa commercialisation
comme matriau dlectrode positive est engage. La socit PhosTech Lithium a en effet t
cre ds 2002 et commercialise actuellement un matriau C-LiFePO
4
pour un usage en
batteries lithium - ion. Dautres socits comme A123 et Valence Technology, Inc. (batterie
Saphion) commercialisent des accumulateurs avec LiFePO
4
comme matriau dlectrode
positive, en exploitant respectivement les tudes menes par Chiang et al. [137,138] et Barker
et al. [139,140]. Des appareils multimdia et doutillage fonctionnent dj avec des batteries
lithium - ion o LiFePO
4
est utilis comme matriau dlectrode positive. Dautres
consortiums se forment ou se sont forms pour tudier et peut tre par la suite commercialiser
des batteries de ce type pour des applications de plus grande taille comme des vhicules
hybrides.
Cette thse, co-finance par le CEA de Grenoble, a t entreprise pour permettre de
mieux comprendre les proprits structurales, physico-chimiques et lectrochimiques de
matriaux C-LiFePO
4
optimiss, dont le mode de synthse a t mis en place par le CEA.
Cette tude sest poursuivie dans le cadre dun projet PREDIT financ par lADEME et
nomm PVE Petit Vhicule Electrique, auquel jai pris part. Saft (Bordeaux) intervient
notamment dans le test des matriaux LiFePO
4
dvelopps dans le cadre du PVE comme
matriaux dlectrode positive pour des accumulateurs lithium-ion prototypes.
Aprs cette brve introduction sur les matriaux dlectrode positive et plus
particulirement les matriaux charpente polyanionique tudis actuellement, ce manuscrit
prsente les travaux mens pendant ma thse sur le systme LiFePO
4
de structure olivine. En
effet, ce systme polyanionique est celui qui prsente les performances lectrochimiques les
plus intressantes et les plus proches de la thorie lorsquil est synthtis dans des conditions
optimales. Dans ce contexte, les recherches menes au CEA ont permis dobtenir des
matriaux LiFePO
4
performants en batteries au lithium.
Le but de ce travail tait donc de relier les proprits structurales et physico-
chimiques de ces matriaux LiFePO
4
avec un revtement carbon leurs performances
lectrochimiques, afin de dterminer quel(s) facteur(s) joue(nt) un rle clef lobtention de
proprits optimales pour LiFePO
4
en tant qulectrode positive pour batteries au lithium.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre I
Magali Maccario 30 novembre 2007 11
Ce mmoire sarticule en quatre parties :
dans un premier temps, nous tudierons linfluence de la stoechiomtrie sur les
proprits structurales, physico-chimiques et lectrochimiques des matriaux C-LiFePO
4
.
dans un second temps, les caractrisations structurales (DRX, DN), physico-
chimiques (Mssbauer, SQUID, ), morphologiques ainsi que la caractrisation du
revtement carbon (conductivit lectronique, spectroscopie Raman) seront prsentes pour
une srie de matriaux C-LiFePO
4
synthtiss avec diffrents traitements thermiques et
diffrentes tempratures de synthse. Ce chapitre prsentera pour finir ltude de linfluence
des conditions de synthse sur les proprits lectrochimiques.
les matriaux dsintercals de type C-Li
x
FePO
4
seront tudis par DRX,
MET-HR, spectroscopie Mssbauer et XPS. Cette tude permettra de dcrire le mcanisme de
dsintercalation / intercalation du lithium dans ce type de matriaux. Ce chapitre mettra
aussi laccent sur une tude lectrochimique longue dure diffrentes tempratures.
le chapitre VI reviendra plus en dtail sur le mcanisme de
dsintercalation / intercalation du lithium dans LiFePO
4
.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre I
Magali Maccario 30 novembre 2007 12
Bibliographie du Chapitre I
1
A. De Guibert, L'actualit chimique, 3 (1998), 15-17.
2
M. B. Armand, in Materials for advanced Batteriesedited by D. W. Murphy, J. Broad
Lead and B. C. H. Steele (Plenum Press, New York, 1980), p. 145-161.
3
JEC Batt. Newsletter, 2 (1994), 31.
4
M. Broussely, L'actualit chimique, 1-2 (1994), 25.
5
H. Takeshita, in 8th International Seminar & Exhibit on Primary & Secondary
Batteries, Fort Lauderlale, Florida (USA), 2001).
6
ITE EXpress News, (2005).
7
http://www.bulletins-electroniques.com/rapports/smm06_061.htm, (2006).
8
B. G. Silbernagel, M. S. Whittingham, Mat. Res. Bull., 11 (1976), 29-36.
9
K. Mizushima, P. C. Jones, P. J. Wiseman, J. B. Goodenough, Materials Research
Bulletin, 15 (1980), 783-789.
10
R. Kanno, H. Kubo, Y. Kawamoto, T. Kamiyama, F. Izumi, Y. Takeda, M. Takano,
Journal of Solid State Chemistry, 110 (1994), 216-225.
11
A. Rougier, P. Gravereau, C. Delmas, Journal of the Electrochemical Society, 143
(1996), 1168-1174.
12
J. R. Dahn, E. W. Fuller, M. Obrovac, U. Von Sacken, Solid State Ionics, 69 (1994),
265-270.
13
M. Guilmard, L. Croguennec, D. Denux, C. Delmas, Chemistry of Materials, 15
(2003), 4476-4483.
14
T. Ohzuku, A. Ueda, T. Hirai, Chemistry Express, 7 (1992), 193-196.
15
M. M. Thackeray, P. J. Johnson, L. A. De Picciotto, P. G. Bruce, J. B. Goodenough,
Materials Research Bulletin, 19 (1984), 179.
16
L. Croguennec, P. Deniard, R. Brec, J. Electrochem. Soc., 144 (1997), 3323-3330.
17
J. M. Tarascon, D. Guyomard, Electrochimica Acta, 38 (1993), 1221-1231.
18
T. Takada, H. Hayakawa, H. Enoki, E. Akiba, H. Slegr, I. Davidson, J. Murray,
Journal of Power Sources, 82 (1999), 505-509.
19
J. M. Tarascon, E. Wang, F. K. Shokoohi, W. R. McKinnon, S. Colson, Journal of the
Electrochemical Society, 138 (1999), 2859.
20
C. Delmas, I. Saadoune, A. Rougier, Journal of Power Sources, 43-44 (1993), 595-
602.
21
E. Zhecheva, R. Stoyanova, Solid State Ionics, 66 (1993), 143-149.
22
C. Pouillerie, F. Perton, P. Biensan, J. P. Prs, M. Broussely, C. Delmas, Journal of
Power Sources, 96 (2001), 293.
23
Y. Nishida, K. Nakane, T. Satoh, Journal of Power Sources, 68 (1997), 561-564.
24
T. Ohzuku, T. Yanagawa, M. Kouguchi, A. Ueda, Journal of Power Sources, 68
(1997), 131-134.
25
T. Ohzuku, A. Ueda, M. Kouguchi, J. Electrochem. Soc., 142 (1995), 4033-4039.
26
H. Arai, S. Okada, Y. Sakurai, J. Yamaki, J. Electrochem. Soc., 144 (1997), 3117-
3125.
27
T. Ohzuku, Y. Makimura, Chem. Lett., (2001), 744.
28
S. H. Chang, S. Kang, S. Song, J. Yoon, J. Choy, Solid State Ionics, 86-88 (1996),
171-175.
29
Y. Koyama, N. Yabuuchi, I. Tanaka, H. Adachi, T. Ohzuku, Journal of the
Electrochemical Society, 151 (2004), A1545-A1551.
30
M. Guilmard, L. Croguennec, C. Delmas, Chemistry of Materials, 15 (2003), 4484-
4493.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre I
Magali Maccario 30 novembre 2007 13
31
Y. K. Lin, C. H. Lu, H. C. Wu, M. H. Yang, Journal Of Power Sources, 146 (1-2)
Special Iss. SI (2005), 594-597.
32
D. C. Li, Y. Sasaki, K. Kobayakawa, Y. Sato, Journal Of Power Sources, 157 (2006),
488-493.
33
N. Tran, L. Croguennec, C. Labrugre, C. Jordy, P. Biensan, C. Delmas, J.
Electrochem. Soc., 153 (2006), A261 -A269.
34
N. Tran, PhD thesis (2005), University Bordeaux I
35
M. G. Kim, H. J. Shin, J. H. Kim, S. H. Park, Y. K. Sun, J. Electrochem. Soc., 152
(2005), A1320-A1328.
36
B. J. Hwang, Y. W. Tsai, D. Carlier, G. Ceder, Chemistry of Materials, 15 (2003),
3676-3682.
37
T. H. Cho, S. M. Park, M. Yoshio, T. Hirai, Y. Hideshima, J. Power Sources, 142
(2005), 306-312.
38
C. Sigala, D. Guyomard, A. Verbaere, Y. Piffard, M. Tournoux, Solid State Ionics, 81
(1995), 167.
39
T. Ohzuku, S. Takeda, M. Iwanaga, Journal of Power Sources, 82 (1999), 90-94.
40
H. J. Choi, K. M. Lee, J. G. Lee, Journal of Power Sources, 103 (2001), 154-159.
41
K. Suryakala, G. P. Kalaignan, T. Vasudevan, Materials Chemistry and Physics, 104
(2007), 479-482.
42
W. Choi, A. Manthiram, Journal of the Electrochemical Society, 154 (7) (2007),
A614-A618.
43
J. Cho, G. B. Kim, H. S. Lim, C. S. Kim, S. I. Yoo, Electrochemical and Solid-State
Letters, 2 (1999), 607-609.
44
Y. K. Sun, K. J. Hong, J. Prakash, K. Amine, Electrochemistry Communications, 4
(2002), 344-348.
45
J. B. Goodenough, H. Y. P. Hong, J. A. Kafalas, Materials Research Bulletin, 11
(1976), 203.
46
L. O. Hagman, P. Kierkegaard, Acta Chemica Scandinavica, 22 (1968), 1822.
47
A. Nadiri, C. Delmas, R. Salmon, P. Hagenmuller, Revue de Chimie minrale (N
spcial Chimie Douce), 21 (1984), 537.
48
W. M. Reiff, J. H. Zhang, C. C. Torardi, Journal of Solid State Chemistry, 62 (1986),
231.
49
A. Manthiram, J. B. Goodenough, Journal of Solid State Chemistry, 71 (1987), 349.
50
A. Manthiram, J. B. Goodenough, Journal of Power Sources, 26 (1989), 403.
51
A. K. Padhi, K. S. Nanjundaswamy, C. Masquelier, J. B. Goodenough, Journal of the
Electrochemical Society, 144 (1997), 2581.
52
J. B. Goodenough, Molecular Crystals and Liquid Crystals, 311 (1998), 1.
53
A. Nadiri, C. Delmas, C.R. Acad. Sci., C304 (1987), 415.
54
C. Delmas, F. Cherkaoui, A. Nadiri, P. Hagenmuller, Materials Research Bulletin, 22
(1987), 631.
55
C. Masquelier, A. K. Padhi, K. S. Nanjundaswamy, J. B. Goodenough, Journal of
Solid State Chemistry, 135 (1998), 228.
56
K. S. Nanjundaswammy, A. K. Padhi, J. B. Goodenough, S. Okada, H. Ohtsuka, H.
Arai, J. Yamaki, Solid State Ionics, 92 (1996), 1.
57
O. Tillement, J. Angenault, J. C. Couturier, M. Quarton, Solid State Ionics, 53-56
(1992), 391.
58
M. Morcrette, C. Wurm, C. Masquelier, Solid State Sciences, 4 (2002), 239-246.
59
S. Patoux, C. Wurm, M. Morcrette, G. Rousse, C. Masquelier, Journal Of Power
Sources, 119 Special Iss. SI (2003), 278-284.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre I
Magali Maccario 30 novembre 2007 14
60
S. Patoux, G. Rousse, J. B. Leriche, C. Masquelier, Chemistry of Materials, 15 (2003),
2084-2093.
61
M. Morcrette, Y. Chabre, G. Vaughan, G. Amatucci, J. B. Leriche, S. Patoux, C.
Masquelier, J. M. Tarascon, Electrochimica Acta, 47 (2002), 3137-3149.
62
J. Gaubicher, C. Wurm, G. Goward, C. Masquelier, L. Nazar, Chemistry of Materials,
12 (2000), 3240.
63
S. C. Yin, P. S. Strobel, H. Grondey, L. F. Nazar, Chemistry of Materials, 16 (2004),
1456-1465.
64
H. Huang, S. C. Yin, T. Kerr, N. Taylor, L. F. Nazar, Advanced Materials, 14 (2002),
1525-1528,1519.
65
A. K. Padhi, K. S. Nanjundaswamy, J. B. Goodenough, Journal of the Electrochemical
Society, 144 (1997), 1188.
66
S. Franger, C. Bourbon, F. Le Cras, Journal of the Electrochemical Society, 151
(2004), A1024-A1027.
67
A. Yamada, S. C. Chung, K. Hinokuma, Journal of the Electrochemical Society, 148
(2001), A224.
68
C. Delacourt, P. Poizot, S. Levasseur, C. Masquelier, Electrochemical And Solid State
Letters, 9 (7) (2006), A352-A355.
69
G. Arnold, J. Garche, R. Hemmer, S. Strobele, C. Vogler, A. Wohlfahrt Mehrens,
Journal Of Power Sources, 119 Special Iss. SI (2003), 247-251.
70
S. Franger, F. Le Cras, C. Bourbon, H. Rouault, Journal Of Power Sources, 119
Special Iss. SI (2003), 252-257.
71
N. Ravet, S. Besner, M. Simoneau, A. Vallee, M. Armand, J. F. Magnan, (Hydro
Qubec, CA, 2002), Vol. EP1049182 p. 22
72
F. Croce, A. D. Epifanio, J. Hassoun, A. Deptula, T. Olczac, B. Scrosati,
Electrochemical And Solid State Letters, 5 (2002), A47-A50.
73
N. Ravet, Y. Chouinard, J. F. Magnan, S. Besner, M. Gauthier, M. Armand, Journal
Of Power Sources, 97-8 Special Iss. SI (2001), 503-507.
74
S. L. Bewlay, K. Konstantinov, G. X. Wang, S. X. Dou, H. K. Liu, Materials Letters,
58 (2004), 1788-1791.
75
H. Huang, S.-C. Yin, L. F. Nazar, Electrochemical and Solid-State Letters, 4 (2001),
A170.
76
A. Ait Salah, A. Mauger, K. Zaghib, J. B. Goodenough, N. Ravet, M. Gauthier, F.
Gendron, C. M. Julien, Journal Of The Electrochemical Society, 153 (9) (2006),
A1692-A1701.
77
K. Dokko, S. Koizumi, K. Kanamura, Chemistry Letters, 35 (2006), 338-339.
78
C. Benoit, C. Bourbon, P. Berthet, S. Franger, Journal Of Physics And Chemistry Of
Solids, 67 (5-6) Special Iss. SI (2006), 1265-1269.
79
R. Dominko, M. Gaberscek, J. Drofenik, M. Bele, J. Jamnik, Electrochimica Acta, 48
(2003), 3709-3716.
80
Z. H. Chen, J. R. Dahn, Journal Of The Electrochemical Society, 149 (2002), A1184-
A1189.
81
S. F. Yang, P. Y. Zavalij, M. S. Whittingham, Electrochemistry Communications, 3
(2001), 505-508.
82
S. Franger, F. Le Cras, C. Bourbon, H. Rouault, Electrochemical And Solid State
Letters, 5 (2002), A231-A233.
83
A. S. Andersson, B. Kalska, L. Haggstrom, J. O. Thomas, Solid State Ionics, 130
(2000), 41-52.
84
S. A. Needham, A. Calka, G. X. Wang, A. Mosbah, H. K. Liu, Electrochemistry
Communications, 8 (2006), 434-438.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre I
Magali Maccario 30 novembre 2007 15
85
A. Yamada, M. Yonemura, Y. Takei, N. Sonoyama, R. Kanno, Electrochemical And
Solid State Letters, 8 (1) (2005), A55-A58.
86
N. Meethong, H. Y. S. Huang, W. C. Carter, Y. M. Chiang, Electrochemical and Solid
State Letters, 10 (5) (2007), A134-A138.
87 L. Laffont, C. Delacourt, P. Gibot, M.Y. Wu, P. Kooyman, C. Masquelier, J.M.
Tarascon, Chem. Mater., 18 (2006), 5520.
88
G. Y. Chen, X. Y. Song, T. J. Richardson, Electrochemical And Solid State Letters, 9
(6) (2006), A295-A298.
89
K. Amine, H. Yasuda, M. Yamachi, Electrochemical and Solid-State Letters, 3 (2000),
178.
90
J. M. Lloris, C. P. Vicente, J. L. Tirado, Electrochemical And Solid State Letters, 5
(2002), A234-A237.
91
N. N. Bramnik, K. G. Bramnik, C. Baehtz, H. Ehrenberg, Journal Of Power Sources,
145 (2005), 74-81.
92
M. E. Rabanal, M. C. Gutierrez, F. Garcia Alvarado, E. C. Gonzalo, M. E. Arroyo de
Dompablo, Journal Of Power Sources, 160 (2006), 523-528.
93
S. Okada, S. Sawa, M. Egashira, J.-I. Yamaki, M. Tabuchi, H. Kageyama, T. Konishi,
A. Yoshino, Journal of Power Sources, 97-98 (2001), 430.
94
J. Wolfenstine, U. Lee, B. Poese, J. L. Allen, Journal Of Power Sources, 144 (2005),
226-230.
95
M. Nakayama, S. Goto, Y. Uchimoto, M. Wakihara, Y. Kitajima, Chemistry of
Materials, 16 (2004), 3399-3401.
96
N. N. Bramnik, K. G. Bramnik, T. Buhrmester, C. Baehtz, H. Ehrenberg, H. Fuess,
Journal of Solid State Electrochemistry, 8 (2004), 558-564.
97
N. N. Bramnik, K. Nikolowski, C. Baehtz, K. G. Bramnik, H. Ehrenberg, Chemistry
of Materials, 19 (2007), 908-915.
98
C. Delacourt, C. Wurm, P. Reale, M. Morcrette, C. Masquelier, Solid State Ionics, 173
(2004), 113-118.
99
N. H. Kwon, T. Drezen, I. Exnar, I. Teerlinck, M. Isono, M. Graetzel, Electrochemical
And Solid State Letters, 9 (6) (2006), A277-A280.
100
M. Yonemura, A. Yamada, Y. Takei, N. Sonoyama, R. Kanno, Journal Of The
Electrochemical Society, 151 (9) (2004), A1352-A1356.
101
G. H. Li, H. Azuma, M. Tohda, Electrochemical And Solid State Letters, 5 (2002),
A135-A137.
102
A. Yamada, M. Hosoya, S. C. Chung, Y. Kudo, K. Hinokuma, K. Y. Liu, Y. Nishi,
Journal Of Power Sources, 119 Special Iss. SI (2003), 232-238.
103
C. Delacourt, L. Laffont, R. Bouchet, C. Wurm, J. B. Leriche, M. Morcrette, J. M.
Tarascon, C. Masquelier, Journal Of The Electrochemical Society, 152 (5) (2005),
A913-A921.
104
J. Molenda, W. Ojczyk, K. Swierczek, W. Zajac, F. Krok, J. Dygas, R. S. Liu, Solid
State Ionics, 177 (2006), 2617-2624.
105
A. Yamada, S.-C. Chung, Journal of the Electrochemical Society, 148 (2001), A960.
106
A. Yamada, Y. Kudo, K.-Y. Liu, Journal of the Electrochemical Society, 148 (2001),
A747.
107
A. Yamada, Y. Kudo, K.-Y. Liu, Journal of the Electrochemical Society, 148 (2001),
A1153.
108
A. Yamada, Y. Takei, H. Koizumi, N. Sonoyama, R. Kanno, Applied Physics Letters,
87 (2005), NIL_548-NIL_550.
109
A. Yamada, Y. Takei, H. Koizumi, N. Sonoyama, R. Kanno, K. Itoh, M. Yonemura,
T. Kamiyama, Chemistry Of Materials, 18 (2006), 804-813.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre I
Magali Maccario 30 novembre 2007 16
110
A. Mauger, A. Ait-Salah, F. Gendron, M. Massot, K. Zaghib, C. Julien, in 210th ECS
Meeting (abstract 186, Cancun, Mexico, 2006).
111
J. Yao, S. Bewlay, K. Konstantionv, V. A. Drozd, R. S. Liu, X. L. Wang, H. K. Liu,
G. X. Wang, Journal Of Alloys And Compounds, 425 (2006), 362-366.
112
G. H. Li, Y. Kudo, K. Y. Liu, H. Azuma, M. Tohda, Journal of the Electrochemical
Society, 149 (2002), A1414-A1418.
113
G. H. Li, H. Azuma, M. Tohda, Journal of the Electrochemical Society, 149 (2002),
A743-A747.
114
N. N. Bramnik, K. G. Bramnik, K. Nikolowski, M. Hinterstein, C. Baehtz, H.
Ehrenberg, Electrochemical And Solid State Letters, 8 (8) (2005), A379-A381.
115
M. Maccario, L. Croguennec, A. Wattiaux, F. Le Cras, C. Delmas, to be submitted.
116
M. Dolle, S. Patoux, T. J. Richardson, Journal Of Power Sources, 144 (2005), 208-
213.
117
M. S. Whittingham, Y. N. Song, S. Lutta, P. Y. Zavalij, N. A. Chernova, Journal Of
Materials Chemistry, 15 (33) (2005), 3362-3379.
118
Y. N. Song, P. Y. Zavalij, N. A. Chernova, M. S. Whittingham, Chemistry Of
Materials, 17 (2005), 1139-1147.
119
S. F. Yang, Y. N. Song, P. Y. Zavalij, M. S. Whittingham, Electrochemistry
Communications, 4 (2002), 239-244.
120
C. Masquelier, P. Reale, C. Wurm, M. Morcrette, L. Dupont, D. Larcher, Journal Of
The Electrochemical Society, 149 (2002), A1037-A1044.
121
Y. N. Song, P. Y. Zavalij, M. Suzuki, M. S. Whittingham, Inorganic Chemistry, 41
(2002), 5778-5786.
122
Y. N. Song, S. F. Yang, P. Y. Zavalij, M. S. Whittingham, Materials Research
Bulletin, 37 (2002), 1249-1257.
123
K. Zaghib, C. M. Julien, Journal Of Power Sources, 142 (2005), 279-284.
124
R. G. Iyer, C. Delacourt, C. Masquelier, J. M. Tarascon, A. Navrotsky,
Electrochemical And Solid State Letters, 9 (2) (2006), A46-A48.
125
E. M. Bauer, C. Bellitto, G. Righini, M. Pasquali, A. Dell' Era, P. P. Prosini, Journal
Of Power Sources, 146 (1-2) Special Iss. SI (2005), 544-549.
126
F. Croce, D. E. A, P. Reale, L. Settimi, B. Scrosati, Journal Of The Electrochemical
Society, 150 (2003), A576-A581.
127
S. Okada, M. Ueno, Y. Uebou, J. Yamaki, Journal Of Power Sources, 146 (1-2)
Special Iss. SI (2005), 565-569.
128
J. Barker, R. K. B. Gover, P. Burns, A. Bryan, M. Y. Saidi, J. L. Swoyer, Journal Of
Power Sources, 146 (1-2) Special Iss. SI (2005), 516-520.
129
R. K. B. Gover, P. Burns, A. Bryan, M. Y. Saidi, J. L. Swoyer, J. Barker, Solid State
Ionics, 177 (2006), 2635-2638.
130
J. Barker, M. Y. Saidi, J. L. Swoyer, Journal of the Electrochemical Society, 150
(2003), A1394-A1398.
131
M. E. Arroyo de Dompablo, U. Amador, M. Alvarez, J. M. Gallardo, F. Garcia
Alvarado, Solid State Ionics, 177 (2006), 2625-2628.
132
A. Nyten, A. Abouimrane, M. Armand, T. Gustafsson, J. O. Thomas, Electrochemistry
Communications, 7 (2005), 156-160.
133
R. Dominko, M. Bele, M. Gaberscek, A. Meden, M. Remskar, J. Jamnik,
Electrochemistry Communications, 8 (2006), 217-222.
134
K. Zaghib, A. A. Salah, N. Ravet, A. Mauger, F. Gendron, C. M. Julien, Journal Of
Power Sources, 160 (2) Special Iss. SI (2006), 1381-1386.
135
A. Nyten, S. Kamali, L. Haggstrom, T. Gustafsson, J. O. Thomas, Journal Of
Materials Chemistry, 16 (23) (2006), 2266-2272.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre I
Magali Maccario 30 novembre 2007 17
136
Z. L. Gong, Y. X. Li, Y. Yang, Electrochemical and Solid State Letters, 9 (12) (2006),
A542-A544.
137
S. Y. Chung, J. T. Bloking, Y. M. Chiang, Nature Materials, 1 (2002), 123-128.
138
A. Hunt, W. Y. Ching, Y. M. Chiang, A. Moewes, Physical Review B, 7320 (2006),
NIL_225-NIL_234.
139
J. Barker, Y. Saidi, J. Swoyer, (Valence technology, Inc., US, 2003), p. 40 pp.
140
J. Barker, Y. Saidi, J. Swoyer, (Valence Technology, Inc. , 2002), p. 40 pp.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre II
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre II
Magali Maccario 30 novembre 2007
19
Chapitre II
Mthodes et Techniques Exprimentales
II-1 Dosages ..................................................................................................................... 19
II-2 Caractrisations structurales.................................................................................... 21
II-3 Caractrisations lectrochimiques............................................................................ 25
II-4 Caractrisations physico-chimiques et texturales..................................................... 29
Bibliographie du Chapitre II............................................................................................ 34
II-1 Dosages
II-1-1 Dosages chimiques
Les teneurs en ions Li, Fe et P prsentes dans les matriaux tudis ont t
dtermines par ICP (Inductively Coupled Plasma). La mise en solution se fait dans leau
rgale. Lincertitude relative est de 2 3 % sur la masse initialement pese. Le carbone a lui
t transform en CO
2
par traitement thermique haute temprature sous O
2
, puis sa teneur a
t dtermine par spectroscopie infrarouge. Lincertitude sur le taux de carbone est de
0.2 %. Les analyses ont t ralises par le Service Commun danalyse du CNRS de
Vernaison.
II-1-2 Analyses par Spectroscopie Mssbauer (en collaboration avec Alain Wattiaux,
ICMCB)
Le spectromtre en transmission utilis est de type HALDER acclration constante
mettant en uvre une source de
57
Co (matrice de Rhodium). Les chantillons, finement
broys, contiennent en moyenne 10 mg de fer par cm
2
. Pour ces concentrations, les effets
dlargissement des raies dus des phnomnes de saturation peuvent tre ngligs. Les
spectres ont t enregistrs 293 K. Deux modes de prparation ont t utiliss selon la nature
des matriaux : les poudres initiales de type C-LiFePO
4
ont t pastilles, tandis que les
matriaux dsintercals C-Li
x
FePO
4
ont t prpars en bote gants sous argon et
introduits dans un porte-chantillon tanche permettant de les prserver de latmosphre
extrieure lors de lacquisition du spectre Mssbauer.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre II
Magali Maccario 30 novembre 2007
20
Les paramtres hyperfins (dplacement isomrique ou chimique ( en mm.s
-1
),
lclatement quadrupolaire ( en mm.s
-1
)) dduits de laffinement des spectres exprimentaux
nous renseignent sur lenvironnement et la structure lectronique de latome sonde.
Le dplacement isomrique () est proportionnel la densit lectronique au niveau
du noyau entre la source et labsorbeur mais galement la variation relative R/R
(R = rayon nuclaire) au noyau nuclaire entre ltat excit et ltat fondamental. Sa
valeur renseigne sur la structure lectronique de latome de fer, savoir sur son tat
de valence, sa coordinence, sa covalence et son tat de spin. Dans tout ce travail, les
dplacements isomriques ont t rapports au fer 293 K.
Lclatement quadrupolaire () (couplage quadrupolaire) reprsente linteraction
entre le moment quadrupolaire du noyau tudi dans ltat excit et le gradient de
champ lectrique d la distribution asymtrique des charges lectriques qui
lentourent. Ce paramtre renseigne sur la dformation du site. Il est noter que le
gradient de champ lectrique dpend de deux contributions, lune provenant des
lectrons de valence du noyau tudi (contribution lectronique) et la seconde
prenant en compte linfluence des ions entourant le noyau sonde (contribution du
rseau). Ainsi, pour le noyau de fer trivalent (3d
5
) en configuration spin fort (HS)
situ dans un octadre idal, la couche demi remplie symtrique ne contribue pas
leffet quadrupolaire. Dans ce cas, seule la contribution des proches voisins externes
intervient. Les valeurs observes sont gnralement infrieures ou voisines de
1 mm.s
-1
. La valeur de nous renseigne alors sur la dformation du site lie aux
proches voisins. En revanche dans le cas du fer divalent (3d
6
4s
0
), il est ncessaire de
tenir compte des deux contributions (lectronique et de rseau). Gnralement, les
valeurs de peuvent tre assez leves jusqu 3 4 mm.s
-1
, lies une contribution
lectronique interne trs forte (1 lectron supplmentaire).
Hormis les paramtres hyperfins, la largeur mi-hauteur ( en mm.s
-1
) et/ou la
forme de la raie peuvent nous renseigner sur des phnomnes de distributions
dclatements quadrupolaires.
Deux mthodes daffinement ont t utilises lors de ce travail pour dterminer les
paramtres hyperfins des divers sites de fer en prsence au sein des composs tudis.
Une premire mthode de calcul permet dajuster les spectres laide de raies de profil
Lorentzien. A partir de ce calcul, la position, lamplitude et la largeur de chaque raie ont t
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre II
Magali Maccario 30 novembre 2007
21
affines. Cet affinement permet de dduire les paramtres hyperfins des diffrents sites du fer
prsents au sein du compos.
Un second mode de calcul permet de dpouiller les spectres en termes de distributions
dclatements quadrupolaires P() par la mthode de Hesse et Rubartsch [1]. Cette mthode
est souvent utilise pour des composs dsordonns pour lesquels une large distribution
denvironnements possibles existe. Ceci se traduit sur le spectre exprimental par des raies de
largeur importante et de forme pouvant scarter du profil Lorentzien. Pour ce calcul, la
valeur de la largeur de la raie mi-hauteur est fixe entre 0.20 et 0.30 mm.s
-1
. Les
dplacements isomriques imposs sont dduits de la premire mthode de calcul. A partir
de cet affinement, est extrait pour chaque site de fer un profil de distribution dclatements
quadrupolaires P(). Il permet de calculer la valeur moyenne de ainsi que la largeur de la
distribution, signature du dsordre pour chaque distribution considre.
Quelle que soit la mthode de calcul utilise pour interprter les spectres exprimentaux
le pourcentage relatif des divers sites de fer en prsence est affin.
II-2 Caractrisations structurales
II-2-1 Diffraction des rayons X (DRX)
Les diagrammes de diffraction des rayons X des matriaux ont t enregistrs sur un
diffractomtre Panalytical XPert Pro quip dune anticathode de cobalt ~ 1.79 (K
1
et
K
2
). Les conditions dacquisition sont diffrentes selon le type dchantillon (cf. Tableau
II-1). Contrairement une anticathode de cuivre, lanticathode de cobalt permet en effet de ne
pas exciter la fluorescence du fer.
Selon la ractivit des chantillons analyss, diffrents porte-chantillons ont t
utiliss. Les poudres initiales sont analyses dans des porte-chantillons classiques de
polycarbonate, alors que les matriaux dsintercals C-Li
x
FePO
4
, potentiellement sensibles
latmosphre extrieure, ont t placs dans des porte-chantillons dits hygroscopiques
qui sont totalement tanches pendant au moins 24 h et transparents aux rayons X. Les
lectrodes enduites C-Li
x
FePO
4
sont scotches sur le porte-chantillon aprs llimination
des sels de lithium par lavage au DMC (Carbonate de DiMthyle) et schage sous vide, tandis
que les poudres C-Li
x
FePO
4
sont arases uniformment.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre II
Magali Maccario 30 novembre 2007
22
Pour permettre laffinement des donnes de diffraction des rayons X par la mthode de
Rietveld, les diffractogrammes exprimentaux doivent tre de bonne qualit. Cela signifie une
optimisation des conditions dacquisition mais galement une prparation minutieuse de
lchantillon en vitant notamment une orientation prfrentielle des cristallites. Pour cela, les
poudres tamises 40 m au-dessus du porte-chantillon sont arases laide dune lame de
rasoir.
Tableau II-1 : Conditions dacquisition utilises pour chaque type dchantillon analys par diffraction
des rayons X.
Echantillons
Matriau
initial
Electrode
Electrode aprs
cyclage longue
dure
Filtre Fe Avant
Fentes de Soller 0.02 rad
Masque 10 mm
Fente antidiffusion 1 1 1/2
Fente de divergence 1 1 1/4
Domaine angulaire 5 120 15 75 15 75
Pas 0.0167 0.0167 0.0167
Dure du pas 2 s 12 s 12 s
Porte chantillon classique hygroscopique hygroscopique
II-2-2 Diffraction des neutrons (DN) (en collaboration avec Emmanuelle Suard,
ILL - Grenoble)
Les mesures ont t ralises sur le diffractomtre haute rsolution D2B de lILL
(Institut Laue-Langevin) avec une longueur donde de 1.595 . Les diagrammes de
diffraction des neutrons ont t enregistrs temprature ambiante dans le domaine angulaire
[0 - 160] par pas de 0.05. Un cylindre creux de vanadium de 8 ou 16 mm de diamtre selon
les chantillons et de 5 cm de hauteur a t utilis comme porte-chantillon. Les lments
comme le lithium et le fer prsents dans les chantillons tant absorbants en diffraction des
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre II
Magali Maccario 30 novembre 2007
23
neutrons, il est ncessaire de corriger la baisse dintensit induite par ce phnomne lors de
laffinement par la mthode de Rietveld. Ce terme est prsent dans le programme Fullprof [2]
sous la forme R o est le coefficient dabsorption linaire pour lchantillon et R le rayon
du porte-chantillon cylindrique de vanadium. est dfini par la relation suivante :
=
ai
i
i
n
V
n
avec n : nombre dunits formulaires par maille,
V : volume de la maille,
ai
: coefficient dabsorption atomique de llment i,
n
i
: nombre datomes i par motif lmentaire.
II-2-3 Affinement structural par la mthode de Rietveld
La structure des diffrents chantillons tudis dans ce manuscrit a t dtermine
partir de laffinement des diagrammes de diffraction des rayons X et des neutrons par la
mthode de Rietveld grce au programme Fullprof [2]. Cette mthode repose sur la
minimisation de la diffrence entre les intensits, y = f(2), observes et calcules, affectes
de leur poids statistique, par la mthode des moindres carrs. Laffinement est ralis en deux
tapes : full pattern matching puis Rietveld.
II-2-3-a Full pattern matching (ou mthode de Le Bail)
Les paramtres affins sont :
le fond continu estim par interpolation linaire entre les points pour lesquels aucune
contribution de pics nexiste,
les paramtres de maille,
les paramtres de profil des raies :
0
, X, U, V, W. Le profil des raies est dcrit par
une fonction pseudo-Voigt qui est une combinaison linaire des fonctions
gaussienne (G) et lorentzienne (L) : pV = L + (1-)G. Le facteur de forme , qui
dfinit la forme des pics entre les limites gaussienne ( = 0) et lorentzienne ( = 1),
varie avec langle de diffraction 2 selon la formule : =
0
+ X(2) o X prend en
compte lvolution du facteur de forme en fonction de langle 2. La largeur des
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre II
Magali Maccario 30 novembre 2007
24
raies (H) varie avec langle 2 selon la formule de Caglioti :
H = Utan + Vtan + W o U, V et W sont les coefficients de Caglioti.
II-2-3-b Mthode de Rietveld
Laffinement se poursuit en prenant en compte une hypothse structurale ; sont alors
introduits les positions atomiques de chaque atome, les taux doccupation des sites
cristallographiques et les facteurs de dplacement atomique isotrope, tout en fixant dans un
premier temps les paramtres de maille aux valeurs affines lors du full pattern matching.
Pour les donnes obtenues par diffraction des neutrons, on fixe galement dans un premier
temps les paramtres de profils U, V, W et aux valeurs obtenues en full pattern matching. A
la fin de laffinement tous ces paramtres sont affins. Pour les donnes obtenues par
diffraction des rayons X, on fixe les paramtres de profil V et W ceux dtermins pour
LaB
6
, matriau de rfrence utilis pour dterminer la fonction instrumentale du fait de sa trs
grande cristallinit. En effet, pour tenir compte des effets de microcontraintes (contribution
gaussienne) et de tailles (contribution lorentzienne), nous avons utilis la fonction dite de
Thompson-Cox-Hastings qui permet une meilleure prise en compte des diverses sources
dlargissement. Seuls les paramtres U et Y sont affins dans le cas dun modle isotrope.
Les positions atomiques de chaque lment sont successivement affines, puis si cela
est justifi les taux doccupation de chaque site et enfin les facteurs de dplacement atomique
isotrope ; la fin de laffinement, tous les autres paramtres (de profil, de maille, ) sont
librs. Laccord entre les diffractogrammes exprimental et calcul pour lhypothse
structurale considre est jug par les facteurs de reliabilit :
le facteur de profil pondr : R
wp
=
i
i i
i
i i i
obs y w
calc y obs y w
) (
)] ( ) ( [
o y
i
(obs) est lintensit observe pour un angle 2
i
,
y
i
(calc) est lintensit calcule pour langle 2
i
,
w
i
est le poids statistique de chaque intensit.
le facteur de Bragg : R
B
=
i
i
i
i i
obs I
calc I obs I
) (
) ( ) (
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre II
Magali Maccario 30 novembre 2007
25
o I
i
est lintensit intgre de la rflexion i.
R
B
est trs sensible aux variations dintensits des raies et des paramtres.
La courbe diffrence entre le profil exprimental et le profil calcul permet galement
de juger de la qualit de laffinement. Les carts-types donns dans le fichier rsultat
considrent une erreur exprimentale provenant seulement de la statistique de comptage mais
ne tiennent pas compte du bruit de fond, de la forme des raies ou dun modle structural non
adapt au matriau. Pour corriger cela, il suffit de multiplier les carts-types par le facteur de
Berar (ou Scor), donn dans le fichier rsultat.
Le calcul des microcontraintes se fait selon la formule : <>
1/2
=
2 ln 8 180
DST
o DST =
6
LaB i
U U avec U
i
le paramtre de profil dtermin par laffinement des donnes
de diffraction du matriau i et
6
LaB
U celui dtermin pour LaB
6
. La taille des domaines de
cohrence est dtermine comme suit : <L> =
360
avec la longueur donde utilise
et Y le paramtre de profil dtermin par laffinement des donnes de diffraction du matriau.
II-3 Caractrisations lectrochimiques
II-3-1 Fonctionnement dune batterie lithium ion
Les batteries sont formes par une chane lectrochimique compose de deux couples
oxydo-rducteurs de potentiels thermodynamiques diffrents spars par un lectrolyte.
Llectrode ngative est compose le plus souvent de carbone alors que llectrode positive
est un compos lithi. Un lectrolyte liquide spare les deux lectrodes et assure la circulation
des ions lithium lors des charges et dcharges successives de la batterie. Pour cela, il doit tre
un bon conducteur ionique mais un isolant lectronique. Le fonctionnement dune batterie
lithium ion est schmatis par la Figure II-1.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre II
Magali Maccario 30 novembre 2007
26
C
Etat
initial
Premire
charge
Premire
dcharge
Li
x
MPO
4
LiMPO
4
Li
1-x
C
+
Li
+
Li
+
Electrolyte
liquide
Electrolyte
liquide
Electrolyte
liquide
e
-
e
-
e
-
e
-
Figure II-1 : Principe de fonctionnement dune batterie lithium ion.
Le fonctionnement dune batterie est associ la dsintercalation et lintercalation
des ions lithium dans la structure LiMPO
4
(M = Fe, Mn, Co) par exemple, entranant
respectivement loxydation et la rduction des mtaux de transition. Lors de la charge de la
batterie, le circuit extrieur impose le transfert dun certain nombre dlectrons de llectrode
positive vers llectrode ngative, ce qui induit une raction redox aux deux lectrodes. A
llectrode positive, larrachage des lectrons saccompagne dune oxydation du mtal de
transition et, pour la compensation des charges, dune dsintercalation des ions Li
+
de la
structure hte. A llectrode ngative le phnomne inverse se produit, larrive des lectrons
induit une rduction de la structure hte du carbone et par consquent pour assurer lquilibre
des charges une intercalation des ions lithium. Au cours de la dcharge, il y a donc rduction
du mtal de transition et rintercalation des ions lithium dans le matriau dlectrode positive.
Cette tape permet la restitution de lnergie lectrique emmagasine sous forme chimique
lors de la charge.
Il est ncessaire de prciser que les batteries de laboratoire utilises dans le cadre de
cette tude sont des batteries au lithium : Li / lectrolyte / LiMPO
4
. Llectrode ngative, qui
est du lithium mtallique, sert galement dlectrode de rfrence. Le potentiel du couple
Li
+
/Li tant constant et gal - 3,04 V vs. ENH. La courbe de cyclage, soit la variation du
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre II
Magali Maccario 30 novembre 2007
27
potentiel en fonction de ltat de charge ou de dcharge, correspond alors exclusivement la
variation du potentiel de llectrode positive.
Une batterie est caractrise par diffrentes grandeurs, dont :
la capacit Q en A.h dont la formule est :
M
m x F
It Q
3600
= =
avec I (A) : courant traversant le gnrateur,
t (h) : temps de passage du courant,
F (C) : nombre de Faraday (96500 C),
x : nombre de moles dions lithium intercals dans Li
x
MPO
4
,
m (g) : masse de matriau lectrochimiquement actif,
M (g.mol
-1
) : masse molaire du matriau actif.
lnergie W en W.h dont la formule est :
= =
e dch e dch
Vdx
M
Fm
Idt V W
arg arg
3600
.
avec V (V) : tension du gnrateur.
Dans la pratique, capacit et nergie sont souvent ramenes au volume ou la masse de
matriau actif ou du gnrateur lui-mme.
le rgime de cyclage C/n, qui correspond la capacit thorique obtenue lors de la
charge en n heures, cest dire, dans le cas de LiMPO
4
, lors de lchange dun
lectron en n heures.
II-3-2 Elaboration de batteries au lithium de laboratoire
Pour cette tude, deux types de cellules ont t utiliss ainsi que deux types
dlectrodes : les lectrodes enduites et les lectrodes poudre.
Les batteries de laboratoire (de type Swagelock ou pile bouton) sont ralises en
bote gants. Les batteries de type Swagelock sont constitues dun tube de tflon filet
pour recevoir deux collecteurs de courant en acier inoxydable. Les batteries de type pile
bouton sont galement constitues de deux collecteurs de courant en acier inoxydable
(coupelles), dune cale, dun ressort qui permet de maintenir une pression constante
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre II
Magali Maccario 30 novembre 2007
28
lintrieur de la cellule et dun joint de polypropylne permettant dassurer ltanchit ;
lensemble est assembl laide dune presse pneumatique en bote gants.
Les lectrodes dites enduites sont constitues dun mlange de 80 % en masse de
matriau actif, de 10 % en masse dun additif conducteur (Super P, MMM Carbon) pour
assurer la conductivit lectronique et de 10% en masse de poly(fluorure de vinylidene), qui
est un liant permettant dassurer une bonne tenue mcanique de llectrode. Ces diffrents
constituants sont introduits dans 0.8 mg de N-methyl pyrrolidone afin dobtenir un mlange
trs homogne. Ce mlange est ensuite enduit au moyen dune table denduction sur une
feuille daluminium pralablement enduite dun liant qui facilite ladhsion entre les deux
parties. Lenduction se fait 100 m, ce qui reprsente in fine une densit de 2 3 mg.cm
-2
de
matire active. Des lectrodes de 10 mm de diamtre sont ensuite dcoupes dans cette feuille
enduite et sche pendant une nuit 55C. Une fois presses (10 T.cm
-2
) et peses, les
lectrodes sont sches 48 h 80C sous vide. Il faut noter qutant donn le mode de
prparation et le faible diamtre des lectrodes, une erreur sur la masse de lordre de 5 % peut
tre constate. Une fois dans la cellule, llectrode est recouverte successivement dun
sparateur constitu dune feuille microporeuse en polypropylne (Celgard
) qui permet
dempcher la formation de dendrites de lithium et donc les courts-circuits, dun non-tiss en
polypropylne imbib dlectrolyte (Viledon
, Freudenberg), dune autre feuille de Celgard
et enfin de llectrode ngative qui est une pastille de lithium mtallique. Llectrolyte utilis
est un sel de lithium (LiPF
6
, 1 M) dissout dans un mlange de solvants organiques
PC / EC / DMC (Carbonate de Propylne / Carbonate dEthylne / Carbonate de DiMthyle)
dans les proportions volumiques 1 : 1 : 3.
Les lectrodes dites poudre permettent de saffranchir de laluminium et du liant, ce
qui est intressant notamment pour les analyses par spectroscopie Mssbauer. Ces lectrodes
sont composes de 90 % en masse de matriau actif et de 10 % en masse dun mlange
suie - graphite (1 : 1) pour amliorer respectivement la porosit et la conductivit. Ce mlange
est tass, pour optimiser les contacts entre les divers constituants, dans un collecteur creus
dlectrode positive dune batterie de type Swagelock. Puis comme prcdemment, les
feuilles de Celgard
, de Viledon
et de lithium mtallique sont ajoutes ainsi que
llectrolyte.
Les diffrents tests lectrochimiques sont raliss sur deux bancs de test : un systme
conu au laboratoire (Battlab) et un systme VMP1 conu et commercialis par la socit
Bio-Logic SAS.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre II
Magali Maccario 30 novembre 2007
29
Une fois cycles, les batteries sont dsassembles en bote gants sous atmosphre
contrle, laves au DMC puis sches sous vide.
II-4 Caractrisations physico-chimiques et texturales
II-4-1 Microscopie Electronique Balayage (MEB)
Avant observation les chantillons sont colls sur plot de microscopie ; une
mtallisation par dpt dune fine couche de platine sous vide primaire est ncessaire afin
dviter laccumulation de charges. Ils ont t observs avec un microscope Hitachi S4500
mission de champ, appartenant au Laboratoire des Composites Nanostructuraux (LCTS),
sous une tension dacclration de 3 kV, avec des grossissements de 200 000, 100 000,
50 000, 25 000, 10 000, 5 000 et 500. Les clichs ont t pris plusieurs endroits du plot avec
les mmes grossissements pour vrifier lhomognit des observations.
II-4-2 Mesures de surface spcifique par la mthode de B. E. T.
Les mesures de surface spcifique ont t ralises par la mthode de Brunauer,
Emmet et Teller (B. E. T.) au CEA Grenoble. Elles consistent mesurer le volume d'azote
adsorb la surface de lchantillon la temprature de l'azote liquide (77 K). Les
chantillons tudis ont t schs 4 heures 300C sous balayage dazote. Lors de la mesure
le tube en U est refroidi dans un bain dazote liquide, les molcules dazote sadsorbent la
surface de lchantillon ; lors du retour temprature ambiante du tube en U, les molcules de
gaz sont dsorbes. La thorie B. E. T. suppose que les molcules de gaz adsorbes forment,
en quilibre dynamique avec lazote gazeux, une monocouche la surface de lchantillon
permettant ainsi de relier la surface accessible de lchantillon au volume de gaz adsorb. La
surface mesure est ramene la masse dchantillon pour obtenir une valeur de surface
spcifique.
II-4-3 Mesures magntiques
Les mesures magntiques ont t ralises laide dun SQUID (Superconducting
Quantum Interference Device) MPMS-5S. Lvolution de la susceptibilit magntique avec la
temprature a t tudie deux valeurs de champ magntique (500 Oe et 10000 Oe) alors
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre II
Magali Maccario 30 novembre 2007
30
que la mesure de la variation de laimantation avec la valeur de champ appliqu a t ralise
deux tempratures diffrentes : 5 K et 298 K.
II-4-4 Conductivit lectronique
Les mesures de conductivit lectronique ont t ralises en courant continu selon la
mthode des quatre pointes en ligne entre 30 K et 300 K. Les quatre pointes sont alignes la
surface de lchantillon. Un courant est appliqu entre les deux pointes extrmes, ce qui
gnre un gradient de potentiel entre les deux pointes centrales, et on peut mesurer la tension
V entre ces deux pointes. La conductivit lectrique est alors obtenue par la relation
suivante : =
V
I
K avec K facteur de forme qui dpend de la gomtrie de lchantillon
(distance entre les pointes, paisseur, ). En gnral, K = 1 dans notre cas.
Les pastilles de 8 mm du matriau analys ont t prpares en bote gants avec
200 mg de matriau en appliquant une pression de 4 T pendant 20 minutes.
II-4-5 Microscopie Electronique Transmission Haute Rsolution (MET-HR) (en
collaboration avec Franois Weill, ICMCB - CREMEM - Talence)
Pour cette tude, nous avons utilis le microscope JEOL 2200 FS, quip dun porte-
objet double tilt, du Centre de Ressources de Microscopie Electronique et Microanalyses de
lUniversit Bordeaux I. Les images haute rsolution des chantillons ont t obtenues avec
une tension dacclration de 200 kV.
Avant lobservation, le matriau est dispers, laide dun mortier en agate, dans de
lhexane sous atmosphre contrle lorsquil sagit de matriaux dsintercals ou dans de
lthanol lair ambiant lorsquil sagit de matriaux initiaux. Une goutte de la prparation
ainsi obtenue est dpose sur une grille trous recouverte dune membrane de carbone.
Toutes les grilles prpares sous atmosphre contrle sont prserves de latmosphre
extrieure jusqu leur entre dans le sas du microscope. De plus, une grille sortie du
microscope et qui a t au contact de latmosphre ambiante nest jamais analyse une
seconde fois.
II-4-6 Spectroscopie infrarouge (en collaboration avec Bernard Desbat,
CBMN - Pessac ; Laurent Servant et Thierry Tassaing, ISM - Talence)
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre II
Magali Maccario 30 novembre 2007
31
Les acquisitions de spectroscopie infrarouge dans le proche infrarouge en rflexion
diffuse ont t ralises lInstitut des Sciences Molculaires (ISM) avec un spectromtre
FTIR Nicolet Magna 560 quip dun dtecteur MCT. La technique de la rflexion diffuse
permet ltude de poudres ou dchantillons prsentant des surfaces rugueuses. Alors quen
rflexion spculaire on analyse la lumire rflchie par une surface polie, en rflexion diffuse
la radiation pntre lintrieur de lchantillon o elle subit des effets de rflexion,
rfraction, absorption et diffusion, puis rmerge dans toutes les directions de lespace. Cest
donc un ensemble de rayons diffuss qui est analys par le dtecteur. Pour recueillir tous ces
rayonnements, un dispositif bas sur la combinaison de deux miroirs elliptiques permettant
dliminer la rflexion spculaire pour ne garder que la rflexion diffuse - est utilis :
Selector P/N Series Graseby Specac. Les spectres obtenus tant complexes et fortement
dpendants des conditions exprimentales, il est possible de corriger les spectres de rflexion
diffuse grce la relation de Kubelka-Munk et dobtenir des spectres comparables des
spectres dabsorption [3-5]. Pour pouvoir appliquer la relation de Kubelka-Munk, les mesures
effectues ont t ralises avec une poudre de KBr broye et sche comme rfrence. Les
matriaux analyss sont mlangs (~ 3 % en masse) et broys avec du KBr pour viter au
maximum des effets de distorsion du signal dabsorption dus des diffrences de
granulomtrie.
Les lectrodes sont analyses par microscopie infrarouge. Cette technique permet
lobservation et lanalyse en rflexion de zones dchantillons pouvant aller de 10 m
quelques centaines de m de cot. Le microscope utilis est un Nic-Plan (NICOLET) coupl
au spectromtre prcdemment utilis. Les rsultats obtenus sont indpendants de la
gomtrie de lchantillon.
Les analyses prcdentes ont t ralises dans la gamme [3000 600] cm
-1
; dans le
cas de nos matriaux, cette gamme ne permet lobservation que des vibrations dues aux
liaisons PO ([1250 850] cm
-1
). Pour accder aux vibrations des liaisons LiO et FeO, il
est ncessaire de se placer dans linfrarouge lointain. Pour raliser ces mesures, des pastilles
de 13 mm de diamtre ont t ralises sous vide. Ces pastilles sont labores avec ~ 1 % en
masse de matriau dispers dans une matrice de polythylne et psent de lordre de 250
300 mg. Une fois la pastille installe dans le spectromtre, on effectue une mise sous vide du
compartiment de mesure pendant 5 minutes puis la mesure est ralise. Les spectres ont t
enregistrs sur un spectromtre Nicolet 20F Vacuum.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre II
Magali Maccario 30 novembre 2007
32
II-4-7 Microspectroscopie Raman (en collaboration avec Bernard Desbat
CBMN - Pessac ; Laurent Servant et Michel Couzi, ISM - Talence)
La spectroscopie Raman est une mthode danalyse non destructive qui requiert peu de
matriau. Les mesures de microspectroscopie Raman ont t ralises lISM avec un
spectromtre Labram HR 800 (Jobin Yvon) quip dun microscope Olympus. Ce
spectromtre dispose de plusieurs sources laser avec diffrentes longueurs donde. Certaines
mesures ont t ralises avec un laser Hlium / Non, soit une longueur donde de 632 nm
dans le visible, dautres mesures ont t ralises avec une longueur donde situe dans lUV
(325 nm). Le filtre utilis a t ajust de telle sorte attnuer 100 fois la puissance du laser
(passage de 10 mW 0.1 mW). La taille de la zone analyse est de lordre de 1.2 m de
diamtre.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre II
Magali Maccario 30 novembre 2007
33
II-4-8 Spectroscopie XPS (en collaboration avec Rmi Ddryvre et Danielle
Gonbeau, IPREM/ECP - Pau)
Les analyses XPS ont t ralises Pau lInstitut Pluridisciplinaire de Recherche
sur l'Environnement et les Matriaux - Equipe de Chimie Physique (IPREM-ECP). Ce
laboratoire est quip dun spectromtre XPS, qui pour viter tout risque de contamination ou
de contact avec un milieu humide, est directement connect une bote gants via une
chambre de transfert. Les chantillons analyss (pastilles de poudres et lectrodes) sont
directement colls sur le porte-chantillon. Les analyses ont t effectues avec un
spectromtre Kratos Axis Ultra spectrometer et une radiation monochromatique de
laluminium K
(h = 1486.6 eV). Le spectromtre est calibr avec le pic de photomission
Ag 3d
5/2
(nergie de liaison 368.3 eV). Les spectres ont t enregistrs avec une nergie de
passage constante de 20 eV. La surface analyse est de 300 700 m
2
sur 5 nm de
profondeur et la pression de la chambre est de lordre de 5.10
-7
Pa. Les effets de charges
induits par le caractre isolant des chantillons sont corrigs par l'utilisation d'un neutraliseur
de charges (canon lectrons lents).
Des acquisitions rapides sont ralises avant et aprs chaque analyse pour vrifier la
conservation de lchantillon sous le faisceau de rayons X. Lchelle des nergies de liaison
est calibre par rapport au pic C 1s 285.0 eV. La position et la surface des pics sont obtenues
par un affinement par la mthode des moindres carrs des spectres (70 % gaussienne, 30 %
Lorentzienne) des donnes exprimentales. La quantification est obtenue en se basant sur les
facteurs de sensibilit relative de Scofield.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre II
Magali Maccario 30 novembre 2007
34
Bibliographie du Chapitre II
1
J. Hesse, A. Rubartsch, J. Phys. E. Sci. Instrum., 7 (1974), 526.
2
J. Rodriguez-Carvajal, Laboratoire Lon Brillouin,
http://www-llb.cea.fr/fullweb/powder.htm, (2004).
3 P. Kubelka, F. Munk, Z. Tech. Phys., 12 (1931), 593.
4 P. Kubelka, J. Opt. Soc. Am., 38 (1948), 448.
5 M.P. Fuller, P.R. Griffith, Analytical Chemistry, 0 (1978), 1906.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre III
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre III
Magali Maccario 30 novembre 2007
35
Chapitre III
Etude prliminaire de la synthse des matriaux C-LiFePO
4
:
Effet du rapport nominal Li/Fe sur les proprits
lectrochimiques en batteries au lithium
III-1 Synthse.................................................................................................................... 36
III2 Analyses physico-chimiques.................................................................................... 37
III3 Mesures de conductivit lectronique..................................................................... 43
III4 Caractrisation lectrochimique............................................................................. 45
III5 Caractrisations morphologiques ........................................................................... 47
III-6 Conclusions.............................................................................................................. 49
Bibliographie du Chapitre III .......................................................................................... 50
Ce chapitre rapporte les quelques rsultats obtenus lors dune tude prliminaire
mene pour dterminer linfluence du rapport nominal Li/Fe sur les proprits des matriaux
C-LiFePO
4
. En effet, une modification du rapport Li/Fe dans la structure olivine et
particulirement un rapport Li/Fe suprieur 1 devrait affecter le rapport Fe
3+
/Fe
2+
et
conduire ainsi la formation de matriaux valence mixte avec une conductivit lectronique
plus leve que les matriaux stoechiomtriques. La possibilit de former la solution-solide
Li
1+y
Fe
1-y
PO
4
autour de la composition LiFePO
4
stoechiomtrique sera tudie dans ce
chapitre, tout comme lexistence dun rapport atomique Li/Fe optimal pour obtenir de bonnes
proprits lectrochimiques pour LiFePO
4
dans les conditions de synthse utilises. Comme
nous allons voir dans la suite de ce chapitre, plusieurs prcurseurs de lithium ont t utiliss
lors des synthses.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre III
Magali Maccario 30 novembre 2007
36
III-1 Synthse
La synthse de C-LiFePO
4
est ralise par activation mcano-chimique du mlange de
prcurseurs selon un mode de synthse tabli par le CEA co-financeur de cette thse. Les
ractifs, le phosphate de fer et le prcurseur de lithium (Aldrich), sont mlangs 10 % en
masse de cellulose (Aldrich). La synthse du phosphate de fer est ralise par prcipitation
en quantit stoechiomtrique dune poudre de sulfate de fer FeSO
4
.7H
2
O dans une solution de
phosphate de sodium (Na
3
PO
4
). Le pH du milieu aqueux est contrl et ajust par addition
dhydroxyde de sodium, ce qui fait que la principale entit phosphate en solution est PO
4
3-
[1].
La caractrisation par spectroscopie Mssbauer du phosphate de fer a montr que
~ 39 at. % du fer tait l'tat trivalent tandis que ~ 61 at. % tait l'tat divalent. De plus, les
dosages raliss par ICP et les analyses thermogravimtriques ont montr respectivement un
rapport Fe/P gal 1.42 et la prsence de ~ 6.5 moles d'eau par unit formulaire, la
composition chimique du phosphate de fer a t ainsi dtermine comme tant
Fe
2.84
(PO
4
)
2
.~ 6.5 H
2
O. En tenant compte de cette composition pour le phosphate de fer,
le rapport nominal Li/Fe est choisi lors des synthses - en jouant sur les prcurseurs de lithium
utiliss - de telle sorte ajuster simultanment les rapports Li/Fe et Fe/P. Les mlanges de
prcurseurs de lithium sont Li
3
PO
4
, Li
3
PO
4
- Li
2
CO
3
et Li
3
PO
4
- LiH
2
PO
4
, leur quantit est
ajuste de telle sorte avoir des rapports Li/Fe nominaux respectivement gaux ~ 1.06,
~ 1.16 et ~ 1.11, ~ 1 et ~ 0.95, quant aux rapports (Li+Fe)/P ils sont respectivement gaux
~ 1.92, ~ 1.97, ~ 2.02, ~ 1.87, ~ 1.83. Les associations des diffrents prcurseurs de lithium
ont t ralises de faon ajuster la stoechiomtrie dsire tout en tenant compte du fait que
le prcurseur de lithium est galement prcurseur de phosphore.
Le mlange de prcurseurs (~ 50 g) est broy quatre fois pendant 1 h 30 min dans un
broyeur plantaire (Fritsch Pulverisette 4) dans des jarres en carbure de tungstne de
250 mL et avec 14 billes en agate (10 mm de diamtre). Entre chaque squence de broyage, la
poudre est dcolmate des parois de la jarre. Toutes les manipulations sont faites sous
atmosphre contrle. Le broyat obtenu est trait thermiquement dans un four tubulaire
800C pendant 15 minutes sous flux dargon.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre III
Magali Maccario 30 novembre 2007
37
III2 Analyses physico-chimiques
III-2-1 Caractrisation par Diffraction des Rayons X
Les diagrammes de diffraction des rayons X enregistrs pour les matriaux C-LiFePO
4
synthtiss en utilisant diffrents rapports nominaux Li/Fe sont prsents la Figure III-1.
Dans un premier temps, on note que les matriaux synthtiss avec un rapport Li/Fe
suprieur ou gal 1 sont purs du point de vue de la diffraction des rayons X, alors que le
matriau C-LiFePO
4
synthtis avec un rapport nominal Li/Fe lgrement infrieur 1
(Li/Fe ~ 0.95) nest pas pur. En effet, on constate la prsence de pics supplmentaires
~ 34.0 et ~ 35.2 (2) sur le diagramme de diffraction des rayons X : ces pics sont
attribuables Fe
2
P
2
O
7
. Ce rsultat est en bon accord avec les rsultats publis par Kim et al.
[2] et Herle et al. [3].
Lanalyse de certaines raies de diffraction, c'est--dire le calcul de la largeur mi-
hauteur (FWHM) des raies corrige de la fonction instrumentale, permet, en utilisant la
formule de Scherrer, destimer la taille des domaines de cohrence selon diffrentes directions
cristallographiques : les rsultats obtenus sont reports au Tableau III-1. Dans ces conditions
de synthse, la taille moyenne des domaines de cohrence est trs similaire (c'est--dire
comprise entre 100 et 140 nm) quels que soient le prcurseur de lithium ou le rapport nominal
Li/Fe.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre III
Magali Maccario 30 novembre 2007
38
(111)
(211)
(311) (101)
C-LiFePO
4
(Li/Fe ~ 0.95)
C-LiFePO
4
(Li/Fe ~ 1.00)
C-LiFePO
4
(Li/Fe ~ 1.06)
C-LiFePO
4
(Li/Fe ~ 1.11)
C-LiFePO
4
(Li/Fe ~ 1.16)
20 30 40 50 60
* *
I
(
A
.
U
.
)
2
Co
()
* Fe
2
P
2
O
7
Figure III-1 : Diagrammes de diffraction des rayons X des matriaux C-LiFePO
4
synthtiss avec diffrents
rapports nominaux Li/Fe.
Tableau III-1 : Comparaison des largeurs mi-hauteur (FWHM : Full Width at Half Maximum) de raies
slectionnes sur les diagrammes de diffraction des rayons X des matriaux C-LiFePO
4
(avec Li/Fe ~ 1.16,
~ 1.11, ~ 1.06, ~ 1.00 et ~ 0.95). Ces valeurs de FWHM ont t corriges de la fonction instrumentale du
diffractomtre en utilisant LaB
6
comme rfrence. La taille des domaines de cohrence (L) est estime
partir de la formule de Scherrer FWHM(2) = 0.9/(L.cos) avec = 1.789 (radiation K du cobalt).
C-LiFePO
4
Li/Fe nominal ratio
(101) (111) (211) (311)
FWHM () 0.08 0.11 0.09 0.09 C-LiFePO
4
(Li/Fe ~ 1.16) L (nm) 115 85 115 110
FWHM () 0.08 0.10 0.10 0.10 C-LiFePO
4
(Li/Fe ~ 1.11) L (nm) 115 100 100 100
FWHM () 0.07 0.10 0.08 0.09 C-LiFePO
4
(Li/Fe ~ 1.06) L (nm) 130 100 120 110
FWHM () 0.07 0.09 0.07 0.08 C-LiFePO
4
(Li/Fe ~ 1.00) L (nm) 140 100 140 120
FWHM () 0.07 0.10 0.09 0.09 C-LiFePO
4
(Li/Fe ~ 0.95) L (nm) 130 100 110 110
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre III
Magali Maccario 30 novembre 2007
39
Les paramtres de maille de ces cinq matriaux ont t dtermins par laffinement par
la mthode de Le Bail des donnes de diffraction des rayons X. Cet affinement a t ralis
dans le groupe despace Pnma avec les paramtres de maille : a ~ 10.33 , b ~ 6.009 et
c ~ 4.695 . Une fonction Pseudo-Voigt a t utilise pour dcrire le profil des raies de
diffraction. Il faut noter que laffinement du diagramme de diffraction des rayons X du
matriau C-LiFePO
4
(Li/Fe ~ 0.95) a t ralis en considrant la prsence de deux phases,
LiFePO
4
et Fe
2
P
2
O
7
, alors que pour les autres matriaux une seule phase a t considre. Les
paramtres structuraux dtermins sont donns dans le Tableau III-2. Les volumes sont
compris entre ~ 291.1
3
et ~ 291.4
3
et sont donc en bon accord avec ceux rapports dans
la littrature pour des composs de type olivine ordonne, comme cela a t rcemment
montr par Chen et al. [4]. En effet, le volume est trs sensible au dsordre cationique, par
consquent les phases de type olivine parfaitement ordonne prsentent des volumes compris
entre [291.0 - 291.5]
3
alors que les phases
prsentant un change cationique entre les sites
4a et 4c ont des volumes suprieurs 291.5
3
.
Tableau III-2: Comparaison des paramtres structuraux obtenus par laffinement par la mthode de Le
Bail des donnes de diffraction des rayons X pour les matriaux C-LiFePO
4
(~ 1.16, ~ 1.11, ~ 1.06, ~ 1.00
et ~ 0.95).
a () b () c () V (
3
)
R
wp
(%)
R
B
(%)
C-LiFePO
4
(Li/Fe ~ 1.16) 10.3253(2) 6.0064(2) 4.6933(2) 291.06(1) 18.3 6.3
C-LiFePO
4
(Li/Fe ~ 1.11) 10.3253(3) 6.0068(2) 4.6935(2) 291.10(1) 17.6 6.0
C-LiFePO
4
(Li/Fe ~ 1.06) 10.3294(3) 6.0086(2) 4.6948(2) 291.38(1) 12.6 9.7
C-LiFePO
4
(Li/Fe ~ 1.00) 10.3271(4) 6.0069(2) 4.6934(2) 291.15(2) 18.0 6.3
C-LiFePO
4
(Li/Fe ~ 0.95) 10.3290(3) 6.0080(2) 4.6938(2) 291.28(2) 15.6 7.1
III-2-2 Dosages chimiques
Le Tableau III-3 donne les rsultats des dosages chimiques. Les cinq matriaux
prsentent approximativement le mme pourcentage massique de carbone compris entre 2.53
et 3.05 wt%. Ces analyses montrent galement que deux chantillons C-LiFePO
4
parmi les
cinq tudis sont caractriss par des rapports Li/Fe exprimentaux significativement
infrieurs aux rapports nominaux. En effet, alors que les rapports nominaux Li/Fe de deux des
matriaux sont gaux ~ 1.16 et ~ 1.11, les rapports Li/Fe exprimentaux sont respectivement
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre III
Magali Maccario 30 novembre 2007
40
gaux ~ 1.06 et ~ 1.01. Ces deux matriaux tant obtenus partir dun mlange de Li
2
CO
3
et Li
3
PO
4
, cela suggre une perte de lithium plus importante pendant le traitement thermique
des matriaux synthtiss avec Li
2
CO
3
par rapport ce qui est observ pour les matriaux
synthtiss partir des prcurseurs Li
3
PO
4
et LiH
2
PO
4
. En effet, pour les trois autres
matriaux (Li/Fe ~ 1.06, ~ 1.00 et ~ 0.95), la prcision du dosage chimique, les rapports
Li/Fe exprimentaux sont en assez bon accord avec les rapports nominaux.
Dans la suite de ce chapitre, nous avons choisi de nommer ces matriaux C-LiFePO
4
grce au rapport nominal Li/Fe utilis pour la synthse.
Tableau III-3 : Rsultats des dosages chimiques du C, Li, Fe et P pour les matriaux C-LiFePO
4
synthtiss avec diffrents rapports nominaux Li/Fe gaux ~ 1.16, ~ 1.11, ~ 1.06, ~ 1.00 et ~ 0.95. La
variation du rapport Li/Fe est obtenue grce lutilisation de diffrents prcurseurs de lithium lors de la
synthse.
III2-3 Dosages redox par spectroscopie Mssbauer
Les analyses Mssbauer de tous ces chantillons C-LiFePO
4
ont galement t
ralises (Figure III-2a). Les spectres ont t affins en ajustant les spectres calculs et
exprimentaux laide de raies de profil lorentzien. Comme le montrent les agrandissements
donns par la Figure III-2b et la Figure III-2c, pour tous les chantillons deux doublets sont
ncessaires, le premier est associ aux ions Fe
2+
prsents dans un environnement octadrique
doxygne dans la structure olivine et le second est dpendant du rapport Li/Fe utilis lors de
la synthse. Les paramtres Mssbauer caractristiques, que sont le dplacement isomrique
(), lclatement quadrupolaire () et la largeur mi-hauteur (), obtenus grce aux
affinements sont donns dans le Tableau III-4.
Tous les chantillons tudis contiennent principalement des ions Fe
2+
haut spin dans
un environnement octadrique doxygne, comme le montre la valeur leve du dplacement
isomrique (1.22 mm.s
-1
) caractristique des ions Fe
2+
dans ce type denvironnement.
C-LiFePO
4
Li/Fe nominal ratio
Li precursor C (wt%) Li/Fe Li/P Fe/P
C-LiFePO
4
(Li/Fe ~ 1.16)
Li
3
PO
4
- Li
2
CO
3
2.53 1.06 0.99 0.93
C-LiFePO
4
(Li/Fe ~ 1.11)
Li
3
PO
4
- Li
2
CO
3
2.70 1.01 0.99 0.98
C-LiFePO
4
(Li/Fe ~ 1.06)
Li
3
PO
4
2.91 1.06 1.04 0.98
C-LiFePO
4
(Li/Fe ~ 1.00)
Li
3
PO
4
- LiH
2
PO
4
3.05 0.99 0.93 0.94
C-LiFePO
4
(Li/Fe ~ 0.95)
Li
3
PO
4
- LiH
2
PO
4
2.85 0.93 0.88 0.95
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre III
Magali Maccario 30 novembre 2007
41
Lclatement quadrupolaire dpend lui de deux contributions : la configuration lectronique
du cation lui-mme (c'est--dire la distribution de ses lectrons de valence) et lenvironnement
lectronique d aux ions voisins, la premire contribution prdomine quand elle existe. Par
exemple, pour les ions Fe
2+
(3d
6
, HS), la distribution asymtrique des lectrons de valence
implique une valeur leve de (ici ~ 2.95 mm.s
-1
), trs peu sensible lenvironnement.
Pour les matriaux (Li/Fe ~ 1.16, ~ 1.11 et ~ 1.06), le second doublet est d la
prsence dune petite quantit de Fe
3+
(~ 5 7 at. %). En effet, le profil asymtrique de la raie
environ -0.25 mm.s
-1
(Figure III-2a et Figure III-2b) ainsi que la diffrence dintensit
entre les deux raies du doublet Mssbauer ne peuvent tre pris en compte quen considrant la
prsence dun doublet supplmentaire associ aux ions Fe
3+
.
Pour les autres chantillons C-LiFePO
4
(Li/Fe ~ 1.00 et ~ 0.95), le second doublet
prsente un dplacement isomrique caractristique dions Fe
2+
en sites octadriques, avec un
clatement quadrupolaire infrieur celui des ions Fe
2+
de LiFePO
4
, qui sont en sites
octadriques trs distordus. Ce doublet serait attribuable Fe
2
P
2
O
7
, en bon accord avec les
observations faites par diffraction des rayons X (cf. Figure III-1) et avec les paramtres
hyperfins de spectroscopie Mssbauer reports dans la littrature ( = 1.2 mm.s
-1
et
= 2.5 mm.s
-1
) [5]. Il est noter que la largeur de raie mi-hauteur (
+
2
Fe
) leve obtenue
pour le matriau Fe
2
P
2
O
7
sexplique par la prsence de deux sites octadriques distincts dans
la structure de Fe
2
P
2
O
7
.
Ces analyses par spectroscopie Mssbauer ont permis de dterminer le taux dions
Fe
3+
prsent dans les trois matriaux C-LiFePO
4
(Li/Fe ~ 1.16, ~ 1.11 et ~ 1.06). Ce taux est
respectivement de ~ 7, ~ 7 et ~ 5 at.%. Nanmoins, ces analyses Mssbauer ne permettent pas
de dterminer si ces ions Fe
3+
sont associs la formation dune phase appartenant la
solution-solide Li
1+y
Fe
1-y
PO
4
, la prsence dune phase amorphe riche en Fe
3+
ou la
prsence de dfauts la surface des cristallites de LiFePO
4
. Cependant, les phases olivine
valence mixte Li
1+y
Fe
1-y
PO
4
devraient montrer une forte augmentation de leur conductivit
lectronique intrinsque [6] : les mesures de conductivit lectronique sont donc prsentes
dans le paragraphe suivant.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre III
Magali Maccario 30 novembre 2007
42
-2 -1 0 1 2 3 4
A
obs.
A
calc.
C-LiFePO
4
(Li/Fe ~ 0.95)
C-LiFePO
4
(Li/Fe ~ 1.00)
C-LiFePO
4
(Li/Fe ~ 1.06)
C-LiFePO
4
(Li/Fe ~ 1.11)
C-LiFePO
4
(Li/Fe ~ 1.16)
Velocity (mm.s
-1
)
A
b
s
o
r
p
t
i
o
n
(
A
.
U
.
)
-2 -1 0 1 2 3 4
C-LiFePO
4
(Li/Fe ~ 0.95)
Velocity (mm.s
-1
)
A
b
s
o
r
p
t
i
o
n
(
A
.
U
.
)
-2 -1 0 1 2 3 4
C-LiFePO
4
(Li/Fe ~ 1.16)
Velocity (mm.s
-1
)
A
b
s
o
r
p
t
i
o
n
(
A
.
U
.
)
a)
b)
c)
Figure III-2 : a) Spectres Mssbauer des matriaux C-LiFePO
4
synthtiss en utilisant diffrents
rapports nominaux Li/Fe, b) Agrandissement du spectre de C-LiFePO
4
(Li/Fe ~ 1.16) permettant de
distinguer les deux doublets (Fe
2+
et Fe
3+
) ncessaires lajustement des spectres calcul et exprimental,
c) Agrandissement du spectre du matriau C-LiFePO
4
(Li/Fe ~ 0.95) permettant de distinguer les deux
doublets (Fe
2+
) ncessaires lajustement des spectres calcul et exprimental.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre III
Magali Maccario 30 novembre 2007
43
Tableau III-4 : Paramtres hyperfins obtenus par spectroscopie Mssbauer pour les deux types dions
prsents dans les matriaux C-LiFePO
4
dont le rapport nominal Li/Fe varie ( : dplacement isomrique,
: clatement quadrupolaire, : largeur mi-hauteur). Lcart-type est donn entre parenthses.
C-LiFePO
4
Li/Fe nominal ratio
Actual
Li/Fe value
(mm.s
-1
) (mm.s
-1
) (mm.s
-1
) % Site
1.214(2) 2.968(2) 0.265(1) 93 Fe
2+
[O
h
] C-LiFePO
4
(Li/Fe ~ 1.16)
1.06
0.4(1) 0.9(1) 0.69(6) 7 Fe
3+
1.214(2) 2.968(2) 0.270(1) 93 Fe
2+
[O
h
] C-LiFePO
4
(Li/Fe ~ 1.11)
1.01
0.4(1) 0.9(1) 0.67(6) 7 Fe
3+
1.217(2) 2.945(2) 0.259(1) 95 Fe
2+
[O
h
] C-LiFePO
4
(Li/Fe ~ 1.06)
1.06
0.4(1) 0.7(1) 0.6(1) 5 Fe
3+
1.224(8) 2.963(8) 0.273(4) 92 Fe
2+
[O
h
] C-LiFePO
4
(Li/Fe ~ 1.00)
0.99
1.3(2) 2.7(2) 0.4(1) 8 Fe
2+
[O
h
]
1.225(3) 2.954(3) 0.231(2) 83 Fe
2+
[O
h
] C-LiFePO
4
(Li/Fe ~ 0.95)
0.93
1.26(5) 2.43(5) 0.48(3) 17 Fe
2+
[O
h
]
III3 Mesures de conductivit lectronique
La comparaison des conductivits lectroniques obtenues pour les cinq matriaux
C-LiFePO
4
est donne la Figure III-3. Ils prsentent tous une conductivit lectronique
assez leve (~ 10
-2
S.cm
-1
temprature ambiante). On peut galement constater que les
matriaux prsentant des rapports nominaux Li/Fe suprieurs 1 (Li/Fe ~ 1.16, ~ 1.11 et
~ 1.06) ne prsentent pas une conductivit lectronique significativement plus leve,
contrairement ce que lon pourrait attendre avec la formation de phases olivine
Li
1+y
Fe
1-y
PO
4
prsentant des valences mixtes. Il est cependant essentiel de remarquer que la
conductivit des matriaux C-LiFePO
4
rsulte majoritairement du revtement de carbone
prsent la surface des particules de LiFePO
4
, la conductivit intrinsque de LiFePO
4
stoechiomtrique est effectivement trs faible de lordre de ~ 10
-9
S.cm
-1
25C [7,8]. On
peut cependant se demander si la variation de conductivit attendue avec la formation de
phases valence mixte ne serait pas trop faible pour tre caractrise en prsence du
revtement de carbone.
Il est intressant de noter que les conductivits lectroniques reportes par Chiang et
coll. pour leurs matriaux LiFePO
4
dits dops avec des cations de valence leve (Mg
2+
, Al
3+
,
Ti
4+
, Nb
5+
, ) mais non enrobs de carbone sont de lordre de 10
-1
S.cm
-1
temprature
ambiante, soit suprieures dun ordre de grandeur celles que nous observons pour nos
matriaux C-LiFePO
4
enrobs de carbone. Ces rsultats restent trs controverss : Chiang et
coll. annoncent la formation de matriaux valence mixte [6], cependant de nombreux
auteurs associent laugmentation de conductivit la formation dun enrobage de carbone ou
de composs conducteurs aux joints de grain. M. Thackeray [9] et Ravet et al. [10] suggrent
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre III
Magali Maccario 30 novembre 2007
44
effectivement que les matriaux sont synthtiss partir de prcurseurs contenant du carbone
(Li
2
CO
3
, FeC
2
O
4
) et quils contiennent donc au final jusqu 1.5 wt% de carbone. On peut
alors se demander si laugmentation de la conductivit nest pas due ce carbone ou la
formation de composs conducteurs aux joints de grain. Les travaux raliss par les groupes
de Nazar [3] et Masquelier [11] ont confort cette analyse.
0 5 10 15 20 25
-5.5
-5.0
-4.5
-4.0
-3.5
-3.0
-2.5
-2.0
-1.5
LiFePO
4
(Li/Fe ~ 1.16)
LiFePO
4
(Li/Fe ~ 1.11)
LiFePO
4
(Li/Fe ~ 1.06)
LiFePO
4
(Li/Fe ~ 1.00)
LiFePO
4
(Li/Fe ~ 0.95)
l
o
g
(
S
.
c
m
-
1
)
1000/T (K
-1
)
Figure III-3 : Mesures de conductivit lectronique ralises dans le domaine de temprature [30 300] K
avec la mthode des quatre pointes pour les cinq matriaux C-LiFePO
4
synthtiss avec diffrents rapports
nominaux Li/Fe (~ 1.16, ~ 1.11, ~ 1.06, ~ 1.00 et ~ 0.95).
La combinaison des caractrisations effectues, c'est--dire les dosages chimiques, les
analyses par spectroscopie Mssbauer et par diffraction des rayons X, ainsi que les mesures
de conductivit, a permis de montrer que, quel que soit le rapport nominal Li/Fe et en
consquence le prcurseur de lithium utilis pour la synthse, la phase forme 800C de
type olivine serait stoechiomtrique, avec plus ou moins dimpurets dont la nature varie avec
les conditions de synthse. On peut rsumer cela ainsi :
quand le rapport nominal Li/Fe est suprieur 1, des ions Fe
3+
sont toujours
prsents dans les chantillons, il ny a pas dimpuret dcelable par diffraction
des rayons X,
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre III
Magali Maccario 30 novembre 2007
45
lorsque le rapport nominal Li/Fe est infrieur 1, limpuret Fe
2
P
2
O
7
est forme.
Des tudes structurales prliminaires par diffraction des rayons X ralises sur ces
matriaux tendent montrer que tous les matriaux tudis prsentent une structure olivine
parfaitement ordonne, sans diffrence significative de paramtres structuraux. Pour
confirmer plus prcisment ces rsultats, des tudes structurales plus dtailles combinant
diffraction des rayons X et des neutrons ainsi que la prise en compte de diffrentes formules
chimiques et distributions cationiques seront prsentes au chapitre suivant.
III4 Caractrisation lectrochimique
Le comportement lectrochimique de ces cinq matriaux a t tudi, grce des
lectrodes enduites, en mode galvanostatique rgime constant C/20 dans la fentre de
potentiel [2 4.5] V (vs. Li
+
/Li). Les premiers cycles obtenus pour tous les matriaux sont
compars la Figure III-4. Ces matriaux peuvent tre classs en deux catgories :
- ceux prsentant dassez bonnes performances lectrochimiques, du moins pendant
les premiers cycles (C-LiFePO
4
avec Li/Fe ~ 1.16, ~ 1.11 et ~ 1.06),
- ceux prsentant de mauvaises performances lectrochimiques (polarisation leve et
faible capacit rversible) ds les premiers cycles (C-LiFePO
4
avec Li/Fe ~ 1.00 et
~ 0.95).
Les courbes de cyclage donnes pour les matriaux C-LiFePO
4
(Li/Fe ~ 1.16, ~ 1.11 et
~ 1.06) montrent en effet une assez faible diffrence de potentiel entre les courbes de charge
et de dcharge (~ 0.10 V vs. Li
+
/Li), mais aussi une faible capacit irrversible (~ 9 mAh/g,
c'est--dire x = 0.05 pour Li
x
FePO
4
). Cependant, pour les matriaux C-LiFePO
4
(Li/Fe ~ 1.16 et ~ 1.11) on note un changement de comportement aprs environ 10 cycles,
avec comme on peut le constater sur linsert de la Figure III-4 une augmentation trs
importante de la polarisation ainsi quune forte diminution de la capacit rversible.
Les matriaux C-LiFePO
4
(Li/Fe ~ 1.00 et ~ 0.95) prsentent quant eux ds le
premier cycle une trs forte diffrence de potentiel entre les courbes de charge et de dcharge
mais galement une faible capacit irrversible, cela est probablement d la prsence de
limpuret Fe
2
P
2
O
7
, inactive lectrochimiquement dans cette fentre de potentiel. Ces
performances lectrochimiques mdiocres sont conserves mme aprs le premier cycle et se
dtriorent encore aprs quelques cycles, avec une augmentation de la polarisation et une
diminution notable de la capacit rversible.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre III
Magali Maccario 30 novembre 2007
46
-0.2 0.0 0.2 0.4 0.6 0.8 1.0
1.5
2.0
2.5
3.0
3.5
4.0
4.5
136 68 102 34 170 0
Capacity (mAh/g)
P
o
t
e
n
t
i
a
l
v
s
.
L
i
+
/
L
i
(
V
)
x in Li
x
FePO
4
(Li/Fe ~ 1.00)
-0.2 0.0 0.2 0.4 0.6 0.8 1.0
1.5
2.0
2.5
3.0
3.5
4.0
4.5
34 68 102 136 170 0
Capacity (mAh/g)
P
o
t
e
n
t
i
a
l
v
s
.
L
i
+
/
L
i
(
V
)
x in Li
x
FePO
4
(Li/Fe ~ 0.95)
-0.2 0.0 0.2 0.4 0.6 0.8 1.0
1.5
2.0
2.5
3.0
3.5
4.0
4.5
136 102 68 34 170 0
Capacity (mAh/g)
P
o
t
e
n
t
i
a
l
v
s
.
L
i
+
/
L
i
(
V
)
x in Li
x
FePO
4
(Li/Fe ~ 1.16)
0.0 0.1 0.2 0.3 0.4 0.5 0.6
2.0
2.5
3.0
3.5
4.0
4.5
-0.2 0.0 0.2 0.4 0.6 0.8 1.0
1.5
2.0
2.5
3.0
3.5
4.0
4.5
Capacity (mAh/g)
136 102 68 34 170 0
P
o
t
e
n
t
i
a
l
v
s
.
L
i
+
/
L
i
(
V
)
x in Li
x
FePO
4
(Li/Fe ~ 1.11)
0.0 0.2 0.4 0.6 0.8 1.0
2.0
2.5
3.0
3.5
4.0
4.5
-0.2 0.0 0.2 0.4 0.6 0.8 1.0
1.5
2.0
2.5
3.0
3.5
4.0
4.5
136 102 68 34 170 0
Capacity (mAh/g)
P
o
t
e
n
t
i
a
l
v
s
.
L
i
+
/
L
i
(
V
)
x in Li
x
FePO
4
(Li/Fe ~ 1.06)
-0.4 -0.2 0.0 0.2 0.4 0.6 0.8
2.0
2.5
3.0
3.5
4.0
4.5
Figure III-4 : Premiers cycles lectrochimiques obtenus pour les chantillons C-LiFePO
4
, dont le rapport
nominal Li/Fe varie (~ 1.16, ~ 1.11, ~ 1.06, ~ 1.00 et ~ 0.95), les cyclages sont raliss temprature
ambiante dans la fentre de potentiel [2 4.5] V (vs. Li
+
/Li) rgime C/20. Le vingtime cycle est donn
en insert pour les matriaux C-LiFePO
4
(~ 1.16, ~ 1.11, ~ 1.06).
Les matriaux C-LiFePO
4
(Li/Fe ~ 1.16 et ~ 1.11) sont trs proches en composition et
en nature (prsence dun taux similaire dions Fe
3+
) du matriau C-LiFePO
4
(Li/Fe ~ 1.06),
ils prsentent nanmoins des performances lectrochimiques nettement infrieures. Par
consquent, on peut penser que la nature du prcurseur lithi a une influence sur la
microstructure et sur le comportement lectrochimique des matriaux en batteries. Il faut
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre III
Magali Maccario 30 novembre 2007
47
cependant aussi garder lesprit que ces matriaux ne sont pas purs, prsence de Fe
2
P
2
O
7
ou dions Fe
3+
supplmentaires, ce qui peut galement jouer sur leurs proprits
lectrochimiques en batteries au lithium.
III5 Caractrisations morphologiques
La taille des particules ainsi que leur morphologie ont t tudies par Microscopie
Electronique Balayage (MEB), la Figure III-5 donne une comparaison des cinq matriaux.
On peut noter une inhomognit dans la distribution de taille des particules. En effet, les
clichs raliss avec les plus faibles grossissements montrent une distribution de gros agrgats
avec un diamtre de 20 - 30 m mais galement des plus petits de diamtre proche de 1 m. Il
y a aussi de nombreuses grosses particules (~ 500 nm) dans les quatre matriaux C-LiFePO
4
(Li/Fe ~ 1.16, ~ 1.11, ~ 1.00 et ~ 0.95). Leur prsence est probablement lie la nature du
(des) prcurseur(s) de lithium utilis(s) lors de la synthse - Li
2
CO
3
Li
3
PO
4
pour les
matriaux C-LiFePO
4
dont le rapport Li/Fe est gal ~ 1.16 et ~ 1.11 et LiH
2
PO
4
Li
3
PO
4
pour les matriaux C-LiFePO
4
dont le rapport Li/Fe est gal ~ 1.00 et ~ 0.95, alors que
Li
3
PO
4
est utilis seul pour le matriau dont le rapport Li/Fe est gal ~ 1.06. En effet le
prcurseur de lithium utilis favoriserait plus ou moins la croissance des particules malgr la
prsence du carbone, qui joue un rle dinhibiteur de croissance des particules lors de la
synthse. On peut donc penser que les prcurseurs comme le carbonate de lithium et
lhydrognophosphate de lithium favorisent la croissance des particules par rapport au
phosphate de lithium.
Dautre part, il est intressant de comparer les rsultats obtenus par MEB et les tailles
des domaines de cohrence dtermines grce au profil des raies de diffraction des rayons X.
En effet, cette dernire technique est plus sensible aux particules primaires de petite taille
plutt quaux particules de grosse taille, ce qui explique les raies larges des diagrammes de
diffraction des rayons X. On constate que les petites particules observes par MEB sont de
lordre de 50 100 nm en bon accord avec la taille des domaines de cohrence dtermines
par DRX, ce qui signifie que ce sont des particules primaires.
Les surfaces spcifiques mesures pour les cinq matriaux par la mthode BET varient
entre 15 et 20 m/g, en bon accord avec des surfaces BET plus faibles pour les matriaux
prsentant les particules primaires les plus grosses.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre III
Magali Maccario 30 novembre 2007
48
C-LiFePO
4
(Li/Fe ~ 1.00)
6.0 m
600 nm
60 m
C-LiFePO
4
(Li/Fe ~ 1.06)
6.0 m
60 m
600 nm
C-LiFePO
4
(Li/Fe ~ 0.95)
6.0 m
60 m
600 nm
600 nm
C-LiFePO
4
(Li/Fe ~ 1.11)
6.0 m
60 m
600 nm
600 nm
C-LiFePO
4
(Li/Fe ~ 1.16)
60 m
6.0 m
600 nm
600 nm
Figure III-5 : Clichs de microscopie lectronique balayage des chantillons C-LiFePO
4
synthtiss avec
diffrents rapports Li/Fe (~ 1.16, ~ 1.11, ~ 1.06, ~ 1.00 et ~ 0.95).
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre III
Magali Maccario 30 novembre 2007
49
III-6 Conclusions
Les matriaux C-LiFePO
4
tudis dans ce chapitre ont t synthtiss partir de
diffrents prcurseurs de lithium, Li
3
PO
4
, Li
2
CO
3
- Li
3
PO
4
et LiH
2
PO
4
- Li
3
PO
4
afin de faire
varier le rapport nominal Li/Fe et de tenter ainsi de synthtiser des composs de type olivine
valence mixte (couple Fe
3+
/Fe
2+
dans le site du mtal au lieu de Fe
2+
uniquement) et former
ainsi la solution-solide Li
1+y
Fe
1-y
PO
4
autour de la composition LiFePO
4
stoechiomtrique. En
effet, de tels matriaux prsenteraient a priori une conductivit lectronique leve, qui
favoriserait lobtention de bonnes performances lectrochimiques en batteries au lithium,
moins dpendantes des conditions de synthse et de la microstructure des chantillons (taille
des particules et organisation du revtement carbon). Les cinq matriaux C-LiFePO
4
tudis
prsentent des rapports Li/Fe nominaux variant de ~ 1.16 ~ 0.95 ; la combinaison diffraction
des rayons X / spectroscopie Mssbauer a montr la prsence de limpuret Fe
2
P
2
O
7
dans les
matriaux C-LiFePO
4
avec un rapport Li/Fe 1 alors que des ions Fe
3+
sont prsents dans les
matriaux C-LiFePO
4
prsentant un rapport Li/Fe > 1. Cependant aucun des matriaux
tudis ne prsente, a priori, les caractristiques dune solution-solide Li
1+y
Fe
1-y
PO
4
. Une
tude structurale plus prcise sur un de ces matriaux sera prsente dans le chapitre suivant
afin de conforter ce rsultat.
Parmi les cinq matriaux tudis, seul le matriau C-LiFePO
4
(Li/Fe ~ 1.06) prsente
des performances lectrochimiques intressantes en batteries au lithium, avec une faible
polarisation et une bonne capacit rversible. Pour les autres chantillons tudis, il semble
que linfluence de la microstructure soit un paramtre clef lobtention de bonnes
performances en batteries au lithium, sans toutefois ngliger limpact que peuvent avoir les
impurets sur leur comportement lectrochimique. En effet, quatre des matriaux C-LiFePO
4
tudis (obtenus partir du carbonate et de lhydrognophosphate de lithium comme
prcurseurs lithis) prsentent un nombre important de grosses particules (> 500 nm de
diamtre), qui sont nfastes de bonnes performances lectrochimiques.
Suite aux rsultats obtenus lors de cette tude prliminaire, le prcurseur lithi Li
3
PO
4
a t retenu pour la synthse des matriaux tudis dans la suite de ce manuscrit selon le
protocole tabli par le CEA. En effet, la suite de ce travail est axe sur ltude de limpact des
conditions de synthse (temprature, dure et vitesse du traitement thermique) sur les
proprits physico-chimiques, structurales et lectrochimiques de matriaux de type olivine
LiFePO
4
.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre III
Magali Maccario 30 novembre 2007
50
Bibliographie du Chapitre III
1
S. Franger, F. Le Cras, C. Bourbon, H. Rouault, Electrochemical And Solid State
Letters, 5 (2002), A231-A233.
2
D. K. Kim, H. M. Park, S. J. Jung, Y. U. Jeong, J. H. Lee, J. J. Kim, Journal Of Power
Sources, 159 (2006), 237-240.
3
P. S. Herle, B. Ellis, N. Coombs, L. F. Nazar, Nature Materials, 3 (2004), 147-152.
4
J. J. Chen, M. S. Whittingham, Electrochemistry Communications, 8 (2006), 855-858.
5
C. Gleitzer, European Journal of Solid State Inorganic Chemistry, 28 (1991), 77-91.
6
S. Y. Chung, J. T. Bloking, Y. M. Chiang, Nature Materials, 1 (2002), 123-128.
7
M. S. Whittingham, Y. N. Song, S. Lutta, P. Y. Zavalij, N. A. Chernova, Journal Of
Materials Chemistry, 15 (33) (2005), 3362-3379.
8
C. Delacourt, L. Laffont, R. Bouchet, C. Wurm, J. B. Leriche, M. Morcrette, J. M.
Tarascon, C. Masquelier, Journal Of The Electrochemical Society, 152 (5) (2005),
A913-A921.
9
M. M. Thackeray, Nature materials, 1 (2002), 81-82.
10
N. Ravet, A. Abouimrane, M. Armand, Nature materials, 2 (2003), 702.
11
C. Delacourt, C. Wurm, L. Laffont, J. B. Leriche, C. Masquelier, Solid State Ionics,
177 (2006), 333-341.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
51
Chapitre IV
Influence des conditions de synthse sur les proprits physico-
chimiques, morphologiques et lectrochimiques de matriaux de
structure olivine LiFePO
4
IV-1 Synthse des matriaux ............................................................................................ 52
IV-2 Caractrisations physico-chimiques ........................................................................ 53
IV-3 Caractrisations structurales : dtermination de la distribution cationique........... 58
IV-4 Caractrisations magntiques.................................................................................. 64
IV-5 Mesures de conductivit lectronique...................................................................... 66
IV-6 Caractrisations par spectroscopie infrarouge ....................................................... 67
IV-7 Caractrisation par spectroscopie Raman............................................................... 72
IV-8 Caractrisations texturales ...................................................................................... 80
IV-9 Caractrisations lectrochimiques........................................................................... 83
IV-10 Conclusions............................................................................................................ 90
Bibliographie du Chapitre IV........................................................................................... 92
Comme on a pu le constater grce ltat de lart sur les matriaux de type LiFePO
4
et
au chapitre prcdent, les conditions de synthse ont une grande influence sur les
performances lectrochimiques de C-LiFePO
4
et de nombreuses tudes ont t menes pour
dterminer le facteur clef loptimisation de ces performances. Le but de cette partie est, dans
un premier temps, de dterminer linfluence que peuvent avoir les diffrentes conditions de
synthse (temprature et traitement thermique), aprs activation mcano-chimique du
mlange des prcurseurs, sur les matriaux obtenus selon le protocole de synthse mis au
point par le CEA. En effet, daprs les tudes prliminaires, les matriaux C-LiFePO
4
obtenus
par le CEA prsentent des proprits lectrochimiques intressantes mais la relation entre ces
bonnes performances et les caractristiques des matriaux nest pas tablie. Pour faire ce lien,
des caractrisations structurales et physico-chimiques approfondies des matriaux seront
ralises, puis dans un second temps, nous corrlerons ces proprits physico-chimiques aux
performances lectrochimiques.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
52
IV-1 Synthse des matriaux
Les matriaux C-LiFePO
4
ont t obtenus par le traitement thermique du mlange des
prcurseurs ayant subi une activation mcano-chimique. Suite ltude prliminaire dcrite
au Chapitre III qui a permis doptimiser le choix du prcurseur de lithium pour le mode de
synthse appliqu cette tude, ce chapitre porte sur linfluence du traitement thermique.
Pour cela deux traitements thermiques sous atmosphre dargon et deux tempratures (575C
et 800C) de synthse ont t choisis.
Les ractifs, le phosphate de fer et le phosphate de lithium (Aldrich), sont
mlangs de telle sorte avoir le rapport Li/Fe gal 1.06, prcurseur de lithium et rapport
qui ont donn les proprits lectrochimiques les plus intressantes lors de ltude
prliminaire dcrite au Chapitre III. A ce mlange de prcurseurs sont ajouts 10 % en masse
de cellulose (Aldrich).
Le broyat obtenu, aprs quatre squences de broyage de 1 h 30, est trait
thermiquement dans un four tubulaire selon deux modes (rapide ou lent) et deux
tempratures (575C ou 800C). Ces conditions de synthse ont t choisies de telle sorte
accentuer les diffrences de proprits physico-chimiques (taille des particules, conductivit
lectronique, ) entre les diffrents matriaux synthtiss.
Traitement thermique lent :
Ce traitement thermique consiste chauffer ~ 10 g du mlange de prcurseurs 575C
(ou 800C) la vitesse de 2C/min, une fois la temprature atteinte le mlange est
immdiatement refroidi 2C/min. Les chantillons obtenus 575C et 800C seront
respectivement nomms Fe
575-slow
et Fe
800-slow
dans la suite de ce chapitre. La dure du
traitement thermique est respectivement de 9 h ou de 13 h, avec ~ 1 h 15 min ou ~ 5 h
au-del de 500C, selon la temprature maximale : 575C ou 800C.
Traitement thermique rapide :
Environ 10 g de mlange de prcurseurs sont introduits dans un four tubulaire
prchauff la temprature de 575C (ou 800C). Ce mlange est maintenu cette
temprature pendant 15 minutes avant d'tre refroidi par une trempe lair. Les
chantillons obtenus 575C et 800C seront respectivement nomms Fe
575-fast
et
Fe
800-fast
dans la suite de ce chapitre.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
53
IV-2 Caractrisations physico-chimiques
IV-2-1 Diffraction des rayons X
Les diffractogrammes des rayons X des matriaux C-LiFePO
4
(Fe
800-fast
, Fe
800-slow
,
Fe
575-fast
et Fe
575-slow
) sont donns la Figure IV-1. Tous les pics observs peuvent tre
indexs dans une maille orthorhombique (groupe d'espace Pnma) avec les paramtres de
maille a ~ 10.33 , b ~ 6.009 et c ~ 4.695 . Aucune impuret n'a t dtecte par DRX,
les quatre chantillons tudis sont donc considrs comme purs du point de vue de la
diffraction des rayons X. La comparaison des largeurs mi-hauteur (FWHM) pour les raies
de diffraction les plus intenses : (101), (111), (211) et (311) est donne dans le Tableau IV-1
pour les quatre matriaux tudis. Ce tableau montre comme attendu que laugmentation de la
temprature de synthse provoque une augmentation de la cristallinit (taille des domaines de
cohrence plus grande). La taille des domaines de cohrence, calcule grce la formule de
Scherrer, est denviron 70 nm pour Fe
575-fast
et Fe
575-slow
et denviron 100 nm pour Fe
800-fast
et
Fe
800-slow
, quelle que soit la direction cristallographique considre.
IV-2-2 Analyses chimiques
Le Tableau IV-2 donne les rsultats des analyses chimiques dont le pourcentage
massique de carbone qui est compris entre 2.91 et 3.43 wt% pour les quatre matriaux. Ces
dosages chimiques montrent, comme attendu daprs la composition nominale, de lgers
excs de lithium et de phosphore par rapport au fer (rapports Li/Fe et P/Fe > 1). Cela suggre
donc la prsence dune impuret riche en lithium et en phosphore et/ou la formation dun
matriau de structure olivine de composition Li
1+y
Fe
1-y
PO
4
, impliquant la prsence dions
lithium dans le site du mtal de transition et donc la prsence dions Fe
3+
dans le matriau
pour permettre la compensation des charges, comme cela a t envisag au chapitre prcdent.
Ltude structurale dtaille sera prsente dans la suite de ce chapitre.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
54
20 40 60 80
Fe
575-slow
Fe
800-slow
Fe
575-fast
Fe
800-fast
I
(
A
.
U
.
)
2
Co
()
a)
b)
20 25 30 35 40 45
Fe
575-slow
Fe
575-fast
Fe
800-slow
Fe
800-fast
(
3
1
1
)
(
2
1
1
)
(
1
1
1
)
(
1
0
1
)
2
Co
()
Figure IV-1 : a) Diagrammes de diffraction des rayons X obtenus pour les quatre matriaux C-LiFePO
4
synthtiss avec diffrents traitements thermiques et diffrentes tempratures, b) Agrandissement de ces
diagrammes de diffraction des rayons X dans le domaine angulaire [17 - 45] (2).
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
55
Tableau IV-1 : Comparaison des largeurs mi-hauteur (FWHM) pour quelques raies slectionnes dans
les diagrammes de diffraction des rayons X ; ces largeurs de raies ont t corriges de la contribution
instrumentale du diffractomtre. Cette correction est ralise avec les donnes obtenues pour LaB
6
. La
taille des domaines de cohrence (L) a t estime grce la formule de Scherrer
FWHM(2) = 0.9/(L.cos) o = 1.789 pour la radiation K du cobalt.
Tableau IV-2 : Rsultats des dosages chimiques des lments C, Li, Fe et P pour Fe
800-fast
, Fe
800-slow
, Fe
575-fast
et Fe
575-slow
, ainsi que la dtermination des compositions Li : Fe : P des matriaux.
C
(wt.%)
Li/Fe Li/P Fe/P Li : Fe : P composition
(P = 1)
Fe
800-fast
2.91 1.06 1.04 0.98 Li
1.04
Fe
0.98
P
Fe
800-slow
3.23 1.05 1.08 0.99 1.05 0.95 0.98 Li
1.05
Fe
0.98
P - Li
0.99
Fe
0.95
P
Fe
575-fast
3.22 1.06 1.08 1.02 1.07 0.96 0.99 Li
1.02
Fe
0.96
P - Li
1.07
Fe
0.99
P
Fe
575-slow
3.43 1.07 1.02 0.96 Li
1.02
Fe
0.96
P
IV-2-3 Analyses par spectroscopie Mssbauer
Lanalyse des matriaux C-LiFePO
4
a galement t ralise par spectroscopie
Mssbauer. Les spectres enregistrs pour ces quatre chantillons sont donns la Figure
IV-2. Lajustement des spectres calcul et exprimental est ralis en utilisant une
combinaison de raies de profil lorentzien. Comme le montre la Figure IV-2b, deux doublets
sont ncessaires pour les quatre matriaux pour ajuster le spectre calcul au spectre
exprimental.
Diffraction line (101) (111) (211) (311)
FWHM () 0.07 0.10 0.08 0.09
Fe
800-fast
L (nm) 130 100 120 110
FWHM () 0.08 0.10 0.09 0.10
Fe
800-slow
L (nm) 120 90 110 100
FWHM () 0.13 0.15 0.14 0.16
Fe
575-fast
L (nm) 75 60 70 60
FWHM () 0.13 0.15 0.14 0.16
Fe
575-slow
L (nm) 75 65 70 65
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
56
-2 -1 0 1 2 3 4
Fe
800-slow
Fe
575-slow
Fe
800-fast
Fe
575-fast
Velocity (mm.s
-1
)
A
obs.
A
calc.
A
b
s
o
r
p
t
i
o
n
(
A
.
U
.
)
-2 -1 0 1 2 3 4
A
b
s
o
r
t
p
i
o
n
(
A
.
U
.
)
Velocity (mm.s
-1
)
a)
b)
Fe
575-fast
Figure IV-2 : a) Spectres Mssbauer obtenus temprature ambiante pour Fe
800-fast
, Fe
800-slow
Fe
575-fast
et
Fe
575-slow
, b) Lagrandissement du spectre de Fe
575-fast
permet de distinguer les doublets ncessaires
lajustement des spectres calcul et exprimental.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
57
Lanalyse des paramtres (dplacement isomrique (), clatement quadrupolaire ()
et largeur mi-hauteur ()) montre que, cette fois, tous les chantillons contiennent
principalement du Fe
2+
dans un environnement octadrique ( ~ 1.22 mm.s
-1
, ~ 2.95 mm.s
-1
et ~ 0.26 mm.s
-1
), mais galement une faible quantit de Fe
3+
, de lordre de 5 6 at. %
( ~ 0.45 mm.s
-1
, ~ 0.76 mm.s
-1
et ~ 0.61 mm.s
-1
) (cf. Tableau IV-3). Le doublet relatif
aux ions Fe
2+
est caractris par un fort clatement quadrupolaire, d la configuration
lectronique haut spin (3d
6
) de cet ion mais galement un environnement local asymtrique
des ions Fe
2+
dans la structure olivine. Les paramtres Mssbauer reports pour Fe
2+
sont trs
proches de ceux publis dans la littrature pour LiFePO
4
[1-3]. Notons que les caractristiques
Mssbauer dtermines pour les ions Fe
3+
ne correspondent pas celles qui seraient obtenues
pour une impuret de type FePO
4
.nH
2
O (0 n 2) [4-6] ou pour Fe
2
O
3
. Pour ce dernier, qui
est magntique temprature ambiante, on attendrait la prsence dun sextuplet, d la leve
de dgnrescence produite par leffet Zeeman, sauf si la distribution de taille de particules est
infrieure 10 nm. Dans ce cas un effet de relaxation se produit et un doublet
superparamagntique est observ au lieu du sextuplet [7,8].
Tableau IV-3 : Paramtres hyperfins dtermins par spectroscopie Mssbauer pour les deux types dions
fer prsents dans les matriaux Fe
800-fast
, Fe
800-slow
, Fe
575-fast
et Fe
575-slow
( : dplacement isomrique, :
clatement quadrupolaire et : largeur mi-hauteur). Les valeurs donnes en italique correspondent
lion Fe
3+
prsent en moindre quantit. Les erreurs sont donnes entre parenthses, pour dterminer
lcart-type il suffit de les multiplier par 3.
(mm.s
-1
) (mm.s
-1
) (mm.s
-1
) % Site
1.217(2) 2.945(2) 0.259(1) 95 Fe
2+
[O
h
]
Fe
800-fast
0.4(1) 0.7(1) 0.6(1) 5 Fe
3+
1.220(2) 2.951(2) 0.256(1) 95 Fe
2+
[O
h
]
Fe
800-slow
0.5(1) 0.8(1) 0.67(6) 5 Fe
3+
1.224(2) 2.951(2) 0.262(1) 94 Fe
2+
[O
h
]
Fe
575-fast
0.45(6) 0.73(6) 0.54(4) 6 Fe
3+
1.219(2) 2.936(2) 0.258(1) 94 Fe
2+
[O
h
]
Fe
575-slow
0.43(6) 0.79(6) 0.53(6) 6 Fe
3+
Les largeurs mi-hauteur () obtenues pour les sites de Fe
2+
et Fe
3+
sont
significativement diffrentes, avec une largeur de 0.2 - 0.3 mm.s
-1
pour le premier et de
lordre de 0.6 mm.s
-1
pour le second. Pour un environnement discret, est attendue dans une
gamme de valeur comprise entre 0.2 mm.s
-1
et 0.3 mm.s
-1
. Cet largissement de la raie
relative aux ions Fe
3+
suggre donc une distribution dclatements quadrupolaires centre
~ 2.95 mm.s
-1
. Grce ces analyses par spectroscopie Mssbauer et les dosages chimiques, on
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
58
peut formuler diffrentes hypothses : (i) les ions Fe
3+
sont distribus statistiquement dans les
sites 4c avec les ions Li
+
et Fe
2+
dune phase olivine de formule Li
1+y
Fe
1-y
PO
4
, (ii) les ions
Fe
3+
sont prsents au sein dune phase amorphe non dtecte par diffraction des rayons X
[3,9] et (iii) les ions Fe
3+
sont prsents comme dfauts de surface dans le matriau [9]. Si lon
considre la premire hypothse, llargissement de la raie relative aux ions Fe
3+
serait d
une distribution denvironnement cationique (c'est--dire lectronique) qui rsulterait de la
prsence dions lithium ainsi que dions fer divalents et trivalents dans le mme site
cristallographique (4c), mais galement au fait que chaque octadre (Li,Fe)O
6
partage des
sommets avec quatre autres octadres (Li,Fe)O
6
. La largeur mi-hauteur serait leve
seulement pour les ions Fe
3+
car ces ions sont trs sensibles leur environnement direct du
fait dune configuration lectronique (3d
5
) symtrique alors que les ions Fe
2+
le sont moins du
fait dune configuration lectronique (3d
6
) asymtrique.
On peut donc rsumer les rsultats prcdents en considrant trois hypothses :
(i) prsence de lithium en excs dans la structure de type olivine ce qui
donnerait une formule chimique de type Li
1+y
Fe
1-y
PO
4
avec une distribution
cationique de type Li(Li
y
Fe
y
III
Fe
1-2y
II
)PO
4
,
(ii) mlange de lolivine LiFePO
4
avec une phase amorphe riche en Fe
3+
comme impuret,
(iii) LiFePO
4
avec des dfauts de surface impliquant la prsence de Fe
3+
.
IV-3 Caractrisations structurales : dtermination de la distribution
cationique
IV-3-1 Diffraction des rayons X
Pour dterminer prcisment la structure de ces matriaux et plus particulirement si
lhypothse (i) considrant la formation dune phase olivine de composition Li
1+y
Fe
1-y
PO
4
est
valide, les donnes de diffraction des rayons X et des neutrons ont t affines par la mthode
de Rietveld avec le programme Fullprof [10]. La combinaison de ces affinements permet de
dterminer les paramtres structuraux ainsi que la distribution cationique dans les sites du
lithium et du fer. Dans un premier temps, un affinement par la mthode de Le Bail est ralis,
il permet de dterminer les paramtres de maille ainsi que les paramtres de profil de la
fonction pseudo-Voigt utilise pour dcrire la forme des pics de diffraction. Puis, laffinement
par la mthode de Rietveld est men en considrant lhypothse structurale [Li]
4a
[Fe]
4c
PO
4
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
59
ainsi que les rapports Li/Fe et P/Fe gaux 1. En effet, bien que les dosages chimiques aient
rvl des rapports Li/Fe et P/Fe suprieurs 1, la diffraction des rayons X nest pas assez
sensible la prsence de lithium dans le site du fer pour prendre en compte ici lhypothse
structurale [Li]
4a
[Li
y
Fe
1-y
]
4c
PO
4
. Les ions Li, (Fe, P, O1, O2) et O3 occupent respectivement
les sites 4a (0, 0, 0), 4c (x, , z) et 8d (x, y, z) du groupe despace Pnma. Le profil des pics de
diffraction a t dcrit avec la fonction de Thompson-Cox-Hastings. Les effets de contraintes
et de tailles sont trs bien dcrits par un modle isotrope considrant respectivement des
contributions lorentzienne et gaussienne [10]. Dans ce cas, seuls les paramtres U et Y sont
affins, tandis que V et W sont fixs aux valeurs dtermines pour LaB
6
; les facteurs de
dplacement atomique isotrope sont galement affins. Les paramtres de maille et de
microstructure obtenus pour les quatre matriaux C-LiFePO
4
sont compars dans le Tableau
IV-4. On constate que les paramtres de maille obtenus sont gaux lcart-type prs ceux
publis pour LiFePO
4
[1,9,11]. Le rsultat dtaill de laffinement des donnes de diffraction
des rayons X enregistres pour Fe
800-fast
est prsent la Figure IV-3, qui donne la
comparaison des diagrammes de diffraction des rayons X exprimental et calcul, et dans le
Tableau IV-5. Les faibles valeurs des facteurs de reliabilit (R
wp
= 12.6 % et R
B
= 9.74 %)
ainsi que la bonne minimisation de la fonction diffrence I
obs.
I
calc.
montrent la qualit de
laffinement et suggrent donc une bonne description de la structure de Fe
800-fast
par une
structure olivine idale. Un rsultat similaire est obtenu pour les trois autres matriaux.
Tableau IV-4 : Comparaison des paramtres de maille et de microstructure dtermins par laffinement
par la mthode de Rietveld des donnes de diffraction des rayons X enregistres pour Fe
800-fast
, Fe
800-slow
,
Fe
575-fast
et Fe
575-slow
. Les affinements ont t raliss en considrant une fonction de profil de type
Thompson-Cox-Hastings, o < >
1/2
reprsente les contraintes et L la taille des domaines de cohrence.
a () b () c () V (
3
) < >
1/2
< L > ()
Fe
800-fast
10.3294(3) 6.0086(2) 4.6948(2) 291.38(1) 6.4(7) x 10
-4
740 20
Fe
800-slow
10.3318(4) 6.0093(2) 4.6955(1) 291.52(1) 5.4(6) x 10
-4
710 15
Fe
575-fast
10.3308(4) 6.0092(2) 4.6976(2) 291.63(2) 1.14(9) x 10
-3
440 10
Fe
575-slow
10.3280(3) 6.0067(2) 4.6959(2) 291.33(2) 9.6(1) x 10
-4
495 10
Les paramtres microstructuraux sont donns dans le Tableau IV-4, comme attendu
les matriaux Fe
800-slow
et Fe
800-fast
synthtiss haute temprature prsentent des tailles de
domaines de cohrence plus grandes que celles dtermines pour les matriaux Fe
575-slow
et
Fe
575-fast
synthtiss basse temprature. Les diffrences observes lorsque lon compare les
tailles des domaines de cohrence dtermines en appliquant la formule de Scherrer
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
60
(~ 100 nm et ~ 70 nm respectivement pour les matriaux synthtiss 800C et 575C)
celles calcules par laffinement ralis avec la fonction de Thompson-Cox-Hastings
(~ 70 nm et ~ 50 nm respectivement pour les matriaux synthtiss 800C et 575C) sont,
notre avis, dues des approximations diffrentes. Nanmoins, un mme ordre de tailles de
domaines de cohrence et une mme hirarchie sont obtenus pour les chantillons traits
575C et 800C (cf. Tableau IV-1 et Tableau IV-4 pour comparaison). On peut galement
constater que, comme attendu, les contraintes diminuent avec la croissance de la taille des
domaines de cohrence et par consquent avec la temprature.
20 25 30 35 40
I
(
A
.
U
.
)
2
Co
()
20 40 60 80 100 120
Yobs
Ycalc
Yobs-Ycalc
I
(
A
.
U
.
)
2
Co
()
Figure IV-3 : Comparaison des diagrammes de diffraction des rayons X exprimental et calcul pour Fe
800-fast
.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
61
Tableau IV-5 : Paramtres de structure et de profil obtenus par laffinement par la mthode de Rietveld
des donnes de diffraction des rayons X enregistres pour Fe
800-fast
.
Fe
800-fast
Space group : Pnma
a
= 10.3294(3)
b = 6.0086(2)
c
= 4.6948(2)
V = 291.38(1)
3
Site Wyckoff positions Occupancy B()
Li 4a 0 0 0 1 2(1)
Fe 4c 0.2823(3) 1/4 0.974(1) 1 1.0(2)
P 4c 0.0966(6) 1/4 0.422(1) 1 0.8(2)
O
l
4c 0.092(1) 1/4 0.747(3) 1 0.6(4)
O
2
4c 0.455(2) 1/4 0.203(2) 1 0.6(1)
O
3
8d 0.164(1) 0.051(2) 0.285(2) 1 0.8(1)
Conditions of the run
Temperature
Angular range
Number of points
Displacement sample holder (2)
Number of fitted parameters
300 K
5 2 120
6876
- 0.194(2)
24
Profile parameters :
Thompson-Cox-Hastings function
* LaB
6
values used as standard
Y = 0.088(2)
U = 0.029(5)
V = - 0.0017*
W = 0.00383*
Conventional Rietveld R-factors for points with Bragg contribution
R
wp
= 12.6 % ; R
B
= 9.74 %
Note : standard deviations have been multiplied by 3, the Scor parameter being 2.39.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
62
IV-3-2 Diffraction des neutrons
IV-3-2-a Prsence dions lithium dans le site du fer
Grce des longueurs de Fermi diffrentes (amplitude et signe) pour le lithium
(b(Li) = - 0.19.10
-12
cm) et le fer (b(Fe) = 0.945.10
-12
cm), la diffraction des neutrons permet
de dterminer prcisment la distribution cationique dans chaque site cristallographique. Pour
vrifier lhypothse (i) (Li)(Li
y
Fe
1-y
)PO
4
, cest dire la prsence dions lithium (Li(2)) en
excs dans le site du fer (4c (x, , z)), qui serait compense par la prsence dions Fe
3+
dans
le matriau, les affinements des diagrammes de diffraction des neutrons ont t raliss par la
mthode de Rietveld avec la somme des taux doccupation du Li(2) et du Fe dans le site 4c
(x, , z) contrainte tre gale 1. Les rsultats de ces affinements sont donns dans le
Tableau IV-6. Les quantits de lithium dtermines comme tant dans le site 4c du fer sont
respectivement gales 0.00(1), 0.00(1), 0.01(2) et 0.009(8) pour Fe
800-fast
, Fe
800-slow
, Fe
575-fast
et Fe
575-slow
. Les rsultats obtenus sont trs proches pour les quatre matriaux et montrent quil
ny a pas dions lithium dans le site du fer. Cela est galement confirm par la comparaison de
la simulation du diagramme de diffraction des neutrons ralise en fixant 5 at. % le taux
dions lithium dans le site cristallographique du fer (Li(Li
0.05
Fe
0.95
)PO
4
) au rsultat de
laffinement par la mthode de Rietveld des donnes de diffraction des neutrons pour Fe
800-fast
(cf. Figure IV-4). Lhypothse (i) nest donc pas valide et ne permet pas dexpliquer la
prsence de ~ 5 - 6 at. % dions Fe
3+
dans les matriaux.
IV-3-2-b Echange cationique entre les ions fer et lithium
La possibilit dun change entre les ions lithium et fer des sites 4a et 4c a galement
t considre par similitude aux rsultats obtenus par le groupe de Whittingham [12] pour
des matriaux C-LiFePO
4
synthtiss par la voie hydrothermale. Laffinement par la mthode
de Rietveld des donnes de diffraction des neutrons a, dans ce cas, t men en considrant la
distribution cationique (Li
1-y
Fe
y
)
4a
(Fe
1-y
Li
y
)
4c
PO
4
. Les rsultats obtenus montrent quil ny a
pas dchange entre les sites 4a et 4c.
En conclusion de cette partie, on peut dire que les quatre matriaux C-LiFePO
4
,
Fe
800-fast
, Fe
800-slow
, Fe
575-fast
et Fe
575-slow
, sont parfaitement dcrits par une structure LiFePO
4
olivine ordonne et stoechiomtrique.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
63
Tableau IV-6 : Paramtres de maille obtenus par laffinement par la mthode de Rietveld des donnes de
diffraction des neutrons pour Fe
800-fast
, Fe
800-slow
, Fe
575-fast
et Fe
575-slow
en considrant lhypothse (i), soit la
prsence dions lithium en excs dans le site du fer (4c(x, , z)). Les taux doccupation du Fe et du Li dans
le site du fer 4c (x ~ 0.281, , z ~ 0.977) sont galement donns.
Occupancy in the Fe site
(4c(x, , z)), x ~ 0.281,
z ~ 0.977
a () b () c () V (
3
) Fe Li(2)
Fe
800-fast
10.3309(7) 6.0094(4) 4.6950(3) 291.48(2) 1.00(1) 0.00(1)
Fe
800-slow
10.3315(9) 6.0094(2) 4.6951(4) 291.50(4) 1.00(1) 0.00(1)
Fe
575-fast
10.330(1) 6.0085(7) 4.6962(5) 291.47(2) 0.99(2) 0.01(2)
Fe
575-slow
10.3298(7) 6.0083(4) 4.6970(3) 291.52(3) 0.991(8) 0.009(8)
20 40 60 80 100
Li(Li
0.05
Fe
III
0.05
Fe
II
0.90
)PO
4
LiFePO
4
(Fe
800-fast
)
Yobs, Ycal, Yobs - Ycal
I
(
A
.
U
.
)
2
=1.596 A
()
20 30 40
I
(
A
.
U
.
)
2
=1.596 A
()
Figure IV-4 : Affinement par la mthode de Rietveld du diagramme de diffraction des neutrons de
Fe
800-fast
(hypothse structurale : LiFePO
4
stoechiomtrique et ordonn) compar laffinement ralis en
tenant compte de lhypothse Li(Li
0.05
Fe
0.95
)PO
4
avec la prsence de 0.05 at. % dions lithium dans le site
cristallographique du fer.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
64
IV-4 Caractrisations magntiques
La Figure IV-5a reprsente lvolution du rapport H/M, avec H le champ appliqu
(dans notre cas fix 10 kOe) et M laimantation molaire. Les quatre chantillons Fe
575-fast
,
Fe
800-fast
, Fe
575-slow
et Fe
800-slow
prsentent le mme comportement avec une transition
antiferromagntique ~ 50.5 K, ces rsultats sont en bon accord avec ceux rapports pour
lolivine LiFePO
4
dans la littrature [13-15]. Les constantes de Curie des quatre matriaux
sont gales 3.3 emu.K.mol
-1
, 3.5 emu.K.mol
-1
, 3.5 emu.K.mol
-1
et 3.6 emu.K.mol
-1
respectivement pour Fe
575-fast
, Fe
800-fast
, Fe
575-slow
et Fe
800-slow
:
eff
est donc compris entre
5.14
B
pour Fe
575-fast
et 5.37
B
pour Fe
800-slow
. Les constantes de Curie ont t calcules
partir de la pente de la partie linaire de la courbe H/M en fonction de T, soit dans le domaine
de temprature [150 - 300] K. Les valeurs des constantes de Curie dtermines pour les quatre
matriaux sont proches ; cependant, elles sont significativement diffrentes de la constante de
Curie thorique qui est de 3.00 emu.K.mol
-1
(
eff
= 4.90
B
) pour LiFePO
4
idal. Si lon
considre la faible quantit de Fe
3+
dtermine par spectroscopie Mssbauer, la constante de
Curie serait de lordre de ~ 3.05 emu.K.mol
-1
dans lhypothse de 6 at. % de Fe
3+
. Cette
valeur nest donc toujours pas conforme aux constantes de Curie exprimentales obtenues.
Cette diffrence entre thorie et exprience pourrait suggrer que les matriaux C-LiFePO
4
tudis contiennent une impuret. On peut en effet citer ltude rcente de Ravet et al. [15]
qui synthtisent des matriaux LiFePO
4
prsentant des faibles taux dimpurets cristallises
mais une volution significative de la constante de Curie. Ils obtiennent
eff
= 5.22
B
, soit
C = 3.40 emu.K.mol
-1
, pour un matriau LiFePO
4
quils considrent pur contre
eff
= 5.47
B
, soit C = 3.74 emu.K.mol
-1
, pour un matriau LiFePO
4
prsentant 1 % de
Li
3
Fe
2
(PO
4
)
3
cristallis [15].
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
65
0 50 100 150 200 250 300
30
40
50
60
70
80
90
100
110
120
Fe
800-fast
Fe
800-slow
Fe
575-fast
Fe
575-slow
10 kOe
H
/
M
(
m
o
l
/
e
m
u
)
T(K)
0.0
5.0x10
3
1.0x10
4
1.5x10
4
2.0x10
4
0
50
100
150
200
250
300
350
298 K
5 K
H (Oe)
Fe
800-fast
Fe
800-slow
Fe
575-fast
Fe
575-slow
M
(
e
m
u
/
m
o
l
)
b)
a)
Figure IV-5 : a) Evolution du rapport H/M en fonction de la temprature (H est le champ appliqu (fix
10 kOe) et M laimantation molaire), b) Evolution de laimantation molaire en fonction du champ
appliqu T (5 K et 298 K) pour Fe
800-fast
, Fe
800-slow
, Fe
575-fast
et Fe
575-slow
.
La Figure IV-5b montre que lvolution de laimantation molaire en fonction du
champ appliqu est linaire quelle que soit la temprature de mesure (5 ou 298 K) et le
matriau tudi. La comparaison de ces rsultats avec ceux publis par le groupe de Julien
[16-18] montre clairement que nos chantillons ne contiennent pas dimpurets
ferromagntiques ou ferrimagntiques cristallises comme Fe
2
O
3
ou Fe
2
P. Ces rsultats sont
en bon accord avec ceux obtenus par spectroscopie Mssbauer qui ne montrent pas, par
exemple, le spectre caractristique de Fe
2
O
3
.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
66
Ces mesures magntiques nous permettent en consquence de conclure que les
matriaux tudis ne contiennent pas dimpurets ferromagntiques ou ferrimagntiques
cristallises riches en ions Fe
3+
. Cependant, lhypothse (ii) ne peut pas tre compltement
carte car la prsence dimpurets magntiques non ou mal cristallises ne peut pas tre
totalement exclue.
IV-5 Mesures de conductivit lectronique
Lvolution de la conductivit lectronique, mesure avec la mthode des quatre
pointes, en fonction de la temprature est donne la Figure IV-6. Linfluence de la
temprature de synthse est vidente. En effet les matriaux synthtiss plus haute
temprature, Fe
800-fast
et Fe
800-slow
, prsentent une conductivit suprieure dau moins cinq
ordres de grandeur en comparaison avec les matriaux synthtiss 575C, Fe
575-fast
et
Fe
575-slow
. Les nergies dactivation calcules aux environs de 300 K diminuent avec
laugmentation de la temprature de synthse. On peut donc galement noter que malgr une
dgradation seulement partielle de la cellulose 575C, les nergies dactivation obtenues
pour Fe
575-fast
et Fe
575-slow
, respectivement 0.30 eV et 0.20 eV, sont infrieures celle obtenue
pour un matriau LiFePO
4
pur (0.60 eV) [19]. Ce rsultat montre bien limportance de la
cellulose, mme mal dgrade, sur la conductivit du systme.
0 5 10 15 20 25 30 35
-11
-10
-9
-8
-7
-6
-5
-4
-3
-2
-1
Ea=0.04 eV
Ea=0.04 eV
Ea=0.20 eV
Ea=0.30 eV
Fe
800-fast
Fe
800-slow
Fe
575-fast
Fe
575-slow
1000/T (K
-1
)
l
o
g
(
S
.
c
m
-
1
)
Figure IV-6 : Mesures de conductivit lectronique ralises avec la mthode des quatre pointes dans le
domaine de temprature [30 300] K pour Fe
800-fast
, Fe
800-slow
, Fe
575-fast
et Fe
575-slow
.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
67
IV-6 Caractrisations par spectroscopie infrarouge
Pour identifier les dfauts structuraux et tudier la structure courte distance des
matriaux, la spectroscopie infrarouge est une technique adapte. Afin de tenter de dterminer
do proviennent les ions fer trivalents, la caractrisation de nos matriaux C-LiFePO
4
a t
effectue par spectroscopie infrarouge lInstitut des Sciences Molculaires de Talence.
Comme cela a dj t mentionn prcdemment, la structure de lolivine LiFePO
4
est
dcrite dans le groupe despace Pnma galement not
16
2h
D selon les rgles de Schonflies. La
maille de base est centrosymtrique avec quatre units formulaires. Par consquent, 71 modes
optiques sont attendus :
= 11A
g
+ 7B
1g
+ 11B
2g
+ 7B
3g
+ 13B
1u
+ 9B
2u
+ 13B
3u
Les 35 modes ungerade (u) (13B
1u
+ 9B
2u
+ 13B
3u
) sont actifs en spectroscopie
infrarouge (IR) mais inactifs en spectroscopie Raman, alors que les 36 modes gerade (g) sont
actifs en spectroscopie Raman et inactifs en spectroscopie IR. Ceci signifie que le nombre de
bandes prvues est lev.
La Figure IV-7 permet la comparaison des spectres infrarouge des matriaux Fe
575-fast
et Fe
800-fast
dans le domaine de nombres donde [4000 - 850] cm
-1
. Cette figure montre une
drive de la ligne de base et une intensit absolue plus importante du spectre du matriau
Fe
800-fast
. Ces deux phnomnes sont dus une conductivit suprieure de cinq ordres de
grandeur du revtement de carbone du matriau Fe
800-fast
compar celui du matriau
Fe
575-fast
, comme on vient de le voir au paragraphe prcdent. En effet, la temprature
diffrente de dgradation de la cellulose (800C pour Fe
800-fast
et 575C pour Fe
575-fast
) induit
la formation dun revtement carbon plus ou moins conducteur. Cette conductivit plus
importante pour Fe
800-fast
implique alors une plus grande absorption du signal. Des rsultats
similaires ont t obtenus pour les spectres infrarouge des autres matriaux synthtiss 575
et 800C (Fe
575-slow
et Fe
800-slow
), qui selon leur temprature de synthse prsentent ou non une
drive de la ligne de base et une absorption plus grande de lintensit.
Ces deux spectres montrent des bandes bien spares et aucune diffrence de largeur
des bandes, comme cela est soulign dans linsert donn la Figure IV-7. Cela montre que
les matriaux Fe
800-fast
et Fe
575-fast
prsentent une bonne cristallinit et quil ny a pas de
perturbations des vibrations intramolculaires qui pourraient tre induites par des dfauts
structuraux. En effet, comme on peut le voir la figure 3 de la rfrence [20], qui est
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
68
reproduite la Figure IV-8, la comparaison des spectres infrarouge enregistrs pour des
matriaux LiFePO
4
de cristallinits trs diffrentes montre que des bandes larges et non
spares sont attendues pour les composs vitreux.
1250 1000 750
1
0
4
1
9
4
8
9
7
9
1
0
6
5
1
0
9
6
1
1
4
1
Fe
800-fast
Fe
575-fast
K
u
b
e
l
k
a
-
M
u
n
k
u
n
i
t
s
Wavenumber (cm
-1
)
4000 3500 3000 2500 2000 1500 1000
Fe
800-fast
Fe
575-fast
K
u
b
e
l
k
a
-
M
u
n
k
u
n
i
t
s
Wavenumber (cm
-1
)
Figure IV-7 : Spectres FTIR des matriaux Fe
575-fast
et Fe
800-fast
, avec en insert un agrandissement de la
zone de nombres donde [1250 750] cm
-1
(Il est noter que cet insert prsente des spectres en intensit
relative).
Figure IV-8 : Comparaison des spectres FTIR de composs LiFePO
4
vitreux et cristallis [20].
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
69
Les spectres infrarouge des matriaux Fe
575-fast
et Fe
800-fast
donns la Figure IV-7 ne
prsentent pas de diffrences significatives que ce soit dans la position des bandes ou dans
leur largeur. Toutes les bandes observes sont situes entre 1250 et 850 cm
-1
. Ces bandes sont
lies aux modes dlongation des anions (PO
4
)
3-
,
1
et
3
, qui sont respectivement les modes
symtrique et antisymtrique des liaisons P-O [21]. Dun point de vue thorique, pour un
ttradre parfait dcrit dans le groupe de symtrie T
d
une seule bande triplement dgnre,
3
, est attendue dans le domaine [1200 850] cm
-1
. Pour les ttradres PO
4
distordus de
symtrie C
s
de la structure olivine, daprs lanalyse de la thorie des groupes la vibration
3
prsente une quintuple leve de dgnrescence (2B
1u
+ B
2u
+ 2B
3u
) et la vibration
1
est
active et dcompose en deux bandes (B
1u
+ B
3u
) [22]. En effet dans la structure olivine
LiFePO
4
, les ttradres PO
4
prsentent des distorsions lies au partage dartes et de sommets
avec les octadres FeO
6
et LiO
6
. Sur le spectre exprimental quatre bandes principales sont
observes : deux fines 1141 cm
-1
et 1096 cm
-1
et deux larges 1065 cm
-1
et 979 cm
-1
, qui
prsentent chacune un paulement respectivement 1041 cm
-1
et 948 cm
-1
. Les trois
premires bandes (1141 cm
-1
, 1096 cm
-1
et 1065 cm
-1
) correspondent
au mode
3
et celle
situe 979 cm
-1
au mode
1
. Cette dernire est galement active en spectroscopie Raman (cf.
paragraphe suivant), ce qui permet de lidentifier comme tant sans ambigut celle associe
au mode dlongation symtrique [22]. La diffrence entre le nombre de bandes thoriques et
le nombre de bandes exprimentales sexplique trs probablement par une trs faible intensit
ou un chevauchement pour certaines dentre elles qui ne permet pas de les rsoudre sur le
spectre exprimental. Des rsultats similaires ont t rapports par Paques-Ledent et al. [22],
Ait-Salah et al. [17] et Burba et al. [23].
La Figure IV-9 compare les spectres FTIR obtenus pour la cellulose (C
6
H
10
O
5
)
n
avant
traitement thermique, aprs 15 minutes 575C sous une atmosphre dargon (conditions de
synthse utilises pour Fe
575-fast
) et aprs 15 minutes 800C sous atmosphre dargon
(conditions de synthse utilises pour Fe
800-fast
). Les deux chantillons tudis, Fe
575-fast
et
Fe
800-fast
, prsentent environ 3 % massique de carbone (cf. paragraphe IV-2-2 de ce mme
chapitre). Le spectre de la cellulose avant tout traitement thermique montre comme attendu
des bandes dans le domaine de nombres donde [3750 2750] cm
-1
attribues aux vibrations
dlongation des liaisons O-H et C-H et dans le domaine [1800 750] cm
-1
associes aux
vibrations de dformation des liaisons C-H et =C-H et dlongation des liaisons C-C, C=C et
C-O. Aprs le traitement thermique 575C, seules sont conserves les bandes dans le
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
70
domaine [1750 - 750] cm
-1
mais elles sont plus larges et moins intenses ; aprs le traitement
thermique 800C aucune bande ne reste observable, ce qui signifie une meilleure
dgradation du prcurseur carbon haute temprature. Ce rsultat signifie comme attendu et
en bon accord avec les mesures de conductivit lectronique, quune augmentation de la
temprature de synthse favorise une meilleure dcomposition du prcurseur organique
carbon (cellulose) et donc la formation dun revtement de carbone plus conducteur.
Cependant, on peut noter que les bandes caractristiques du revtement de carbone ne
sont pas visibles sur le spectre IR de Fe
575-fast
(cf. Figure IV-7) ce qui laisse penser que cette
technique danalyse nest pas adapte la dtermination de la nature du revtement de
carbone prsent en faible quantit la surface des particules de C-LiFePO
4
.
a)
O-H, -C-H
-C-H, =C-H, C-C
C=C, C-O
b)
c)
5
7
5
C
/
A
r
/
1
5
m
i
n
.
8
0
0
C
/
A
r
/
1
5
m
i
n
.
4000 3500 3000 2500 2000 1500 1000
A
b
s
o
r
b
a
n
c
e
(
A
.
U
.
)
Wavenumber (cm
-1
)
Figure IV-9 : Comparaison des spectres FTIR du prcurseur carbon a) avant traitement thermique, b)
aprs 15 min 575C sous argon (conditions de synthse utilises pour Fe
575-fast
) et c) aprs 15 min
800C sous argon (conditions de synthse utilises pour Fe
800-fast
).
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
71
La Figure IV-10 prsente une tude dans linfrarouge lointain des poudres Fe
575-fast
et
Fe
800-fast
. Ces spectres prsentent le mme nombre de bandes avec les mmes positions,
intensits et largeurs mi-hauteur. Les positions et intensits observes sont en bon accord
avec les rsultats prsents dans la rfrence [18]. Selon la rfrence [21], les modes de
dformation (
2
et
4
) de lanion (PO
4
)
3-
sont situs dans le domaine de nombres donde
[570 420] cm
-1
. Cependant, une attribution prcise de ces bandes est difficile dans la mesure
o dans ce systme il y a un fort couplage entre ces modes impliquant galement la mobilit
des ions lithium [22]. En dessous de 400 cm
-1
, les pics sont attribus aux modes externes ou
aux vibrations de rseau, celles-ci tant principalement dues aux translations et librations des
anions (PO
4
)
3-
, mais galement aux mouvements de translation des ions Fe
2+
et Li
+
.
Cependant, la comparaison des spectres de LiFePO
4
et FePO
4
ralise par Burba et al. [24]
suggre que les bandes 230 cm
-1
, 469 cm
-1
et 501 cm
-1
pourraient tre assignes aux modes
des cages de lithium alors que les bandes 349 cm
-1
et 380 cm
-1
rsultent du mouvement
des ions lithium [20,23,24].
600 500 400 300 200 100
6
4
7
6
3
7
5
7
8
5
5
0
5
0
1
4
6
9
3
8
0
2
4
9
3
4
9
2
8
6
2
3
0
1
9
5
Fe
800-fast
Fe
575-fast
A
b
s
o
r
b
a
n
c
e
(
A
.
U
.
)
Wavenumber (cm
-1
)
Figure IV-10 : Spectres de Fe
575-fast
et Fe
800-fast
en infrarouge lointain dans le domaine de nombres donde
[675 100] cm
-1
.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
72
Il est galement important de noter quil ny a pas de bandes entre les modes
dlongation et de dformation des ions, c'est--dire dans le domaine de nombres donde
~ [900 - 700] cm
-1
. Cela permet de diffrencier et dattribuer les bandes dlongation avec
confiance au groupement phosphate (PO
4
)
3-
et non pas
dautres groupements tels que
(P
2
O
7
)
2-
[25,26], (P
3
O
9
)
3-
[27] ou (P
3
O
10
)
5-
[28] pour lesquels des bandes sont prsentes dans
le domaine [900 - 700] cm
-1
. Cela confirme donc quil ny a pas de tels groupements
phosphates complexes dans les matriaux tudis.
En rsum, on peut dire que ces matriaux, Fe
575-fast
et Fe
800-fast
, tudis dans le proche
et lointain infrarouge ne sont pas significativement diffrents du point de vue de la
spectroscopie FTIR, ils sont trs similaires courte distance et ne prsentent pas de dfauts
particuliers. La spectroscopie infrarouge a permis de confirmer la bonne cristallinit de
Fe
575-fast
et Fe
800-fast
mais a galement montr, grce la drive de la ligne de base et la
diffrence dintensit relative des spectres, une diffrence de conductivit lectronique entre
ces deux matriaux. Ces rsultats peuvent tre gnraliss tous les autres matriaux tudis
dans ce chapitre et synthtiss avec un traitement thermique dit lent, Fe
575-slow
et Fe
800-slow.
IV-7 Caractrisation par spectroscopie Raman
La spectroscopie Raman est une technique de choix pour caractriser le carbone
prsent dans les matriaux C-LiFePO
4
. Les spectres Raman apparaissent plus simples que les
spectres IR car les bandes Raman du carbone sont amplifies par rsonance [29,30] et sont
donc largement plus intenses que les bandes des modes non rsonants des phosphates, qui
sont de trs faibles intensits.
Pour chaque chantillon, sa surface a t analyse en diffrents points. Quatre dentre
eux, les plus reprsentatifs, sont donns (cf. Figure IV-11) titre dexemple pour les
matriaux Fe
800-fast
et Fe
575-fast
. Les spectres Raman des matriaux C-LiFePO
4
, enregistrs
avec une longueur donde incidente de 632.8 nm, prsentent deux bandes larges et trs
intenses ~ 1350 cm
-1
et ~ 1600 cm
-1
dans le domaine [600 - 2000] cm
-1
. Ces deux bandes
sont caractristiques dun film de carbone trs fortement dsorganis [31,32]. Il est noter
que la position des bandes Raman est trs dpendante de la longueur donde utilise pour
raliser la mesure, une comparaison quantitative de diffrents spectres peut donc seulement
tre ralise lorsque les expriences ont t faites la mme longueur donde incidente.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
73
Point 1
Point 2
Point 3
Point 4
a)
750 1000 1250 1500 1750 2000
9
5
4
I
(
A
.
U
.
)
Raman shift (cm
-1
)
Point 1
Point 2
Point 3
Point 4
750 1000 1250 1500 1750 2000
9
5
0
I
(
A
.
U
.
)
Raman shift (cm
-1
)
Fe
575-fast
Fe
800-fast
Figure IV-11 : Spectres Raman enregistrs avec une longueur donde dexcitation de 632.8 nm diffrents
points des matriaux a) Fe
575-fast
et b) Fe
800-fast
.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
74
Les spectres Raman de la Figure IV-11 montrent galement la prsence dun pic de trs
faible intensit ~ 950 cm
-1
. Lintensit de ce pic varie entre les diffrents points enregistrs
sur un mme chantillon, mais galement entre les diffrents matriaux tudis. Ce pic
correspond la bande Raman la plus intense de lanion (PO
4
)
3-
: le mode dlongation
symtrique
1
(
s
(PO
4
)). Les autres modes intramolculaires, attendus ~ 620 cm
-1
(
4
),
~ 986 cm
-1
et ~ 1058 cm
-1
(
3
) daprs la rfrence [33], ne sont pas assez intenses pour tre
observs. Contrairement aux rsultats reports par Julien et al. [33], dans notre cas la position
de la bande associe au mode dlongation
1
~ 950 cm
-1
nest pas sensible la prsence du
revtement de carbone (~ 951 cm
-1
pour le matriau LiFePO
4
sans revtement de carbone,
spectre non prsent ici). On note que seules les deux larges bandes dues au carbone sont
observables sur la plupart des spectres Raman, ne permettant pas lobservation des bandes de
vibration associes au phosphate : ceci dmontre que le carbone est prsent la surface de
LiFePO
4
sous la forme dun revtement.
Pour dterminer prcisment les caractristiques des bandes associes au carbone et en
dduire ainsi sa nature, les spectres exprimentaux ont t affins en utilisant une
combinaison de quatre bandes de type Gaussienne-Lorentzienne. Le calcul est ralis une fois
la ligne de base dtermine ; la largeur mi-hauteur (FWHM), la position et lintensit des
bandes sont affines. La bande ~ 1600 cm
-1
, dont la position est proche de celle du mode E
2g
du graphite cristallis, est nomme
la bande G. La bande large situe ~ 1350 cm
-1
correspond principalement la bande D associe aux imperfections du rseau graphitique
[31,32]. Ces bandes D et G sont associes aux proprits structurales et physiques des
carbones : plus la graphitisation du carbone est leve, plus la bande G est intense par rapport
la bande D. Pour le graphite cristallin seule la bande G est prsente. Lattribution des deux
bandes supplmentaires ~ 1200 cm
-1
et ~ 1530 cm
-1
nest pas vidente. Elles sont parfois
attribues des matriaux carbons trs faiblement organiss et en particulier des dfauts
qui sont hors du plan des couches aromatiques comme les atomes de carbone en conformation
ttradrique [34,35] ; en particulier, Doeff et al. les attribuent respectivement des atomes de
carbone en configuration ttradrique et des environnements de type sp
3
(~ 1530 cm
-1
)
[36]. Cependant, une interprtation totalement diffrente a galement t propose : ces
bandes peuvent rsulter de modes phonons lintrieur de la premire zone de Brillouin
appartenant diffrentes courbes de dispersion des feuillets de graphne et qui deviennent
actifs en spectroscopie Raman du fait dun processus de double rsonance [37]. Une bande
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
75
supplmentaire, la bande D, peut galement tre observe 1620 cm
-1
, elle apparat comme
un paulement de la bande G et est absente pour un graphite bien cristallis [34,35].
La Figure IV-12 montre la dsommation de spectres Raman des matriaux Fe
575-fast
et
Fe
800-fast
avec la combinaison de bandes de type Gaussienne-Lorentzienne. La position des
bandes est trs similaire pour les deux matriaux ( ~ 22 cm
-1
pour les bandes situes
~ 1200 cm
-1
, ~ 12 cm
-1
pour les bandes situes ~ 1350 cm
-1
et ~ 5 cm
-1
pour les
bandes situes ~ 1530 cm
-1
et ~ 1600 cm
-1
). Cependant, il faut noter quune approximation
est ralise sur la bande G (~ 1600 cm
-1
), en effet cette bande est en ralit la somme de deux
bandes : la bande G et la bande D (avec une contribution infrieure 10 % pour cette
dernire). Les rsultats obtenus pour les spectres Raman du matriau Fe
800-fast
prsents la
Figure IV-11 sont reports dans le Tableau IV-7. On peut noter la bonne reproductibilit
dans les positions des bandes pour les diffrents points reports dans ce tableau, en effet leur
position varie de moins de 5 cm
-1
. Les largeurs mi-hauteur de ces bandes restent aussi trs
similaires quel que soit le point tudi. La valeur trs leve observe pour les FWHM des
bandes D (> 50 cm
-1
) est la signature dun compos carbon faiblement ordonn [31,32,38].
La valeur du rapport des intensits des bandes D et G (I
D
/I
G
= R(
L
)) donne une bonne
information sur la nature du carbone [31,32,38,39]. En particulier pour les matriaux
graphitiques et avec une longueur donde dexcitation
L
situe dans le visible
(400 <
L
< 700 nm), le rapport R(
L
) peut tre reli la longueur de cohrence dans le plan
L
a
, qui est quivalente la taille des clusters de C sp
2
, grce la relation de Tuinstra-Koenig
[40] :
L
a
= C(
L
)/R(
L
) (1)
o C(
L
) est un facteur dchelle qui dpend de la longueur donde
L
et
qui est donn par la
relation :
C(
L
) = C
0
+
L
C
1
(2)
avec C
0
= -126 et C
1
= 0.033 [40].
Pour les deux matriaux, une large distribution des rapports I
D
/I
G
est observe de 3.0 3.8
avec une valeur moyenne de 3.4 pour Fe
575-fast
et de 3.3 3.6 avec une valeur moyenne de 3.4
pour Fe
800-fast
. Les valeurs correspondantes de L
a
, dduites des deux relations prcdentes
avec dans notre cas
L
= 6328 , sont telles que 2.2 < L
a
< 2.7 nm. La dispersion des valeurs
de L
a
montre lhtrognit du revtement de carbone, qui est plus importante pour Fe
575-fast
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
76
que pour Fe
800-fast
. Dautre part, les valeurs de L
a
relativement faibles rvlent que le compos
carbon prsent la surface de LiFePO
4
est fortement dsordonn [39].
I
(
A
.
U
.
)
1597.4
1533.0
1351.6
1000 1200 1400 1600 1800
1207.5
Raman shift (cm
-1
)
D G
I
(
A
.
U
.
)
1603.3
1528.2
1338.4
1185.6
1000 1200 1400 1600 1800
Raman shift (cm
-1
)
D G
a)
b)
Fe
800-fast
Fe
575-fast
Figure IV-12 : Dsommations de spectres Raman ralises avec des bandes de type Gaussienne-
Lorentzienne pour a) Fe
575-fast
et b) Fe
800-fast
.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
77
Tableau IV-7 : Paramtres des quatre bandes de type Gaussienne-Lorentzienne utilises pour affiner les
bandes D et G des spectres Raman enregistrs diffrents points de lchantillon Fe
800-fast
. Ces spectres
sont ceux reports la Figure IV-11.
Point 1 Point 2 Point 3 Point 4
Band position (cm
-1
)
1185.6
1338.4
1528.2
1603.3
1181.5
1340.1
1533.4
1602.4
1185.6
1341.7
1530.6
1604.0
1185.4
1340.1
1531.5
1603.0
FWHM (cm
-1
)
187.0
169.2
161.5
66.1
188.4
173.2
156.2
67.9
206.6
164.4
162.3
66.8
189.0
171.5
157.9
68.0
Surface
98770
292795
134129
87562
114805
364479
169964
105163
141148
305275
164161
86077
77954
223553
103401
66492
I
D
/I
G
3.6 3.3 3.5 3.4
La spectroscopie Raman ralise 632.8 nm permet de confirmer que le compos
carbon prsent la surface des particules est fortement dsorganis avec une trs faible
longueur de cohrence dans le plan. Kostecki et coll. [36] proposent une corrlation directe
entre le rapport I
D
/I
G
, le rapport sp
3
/sp
2
, la conductivit lectronique et la capacit rversible.
Cependant comme cela a t mentionn prcdemment, lattribution des bandes ~ 1200 cm
-1
et ~ 1530 cm
-1
au carbone sp
3
[36] est discutable. En effet, ltude de composs carbons
amorphes (cest--dire des Diamond Like Carbons DLC) a montr que la diffusion Raman
ralise avec des longueurs donde excitatrices dans le visible nest pas capable de dtecter la
prsence de carbone sp
3
alors que ces matriaux sont constitus la fois despces
sp
2
et sp
3
,
cette dernire tant prsente en grande proportion [39,41]. Cela est d au fait quen
spectroscopie Raman la section efficace du carbone dhybridation sp
2
est plus grande que
celle du carbone dhybridation sp
3
cause des effets de rsonance. Lexcitation avec une
lumire UV provoque une forte dcroissance des processus de rsonance et rend possible
lobservation des modes impliquant les espces dhybridation sp
3
, qui apparaissent
alors sous
la forme dune trs large bande centre ~ 1060 cm
-1
et appele la bande T [39,41].
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
78
Pour obtenir plus dinformations sur la contribution C sp
3
dans les deux matriaux
Fe
575-fast
et Fe
800-fast
, synthtiss respectivement 575C et 800C, des mesures
complmentaires ont t ralises par spectroscopie Raman en utilisant la longueur donde
incidente de 325 nm. Les spectres enregistrs avec cette longueur donde diffrents points
de lchantillon Fe
800-fast
sont donns la Figure IV-13, selon le point analys diffrents
spectres ont t obtenus. Cependant, la plupart des spectres enregistrs prsentent les mmes
caractristiques que le spectre prsent au Point 1, ce point est donc considr comme le plus
reprsentatif pour le matriau Fe
800-fast
. Il est noter que Fe
575-fast
prsente des rsultats trs
similaires. Sur ces spectres sont observes les deux bandes larges caractristiques du carbone.
On peut noter, comme attendu [29,30,37], que la bande G conserve la mme position
(~ 1600 cm
-1
), alors que la bande D est dplace vers des nombres donde plus levs
(~ 1390 cm
-1
). Dans tous les spectres, on note galement que les bandes relatives lanion
(PO
4
)
3-
sont prsentes ~ 950 cm
-1
, ~ 993 cm
-1
, ~ 1020 cm
-1
et ~ 1062 cm
-1
, en bon accord
avec les donnes reportes dans la littrature [22]. Cependant, lintensit relative de ces
bandes est plus leve que celle observe pour les spectres raliss la longueur donde
dexcitation de 632.8 nm, grce la rduction du processus de rsonance associ au
revtement de carbone lors de lexcitation dans lUV. La bande attribue au C sp
3
devrait tre
large et centre ~ 1060 cm
-1
[39,41]. Une analyse attentive des spectres obtenus pour
Fe
575-fast
et Fe
800-fast
ne montre aucune contribution du C sp
3
. La diffrence de conductivit
lectronique entre Fe
575-fast
et Fe
800-fast
ne peut donc pas tre attribue une diffrence
dhybridation du carbone prsent dans le revtement carbon. Le facteur qui jouerait
majoritairement sur la conductivit lectronique serait lordre (dsordre) prsent dans les
feuillets de graphne [39].
Il est noter que des cartographies ont galement t ralises sur des lectrodes,
rcupres diffrents tats de charge et de dcharge (Li
x
FePO
4
) en batteries LiFe
800-fast
.
Nous avons choisi de ne pas prsenter ces rsultats ici car les spectres Raman sont domins
par les bandes D et G associes au noir de carbone, mais galement par celles associes au
liant utilis pour la ralisation de llectrode. Par consquent, il est difficile dobserver les
bandes associes au matriau C-LiFePO
4
, au matriau actif lui-mme ou son revtement de
carbone.
Lanalyse par spectroscopie Raman a permis de montrer que le carbone introduit lors
de la synthse dans les matriaux C-LiFePO
4
est la surface des particules. Cette tude a
montr que le revtement carbon des deux matriaux Fe
575-fast
et Fe
800-fast
est constitu de
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
79
carbone fortement dsordonn avec de faibles longueurs de cohrence (infrieures 3 nm).
Aucune contribution du carbone dhybridation sp
3
nest observe. Cependant, on peut
conclure comme attendu que Fe
575-fast
prsente une plus grande inhomognit dans la qualit
de son revtement de carbone.
Point 1
Point 2
Point 3
Point 4
Point 5
800 1000 1200 1400 1600 1800
1
3
9
1
1
6
0
7
1
0
2
0
1
0
6
2
9
9
3
9
5
0
I
(
A
.
U
.
)
Raman shift (cm
-1
)
Figure IV-13 : Spectres Raman enregistrs la longueur donde dexcitation de 325 nm et diffrents
points de lchantillon Fe
800-fast
.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
80
IV-8 Caractrisations texturales
IV-8-1 Microscopie Electronique Balayage
La morphologie des particules ainsi que leur taille ont t tudies par Microscopie
Electronique Balayage Haute Rsolution. La Figure IV-14 donne une comparaison de
clichs MEB obtenus pour les quatre matriaux C-LiFePO
4
. Trois dentre eux, Fe
575-fast
,
Fe
575-slow
et Fe
800-fast
, prsentent des tailles de particules trs similaires de lordre de 60
100 nm. Pour lchantillon Fe
800-slow
, il y a une inhomognit de tailles de particules plus
significative, avec comme pour les autres matriaux des tailles de particules variant de 60
100 nm de diamtre mais galement des particules plus grosses avec un diamtre suprieur
600 nm. On peut supposer que la croissance de ces particules est due un traitement
thermique plus long haute temprature, 100 min au-del de 700C contre seulement 15 min
pour Fe
800-fast
.
IV-8-2 Microscopie Electronique Transmission
La Figure IV-15 prsente des images de Microscopie Electronique en Transmission
(MET) obtenues pour des particules primaires des chantillons Fe
575-fast
et Fe
800-fast
. La plupart
des particules prsente une taille comprise entre 50 et 100 nm, en bon accord avec les tailles
des domaines de cohrence dtermines partir des donnes de diffraction des rayons X. Il
faut donc noter que les particules observes par MEB sont des particules primaires car de
taille similaire aux particules observes par MET.
De plus, sur la Figure IV-15 on note la prsence de moirs quelle que soit la
temprature de synthse, ce qui montre la bonne cristallinit de ces matriaux. En effet, les
moirs sont dus la superposition des plans atomiques de deux cristallites diffrentes.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
81
Fe
800-fast
Fe
575-fast
600 nm
6.0 m
60 m
600 nm
600 nm
Fe
575-slow
Fe
800-slow
6.0 m
6.0 m
600 nm
60 m 60 m
6.0 m
60 m
600 nm
Figure IV-14 : Clichs de Microscopie Electronique Balayage obtenus pour les matriaux Fe
800-fast
,
Fe
800-slow
, Fe
575-fast
et Fe
575-slow
. Pour avoir une vision plus reprsentative de la microstructure de Fe
800-slow
,
deux micrographies sont donnes lchelle de 600 nm.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
82
Moir
a)
Fe
800-fast
b)
Fe
575-fast
50 nm
50 nm
Figure IV-15 : Micrographies de Microscopie Electronique en Transmission ralises pour a) Fe
575-fast
et b)
Fe
800-fast
.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
83
IV-8-3 Mesure de surface spcifique
Dans le Tableau IV-8 sont reportes les mesures de surface spcifique ralises par la
mthode BET pour les quatre matriaux C-LiFePO
4
tudis. Toutes les valeurs reportes sont
du mme ordre de grandeur, comprises entre 20 et 30 m.g
-1
. Ces valeurs exprimentales sont
en bon accord avec les valeurs thoriques dtermines en considrant des particules
sphriques, soit 18 m.g
-1
et 28 m.g
-1
pour des particules ayant respectivement un diamtre de
100 nm et de 60 nm. Ces surfaces spcifiques sont en bon accord avec la taille des particules
estimes par les diffrentes techniques utilises : DRX, MEB et MET.
Notons que le carbone en plus de contribuer une augmentation de la surface
spcifique gnre des porosits fermes au sein des agglomrats.
Tableau IV-8 : Comparaison des surfaces spcifiques mesures par la mthode BET pour Fe
800-fast
,
Fe
800-slow
, Fe
575-fast
et Fe
575-slow
.
S
BET
(m.g
-1
)
Fe
800-fast
20
Fe
800-slow
21
Fe
575-fast
23
Fe
575-slow
28
IV-9 Caractrisations lectrochimiques
Le comportement lectrochimique de ces quatre chantillons C-LiFePO
4
a t tudi
en mode galvanostatique dans diffrentes conditions de cyclage.
IV-9-1 Cyclages continus rgime constant
Pour cette tude lectrochimique, les cyclages ont t raliss rgime continu (C/20)
dans la gamme de potentiel [2 4.5] V (vs. Li
+
/Li). La Figure IV-16 montre les dix premiers
cycles obtenus dans ces conditions pour les quatre matriaux C-LiFePO
4
, mais galement
lvolution de la capacit rversible en fonction du nombre de cycles. La Figure IV-16a
montre que la raction de dsintercalation / intercalation du lithium est associe un plateau
de potentiel ~ 3.5 V vs. Li
+
/Li [42,43], elle se fait donc selon un mcanisme biphas. Dans
la suite de ce manuscrit, nous confirmerons les rsultats obtenus par Yamada et
collaborateurs, qui ont montr lexistence de deux domaines de solution-solide autour des
deux compositions extrmes : Li
1-
FePO
4
et Li
FePO
4
, avec et qui tendent vers 0 [44].
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
84
Comme le montre la Figure IV-16b, aprs le premier cycle il y a une lgre augmentation de
la capacit rversible, mais celle-ci demeure constante sur le reste du cyclage et ce au moins
jusqu 80 cycles.
Les matriaux Fe
575-fast
et Fe
800-fast
, synthtiss avec des traitements thermiques
rapides, prsentent les capacits rversibles les plus leves, avec par exemple pour le second,
une capacit rversible de lordre de 160 mAh/g, valeur trs proche de la valeur thorique
(170 mAh/g). Les capacits rversibles des deux autres matriaux sont beaucoup plus faibles,
~ 130 mAh/g pour Fe
800-slow
et ~ 120 mAh/g pour Fe
575-slow
. La capacit irrversible varie
entre 5 et 14 mAh/g, soit 0.03 < x < 0.08 pour Li
x
FePO
4
pour les quatre matriaux
C-LiFePO
4
tudis. La diffrence de potentiel observe entre la courbe de charge et de
dcharge lors du premier cycle lectrochimique est denviron 0.10 V. Cependant, il est noter
que cette diffrence de potentiel a tendance dcrotre entre le premier et le second cycle
pour tous les matriaux, puis demeurer constante tout au long du cyclage lectrochimique.
Dans ces conditions de cyclage, Fe
800-fast
donne les meilleures performances lectrochimiques.
Les rsultats prsents la Figure IV-16 sont caractristiques, plusieurs cyclages ont en effet
t effectus pour chaque matriau et tous montrent une bonne reproductibilit.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
85
Figure IV-16 : Comparaison a) des courbes de cyclage (potentiel en fonction de x pour Li
x
FePO
4
) et b) de
la capacit rversible en fonction du nombre de cycles pour les quatre matriaux C-LiFePO
4
utiliss
comme lectrode positive dans les batteries au lithium. Ces cellules lectrochimiques ont t cycles en
mode galvanostatique rgime constant (C/20) dans la fentre de potentiel [2 - 4.5] V (vs. Li
+
/Li ).
-0.2 0.0 0.2 0.4 0.6 0.8 1.0
2.0
2.5
3.0
3.5
4.0
4.5
Fe
575-fast
P
o
t
e
n
t
i
a
l
v
s
L
i
+
/
L
i
(
V
)
x in Li
x
FePO
4
-0.2 0.0 0.2 0.4 0.6 0.8 1.0
2.0
2.5
3.0
3.5
4.0
4.5
Fe
800-fast
P
o
t
e
n
t
i
a
l
v
s
L
i
+
/
L
i
(
V
)
x in Li
x
FePO
4
-0.2 0.0 0.2 0.4 0.6 0.8 1.0
2.0
2.5
3.0
3.5
4.0
4.5
Fe
800-slow
P
o
t
e
n
t
i
a
l
v
s
L
i
+
/
L
i
(
V
)
x in Li
x
FePO
4
-0.2 0.0 0.2 0.4 0.6 0.8 1.0
2.0
2.5
3.0
3.5
4.0
4.5
Fe
575-slow
P
o
t
e
n
t
i
a
l
v
s
L
i
+
/
L
i
(
V
)
x in Li
x
FePO
4
a)
b)
0 20 40 60 80
0
20
40
60
80
100
120
140
160
Fe
800-fast
Fe
800-slow
Fe
575-fast
Fe
575-slow
R
e
v
e
r
s
i
b
l
e
c
a
p
a
c
i
t
y
(
m
A
h
/
g
)
Number of cycles
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
86
IV-9-2 Cyclages lectrochimiques avec variation du rgime de cyclage
Pour caractriser la rponse de ces quatre matriaux aux changements de rgimes,
deux modes de cyclage en puissance ont t effectus.
IV-9-2-a Cyclage en puissance n1
Toutes les charges sont effectues rgime C/5 jusqu 4.5 V vs. Li
+
/Li, puis sont
suivies par une priode de relaxation de 30 min. Les dcharges sont ralises successivement
aux rgimes 30C, 20C, 10C, 5C, 2C, C, C/2, C/10 et C/50 jusqu 2 V vs. Li
+
/Li. Ces neuf
cycles de charge / dcharge sont suivis dune priode de relaxation de 30 min puis par onze
cycles rgime C/5 entre 2 et 4.5 V vs. Li
+
/Li. Ce programme de cyclage est ensuite rpt n
fois.
La Figure IV-17 montre une comparaison des capacits rversibles obtenues pour les
quatre matriaux C-LiFePO
4
cycls en batteries au lithium selon ce programme. Tous les
matriaux tudis prsentent une bonne cyclabilit au moins jusqu 100 cycles. La Figure
IV-17b donne un agrandissement de la Figure IV-17a pour une meilleure comprhension et
illustre lvolution du rgime de cyclage. On peut noter que les matriaux recuits plus haute
temprature (Fe
800-fast
et Fe
800-slow
), quel que soit le traitement thermique, prsentent les
capacits rversibles les plus leves nimporte quel rgime de dcharge. En effet, des
capacits rversibles de ~ 155 mAh/g et ~ 140 mAh/g sont obtenues pour les cyclages raliss
rgime C/5 pour Fe
800-fast
et Fe
800-slow
, alors que seulement ~ 130 mAh/g et ~ 120 mAh/g
sont obtenues pour Fe
575-slow
et Fe
575-fast
. De plus, la perte de capacit rversible entre la
premire et la dernire srie de cycles raliss rgime C/5 est la plus faible pour les
matriaux synthtiss 800C ; on constate en effet une perte de ~ 7 % pour Fe
800-slow
et
Fe
800-fast
alors quelle est respectivement de ~ 13 % et ~ 20 % pour Fe
575-fast
et Fe
575-slow
.
Fe
800-fast
prsente une nouvelle fois les meilleures performances lectrochimiques, du moins
pour des rgimes de cyclage compris entre 2C et C/5. Cependant, il est difficile danalyser ces
rsultats trs fort rgime du fait du rle jou par la technologie dlectrode qui dans ce cas a
une contribution majeure. En effet rgime de courant lev, diffrents paramtres
indpendants du matriau lui-mme, peuvent influer de manire prpondrante sur la rponse
lectrochimique enregistre : composition de llectrode, types dlectrolyte et de sparateur,
.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
87
a)
b)
0 5 10 15 20 25 30
0
20
40
60
80
100
120
140
160
30C
20C
10C
5C
2C
C
C/2
C/10
C/50
C/5
R
e
v
e
r
s
i
b
l
e
c
a
p
a
c
i
t
y
(
m
A
h
/
g
)
Number of cycles
0 25 50 75 100
0
20
40
60
80
100
120
140
160
Fe
800-fast
, Fe
800-slow
, Fe
575-fast
, Fe
575-slow
R
e
v
e
r
s
i
b
l
e
c
a
p
a
c
i
t
y
(
m
A
h
/
g
)
Number of cycles
Figure IV-17 : a) Comparaison de lvolution des capacits rversibles en fonction du nombre de cycles pour
les quatre matriaux C-LiFePO
4
utiliss comme lectrode positive pour batteries au lithium. Toutes les
charges sont ralises rgime C/5 jusqu un potentiel de 4.5 V vs. Li
+
/Li, tandis que les dcharges ont t
ralises rgimes C/n jusqu 2 V vs. Li
+
/Li. Un agrandissement des courbes dvolution est donn en b)
pour les 30 premiers cycles ainsi que les rgimes de cyclage des dcharges (C/n).
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
88
IV-9-2-b Cyclage en puissance n2
Des cycles de charge / dcharge sont raliss par squences diffrents rgimes C/n
dans la gamme de potentiel [2 4.5] V (vs. Li
+
/Li), n varie de 10 1 : le cyclage se fait donc
en alternant rgimes rapides et rgimes lents.
La Figure IV-18 montre lvolution des capacits rversibles obtenues pour les quatre
matriaux utiliss comme lectrode positive dans les batteries au lithium dont les cyclages ont
t raliss selon le programme dfini ci-dessus. Ce test lectrochimique montre que les
matriaux C-LiFePO
4
tudis conservent une bonne capacit rversible rgime C/10 la
capacit rversible reste comparable celle obtenue initialement mme aprs quelques
cycles un rgime plus lev, C par exemple. De plus, une meilleure rtention de capacit
entre des squences successives rgime lent (C/10) et rgime rapide (C) est de nouveau
observe pour les matriaux synthtiss haute temprature (800C), en bon accord avec les
rsultats dj reports la Figure IV-17. En effet, on ne note quune faible diminution de la
capacit rversible de ~ 11.5 % pour Fe
800-fast
, de ~ 13 % pour Fe
800-slow
et de ~ 12 % pour
Fe
575-slow
, alors quelle est de ~ 30 % pour Fe
575-fast
. Cependant, on peut remarquer que la
capacit rversible obtenue rgime C reste suprieure 100 mAh/g pour tous les
composites, ce qui est une valeur de capacit rversible tout fait intressante.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
89
0 20 40 60 80
0
20
40
60
80
100
120
140
160
Fe
800-fast
Fe
800-slow
Fe
575-fast
Fe
575-slow
C/10
C
C/10
C/5 C/2 C/5 C/5
C/10 C/10 C/10
R
e
v
e
r
s
i
b
l
e
c
a
p
a
c
i
t
y
(
m
A
h
/
g
)
Number of cycles
Figure IV-18 : Comparaison de lvolution des capacits rversibles obtenues en fonction du nombre de cycles
pour les quatre matriaux C-LiFePO
4
tudis comme matriaux dlectrode positive pour batteries au lithium.
Les cellules lectrochimiques ont t cycles entre 2 et 4.5 V vs. Li
+
/Li pendant des squences successives de
quelques cycles diffrents rgimes C/n.
On peut rsumer cette tude lectrochimique en constatant que quelles que soient les
conditions de cyclage utilises, Fe
800-fast
prsente les meilleures performances
lectrochimiques en batteries au lithium, avec les capacits rversibles les plus leves, la
plus faible perte de capacit en cyclage mais galement une faible capacit irrversible et une
faible polarisation. Les autres matriaux prsentent des performances lectrochimiques
moins bonnes. Ces diffrences de comportement lectrochimique ne peuvent pas tre
attribues des diffrences structurales (distribution des cations), chimiques (composition)
ou magntiques. Une distribution de petites tailles de particules et la nature conductrice du
revtement de carbone obtenu 800C sont les facteurs clefs de bonnes performances en
batteries au lithium. .
Pour des applications de puissance, les matriaux synthtiss 800C (Fe
800-fast
mais
aussi Fe
800-slow
) prsentent les meilleures proprits lectrochimiques : le bon revtement de
carbone, lorigine de proprits lectroniques leves pour le matriau, est probablement le
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
90
facteur clef. Cependant, pour des applications de cyclages longue dure, une distribution de
taille de particules isotrope, ce que lon peut traduire par la prsence de petites particules
primaires seulement, est probablement le facteur dterminant. Les rsultats prcdents
suggrent galement qutablir un lien direct entre la bonne conductivit lectronique de ces
matriaux C-LiFePO
4
et leurs bonnes performances lectrochimiques, comme ont pu le
suggrer certains auteurs [45-47], nest pas si vident.
Ltude par spectroscopie Raman a permis de calculer le rapport I
D
/I
G
qui donne une
information sur la nature et lorganisation du compos carbon. Ce rapport est suprieur 3
pour les deux matriaux tudis : Fe
575-fast
et Fe
800-fast
. Ces deux matriaux prsentent
respectivement des capacits rversibles de ~ 140 mAh/g et ~ 160 mAh/g. Ce rsultat nest
donc pas en accord avec les travaux de Doeff et al. [48] qui lient linairement une
augmentation du rapport I
D
/I
G
avec une diminution de la capacit rversible. Selon cette
tude un matriau prsentant un rapport I
D
/I
G
de ~ 3 devraient prsenter des capacits
rversibles de 60 mAh/g.
IV-10 Conclusions
Les matriaux CLiFePO
4
synthtiss partir dun mlange des prcurseurs de
phosphates de fer et de lithium et de cellulose activs mcano-chimiquement sont obtenus
suite diffrents traitements thermiques (vitesse de chauffe et de refroidissement ainsi que
diffrentes tempratures). Les quatre matriaux tudis : Fe
800-fast
, Fe
800-slow
, Fe
575-fast
et
Fe
575-slow
sont des phases de type olivine obtenues pures du point de vue de la diffraction des
rayons X, une analyse structurale dtaille a montr quelles taient galement ordonnes et
parfaitement stoechiomtriques. Cependant, les analyses chimiques ainsi que la spectroscopie
Mssbauer ont montr que les rapports Li/Fe et P/Fe sont suprieurs 1 et que ~ 5 6 at. %
dions Fe
3+
sont prsents dans les matriaux.
Laffinement des donnes de diffraction des neutrons et des rayons X par la mthode
de Rietveld a montr que la prsence dions lithium supplmentaires dans le site du fer ne
permet pas dexpliquer que tous les matriaux tudis prsentent des rapports de lithium et de
phosphore par rapport au fer suprieurs 1 ainsi quune petite quantit dions Fe
3+
. Cela
confirme et complte ltude mene au Chapitre III qui na pas montr la formation dune
solution solide Li
1+y
Fe
1-y
PO
4
lorsque lon fait varier le rapport Li/Fe. La spectroscopie
Mssbauer ainsi que les mesures magntiques ont galement permis dexclure la prsence
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
91
dimpurets ferro (ou ferri) magntiques cristallises, sans toutefois exclure la possibilit de
la prsence dune impuret amorphe riche en Fe
3+
. Dautre part, lanalyse des matriaux
Fe
800-fast
et Fe
575-fast
par spectroscopie infrarouge na pas montr de diffrence courte
distance entre ces matriaux ni la prsence de dfauts particuliers. Cependant, dun point de
vue gnral et plus particulirement pour des nanomatriaux, on ne peut pas exclure que la
surface des particules soit diffrente du cur. On peut donc supposer que, dans notre cas, les
rapports Li/Fe et P/Fe suprieurs 1 et la prsence des ions Fe
3+
soient le rsultat dun effet
de surface, qui peut tre sous forme de dfauts de surface et/ou dune impuret amorphe riche
en Fe
3+
.
Ce chapitre a donc montr limportance des conditions de synthse sur le
comportement lectrochimique des matriaux C-LiFePO
4
. Seul le matriau C-LiFePO
4
(Fe
800-fast
) prsente de bonnes performances lectrochimiques, que ce soit pour des cyclages
longue dure rgime constant ou pour des cyclages en puissance. Ce matriau prsente un
bon compromis entre un revtement de carbone, caractris par spectroscopie Raman comme
trs dsordonn sans hybridation sp
3
et prsentant une conductivit lectronique leve, car
obtenu grce la dgradation de la cellulose 800C et de petites particules primaires (70 -
100 nm) qui favorisent une conductivit ionique leve. Le matriau Fe
800-slow
qui a
galement t synthtis haute temprature mais avec un traitement thermique plus long
prsente un nombre important de grosses particules primaires qui sont un inconvnient majeur
de bonnes proprits de transport. Ses performances lectrochimiques lors des cyclages
longue dure sont donc significativement infrieures celles obtenues pour Fe
800-fast
.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
92
Bibliographie du Chapitre IV
1
A. S. Andersson, B. Kalska, L. Haggstrom, J. O. Thomas, Solid State Ionics, 130
(2000), 41-52.
2
M. A. E. Sanchez, G. E. S. Brito, M. C. A. Fantini, G. F. Goya, J. R. Matos, Solid
State Ionics, 177 (2006), 497-500.
3
A. Yamada, S. C. Chung, K. Hinokuma, Journal of the Electrochemical Society, 148
(2001), A224.
4
S. Okada, T. Yamamoto, Y. Okazaki, J. Yamaki, M. Tokunaga, T. Nishida, Journal Of
Power Sources, 146 (1-2) Special Iss. SI (2005), 570-574.
5
C. Gleitzer, European Journal of Solid State Inorganic Chemistry, 28 (1991), 77-91.
6
C. Delacourt, PhD thesis (2005), University Picardie - Jules Verne.
7
J. L. Dormann, D. Fiorani, E. Tronc, Magnetic relaxation in fine-particle systems in
Advances in Chemical Physics (John wiley et Sons, Inc., 1997).
8
K. Shafi, A. Ulman, A. Dyal, X. Z. Yan, N. L. Yang, C. Estournes, L. Fournes, A.
Wattiaux, H. White, M. Rafailovich, Chemistry Of Materials, 14 (2002), 1778-1787.
9
A. A. M. Prince, S. Mylswamy, T. S. Chan, R. S. Liu, B. Hannoyer, M. Jean, C. H.
Shen, S. M. Huang, J. F. Lee, G. X. Wang, Solid State Communications, 132 (2004),
455-458.
10
J. Rodriguez-Carvajal, Laboratoire Lon Brillouin, http://www-
llb.cea.fr/fullweb/powder.htm, (2004).
11
Y. N. Xu, W. Y. Ching, Y. M. Chiang, Journal Of Applied Physics, 95 (11) Part 2
(2004), 6583-6585.
12
S. F. Yang, Y. N. Song, P. Y. Zavalij, M. S. Whittingham, Electrochemistry
Communications, 4 (2002), 239-244.
13
G. Rousse, J. Rodriguez-Carvajal, S. Patoux, C. Masquelier, Chemistry of Materials,
15 (2003), 4082-4090.
14
D. Arcon, A. Zorko, R. Dominko, Z. Jaglicic, Journal of Physics Condensed Matter,
16 (2004), 5531-5548.
15
N. Ravet, M. Gauthier, K. Zaghib, J. B. Goodenough, A. Mauger, F. Gendron, C. M.
Julien, Chemistry of Materials, 19 (2007), 2595-2602.
16
A. Ait Salah, K. Zaghib, A. Mauger, F. Gendron, C. M. Julien, Physica Status Solidi A
Applications And Materials Science, 203 (2006), R1-R3.
17
A. Ait Salah, A. Mauger, C. M. Julien, F. Gendron, Materials Science And
Engineering B Solid State Materials For Advanced Technology, 129 (2006), 232-244.
18
A. Ait Salah, A. Mauger, K. Zaghib, J. B. Goodenough, N. Ravet, M. Gauthier, F.
Gendron, C. M. Julien, Journal Of The Electrochemical Society, 153 (9) (2006),
A1692-A1701.
19
C. Delacourt, L. Laffont, R. Bouchet, C. Wurm, J. B. Leriche, M. Morcrette, J. M.
Tarascon, C. Masquelier, Journal Of The Electrochemical Society, 152 (5) (2005),
A913-A921.
20
A. Ait salah, P. Jozwiack, K. Zaghib, J. Garbarczyck, F. Gendron, A. Mauger, C. M.
Julien, Spectrochimica Acta Part A, 65 (2006), 1007-1013.
21
K. Nakamoto, Infrared and Raman Spectra of Inorganic and Coordination compounds,
New York, 1978).
22
M. T. Paques-Ledent, P. Tarte, Spectrochemica Acta, 30A (1973), 673-689.
23
C. M. Burba, R. Frech, Journal of the Electrochemical Society, 151 (2004), A1032-
A1038.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre IV
Magali Maccario 30 novembre 2007
93
24
C. M. Burba, R. Frech, Spectrochimica Acta Part A Molecular And Biomolecular
Spectroscopy, 65 (2006), 44-50.
25
N. Khay, A. Ennaciri, A. Harcharras, Vibrational Spectroscopy, 27 (2001), 119-126.
26
W. Choi, A. Manthiram, Journal Of The Electrochemical Society, 153 (9) (2006),
A1760-A1764.
27
K. El Kababi, K. Sbai, S. Vilminot, Comptes Rendus De L Academie Des Sciences
Serie Ii Fascicule C Chimie, 3 (2000), 693-701.
28
R. Podor, M. Francois, N. Dacheux, Journal Of Solid State Chemistry, 172 (2003), 66-
72.
29
C. Thomsen, S. Reich, Physical Review Letters, 85 (2000), 5214-5217.
30
R. Saito, A. Jorio, A. G. Souza, G. Dresselhaus, M. S. Dresselhaus, M. A. Pimenta,
Physical Review Letters, 8802 (2002), 7401,NIL_7113-NIL_7115.
31
P. Lespade, A. Marchand, M. Couzi, F. Cruege, Carbon, 22 (1984), 375-385.
32
F. Tuinstra, J. L. Koenig, Journal of chemical physics, 53 (1970), 1126.
33
C. M. Julien, K. Zaghib, A. Mauger, M. Massot, A. Ait Salah, M. Selmane, F.
Gendron, Journal Of Applied Physics, 100 (2006), NIL_215-NIL_221.
34
O. Beyssac, J. N. Rouzaud, B. Goffe, F. Brunet, C. Chopin, Contributions To
Mineralogy And Petrology, 143 (2002), 19-31.
35
J. M. Walter, www.jumwalter.de/raman.htm.
36
M. M. Doeff, Y. Q. Hu, F. McLarnon, R. Kostecki, Electrochemical And Solid State
Letters, 6 (2003), A207-A209.
37
R. Saito, A. Jorio, A. G. Souza, A. Grueneis, M. A. Pimenta, G. Dresselhaus, M. S.
Dresselhaus, Physica B Condensed Matter, 323 (2002), 100-106.
38
C. Beny-Bassez, J. N. Rouzaud, Scanning Electron Microscopy, 1985 (1985), 119-
132.
39
J. Robertson, Materials Science And Engineering R Reports, 37 (2002), 129-281.
40
M. J. Matthews, M. A. Pimenta, G. Deresselhaus, M. S. Deresselhaus, M. Endo,
Physical Review B, 59 (1999), R6585-R6588.
41
A. C. Ferrari, Diamond and Related Materials, 11 (3-6) Special Iss. SI (2002), 1053-
1061.
42
A. K. Padhi, K. S. Nanjundaswamy, J. B. Goodenough, Journal of the Electrochemical
Society, 144 (1997), 1188.
43
A. S. Andersson, J. O. Thomas, Journal Of Power Sources, 97-8 Special Iss. SI
(2001), 498-502.
44
A. Yamada, H. Koizumi, N. Sonoyama, R. Kanno, Electrochemical And Solid State
Letters, 8 (8) (2005), A409-A413.
45
S. Y. Chung, J. T. Bloking, Y. M. Chiang, Nature Materials, 1 (2002), 123-128.
46
C. Delacourt, C. Wurm, L. Laffont, J. B. Leriche, C. Masquelier, Solid State Ionics,
177 (2006), 333-341.
47
Y. B. Xu, Y. J. Lu, L. Yan, Z. Y. Yang, R. D. Yang, Journal Of Power Sources, 160
(2006), 570-576.
48
J. P. Prs, C. Delmas, A. Rougier, M. Broussely, F. Perton, P. Biensan, P. Willmann,
J. Phys. Chem. Solids, 57 (1996), 1057.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
95
Chapitre V
Caractrisation du matriau LiFePO
4
au cours du cyclage
lectrochimique en batteries au lithium
PARTIE A : ETUDE DU MECANISME DE DESINTERCALATION / INTERCALATION DU LITHIUM
DANS LIFEPO
4
AU COURS DU CYCLAGE ELECTROCHIMIQUE EN BATTERIES AU
LITHIUM..............................................................................................................................98
A-V-1 Etude par diffraction des rayons X dlectrodes rcupres au cours du premier
cycle lectrochimique des cellules LiFe
800-fast
.............................................................. 98
A-V-2 Etude par spectroscopie Mssbauer de matriaux C-Li
x
FePO
4
obtenus au cours
de la premire charge lectrochimique des cellules LiFe
800-fast
................................. 113
A-V-3 Etude par spectroscopie XPS dlectrodes enduites rcupres au cours des
premiers cycles lectrochimiques des cellules LiFe
575-fast
.......................................... 117
A-V-4 Etude par MET - HR de matriaux C-Li
x
FePO
4
rcuprs diffrents tats de
charge des cellules LiFe
800-fast
.................................................................................... 127
PARTIE B : ETUDE DE CYCLAGES LONGUE DUREE A TEMPERATURE AMBIANTE, 40C ET
60C............................................................................................................................... 134
B-V-1 Cyclages longue dure de cellules Li C-LiFePO
4
(Fe
800-fast
) diffrentes
tempratures.................................................................................................................. 134
B-V-2 Etude par diffraction des rayons X des matriaux rcuprs aprs des cyclages
longue dure.................................................................................................................. 141
PARTIE C : CONCLUSIONS ............................................................................................. 150
Bibliographie du Chapitre VI........................................................................................ 152
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
96
Nous venons de voir une tude dtaille des proprits structurales, physico-chimiques
et lectrochimiques de matriaux C-LiFePO
4
, ce chapitre portera sur ltude de ces matriaux
au cours du premier cycle lectrochimique mais galement lors de cyclages longue dure
diffrentes tempratures.
Dans un premier temps, lobjet de ce chapitre est ltude du mcanisme de
dsintercalation / intercalation du lithium dans LiFePO
4
. Ce mcanisme est usuellement dcrit
comme une raction biphase entre une phase riche en lithium (Li
1-
FePO
4
, 0) et une
phase pauvre en lithium (Li
FePO
4
, ' 0) ce qui est en bon accord avec la prsence dun
plateau 3.5 V vs. Li
+
/Li sur la courbe de cyclage lectrochimique [1,2]. Nanmoins, deux
domaines de solution-solide sont observs par Yamada et al. aux deux extrmits des courbes
de charge et de dcharge [3]. Cependant la description de ce mcanisme de
dsintercalation / intercalation du lithium dans LiFePO
4
en dbut et fin de charge / dcharge
reste trs controverse.
En effet ds 1997, J.B Goodenough et coll., qui furent les premiers envisager
lutilisation de LiFePO
4
comme lectrode positive pour batteries au lithium, dcrivirent le
mcanisme de dsintercalation du lithium dans Li
x
FePO
4
comme la migration de linterface
FePO
4
/ LiFePO
4
vers lintrieur de chaque particule [1]. Ce modle est appel mcanisme
cur corce. J. Thomas et coll. ont galement considr ce modle comme une description
approprie du mcanisme de dsintercalation / intercalation du lithium dans Li
x
FePO
4
, mais
en considrant la possibilit davoir diffrents centres de nuclation dans la particule : le
modle a t appel mosaque [2]. Ces deux modles sont trs proches lun de lautre, si ce
nest que le modle cur corce est une description locale du modle mosaque. Pendant la
charge, une corce de la phase pauvre en lithium (Li
'
FePO
4
) enroberait le cur compos de la
phase riche en lithium (Li
1-
FePO
4
). Les ions lithium et les lectrons migreraient du coeur vers
la surface et la phase Li
'
FePO
4
se formerait de la surface vers le coeur. Le phnomne inverse
se produirait pendant la dcharge.
Rcemment, des tudes par Microscopie Electronique Transmission Haute
Rsolution ont t ralises par les groupes de Richardson [4] et de Masquelier [5] pour
analyser exprimentalement le mcanisme de dsintercalation / intercalation du lithium dans
Li
x
FePO
4
. En effet, en utilisant des cristaux, en forme de plaquettes avec laxe b normal la
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
97
surface et dsintercals chimiquement, Chen et al. ont clairement montr la formation de
domaines ordonns FePO
4
et LiFePO
4
spars les uns des autres par des domaines
dsordonns. La raction se ferait avec une diffusion des ions lithium selon la direction b en
bon accord avec les tudes thoriques menes par Morgan et al. et plus rcemment par Islam
et al. [6,7], et avec un front de phase, dsordonn mais pas amorphe, parallle la direction a.
Ces rsultats montrent donc que le modle cur corce nest pas valide pour dcrire le
mcanisme de dsintercalation / intercalation du lithium dans LiFePO
4
. Ces rsultats ont de
plus t conforts rcemment par Laffont et al. qui ont montr par des tudes MET-HR et
EELS que la transition de phase se produit par les remplissages (ou vidages) successifs des
canaux occups par les ions lithium selon laxe b, ce qui conduit la formation de particules
partiellement lithies (ou dlithies) systmatiquement constitues dun corps de FePO
4
enrob dune corce de LiFePO
4
.
En considrant ces diffrents rsultats et dans le but de mieux comprendre le
phnomne de dsintercalation / intercalation du lithium dans Li
x
FePO
4
, la suite de ce
chapitre sera consacre ltude des matriaux Li
x
FePO
4
obtenus lectrochimiquement en
combinant la diffraction des rayons X, les spectroscopies Mssbauer et XPS et la Microscopie
Electronique Transmission Haute Rsolution. Les deux matriaux Fe
575-fast
et Fe
800-fast
ont t
choisis du fait de leurs diffrences en termes de comportement lectrochimique et surface
spcifique.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
98
PARTIE A : ETUDE DU MECANISME DE DESINTERCALATION / INTERC ALATION
DU LITHIUM DANS LIFEPO
4
AU COURS DU CYCLAGE ELECTROCHIMIQUE EN
BATTERIES AU LITHIUM
A-V-1 Etude par diffraction des rayons X dlectrodes rcupres au cours
du premier cycle lectrochimique des cellules LiFe
800-fast
A-V-1-1 Etude par diffraction des rayons X
La premire partie de ce chapitre est une tude par diffraction des rayons X de
matriaux Li
x
FePO
4
obtenus lors du premier cycle lectrochimique rgime C/20 de
batteries au lithium LiFe
800-fast
dans le domaine de potentiel [2 - 4.5] V (vs. Li
+
/Li). La
Figure V-1 donne un exemple de la courbe lectrochimique obtenue pour une cellule
LiFe
800-fast
. Cette figure confirme la prsence du plateau ~ 3.5 V vs. Li
+
/Li suggrant
lexistence dun domaine biphas entre Li
1-
FePO
4
et Li
FePO
4
( et 0). Les points ()
reprsents sur la courbe montrent les compositions Li
x
FePO
4
synthtises partir
dlectrodes enduites et tudies ex-situ par diffraction des rayons X.
0.0 0.2 0.4 0.6 0.8 1.0
2.0
2.5
3.0
3.5
4.0
4.5
P
o
t
e
n
t
i
a
l
v
s
.
L
i
+
/
L
i
(
V
)
x in Li
x
FePO
4
Figure V-1 : Exemple dune courbe de cyclage obtenue rgime de cyclage C/20 dans le domaine de
potentiel [2 - 4.5] V (vs. Li
+
/Li) pour Fe
800-fast
. Les compositions tudies ex-situ par diffraction des rayons
X sont mentionnes par des points sur la courbe.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
99
La Figure V-2 compare les diagrammes de diffraction des rayons X collects ex-situ
pour les diffrents matriaux Li
x
FePO
4
et illustre parfaitement le mcanisme biphas se
produisant au cours de la dsintercalation du lithium de LiFePO
4
. En effet, la phase riche en
lithium Li
1-
FePO
4
( 0) disparat progressivement alors que paralllement la phase pauvre
en lithium Li
FePO
4
( 0) apparat. La disparition de la phase riche en lithium se traduit
par la dcroissance de lintensit de certains pics observs ~ 19.8, ~ 26.3 et ~ 41.5 (2
Co
),
qui sont indexs comme tant respectivement les plans (200), (210) et (311) dans le groupe
despace Pnma, tandis que lapparition de la phase pauvre en lithium est associe lapparition
de nouveaux pics de diffraction observs ~ 20.8, ~ 27.5 et ~ 35.8 (2
Co
), qui sont
respectivement les plans (200)
Pnma
, (210)
Pnma
et (020)
Pnma
. Pendant la dcharge qui suit, le
mcanisme inverse se produit avec la croissance de la phase riche en lithium Li
1-
FePO
4
aux
dpens de la phase pauvre en lithium Li
'
FePO
4
. Il est noter que des rsultats similaires sont
obtenus pour les matriaux Li
x
FePO
4
obtenus partir dlectrodes poudre et que tous ces
rsultats sont en bon accord avec la littrature [1,8]. Le mcanisme de
dsintercalation / intercalation du lithium en tout dbut et fin de charge ou de dcharge sera
discut par la suite en comparant les paramtres de maille dtermins pour les phases
Li
x
FePO
4
tudies.
Le Tableau V-1 compare les FWHM des raies (200), (210), (311) et (200), (210),
(020) obtenues respectivement pour Li
1-
FePO
4
et Li
FePO
4
partir des diagrammes de
diffraction enregistrs pour les matriaux Li
x
FePO
4
synthtiss au cours de la charge et de la
dcharge. Pendant la charge pour la phase Li
1-
FePO
4
, les largeurs de raies mi-hauteur sont
lgrement plus faibles que celles observes pour la phase Li
FePO
4
. Le phnomne inverse,
c'est--dire des valeurs de FWHM lgrement plus faibles pour la phase Li
FePO
4
, est observ
lors de la dcharge suivante. Cependant, la faible prcision sur les valeurs de FWHM implique
que cette diffrence entre les deux phases demeure assez faible. De plus, on ne note pas
dvolution continue des valeurs de FWHM tout au long de la charge, contrairement ce que
lon pourrait attendre si il y avait croissance dune phase (Li
FePO
4
) au dtriment de la
seconde (Li
1-
FePO
4
) lors de la progression du front de phase.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
100
1
s
t
c
h
a
r
g
e
1
s
t
d
i
s
c
h
a
r
g
e
*
LiFePO
4
( )
Li
0.39
FePO
4
Li
0.53
FePO
4
Li
0.61
FePO
4
Li
0.72
FePO
4
Li
0.83
FePO
4
Li
0.36
FePO
4
Li
'
FePO
4
Li
0.06
FePO
4
Li
0.38
FePO
4
Li
0.46
FePO
4
Li
0.67
FePO
4
Li
0.78
FePO
4
Li
1-
FePO
4
* Sample-holder
Li
1-
FePO
4
Li
FePO
4
Li
0.96
FePO
4
(200) (200) (210) (210) (020) (311)
20 30 40 50
I
(
A
.
U
.
)
2
Co
()
Figure V-2 : Diffractogrammes des rayons X obtenus ex-situ pour des lectrodes enduites Li
x
FePO
4
rcupres diffrents tats de charge ou de dcharge pendant le premier cycle lectrochimique de la
cellule LiFe
800-fast
. Lindexation des pics de diffraction dans le groupe despace Pnma est donne pour
certains pics associs la phase riche en lithium (Li
1-
FePO
4
) et la phase pauvre en lithium
(Li
FePO
4
).
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
101
Tableau V-1 : Comparaison des largeurs de raies (FWHM) dtermines pour des pics slectionns sur les
diagrammes de diffraction des rayons X enregistrs pour les lectrodes enduites de composition
Li
x
FePO
4
rcupres diffrents tats de charge ou de dcharge pendant le premier cycle de la batterie
au lithium LiFe
800-fast
: (200), (210) et (311) pour Li
1-
FePO
4
et (200), (210) et (020) pour Li
FePO
4
. Les
paramtres microstructuraux, < >
1/2
pour les contraintes et < L > pour la taille des domaines de
cohrence, sont dtermins en considrant la fonction de ThompsonCoxHastings pour dcrire le profil
des pics de diffraction.
(*) calculation of < >
1/2
and < L > was not possible due to the lack of accuracy for this
minor phase.
Estimated formula FWHM () < >
1/2
< L >
Li
1-
FePO
4
Li
'
FePO
4
(200)
(200)
(210)
(210)
(311)
(020)
Fe
800-fast
0.07 0.08 0.09 6.4(7) x 10
-4
740 20
Li
~0.96
FePO
4
Li
1-
FePO
4
0.06 0.08 0.09 6(2) x 10
-4
750 60
Li
'
FePO
4
0.07 0.09 - (*) (*)
Li
~0.83
FePO
4
Li
1-
FePO
4
0.05 0.07 0.08 9(1) x 10
-4
800 30
Li
'
FePO
4
0.10 0.10 0.13 2.4(5) x 10
-3
730 20
Li
~0.72
FePO
4
Li
1-
FePO
4
0.06 0.06 0.08 5(1) x 10
-4
700 20
Li
'
FePO
4
0.10 0.12 0.12 2.5(5) x 10
-3
600 50
Li
~0.61
FePO
4
Li
1-
FePO
4
0.07 0.07 0.08 6(2) x 10
-4
730 40
Li
'
FePO
4
0.10 0.12 0.13 2.0(3) x 10
-3
650 70
Li
~0.53
FePO
4
Li
1-
FePO
4
0.07 0.07 0.09 9.6(5) x 10
-4
700 20
Li
'
FePO
4
0.10 0.12 0.14 2.1(2) x 10
-3
750 60
Li
~0.39
FePO
4
Li
1-
FePO
4
0.08 0.06 0.08 7(2) x 10
-4
820 100
Li
'
FePO
4
0.09 0.11 0.14 2.1(2) x 10
-3
930 140
Li
~0.36
FePO
4
Li
1-
FePO
4
0.10 0.08 0.10 9(3) x 10
-4
650 70
Li
'
FePO
4
0.10 0.11 0.13 1.8(2) x 10
-3
700 60
Li
FePO
4
Li
1-
FePO
4
- - - - -
1
s
t
c
h
a
r
g
e
Li
'
FePO
4
0.07 0.09 0.11 1.5(2) x 10
-3
760 100
Li
~0.06
FePO
4
Li
1-
FePO
4
0.15 0.10 0.17 (*) (*)
Li
'
FePO
4
0.08 0.10 0.10 1.2(2) x 10
-3
660 40
Li
~0.38
FePO
4
Li
1-
FePO
4
0.11 0.12 0.16 1.9(4) x 10
-3
540 100
Li
'
FePO
4
0.08 0.10 0.11 1.7(2) x 10
-3
840 100
Li
~0.46
FePO
4
Li
1-
FePO
4
0.11 0.11 0.14 1.4(4) x 10
-3
500 40
Li
'
FePO
4
0.07 0.09 0.11 1.5(2) x 10
-3
810 90
Li
~0.67
FePO
4
Li
1-
FePO
4
0.11 0.09 0.13 1.5(2) x 10
-3
650 50
Li
'
FePO
4
0.08 0.08 0.10 1.5(4) x 10
-3
930 140
Li
~0.78
FePO
4
Li
1-
FePO
4
0.08 0.09 0.12 1.2(2) x 10
-3
650 30
Li
'
FePO
4
0.07 0.08 0.09 1.6(2) x 10
-3
930 140
Li
1-
FePO
4
Li
1-
FePO
4
0.07 0.08 0.10 1.0(1) x 10
-3
740 40
1
s
t
d
i
s
c
h
a
r
g
e
Li
'
FePO
4
- - - - -
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
102
Un tel mcanisme a, par exemple, t dcrit lors dune tude ralise au laboratoire sur
lchange des ions sodium par des ions lithium dans la phase lamellaire P2-Na
0.7
CoO
2
[9]. Au
dbut de la raction dchange, les valeurs de FWHM associes la phase riche en lithium
O2-LiCoO
2
sont trs grandes (~ 0.55), en bon accord avec la formation de domaines de type
O2 de petite taille (~ 60 ) dans la phase P2. Au fur et mesure de la progression de la
raction dchange du Na
+
par le Li
+
, une dcroissance constante des FWHM est observe
pour la phase O2-LiCoO
2
indiquant ainsi une augmentation de la taille des domaines de
cohrence, dans le mme temps le phnomne inverse se produit pour la phase P2-Na
0.7
CoO
2
ce qui se traduit par une augmentation des FWHM et une dcroissance de la taille des
domaines. Quand lchange du Na
+
par le Li
+
est termin, des domaines de cohrence de
grande taille sont obtenus avec des valeurs de FWHM constantes et de lordre de 0.10 - 0.16
[9]. Une telle volution continue des valeurs de FWHM serait attendue pour les modles
mosaque ou coeur corce qui sont utiliss pour dcrire le mcanisme de
dsintercalation / intercalation du lithium dans le systme LiFePO
4
[8,10,11]. Le modle
cur - corce implique en effet la croissance de lcorce de composition FePO
4
autour du
cur de LiFePO
4
pendant la charge et linverse pendant la dcharge. Ltude par diffraction
des rayons X suggre donc, au moins pour les matriaux de type olivine LiFePO
4
tudis ici,
que le mcanisme de dsintercalation / intercalation du lithium doit tre diffrent du modle
cur corce.
Comme cela a dj t mentionn un peu plus tt, une tude par EELS-HR reporte par
le groupe de Masquelier [12] du systme biphas LiFePO
4
/ FePO
4
a galement montr que le
mcanisme de dsintercalation / intercalation du lithium nest pas bien dcrit par le modle
classique cur - corce. Ces auteurs ont tudi des particules fines en forme de plaquettes dont
la croissance sest faite dans le plan ac ; lobservation a donc t ralise dans le plan ac et
paralllement laxe b en bon accord avec les travaux de Morgan et al. [6] et plus rcemment
de Islam et al. [7], qui ont montr que la direction b serait privilgie pour la diffusion des ions
lithium dans la structure olivine. Pour ces auteurs, linterface entre ce cur de FePO
4
et cette
corce de LiFePO
4
serait de petite taille (10 15 nm) et serait un mlange des deux phases
extrmes, alors que Chen et al. considre que ce domaine intermdiaire serait dsordonn sous
la forme dune solution-solide [4]. Cependant, de la mme manire que pour le mcanisme
coeur corce, notre tude par diffraction des rayons X nest pas en accord avec ce
mcanisme de dsintercalation / intercalation du lithium dcrit par Laffont et al.. En effet, dans
le plan ac pendant la charge on assiste la croissance du coeur de FePO
4
et au rtrcissement
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
103
de lcorce de LiFePO
4
alors que pendant la dcharge il y a un rtrcissement du cur de
composition FePO
4
paralllement la croissance de lcorce de LiFePO
4
. Cela signifie que
pour une composition Li
x
FePO
4
, quand x augmente, il y a une dcroissance de la taille des
domaines de cohrence de la phase LiFePO
4
dans le plan ac alors quil y a croissance de la
taille des domaines de cohrence de la phase FePO
4
. On devrait donc observer une
augmentation des valeurs de FWHM pour les pics dont lindexation dpend de h pour la phase
LiFePO
4
et inversement une diminution de la valeur des FWHM pour les pics de mme
indexation pour la phase FePO
4
. De plus, cette volution doit tre continue avec x. Cependant,
comme on peut le voir dans le Tableau V-1, pour toutes les compositions tudies et pour les
deux phases Li
1-
FePO
4
et Li
FePO
4
, la comparaison des valeurs de FWHM des pics de
diffraction dindexation (200) ou (210) ne montre pas dvolution significative que ce soit en
charge ou en dcharge ; cela suggre au moins pour le matriau LiFePO
4
tudi dans ce
manuscrit que ds que la raction de dsintercalation / intercalation du lithium est initie
un point de la cristallite, elle se rpand immdiatement dans tout le reste de la cristallite.
Le matriau de composition Li
x
FePO
4
serait donc, quel que soit son tat de charge
ou de dcharge, un mlange de cristallites de composition Li
1-
FePO
4
et Li
FePO
4
,
chacune
serait homogne dans nimporte quelle direction cristallographique.
A-V-1-2 Etude structurale des matriaux obtenus au cours du premier cycle
lectrochimique
Pour dterminer prcisment la structure cristallographique de chaque composition
Li
x
FePO
4
obtenue mais galement comparer ces matriaux au matriau initial, des
affinements par la mthode de Rietveld des donnes de diffraction des rayons X enregistres
pour chaque composition ont t raliss [13]. Dans un premier temps, un full pattern
matching a t effectu pour dterminer les paramtres de maille de la (ou des) phase(s)
prsente(s) mais galement les paramtres de profil de la fonction pseudo-Voigt utilise pour
dcrire la forme des raies de diffraction. Les mailles des deux phases sont dcrites dans le
groupe despace Pnma avec les paramtres a ~ 10.32 , b ~ 6.01 et c ~ 4.70 pour
Li
1-
FePO
4
et a ~ 9.82 , b ~ 5.80 et c ~ 4.78 pour Li
FePO
4
[8].
La seconde tape est laffinement structural par la mthode de Rietveld en considrant
les hypothses structurales [Li]
4a
[Fe]
4c
PO
4
et [Fe]
4c
PO
4
pour ces deux phases. Le choix de ces
hypothses repose sur les tudes ralises sur les matriaux initiaux (cf. Chapitre IV) qui ont
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
104
montr que Fe
800-fast
peut tre dcrit par une structure olivine parfaitement ordonne. Comme
prcdemment le profil des pics de diffraction est dcrit grce la fonction de Thompson-Cox-
Hastings pour tenir compte pour ce type de matriaux Li
x
FePO
4
des possibles effets dus la
microstructure ; cela permet de dcrire prcisment lvolution, tout au long du cyclage
lectrochimique, des contraintes et des tailles de domaine de cohrence pour les phases
Li
1-
FePO
4
et Li
FePO
4
. Le modle qui dcrit le mieux les donnes de diffraction des rayons
X est celui qui considre une contribution isotrope dcrite par des fonctions lorentzienne et
gaussienne pour considrer respectivement les effets de taille et de contraintes [13]. Seuls les
paramtres U et Y sont affins alors que V et W sont fixs aux valeurs dtermines pour LaB
6
utilis comme chantillon de rfrence.
A-V-1-2-a Etude structurale des compositions Li
~0.39
FePO
4
et
Li
~0.38
FePO
4
obtenues respectivement en charge et en dcharge
Ltude des deux compositions proches Li
~0.39
FePO
4
et Li
~0.38
FePO
4
obtenues
lectrochimiquement partir dlectrodes enduites, respectivement aprs une charge partielle
et aprs une charge suivie dune dcharge partielle, est prsente ici en dtails. Les
diffractogrammes X ont fait lobjet dun affinement par la mthode de Rietveld dont les
rsultats sont rsums au Tableau V-2 et au Tableau V-3 pour ces deux compositions. Ces
affinements montrent des facteurs de reliabilit faibles (par exemple pour Li
~0.39
FePO
4
:
R
wp
= 12.7 %, R
B
(Li
1-
FePO
4
) = 8.09 % et R
B
(Li
FePO
4
) = 7.34 %) mais galement une bonne
minimisation de la diffrence I
obs.
- I
calc.
, comme on peut le voir sur la Figure V-3 qui
donne pour ces matriaux une comparaison des diffractogrammes exprimentaux et calculs.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
105
Tableau V-2 : Paramtres structuraux et de profil dtermins pour le matriau biphas Li
~0.39
FePO
4
(lectrode enduite) obtenu lectrochimiquement aprs une charge partielle de la cellule lectrochimique
LiFe
800-fast
.
Li
~0.39
FePO
4
(Cast electrode, obtained during the first charge)
Li
1-
FePO
4
Space group: Pnma
a = 10.323(1)
b = 6.0041(7)
c = 4.6937(6)
V = 290.91(6)
3
Li
FePO
4
Space group: Pnma
a = 9.828(1)
b = 5.7957(6)
c = 4.7816(6)
V = 272.36(6)
3
Li
1-
FePO
4
Site Wyckoff positions Occupancy B()
Li 4a 0 0 0 1 6(5)
Fe 4c 0.283(2) 0.973(5) 1 4(1)
P 4c 0.090(4) 0.405(7) 1 5(1)
O1 4c 0.100(7) 0.73(1) 1 5(3)
O2 4c 0.454(6) 0.22(1) 1 5(2)
O3 8d 0.161(4) 0.050(7) 0.287(8) 1 2(1)
Li
FePO
4
Fe 4c 0.276(2) 0.957(5) 1 6.1(9)
P 4c 0.098(3) 0.398(7) 1 6(1)
O1 4c 0.115(5) 0.72(1) 1 6(2)
O2 4c 0.452(6) 0.18(1) 1 6(2)
O3 8d 0.157(4) 0.025(8) 0.256(7) 1 8(1)
Conditions of the run
Temperature
Angular range
Number of points
Displacement sample holder (2)
Number of fitted parameters
300 K
15 2 75
3884
-0.170(7)
46
Profile parameters
Thompson-Cox-Hastings function (*LaB
6
used as standard)
Li
1-
FePO
4
Li
'
FePO
4
Y = 0.08(1)
U = 0.03(2)
V = -0.0017 fixed*
W = 0.00383 fixed*
Y = 0.07(1)
U = 0.21(4)
V = -0.0017 fixed*
W = 0.00383 fixed*
Conventional Rietveld R-factors for points with Bragg contribution
R
wp
= 12.7 %
Li
1-
FePO
4
R
B
= 8.09 %
Li
'
FePO
4
R
B
= 7.34 %
Note: standard deviations have been multiplied by the Scor parameter (~ 4.8) to correct for
local correlations.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
106
Tableau V-3 : Paramtres structuraux et de profil dtermins pour le matriau biphas Li
~0.38
FePO
4
(lectrode enduite) obtenu lectrochimiquement aprs une charge et une dcharge partielle de la cellule
lectrochimique LiFe
800-fast
.
Li
~0.38
FePO
4
(Cast electrode, obtained during the first discharge)
Li
1-
FePO
4
Space group: Pnma
a = 10.314(2)
b = 6.0014(8)
c = 4.6941(8)
V = 290.57(8)
3
Li
FePO
4
Space group: Pnma
a = 9.822(1)
b = 5.7931(5)
c = 4.7801(6)
V = 271.99(5)
3
Li
1-
FePO
4
Site Wyckoff positions Occupancy B()
Li 4a 0 0 0 1 0(5)
Fe 4c 0.282(2) 0.975(6) 1 3(1)
P 4c 0.099(4) 0.427(7) 1 3(1)
O1 4c 0.07(1) 0.74(2) 1 8(3)
O2 4c 0.460(6) 0.20(1) 1 2(2)
O3 8d 0.170(5) 0.054(8) 0.276(9) 1 3(2)
Li
FePO
4
Fe 4c 0.274(1) 0.957(4) 1 4.1(6)
P 4c 0.096(3) 0.398(6) 1 5(1)
O1 4c 0.121(4) 0.702(9) 1 6(2)
O2 4c 0.450(5) 0.164(7) 1 2(1)
O3 8d 0.159(3) 0.037(6) 0.254(6) 1 6(1)
Conditions of the run
Temperature
Angular range
Number of points
Displacement sample holder (2)
Number of fitted parameters
300 K
15 2 75
3884
-0.170(7)
46
Profile parameters
Thompson-Cox-Hastings function (*LaB
6
used as standard)
Li
1-
FePO
4
Li
'
FePO
4
Y = 0.12(2)
U = 0.17(6)
V = -0.0017 fixed*
W = 0.00383 fixed*
Y = 0.078(9)
U = 0.14(3)
V = -0.0017 fixed*
W = 0.00383 fixed*
Conventional Rietveld R-factors for points with Bragg contribution
R
wp
= 11.9 %
Li
1-
FePO
4
R
B
= 8.84 %
Li
'
FePO
4
R
B
= 5.65 %
Note: standard deviations have been multiplied by the Scor parameter (~ 4.8) to correct for
local correlations.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
107
Le Tableau V-2 et le Tableau V-3 permettent une comparaison des paramtres de
maille dtermins pour des matriaux prsentant approximativement la mme composition,
mais avec des historiques de cyclage diffrents : les paramtres de maille a et b dtermins
pour les phases riche en lithium Li
1-
FePO
4
et pauvre en lithium Li
FePO
4
sont lgrement
infrieurs pour le matriau biphas Li
~0.38
FePO
4
obtenu aprs une charge et une dcharge
partielle compars ceux dtermins pour le matriau Li
~0.39
FePO
4
obtenu aprs une charge
partielle. Les paramtres c des deux phases Li
1-
FePO
4
et Li
FePO
4
sont similaires lcart-
type prs, quel que soit le mode de synthse du matriau, c'est--dire quil soit obtenu en
charge ou en dcharge. Il est galement noter que lamplitude de la diffrence entre les
paramtres de maille des phases riche en lithium Li
1-
FePO
4
et pauvre en lithium Li
FePO
4
demeure stable quel que soit lhistorique de cyclage. On observe une contraction des
paramtres a et b entre Li
1-
FePO
4
et Li
FePO
4
respectivement de ~ 5 % et ~ 3.5 % et une
augmentation du paramtre c de ~ 2%.
A-V-1-2-b Etude structurale gnrale des diffrentes compositions obtenues en
charge ou en dcharge
Une tude structurale plus gnrale a galement t ralise, partir des donnes de
diffraction des rayons X, pour les diffrentes lectrodes enduites et poudre rcupres
diffrentes compositions Li
x
FePO
4
, que ce soit aprs une charge partielle ou aprs une
charge et une dcharge partielle. Les paramtres de maille dtermins pour les diffrents
matriaux obtenus (monophass ou biphass) sont compars la Figure V-4.
Comme cela a dj t soulign pour les deux matriaux Li
~0.39
FePO
4
(obtenu au
cours de la premire charge) et Li
~0.38
FePO
4
(obtenu au cours de la premire dcharge), les
paramtres de maille a et b sont lgrement infrieurs pour les matriaux obtenus au cours
dune charge puis dune dcharge partielle (, ) compars ceux dtermins pour les
matriaux obtenus aprs une premire charge partielle (, ) ; le paramtre c demeure constant
quel que soit lhistorique de cyclage des lectrodes. Ces rsultats paramtres de maille
infrieurs pour les matriaux rcuprs aprs une charge et une dcharge partielle sont
gnralisables aux matriaux rcuprs aprs un plus grand nombre de cycles, quel que soit ce
nombre.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
108
Li
~0.39
FePO
4
Li
~0.38
FePO
4
20 30 40 50 60 70
Li
'
FePO
4
Li
1-
FePO
4
*
*
Yobs
Ycalc
Yobs-Ycalc
* Sample-holder
I
(
A
.
U
.
)
2
Co
()
25 30 35 40
Li
'
FePO
4
Li
1-
FePO
4
I
(
A
.
U
.
)
2
Co
()
20 30 40 50 60 70
Li
'
FePO
4
Li
1-
FePO
4
*
*
Yobs
Ycal
Yobs-Ycal
* Sample-holder
I
(
A
.
U
.
)
2
Co
()
25 30 35 40
Li
'
FePO
4
Li
1-
FePO
4
I
(
A
.
U
.
)
2
Co
()
a)
b)
Figure V-3 : Comparaison des diagrammes de diffraction des rayons X exprimental et calcul pour les
matriaux biphass a) Li
~0.39
FePO
4
(lectrode enduite) obtenu lectrochimiquement aprs une charge
partielle de la cellule lectrochimique LiFe
800-fast
et b) Li
~0.38
FePO
4
(lectrode enduite) obtenu
lectrochimiquement aprs une charge et une dcharge partielle de la cellule lectrochimique
LiFe
800-fast
.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
109
Comme attendu, on ne note pas de diffrences entre les paramtres de maille
dtermins pour les phases riche et pauvre en lithium, Li
1-
FePO
4
et Li
FePO
4
, entre les
lectrodes enduites ou poudre rcupres au cours de la premire charge.
La comparaison des paramtres de maille des matriaux dsintercals avec ceux des
deux phases extrmes LiFePO
4
et Li
FePO
4
, reprsents par des lignes pointilles la Figure
V-4, montre que quel que soit lhistorique de cyclage pendant le premier cycle
lectrochimique, les paramtres structuraux (a, b et V) de la phase riche en lithium Li
1-
FePO
4
prsente dans les matriaux biphass Li
x
FePO
4
sont toujours infrieurs ceux dtermins
pour le matriau initial LiFePO
4
; les paramtres structuraux (a, b et V) de la phase pauvre en
lithium Li
FePO
4
prsente dans le matriau biphas sont gnralement suprieurs ceux
dtermins pour la phase extrme FePO
4
. Cependant, quels que soient la phase tudie et
lhistorique de cyclage, il ny a pas dvolution majeure du paramtre c. Ces rsultats,
paramtres de maille infrieurs ou suprieurs ceux des phases extrmes selon que lon tudie
Li
1-
FePO
4
ou Li
FePO
4
, sont aussi observs pour les matriaux ayant effectu un plus grand
nombre de cycles lectrochimiques.
Les rsultats obtenus par diffraction des rayons X montrent que la dsintercalation du
lithium partir de LiFePO
4
se fait selon une solution-solide en tout dbut et fin de charge : en
effet, dans le cas contraire les paramtres de maille des deux phases prsentes dans le
mlange biphas devraient tre gaux aux paramtres des phases extrmes. Ces domaines de
solution-solide sont galement observs en dbut et en fin de dcharge. Ces rsultats
confirment donc les rsultats publis par Yamada et al. [3].
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
110
F
i
g
u
r
e
V
-
4
:
C
o
m
p
a
r
a
i
s
o
n
d
e
s
p
a
r
a
m
t
r
e
s
s
t
r
u
c
t
u
r
a
u
x
o
b
t
e
n
u
s
p
a
r
l
a
f
f
i
n
e
m
e
n
t
p
a
r
l
a
m
t
h
o
d
e
d
e
R
i
e
t
v
e
l
d
d
e
s
d
o
n
n
e
s
d
e
d
i
f
f
r
a
c
t
i
o
n
d
e
s
r
a
y
o
n
s
X
e
n
r
e
g
i
s
t
r
e
s
p
o
u
r
l
e
s
l
e
c
t
r
o
d
e
s
e
n
d
u
i
t
e
s
e
t
p
o
u
d
r
e
.
L
e
s
p
o
i
n
t
i
l
l
s
r
e
p
r
s
e
n
t
e
n
t
l
e
s
p
a
r
a
m
t
r
e
s
o
b
t
e
n
u
s
p
o
u
r
l
e
s
m
a
t
r
i
a
u
x
d
e
c
o
m
p
o
s
i
t
i
o
n
s
e
x
t
r
m
e
s
L
i
F
e
P
O
4
e
t
L
i
F
e
P
O
4
,
c
e
u
x
-
c
i
s
o
n
t
m
o
n
o
p
h
a
s
s
.
L
i
1
-
e
F
e
P
O
4
(
P
r
e
s
s
e
d
p
o
w
d
e
r
e
l
e
c
t
r
o
d
e
s
,
1
s
t
c
h
a
r
g
e
)
L
i
e
'
F
e
P
O
4
(
P
r
e
s
s
e
d
p
o
w
d
e
r
e
l
e
c
t
r
o
d
e
s
,
1
s
t
c
h
a
r
g
e
)
L
i
1
-
e
F
e
P
O
4
(
C
a
s
t
e
l
e
c
t
r
o
d
e
s
,
1
s
t
c
h
a
r
g
e
)
L
i
e
'
F
e
P
O
4
(
C
a
s
t
e
l
e
c
t
r
o
d
e
s
,
1
s
t
c
h
a
r
g
e
)
L
i
1
-
e
F
e
P
O
4
(
C
a
s
t
e
l
e
c
t
r
o
d
e
s
,
1
s
t
d
i
s
c
h
a
r
g
e
)
L
i
e
'
F
e
P
O
4
(
C
a
s
t
e
l
e
c
t
r
o
d
e
s
,
1
s
t
d
i
s
c
h
a
r
g
e
)
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
111
Les liaisons Li-O, Fe-O et P-O calcules pour la phase Li
1-
FePO
4
prsente dans le
matriau biphas Li
~0.39
FePO
4
varient respectivement de 2.04(3) 2.23(4) , de 2.08(4)
2.28(4) et de 1.51(6) 1.53(7) avec des valeurs moyennes de 2.14 , 2.18 et
1.52 . Pour la phase pauvre en lithium (Li
FePO
4
), les distances Fe-O varient entre 1.96(5)
et 2.26(4) et les distances P-O entre 1.48(7) et 1.58(5) avec des valeurs moyennes
respectivement gales 2.08 et 1.54 . Lors des affinements, les distances P-O sont
contraintes appartenir lintervalle [1.48 1.60] , qui correspond aux valeurs attendues
pour les distances P-O dans un ttradre PO
4
. Cependant, certaines liaisons P-O sont
lgrement infrieures la somme des rayons ioniques des ions P
5+
et O
2-
(1.57 ) [14], ce qui
est en bon accord avec la distorsion importante des ttradres PO
4
dans Li
FePO
4
par rapport
un ttradre parfait et avec la forte covalence des liaisons P-O
Comme attendu du fait des faibles diffrences structurales entre Li
~0.39
FePO
4
et
Li
~0.38
FePO
4
, obtenus respectivement au cours dune charge partielle et aprs une charge et
une dcharge partielle, les diffrentes liaisons calcules sont trs similaires.
La Figure V-5 prsente une comparaison des polydres FeO
6
et PO
4
des phases
extrmes (LiFePO
4
et Li
FePO
4
( 0)) obtenues dans ce travail. On peut clairement noter
lvolution de la distorsion des polydres avec la composition en lithium. Par exemple, langle
O1-Fe-O2 volue de 177.3 dans la structure de LiFePO
4
167.6 dans la structure de
Li
FePO
4
. Cette dformation plus importante de loctadre FeO
6
dans Li
FePO
4
est confirme
par le calcul qui donne des distorsions gales
6
FeO
~ 1.4 x 10
-3
et
6
FeO
~ 3.1 x 10
-3
respectivement pour LiFePO
4
et Li
FePO
4
. Cependant, la distorsion des ttradres PO
4
est
infrieure pour Li
FePO
4
(
4
PO
~ 1.4 x 10
-4
) compare celle calcule pour LiFePO
4
(
4
PO
~ 2.6 x 10
-4
). Il est noter que la distorsion se calcule daprs la formule
2
1
) (
1
=
=
N
i
i
d
d d
N
, o d
i
est la longueur de la liaison, d la longueur moyenne de la
liaison et N le nombre de liaisons.
Les paramtres microstructuraux, c'est--dire les contraintes (<
2
>
1/2
) et la taille des
domaines de cohrence (< L >), dtermins partir des affinements par la mthode de Rietveld
des matriaux obtenus au cours du premier cycle lectrochimique, sont rapports dans le
Tableau V-1.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
112
2.28
LiFePO
4
Li
FePO
4
2.33
a) b)
Figure V-5 : Polydres FeO
6
et PO
4
a) dans la structure olivine LiFePO
4
et b) dans la structure olivine
Li
FePO
4
.
La comparaison des valeurs de contraintes montre quelles restent quasi constantes
pour chaque phase (la phase riche en lithium (Li
1-
FePO
4
) ou la phase pauvre en lithium
(Li
FePO
4
)) quel que soit ltat de charge ou de dcharge. Cependant, les contraintes
dtermines pour la phase Li
1-
FePO
4
semblent infrieures pendant la premire charge, puis
elles augmentent progressivement au cours de la dcharge et deviennent quasiment gales
celles dtermines pour la phase Li
FePO
4
.
La comparaison de la taille des domaines de cohrence montre quil ny a pas
dvolution majeure lcart-type prs quels que soient la phase (Li
FePO
4
ou Li
1-
FePO
4
), la
composition en lithium Li
x
FePO
4
ou lhistorique de cyclage (matriau obtenu en cours de
charge ou de dcharge). De plus, pour une composition donne, les tailles des domaines de
cohrence sont trs similaires pour les deux phases mais galement celle des cristallites
dtermines par Microscopie Electronique Transmission (cf. paragraphe IV-8-2 du Chapitre
IV). Ces rsultats sont en bon accord avec les rsultats discuts au paragraphe A-V-1-1 de ce
chapitre, qui ont montr quil ny a pas dvolution des FWHM des raies de diffraction des
deux phases au cours de la charge et de la dcharge, et montrent une nouvelle fois que les
contraintes et les tailles des domaines de cohrence nvoluent pas continment au cours du
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
113
processus de charge / dcharge comme cela serait attendu pour un modle cur corce ou
mosaque.
Ltude par diffraction des rayons X ne montre pas dvolution continue des tailles
des domaines de cohrence des deux phases Li
FePO
4
et Li
1-
FePO
4
au cours du cyclage
lectrochimique quels que soient ltat de charge ou la direction cristallographique. Ces
rsultats montrent que les modles proposs dans la littrature ne permettent pas dexpliquer
le mcanisme de dsintercalation / intercalation du lithium observ pour nos matriaux
C-LiFePO
4
.
A-V-2 Etude par spectroscopie Mssbauer de matriaux C-Li
x
FePO
4
obtenus au cours de la premire charge lectrochimique des cellules
LiFe
800-fast
Ltude par spectroscopie Mssbauer a t ralise pour suivre lvolution du degr
doxydation du fer et par consquent le mcanisme redox se produisant au cours du processus
lectrochimique. La Figure V-6 donne lvolution des spectres Mssbauer avec la
dsintercalation du lithium de LiFePO
4
partir dlectrodes poudre.
Le spectre initial peut tre dcompos en deux doublets, comme on a dj pu le
discuter aux Chapitres III et IV : un doublet associ aux ions Fe
2+
dans la phase de structure
olivine LiFePO
4
et un doublet associ aux ions Fe
3+
, dont la prsence peut tre lie la
prsence dune impuret amorphe riche en Fe
3+
et/ou de dfauts de surface. La dsintercalation
du lithium provoque la croissance dun autre doublet dont le dplacement isomrique
( ~ 0.43 mm.s
-1
) est caractristique dions Fe
3+
dans un environnement octadrique
doxygne. De plus, la valeur leve de lclatement quadrupolaire ( ~ 1.5 mm.s
-1
) de ce
doublet est caractristique dun environnement trs distordu. Lapparition de ce doublet est
associer un nouveau ion fer trivalent et sa croissance avec la dsintercalation du lithium
partir de LiFePO
4
est en bon accord avec le mcanisme biphas dj observ par diffraction
des rayons X [8]. De plus les paramtres hyperfins dtermins dans cette tude, c'est--dire
~ 0.43 mm.s
-1
et ~ 1.5 mm.s
-1
, sont en bon accord avec les paramtres reports dans la
littrature pour la phase htrosite Li
FePO
4
( 0) par les groupes de Thomas et Nazar
[8,15].
La comparaison des paramtres hyperfins obtenus pour les ions Fe
3+
dans la phase
htrosite et dans les deux phases hydrates FePO
4
.2H
2
O montre une large gamme de valeurs
([0.25 - 1.6] mm.s
-1
) possibles pour lclatement quadrupolaire, avec un dplacement
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
114
isomrique constant de ~ 0.4 mm.s
-1
[16-18]. On peut noter que lclatement quadrupolaire
varie continment avec la distorsion de loctadre FeO
6
(
6
FeO
). En effet, cet clatement varie
de ~ 0.25 mm.s
-1
pour FePO
4
.2H
2
O (P2
1
/n), ~ 0.36 mm.s
-1
pour FePO
4
.2H
2
O (Pbca) et
finalement ~ 1.5 mm.s
-1
pour la phase FePO
4
htrosite [18], paralllement aux distorsions
des octadres FeO
6
qui sont respectivement ~ 2 x 10
-4
, ~ 8 x 10
-4
et ~ 3 x 10
-3
. En effet, comme
cela a dj t signal lclatement quadrupolaire dpend de deux contributions : la
configuration lectronique du cation lui-mme, pour ces trois matriaux on a la mme
distribution symtrique des lectrons de valence (d
5
:
2 3
2 g g
e t ) il ny a donc aucune contribution,
et lenvironnement lectronique des voisins, qui est diffrent pour les trois matriaux et qui les
diffrencie au niveau de lanalyse par spectroscopie Mssbauer.
Dans un premier temps, les analyses des spectres Mssbauer ont t ralises en
ajustant les raies avec un profil lorentzien. Cependant la largeur des raies, nettement suprieure
la valeur thorique de ~ 0.20 0.30 mm.s
-1
, nous a conduit raliser le calcul des spectres
avec une distribution dclatements quadrupolaires. Lors de cet affinement, une seule
population est considre pour les ions Fe
2+
alors quau moins deux sont prendre en compte
pour les ions Fe
3+
. Un exemple de la distribution dclatements quadrupolaires des ions Fe
3+
est donn la Figure V-7 pour le matriau Li
~0.32
FePO
4
. La population intense centre
~ 1.5 mm.s
-1
correspond aux ions Fe
3+
prsents dans la phase de structure olivine forme par
la dsintercalation du lithium, alors que la population la moins importante (~ 5 at. % de la
quantit totale de fer) observe des valeurs dclatement quadrupolaire infrieures
(< 1.2 mm.s
-1
) est celle relative aux ions Fe
3+
qui taient dj prsents dans le matriau initial.
Cependant, la position exacte de lclatement quadrupolaire de cette population est difficile
dterminer du fait de la valeur leve de la largeur mi-hauteur des raies des doublets (~ 0.5
0.6 mm.s
-1
). Le Tableau V-4 rapporte, pour chaque matriau Li
x
FePO
4
, seulement les
pourcentages relatifs associs aux ions Fe
2+
et Fe
3+
prsents dans les phases de structure
olivine Li
1-
FePO
4
et Li
FePO
4
. En effet, tous les matriaux tudis prsentent sensiblement la
mme quantit dions Fe
3+
supplmentaires, donc ses paramtres Mssbauer ne sont pas
reports dans le Tableau V-4. Ces ions Fe
3+
supplmentaires sont inactifs
lectrochimiquement, il ny a en effet pas dvolution de leurs paramtres Mssbauer
( = 0.4 mm.s
-1
, = 0.72 mm.s
-1
et = 0.55 mm.s
-1
) ni de leur quantit au cours de cette
premire charge. Dautre part, on peut noter le bon accord entre les formules chimiques
dtermines par laffinement par la mthode de Rietveld des donnes de diffraction des rayons
X (colonne de gauche) et celles dtermines partir des donnes de spectroscopie Mssbauer.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
115
-2 0 2 4
A
obs.
A
calc.
"Li
~0.99
FePO
4
"
"Li
~0.32
FePO
4
"
"Li
~0.36
FePO
4
"
"Li
~0.39
FePO
4
"
"Li
~0.41
FePO
4
"
"Li
~0.61
FePO
4
"
"Li
~0.85
FePO
4
"
LiFePO
4
(Fe
800-fast
)
Velocity (mm.s
-1
)
A
b
s
o
r
p
t
i
o
n
(
A
.
U
.
)
Fe
2+
Fe
3+
Figure V-6 : Spectres Mssbauer enregistrs pour des lectrodes poudre de composition Li
x
FePO
4
rcupres diffrents tats de charge pendant le premier cycle lectrochimique en batterie au lithium
LiFe
800-fast
.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
116
0.0 0.5 1.0 1.5 2.0 2.5 3.0
P
(
)
(
A
.
U
.
)
(mm.s
-1
)
Figure V-7 : Distribution dclatements quadrupolaires associe aux ions Fe
3+
pour le matriau
Li
~0.32
FePO
4
.
Tableau V-4 : Paramtres hyperfins dtermins par spectroscopie Mssbauer ( : dplacement isomrique,
: clatement quadrupolaire moyen et : largeur mi-hauteur) partir de lanalyse des spectres des
diffrents matriaux Li
x
FePO
4
synthtiss lectrochimiquement pendant la premire charge dune
cellule lectrochimique LiFe
800-fast
. Les spectres ont t analyss avec une distribution dclatements
quadrupolaires. Il est noter que les valeurs de et sont fixes aux valeurs dtermines lors de
laffinement des raies avec un profil lorentzien. Il est noter que les ions Fe
3+
supplmentaires, prsents
dans le matriau initial et attribus des dfauts de surface ou une impuret amorphe riche en Fe
3+
,
nont pas t pris en compte dans le calcul des proportions prsent dans ce tableau pour les phases
dsintercales Li
x
FePO
4
: ces 5% dions Fe
3+
se sont effectivement avrs tre lectrochimiquement inactifs
avec des caractristiques Mssbauer qui nvoluent donc pas.
(*) fixed
Formula determined by
Rietveld refinement
(mm/s) (mm/s) (mm/s) % Iron-type
1.217(2) 2.945(2) 0.259(1) 95 Fe
2+
[O
h
]
Fe
800-fast
0.4(1) 0.8(1) 0.6(1) 5 Fe
3+
Li
~0.99
FePO
4
1.23 2.96 0.20 100 Fe
2+
[O
h
]
1.23
(*)
2.94 0.20
(*)
86 Fe
2+
[O
h
]
Li
~0.85
FePO
4
0.43
(*)
1.37 0.20
(*)
14 Fe
3+
[O
h
]
1.23
(*)
2.94 0.20
(*)
59 Fe
2+
[O
h
]
Li
~0.61
FePO
4
0.43
(*)
1.65 0.20
(*)
41 Fe
3+
[O
h
]
1.24
(*)
2.92 0.20
(*)
41 Fe
2+
[O
h
]
Li
~0.41
FePO
4
0.44
(*)
1.60 0.20
(*)
59 Fe
3+
[O
h
]
1.24
(*)
2.90 0.20
(*)
37 Fe
2+
[O
h
]
Li
~0.39
FePO
4
0.43
(*)
1.54 0.20
(*)
63 Fe
3+
[O
h
]
1.24
(*)
2.89 0.20
(*)
38 Fe
2+
[O
h
]
Li
~0.36
FePO
4
0.43
(*)
1.46 0.20
(*)
62 Fe
3+
[O
h
]
1.23
(*)
2.89 0.20
(*)
33 Fe
2+
[O
h
]
Li
~0.32
FePO
4
0.43
(*)
1.48 0.20
(*)
67 Fe
3+
[O
h
]
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
117
A-V-3 Etude par spectroscopie XPS dlectrodes enduites rcupres au
cours des premiers cycles lectrochimiques des cellules LiFe
575-fast
Les analyses XPS, en collaboration avec lIPREM de Pau, ont t ralises dune part
pour suivre le processus redox se produisant au cours de la raction de
dsintercalation / intercalation du lithium de LiFePO
4
et, dautre part, pour observer les
changements pouvant se produire linterface lectrode / lectrolyte. Les rsultats prsents en
dtail dans ce paragraphe sont ceux obtenus pour le matriau Fe
575-fast
qui est le matriau
C-LiFePO
4
de la srie tudie au Chapitre IV qui prsente la plus grande surface spcifique.
A-V-3-1 Etude des matriaux initiaux (poudre et lectrode enduite)
La Figure V-8 (a-d) montre les spectres XPS de Fe 2p, P 2p, O 1s et C 1s obtenus
pour le matriau initial Fe
575-fast
(poudre) et pour une lectrode enduite prpare partir de ce
matriau. Le pic Li 1s (~ 55 eV) nest pas prsent car il est totalement cach par le pic Fe 3p
dont le facteur de sensibilit est approximativement 30 fois suprieur celui de Li 1s.
Comme le montre la Figure V-8a, le spectre de Fe 2p est scind en deux parties
cause du couplage spin-orbite : Fe 2p
3/2
et Fe 2p
1/2
, avec un rapport dintensit de 2/1 entre ces
deux massifs de pics. Chaque partie est constitue dun pic principal et dun pic satellite
shake-up [19]. LiFePO
4
prsente un pic principal Fe 2p
3/2
710 eV avec son satellite
~ 715 eV et de la mme manire pour Fe 2p
1/2
on a respectivement 724 et 729 eV. Ces spectres
sont en bon accord avec ce qui est attendu pour des ions Fe
2+
en environnement octadrique
doxygne. Lclatement en deux composantes du pic principal de Fe 2p
3/2
( 709.5 et
710.5 eV) ne peut pas sexpliquer par la prsence la surface du matriau des ions Fe
3+
dtects par spectroscopie Mssbauer. En effet, lclatement observ (E ~ 5.7 eV) sur le
spectre Fe 3s (cf. Figure V-9) est caractristique dions Fe
2+
[19] car il serait de ~ 6.5 eV pour
des ions Fe
3+
. Dautre part, la signature XPS des ions Fe
3+
est
trs diffrente de celle des ions
Fe
2+
, comme on le verra au cours de la dsintercalation du lithium au paragraphe suivant. Cet
clatement de 1 eV du pic Fe 2p
3/2
serait plutt expliqu par leffet multiplet [19]. Daprs ces
analyses, on peut penser que les ions Fe
3+
observs par spectroscopie Mssbauer seraient
associs un effet de cur plutt qu un effet de surface, cependant la faible quantit dions
Fe
3+
ne permet pas de conclure rellement. La comparaison des pics relatifs au fer entre les
spectres de la poudre du matriau initial et de llectrode de mme matriau ne montre aucune
diffrence.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
118
Figure V-8 : Comparaison des spectres XPS des pics de cur de a) Fe 2p, b) P 2p, c) O 1s et d) C 1s
obtenus pour le matriau initial (Fe
575-fast
) sous la forme dune poudre et dune lectrode enduite.
Cast
electrode
Cast
electrode
Cast
electrode
Powder
pristine
material
(Fe
575-fast
)
Powder
pristine
material
(Fe
575-fast
)
735 730 725 720 715 710
Binding energy (eV)
2p
3/2
2p
1/2
Fe 2p
138 137 136 135 134 133 132 131 130
Binding energy (eV)
2p
3/2
2p
1/2
P 2p
536 534 532 530 528
Binding energy (eV)
O 1s
294 292 290 288 286 284 282
PVdF
Binding energy (eV)
carbon
black
PVdF
C 1s
Cast
electrode
Powder
pristine
material
(Fe
575-fast
)
Powder
pristine
material
(Fe
575-fast
)
a) b)
c) d)
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
119
102 100 98 96 94 92 90
Fe 3s
Powder
pristine
material
(Fe
575-fast
)
Cast
electrode
Binding energy (eV)
E ~ 5.7 eV
Figure V-9 : Spectres XPS Fe 3s enregistrs pour le matriau initial (Fe
575-fast
) et pour une lectrode
enduite partir de celui-ci.
De la mme manire, les spectres P 2p des deux matriaux initiaux sont prsents la
Figure V-8b. On constate que le spectre nest pas modifi par la prparation de llectrode. Le
pic P 2p est galement scind en deux composantes 2p
3/2
et 2p
1/2
, cause du couplage spin
orbite, respectivement 133.4 et 134.3 eV. Lobservation dun doublet unique cette nergie
de liaison est due au fait quil ny a quun seul environnement pour le phosphore, les
groupements phosphates (PO
4
)
3-
. De plus, la prsence de phosphures (Fe
2
P ou Fe
3
P) comme
cela a t suggr dans dautres tudes [20,21] peut ici tre exclue car leur pic caractristique
P 2p une nergie de liaison de 129.5 eV nest pas observ [22,23].
La Figure V-8c montre les pics de coeur O 1s pour le matriau initial (Fe
575-fast
) et
llectrode enduite ralise partir de celui-ci. Les deux spectres prsentent un pic
relativement fin 531.4 eV attribuable aux atomes doxygne prsents dans le groupement
phosphate (PO
4
)
3-
. Le spectre du matriau initial prsente galement un pic 533.2 eV qui
peut tre d une contamination de surface par des espces adsorbes, alors que celui de
llectrode frachement enduite montre dautres contaminations de surface rsultant de
llaboration de llectrode.
Les pics de cur du carbone C 1s sont donns la Figure V-8d. Le spectre du
matriau initial Fe
575-fast
prsente un pic asymtrique 284.6 eV qui est d au revtement de
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
120
carbone de C-LiFePO
4
obtenu par la dcomposition de la cellulose 575C lors de la synthse.
Cette forme particulire est caractristique dun carbone graphitique, la largeur mi-hauteur
observe (1.2 eV) pour ce pic est cependant bien plus leve que celle du graphite (0.6 eV), en
bon accord avec la nature amorphe et dsorganis du carbone de surface (cf. paragraphe IV-7
du Chapitre IV). La quantification XPS montre la surface des particules la prsence de 43 %
de carbone contre 57 % de LiFePO
4
, alors que dans le cur du matriau ce pourcentage de
carbone nest que de 4.6 % daprs les dosages chimiques. Ce rsultat confirme donc la
prsence dun revtement de carbone la surface des particules. Le spectre C 1s de llectrode
enduite partir de Fe
575-fast
est compltement modifi par rapport la description prcdente
cause de lutilisation dadditifs lors de llaboration de llectrode. En effet, on observe deux
nouveaux pics 291.9 et 286.4 eV, qui peuvent tre attribus au liant utilis : PVdF
(CH
2
-CF
2
)
n
. Le pic principal 284.3 eV, associ au noir de carbone, dissimule totalement le
pic relatif au revtement de carbone de C-LiFePO
4
.
A-V-3-2 Etude des matriaux C-Li
x
FePO
4
De la mme manire que pour les tudes menes par diffraction des rayons X et
spectroscopie Mssbauer, une tude XPS a t ralise diffrents tats de charge et de
dcharge. Aprs cyclage en batteries au lithium LiFe
575-fast
rgime C/20 dans la gamme de
potentiel [2 - 4.5] V (vs. Li
+
/Li), les lectrodes sont laves au DMC et analyses. La
Figure V-10 montre lvolution des pics XPS Fe 2p et Fe 3p tout au long du cyclage.
Les deux composantes Fe 2p
3/2
et 2p
1/2
prsentent les mmes volutions. En effet
pendant la charge, le spectre Fe 2p
3/2
prsente une dcroissance continue du pic principal
caractristique de Fe
2+
710 eV, et en parallle une augmentation dintensit dun nouveau pic
711 - 712 eV, qui est caractristique de Fe
3+
. Ce mcanisme est, comme attendu, en bon
accord avec la disparition progressive de la phase riche en lithium Li
1-
FePO
4
paralllement
lapparition de la phase
pauvre en lithium Li
FePO
4
. La nouvelle composante caractristique
de Fe
3+
prsente aussi un profil complexe, par consquent il nest pas possible de quantifier le
rapport Fe
3+
/Fe
2+
pendant la charge. Cependant, les quantits de Fe
3+
et Fe
2+
semblent
quivalentes aprs une demi-charge. Il est noter quun petit paulement de Fe
2+
est toujours
prsent sur le spectre XPS Fe 2p
3/2
la fin de la charge. Ce pic provient en partie dun
processus de rduction provoqu dans la chambre danalyse par lexprience XPS elle-mme
et son intensit augmente avec le temps. Cependant, on peut affirmer que le Fe
3+
est prsent
majoritairement la surface du matriau dlectrode la fin de la charge.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
121
1 cycle + 1 charge
Li
FePO
4
1 charge + discharge
Li
~0.5
FePO
4
1 charge Li
FePO
4
1 cycle Li
1-
FePO
4
charge Li
~0.5
FePO
4
Cast electrode Fe
575-fast
2
n
d
c
h
a
r
g
e
1
s
t
c
h
a
r
g
e
1
s
t
d
i
s
c
h
a
r
g
e
1 cycle + 1 charge
Li
FePO
4
1 charge + discharge
Li
~0.5
FePO
4
1 charge Li
FePO
4
1 cycle Li
1-
FePO
4
charge Li
~0.5
FePO
4
Cast electrode Fe
575-fast
735 730 725 720 715 710
Binding energy (eV)
Fe 2p
Fe
3+
Fe
3+
Fe
2+
Fe
2+
a)
b)
66 64 62 60 58 56 54 52
Binding energy (eV)
Fe 3p
(+ Li 1s)
Fe
3+
Fe
2+
2
n
d
c
h
a
r
g
e
1
s
t
c
h
a
r
g
e
1
s
t
d
i
s
c
h
a
r
g
e
Figure V-10 : Spectres XPS Fe 2p et Fe 3p obtenus pour des lectrodes enduites de composition
Li
x
FePO
4
, rcupres diffrents tats de charge ou de dcharge de batteries au lithium LiFe
575-fast
cycles rgime C/20 dans le domaine de potentiel [2 4.5] V (vs. Li
+
/Li).
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
122
Pendant la dcharge suivante, le processus oppos est observ avec la dcroissance
progressive du pic de Fe
3+
et la croissance progressive du pic de Fe
2+
. Le spectre obtenu aprs
une charge et une demi-dcharge est trs proche de celui obtenu aprs une demi-charge. De la
mme faon, le spectre obtenu aprs un cycle est trs proche de celui de llectrode initiale.
Les spectres obtenus aprs une charge et aprs un cycle complet et une charge sont galement
trs similaires. Pour ces deux spectres on observe galement un petit paulement d la
prsence dune petite quantit de Fe
2+
. Cette tude montre donc la bonne rversibilit du
processus redox Fe
3+
/Fe
2+
au cours des cycles de charge et de dcharge.
Le spectre Fe 3p montre la mme volution (cf. Figure V-10b), le pic observ 55 eV
caractristique de Fe
2+
est progressivement remplac au cours de la charge par un pic observ
57 eV caractristique de Fe
3+
. Le processus inverse est observ au cours de la dcharge. De
la mme manire, on peut remarquer le petit paulement d la prsence dions Fe
2+
la fin
de la charge qui sexpliquerait au moins en partie par la rduction dynamique se produisant
dans la chambre danalyse XPS, cependant la fin de la charge les ions Fe
3+
sont largement
majoritaires. Comme cela a dj t mentionn, le pic de cur de Li 1s est totalement cach
par le pic Fe 3p mais ne gne pas lanalyse de ce dernier grce des facteurs de sensibilit trs
diffrents.
En rsum, on peut dire que les analyses des pics de cur Fe 2p et 3p permettent de
conforter les analyses ralises par spectroscopie Mssbauer. Les caractrisations XPS
permettent une analyse de la surface des matriaux alors que la spectroscopie Mssbauer
permet une analyse du cur. Ces deux techniques ne semblent, nanmoins, pas montrer de
diffrences entre surface et cur des particules pendant le mcanisme redox se produisant lors
de la dsintercalation / intercalation du lithium de LiFePO
4
.
Cette analyse XPS est concordante avec lhypothse de lexistence dun mlange de
cristallites de composition Li
1-
FePO
4
et Li
FePO
4
dont les proportions varient selon ltat de
charge ou de dcharge, en bon accord avec le mcanisme suggr par ltude par diffraction
des rayons X. En effet, le mcanisme cur corce lors de la dsintercalation / intercalation
du lithium, impliquerait, par exemple durant la charge, la prsence en surface dune corce de
FePO
4
trs majoritaire par rapport la phase LiFePO
4
. Cela se traduirait sur les spectres
XPS par la prdominance des pics relatifs aux ions Fe
3+
, ce qui nest pas le cas sur les
spectres prsents qui montrent une volution parallle des intensits des pics de Fe
3+
/Fe
2+
.
De la mme manire, le processus dcrit par Laffont et al. implique la prsence en surface de
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
123
la phase LiFePO
4
donc cela devrait se traduire sur nos spectres XPS par la prdominance des
pics relatifs Fe
2+
.
Des rsultats semblables ont t obtenus pour Fe
800-fast
. Pour tous les matriaux tudis
la spectroscopie XPS confirme loxydation du Fe
2+
en Fe
3+
au cours de la charge et bien
videmment la rduction du fer au cours de la dcharge.
A-V-3-3 Etude de linterface lectrode / lectrolyte par XPS
Des analyses XPS ont galement t ralises pour observer les changements pouvant
se produire linterface lectrode / lectrolyte : la profondeur danalyse de la spectroscopie
XPS est en effet de ~ 5 nm. Les matriaux tudis prsentent une taille nanomtrique, ils
peuvent donc tre sujets une ractivit spcifique vis--vis de llectrolyte (dissolution, ),
mais galement catalyser une dgradation de llectrolyte leur surface.
Ltude de linterface lectrode / lectrolyte est possible par XPS en tudiant les
spectres O 1s et P 2p. Ces spectres sont donns la Figure V-11 et la Figure V-12 pour des
lectrodes rcupres partir de batteries au lithium LiFe
575-fast
au cours des deux premiers
cycles lectrochimiques.
Pendant le processus lectrochimique, le maximum du pic O 1s est toujours observ
la mme nergie de liaison, soit 531.4 eV. Cependant, ce spectre montre une accentuation de
sa composante haute nergie de liaison ( 533 eV) au cours de la charge et une dcroissance
au cours de la dcharge. Ce phnomne est reproductible au cours de la seconde charge. Il est
accompagn par une augmentation du taux doxygne global au cours de la charge et par une
diminution au cours de la dcharge. Lvolution du rapport quantitatif Fe 2p/O 1s montre que
cette composante 533 eV ne peut pas tre attribue au matriau actif (cf. paragraphe
A-V-3-1) et donc quelle ne peut pas tre lie lapparition de la phase dficiente en lithium
Li
FePO
4
. En effet, la proportion doxygne qui ne peut tre attribue au matriau actif est de
30 % pour llectrode initiale, puis atteint 58 % aprs une demi-charge, 77 % aprs une charge,
59 % aprs une charge et une demi-dcharge, 50 % aprs un cycle et 77 % aprs un cycle et
une charge. Cette tude montre donc lapparition au cours du cyclage de nouvelles espces
oxygnes linterface lectrode / lectrolyte provenant de la dgradation de llectrolyte. Ces
espces peuvent tre organiques ou inorganiques comme cela a pu tre observ la surface
dlectrodes de graphite [24]. Cependant, lidentification des espces organiques est difficile
car le pic de coeur C 1s du matriau est largement domin par les pics relatifs au liant (PVdF)
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
124
et au noir de carbone. Tous les spectres des matriaux tudis prsentent cet inconvnient,
cest pour cette raison que ces spectres ne sont pas prsents dans ce manuscrit.
1 cycle
(Li
1-
FePO
4
)
1 cycle + 1 charge
(Li
FePO
4
)
1 charge + discharge
(Li
~0.5
FePO
4
)
1 charge
(Li
FePO
4
)
charge
(Li
~0.5
FePO
4
)
Cast electrode Fe
575-fast
2
n
d
c
h
a
r
g
e
1
s
t
c
h
a
r
g
e
1
s
t
d
i
s
c
h
a
r
g
e
536 534 532 530 528
Binding energy (eV)
O 1s
Figure V-11 : Spectres XPS O 1s pour les lectrodes enduites de composition Li
x
FePO
4
rcupres
diffrents tats de charge et de dcharge de cellules LiFe
575-fast
cycles rgime C/20 dans la fentre de
potentiel [2 4.5] V (vs. Li
+
/Li).
Comme le montre la Figure V-12, les pics de cur P 2p prsentent de faibles
modifications au cours du cyclage. On peut observer un changement de la forme du spectre
avec un largissement progressif au cours de la charge, qui est rversible au cours de la
dcharge. Ce phnomne est reproductible au cours de la seconde charge. Le rapport
Fe 2p/P 2p montre une nouvelle fois que cette volution ne peut tre impute lapparition de
la phase pauvre en lithium Li
FePO
4
. La proportion de phosphore qui ne peut pas tre
attribue au matriau actif est de 20 % aprs une demi-charge, 41 % aprs une charge, 42 %
aprs une charge et une demi-dcharge, 48 % aprs un cycle et 48 % aprs un cycle et une
charge. En consquence le changement de forme du spectre P 2p est principalement d au
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
125
dpt de phosphate la surface de llectrode qui peut provenir de la dgradation du sel LiPF
6
prsent dans llectrolyte. Plusieurs mcanismes ont t proposs pour expliquer la formation
de ces espces phosphates [25], particulirement la raction du sel LiPF
6
avec des traces
deau pouvant tre prsentes dans llectrolyte. Cette raction implique par consquent la
formation du fluorure de lithium LiF, que lon peut voir la Figure V-13 sur le spectre F 1s
des chantillons. LiF reprsente 2 5 % des espces prsentes la surface des particules.
1 cycle
(Li
1-
FePO
4
)
1 cycle + 1 charge
(Li
FePO
4
)
1 charge + discharge
(Li
~0.5
FePO
4
)
1 charge
(Li
FePO
4
)
charge
(Li
~0.5
FePO
4
)
Cast electrode Fe
575-fast
2
n
d
c
h
a
r
g
e
1
s
t
c
h
a
r
g
e
1
s
t
d
i
s
c
h
a
r
g
e
138 136 134 132 130
Binding energy (eV)
P 2p
Figure V-12 : Spectres XPS P 2p pour les lectrodes enduites de composition Li
x
FePO
4
rcupres
diffrents tats de charge et de dcharge de cellules LiFe
575-fast
cycles rgime C/20 dans la fentre de
potentiel [2 4.5] V (vs. Li
+
/Li).
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
126
1 cycle
(Li
1-
FePO
4
)
1 cycle + 1 charge
(Li
FePO
4
)
1 charge + discharge
(Li
~0.5
FePO
4
)
1 charge
(Li
FePO
4
)
charge
(Li
~0.5
FePO
4
)
Cast electrode Fe
575-fast
2
n
d
c
h
a
r
g
e
1
s
t
c
h
a
r
g
e
1
s
t
d
i
s
c
h
a
r
g
e
692 690 688 686 684 682
Binding energy (eV)
F 1s
PVdF
LiF
Figure V-13 : Spectres XPS F 1s pour les lectrodes enduites de composition Li
x
FePO
4
rcupres
diffrents tats de charge et de dcharge de cellules LiFe
575-fast
cycles rgime C/20 dans la fentre de
potentiel [2 4.5] V (vs. Li
+
/Li).
Lvolution des spectres P 2p et O 1s nest pas analogue au cours du processus
lectrochimique ; en effet des espces phosphates sont formes pendant la premire charge et
conserves au cours de la dcharge alors que les espces oxygnes sont partiellement formes
puis dissoutes, ce qui signifie que la forme particulire du spectre O 1s au cours de la charge
ne peut tre explique que par le dpt la surface de llectrode despces organiques issues
de la dgradation des solvants de llectrolyte. Les rsultats obtenus dans ce travail sont assez
diffrents de ceux obtenus par Herstedt et al. [26] pour la caractrisation de linterface forme
la surface dun matriau LiFePO
4
avec un revtement de carbone aprs cyclage
lectrochimique. Cependant leurs conditions exprimentales et llectrolyte utilis (LiPF
6
dans
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
127
EC/DEC (2 : 1)) sont trs diffrents des ntres. Ces auteurs nobservent pas de produits de
dgradation des solvants de llectrolyte mais plutt une interface compose majoritairement
de produits de dgradation des sels de llectrolyte, suffisamment paisse pour empcher
lobservation des pics relatifs au fer par XPS, ce qui nest pas le cas dans cette tude.
On peut rsumer cette partie de ltude en considrant la prsence dune trs fine
couche la surface des lectrodes de C-LiFePO
4
qui est constitue de LiF et despces
phosphates provenant de la dgradation du sel prsent dans llectrolyte et/ou despces
organiques non identifies provenant srement de la dgradation des solvants de llectrolyte.
On peut galement noter que des rsultats semblables ont t obtenus pour Fe
800-fast
.
Malgr une plus faible surface spcifique par rapport Fe
575-fast
, la quantit de produits de
dgradation prsents la surface des lectrodes Fe
800-fast
est similaire. Cependant en dpit de
la taille nanomtrique de ces matriaux, le phnomne de ractivit de llectrode vis--vis de
llectrolyte nimplique pas la formation dune couche paisse qui gnerait le bon
fonctionnement lectrochimique du matriau actif.
A-V-4 Etude par MET - HR de matriaux C-Li
x
FePO
4
rcuprs
diffrents tats de charge des cellules LiFe
800-fast
Pour tudier lvolution de la microstructure au sein des cristallites de LiFePO
4
lors du
processus de dsintercalation / intercalation du lithium, une tude par Microscopie
Electronique Transmission Haute Rsolution a t ralise. Des matriaux Li
x
FePO
4
ont
t synthtiss par dsintercalation lectrochimique du lithium. Quel que soit le type
dlectrode utilis (lectrode enduite ou lectrode poudre), des rsultats identiques ont t
obtenus lors de ltude mene par MET-HR. Dans cette partie, nous avons donc choisi de ne
prsenter que les rsultats obtenus pour le matriau Li
~0.55
FePO
4
synthtis
lectrochimiquement rgime C/20 partir dune lectrode enduite du compos Fe
800-fast
. La
composition en lithium de ce matriau a t estime partir dune analyse quantitative
rsultant de laffinement des donnes de diffraction des rayons X par la mthode de Rietveld.
Morgan et al., ainsi que plus rcemment Islam et al. [6,7], ont montr par des calculs
thoriques ab initio que la diffusion du lithium se ferait prfrentiellement et rapidement selon
la direction b, alors que la propagation du front de phase se ferait selon laxe a. Ces rsultats
ont t confirms exprimentalement par les tudes de MET-HR ralises par les quipes de
Richardson [4] et de Masquelier [5]. Conformment ces rsultats thoriques et
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
128
exprimentaux, dans un premier temps les cristallites ont t orientes de telle sorte observer
la direction a. Dans un second temps, des images ont t ralises diffrents grossissements
pour avoir une vue densemble et juger ainsi de lhomognit de la cristallite.
Un chantillon dimages reprsentatives est donn la Figure V-14 et la
Figure V-15. Les cristallites observes ont des diamtres compris entre 100 et 150 nm,
en bon accord avec la taille des domaines de cohrence dtermine par diffraction des rayons
X (cf. paragraphe IV-2-1 du Chapitre IV). Sur ces images de MET-HR, on voit clairement les
plans atomiques. De plus, on constate une grande rgularit de ces plans dans toutes les
cristallites, ce qui signifie quil ny a pas de zones dsordonnes contrairement ce quont pu
observer Chen et al. [4]. De mme, il ny a pas de zones amorphes ou dsordonnes en bordure
de cristallite, en effet les plans atomiques sont nettement visibles jusquaux bords des
cristallites. Daprs la relation L g d
hkl hkl
= o est la longueur donde des lectrons
incidents et L la longueur de camra, le rapport de deux distances
2
1
hkl
hkl
g
g
du rseau rciproque
entre deux spots conscutifs des directions principales du clich de diffraction lectronique ou
de la transforme de Fourier est gal au rapport R des distances cristallographiques
correspondantes dans le rseau direct
1
2
hkl
hkl
d
d
. La comparaison des rapports
2
1
hkl
hkl
g
g
exprimentaux
avec les rapports thoriques des distances cristallographiques
1
2
hkl
hkl
d
d
des phases Li
1-
FePO
4
et
Li
FePO
4
nous a donc permis dassocier les clichs de diffraction ou les transformes de
Fourier lune ou lautre de ces deux phases. Quelques uns des rapports de distances, les plus
caractristiques des deux phases Li
1-
FePO
4
et Li
FePO
4
, sont donns dans le Tableau V-5.
Par ailleurs, chaque image enregistre a t traite en dtail, cest--dire que chaque zone de
limage et donc de la cristallite a fait lobjet dune transforme de Fourier, ce qui a permis de
sassurer de lhomognit des particules.
La Figure V-14 montre la micrographie haute rsolution dune cristallite de
lchantillon Li
~0.55
FePO
4
. Les deux agrandissements donns prsentent sa traverse de part en
part selon deux zones perpendiculaires. A partir du clich de diffraction lectronique associ
cette image (cf. Figure V-14), on peut calculer le rapport (R =
100
011
g
g
) des distances entre deux
spots conscutifs des directions principales, qui est gale 2.8. Des transformes de Fourier
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
129
ont t ralises sur des dtails des zones reprsentes la Figure V-14, les rapports de
distances sont homognes et restent proches de 2.8. Ce rapport est trs proche de 2.79, valeur
du rapport
011
100
d
d
pour la phase Li
1-
FePO
4
calcul partir des donnes cristallographiques
obtenues au paragraphe IV-3-1 du Chapitre IV par laffinement des donnes de diffraction des
rayons X, cette cristallite est compose uniquement de la phase Li
1-
FePO
4
. En effet, aucun
autre rapport de distances interrticulaires perpendiculaires entre elles et correspondant aux
conditions dexistence dfinies par le groupe despace Pnma nest proche de cette valeur de R,
que ce soit pour cette phase Li
1-
FePO
4
ou pour la phase Li
FePO
4
.
De la mme manire, le clich de diffraction associ limage de la cristallite donne
la Figure V-15 a permis de calculer, une valeur de R gale 2.1. Ce rapport ne peut tre reli
quau rapport des distances cristallographiques
001
100
d
d
de la phase Li
FePO
4
dont la valeur
thorique est de 2.05. En effet, ce sont les seules directions cristallographiques des phases
Li
1-
FePO
4
et Li
FePO
4
, perpendiculaires, qui donnent un rapport proche de 2.05. De la mme
faon, on peut calculer le rapport R pour les micrographies obtenues sur diffrentes zones de la
cristallite et on obtient systmatiquement une valeur proche de 2.05, ce qui confirme
lhomognit de cette cristallite, et donc la prsence dune phase unique Li
FePO
4
au sein de
cette cristallite.
Ces rsultats c'est--dire la prsence dune seule phase Li
1-
FePO
4
ou Li
'
FePO
4
au
sein des cristallites et labsence de zones dsordonnes sont gnralisables aux nombreuses
cristallites de composition Li
1-
FePO
4
ou Li
'
FePO
4
observes pour ce matriau mais
galement toutes les autres compositions tudies.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
130
8 . 2
100
011
=
g
g
a*
[011]*
8 . 2
100
011
=
g
g
a*
[011]*
Figure V-14 : Micrographie haute rsolution dune cristallite de Li
1-
FePO
4
du matriau Fe
800-fast
avec en
insert le clich de diffraction associ. Un agrandissement de deux zones traversant la cristallite de part en part
est galement donn.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
131
1 . 2
100
001
=
g
g
a*
c*
1 . 2
100
001
=
g
g
a*
c*
Figure V-15 : Micrographie haute rsolution dune cristallite de Li
'
FePO
4
du matriau Fe
800-fast
avec en insert
le clich de diffraction associ. Un agrandissement de deux zones traversant la cristallite de part en part est
galement donn.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
132
Tableau V-5 : Rapports des distances cristallographiques thoriques des phases Li
1-
FePO
4
et Li
'
FePO
4
.
Li
1-
FePO
4
Li
'
FePO
4
010
100
d
d
1.72 1.69
001
100
d
d
2.20 2.05
011
100
d
d
2.79 2.66
020
100
d
d
3.43 3.38
Cette homognit des particules montre que le modle cur - corce [1,2] ne permet
pas de dcrire le mcanisme de dsintercalation / intercalation du lithium dans les matriaux
tudis dans ce manuscrit, qui sont synthtiss de manire rapide et qui prsentent donc des
tailles de cristallites trs petites (~ 100 nm de diamtre). Selon ce mcanisme cur - corce
pendant la charge (respectivement, dcharge) lcorce constitue de Li
FePO
4
(respectivement, Li
1-
FePO
4
) crot au dtriment du cur constitu de Li
1-
FePO
4
(respectivement, Li
FePO
4
), ce qui implique donc au sein dune cristallite la coexistence des
deux phases et donc des rapports de distances R diffrents selon la zone de la cristallite
analyse. Dautre part, des analyses MET-HR ont t ralises par Chen et al. [4] et Laffont et
al. [5] sur des cristallites en forme de plaquettes (axe b normal la surface), de diamtres
respectifs ~ 3 m et ~ 140 nm, pour lesquelles la composition Li
x
FePO
4
a t obtenue
chimiquement. Ils ont montr la formation, au sein de chaque cristallite, de domaines spars
de Li
1-
FePO
4
et de Li
FePO
4
, de taille de lordre de 100 nm pour Chen et al. et de 70 nm pour
Laffont et al.. Lattribution de chaque domaine une phase a t ralise, comme lors de cette
tude, par mesure des distances interrticulaires sur les clichs de diffraction ou les
transformes de Fourier. Les domaines associs ces deux phases sont spars par un
domaine, qui selon les auteurs, est dsordonn avec une taille de lordre de 50 nm [4] ou
ordonn et cristallis caractris par un mlange des paramtres des deux phases [5]. Au final
pour Laffont et al., quel que soit ltat de charge ou de dcharge, les cristallites sont
constitues dun coeur de Li
FePO
4
et dune corce de Li
1-
FePO
4
[5].
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
133
Comme nous venons de le voir, tout comme le mcanisme cur - corce, les
mcanismes dcrits plus rcemment par Laffont et al. et Chen et al. [4,5] impliquent la
coexistence des deux phases (Li
FePO
4
et Li
1-
FePO
4
) au sein dune mme cristallite. Dans le
cas de notre tude, le mcanisme de dsintercalation / intercalation du lithium apparat
diffrent. En effet les images MET-HR ne montrent quune seule phase (Li
FePO
4
ou
Li
1-
FePO
4
) au sein des cristallites, confirmant ainsi que le passage de la phase Li
1-
FePO
4
la phase Li
FePO
4
se produit de manire trs rapide dans une cristallite sans quil y ait
coexistence durable des deux phases. Cette tude MET-HR confirme ce qui a dj t voqu
lors de paragraphes prcdents : lors de la charge (respectivement dcharge), ds que la
dsintercalation (respectivement intercalation) du lithium est initie un point de la
cristallite, le phnomne se propage rapidement dans tout le reste de la cristallite pour viter
une forte augmentation des contraintes que provoquerait la coexistence des deux phases
Li
FePO
4
ou Li
1-
FePO
4
, qui prsentent chacune des octadres FeO
6
trs distordus (comme
cela a t discut au paragraphe A-V-1-2-b de ce chapitre). Cette minimisation des
contraintes est aussi mise en avant par Laffont et al. qui supposent que la nuclation de
Li
FePO
4
au cur de la particule, avec des domaines assez larges (~ 70 nm) compars aux
zones de transition, permet daccommoder les contraintes [5]. On peut donc conclure que quel
que soit ltat de charge ou de dcharge, les diffrents chantillons Li
x
FePO
4
tudis
(lectrodes enduites ou poudre, diffrentes valeurs de x), obtenus par voie lectrochimique
partir dun matriau synthtis de manire rapide, sont composs de cristallites homognes de
Li
1-
FePO
4
et de Li
FePO
4
, dont la proportion varie selon la composition.
Il faut souligner quun travail rcent de Wagemaker et al. [27] tudie mthodiquement
linfluence de la taille des particules de TiO
2
sur ltendue du domaine de solution-solide lors
de lintercalation du lithium mais aussi sur la possibilit pour deux phases de coexister au sein
de la mme particule. En effet, plus les particules sont petites plus il est difficile deux phases
de coexister au sein de ces particules, tout spcialement lorsquil existe une forte diffrence de
volume entre les deux structures : lexistence dun front de phase dstabilise en effet fortement
le systme biphas.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
134
PARTIE B : ETUDE DE CYCLAGES LONGUE DUREE A TEMPERATURE AMBIANTE,
40C ET 60C
B-V-1 Cyclages longue dure de cellules Li C-LiFePO
4
(Fe
800-fast
)
diffrentes tempratures
Comme cela a t dcrit au Chapitre IV, diffrentes conditions de synthse de
matriaux C-LiFePO
4
ont t testes puis les matriaux ainsi obtenus ont t caractriss
structuralement et physico-chimiquement sans toutefois prsenter de diffrences significatives,
si ce nest de petites diffrences du point de vue microstructural (taille des particules et des
agglomrats ainsi que nature du revtement de carbone). Cependant, les matriaux obtenus
prsentent des proprits lectrochimiques diffrentes, ce qui suggre que cette microstructure
joue un rle important pour le contrle des proprits lectrochimiques.
Le matriau C-LiFePO
4
synthtis grce un traitement thermique 800C de courte
dure Fe
800-fast
montre de bonnes performances lectrochimiques pendant le cyclage
galvanostatique temprature ambiante (~ 160 mAh/g C/20). Cette partie traite donc plus en
dtail des performances lectrochimiques de ce matriau lors de cyclages longue dure,
temprature ambiante, 40C et 60C, puis des caractrisations structurales effectues sur les
lectrodes rcupres aprs cyclage seront prsentes [28]. Cette tude est apparue dautant plus
importante que ces matriaux C-LiFePO
4
sont des nanomatriaux qui pourraient donc prsenter
une ractivit de surface accrue notamment lors de cyclages en temprature.
B-V-1-1 Cyclages longue dure temprature ambiante (RT)
Les cyclages longue dure ont t raliss diffrentes tempratures : temprature
ambiante (RT), 40C et 60C dans la gamme de potentiel [2 - 4.5] V vs. Li
+
/Li, pour tudier le
comportement lectrochimique mais galement la stabilit structurale du matriau C-LiFePO
4
Fe
800-fast
. La Figure V-16a montre une comparaison des courbes de charge et de dcharge
obtenues temprature ambiante pour les 1
er
, 20
me
, 70
me
et 100
me
cycles. Pour une
comparaison plus aise, les courbes de charge et de dcharge donnes la Figure V-16 ont t
dcales les unes des autres de 0.1 V. Pour permettre dapprcier les capacits rversibles et les
diffrences de potentiel entre les courbes de charge et de dcharge, la Figure V-17 prsente les
1
er
, 20
me
et 100
me
cycles complets temprature ambiante et 40C mais galement les 1
er
,
15
me
et 40
me
cycles complets 60C.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
135
La Figure V-18 montre lvolution de la capacit rversible pour des cellules
lectrochimiques Li C-LiFePO
4
(Fe
800-fast
) charges 4.5 V vs. Li
+
/Li et dcharges jusqu
2 V vs. Li
+
/Li temprature ambiante, 40C et 60C. A temprature ambiante, la capacit
rversible moyenne reste constante au cours des 100 cycles avec une valeur de capacit
rversible de ~ 160 mAh/g, proche de la valeur thorique de ~ 170 mAh/g. On peut galement
noter quil ny a pas dvolution de la forme des courbes de charge ou de dcharge au cours
des 100 cycles, ce qui est en adquation avec la bonne rtention de capacit observe.
Cependant, le premier cycle est lgrement diffrent des cycles suivants. En effet, une
polarisation plus importante est observe en fin de premire charge et en fin de premire
dcharge, ce qui peut tre d une limitation de la dsintercalation / intercalation du lithium
du fait de faibles conductivits ionique et lectronique du matriau.
Au cours des cyclages longue dure raliss temprature ambiante pour Fe
800-fast
la
diffrence de potentiel observe sur le plateau entre les courbes de charge et de dcharge reste
faible et constante (~ 0.10 V), la capacit irrversible la fin du premier cycle lectrochimique
est galement relativement faible et de lordre de ~ 9 mAh/g (soit x ~ 0.05) (cf. Figure V-17).
Fe
800-fast
prsente donc, temprature ambiante, de bonnes performances lectrochimiques,
stables au cours des cyclages de longue dure. Ces rsultats sont en bon accord avec ceux
reports rcemment par Amine et al., c'est--dire une capacit rversible de 140 mAh/g
rgime C/3 pour une dure de 100 cycles. Ces rsultats ont t obtenus pour des matriaux
LiFePO
4
synthtiss par une raction ltat solide avec un revtement de carbone de lordre de
3.5 % en masse [29].
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
136
a)
b)
c)
0.0 0.2 0.4 0.6 0.8 1.0
2.0
2.5
3.0
3.5
4.0
4.5
100
th
discharge
70
th
discharge
20
th
discharge
1
st
discharge
P
o
t
e
n
t
i
a
l
v
s
L
i
+
/
L
i
(
V
)
x in Li
x
FePO
4
0.0 0.2 0.4 0.6 0.8 1.0
2.0
2.5
3.0
3.5
4.0
4.5
100
th
charge
70
th
charge
20
th
charge
1
st
charge
P
o
t
e
n
t
i
a
l
v
s
L
i
+
/
L
i
(
V
)
x in Li
x
FePO
4
0.0 0.2 0.4 0.6 0.8 1.0
2.0
2.5
3.0
3.5
4.0
4.5
100
th
discharge
70
th
discharge
20
th
discharge
1
st
discharge
P
o
t
e
n
t
i
a
l
v
s
L
i
+
/
L
i
(
V
)
x in Li
x
FePO
4
0.0 0.2 0.4 0.6 0.8 1.0
2.0
2.5
3.0
3.5
4.0
4.5
100
th
charge
70
th
charge
20
th
charge
1
st
charge
P
o
t
e
n
t
i
a
l
v
s
L
i
+
/
L
i
(
V
)
x in Li
x
FePO
4
RT RT
40C 40C
60C 60C
0.0 0.2 0.4 0.6 0.8 1.0
2.0
2.5
3.0
3.5
4.0
4.5
40
th
discharge
30
th
discharge
15
th
discharge
1
st
discharge
P
o
t
e
n
t
i
a
l
v
s
L
i
+
/
L
i
(
V
)
x in Li
x
FePO
4
0.0 0.2 0.4 0.6 0.8 1.0
2.0
2.5
3.0
3.5
4.0
4.5
40
th
charge
30
th
charge
15
th
charge
1
st
charge
P
o
t
e
n
t
i
a
l
v
s
L
i
+
/
L
i
(
V
)
x in Li
x
FePO
4
Figure V-16 : Courbes de cyclage obtenues pour la cellule lectrochimique Li C-LiFePO
4
(Fe
800-fast
)
dans le domaine de potentiel [2 - 4.5] V vs. Li
+
/Li rgime C/20 et a) temprature ambiante (RT), b)
40C et c) 60C. Comparaison des courbes de charge et de dcharge obtenues temprature ambiante et
40C pour les 1
er
, 20
me
, 70
me
et 100
me
cycles et 60C pour les 1
er
, 15
me
, 30
me
et 40
me
cycles. Chaque
courbe de charge / dcharge est dcale de 0.1 V par rapport la courbe prcdente pour une
comparaison plus aise, cependant les courbes de premire charge ou dcharge ne sont pas dcales.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
137
0.0 0.2 0.4 0.6 0.8 1.0
2.0
2.5
3.0
3.5
4.0
4.5
0.0 0.2 0.4 0.6 0.8 1.0
2.0
2.5
3.0
3.5
4.0
4.5
0.0 0.2 0.4 0.6 0.8 1.0
2.0
2.5
3.0
3.5
4.0
4.5
1
st
cycle
P
o
t
e
n
t
i
a
l
v
s
L
i
+
/
L
i
(
V
)
x in Li
x
FePO
4
20
th
cycle
100
th
cycle
0.0 0.2 0.4 0.6 0.8 1.0
2.0
2.5
3.0
3.5
4.0
4.5
0.0 0.2 0.4 0.6 0.8 1.0
2.0
2.5
3.0
3.5
4.0
4.5
0.0 0.2 0.4 0.6 0.8 1.0
2.0
2.5
3.0
3.5
4.0
4.5
1
st
cycle
P
o
t
e
n
t
i
a
l
v
s
L
i
+
/
L
i
(
V
)
x in Li
x
FePO
4
20
th
cycle
100
th
cycle
0.0 0.2 0.4 0.6 0.8 1.0
2.0
2.5
3.0
3.5
4.0
4.5
0.0 0.2 0.4 0.6 0.8 1.0
2.0
2.5
3.0
3.5
4.0
4.5
0.0 0.2 0.4 0.6 0.8 1.0
2.0
2.5
3.0
3.5
4.0
4.5
1
st
cycle
P
o
t
e
n
t
i
a
l
v
s
L
i
+
/
L
i
x in Li
x
FePO
4
15
th
cycle
40
th
cycle
RT
40C
60C
a)
b)
c)
Figure V-17 : Comparaison des courbes de cyclage obtenues pour la cellule lectrochimique
Li C-LiFePO
4
(Fe
800-fast
) dans le domaine de potentiel [2 - 4.5] V vs. Li
+
/Li rgime C/20 et a)
temprature ambiante (RT), b) 40C et c) 60C, permettant de visualiser la capacit irrversible et la
diffrence de potentiel entre la courbe de charge et de dcharge (prsentation des 1
er
, 20
me
et 100
me
cycles
RT et 40C et prsentation des 1
er
, 15
me
et 40
me
cycles 60C).
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
138
0 20 40 60 80 100
0
20
40
60
80
100
120
140
160
60C
40C
RT
C
a
p
a
c
i
t
y
(
m
A
h
/
g
)
Number of cycles
Figure V-18 : Evolution de la capacit rversible en fonction du nombre de cycles pour la cellule
lectrochimique Li C-LiFePO
4
(Fe
800-fast
) cycle dans le domaine de potentiel [2 - 4.5] V vs. Li
+
/Li
rgime C/20 et temprature ambiante, 40C et 60C.
B-V-1-2 Cyclages longue dure 40C
Les courbes de charge et de dcharge obtenues 40C pour une cellule lectrochimique
Li C-LiFePO
4
(Fe
800-fast
) cycle rgime C/20 dans le domaine de potentiel [2 - 4.5] V vs.
Li
+
/Li sont donnes la Figure V-16b. Lvolution de la capacit rversible obtenue en
fonction du nombre de cycles est donne la Figure V-18. Une bonne rtention de capacit est
observe jusqu 50 cycles avec une capacit rversible de lordre de 155 mAh/g, cette valeur
est proche de celle obtenue lors du cyclage ralis temprature ambiante en tenant compte de
lerreur sur la pese. Les proprits de transport tant sensibles la temprature, llvation de
la temprature favorise laugmentation des conductivits ionique et lectronique ; il en rsulte
que la capacit irrversible ainsi que la diffrence de potentiel observe sur le plateau entre la
charge et la dcharge sont lgrement infrieures celles dtermines pour un cyclage ralis
temprature ambiante (cf. Figure V-18). Elles sont respectivement gales ~ 7 mAh/g
(x ~ 0.04) et ~ 0.08 mV. En tenant compte du fait que les piles bouton utilises pour ces
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
139
cyclages 40C sont ralises au laboratoire - c'est--dire dans des conditions non optimises -
les rsultats obtenus pour les cellules lectrochimiques Li C-LiFePO
4
avec Fe
800-fast
comme
lectrode positive sont prometteurs. En effet, on note une bonne stabilit en cyclage et une
conservation de plus de 80 % de la capacit rversible initiale aprs 100 cycles. Sur les courbes
de cyclage obtenues 40C, on peut noter que la forme de la courbe en fin de premire charge
et de premire dcharge est modifie de manire significative avec une augmentation de la
temprature.
B-V-1-3 Cyclages longue dure 60C
Sur la Figure V-16c sont reprsents les rsultats obtenus pour une tude similaire aux
prcdentes mais ralise 60C. La tendance observe 40C est accentue. En effet, la perte
de capacit rversible est plus rapide avec 40 % de perte de capacit rversible aprs seulement
40 cycles. Les caractristiques lectrochimiques c'est--dire une capacit rversible de
~ 150 mAh/g et une diffrence de potentiel sur le plateau entre la charge et la dcharge de
~ 0.06 mV observes en dbut de cyclage lectrochimique sont similaires celles obtenues
temprature ambiante et 40C. La capacit irrversible est significativement suprieure
(~ 25.5 mAh/g avec x ~ 0.15) (cf. Figure V-17). Cela peut tre d lapparition dun nouveau
plateau au-dessus de 4 V vs. Li
+
/Li, trs bien mis en vidence par la comparaison des courbes
de premire charge. Nanmoins, la forme de la premire dcharge nest pas affecte, on observe
seulement une lgre dcroissance de la capacit rversible ainsi quune augmentation de la
capacit irrversible ; cela signifie que sur le plateau 4 4.5 V vs. Li
+
/Li le mcanisme de
dsintercalation du lithium est toujours en cours mais quil est concurrenc par une raction
secondaire qui, elle, est irrversible. Ce phnomne peut sexpliquer en supposant quune
raction lectrochimique irrversible oxydation de llectrolyte et/ou dgradation du matriau
dont la cintique augmente fortement avec la temprature, se produit la surface des
particules. En effet, cette raction, qui devient majoritaire au-del de la valeur de potentiel
critique de 4.13 V, augmente continuellement avec la temprature comme on peut le voir sur la
Figure V-16. Des tests potentiostatiques raliss avec llectrolyte utilis seul LiPF
6
(1 M)
dans un mlange de carbonates de propylne (PC), dthylne (EC) et de dimthyle (DMC)
(1 : 1 : 3) temprature ambiante et une vitesse de balayage lente (pas de 10 mV par heure)
montrent une augmentation du courant doxydation et donc la dgradation de llectrolyte
partir de 4.1 V vs. Li
+
/Li. On peut donc supposer que la raction lectrochimique se produisant
potentiel lev est due la dgradation de llectrolyte ; cette raction est fortement catalyse
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
140
par laugmentation de la temprature de cyclage en prsence de C-LiFePO
4
trs divis. La chute
de capacit rversible peut expliquer la grande capacit irrversible observe pour la cellule
lectrochimique Li Fe
800-fast
cycle 60C, probablement due en partie la raction
doxydation irrversible de llectrolyte. De plus, la polarisation observe la fin de la premire
charge aurait d diminuer avec laugmentation de la temprature de cyclage si elle tait
uniquement attribuable une mauvaise conductivit lectronique et ionique ; le phnomne
inverse est observ, ce qui confirme quun facteur supplmentaire, tel que la dgradation de
llectrolyte, est prendre en compte pour expliquer, du moins partiellement, cette
augmentation de polarisation.
La ralisation dune nouvelle pile bouton - en changeant llectrolyte, les sparateurs
et llectrode ngative de lithium - avec la mme lectrode positive c'est--dire celle rcupre
de la cellule lectrochimique dont les rsultats sont prsents la Figure V-16c, permet
dobtenir une capacit rversible de ~ 150 mAh/g lors du premier cycle. Ce rsultat montre que
la perte de capacit rversible observe durant le cyclage lectrochimique 60C, est
probablement due un problme de mouillage de llectrode qui est corrler avec la
dgradation de llectrolyte plutt qu la formation la surface de llectrode dune couche
trs paisse de produits de dgradation, qui aurait pour consquence daugmenter la rsistance
de la cellule (cf. paragraphe A-V-3-3 de ce chapitre).
Morgan et al. ont rcemment montrs par des calculs ab initio que la diffusion du
lithium se ferait selon une direction prfrentielle qui est laxe b dans la structure olivine
(dcrite dans le groupe despace Pnma) et que la diffusion des ions dans Li
'
FePO
4
serait plus
aise dun ordre de grandeur par rapport Li
1-
FePO
4
( et 0) [6]. Ce rsultat implique
donc une diffrence significative des proprits de transport durant la charge et la dcharge en
bon accord avec ltude mene par Srinivasan et al. [10,11] qui ont montr un comportement
asymtrique entre la charge et la dcharge, impliquant une plus grande efficacit en charge
quen dcharge. Ce phnomne peut dailleurs expliquer limportante polarisation obtenue en
fin de premire dcharge lors du cyclage temprature ambiante (Figure V-16a) mais qui
dcrot avec laugmentation de la temprature Figure V-16b c.
Ce matriau Fe
800-fast
prsente une bonne tenue en cyclage quelle que soit la
temprature, il faut cependant noter une dgradation plus rapide 60C des performances
lectrochimiques. Des rsultats similaires en terme de comportement ont t obtenus pour
Fe
575-fast
.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
141
B-V-2 Etude par diffraction des rayons X des matriaux rcuprs aprs des
cyclages longue dure
Les matriaux rcuprs aprs ces cyclages longue dure temprature ambiante, 40C
et 60C, ont t tudis dun point de vue structural par diffraction des rayons X. Ils seront
nomms respectivement Fe
800
-RT-100cycles, Fe
800
-40C-100cycles et Fe
800
-60C-40cycles par
la suite (par exemple, Fe
800
-RT-100cycles reprsente le matriau cycl temprature ambiante
pendant 100 cycles). La Figure V-19 compare leurs diagrammes de diffraction des rayons X
avec ceux du matriau initial Fe
800-fast
et avec ceux des matriaux Fe
800-fast
rcuprs aprs une
demi-charge (Fe
800
-RT-1/2charge), aprs une premire charge (Fe
800
-RT-1charge), aprs une
premire charge et une demi-dcharge (Fe
800
-RT-1/2discharge) et aprs un cycle
(Fe
800
-RT-1cycle). Tous ces matriaux ont t rcuprs aprs un cyclage rgime C/20 dans la
gamme de potentiel [2 4.5] V vs. Li
+
/Li et temprature ambiante.
Les diagrammes de diffraction des rayons X enregistrs pour les matriaux
Fe
800
-RT-1/2charge et Fe
800
-RT-1/2discharge sont comme attendu caractristiques dun
mlange biphas (Li
1-
FePO
4
- Li
FePO
4
). Les diagrammes de DRX enregistrs la fin de la
premire charge et de la premire dcharge sont quant eux caractristiques dune phase
unique, en bon accord avec une composition en lithium proche de x = 0 et de x = 1 dans
Li
x
FePO
4
et appartenant aux domaines de solution-solide observs la toute fin du processus
de charge et de dcharge [3]. Fe
800
-RT-100cycles rcupr aprs un cyclage lectrochimique
longue dure temprature ambiante prsente un diagramme de diffraction des rayons X
caractristique dune phase unique, identifie comme tant la phase riche en lithium Li
1-
FePO
4
,
tandis que les deux matriaux Fe
800
-40C-100cycles et Fe
800
-60C-40cycles sont des mlanges
biphass, la phase majoritaire tant la phase riche en lithium Li
1-
FePO
4
( 0) et lautre phase
tant la phase pauvre en lithium Li
FePO
4
(' 0). Les pics de diffraction supplmentaires
observs dans le domaine angulaire [15 - 22] sur les diagrammes de diffraction des rayons X
des matriaux cycls 40C et 60C ont t identifis et associs au sparateur (Celgard
). En
effet, lors du dsassemblage de la cellule lectrochimique ayant cycl en temprature,
llectrode positive est systmatiquement rcupre colle au sparateur au lieu dtre toujours
solidaire de la feuille daluminium sur laquelle elle avait t enduite. Il y a une superposition de
ces pics avec les pics (200) des phases de type olivine. Dans la suite de ce paragraphe, le
domaine angulaire [15 - 22] est donc exclu des affinements par la mthode de Rietveld.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
142
Overlapping of peaks associated to the
olivine phases and to the batterys
separators (S)
S
S
Pristine material
Fe
800-fast
Sample-holder
(200) (210) (020)
Fe
800
-RT-1/2charge
Fe
800
-RT-1charge
Fe
800
-RT-1cycle
Fe
800
-RT-100cycles
Fe
800
-60C-40cycles
1
s
t
c
h
a
r
g
e
1
s
t
d
i
s
c
h
a
r
g
e
Fe
800
-RT-1/2discharge
Fe
800
-40C-100cycles
20 25 30 35 40 45 50
I
(
A
.
U
.
)
2
Co
()
Figure V-19 : Comparaison des diffractogrammes de rayons X enregistrs pour le matriau initial
Fe
800-fast
, pour les matriaux rcuprs aprs une charge rgime C/20 et temprature ambiante
(Fe
800
-RT-1/2charge), aprs une premire charge rgime C/20 et temprature ambiante
(Fe
800
-RT-1charge), aprs une premire charge et une premire dcharge rgime C/20 et
temprature ambiante (Fe
800
-RT-1/2discharge), la fin du premier cycle lectrochimique rgime C/20
et temprature ambiante (Fe
800
-RT-1cycle), aprs 100 cycles rgime C/20 et temprature ambiante
(Fe
800
-RT-100cycles), aprs 100 cycles rgime C/20 et 40C (Fe
800
-40C-100cycles) et aprs 40 cycles
rgime C/20 et 60C (Fe
800
-60C-40cycles).
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
143
B-V-2-1 Matriaux rcuprs aprs un cyclage temprature ambiante (RT)
Pour dterminer prcisment la structure de Fe
800
-RT-100cycles et identifier les
modifications structurales par rapport au matriau initial Fe
800-fast
, un affinement par la mthode
de Rietveld des donnes de diffraction de rayons X a t ralis laide du programme Fullprof
[13]. La premire tape consiste raliser un full pattern matching pour dterminer les
paramtres de maille la structure de lolivine est dcrite dans le groupe despace Pnma avec
les paramtres de maille suivants a ~ 10.3224(5) , b ~ 6.0025(3) et c ~ 4.6988(3) en
utilisant une fonction de type pseudo-Voigt pour dcrire la forme des pics de diffraction. Puis
laffinement par la mthode de Rietveld est ralis en considrant lhypothse structurale
[Li]
4a
[Fe]
4c
PO
4
. Le rapport Li/Fe tant trs proche de 1, il a t fix cette valeur. Les facteurs
de dplacement atomique isotrope (Biso()) ont galement t affins. Tous les rsultats
paramtres de profil et structuraux obtenus pour Fe
800
-RT-100cycles par laffinement des
donnes de diffraction des Rayons X par la mthode de Rietveld sont donns dans le Tableau
V-6, alors que la comparaison des diagrammes de diffraction des rayons X exprimental et
calcul est donne la Figure V-20. Les faibles valeurs obtenues pour les facteurs de reliabilit
(R
wp
= 12.8 % et R
B
= 5.57 %) ainsi que la bonne minimisation de la fonction diffrence
I
obs.
- I
calc.
suggrent une bonne description de la structure de Fe
800
-RT-100cycles par la
structure de la phase olivine riche en lithium. Les principaux paramtres obtenus pour les
matriaux Fe
800-fast
et Fe
800
-RT-1cycle sont donns pour comparaison dans le Tableau V-7. Les
paramtres de maille ainsi que le volume (V = 290.52(3)
3
) dtermins pour
Fe
800
-RT-100cycles sont lgrement infrieurs ceux dtermins pour le matriau initial
Fe
800-fast
(V = 291.38(1)
3
) et pour Fe
800
-RT-1cycle (V = 290.95(4)
3
) (cf. Tableau V-7).
Cette diminution de volume est associer une plus faible quantit de lithium prsente dans la
phase de la solution-solide : Li
1-
FePO
4
; ce rsultat est en bon accord avec ce qui est attendu
pour un matriau rcupr aprs un plus grand nombre de cycles lectrochimiques. La
comparaison des distances moyennes entre Fe
800
-RT-100cycles (P-O ~ 1.54 , Fe-O ~ 2.16 ,
Li-O ~ 2.15 ) et Fe
800-fast
(P-O ~ 1.54 , Fe-O ~ 2.17 , Li-O ~ 2.14 ) ne montre aucune
volution structurale significative.
On peut donc conclure que ltude structurale de Fe
800
-RT-100cycles na pas montr de
changement structural significatif de Fe
800-fast
aprs 100 cycles entre 2 et 4.5 V (vs. Li
+
/Li),
rgime C/20 et temprature ambiante.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
144
Tableau V-6 : Paramtres structuraux et de profil obtenus par laffinement par la mthode de Rietveld des
donnes de diffraction de rayons X enregistres pour Fe
800-fast
aprs 100 cycles rgime C/20 et
temprature ambiante (Fe
800
-RT-100cycles).
Fe
800
-RT-100cycles
Space group : Pnma
a = 10.3226(5)
b = 6.0028(3)
c
= 4.6888(3)
V = 290.52(3)
Site Wyckoff positions Occupancy B(
2
)
Li 4a 0 0 0 1 4(2)
Fe 4c 0.2823(6) 1/4 0.976(2) 1 4.6(3)
P 4c 0.095(1) 1/4 0.416(3) 1 3.4(3)
O
l
4c 0.097(3) 1/4 0.740(6) 1 4.4(9)
O
2
4c 0.460(3) 1/4 0.201(3) 1 2.9(7)
O
3
8d 0.165(2) 0.041(3) 0.289(3) 1 2.8(5)
Conditions of the run
Temperature
Angular range
Number of points
Displacement sample holder (2)
Number of fitted parameters
300 K
5 2 75
3584
-0.171(3)
24
Profile parameters :
Thompson-Cox-Hastings function
* LaB
6
used as standard
Y = 0.088(4)
U = 0.12(1)
V = -0.0017*
W = 0.00383*
Conventional Rietveld R-factors for points with Bragg contribution
R
wp
= 12.8 % ; R
B
= 5.57 %
Note : standard deviations have been multiplied by 3, the Scor parameter being 2.75.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
145
20 30 40 50 60 70
Yobs
Ycalc
Yobs-Ycalc
* Sampler holder
*
*
I
(
A
.
U
.
)
2
Co
()
25 30 35 40
I
(
A
.
U
.
)
2
Co
()
Figure V-20 : Comparaison des diagrammes de diffraction des rayons X exprimental et calcul obtenus
pour Fe
800-fast
aprs 100 cycles dune cellule lectrochimique Li C-LiFePO
4
(Fe
800-fast
) entre 2 et 4.5 V (vs.
Li
+
/Li) rgime C/20 et temprature ambiante (Fe
800
-RT-100cycles).
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
146
Tableau V-7 : Comparaison des paramtres de maille obtenus par laffinement par la mthode de Rietveld
des donnes de diffraction des rayons X enregistres pour le matriau initial Fe
800-fast
, pour les matriaux
rcuprs aprs une charge rgime C/20 et temprature ambiante (Fe
800
-RT-1/2charge), aprs une
premire charge rgime C/20 et temprature ambiante (Fe
800
-RT-1charge), aprs une premire charge
et une premire dcharge rgime C/20 et temprature ambiante (Fe
800
-RT-1/2discharge), la fin du
premier cycle lectrochimique rgime C/20 et temprature ambiante (Fe
800
-RT-1cycle), aprs 100 cycles
rgime C/20 et temprature ambiante (Fe
800
-RT-100cycles), aprs 100 cycles rgime C/20 et 40C
(Fe
800
-40C-100cycles) et enfin aprs 40 cycles rgime C/20 et 60C (Fe
800
-60C-40cycles).
B-V-2-2 Matriaux rcuprs aprs un cyclage 40C
La structure du matriau dlectrode rcupr aprs un cyclage longue dure 40C a
galement t caractrise par diffraction des rayons X. De la mme manire que
prcdemment, un affinement des donnes de diffraction des rayons X par la mthode de
Rietveld a t ralis pour Fe
800
-40C-100cycles, en considrant cette fois la prsence de deux
phases. Ces deux phases sont dcrites par une structure de type olivine et [Li
x
]
4a
[Fe]
4c
PO
4
est
choisi comme modle structural, avec x gal 1 ou 0 respectivement pour la phase riche en
lithium Li
1-
FePO
4
et pour la phase pauvre en lithium Li
'
FePO
4
, la Figure V-21 donne la
comparaison des diagrammes de DRX exprimental et calcul. Une bonne minimisation de la
fonction diffrence |I
obs.
- I
calc.
| est obtenue ainsi que de faibles valeurs pour les facteurs de
reliabilit R
wp
= 14.4 %, R
B(Li-rich)
= 5.84 % et R
B(Li-deficient)
= 11.8 %, ce qui prouve que la
description de ce mlange de phases avec deux phases de structure olivine est en bon accord
avec le diagramme de diffraction des rayons X de Fe
800
-40C-100cycles. Les paramtres de
maille dtermins pour ces deux phases sont en bon accord avec ceux dtermins pour
Fe
800
-RT-1/2discharge, qui est galement un matriau biphas obtenu aprs une charge et une
dcharge partielle (cf. Tableau V-7).
a () b () c () V (
3
)
10.3263(6) 6.0057(4) 4.6931(4) 291.05(4)
Fe
800
-60C-40cycles
9.821(2) 5.7917(9) 4.7852(8) 272.17(9)
10.3236(6) 6.0042(4) 4.6926(4) 290.87(3)
Fe
800
-40C-100cycles
9.822(8) 5.790(1) 4.782(2) 271.9(3)
Fe
800
-RT-100cycles 10.3224(5) 6.0025(3) 4.6888(3) 290.52(3)
Fe
800
-RT-1cycle 10.3239(6) 6.0050(4) 4.6932(4) 290.95(4)
10.314(1) 6.0011(8) 4.6941(7) 290.55(7)
Fe
800
-RT-1/2discharge
9.820(1) 5.7921(5) 4.7796(5) 271.87(5)
Fe
800
-RT-1charge 9.8207(8) 5.7913(4) 4.7798(5) 271.85(4)
10.3224(6) 6.0043(4) 4.6932(4) 290.88(4)
Fe
800
-RT-1/2charge
9.828(1) 5.7955(4) 4.7815(4) 272.32(4)
Fe
800-fast
(pristine material)
10.3294(3) 6.0086(2) 4.6948(1) 291.38(1)
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
147
De la mme manire, on peut donc dire que pour Fe
800
-40C-100cycles, il ny a pas de
modifications structurales significatives par rapport au matriau initial Fe
800-fast
.
20 30 40 50 60 70
S
S
Li-deficient phase
Li-rich phase
Yobs
Ycalc
Yobs-Ycalc
S Battery's separators
I
(
A
.
U
.
)
2
Co
()
25 30 35 40
Li-deficient phase
Li-rich phase
I
(
A
.
U
.
)
2
Co
()
Figure V-21 : Comparaison des diagrammes de diffraction des rayons X exprimental et calcul obtenus
pour Fe
800-fast
aprs 100 cycles dune cellule lectrochimique Li C-LiFePO
4
(Fe
800-fast
) entre 2 et 4.5 V (vs.
Li
+
/Li) rgime C/20 et 40C (Fe
800
-40C-100cycles).
B-V-2-3 Matriaux rcuprs aprs un cyclage 60C
La mme procdure daffinement des donnes de diffraction des rayons X que pour
Fe
800
-40C-100cycles mlange de deux phases a t utilise pour Fe
800
-60C-40cycles. La
Figure V-22 montre la bonne minimisation de la fonction diffrence |I
obs.
I
calc.
| obtenue par la
comparaison des diagrammes de diffraction des rayons X exprimental et calcul. Les facteurs
de reliabilit calculs sont faibles R
wp
= 13.1 %, R
B(Li-rich)
= 4.27 % et R
B(Li-deficient)
= 9.86 %. La
comparaison des paramtres structuraux obtenus pour Fe
800
-60C-40cycles (cf. Tableau V-7)
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
148
montre quil ny a pas de changements structuraux significatifs lors de cyclages
lectrochimiques temprature leve (60C).
20 30 40 50 60 70
S
S
Li-deficient phase
Li-rich phase
Yobs
Ycalc
Yobs-Ycalc
S Battery's separators
I
(
A
.
U
.
)
2
Co
()
25 30 35 40
Li-deficient phase
Li-rich phase
I
(
A
.
U
.
)
2
Co
()
Figure V-22: Comparaison des diagrammes de diffraction des rayons X exprimental et calcul obtenus
pour Fe
800-fast
aprs 40 cycles dune cellule lectrochimique Li C-LiFePO
4
(Fe
800-fast
) entre 2 et 4.5 V (vs.
Li
+
/Li) rgime C/20 et 60C (Fe
800
-60C-40cycles).
Cependant, bien quaucun changement structural significatif nait t dtermin que ce
soit temprature ambiante ou temprature plus leve, nous ne pouvons pas exclure au cours
de cyclages longue dure la possible dissolution du fer pour les matriaux CLiFePO
4
. En effet
selon Amine et al., la prsence de fer dans llectrolyte aprs cyclage serait due la dissolution
du fer provenant de llectrode positive [29]. Cependant, Koltypin et al. ont propos que la
dissolution du fer serait seulement possible en prsence deau ou despces acides dans
llectrolyte due la formation de HF [30]. Les rsultats rcemment reports par Axmann et al.
suggrent que la dissolution du fer serait probablement associe la prsence dimpurets dans
le matriau. En effet, ils ont montr que la prsence de Fe
2
P comme impuret dans LiFePO
4
provoque une augmentation de la concentration en fer dans llectrolyte aprs un stockage de
deux semaines 60C. Cette dernire tude montre galement quen dpit de ce problme de
dissolution du fer, le matriau LiFePO
4
montre - lorsquil est stock deux semaines 60C dans
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
149
llectrolyte - une excellente stabilit en comparaison de celle observe pour dautres matriaux
dlectrode positive commerciaux tels que LiNi
1/3
Co
1/3
Al
1/3
O
2
, LiMn
2
O
4
[31].
Il est noter quune dissolution non ngligeable du fer dans llectrolyte provoquerait
une perte de capacit. En effet, ces ions fer mme ltat de traces seraient rduits sur
llectrode ngative et empcheraient ainsi la bonne rversibilit du mcanisme redox cause
dun empoisonnement de llectrode ngative et dune perte de masse de matriau
lectrochimiquement actif. De plus, la dissolution du fer est active par laugmentation de la
temprature. Les conditions de cyclage utilises en comparaison de celles utilises par Amine
et al. [29], cest dire un rgime de cyclage plus lent (C/20 au lieu de C/3), une temprature de
cyclage plus leve (60C au lieu de 55C) mais galement un potentiel plus lev (4.5 V au
lieu de 4.0 V (vs. Li
+
/Li)) auraient donc d accentuer les ractions de dissolution du fer. A la
fin du cyclage lectrochimique, des analyses qualitatives par spectroscopie de fluorescence X
ont t ralises sur diffrentes lectrodes ngatives issues de cyclage 60C (cf. Figure V-23)
et il a t possible didentifier les pics K
1
et K
1
du fer sur les spectres de fluorescence X.
Cependant des analyses quantitatives sont ncessaires pour corrler la prsence de
fer dans llectrolyte et la possible perte de capacit des matriaux C-LiFePO
4
lors de cyclages
longue dure et spcialement tempratures leves. Pour cela, des analyses sur les lectrodes
ngatives de plus grande taille sont envisages pour dterminer ainsi la quantit et lorigine de
ce fer : provientil de LiFePO
4
lui-mme ou alors dune impuret ?
15 5 10
Energy (keV)
C
p
s
(
A
.
U
.
)
Fe
Figure V-23 : Comparaison des spectres de fluorescence X obtenus pour une lectrode de lithium nayant
pas subi de cyclage lectrochimique (courbe rouge) et pour une lectrode ngative rcupre (lithium)
dune cellule lectrochimique Li C-LiFePO
4
(Fe
800-fast
) aprs un cyclage 60C (courbe bleue).
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
150
PARTIE C : CONCLUSIONS
La combinaison des analyses par diffraction des rayons X et par spectroscopie
Mssbauer et XPS pour caractriser les matriaux dsintercals Li
x
FePO
4
, issus des
matriaux C-LiFePO
4
synthtiss de manire rapide aprs mcano-activation des prcurseurs,
montre comme attendu un mcanisme biphas pour la dsintercalation / intercalation du
lithium avec deux domaines de solution-solide en tout dbut et fin de charge et de dcharge en
bon accord avec ce qui a t publi par Yamada et al. [3]. La combinaison des techniques
spectroscopiques, cest dire du Mssbauer et de lXPS, a montr une homognit des
chantillons au cur et en surface.
Cette tude combinant la diffraction des rayons X, la spectroscopie XPS et la
microscopie lectronique transmission haute rsolution a galement permis de mettre en
vidence que pour ce type de matriaux LiFePO
4
, le mcanisme de dsintercalation
(intercalation) du lithium nest pas conforme ceux dj dcrits dans la littrature. En effet,
quels que soient la direction cristallographique ou ltat de charge (ou de dcharge), il ny a
pas dvolutions des contraintes et des tailles de domaines de cohrence (du moins sans
volution continue) pour chacune des phases Li
1-
FePO
4
et Li
FePO
4
au cours du cyclage
lectrochimique. Ceci suggre que le mcanisme cur-corce ou celui dcrit plus rcemment
par Chen et al. [4] et Laffont et al. [5] ne permettent pas de dcrire le mcanisme de
dsintercalation / intercalation du lithium dans nos matriaux C-LiFePO
4
. En effet, les
rsultats obtenus dans cette tude impliquent que le mcanisme biphas de dsintercalation
(intercalation) du lithium se droule, cristallite par cristallite, de manire trs rapide. Quand le
processus de dlithiation est initi un point de la cristallite, le mcanisme se propage
immdiatement au reste de la cristallite pour minimiser les contraintes au sein du matriau et
stabiliser le systme.
Ce mcanisme a t confirm par une tude MET-HR, qui a montr sur diffrentes
cristallites de diffrents chantillons, que les matriaux Li
x
FePO
4
tudis prsentent, sans
ambigut, des cristallites homognes de bout en bout de composition LiFePO
4
ou FePO
4
.
La seconde partie de ce chapitre a port sur ltude des performances lectrochimiques
et de la stabilit structurale au cours de cyclages longue dure rgime C/20 du matriau
C-LiFePO
4
(Fe
800-fast
), que ce soit temprature ambiante ou temprature plus leve (40C
ou 60C). Les cellules Li C-LiFePO
4
(Fe
800-fast
) cycles temprature ambiante et 40C
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
151
prsentent de bonnes performances lectrochimiques, alors qu 60C la perte de capacit
rversible est rapide.
Bien que les analyses XPS aient permis de mettre en vidence la formation dune
couche linterface lectrode / lectrolyte au cours du cyclage lectrochimique, aucune
influence majeure de celle-ci na t constate lors des cyclages longue dure. Cette couche est
constitue de LiF, despces phosphates et organiques. LiF et les espces phosphates rsultent
de la dgradation du sel LiPF
6
prsent dans llectrolyte tandis que les espces organiques sont
associes la dgradation des solvants de ce mme lectrolyte. Les matriaux rcuprs aprs
des cyclages longue dure ont t caractriss structuralement par laffinement par la mthode
de Rietveld des donnes de diffraction des rayons X. Quelle que soit la temprature de cyclage
(RT, 40C ou 60C), aucune volution structurale nest observe.
Des analyses quantitatives sur de plus grandes quantits de matire, donc sur des
lectrodes de plus grande taille, seraient ncessaires pour clairement relier (quantit et origine
matriau LiFePO
4
lui-mme ou ions Fe
3+
prsents dans le matriau initial encore non identifis)
la prsence de fer llectrode ngative et la perte de capacit des composites C-LiFePO
4
au
cours de cyclages longue dure, spcialement tempratures leves.
Dans ce chapitre, seuls les rsultats de cyclage longue dure et de caractrisation
structurale obtenus pour Fe
800-fast
ont t reports en dtail mais il est noter que les rsultats
obtenus pour Fe
575-fast
sont similaires. En effet, on observe une bonne cyclabilit temprature
ambiante et 40C. Dautre part comme pour Fe
800-fast
et de manire plus accentue, une moins
bonne tenue en cyclage est observe 60C. La caractrisation structurale de ces lectrodes
rcupres aprs des cyclages longue dure na pas montr dvolution significative par rapport
au matriau initial.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
152
Bibliographie du Chapitre V
1
A. K. Padhi, K. S. Nanjundaswamy, J. B. Goodenough, Journal of the Electrochemical
Society, 144 (1997), 1188.
2
A. S. Andersson, J. O. Thomas, Journal Of Power Sources, 97-8 Special Iss. SI (2001),
498-502.
3
A. Yamada, H. Koizumi, N. Sonoyama, R. Kanno, Electrochemical And Solid State
Letters, 8 (8) (2005), A409-A413.
4
G. Y. Chen, X. Y. Song, T. J. Richardson, Electrochemical And Solid State Letters, 9
(6) (2006), A295-A298.
5
L. Laffont, C. Delacourt, P. Gibot, M. Y. Wu, P. Kooyman, C. Masquelier, J. M.
Tarascon, Chemistry Of Materials, 18 (2006), 5520-5529.
6
D. Morgan, A. Van der Ven, G. Ceder, Electrochemical And Solid State Letters, 7 (2)
(2004), A30-A32.
7
M. S. Islam, D. J. Driscoll, C. A. J. Fisher, P. R. Slater, Chemistry Of Materials, 17
(2005), 5085-5092.
8
A. S. Andersson, B. Kalska, L. Haggstrom, J. O. Thomas, Solid State Ionics, 130
(2000), 41-52.
9
F. Tournadre, L. Croguennec, P. Willmann, C. Delmas, Journal of Solid State
Chemistry, 177 (2004), 2803-2809.
10
V. Srinivasan, J. Newman, Journal Of The Electrochemical Society, 151 (10) (2004),
A1517-A1529.
11
V. Srinivasan, J. Newman, Electrochemical And Solid State Letters, 9 (3) (2006),
A110-A114.
12
Y. K. Lin, C. H. Lu, H. C. Wu, M. H. Yang, Journal Of Power Sources, 146 (1-2)
Special Iss. SI (2005), 594-597.
13
J. Rodriguez-Carvajal, Laboratoire Lon Brillouin, http://www-
llb.cea.fr/fullweb/powder.htm, (2004).
14
R. D. Shannon, C. T. Prewitt, Acta Crystallographica, B25 (1969), 925.
15
B. Ellis, L. K. Perry, D. H. Ryan, L. F. Nazar, Journal Of The American Chemical
Society, 128 (2006), 11416-11422.
16
S. Okada, T. Yamamoto, Y. Okazaki, J. Yamaki, M. Tokunaga, T. Nishida, Journal Of
Power Sources, 146 (1-2) Special Iss. SI (2005), 570-574.
17
C. Gleitzer, European Journal of Solid State Inorganic Chemistry, 28 (1991), 77-91.
18
C. Delacourt, PhD thesis (2005), University Picardie - Jules Verne.
19
S. Hfner, Photoelectron spectroscopy: principles and applications (Springer-Verlag,
1995).
20
A. Ait Salah, A. Mauger, C. M. Julien, F. Gendron, Materials Science And Engineering
B Solid State Materials For Advanced Technology, 129 (2006), 232-244.
21
P. S. Herle, B. Ellis, N. Coombs, L. F. Nazar, Nature Materials, 3 (2004), 147-152.
22
C. D. Wagner, A. V. Naumkin, A. Kraut-Vass, J. W. Allison, C. J. Powell, J. R. J.
Rumble, NIST Standard Reference Database 20, Version 3.4 (Web Version), (2006).
23
C. E. Myers, H. F. Franzen, J. W. Anderegg, Inorganic Chemistry, 24 (1985), 1822-
1824.
24
D. Aurbach, Journal of Power Sources, 89 (2000), 206-218.
25
J. Vetter, P. Novak, M. R. Wagner, C. Veit, K. C. Moller, J. O. Besenhard, M. Winter,
M. Wohlfahrt Mehrens, C. Vogler, A. Hammouche, Journal of Power Sources, 147
(2005), 269-281.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre V
Magali Maccario 30 novembre 2007
153
26
M. Herstedt, M. Stjerndahl, A. Nyten, T. Gustafsson, H. Rensmo, H. Siegbahn, N.
Ravet, M. Armand, J. O. Thomas, K. Edstrom, Electrochemical And Solid State
Letters, 6 (2003), A202-A206.
27
M. Wagemaker, W. J. H. Borghols, F. M. Mulder, Journal of the American Chemical
Society, 129 (2007), 4323-4327.
28
M. Maccario, L. Croguennec, F. Le Cras, C. Delmas, Journal Of Power Sources,
Accepted (2007).
29
K. Amine, J. Liu, I. Belharouak, Electrochemistry Communications, 7 (2005), 669-673.
30
M. Koltypin, D. Aurbach, L. Nazar, B. Ellis, in IMLB, Biarritz, 2006), p. 174.
31
P. Axmann, C. Stinner, G. Arnold, S. Strbele, M. Kinyanjui, M. Wohlfahrt-Mehrens,
in IMLB, Biarritz, 2006), p. 177.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre VI
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre VI
M. Maccario 30 novembre 2007
155
Chapitre VI
Description du mcanisme domino-cascade de
dsintercalation / intercalation du lithium dans LiFePO
4
Ce chapitre revient, de manire plus fondamentale, sur le mcanisme de
dsintercalation / intercalation du lithium dans LiFePO
4
, rsultat majeur de ce travail. En
effet, le chapitre prcdent prsente une tude diffrents tats de charge et de dcharge des
matriaux Li
x
FePO
4
par diffraction des rayons X, spectroscopies Mssbauer et XPS. La
combinaison de ces diffrentes techniques a montr, comme attendu, que le mcanisme de
dsintercalation / intercalation du lithium est principalement biphas. De petits domaines de
solution-solide sont en effet observs au dbut et en fin de charge et de dcharge. Ce rsultat
restait controvers mais nos rsultats confortent ceux reports par Yamada et al. [1],
rcemment confirms par Meethong et al. [2]. Dautre part, labsence dvolution continue
des contraintes et des tailles des domaines de cohrence obtenues par lanalyse des donnes
de DRX au cours du cyclage lectrochimique nous a conduit envisager un autre mcanisme
de dsintercalation / intercalation du lithium dans LiFePO
4
. En effet, le mcanisme cur-
corce implique la croissance dune des deux phases au dtriment de la seconde, donc la
diminution de la taille des domaines de cohrence de cette dernire par rapport ceux de la
premire ; alors que le mcanisme dcrit plus rcemment par Chen et al. [3] et Laffont et al.
[4] implique lvolution continue avec x des FWHM dpendant de lindice h cause de la
croissance (ou dcroissance) des domaines des deux phases dans le plan ac, ainsi en fin de
raction (charge ou dcharge) Laffont et al. dcrivent des particules prsentant
systmatiquement un cur de FePO
4
enrob dune corce de LiFePO
4
.
Pour expliquer le mcanisme de dsintercalation / intercalation du lithium dans
LiFePO
4
, il faut considrer attentivement la structure du matriau. Elle est constitue, comme
on la vu au Chapitre I de damiers doctadres FeO
6
dans le plan bc. Pour former le rseau
3D, ces damiers sont connects entre eux via les ttradres PO
4
. En gnral, dans les
phosphates, du fait de la forte covalence des liaisons P-O, les distances P-O et O-O des
ttradres PO
4
sont fixes et invariantes. Cependant dans la structure olivine, le partage dune
arte entre chaque octadre FeO
6
et ttradre PO
4
, en plus de leurs connections via des
sommets induit de fortes distorsions lchelle locale qui se rpartissent dune manire
cooprative dans toute la structure 3D.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre VI
M. Maccario 30 novembre 2007
156
Lors de la dsintercalation du lithium, les ions fer divalents sont oxyds ltat
trivalent avec une forte variation des longueurs de liaisons Fe-O et O-O dans les octadres
FeO
6
, qui a pour consquence une dformation cooprative de la structure. La variation des
distances entre les octadres FeO
6
des phases LiFePO
4
et FePO
4
est trs importante, comme
on la vu au paragraphe A-V-1-2b du Chapitre V. Cette diffrence implique quil est trs
difficile dintroduire une quantit importante de Fe
3+
dans LiFePO
4
et rciproquement une
grande quantit de Fe
2+
dans FePO
4
. Par consquent, il nexiste pas de solution-solide sur la
majeure partie du domaine de composition en lithium mais plutt un domaine biphas entre
les deux compositions extrmes Li
1-
FePO
4
( 0) et Li
FePO
4
( 0), avec des petits
domaines de solution-solide aux extrmits.
Ltendue des domaines de solution-solide tant trs petite, la concentration en
porteurs de charges est trs faible. De plus, quand un ion Fe
3+
est localis dans le rseau de
LiFePO
4
(ou rciproquement un ion Fe
2+
dans FePO
4
), il y a formation dun petit polaron,
dont la mobilit intrinsque est, selon Ceder et al., assez leve [5]. Cependant, selon ces
mmes auteurs il y a un fort couplage de ce petit polaron avec la lacune de lithium,
lnergie dactivation ncessaire pour le transfert du petit polaron devient alors
significativement plus leve (500 meV contre 215 meV). La combinaison des deux
phnomnes, petite concentration en porteurs de charges et fort couplage petit polaron / ion
lithium, explique donc la trs faible conductivit lectronique de LiFePO
4
. Si lon considre
maintenant la diffusion des ions lithium, toutes les expriences et simulations faites sur les
matriaux de type LiFePO
4
ont montr que la diffusion des ions lithium dans ce matriau est
trs anisotrope [6-8]. En particulier, Ceder et al. et Islam et al. ont montr que la conductivit
ionique est leve selon laxe b (tunnels de la structure) et ngligeable dans les deux autres
directions [6,7].
Pendant le processus lectrochimique de dsintercalation / intercalation du lithium de
nos petites particules de LiFePO
4
, nous avons observ exprimentalement que les cristallites
sont de composition Li
1-
FePO
4
ou Li
FePO
4
dans tout leur volume, en bon accord avec les
valeurs constantes des tailles de domaine de cohrence dtermines par DRX et avec
lanalyse des images haute rsolution de microscopie lectronique transmission. Pour
comprendre le mcanisme de croissance dune des phases au dtriment de la seconde pendant
le processus de dsintercalation / intercalation du lithium dans LiFePO
4
, il faut considrer
simultanment, le couplage des ions (lacunes) et des lectrons (trous) lchelle
microscopique et leffet de fortes distorsions locales.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre VI
M. Maccario 30 novembre 2007
157
Si on considre une chane doctadres LiO
6
parallle laxe b de laquelle les ions
lithium commencent tre dsintercals, les lectrons sont extraits des ions Fe
2+
voisins pour
former les ions Fe
3+
. Localement, dans les couches doctadres FeO
6
lis par les sommets (cf.
Figure VI-1), les petits polarons peuvent se dplacer dun octadre FeO
6
loctadre FeO
6
voisin, qui est lui aussi proche de la lacune de lithium. Les canaux o se trouvent les ions
lithium sont donc ainsi entirement vids de proche en proche en bon accord avec la direction
privilgie de diffusion des ions lithium, soit laxe b. Dans ce cas, lnergie dactivation reste
trs faible car la lacune na pas se dplacer [5]. Ensuite, la dsintercalation des ions lithium
se poursuit dans les tunnels voisins adjacents de cette couche doctadres FeO
6
, puisque la
conductivit lectronique rsultant dun hopping Fe
3+
/Fe
2+
facilite cette dsintercalation. Au
contraire, comme les octadres FeO
6
ne sont pas directement connects dans la direction a, le
transfert lectronique est trs faible dans cette direction. Cette mobilit deux dimensions des
petits polarons, c'est--dire dans le plan bc, a rcemment t discute par Nazar et al. lors de
tude du systme Li
x
FePO
4
temprature leve [9]. Ces rsultats peuvent tre extrapols
temprature ambiante dans le domaine situ la jonction entre le domaine riche en lithium
LiFePO
4
et le domaine pauvre en lithium Li
FePO
4
qui peut tre considr comme une
solution-solide trs localise dans la cristallite. Quand le lithium commence tre
dsintercal dun tunnel parallle la direction b, la conductivit lectronique, qui apparat
localement dans une couche doctadres FeO
6
, facilite la dsintercalation du lithium dans un
tunnel voisin et adjacent cette couche. Le mcanisme de dsintercalation se produit ainsi
trs rapidement dans ce bloc, ce qui favorise la formation dune couche tendue de FePO
4
dans la cristallite, sil ny a pas de dfauts qui gnent la migration des ions lithium et des
lectrons. Cela permet dexpliquer pourquoi la zone intermdiaire a t observe dans le plan
bc par Richardson et coll. [3].
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre VI
M. Maccario 30 novembre 2007
158
Figure VI-1 : Cration dune lacune de lithium avec formation dun ion Fe
3+
dans son environnement.
Le saut du petit polaron (trou) jusqu un site de fer galement proche de la lacune de lithium est trs
facile. La prsence dun ion Fe
3+
dans un autre site permet daider la diffusion des ions lithium dans le
tunnel de la lacune mais aussi dans les tunnels voisins et de faciliter ainsi la dsintercalation du lithium.
A cause de la diffrence significative de longueurs de liaisons et dangles entre la
phase LiFePO
4
largement majoritaire au sein de la cristallite et la couche tendue de FePO
4
forme dans le plan bc, de fortes distorsions apparaissent localement ce qui dstabilise les
couches adjacentes selon la direction a. Il est donc plus facile de dsintercaler les ions lithium
des couches adjacentes plutt que de crer un point de dsintercalation un autre endroit du
cristal. La nuclation dun nouveau micro-domaine de FePO
4
dans une autre partie du cristal
de LiFePO
4
ncessiterait une forte nergie dactivation alors que la dsintercalation
proximit de la frontire entre les deux phases, o les porteurs de charges (ions / lacunes et
lectrons / trous) sont concentrs, consiste seulement au dplacement de cette frontire sans
augmentation de lnergie dactivation. Plus le nombre de zones intermdiaires
LiFePO
4
/ FePO
4
est important plus lnergie dactivation et la polarisation de la cellule
Fe
3+
Lithium vacancy Fe
3+
Lithium vacancy Fe
3+
Lithium vacancy Fe
3+
Lithium vacancy Fe
3+
Lithium vacancy Fe
3+
Lithium vacancy
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre VI
M. Maccario 30 novembre 2007
159
lectrochimique augmentent pendant le mcanisme lectrochimique de
dsintercalation / intercalation du lithium.
La zone intermdiaire distordue entre le domaine intercal et le domaine
dsintercal implique lapparition de contraintes lintrieur du matriau qui facilitent la
dsintercalation du lithium au voisinage de cette zone frontire. Cette zone de contraintes est
reprsente la Figure VI-2. Dans ce modle, quand un plan bc de transition est form, il se
dplace travers tout le cristal selon a. Ce dplacement peut tre considr comme un front
de phase infiniment rapide se dplaant travers tout le cristal sans barrire nergtique ce
qui permet au mcanisme de dsintercalation / intercalation du lithium dtre trs rapide. La
Figure VI-3 et la Figure VI-4 donnent la reprsentation schmatique de ce mcanisme
domino-cascade travers une cristallite. Ce modle est en bon accord avec ltude EELS
ralise par Laffont et al. [4] qui montre quil nexiste pas de solution-solide dans la rgion
intermdiaire entre les deux domaines de compositions limites. Dans notre modle, linterface
est idalement limite une couche atomique. En fait cela dpend principalement de la taille
des cristallites dans le plan bc, lorsque celle-ci est grande la zone intermdiaire peut en effet
ncessiter la prsence de plusieurs couches atomiques, comme lont montr
exprimentalement Chen et al. sur des cristaux de grande taille [3], de faon accommoder la
diffrence importante de volumes de maille entre les deux phases. Laugmentation de la taille
des cristallites augmente en effet la probabilit quil y ait un dfaut et donc que la forme de la
zone intermdiaire soit plus complexe. On peut galement considrer que le mcanisme de
dsintercalation du lithium, selon quelle soit chimique ou lectrochimique, peut conduire
des rsultats lgrement diffrents. En effet, la dsintercalation chimique peut favoriser la
nuclation simultane dans toutes les cristallites et mme diffrents endroits dune mme
cristallite de grande taille, ce qui par consquent peut conduire une distribution de phases
diffrente de celle obtenue par dsintercalation lectrochimique. Ce mcanisme est donc trs
sensible la prsence de dfauts dans le matriau qui peuvent piger la zone intermdiaire et
donc limiter le dplacement du front de raction ; plus le cristal est de grande taille plus la
probabilit de trouver un dfaut est grande et donc plus la cintique est limite. En effet,
quand le dplacement coopratif du front de phase est stopp par un dfaut il y a cration
dun nouveau centre de nuclation dans le cristal. Comme cela a t discut par Richardson et
ses collaborateurs [3] et par Masquelier et ses collaborateurs [4], plus la taille de la cristallite
est petite selon b, plus la dsintercalation du lithium est favorise dans les tunnels parallles
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre VI
M. Maccario 30 novembre 2007
160
cette direction, ce qui est le point de dpart du mcanisme de dsintercalation / intercalation
du lithium.
Figure VI-2 : Reprsentation dans le plan ac de la zone distordue forme entre le domaine lithi
(LiFePO
4
) et le domaine non lithi (FePO
4
) lors du mcanisme de dsintercalation / intercalation du
lithium dans LiFePO
4
.
Ce schma est aussi en bon accord avec les rsultats rcents obtenus par Allen et al.
qui ont simul le mcanisme de dsintercalation / intercalation du lithium dans LiFePO
4
avec
lquation de Avrami Johnson Mehl Eroofev [10]. Ils ont montr que le taux de
nuclation est nul et que la transformation de phase est contrle par le dplacement du front
de raction. De plus, lnergie dactivation pour la lithiation de la phase FePO
4
en LiFePO
4
est trs faible (13 kj.mol
-1
). Notre modle, qui considre que le dplacement du front de
raction est quivalent un front de phase infiniment rapide se dplaant le long de la
direction a et que le mcanisme de dsintercalation / intercalation du lithium se produit en
bordure du front de phase, est en bon accord avec ce rsultat.
FePO
4
LiFePO
4
Distorted zone
z
x
y
2
C
=
9
.
3
9
A
2
C
=
9
.
5
6
Displacement of the reaction front
FePO
4
LiFePO
4
Distorted zone
z
x
y
z
x
y
2
C
=
9
.
3
9
A
2
C
=
9
.
3
9
A
2
C
=
9
.
5
6
Displacement of the reaction front
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre VI
M. Maccario 30 novembre 2007
161
50 nm
60 nm
150 nm
LiFePO
4
b
a
c
50 nm
FePO
4
/ LiFePO
4
Displacement of the
deintercalation front
Lithium
deintercalation
61 nm
46 nm
60 nm
75 nm
75 nm
50 nm
60 nm
150 nm
LiFePO
4
50 nm
60 nm
150 nm
LiFePO
4
b
a
c
b
a
c
a
c
50 nm
FePO
4
/ LiFePO
4
Displacement of the
deintercalation front
Lithium
deintercalation
61 nm
46 nm
60 nm
75 nm
75 nm
FePO
4
/ LiFePO
4
Displacement of the
deintercalation front
Lithium
deintercalation
61 nm
46 nm
60 nm
75 nm
75 nm
Figure VI-3 : Reprsentation schmatique du mcanisme, dit domino-cascade, de
dsintercalation / intercalation du lithium dans une cristallite de LiFePO
4
. Les cotes sont arbitraires
et ne reprsentent pas les cristallites tudies qui sont isotropes mais donnent une meilleure
apprciation des contraintes se produisant lors du mcanisme de dsintercalation / intercalation du
lithium.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre VI
M. Maccario 30 novembre 2007
162
Lithium
deintercalation
Lithium
intercalation
LiFePO
4
FePO
4
b
a
c
b
a
c
a
c
Lithium and electron
deintercalation
Figure VI-4: Reprsentation schmatique de lavancement du front de dsintercalation / intercalation du
lithium dans LiFePO
4
.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre VI
M. Maccario 30 novembre 2007
163
Bibliographie du Chapitre VI
1
A. Yamada, H. Koizumi, N. Sonoyama, R. Kanno, Electrochemical And Solid State
Letters, 8 (8) (2005), A409-A413.
2
N. Meethong, H. Y. S. Huang, W. C. Carter, Y. M. Chiang, Electrochemical and Solid
State Letters, 10 (5) (2007), A134-A138.
3
G. Y. Chen, X. Y. Song, T. J. Richardson, Electrochemical And Solid State Letters, 9
(6) (2006), A295-A298.
4
L. Laffont, C. Delacourt, P. Gibot, M. Y. Wu, P. Kooyman, C. Masquelier, J. M.
Tarascon, Chemistry Of Materials, 18 (2006), 5520-5529.
5
T. Maxisch, F. Zhou, G. Ceder, Physical Review B, 7310 (2006), NIL_258-NIL_263.
6
D. Morgan, A. Van der Ven, G. Ceder, Electrochemical And Solid State Letters, 7 (2)
(2004), A30-A32.
7
M. S. Islam, D. J. Driscoll, C. A. J. Fisher, P. R. Slater, Chemistry Of Materials, 17
(2005), 5085-5092.
8
V. Srinivasan, J. Newman, Electrochemical And Solid State Letters, 9 (3) (2006),
A110-A114.
9
B. Ellis, L. K. Perry, D. H. Ryan, L. F. Nazar, Journal Of The American Chemical
Society, 128 (2006), 11416-11422.
10
J. L. Allen, T. R. Jow, J. Wolfenstine, Chemistry of Materials, 19 (2007), 2108-2111.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre VII
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre VII
M. Maccario 30 novembre 2007
165
Chapitre VII
Conclusion gnrale
Les travaux raliss au cours de cette thse avaient pour but principal de dterminer
le (ou les) facteur(s) clef(s) de bonnes performances en batteries au lithium de matriaux
C-LiFePO
4
obtenus avec un mode de synthse dvelopp par le CEA. En effet, les tests
lectrochimiques prliminaires de ces matriaux C-LiFePO
4
avaient montr de bons
rsultats sans toutefois pouvoir les attribuer des caractristiques physico-chimiques,
structurales ou morphologiques particulires. Dans le cadre de cette tude, linfluence de
diffrents paramtres de synthse a donc t analyse. Ces travaux ont galement permis
de mieux comprendre le processus de dsintercalation / intercalation du lithium dans ces
matriaux. Les principaux rsultats obtenus sont rsums dans la suite de cette partie.
Dans un premier temps nous avons montr en faisant varier le rapport Li/Fe lors
de la synthse que nous ne formions pas de compos LiFePO
4
valence mixte, soit la
solution-solide Li
1+y
Fe
1-y
PO
4
autour de la composition stoechiomtrique. Ces premiers
rsultats nous ont nanmoins permis doptimiser le mode de synthse. Une srie de
matriaux C-LiFePO
4
a ensuite t synthtise par activation mcano-chimique des
prcurseurs de phosphore, de fer et de lithium (Li
3
PO
4
) en prsence de cellulose, celle-ci se
dcomposant avec laugmentation de la temprature pour former un revtement carbon
la surface des particules de LiFePO
4
. Ce revtement a pour rle dinhiber la croissance des
particules, de favoriser la rduction du Fe
3+
en Fe
2+
mais galement damliorer
considrablement les proprits conductrices du matriau C-LiFePO
4
. Les matriaux
C-LiFePO
4
prsents dans ce manuscrit ont t obtenus par deux traitements thermiques
(lent ou rapide) 575C ou 800C, ils sont parfaitement dcrits par une structure LiFePO
4
olivine ordonne et stoechiomtrique ; cependant tous ces matriaux contiennent un faible
pourcentage de Fe
3+
(5 6 at.%) pouvant tre associ une impuret amorphe riche en
Fe
3+
ou des dfauts de surface. Nous avons en effet montr en combinant diffraction des
rayons X et des neutrons que la solution-solide Li(Li
y
Fe
y
III
Fe
1-2y
II
)PO
4
nest pas forme.
Les tailles des domaines de cohrence des matriaux C-LiFePO
4
tudis sont comprises
entre 60 et 100 nm, en bon accord avec les mesures de surface spcifique ralises. Ces
domaines de cohrence correspondent aux particules primaires observes en microscopie
lectronique transmission et balayage. Le revtement carbon prsent la surface des
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre VII
M. Maccario 30 novembre 2007
166
cristallites de LiFePO
4
a t caractris par spectroscopie Raman, cest un compos
carbon trs fortement dsordonn prsentant une faible longueur de cohrence (< 3 nm) et
sans aucune contribution de carbone sp
3
. Leffet de ce carbone sur la conductivit
lectronique du composite a t mis en vidence par des mesures de conductivit
lectronique et par spectroscopie infrarouge. En effet, plus la temprature de synthse est
leve plus la dcomposition du prcurseur carbon est efficace (moins de fonctions
organiques rsiduelles) et donc plus la conductivit lectronique augmente.
Les bonnes performances lectrochimiques rsultent dun bon compromis entre un
revtement carbon conducteur et une distribution isotrope et homogne de particules
primaires de petite taille (~ 100 nm) favorisant une bonne conductivit ionique et
lectronique. Le matriau synthtis 800C de manire rapide prsente ces
caractristiques et est donc caractris par un comportement lectrochimique trs
intressant lors de cyclages rgimes constants ou en puissance (alternance de rgimes
rapides et lents). Ce matriau Fe
800-fast
a donc fait lobjet dune tude lectrochimique
longue dure temprature ambiante, 40C et 60C. Une bonne capacit rversible est
maintenue au-del de 100 cycles lors des cyclages temprature ambiante et plus de 80 %
de la capacit rversible est galement conserve 40C. Par contre 60C, la tenue en
cyclage est beaucoup plus faible. Quelle que soit la temprature de cyclage, aucune
modification structurale na t observe pour les matriaux C-LiFePO
4
tudis.
La combinaison de la diffraction des rayons X et des spectroscopies Mssbauer et
XPS a, comme attendu, permis de confirmer que le mcanisme de
dsintercalation / intercalation du lithium dans LiFePO
4
est biphas avec deux petits
domaines de solution-solide en dbut et en fin de charge (dcharge), en bon accord avec les
rsultats obtenus par Yamada et al. [1] et Meethong et al. [2]. Ltude par diffraction des
rayons X na pas montr dvolution continue des FWHM et par consquent des tailles de
domaines de cohrence et des contraintes dans les matriaux Li
x
FePO
4
au cours de la
dsintercalation / intercalation du lithium. Ces rsultats montrent que pour les matriaux
tudis le modle cur-corce [3,4] et mme les modles plus rcents proposs par les
groupes de Masquelier et al. [5] et de Richardson et al. [6] ne permettent pas de dcrire le
mcanisme de dsintercalation / intercalation du lithium dans les matriaux tudis : ils
considrent en effet tous que les deux phases extrmes, LiFePO
4
et FePO
4
, coexistent dans
une cristallite. Pour les matriaux tudis, chaque cristallite est constitue dune des deux
phases extrmes. La coexistence de deux phases dans une mme cristallite dpend
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre VII
M. Maccario 30 novembre 2007
167
principalement de la taille des cristallites dans le plan bc. En effet, plus la cristallite est de
grande taille plus la zone daccommodation entre les deux phases doit ncessiter la
prsence de plusieurs couches atomiques, ce qui augmente, par consquent la probabilit
de prsence de dfauts. La prsence dune phase unique dans chaque cristallite a bien t
confirme par microscopie lectronique transmission haute rsolution qui montre que
toutes les cristallites observes sont de composition LiFePO
4
ou FePO
4
et bien cristallises
de part en part. Le mcanisme de dsintercalation / intercalation du lithium de LiFePO
4
a
t dcrit comme un front de phase, qui est dans le plan bc et se dplaant trs rapidement
selon la direction a de la cristallite. Nous avons appel ce mcanisme, le mcanisme
domino-cascade. Il a t propos en prenant la fois en compte le couplage lchelle
microscopique des porteurs / ions lithium (lacunes) et leffet de fortes distorsions locales
dues aux diffrences de volume entre LiFePO
4
et FePO
4
.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Chapitre VII
M. Maccario 30 novembre 2007
168
Bibliographie du Chapitre VII
1
A. Yamada, H. Koizumi, N. Sonoyama, R. Kanno, Electrochemical And Solid
State Letters, 8 (8) (2005), A409-A413.
2
N. Meethong, H. Y. S. Huang, W. C. Carter, Y. M. Chiang, Electrochemical and
Solid State Letters, 10 (5) (2007), A134-A138.
3
A. K. Padhi, K. S. Nanjundaswamy, J. B. Goodenough, Journal of the
Electrochemical Society, 144 (1997), 1188.
4
A. S. Andersson, B. Kalska, L. Haggstrom, J. O. Thomas, Solid State Ionics, 130
(2000), 41-52.
5
L. Laffont, C. Delacourt, P. Gibot, M. Y. Wu, P. Kooyman, C. Masquelier, J. M.
Tarascon, Chemistry Of Materials, 18 (2006), 5520-5529.
6
G. Y. Chen, X. Y. Song, T. J. Richardson, Electrochemical And Solid State Letters,
9 (6) (2006), A295-A298.
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Liste des figures
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Liste des figures
Magali Maccario 30 novembre 2007 169
LISTE DES FIGURES
CHAPITRE I
Figure I-1 : Comparaison des nergies volumiques et massiques de diffrents types de
batteries rechargeables. 2
Figure I-2 : Vue en perspective de la structure olivine de LiFePO
4
dans le plan ac, les ions
lithium tant dans les tunnels parallles la direction b (octadres FeO
6
reprsents en
marron, ttradres PO
4
reprsents en vert et atomes de lithium reprsents en bleu). 7
CHAPITRE II
Figure II-1 : Principe de fonctionnement dune batterie lithium ion. 26
CHAPITRE III
Figure III-1 : Diagrammes de diffraction des rayons X des matriaux C-LiFePO
4
synthtiss
avec diffrents rapports nominaux Li/Fe. 38
Figure III-2 : a) Spectres Mssbauer des matriaux C-LiFePO
4
synthtiss en utilisant
diffrents rapports nominaux Li/Fe, b) Agrandissement du spectre de C-LiFePO
4
(Li/Fe ~ 1.16) permettant de distinguer les deux doublets (Fe
2+
et Fe
3+
) ncessaires
lajustement des spectres calcul et exprimental, c) Agrandissement du spectre du matriau
C-LiFePO
4
(Li/Fe ~ 0.95) permettant de distinguer les deux doublets (Fe
2+
) ncessaires
lajustement des spectres calcul et exprimental. 42
Figure III-3 : Mesures de conductivit lectronique ralises dans le domaine de temprature
[30 300] K avec la mthode des quatre pointes pour les cinq matriaux C-LiFePO
4
synthtiss avec diffrents rapports nominaux Li/Fe (~ 1.16, ~ 1.11, ~ 1.06, ~ 1.00 et ~ 0.95).
44
Figure III-4 : Premiers cycles lectrochimiques obtenus pour les chantillons C-LiFePO
4
,
dont le rapport nominal Li/Fe varie (~ 1.16, ~ 1.11, ~ 1.06, ~ 1.00 et ~ 0.95), les cyclages sont
raliss temprature ambiante dans la fentre de potentiel [2 4.5] V (vs. Li
+
/Li) rgime
C/20. Le vingtime cycle est donn en insert pour les matriaux C LiFePO4 (~ 1.16, ~ 1.11,
~ 1.06). 46
Figure III-5 : Clichs de microscopie lectronique balayage des chantillons C-LiFePO
4
synthtiss avec diffrents rapports Li/Fe (~ 1.16, ~ 1.11, ~ 1.06, ~ 1.00 et ~ 0.95). 48
CHAPITRE IV
Figure IV-1 : a) Diagrammes de diffraction des rayons X obtenus pour les quatre matriaux
C-LiFePO
4
synthtiss avec diffrents traitements thermiques et diffrentes tempratures, b)
Agrandissement de ces diagrammes de diffraction des rayons X dans le domaine angulaire
[17 - 45] (2). 54
Figure IV-2 : a) Spectres Mssbauer obtenus temprature ambiante pour Fe
800-fast
, Fe
800- slow
Fe
575-fast
et Fe
575-slow
, b) Lagrandissement du spectre de Fe
575-fast
permet de distinguer les
doublets ncessaires lajustement des spectres calcul et exprimental. 56
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Liste des figures
Magali Maccario 30 novembre 2007 170
Figure IV-3 : Comparaison des diagrammes de diffraction des rayons X exprimental et
calcul pour Fe
800-fast
. 60
Figure IV-4 : Affinement par la mthode de Rietveld du diagramme de diffraction des
neutrons de Fe
800-fast
(hypothse structurale : LiFePO
4
stoechiomtrique et ordonn) compar
laffinement ralis en tenant compte de lhypothse Li(Li
0.05
Fe
0.95
)PO
4
avec la prsence de
0.05 at. % dions lithium dans le site cristallographique du fer. 63
Figure IV-5 : a) Evolution du rapport H/M en fonction de la temprature (H est le champ
appliqu (fix 10 kOe) et M laimantation molaire), b) Evolution de laimantation molaire
en fonction du champ appliqu T (5 K et 298 K) pour Fe
800-fast
, Fe
800-slow
, Fe
575-fast
et
Fe
575-slow
. 65
Figure IV-6 : Mesures de conductivit lectronique ralises avec la mthode des quatre
pointes dans le domaine de temprature [30 300] K pour Fe
800-fast
, Fe
800-slow
, Fe
575-fast
et
Fe
575-slow
. 66
Figure IV-7 : Spectres FTIR des matriaux Fe
575-fast
et Fe
800-fast
, avec en insert un
agrandissement de la zone de nombres donde [1250 750] cm
-1
(Il est noter que cet insert
prsente des spectres en intensit relative). 68
Figure IV-8 : Comparaison des spectres FTIR de composs LiFePO
4
vitreux et cristallis
[19]. 68
Figure IV-9 : Comparaison des spectres FTIR du prcurseur carbon a) avant traitement
thermique, b) aprs 15 min 575C sous argon (conditions de synthse utilises pour
Fe
575-fast
) et c) aprs 15 min 800C sous argon (conditions de synthse utilises pour
Fe
800-fast
). 70
Figure IV-10 : Spectres de Fe
575-fast
et Fe
800-fast
en infrarouge lointain dans le domaine de
nombres donde [675 100] cm
-1
. 71
Figure IV-11 : Spectres Raman enregistrs avec une longueur donde dexcitation de
632.8 nm diffrents points des matriaux a) Fe
575-fast
et b) Fe
800-fast
. 73
Figure IV-12 : Dsommation de spectres Raman ralises avec des bandes de type
Gaussienne-Lorentzienne ( ) pour a) Fe
575-fast
et b) Fe
800-fast
. 76
Figure IV-13 : Spectres Raman enregistrs la longueur donde dexcitation de 325 nm et
diffrents points de lchantillon Fe
800-fast
. 79
Figure IV-14 : Clichs de Microscopie Electronique Balayage obtenus pour les matriaux
Fe
800-fast
, Fe
800 slow
, Fe
575-fast
et Fe
575-slow
. Pour avoir une vision plus reprsentative de la
microstructure de Fe800-slow, deux micrographies sont donnes lchelle de 600 nm. 81
Figure IV-15 : Micrographies de Microscopie Electronique en Transmission ralises pour a)
Fe
575-fast
et b) Fe
800-fast
. 82
Figure IV-16 : Comparaison a) des courbes de cyclage (potentiel en fonction de x pour
Li
x
FePO
4
) et b) de la capacit rversible en fonction du nombre de cycles pour les quatre
matriaux C-LiFePO
4
utiliss comme lectrode positive dans les batteries au lithium. Ces
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Liste des figures
Magali Maccario 30 novembre 2007 171
cellules lectrochimiques ont t cycles en mode galvanostatique rgime constant (C/20)
dans la fentre de potentiel [2 - 4.5] V (vs. Li
+
/Li ). 85
Figure IV-17 : a) Comparaison de lvolution des capacits rversibles en fonction du
nombre de cycles pour les quatre matriaux C-LiFePO
4
utiliss comme lectrode positive
pour batteries au lithium. Toutes les charges sont ralises rgime C/5 jusqu un potentiel
de 4.5 V vs. Li
+
/Li, tandis que les dcharges ont t ralises rgimes C/n jusqu 2 V vs.
Li
+
/Li. Un agrandissement des courbes dvolution est donn en b) pour les 30 premiers
cycles ainsi que les rgimes de cyclage des dcharges (C/n). 87
Figure IV-18 : Comparaison de lvolution des capacits rversibles obtenues en fonction du
nombre de cycles pour les quatre matriaux C-LiFePO
4
tudis comme matriaux dlectrode
positive pour batteries au lithium. Les cellules lectrochimiques ont t cycles entre 2 et
4.5 V vs. Li
+
/Li pendant des squences successives de quelques cycles diffrents rgimes
C/n. 89
CHAPITRE V
Figure V-1 : Exemple dune courbe de cyclage obtenue rgime de cyclage C/20 dans le
domaine de potentiel [2 - 4.5] V (vs. Li
+
/Li) pour Fe
800-fast
. Les compositions tudies ex-situ
par diffraction des rayons X sont mentionnes par des points sur la courbe. 98
Figure V-2 : Diffractogrammes des rayons X obtenus ex-situ pour des lectrodes enduites
Li
x
FePO
4
rcupres diffrents tats de charge ou de dcharge pendant le premier cycle
lectrochimique de la cellule LiFe
800-fast
. Lindexation des pics de diffraction dans le groupe
despace Pnma est donne pour certains pics associs la phase riche en lithium
(Li
1-
FePO
4
) et la phase pauvre en lithium (Li
FePO
4
). 100
Figure V-3 : Comparaison des diagrammes de diffraction des rayons X exprimental et
calcul pour les matriaux biphass a) Li
~0.39
FePO
4
(lectrode enduite) obtenu
lectrochimiquement aprs une charge partielle de la cellule lectrochimique LiFe
800-fast
et b)
Li
~0.38
FePO
4
(lectrode enduite) obtenu lectrochimiquement aprs une charge et une
dcharge partielle de la cellule lectrochimique LiFe
800 fast
. 108
Figure V-4 : Comparaison des paramtres structuraux obtenus par laffinement par la
mthode de Rietveld des donnes de diffractions des rayons X enregistres pour les lectrodes
enduites et poudre. Les pointills reprsentent les paramtres obtenus pour les matriaux de
compositions extrmes LiFePO
4
et Li
FePO
4
, ceux-ci sont monophass. 110
Figure V-5 : Polydres FeO
6
et PO
4
a) dans la structure olivine LiFePO
4
et b) dans la
structure olivine Li
FePO
4
. 112
Figure V-6 : Spectres Mssbauer enregistrs pour des lectrodes poudre de composition
Li
x
FePO
4
rcupres diffrents tats de charge pendant le premier cycle lectrochimique
en batterie au lithium LiFe
800-fast
. 115
Figure V-7 : Distribution dclatements quadrupolaires associe aux ions Fe
3+
pour le
matriau Li
~0.32
FePO
4
. 116
Figure V-8 : Comparaison des spectres XPS des pics de cur de a) Fe 2p, b) P 2p, c) O 1s et
d) C 1s obtenus pour le matriau initial (Fe
575-fast
) sous la forme dune poudre et dune
lectrode enduite. 118
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Liste des figures
Magali Maccario 30 novembre 2007 172
Figure V-9 : Spectres XPS Fe 3s enregistrs pour le matriau initial (Fe
575-fast
) et pour une
lectrode enduite partir de celui-ci. 119
Figure V-10 : Spectres XPS Fe 2p et Fe 3p obtenus pour des lectrodes enduites de
composition Li
x
FePO
4
, rcupres diffrents tats de charge ou de dcharge de batteries
au lithium LiFe
575-fast
cycles rgime C/20 dans le domaine de potentiel [2 - 4.5] V (vs.
Li
+
/Li). 121
Figure V-11 : Spectres XPS O 1s pour les lectrodes enduites de composition Li
x
FePO
4
rcupres diffrents tats de charge et de dcharge de cellules LiFe
575-fast
cycles rgime
C/20 dans la fentre de potentiel [2 4.5] V (vs. Li
+
/Li). 124
Figure V-12 : Spectres XPS P 2p pour les lectrodes enduites de composition Li
x
FePO
4
rcupres diffrents tats de charge et de dcharge de cellules LiFe
575-fast
cycles rgime
C/20 dans la fentre de potentiel [2 4.5] V (vs. Li
+
/Li). 125
Figure V-13 : Spectres XPS F 1s pour les lectrodes enduites de composition Li
x
FePO
4
rcupres diffrents tats de charge et de dcharge de cellules LiFe
575-fast
cycles rgime
C/20 dans la fentre de potentiel [2 4.5] V (vs. Li
+
/Li). 126
Figure V-14 : Micrographie haute rsolution dune cristallite de Li
1-
FePO
4
du matriau
Fe
800-fast
avec en insert le clich de diffraction associ. Un agrandissement de deux zones
traversant la cristallite de part en part est galement donn. 130
Figure V-15 : Micrographie haute rsolution dune cristallite de Li
'
FePO
4
du matriau
Fe
800-fast
avec en insert le clich de diffraction associ. Un agrandissement de deux zones
traversant la cristallite de part en part est galement donn. 131
Figure V-16 : Courbes de cyclage obtenues pour la cellule lectrochimique LiC-LiFePO
4
(Fe
800-fast
) dans le domaine de potentiel [2 - 4.5] V vs. Li
+
/Li rgime C/20 et a) temprature
ambiante (RT), b) 40C et c) 60C. Comparaison des courbes de charge et de dcharge
obtenues temprature ambiante et 40C pour les 1
er
, 20
me
, 70
me
et 100
me
cycles et 60C
pour les 1
er
, 15
me
, 30
me
et 40
me
cycles. Chaque courbe de charge / dcharge est dcale de
0.1 V par rapport la courbe prcdente pour une comparaison plus aise, cependant les
courbes de premire charge ou dcharge ne sont pas dcales. 136
Figure V-17 : Comparaison des courbes de cyclage obtenues pour la cellule lectrochimique
LiC-LiFePO
4
(Fe
800-fast
) dans le domaine de potentiel [2 - 4.5] V vs. Li
+
/Li rgime C/20 et
a) temprature ambiante (RT), b) 40C et c) 60C, permettant de visualiser la capacit
irrversible et la diffrence de potentiel entre la courbe de charge et de dcharge (prsentation
des 1
er
, 20
me
et 100
me
cycles RT et 40C et prsentation des 1
er
, 15
me
et 40
me
cycles
60C). 137
Figure V-18 : Evolution de la capacit rversible en fonction du nombre de cycles pour la
cellule lectrochimique LiC-LiFePO
4
(Fe
800-fast
) cycle dans le domaine de potentiel
[2 - 4.5] V vs. Li
+
/Li rgime C/20 et temprature ambiante, 40C et 60C. 138
Figure V-19 : Comparaison des diffractogrammes de rayons X enregistrs pour le matriau
initial Fe
800-fast
, pour les matriaux rcuprs aprs une charge rgime C/20 et
temprature ambiante (Fe
800
-RT-1/2charge), aprs une premire charge rgime C/20 et
temprature ambiante (Fe
800
-RT-1charge), aprs une premire charge et une premire
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Liste des figures
Magali Maccario 30 novembre 2007 173
dcharge rgime C/20 et temprature ambiante (Fe
800
-RT-1/2discharge), la fin du
premier cycle lectrochimique rgime C/20 et temprature ambiante (Fe
800
-RT-1cycle),
aprs 100 cycles rgime C/20 et temprature ambiante (Fe
800
-RT-100cycles), aprs 100
cycles rgime C/20 et 40C (Fe
800
-40C-100cycles) et aprs 40 cycles rgime C/20 et
60C (Fe
800
-60C-40cycles). 142
Figure V-20 : Comparaison des diagrammes de diffraction des rayons X exprimental et
calcul obtenus pour Fe
800
-fast aprs 100 cycles dune cellule lectrochimique LiC-LiFePO
4
(Fe
800-fast
) entre 2 et 4.5 V (vs. Li
+
/Li) rgime C/20 et temprature ambiante
(Fe
800-
RT-100cycles). 145
Figure V-21 : Comparaison des diagrammes de diffraction des rayons X exprimental et
calcul obtenus pour Fe
800-fast
aprs 100 cycles dune cellule lectrochimique LiC-LiFePO
4
(Fe
800-fast
) entre 2 et 4.5 V (vs. Li
+
/Li) rgime C/20 et 40C (Fe
800
-40C-100cycles). 147
Figure V-22 : Comparaison des diagrammes de diffraction des rayons X exprimental et
calcul obtenus pour Fe
800-fast
aprs 40 cycles dune cellule lectrochimique LiC-LiFePO
4
(Fe
800-fast
) entre 2 et 4.5 V (vs. Li
+
/Li) rgime C/20 et 60C (Fe
800
-60C-40cycles). 148
Figure V-23 : Comparaison des spectres de fluorescence X obtenus pour une lectrode de
lithium nayant pas subi de cyclage lectrochimique (courbe rouge) et pour une lectrode
ngative rcupre (lithium) dune cellule lectrochimique LiC-LiFePO
4
(Fe
800-fast
) aprs un
cyclage 60C (courbe bleue). 149
CHAPITRE VI
Figure VI-1 : Cration dune lacune de lithium avec formation dun ion Fe
3+
dans son
environnement. Le saut du petit polaron (trou) jusqu un site de fer galement proche de la
lacune de lithium est trs facile. La prsence dun ion Fe
3+
dans un autre site permet daider
la diffusion des ions lithium dans le tunnel de la lacune mais aussi dans les tunnels voisins et
de faciliter ainsi la dsintercalation du lithium. 158
Figure VI-2 : Reprsentation dans le plan ac de la zone distordue forme entre le domaine
lithi (LiFePO
4
) et le domaine non lithi (FePO
4
) lors du mcanisme de
dsintercalation / intercalation du lithium dans LiFePO
4
. 160
Figure VI-3 : Reprsentation schmatique du mcanisme, dit domino-cascade, de
dsintercalation / intercalation du lithium dans une cristallite de LiFePO
4
. Les cotes sont
arbitraires et ne reprsentent pas les particules tudies qui sont isotropes mais donnent une
meilleure apprciation des contraintes se produisant lors du mcanisme de
dsintercalation / intercalation du lithium. 161
Figure VI-4: Reprsentation schmatique de la vague de dsintercalation du lithium dans
LiFePO
4
. 162
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Liste des
tableaux
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Liste des tableaux
Magali Maccario 30 novembre 2007
175
LISTE DES TABLEAUX
CHAPITRE I
Tableau II-1 : Conditions dacquisition utilises pour chaque type dchantillon analys par
diffraction des rayons X. 22
CHAPITRE III
Tableau III-1 : Comparaison des largeurs mi-hauteur (FWHM : Full Width at Half
Maximum) de raies slectionnes sur les diagrammes de diffraction des rayons X des
matriaux C-LiFePO
4
(avec Li/Fe ~ 1.16, ~ 1.11, ~ 1.06, ~ 1.00 et ~ 0.95). Ces valeurs de
FWHM ont t corriges de la fonction instrumentale du diffractomtre en utilisant LaB
6
comme rfrence. La taille des domaines de cohrence (L) est estime partir de la formule
de Scherrer FWHM(2) = 0.9(L.cos) avec = 1.789 (radiation K du cobalt). 38
Tableau III-2 : Comparaison des paramtres structuraux obtenus par laffinement par la
mthode de Le Bail des donnes de diffraction des rayons X pour les matriaux C-LiFePO
4
(~ 1.16, ~ 1.11, ~ 1.06, ~ 1.00 et ~ 0.95). 39
Tableau III-3 : Rsultats des dosages chimiques du C, Li, Fe et P pour les matriaux
C-LiFePO
4
synthtiss avec diffrents rapports nominaux Li/Fe gaux ~ 1.16, ~ 1.11,
~ 1.06, ~ 1.00 et ~ 0.95. La variation du rapport Li/Fe est obtenue grce lutilisation de
diffrents prcurseurs de lithium lors de la synthse. 40
Tableau III-4 : Paramtres hyperfins obtenus par spectroscopie Mssbauer pour les deux
types dions prsents dans les matriaux C-LiFePO
4
dont le rapport nominal Li/Fe varie ( :
dplacement isomrique, : clatement quadrupolaire, : largeur mi-hauteur). Lcart-type
est donn entre parenthses. 43
CHAPITRE IV
Tableau IV-1 : Comparaison des largeurs mi-hauteur (FWHM) pour quelques raies
slectionnes dans les diagrammes de diffraction des rayons X ; ces largeurs de raies ont t
corriges de la contribution instrumentale du diffractomtre. Cette correction est ralise avec
les donnes obtenues pour LaB6. La taille des domaines de cohrence (L) est estime partir
de la formule de Scherrer FWHM(2) = 0.9(L.cos) avec = 1.789 (radiation K du
cobalt). 55
Tableau IV-2 : Rsultats des dosages chimiques des lments C, Li, Fe et P pour Fe
800-fast
,
Fe
800-slow
, Fe
575-fast
et Fe
575 slow
, ainsi que la dtermination des compositions Li : Fe : P des
matriaux. 55
Tableau IV-3 : Paramtres hyperfins dtermins par spectroscopie Mssbauer pour les deux
types dions fer prsents dans les matriaux Fe
800-fast
, Fe
800-slow
, Fe
575-fast
et Fe
575-slow
( :
dplacement isomrique, : clatement quadrupolaire et : largeur mi-hauteur). Les
valeurs donnes en italique correspondent lion Fe
3+
prsent en moindre quantit. Les
erreurs sont donnes entre parenthses, pour dterminer lcart-type il suffit de les multiplier
par 3. 57
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Liste des tableaux
Magali Maccario 30 novembre 2007
176
Tableau IV-4 : Comparaison des paramtres de maille et de microstructure dtermins par
laffinement par la mthode de Rietveld des donnes de diffraction des rayons X enregistres
pour Fe
800-fast
, Fe
800-slow
, Fe
575-fast
et Fe
575-slow
. Les affinements ont t raliss en considrant
une fonction de profil de type Thompson-Cox-Hastings, o <>
1/2
reprsente les contraintes
et L la taille des domaines de cohrence. 59
Tableau IV-5 : Paramtres de structure et de profil obtenus par laffinement par la mthode
de Rietveld des donnes de diffraction des rayons X enregistres pour Fe
800-fast
. 61
Tableau IV-6 : Paramtres de maille obtenus par laffinement par la mthode de Rietveld des
donnes de diffraction des neutrons pour Fe
800-fast
, Fe
800-slow
, Fe
575-fast
et Fe
575-slow
en
considrant lhypothse (i), soit la prsence dions lithium en excs dans le site du fer (4c(x,
, z)). Les taux doccupation du Fe et du Li dans le site du fer 4c (x ~ 0.281, , z ~ 0.977)
sont galement donns. 63
Tableau IV-7 : Paramtres des quatre bandes de type Gaussienne-Lorentzienne utilises pour
affiner les bandes D et G des spectres Raman enregistrs diffrents points de lchantillon
Fe
800-fast
. Ces spectres sont ceux reports la Figure IV-11. 77
Tableau IV-8 : Comparaison des surfaces spcifiques mesures par la mthode BET pour
Fe
800-fast
, Fe
800-slow
, Fe
575-fast
et Fe
575-slow
. 83
CHAPITRE V
Tableau V-1 : Comparaison des largeurs de raies (FWHM) dtermines pour des pics
slectionns sur les diagrammes de diffraction des rayons X enregistrs pour les lectrodes
enduites de composition Li
x
FePO
4
rcupres diffrents tats de charge ou de dcharge
pendant le premier cycle de la batterie au lithium LiFe
800-fast
: (200), (210) et (311) pour
Li
1-
FePO
4
et (200), (210) et (020) pour Li
FePO
4
. Les paramtres microstructuraux, <>
1/2
pour les contraintes et <L> pour la taille des domaines de cohrence, sont dtermins en
considrant la fonction de ThompsonCoxHastings pour dcrire le profil des pics de
diffraction. 101
Tableau V-2 : Paramtres structuraux et de profil dtermins pour le matriau biphas
Li
~0.39
FePO
4
(lectrode enduite) obtenu lectrochimiquement aprs une charge partielle de
la cellule lectrochimique LiFe
800-fast
. 105
Tableau V-3 : Paramtres structuraux et de profil dtermins pour le matriau biphas
Li
~0.38
FePO
4
(lectrode enduite) obtenu lectrochimiquement aprs une charge et une
dcharge partielle de la cellule lectrochimique LiFe
800-fast
. 106
Tableau V-4 : Paramtres hyperfins dtermins par spectroscopie Mssbauer ( :
dplacement isomrique, : clatement quadrupolaire moyen et : largeur mi-hauteur)
partir de lanalyse des spectres des diffrents matriaux Li
x
FePO
4
synthtiss
lectrochimiquement pendant la premire charge dune cellule lectrochimique LiFe
800-fast
.
Les spectres ont t analyss avec une distribution dclatements quadrupolaires. Il est noter
que les valeurs de et sont fixes aux valeurs dtermines lors de laffinement des raies
avec un profil lorentzien. 116
Tableau V-5 : Rapports des distances cristallographiques thoriques des phases Li
1-
FePO
4
et
Li
'
FePO
4
. 132
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Liste des tableaux
Magali Maccario 30 novembre 2007
177
Tableau V-6 : Paramtres structuraux et de profil obtenus par laffinement par la mthode de
Rietveld des donnes de diffraction de rayons X enregistres pour Fe
800
-fast aprs 100 cycles
rgime C/20 et temprature ambiante (Fe
800
-RT-100cycles). 144
Tableau V-7 : Comparaison des paramtres de maille obtenus par laffinement par la
mthode de Rietveld des donnes de diffraction des rayons X enregistres pour le matriau
initial Fe
800-fast
, pour les matriaux rcuprs aprs une charge rgime C/20 et
temprature ambiante (Fe
800
-RT-1/2charge), aprs une premire charge rgime C/20 et
temprature ambiante (Fe
800
-RT-1charge), aprs une premire charge et une premire
dcharge rgime C/20 et temprature ambiante (Fe
800
-RT-1/2discharge), la fin du
premier cycle lectrochimique rgime C/20 et temprature ambiante (Fe
800
-RT-1cycle),
aprs 100 cycles rgime C/20 et temprature ambiante (Fe
800
-RT-100cycles), aprs 100
cycles rgime C/20 et 40C (Fe
800
-40C-100cycles) et enfin aprs 40 cycles rgime C/20
et 60C (Fe
800
-60C-40cycles). 146
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Caractrisation de nanomatriaux C-LiFePO
4
optimiss comme matriaux dlectrode
positive pour batteries lithium-ion. Dtermination du mcanisme de
dsintercalation / intercalation du lithium partir de ces matriaux.
Des nanomatriaux C-LiFePO
4
dlectrode positive pour batteries lithium-ion ont t
synthtiss dans diffrentes conditions de synthse (rapport Li/Fe, temprature, traitement
thermique), aprs mcano-activation du mlange des prcurseurs. Une tude des proprits
physico-chimiques et structurales de diffrents matriaux C-LiFePO
4
a t ralise par les
techniques classiques de la Chimie du Solide et de la Science des Matriaux : diffraction (X,
neutrons et lectrons), spectroscopies (Mssbauer, IR, Raman, ) et microscopie (MEB et
MET-HR) de faon essayer de dterminer le (les) facteur(s) cl(s) de bonnes performances
lectrochimiques en batteries au lithium. La combinaison des analyses des matriaux
dsintercals par DRX et MET-HR nous a permis de proposer le mcanisme dit domino-
cascade pour expliquer la dsintercalation / intercalation rapide du lithium dans ces
matriaux Li
x
FePO
4
et donc leurs bonnes performances lectrochimiques en batteries
lithium-ion. Leffet des cyclages longue dure diffrentes tempratures a galement t
tudi.
Mots clefs : LiFePO
4
, olivine, phosphates, batteries lithium ion, diffraction des
rayons X, microscopie lectronique haute rsolution, spectroscopie Mssbauer,
performances lectrochimiques
Characterization of optimized C-LiFePO
4
nanomaterials as positive electrodes for
lithium ion batteries. Study of the lithium deintercalation / intercalation mechanism.
C-LiFePO
4
nanomaterials used as positive electrodes in lithium ion batteries were
obtained in various synthesis conditions (Li/Fe ratio, temperature, thermal treatment), after a
mechano-chemical activation of the precursors mixture. An in-depth study of their physico-
chemical and structural properties was done combining Solid State Chemistry and Material
Sciences techniques such as diffraction (X-Ray, neutrons and electrons), spectroscopy
(Mssbauer, IR, Raman, ...) and microscopy (SEM and HR-TEM) to determine the key
factors for good electrochemical performance in lithium ion batteries. X-Ray diffraction and
HR-TEM studies allowed proposing the domino-cascade mechanism to explain fast lithium
deintercalation / intercalation in LiFePO
4
and thus its good electrochemical performance in
lithium ion batteries. Long range cyclings were also studied at various temperatures.
Keywords: LiFePO
4
, olivine, phosphates, lithium-ion batteries, X-Ray diffraction, high
resolution transmission electron microscopy, Mssbauer spectroscopy,
electrochemical performance
t
e
l
-
0
0
3
6
2
2
1
7
,
v
e
r
s
i
o
n
1
-
1
7
F
e
b
2
0
0
9
Vous aimerez peut-être aussi
- Des pratiques inspirantes au coeur de la formation à l'enseignementD'EverandDes pratiques inspirantes au coeur de la formation à l'enseignementPas encore d'évaluation
- L' INSTALLATION INTERACTIVE: Un laboratoire d’expériences perceptuelles pour le participant-chercheurD'EverandL' INSTALLATION INTERACTIVE: Un laboratoire d’expériences perceptuelles pour le participant-chercheurPas encore d'évaluation
- HDR Eml TMSR SmallDocument135 pagesHDR Eml TMSR SmallgodofthebroceanPas encore d'évaluation
- These JacobDocument214 pagesThese JacobpoooolePas encore d'évaluation
- RemerciementsDocument4 pagesRemerciementsRissay El KhattabiPas encore d'évaluation
- These Tricoit Sandy 00 00Document288 pagesThese Tricoit Sandy 00 00YasminFernandesPas encore d'évaluation
- Arenal PHD 1Document234 pagesArenal PHD 1Youssef KhaledPas encore d'évaluation
- UntitledDocument293 pagesUntitledMohamed AIT KASSIPas encore d'évaluation
- ROGER 2013 DiffusionDocument160 pagesROGER 2013 Diffusionhayet debbichPas encore d'évaluation
- These ElgibariDocument158 pagesThese ElgibarimikefirminoPas encore d'évaluation
- Salem D. Synthèse de Nanotubes de CarboneDocument168 pagesSalem D. Synthèse de Nanotubes de CarboneniebelungenPas encore d'évaluation
- Détection Et Localisation de Défauts Pour Un Système PVDocument206 pagesDétection Et Localisation de Défauts Pour Un Système PVHamza Baraket100% (3)
- 2015limo0109 PDFDocument216 pages2015limo0109 PDFRaNià itPas encore d'évaluation
- Monnier Laurine MergedDocument154 pagesMonnier Laurine MergedfkdfokPas encore d'évaluation
- Matériauw PDFDocument194 pagesMatériauw PDFKàoutarAllabouchePas encore d'évaluation
- Vd2 Martinand-Lurin Elodie 06022015Document397 pagesVd2 Martinand-Lurin Elodie 06022015jijax-ukobPas encore d'évaluation
- These S PacchiniDocument172 pagesThese S PacchiniNadia Ait AhmedPas encore d'évaluation
- Thèse Eric RosenkrantzDocument226 pagesThèse Eric RosenkrantzAmine EminePas encore d'évaluation
- 2016PA066311Document225 pages2016PA066311pedro66Pas encore d'évaluation
- Marconnet C. Influence de L'adhésion Et de L'activité EnzymatiqueDocument329 pagesMarconnet C. Influence de L'adhésion Et de L'activité Enzymatiqueniebelungen100% (1)
- Texier Partie 1 Sur 2Document157 pagesTexier Partie 1 Sur 2Azabou MariamPas encore d'évaluation
- Thèse David RiassettoDocument364 pagesThèse David RiassettoVazel22100% (2)
- 2006LEMA1026Document219 pages2006LEMA1026KHALID1969Pas encore d'évaluation
- Hydorxydes Double Lamélaire HDLDocument188 pagesHydorxydes Double Lamélaire HDLbenahmed100% (1)
- ChevalierDocument302 pagesChevalierfullaPas encore d'évaluation
- These de BureDocument285 pagesThese de BureGeorges AouadPas encore d'évaluation
- Etude Et Développement D'un Oscillateur À Quartz Intégré - These - PTINGUYDocument212 pagesEtude Et Développement D'un Oscillateur À Quartz Intégré - These - PTINGUYOstensiblePas encore d'évaluation
- 2015LIMO0124Document241 pages2015LIMO0124lili loulouPas encore d'évaluation
- These Camille Decroix 2019Document222 pagesThese Camille Decroix 2019Chrif MouradPas encore d'évaluation
- Modélisation FlavonoidesDocument0 pageModélisation FlavonoidesmekaekPas encore d'évaluation
- KETEP 2012 Archivage PDFDocument317 pagesKETEP 2012 Archivage PDFkhalid bouitiPas encore d'évaluation
- 2 Manuscrit MV PDFDocument274 pages2 Manuscrit MV PDFmedaminePas encore d'évaluation
- Liang C. Caractérisations Électriques de Polymères ConducteursDocument152 pagesLiang C. Caractérisations Électriques de Polymères ConducteursniebelungenPas encore d'évaluation
- Acide NitriqueDocument231 pagesAcide NitriqueJe TePas encore d'évaluation
- Thèse: #D'ordre: 298-2009Document191 pagesThèse: #D'ordre: 298-2009Gaël HenriotPas encore d'évaluation
- Arenal PHD 1Document234 pagesArenal PHD 1Ilham ZitouniPas encore d'évaluation
- Optical Properties of Point Defects in Hexagonal BDocument139 pagesOptical Properties of Point Defects in Hexagonal BAhamed Al ArifinPas encore d'évaluation
- Allab Farid TheseDocument196 pagesAllab Farid TheseMourad HMPas encore d'évaluation
- Tran 2010 PDFDocument182 pagesTran 2010 PDFFatima EssaiPas encore d'évaluation
- 2014ISAR0005Document185 pages2014ISAR0005Georges TaradauxPas encore d'évaluation
- Etude de La Relaxation Structurale Dans Un VerreDocument194 pagesEtude de La Relaxation Structurale Dans Un VerreAkabli YounesPas encore d'évaluation
- HENROTTE 2018 ArchivageDocument188 pagesHENROTTE 2018 ArchivageOuchaou MehdiPas encore d'évaluation
- Membranes Électrolytes À Porteurs de Charge Li+: To Cite This VersionDocument203 pagesMembranes Électrolytes À Porteurs de Charge Li+: To Cite This VersionMohamed AIT KASSIPas encore d'évaluation
- Thse Thomas Parent VersionfinaleDocument276 pagesThse Thomas Parent VersionfinaleKARIMPas encore d'évaluation
- Ddoc T 2012 0314 FaizDocument169 pagesDdoc T 2012 0314 FaizLaura R.Pas encore d'évaluation
- LANNELONGUE 2018 ArchivageDocument227 pagesLANNELONGUE 2018 ArchivageProfesseur BoughrietPas encore d'évaluation
- BAJJA 2016 ArchivageDocument245 pagesBAJJA 2016 ArchivageAbdellah El hadekPas encore d'évaluation
- These Ahmed Ziani 2009 Univ Rennes 1Document227 pagesThese Ahmed Ziani 2009 Univ Rennes 1Sofa ChaPas encore d'évaluation
- 2018LIMO0089Document175 pages2018LIMO0089Hichem NaghmouchiPas encore d'évaluation
- These GuilleminDocument234 pagesThese GuilleminnassirouPas encore d'évaluation
- Baillieul MarionDocument259 pagesBaillieul Marionkuzgun cebeciPas encore d'évaluation
- Enscm 2022 CuminetDocument242 pagesEnscm 2022 CuminetmicmacPas encore d'évaluation
- These Camelia StingaDocument243 pagesThese Camelia StingaRahme NormanPas encore d'évaluation
- These A JeanDocument285 pagesThese A JeanPerezPas encore d'évaluation
- 2014ENMP0062Document226 pages2014ENMP0062Jean Jules BadiangPas encore d'évaluation
- PONS 2016 ArchivageDocument268 pagesPONS 2016 Archivagelabo estPas encore d'évaluation
- RemerciementsDocument3 pagesRemerciementsTuan NguyenPas encore d'évaluation
- 2016TOU30080b PDFDocument227 pages2016TOU30080b PDFmyskyshepherdPas encore d'évaluation
- Mary HHDocument135 pagesMary HHMariam ZouhairPas encore d'évaluation
- 2011 Beguin These Erosion de ContactDocument334 pages2011 Beguin These Erosion de ContactPvinaigrettePas encore d'évaluation
- Chimie AnalytiqueDocument162 pagesChimie AnalytiqueIbrahim Lahmid100% (3)
- Perturbations Electromagnetiques BF Et HF - MR Guignabel PDFDocument16 pagesPerturbations Electromagnetiques BF Et HF - MR Guignabel PDFعادل الحمديPas encore d'évaluation
- Le Transistor Bipolaire en Haute FrequenceDocument4 pagesLe Transistor Bipolaire en Haute Frequencedavinccicode100% (2)
- Elargissement Des RaiesDocument12 pagesElargissement Des RaiesdavinccicodePas encore d'évaluation
- These HosniDocument133 pagesThese HosnidavinccicodePas encore d'évaluation
- Présentation Réservoir D'eau PotableDocument14 pagesPrésentation Réservoir D'eau PotabledavinccicodePas encore d'évaluation
- App D'auscultationDocument4 pagesApp D'auscultationdavinccicodePas encore d'évaluation
- 2014TOU30095Document212 pages2014TOU30095davinccicodePas encore d'évaluation
- Étude Feu Volume1Document30 pagesÉtude Feu Volume1davinccicodePas encore d'évaluation
- Lumiere Et Environnement Visuel. Jean-Jacques DamelincourtDocument18 pagesLumiere Et Environnement Visuel. Jean-Jacques DamelincourtdavinccicodePas encore d'évaluation
- Soutien LogistiqueDocument76 pagesSoutien LogistiquedavinccicodePas encore d'évaluation
- Bel 5688Document147 pagesBel 5688YahiaRealPas encore d'évaluation
- EC2 Base PDFDocument154 pagesEC2 Base PDFFarid Ben MustaphaPas encore d'évaluation
- Calcul Et Conception Des SilosDocument46 pagesCalcul Et Conception Des Silosnabilou9389% (19)
- Perturbations Electromagnetiques BF Et HF - MR Guignabel PDFDocument16 pagesPerturbations Electromagnetiques BF Et HF - MR Guignabel PDFعادل الحمديPas encore d'évaluation
- Perturbations Electromagnetiques BF Et HF - MR Guignabel PDFDocument16 pagesPerturbations Electromagnetiques BF Et HF - MR Guignabel PDFعادل الحمديPas encore d'évaluation
- LatexDocument2 pagesLatexYassine SaidPas encore d'évaluation
- Thermodynamique ClassiqueDocument81 pagesThermodynamique Classiquedavinccicode100% (1)
- Chimie QuantiqueDocument5 pagesChimie Quantiquedavinccicode100% (1)
- Mole C UlaireDocument49 pagesMole C Ulairedavinccicode100% (1)
- 1s 2-Ecran PlatDocument6 pages1s 2-Ecran PlatdavinccicodePas encore d'évaluation
- Nano Brochure FRDocument57 pagesNano Brochure FRameetjayaswalPas encore d'évaluation
- Etude Et Conception D'un Reducteur de Vitesse Coxial À Deux ÉtagesDocument125 pagesEtude Et Conception D'un Reducteur de Vitesse Coxial À Deux ÉtagesKhemili Sayf100% (1)
- Oiml D 25: Ocument NternationalDocument13 pagesOiml D 25: Ocument NternationalLarios RolaPas encore d'évaluation
- Séance 1 - V ': 1. RappelsDocument11 pagesSéance 1 - V ': 1. RappelsAssilePas encore d'évaluation
- Dossier Ecrit Pm16gr3 Savu VladimirDocument4 pagesDossier Ecrit Pm16gr3 Savu VladimirVladimir SavuPas encore d'évaluation
- Projet de Thèse - Mamadou COULIBALYDocument5 pagesProjet de Thèse - Mamadou COULIBALYMamadou CoulibalyPas encore d'évaluation
- Chapitre IV-Le Second Principe de La Thermodynamique PDFDocument13 pagesChapitre IV-Le Second Principe de La Thermodynamique PDFInes MazgarPas encore d'évaluation
- Rapport de StageDocument32 pagesRapport de StageMarwane Ch100% (1)
- Cours TB2Document40 pagesCours TB2رؤوف بوسعيدPas encore d'évaluation
- J. Robert Lalonde, Marie-Danielle Cyr - Observatoire - L'humain - Manuel de L'élève, 1re Année Du 2e Cycle Du Secondaire-ERPI (2007)Document465 pagesJ. Robert Lalonde, Marie-Danielle Cyr - Observatoire - L'humain - Manuel de L'élève, 1re Année Du 2e Cycle Du Secondaire-ERPI (2007)Nazim Benbouabdallah100% (1)
- A Laboratory Study of The Strength of ClaysDocument24 pagesA Laboratory Study of The Strength of ClayslorenaPas encore d'évaluation
- Meca Roche 3Document34 pagesMeca Roche 3Zakaria El GhabriPas encore d'évaluation
- Cours 14Document10 pagesCours 14lamia temmouchePas encore d'évaluation
- Enoncé TP2 Réaliser CompositeDocument4 pagesEnoncé TP2 Réaliser CompositeazertyPas encore d'évaluation
- TD Circuits CCDocument10 pagesTD Circuits CCAzzedine Bouadma100% (1)
- Sujet Maths Ecricomes 2012Document4 pagesSujet Maths Ecricomes 2012Hamza HaPas encore d'évaluation
- Inbound 8152076117833357287 UDocument4 pagesInbound 8152076117833357287 UWkPas encore d'évaluation
- Syllabus Formation SolaireDocument3 pagesSyllabus Formation SolaireYvan Onana EssindiPas encore d'évaluation
- Détection Des Défauts D'une Machine Tournantes Par L'analyse FFTDocument82 pagesDétection Des Défauts D'une Machine Tournantes Par L'analyse FFTSofiane HAMCHAOUIPas encore d'évaluation
- Compensateur - DilatationDocument127 pagesCompensateur - DilatationSébastien DeprostPas encore d'évaluation
- TDs 2013 EnonceDocument24 pagesTDs 2013 EnonceMohamed El HajjamPas encore d'évaluation
- Corrigé Examenfinal2Document3 pagesCorrigé Examenfinal2An IsPas encore d'évaluation
- Série D'exercices - Équilibre D'un Corps Sous L'action de Trois Forces - TCS - DR Karam OuharouDocument4 pagesSérie D'exercices - Équilibre D'un Corps Sous L'action de Trois Forces - TCS - DR Karam Ouharouأكاديمية التأكدم - Taakdom AcademyPas encore d'évaluation
- Chapitre1 Chimie 2Document8 pagesChapitre1 Chimie 2bachir bennaoumPas encore d'évaluation
- TP N°9: Etude Du Mouvement de Rotation D'Un Solide Autour D'Un Axe FixeDocument3 pagesTP N°9: Etude Du Mouvement de Rotation D'Un Solide Autour D'Un Axe FixeOUSSAMA BOUTRIAPas encore d'évaluation
- R1280Ts-UserManual r15Ae3iGPDocument1 pageR1280Ts-UserManual r15Ae3iGPMarvin Eduardo MartinezPas encore d'évaluation
- L3-Antennes Et Lignes de transmission-TD2-SolutionDocument8 pagesL3-Antennes Et Lignes de transmission-TD2-SolutionFerroudj FeryalPas encore d'évaluation
- Hyp de CalculDocument12 pagesHyp de CalculIheb IsmailPas encore d'évaluation
- Exercices Convertir Et Distribuer 2022 ALFARABI Nndoc-1Document17 pagesExercices Convertir Et Distribuer 2022 ALFARABI Nndoc-1FatimaZahra QOBBIPas encore d'évaluation
- Variogramme GeostatistiqueDocument22 pagesVariogramme GeostatistiquedimaPas encore d'évaluation
- 1-Conception Et Analyse Des Syst MécDocument6 pages1-Conception Et Analyse Des Syst Méchamza100% (1)