Académique Documents
Professionnel Documents
Culture Documents
Calculos Dilusiones
Transféré par
Luz Angela MorenoDescription originale:
Titre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Calculos Dilusiones
Transféré par
Luz Angela MorenoDroits d'auteur :
Formats disponibles
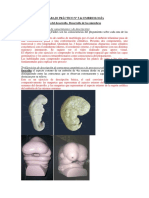
Paralaprimeraprctica
Preparacin de
Disoluciones
Clculos de concentracin
Manejodeconcentracinmolarymsica
Clculodecantidaddesoluto(masa)parauna
concentracindada
Clculodevolumenparapreparacinpor
dilucin
Procedimientos
Como regla general el disolvente es agua Destilada
Concentracinmsica
Masadesoluto(s)porunidaddevolumende
disolucin(D)
Ojo!Nodedisolvente(d)
Molaridad
Cantidad(enmol)desolutoporunidadde
volumen(enL)dedisolucin
Ojo!Nodedisolvente(d)
c=ms /VD
Unidadesaemplear:g/L,mg/L
Otraexpresinmses%p/v:masa(eng)desoluto
enunvolumende100mL dedisolucin
Portanto,como100mL =0,100L,%p/v=gen0,1Ly
1L
x
%p/v=%p/vx10=c(g/L)
0,1L
M = ns / vD =
moles de soluto
litros de disolucin
Unidad:mol/L=M(seleemolar)
PREPARACION DE DISOLUCIONES
MOLARIDAD
Cuando se consideran concentraciones pequeas (como las de ciertos
nutrientes o metabolitos en los seres vivos, contaminantes en el medio,
etc.) se emplean submltiplos de esta unidad:
UNIDAD
CONCENTRACION
mmol/L (milimolar)
EQUIVALENCIA
mM
0,001 M (10-3 M)
mol/L (micromolar)
0,001 mM (10-6 M)
nmol/L (nanomolar)
nM
0,001 M (10-9 M)
pmol/L (picomolar)
pM
0,001 nM (10-12 M)
- Calcular la masa (peso) m de soluto para preparar un
volumen v de disolucin de concentracin c g/L de un soluto
-m=cxv
[ (g/L)L = g ]
- Cuidado con las unidades: si v en mL convertir a L
- Si c en mg/L, es igual pero convertir a g/L
- Calcular la masa (peso) m de soluto para preparar un
volumen v de disolucin de concentracin c M de un soluto
de masa molar MM.
- Como n = m / MM
- m = c x v x MM
[(mol/L) L (g/mol) = g ]
- Cuidado con las unidades: si v en mL, convertir a L
- Si c en mmol/L, es igual pero convertir a mol/L
Otra forma
Ejemplo
Es equivalente:
Cuntos gramos de NiCl2 se necesitan para
preparar 250 mL de una disolucin 0,30 M?
Utilizar factores de conversin
Qu masa de KI se requiere para preparar 500 mL
de una disolucin 2,80 M de KI?
MM =129,7g/mol
m = c x v x MM =
M KI
volumen de disolucin de KI
= 0,30 mol/L 0,250 L 129,7 g/mol =
500 mL x
= 9,73 g
1L
1000 mL
moles KI
2,80 mol KI
1 L disn
166 g KI
1 mol KI
MM KI
gramos KI
= 232 g KI
Preparacin de una disolucin de concentracin dada
Otroejemplo
Queremos preparar exactamente 250 mL de una
disolucin 0,250 M de K2CrO4 en agua. Qu masa de
K2CrO4 habremos de usar?
Tras pesar y disolver en
un vaso se trasfiere al
matraz
aforado
Volumen moles masa
Estrategia:
Necesitamos 2 factores de conversin!
Agitar
MM
Calculamos:
Menisco
Diluir con
agua destilada
mK2CrO4 = 0,250 L 0,250 mol 194,02 g = 12,1 g
1,00 mol
1,00 L
Mezclar
Ver: http://politube.upv.es/play.php?vid=2948
Dilucin es el procedimiento para preparar una disolucin
menos concentrada a partir de otra de mayor concentracin.
Enrasar (ajustar el nivel
a la marca) con cuidado
Dilucindeunadisolucin
La cantidad de soluto no cambia
ni = nf
Dilucin
Porcin tomada
(alcuota)
Aadimos
disolvente
M=
Disolucin inicial
Moles (o masa) de soluto
antes de la dilucin (i)
Moles (o masa) de soluto
despus de la dilucin (f)
mi
mf
ni
Mi
Vf =
nf
Mi
Vi
Mf
n
V
Disolucin final
Vi = Mf Vf
Vi = Vf
Mf
Mi
Ejemplo: Preparar 250 mL de CuSO4 de 1,596 g/L a partir de CuSO4 0,100 M
Ejemplo
CiertoprocedimientoanalticorequieredisolucindeK2CrO4
0,0100M.Quvolumendeunadisolucin0,250Mde
K2CrO4 habradeutilizarseparapreparar0,500LdelK2CrO4
0,0100M?
Estrategia:Ponemosprimerolasdosconcentracionesenlasmismasunidades
C = m / V = (n x MM)/V = M x MM = 0,1 mol/L x 159,6 g CuSO4/mol
Cinicial = 15,96 g/L
Vinicial=
Estrategia:
Vi =
Vf
Mf
Mi
(1,596 g/L)(250mL)
Vinicial= 25 mL
15,96 g/L
Procedimiento:
Calculamos:
Cinicial Vinicial = Cfinal Vfinal
Estafrmulamsgenerales
vlidaparaconcentraciones
dadasporunidaddevolumen
yenlasmismasunidades
Tomar
conpipeta
1,000L
VK2CrO4 =0,500L 0,0100mol
=0,0200L =20,0mL
0,250mol
1,00L
Transferir
Enrasar,
tapary
mezclar
Otro ejemplo: Se quieren preparar 50 mL de disolucin 0,100 M en Na, a
partir de otra de concentracin 5,84 % p/v en NaCl.
Estrategia:Ponemosprimerolasdosconcentracionesenlasmismasunidades.
Vamosapasar,enestecaso,5,84%p/venNaClaMenNa.
5,84 % p/v en NaCl = 5,84 g de NaCl en 100 mL de disolucin
Tendremosquepasargramosamoles(MM NaCl = 58,4 g/mol) yreferirloa1L;
tambinhayquetenerencuentalosmolesdeNaquehayencadamoldeNaCl.
5,84 g de NaCl en 100 mL x 1,0 L = 58,4 g de NaCl en 1L
0,1 L
58,4 g NaCl / L x 1 mol NaCl = 1,0 mol NaCl/ L = 1,0 M en NaCl
58,4 g
1,0 M NaCl x 1 mol Na = 1,0 M Na
1 mol NaCl
Cinicial Vinicial = Cfinal Vfinal
Vinicial=
(0,100 M)(50mL)
1,0 M
Vinicial=
5,0 mL
Vous aimerez peut-être aussi
- Técnicas analíticas básicas: En el control de la calidad del agua según normatividadD'EverandTécnicas analíticas básicas: En el control de la calidad del agua según normatividadPas encore d'évaluation
- 3 .Disoluciones 2Document31 pages3 .Disoluciones 2Karen Vidal CortezPas encore d'évaluation
- 3ro Medio Disoluciones QuimicasDocument40 pages3ro Medio Disoluciones Quimicaseioa3Pas encore d'évaluation
- QUIMICADocument4 pagesQUIMICAric3104Pas encore d'évaluation
- Soluciones DisolucionesDocument34 pagesSoluciones DisolucionesErika Rodriguez0% (1)
- Tarea - Virtual - N - 2 - QG - 2023 - 2 - M2 QUIMICADocument5 pagesTarea - Virtual - N - 2 - QG - 2023 - 2 - M2 QUIMICArodrigo.ventura.quintanillaPas encore d'évaluation
- Nervios CranealesDocument26 pagesNervios CranealesAlamiro Vásquez DíazPas encore d'évaluation
- Disoluciones Tema 2Document8 pagesDisoluciones Tema 2Saideth RojasPas encore d'évaluation
- Taller: Medidas de Concentracion de SolucionesDocument4 pagesTaller: Medidas de Concentracion de SolucionesDiana GallegoPas encore d'évaluation
- Quimica Guia 1 Soluciones y ConcentracionesDocument6 pagesQuimica Guia 1 Soluciones y Concentracioneszy4d7n589gPas encore d'évaluation
- Experimento 3Document7 pagesExperimento 3Dahir CarreraPas encore d'évaluation
- Semana 14Document10 pagesSemana 14JOSE LUIS DEL CASTILLO MARTINEZPas encore d'évaluation
- Disoluciones QuimicaDocument33 pagesDisoluciones QuimicamarielPas encore d'évaluation
- Estiometria de DisolucionesDocument11 pagesEstiometria de DisolucionesBryan José SarangoPas encore d'évaluation
- MolaridadDocument9 pagesMolaridadEduardo KlintworthPas encore d'évaluation
- Práctica 4. CálculosDocument7 pagesPráctica 4. CálculosDavid AnlaPas encore d'évaluation
- Unidades QuimicasDocument15 pagesUnidades QuimicasfhelenPas encore d'évaluation
- Taller de Quimica 2Document17 pagesTaller de Quimica 2Jeisson AlvarezPas encore d'évaluation
- Actividad Grupal - DisolucionesDocument5 pagesActividad Grupal - Disolucionesfernanda valenzuelaPas encore d'évaluation
- QUIMICADocument8 pagesQUIMICALuis Miguel Castro VegaPas encore d'évaluation
- Módulo Concentración de SolucionesDocument28 pagesMódulo Concentración de SolucionesEstela VillarrealPas encore d'évaluation
- 60cb558c40e4f184 20210514 101541tyl8mDocument31 pages60cb558c40e4f184 20210514 101541tyl8mJosue brownPas encore d'évaluation
- Expresión de Concentración de SolucionesDocument60 pagesExpresión de Concentración de SolucionesPatricia BusteloPas encore d'évaluation
- Guia de Laboratorio #3 Soluciones 2021 GRUPOBDocument23 pagesGuia de Laboratorio #3 Soluciones 2021 GRUPOBDenesis TejedaPas encore d'évaluation
- Actividad de Estequiometria 2Document8 pagesActividad de Estequiometria 2BRIAN JULIO SOLANO0% (2)
- 7 Estequiometria de SolucionDocument10 pages7 Estequiometria de SolucionHair Samayoa BrionesPas encore d'évaluation
- De Ejemplo de SolucionesDocument6 pagesDe Ejemplo de SolucionesdorgelyPas encore d'évaluation
- Taller de SolucionesDocument5 pagesTaller de SolucionesJacqueline Humanez MartinezPas encore d'évaluation
- OsmolaridadDocument17 pagesOsmolaridadSamuel Velasquez NaviaPas encore d'évaluation
- PRACTICA 8a DISOLUCIONES. PREPARACION Y UNIDADES DE CONCENTRACIÓNDocument8 pagesPRACTICA 8a DISOLUCIONES. PREPARACION Y UNIDADES DE CONCENTRACIÓNmecha crowPas encore d'évaluation
- Disolución de ConcentraciónDocument6 pagesDisolución de ConcentraciónNorwis GonzalezPas encore d'évaluation
- Unidades QuimicasDocument15 pagesUnidades Quimicasrussellcyber100% (2)
- Tema 8 - Soluciones PDFDocument30 pagesTema 8 - Soluciones PDFGabriela fajardoPas encore d'évaluation
- Estequimetria de SolucionesDocument30 pagesEstequimetria de SolucionesSara Rueda JPas encore d'évaluation
- EJERCICIOSDocument13 pagesEJERCICIOSDELMY ISABEL ÁLVAREZ VILLAFRANCOPas encore d'évaluation
- Definición de Molaridad y EjerciciosDocument6 pagesDefinición de Molaridad y EjerciciosGonzalo SandovalPas encore d'évaluation
- Raquel Física e Química 3º ESO A B DisoluciónsDocument4 pagesRaquel Física e Química 3º ESO A B DisoluciónsanarimiPas encore d'évaluation
- FRACCIÓN MOLAR Y PPMDocument2 pagesFRACCIÓN MOLAR Y PPMconsuelo buitragoPas encore d'évaluation
- Química 2°MB K. Palma 15 06 20Document5 pagesQuímica 2°MB K. Palma 15 06 20Luis fernando AriasPas encore d'évaluation
- Guía 8 Química 10ºDocument5 pagesGuía 8 Química 10ºyureina parra pinedoPas encore d'évaluation
- Taller SolucionesDocument13 pagesTaller SolucionesAdolf ReinhardtPas encore d'évaluation
- SESIÓN 3 ActualizadoDocument50 pagesSESIÓN 3 ActualizadoAdriana Flores DepazPas encore d'évaluation
- Unidades de Concentracion QuimicasDocument28 pagesUnidades de Concentracion QuimicasOMAR ROLANDO CORREA FELIPEPas encore d'évaluation
- NormalidadDocument21 pagesNormalidadEsbave BVPas encore d'évaluation
- PREPARARDocument87 pagesPREPARARGega123Pas encore d'évaluation
- Cuaderno de Estequiometría Ii Paso A Paso 1º Bachillerato Ies Zaidín Vergeles PDFDocument12 pagesCuaderno de Estequiometría Ii Paso A Paso 1º Bachillerato Ies Zaidín Vergeles PDFJose Antonio Vargas GonzalezPas encore d'évaluation
- Taller de Soluciones #1Document12 pagesTaller de Soluciones #1Danna Paternina Maussa100% (1)
- Actividades de AprendizajeDocument14 pagesActividades de Aprendizajeafrich81Pas encore d'évaluation
- EjrcicopDocument8 pagesEjrcicopNorwis GonzalezPas encore d'évaluation
- Unutr0100 - s6 Ordinario IIDocument30 pagesUnutr0100 - s6 Ordinario IIMILENA DANIELA TUTIVEN VELIZPas encore d'évaluation
- V Informe Laboratorio QuímicaDocument13 pagesV Informe Laboratorio QuímicaDHORA ALEXANDRA MENDOZA VITEPas encore d'évaluation
- Quimica II BTP-decimo - 6 y 7 de AgostoDocument4 pagesQuimica II BTP-decimo - 6 y 7 de AgostoAlejandra Sofia Cortes SandovalPas encore d'évaluation
- Informe Lab. Prepracion de SolucionesDocument18 pagesInforme Lab. Prepracion de Solucionesjuan sebastian avilaPas encore d'évaluation
- DisolucionesDocument39 pagesDisolucionesJimenaPas encore d'évaluation
- Estequiometría de DisolucionesDocument47 pagesEstequiometría de DisolucionesAllen50% (2)
- Ejercicios de Propiedades Coligativas) ) )Document20 pagesEjercicios de Propiedades Coligativas) ) )ELIAS BARGAS CRUZPas encore d'évaluation
- Unidad 2 Disoluciones IIDocument8 pagesUnidad 2 Disoluciones IIDK Samano RamosPas encore d'évaluation
- InformeeeeeeeeeDocument14 pagesInformeeeeeeeeemari aisabelPas encore d'évaluation
- Práctica 2 Preparación de DisolucionesDocument16 pagesPráctica 2 Preparación de DisolucionesDiana Laura Durán ChabléPas encore d'évaluation
- Guía de TP 5 Embrio 4 y 5 Semana Miembros RESUELTADocument6 pagesGuía de TP 5 Embrio 4 y 5 Semana Miembros RESUELTALuz Angela Moreno100% (1)
- Guía de TP 2 Embrio 1 y Semanas Segmentacion e Implantacion RESUELTADocument11 pagesGuía de TP 2 Embrio 1 y Semanas Segmentacion e Implantacion RESUELTALuz Angela MorenoPas encore d'évaluation
- Guía de TP 4 Embrio Gastrulación RESUELTADocument4 pagesGuía de TP 4 Embrio Gastrulación RESUELTALuz Angela MorenoPas encore d'évaluation
- Guía de TP 3 Embrio Placenta RESUELTADocument6 pagesGuía de TP 3 Embrio Placenta RESUELTALuz Angela MorenoPas encore d'évaluation
- GuÍa de TP 1 Embrio Gamatogenesis Ciclo Sex Fecundacion RESUELTADocument3 pagesGuÍa de TP 1 Embrio Gamatogenesis Ciclo Sex Fecundacion RESUELTALuz Angela MorenoPas encore d'évaluation
- Primer Turno 2P Primer Cuatrimestre 2018 ResueltoDocument8 pagesPrimer Turno 2P Primer Cuatrimestre 2018 ResueltoLuz Angela MorenoPas encore d'évaluation
- Biologia Celular Segundo P Turno 2P Primer Cuatrimestre 2018 ResueltoDocument8 pagesBiologia Celular Segundo P Turno 2P Primer Cuatrimestre 2018 ResueltoLuz Angela MorenoPas encore d'évaluation
- Ej Resueltos U2 Quimica UBA XXI 2018Document24 pagesEj Resueltos U2 Quimica UBA XXI 2018Luz Angela MorenoPas encore d'évaluation
- Curso de CBC de MatemáticasDocument103 pagesCurso de CBC de MatemáticasLuz Angela MorenoPas encore d'évaluation
- 1C 2018 1P 1T Con RespuestasDocument7 pages1C 2018 1P 1T Con RespuestasLuz Angela MorenoPas encore d'évaluation
- Actividad 2 - Unidad 6Document2 pagesActividad 2 - Unidad 6Luz Angela Moreno0% (1)
- Actividad 1 - Sesion 3 ICSE IntensivoDocument2 pagesActividad 1 - Sesion 3 ICSE IntensivoLuz Angela MorenoPas encore d'évaluation
- ICSE - Hoja de Ruta Intensivo 2018Document5 pagesICSE - Hoja de Ruta Intensivo 2018Luz Angela MorenoPas encore d'évaluation
- Biología Celular 2do Parcial 23-11-13 Tema 2 CON GrillaDocument5 pagesBiología Celular 2do Parcial 23-11-13 Tema 2 CON GrillaLuz Angela MorenoPas encore d'évaluation
- Practica 4 Rectificacion ContinúaDocument16 pagesPractica 4 Rectificacion ContinúaAlfredo TlapalePas encore d'évaluation
- Proyecto de LubricanteDocument20 pagesProyecto de LubricanteEdwin Alvaro67% (3)
- Las Renovables y Sus Nuevos Desafíos en El Mundo Post Pandemia - Nota Central E&N 20Document4 pagesLas Renovables y Sus Nuevos Desafíos en El Mundo Post Pandemia - Nota Central E&N 20Pablo Javier DehezaPas encore d'évaluation
- S1.2 Actividad Aplicativa 02 Caso Shell - ESPDocument7 pagesS1.2 Actividad Aplicativa 02 Caso Shell - ESPVladimir Noriega ChingPas encore d'évaluation
- FisurasDocument7 pagesFisurasCinthiaPas encore d'évaluation
- Elogio de La FilosofiaDocument4 pagesElogio de La FilosofiaPatricia KingsleighPas encore d'évaluation
- Columnas Con Empaque EstructuradoDocument22 pagesColumnas Con Empaque EstructuradoDiana Patricia Nieto PomaPas encore d'évaluation
- El Plan Nacional de Desarrollo 2021Document3 pagesEl Plan Nacional de Desarrollo 2021juan y Stephano tejenaPas encore d'évaluation
- Cuaderno 7 - Sibila NúñezDocument10 pagesCuaderno 7 - Sibila NúñezRaquel LeanizPas encore d'évaluation
- Estudio de Impacto AmbientalDocument12 pagesEstudio de Impacto AmbientalYersin Edison Machacuay CrispinPas encore d'évaluation
- Normas Tecnicas Dibujo GponDocument34 pagesNormas Tecnicas Dibujo GponAlexandra Almache100% (3)
- Laboratorio Tema 1 RLSDocument3 pagesLaboratorio Tema 1 RLSanahi tristanPas encore d'évaluation
- 1.5 - PPA Primera Etapa Ecosistema MarinoDocument7 pages1.5 - PPA Primera Etapa Ecosistema Marinojavier alexisPas encore d'évaluation
- Plan de Mejora de Los Aprendizajes de Tercer Grado 2021-81700Document17 pagesPlan de Mejora de Los Aprendizajes de Tercer Grado 2021-81700Victoria Gonzalez Martell100% (1)
- Ejercicio 4 SimceDocument6 pagesEjercicio 4 SimceMaría José Vergara Pinto De ArellanoPas encore d'évaluation
- Locomotoras en ArgentinaDocument19 pagesLocomotoras en ArgentinaSantiago CruzadoPas encore d'évaluation
- DIAZ MARTINEZ GABRIEL AZAEL 303 Teoría y Estructura CelularDocument31 pagesDIAZ MARTINEZ GABRIEL AZAEL 303 Teoría y Estructura CelularGabo MartzPas encore d'évaluation
- Reto 7-2Document1 pageReto 7-2LUIS ALFONSOPas encore d'évaluation
- Ejercicios CohesiónDocument6 pagesEjercicios CohesiónMarta Gallego medinaPas encore d'évaluation
- Trabajo Del OxigenoDocument10 pagesTrabajo Del OxigenoLuis Alberto Tello CequeroPas encore d'évaluation
- Autobús 7300-1Document2 pagesAutobús 7300-1Alberto Caín100% (1)
- Fisio 123Document7 pagesFisio 123Ximena SantosPas encore d'évaluation
- Cuadro SinopticoDocument2 pagesCuadro Sinopticoguadalupe del carmen gordillo lugo100% (1)
- Argumentacion - Articulo de OpinionDocument8 pagesArgumentacion - Articulo de Opinionyuliana elizabethPas encore d'évaluation
- Universidad San Pedro: Facultad de IngenieriaDocument95 pagesUniversidad San Pedro: Facultad de IngenieriaClinton Amancio OcañaPas encore d'évaluation
- PROYECTO VIDA SALUDABLE BUENA ALIMENTACION Williams LDocument32 pagesPROYECTO VIDA SALUDABLE BUENA ALIMENTACION Williams LRonald SolisPas encore d'évaluation
- 06-12-2020 120509 PM 5. Trabajo-EnergiaDocument3 pages06-12-2020 120509 PM 5. Trabajo-Energialexmar chinchay bermeoPas encore d'évaluation
- Piezómetros de Casa Grande IncompletoDocument12 pagesPiezómetros de Casa Grande IncompletoNEHEMIASPas encore d'évaluation
- Amor Sirenas FriasDocument247 pagesAmor Sirenas FriasLaura GandolfiPas encore d'évaluation
- Naga Brides 5 - Boomslang - Naomi LucasDocument323 pagesNaga Brides 5 - Boomslang - Naomi Lucasanalista2hospitalclinicoPas encore d'évaluation