Académique Documents
Professionnel Documents
Culture Documents
Informe de Laboratorio I
Transféré par
AlvaroFloresDescription originale:
Titre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Informe de Laboratorio I
Transféré par
AlvaroFloresDroits d'auteur :
Formats disponibles
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
LABORATORIO N1
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 1 de ...
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 2 de ...
LABORATORIO N1
RESUMEN
En el desarrollo del laboratorio experimental, se inici dando un concepto elemental de que la
energa no se crea ni se destruye solo se transforma.
Tambin durante el proceso de reconocimiento de los manmetros, se realizaran mediciones de
presin con un manmetros patrn y otro el manmetro regulador, y tambin se sacaran las
caractersticas geomtricas vinculadas con el volumen del compresor. Con estos datos y tomando en
cuenta las condiciones del ambiente presin, temperatura se pudo hallar la velocidad media
cuadrtica de las molculas, se calculo la capacidad de almacenamiento de aire para cada una de las
presiones ledas en el manmetro patrn.
Los resultados ms importantes calculados para la medicin de la presin son:
=503.424
m
s
1.759
m
s
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
LABORATORIO N1
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 3 de ...
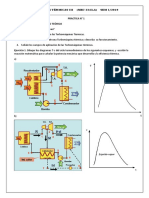
1. Introduccin:
Para llevar a cabo la prctica de laboratorio, se dio conocer el uso y manejo de los diferentes
instrumentos de medicin, en este caso instrumentos de medicin de presin.
En esta prctica experimental, se encarar la medicin de la presin, mediante los manmetros de
Bourdon. Con las lecturas de los manmetros patrn y regulador, se calcul la incertidumbre de datos
con las lecturas de presin.
Luego se intentara demostrar que la Termodinmica no solamente se basa en los fenmenos
macroscpicos, sino tambin que se encuentra ntimamente ligada con fenmenos microscpicos.
Antecedentes:
Partiendo del principio de que los primeros pasos a la disciplina de laboratorio tienen que tener una
clara percepcin de la instrumentacin, la adquisicin y el uso de datos basados en la medicin, es
que se encara este laboratorio. Esto permitir a los practicantes de laboratorio repasar y reforzar sus
tcnicas y conceptos de la medicin direccionados especialmente a las dimensiones termodinmicas
vinculadas con el sistema neumtico de laboratorio: compresor, red, vlvulas de regulacin y
manmetros.
Objetivos:
Conocer los instrumentos para medir presin ms comnmente empleados en la industria.
Reforzar la disciplina de medicin y tratamientos de datos experimentales a travs del manejo
de manmetros de Bourdon.
A travs de la definicin de presin como propiedad termodinmica, reforzar los fundamentos
introductorios de la termodinmica.
Consolidar, en el uso y cumplimiento de normas bsicas de elaboracin y presentacin de un
informe de laboratorio de la naturaleza disciplinaria de esta actividad.
Fundamento terico:
Propiedades termodinmicas.- En el clculo de cambios de energa que hayan ocurrido en un sistema
o sustancia operante, se debe expresar el comportamiento del sistema en funcin de caractersticas
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 4 de ...
LABORATORIO N1
descriptivas llamadas propiedades. Las propiedades macroscpicas son presin, temperatura,
densidad, volumen especfico, etc.
Estas propiedades se pueden clasificar en intensivas y extensivas. Las propiedades intensivas son
independientes de la masa, como la presin, temperatura, densidad, potencial elctrico; y las
propiedades extensivas dependen de la masa total del sistema, como el volumen total y la energa
total del sistema.
Las propiedades termodinmicas ms importantes o variables de estado, que nos permiten describir
un sistema, son el volumen, la temperatura y la presin.
Presin
Definicin macroscpica.- Desde el punto de vista tradicional y macroscpico se define la presin
como el cociente entre la fuerza aplicada a un rea determinada, es decir:
F
A
[Pa]
(1.1)
Es una cantidad escalar, que segn el Sistema Internacional de Unidades se mide en Pascales.
Definicin segn la teora cintica.- La presin en un gas, la produce el impacto de un gran nmero
de molculas del gas sobre la superficie considerada. Segn la teora cintica de los gases, el
volumen de una molcula es despreciable, las fuerzas de interaccin entre las molculas son tambin
despreciables, y se admite que dichas molculas son esferas rgidas que chocan elsticamente entre s
y contra las paredes del recipiente que contiene al gas.
Velocidad media cuadrtica.- Aplicando el principio de conservacin de cantidad de movimiento
lineal en una molcula A y en la direccin del eje Y, se tiene que:
mv2 mv1 m A v A1 y (v A 2 y )
(1.2)
Como la colisin es elstica, las dos velocidades del segundo miembro de la ecuacin son iguales,
entonces se tiene que la cantidad de movimiento para cada molcula es:
p 2mv y
[Kg*m/s]
(1.3)
El tiempo que tarda una molcula en llegar a la pared opuesta y rebotar con dicha pared es:
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 5 de ...
LABORATORIO N1
2L
vy
[s]
(1.4)
Dividiendo la variacin de cantidad de movimiento entre el tiempo, se tiene que la fuerza de impacto
producida por las molculas es:
N
m N
Nm
F v 2 yi
L i 1
L
iy
i 1
N
[N]
(1.5)
Aplicando la definicin de presin se tiene:
F Nm 2
3 v y [ Pa]
A
L
(1.6)
Para las velocidades se tiene que:
2
v 2 vx v y vz
(1.7)
Como los movimientos de las molculas son completamente al azar, se puede decir que:
vx v y vz
(1.8)
Combinando las ecuaciones (1.6) y (1.7), obtenemos que:
2
vy
v2
3
(1.9)
De donde finalmente se tiene que:
Nmv 2 N v 2
[ Pa]
3V
3
(1.10)
Dnde: N es el nmero de molculas, es la densidad del gas, y v se conoce como velocidad media
cuadrtica de las molculas.
Presin atmosfrica, manomtrica y absoluta.La presin atmosfrica se debe a la presin que ejerce al aire atmosfrico sobre nosotros. Se puede
medir la presin atmosfrica utilizando una columna de mercurio, segn el experimento realizado por
Torricelli. A nivel del mar, se observa que el mercurio alcanza una altura de 760 mm respecto al nivel
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
LABORATORIO N1
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 6 de ...
de mercurio en el recipiente; por esta razn se dice que la presin atmosfrica a nivel del mar es de
760 mm Hg.
Sin embargo, la presin atmosfrica, vara de acuerdo a la altura respecto al nivel del mar de cada
lugar, ya que a mayor altura existe una menor cantidad de aire, y por lo tanto, a mayor altura ste
ejerce una menor presin. En Oruro, utilizando el mismo experimento de Torricelli, la columna de
mercurio tiene una altura aproximada de 486 mm, equivalente a 0,64 atm.
La presin atmosfrica se mide con aparatos denominados barmetros.
La presin manomtrica, es aquella que se mide con los manmetros, y es una presin relativa; es
decir que la presin manomtrica indica el valor en que la presin se encuentra por encima (o por
debajo) de la presin atmosfrica local.
La presin absoluta es la suma de las presiones atmosfrica y manomtrica
Figura. Relacin de los diferentes tipos de presin
Manmetros de Bourdon.- Se trata de un tipo de manmetro aneroide conocido como instrumento de
un solo tubo. El fluido entra al aparato por la conexin roscada. A medida que aumenta la presin, el
tubo de la seccin elptica, tiende a enderezarse, y el extremo que est ms prximo al sistema
articulado se mueve hacia la derecha. Este dispositivo produce la rotacin del sector de engrane, el
cual mueve un pin unido a la aguja indicadora. Todo el mecanismo est, desde luego, encerrado en
una caja, y un disco graduado sobre el cual se lee la presin, se halla colocado bajo el ndice de la
aguja.
(1) Tubo de Bourdon
(2) Soporte fijo del tubo
(3) Extremo mvil del tubo
(4) Corredera
(5) Biela
(6) Engranaje
(7) Aguja indicadora
(8) Escala calibrada
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
LABORATORIO N1
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 7 de ...
Figura Partes de un manmetro de Bourdon
Barmetros.Definicin y clasificacin.- Un barmetro es un instrumento que mide la presin atmosfrica. La
presin atmosfrica es el peso por unidad de superficie ejercida por la atmsfera.
Los primeros barmetros estaban formados por una columna de lquido encerrada en un tubo cuya
parte superior est cerrada. El peso de la columna de lquido compensa exactamente el peso de la
atmsfera. Los primeros barmetros fueron realizados por el fsico y matemtico italiano Evangelista
Torricelli en el siglo XVII. La presin atmosfrica equivale a la altura de una columna de agua de
unos 10 m de altura. En los barmetros de mercurio, cuya densidad es 13.6 veces mayor que la del
agua, la columna de mercurio sostenida por la presin atmosfrica al nivel del mar en un da
despejado es de aproximadamente unos 760 mm.
Los barmetros son instrumentos fundamentales para medir el estado de la atmsfera y realizar
predicciones meteorolgicas. Las altas presiones se corresponden con buen tiempo mientras que las
bajas presiones son indicadores de regiones de tormentas y borrascas.
Los barmetros se clasifican en: barmetros de mercurio y barmetros metlicos.
Barmetros de mercurio.- Se basan en le dispositivo usado por Torricelli para sus experimentaciones
los ms usados son los de cubeta, de sifn y el de fortn.
- Barmetro de cubeta: Es un simple tubo de Torricelli T con su cubeta C aplicado sobre una tabla
provista de una escala graduada, cuyos cero correspondiente al nivel del mercurio en la cubeta. Este
barmetro, con algunos perfeccionamientos, que lo hacen ms preciso, se llama barmetro normal
- Barmetro de sifn: Ideado por Pascal, consiste en un tubo encorvado, de dos ramas desiguales, la
mayor est cerrada y abierta la menor, pero tapada con una gamuza a travs de la cual se ejerce la
presin atmosfrica. La altura de la columna mercurial, que hace equilibrio a la presin atmosfrica,
es la distancia vertical de los dos niveles.
- Barmetro de fortn: El fondo de la cubeta est formado por una gamuza, que un tornillo puede
alzar o bajar en el momento de la observacin se corre el tornillo hasta que el nivel del mercurio
toque la punta del marfil que seala el cero de la graduacin. En la parte superior del tubo existen
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
LABORATORIO N1
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 8 de ...
ventanas longitudinales horadadas en la cubierta metlica que protege el tubo baromtrico a travs
de las cuales se observa el nivel del mercurio. En los lados de dichas ventanas estn sealadas las
divisiones de la escala a lo largo de la cual puede correr en nonio. Una superficie cardanica, sobre un
trpode permite dar al aparato una posicin rigurosamente vertical.
B) Barmetros metlicos.- Llamados tambin aneroides, son instrumentos con los cuales se miden las
presiones por deformaciones de recipiente metlicos delgados en los que se ha hecho un vaco
parcial. Son muy prcticos pero no tan sensibles. Los ms conocidos son barmetros de Bourdon, Vidi
y Registrador de Richard.
- Barmetro metlico de Bourdon: Se compone de un tubo de latn delgado de seccin elptica y
curvada en forma de crculo incompleto. Uno de sus extremos esta fijo a la caja el otro mediante un
sistema de palancas accionan una aguja que se mueve sobre un cuadrante graduado. Si aumenta la
presin, el tubo se cierra, y si disminuye, se abre. Estos movimientos son amplificados por las
palancas y transmitidos por la cremallera y pin a la aguja indicadora. El barmetro de Bourdon se
grada por comparacin con los barmetros de mercurio.
- Barmetro de Vidi: Tanto el barmetro de Vidi como el de Bourdon son recipientes de paredes
delgadas en los que se ha hecho un vaco parcial. El de Bourdon es un tubo, el De Vidi es un disco
acanalado. Las presiones que se ejercen sobre la pared superior se amplifican con palancas y se
transmiten con engranajes a la aguja indicadora.
- Barmetro Registradores de Richard o bargrafos: En las estaciones meteorolgicas se usan mucho
los bargrafos para llevar la inscripcin continuada en bandas diarias o hebdomadarias, de las
variaciones de las presiones atmosfricas.
Desarrollo monogrfico de la primera ley de la termodinmica (cuestionario)
Introduccin.En la siguiente dcada asistir a la progresiva puesta en prctica de los hallazgos de la ciencia y los
experimentos, con dos extensos grupos de aplicaciones: el de la electricidad y el del calor.
Y al mismo tiempo tienen lugar dos grandes sntesis cientficas: primero la del calor y la energa, que
darn lugar a la ciencia de la termodinmica, y despus la de la electricidad, el magnetismo y la luz,
que hallarn explicacin conjunta con la teora electromagntica.
Ambas novedades iniciarn la decadencia de la teora newtoniana, de interpretacin mecnica del
universo y la naturaleza, ya que se encontrar con que no puede explicarlo todo. Habr que esperar,
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
LABORATORIO N1
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 9 de ...
no obstante, a que la dcada de 1880 imprima los cambios que sern ya irreversibles en la fsica, una
vez que la etapa clsica alcance el ms alto grado de positivismo, es decir, de elevacin de lo
comprobable a la mxima categora del conocimiento y, adems, de la generalizacin de la
interpretacin mecnica de la realidad.
Resumen.En esta investigacin tomamos las referencias histricas del proceso de aceptacin de la primera ley
de la termodinmica a travs de los hechos cientficos y estudios experimentales, para que al mismo
se definan las variables de calor, trabajo y energa interna para as poder determinar este principio
de conservacin de la energa en sistemas termodinmicos abiertos y cerrados.
Descripcin del Problema.Con los impulsos de electricidad y del calor, y por acrecentar las ideas de estas se formaron varias
interrogantes acerca de las mquinas de vapor por mejorarlas y determinar su eficiencia para un
mejor uso.
Las ideas de la poca sirvieron como apoyo a hechos cientficos trascendentales y diseminaron varios
aspectos a tratar como el calor y la energa y por la relacin de estas a travs de datos recogidos de
manera experimental se acentuaron en encontrar una ley que justificar este fenmeno.
Formulacin del Problema.
Problema General
En qu fundamentos experimentales y tericos se basa la primera ley de la termodinmica para
determinar las variaciones de calor, trabajo y energa para un sistema termodinmico?
Problemas Especficos
Cmo se determin la relacin de las definiciones y/o aplicaciones de calor, trabajo y energa
en la primera ley de la termodinmica?
Cmo se logr hallar el equivalente mecnico del calor y de qu manera influye sobre esta ley?
Los objetivos de la investigacin
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
LABORATORIO N1
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 10 de ...
Objetivo General
Relacionar los datos experimentales y tericos en que se basan sus principales aportadores para
sintetizar la ley de la conservacin de energa en un sistema termodinmico.
Objetivos Especficos
Denotar las definiciones de calor, trabajo y energa en el desarrollo previo de la primera ley de
la termodinmica.
Manifestar al equivalente mecnico del calor como un indicador considerable sobre el
desarrollo de esta ley.
El principio conocido como la ley de la conservacin de la energa su importancia hasta hoy en da
por su aplicabilidad a la suministracin de energa a travs del calor o de la electricidad.
Su uso se hizo primordial para el creciente avance cientfico del entorno en el que se encontraba para
ayudar a encontrar otras formas de llevar energa a travs de otras mquinas que recibieran calor
dndole lugar a los ferrocarriles de ese entonces como orgullo de sus naciones por encontrar un
sistema an ms eficiente.
Marco terico.La primera ley de la termodinmica relaciona el trabajo y el calor transferido intercambiado en un
sistema a travs de una nueva variable termodinmica, la energa interna.
DICHA ENERGA NI SE CREA NI SE DESTRUYE, SLO SE TRANSFORMA.
Empezaremos conceptualizando los siguientes puntos:
Qu es la energa interna de un cuerpo o sistema
El primer principio de la termodinmica
El concepto de trabajo termodinmico
Cmo extraer informacin til de las grficas presin - volumen
Cules son los principales tipos de procesos termodinmicos
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
LABORATORIO N1
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 11 de ...
Energa interna.La energa interna de un sistema es una caracterizacin macroscpica de la energa microscpica de
todas las partculas que lo componen. Un sistema est formado por gran cantidad de partculas en
movimiento. Cada una de ellas posee:
energa cintica, por el hecho de encontrarse a una determinada velocidad
energa potencial gravitatoria, por el hecho de encontrarse en determinadas posiciones unas
respecto de otras
energa potencial elstica, por el hecho vibrar en el interior del sistema
Existen, adems, otros tipos de energa asociadas a las partculas microscpicas tales como
la energa qumica o la nuclear.
En definitiva, en el interior de un sistema conviven distintos tipos de energa, asociadas a las
partculas microscpicas que los componen y que forman su energa interna.
En termodinmica la Energa Interna de un sistema ( U ) es una variable de estado. Representa la
suma de todas las energas de las partculas microscpicas que componen el sistema. Su unidad de
medida en el Sistema Internacional es el julio ( J ).
Observa que el valor de U es la suma de todas las energas del interior del sistema, por lo que no se
incluye ni la energa cintica global ni la energa potencial gravitatoria global ni la energa potencial
elstica global del mismo.
Energa interna en gases ideales.En los gases ideales, la energa interna se puede aproximar a la energa cintica media de las
partculas que lo componen. La expresin que se recoge ms abajo permite determinar su variacin
en un proceso cuyo volumen permanece constante (proceso isocrico).
La energa interna de un gas ideal depende nicamente de la temperatura que tenga el gas.
La variacin de energa interna que experimenta un gas al cambiar de temperatura viene dada por:
U=mcvT
Dnde:
U : Incremento de energa interna del gas ( U = Ufinal - Uinicial ). Su unidad de medida en el
Sistema Internacional es el julio ( J )
m : Masa. Cantidad de gas considerada. Su unidad de medida en el Sistema Internacional es el
kilogramo ( kg )
cv : Calor especfico a volumen constante. Representa la facilidad que el gas tiene para variar su
temperatura cuando intercambia calor con el entorno. Su unidad de medida en el Sistema
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
LABORATORIO N1
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 12 de ...
Internacional es el julio por kilogramo por kelvin ( J/kgK ) aunque tambin se usa con frecuencia la
calora por gramo y por grado centgrado ( cal/gC ). Cuando conocemos el nmero de moles de
sustancia en lugar de su peso (nos dan m en moles), podemos usar el calor especfico molar que se
suele especificar en J/molK cal/gC
T : Variacin de temperatura. Viene determinada por la diferencia entre la temperatura inicial
y la final T = Tf -Ti . Su unidad de medida en el Sistema Internacional es el kelvin ( K ) aunque
tambin se suele usar el grado centgrado o Celsius ( C )
La expresin anterior nos da un mtodo operativo para medir la variacin de energa interna en un
sistema gaseoso, proporcional al cambio de temperatura. Para llegar a ella aplicamos la primera ley
de la termodinmica a un proceso a volumen constante (denominado isocrico) como podrs
comprobar ms abajo.
Primera ley de la termodinmica
La primera ley de la termodinmica establece una relacin entre la energa interna del sistema y la
energa que intercambia con el entorno en forma de calor o trabajo.
La primera ley de la termodinmica determina que la energa interna de un sistema aumenta cuando
se le transfiere calor o se realiza un trabajo sobre l. Su expresin depende del criterio de signos para
sistemas termodinmicos elegido:
Criterio IUPAC
Criterio tradicional
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
LABORATORIO N1
Se considera positivo aquello que
aumenta la energa interna del sistema,
o lo que es lo mismo, el trabajo
recibido o el calor absorbido.
U=Q+W
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 13 de ...
Se
considera
positivo
el
calor
absorbido y el trabajo que realiza el
sistema sobre el entorno.
U=QW
Dnde:
U : Incremento de energa interna del sistema ( U = Ufinal - Uinicial ). Su unidad de medida en el
Sistema Internacional es el julio ( J )
Q : Calor intercambiado por el sistema con el entorno. Su unidad de medida en el Sistema
Internacional es el julio ( J ), aunque tambin se suele usar la calora ( cal ). 1 cal = 4.184 J
W: Trabajo intercambiado por el sistema con el entorno. Su unidad de medida en el Sistema
Internacional es el julio ( J )
Al igual que todos los principios de la termodinmica, el primer principio se basa en sistemas en
equilibrio. Por otro lado, es probable que hayas odo ms de una vez que la energa ni se crea ni se
destruye, solo se transforma. Se trata del principio general de conservacin de la energa. Pues bien,
la primera ley de la termodinmica es la aplicacin a procesos trmicos de este principio. En un
sistema aislado, en el que no se intercambia energa con el exterior, nos queda:
U=0
El universo en su totalidad se podra considerar un sistema aislado, y por tanto, su energa total
permanece constante. Finalmente observa que, al ser una funcin de estado, la diferencia de energa
interna solo depende de los estados inicial y final, U = Uf - U, y no del camino que haya seguido el
proceso. El calor y el trabajo, en cambio, no son funciones de estado, por lo que sus valores dependen
del camino seguido por el proceso. Esto quedar bien ilustrado en los diagramas presin volumen para gases ideales, como vers ms abajo.
Trabajo termodinmico.-
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
LABORATORIO N1
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 14 de ...
La energa interna de un cuerpo no incluye la energa cintica global o potencial mecnica del
mismo, tal y como sealamos anteriormente. Es por ello que no se ve alterada con el trabajo
mecnico. En termodinmica nos interesa otro tipo de trabajo, capaz de variar la energa interna de
los sistemas. Se trata del trabajo termodinmico.
Se denomina trabajo termodinmico a la transferencia de energa entre el sistema y el entorno por
mtodos que no dependen de la diferencia de temperaturas entre ambos. Es capaz de variar la energa
interna del sistema.
Normalmente el trabajo termodinmico est asociado al movimiento de alguna parte del entorno, y
resulta indiferente para su estudio si el sistema en s est en movimiento o en reposo. Por ejemplo,
cuando calientas un gas ideal en un recipiente con un pistn mvil en su parte superior, las partculas
adquieren mayor energa cintica. Este aumento en la energa de las partculas se traduce en un
aumento de la energa interna del sistema que, a su vez, puede traducirse en un desplazamiento del
pistn. El estudio de este proceso desde el punto de vista de la termodinmica es independiente de si
el sistema, como un todo, se encuentra en reposo o en movimiento, que sera una cuestin de
mecnica. Sin embargo s es cierto que, tal y como ocurre en una mquina de vapor, la energa de
dicho trabajo termodinmico puede transformarse en energa mecnica.
Trabajo termodinmico presin volumen.El trabajo termodinmico ms habitual tiene lugar cuando un sistema se comprime o se expande y se
denomina trabajo presin - volumen (p - v). En este nivel educativo estudiaremos su expresin en
procesos isobricos o isobaros, que son aquellos que se desarrollan a presin constante.
El trabajo presin - volumen realizado por un sistema que se comprime o se expande a presin
constante viene dado por la expresin:
Dnde:
Criterio IUPAC
Criterio tradicional
Wsistema=pV
Wsistema=pV
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
LABORATORIO N1
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 15 de ...
Wsistema: Trabajo intercambiado por el sistema con el entorno. Su unidad de medida en el Sistema
Internacional es el julio ( J )
p : Presin. Su unidad de medida en el Sistema Internacional es el pascal (Pa ) aunque tambin
se suele usar la atmsfera ( atm ). 1 atm = 101325 Pa
V : Variacin de volumen ( V=Vf - Vi ). Su unidad de medida en el Sistema Internacional es
metro cbico ( m3 ) aunque tambin se suele usar el litro ( l o L ). 1 L = 1 dm3 = 10-3 m3
Presta atencin al signo del trabajo, realizado por el sistema, en funcin del criterio de signos.
Criterio IUPAC
Compresin Vi > Vf Wsistema > 0 El trabajo lo recibe el sistema del entorno
Aumenta la energa interna del sistema U > 0
Expansin: Vi < Vf Wsistema < 0 El trabajo lo cede el sistema al entorno Disminuye
la energa interna del sistema U < 0
Criterio tradicional
Compresin Vi > Vf Wsistema < 0 El trabajo lo recibe el sistema del entorno
Aumenta la energa interna del sistema U > 0
Expansin: Vi < Vf Wsistema > 0 El trabajo lo cede el sistema al entorno Disminuye
la energa interna del sistema U < 0
Grficas presin - volumen
En el estudio del trabajo realizado por un sistema termodinmico con gases ideales es bastante
comn el uso de diagramas presin - volumen ( p - v ).
Se representa el volumen V en el eje x
Se representa la presin p en el eje y
Se representa el proceso mediante una lnea que une los puntos ( V ,p ) por los que este pasa
entre el punto inicial ( Vi ,pi ) y el final ( Vf ,pf )
Utilizaremos una flecha sobre la lnea para indicar el sentido de la transformacin
termodinmica
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
LABORATORIO N1
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 16 de ...
Las grficas presin volumen nos sirven para calcular el trabajo realizado en un proceso en el que la
presin no necesariamente tenga que ser constante.
El trabajo realizado por un sistema termodinmico coincide numricamente con el rea encerrada
bajo la grfica presin - volumen entre los valores de volumen inicial Vi y final Vf. El sentido de la
flecha sobre la lnea indica el signo del trabajo, segn el criterio elegido
Criterio IUPAC
Criterio tradicional
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
LABORATORIO N1
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 17 de ...
Observa que en un proceso cclico el rea encerrada por la curva se puede calcular como la resta
entre el valor del rea encerrada por la curva cuando el proceso se encuentra aumentando su
volumen (en expansin) y el valor del rea encerrada por la curva cuando el proceso se encuentra
disminuyendo su volumen (en compresin), tal y como puede verse en la siguiente figura.
Interpretacin de grficas de gases ideales.Los diagramas presin volumen aportan gran cantidad de informacin, adems de servir para el
clculo del trabajo realizado por el sistema. Vamos a particularizar en el caso de los gases ideales
por ser su ecuacin de estado pV=nRT la ms sencilla.
Cada punto de la grfica marca un estado del sistema. Las variables de estado para una
determinada cantidad de gas, son la presin, el volumen y la temperatura. Un punto en la grfica p v tiene una nica temperatura asociada, segn la expresin pV=nRTT=pVnR , y por tanto cada
punto marca un estado
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
LABORATORIO N1
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 18 de ...
Se puede demostrar que la energa interna U de un gas ideal depende nicamente de su
temperatura. As, a cada punto en la grfica se le asocia, adems de una temperatura, una energa
interna.
Se denominan isotermas a las lneas que representan igual temperatura. Siguen la
expresin piVi=nRTi=ctte. y corresponden con el conjunto de puntos que tienen, adems, igual
energa interna
Trabajo y calor dependen, en general, del camino seguido para llegar a un punto a otro de la
grfica, de la transformacin.
En un proceso cclico, la temperatura inicial y final es la misma, por tanto la energa interna del
sistema no vara U=UfUi=0 , independientemente del camino seguido. Sin embargo recuerda que
calor y trabajo intercambiados en el proceso no son funciones de estado y s dependen, en general,
del camino
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 19 de ...
LABORATORIO N1
Para determinar el incremento de energa interna U en cualquier tipo de proceso, se utiliza la
expresin U=mcvT . De dnde viene? En un proceso a volumen constante (denominado proceso
isocrico) no se realiza trabajo, pues el rea bajo la curva del proceso es 0 y, en consecuencia, la
primera ley de la termodinmica queda:
U=Q
El calor recibido por un gas a volumen constante viene dado por la expresin Q=mcvT.
Combinando
las
dos
expresiones
anteriores,
nos
queda
justamente
la
expresin
buscada U=mcvT.
Observa que, al depender el incremento de energa interna nicamente de los estados inicial y final
(de la temperatura inicial y final), el valor obtenido ser el mismo siempre que nos desplacemos a la
misma isoterma, independientemente del camino seguido. Esto significa que, aunque el valor del
incremento de energa se haya obtenido para un proceso a volumen constante, tambin ser vlido
para cualquier proceso que se desplace a la misma isoterma. Puedes comprobarlo en este ejercicio.
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 20 de ...
LABORATORIO N1
Como puedes observar en la figura si conocemos el incremento de energa interna en un proceso a
volumen constante (proceso A), que experimentalmente es sencillo de determinar, se puede aplicar la
primera ley de la termodinmica para conocer el trabajo el calor de otro proceso (proceso B) que
termine en el mismo estado, o lo que es lo mismo, en la misma lnea isoterma.
Tipos de procesos
Los procesos termodinmicos se suelen clasificar en:
Q = 0 Procesos adiabticos. Aquellos en los que el sistema no intercambia calor. Por ejemplo, al
usar un ambientador o desodorante en aerosol se produce un proceso casi adiabtico. En estos
casos U=W ( U=W , segn criterio de signos elegido), es decir, el trabajo es funcin de estado.
Cuando comprimimos o expandimos un gas en un proceso en el que no se intercambia calor, variamos
su energa interna y, por tanto, su temperatura
V = cte. Procesos isocricos. Aquellos en los que el volumen permanece constante. Por ejemplo,
una botella de champn metida en un recipiente con hielo. Al no haber variacin de volumen, el
trabajo del sistema es cero. Wsistema=0 . Siguiendo el primer principio, nos queda U=Q , es decir,
el calor es una funcin de estado. Esto significa que la nica forma de variar la energa interna en un
proceso en el que no se vara el volumen es a travs del intercambio de calor
p = cte. Procesos isobricos. Aquellos en los que la presin permanece constante. Por ejemplo,
las
reacciones
qumicas.
El
valor
del
trabajo
se
calcula
partir
de
la
expresin Wsistema=pV Wsistema=pV , segn criterio IUPAC o tradicional respectivamente
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
LABORATORIO N1
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 21 de ...
Por otro lado, este tipo de procesos permiten definir una nueva variable de estado, la entalpa H. De
manera que:
U=Q+WU=QW}U2U1=Qp(V2V1)Q=U2+pV2(U1+pV1)=H2H1=H
Donde, como ves, la expresin de la entalpa no depende del criterio de signos seguido para llegar a
ella
T = cte. Procesos isotrmicos. Aquellos en los que la temperatura permanece constante. Por
ejemplo, un recipiente con gas y un pistn en la zona superior, sumergido en un depsito calorfico a
temperatura constante. Al ser la temperatura constante, la variacin de energa interna es
cero U=0 y en consecuencia:
U=Q+WU=QW}0=Q+W0=QW}Q=WQ=W}
Donde se han tenido en cuenta los dos criterios de signos posibles. Observa que el proceso se realiza
sobre una nica isoterma:
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 22 de ...
LABORATORIO N1
2. Metodologa:
El presente trabajo fue realizado el da jueves 13 de agosto del 2015, por un grupo de diez y
seis universitarios con el asesoramiento del Ing. Edgar Pearanda M., en el laboratorio de
Mquinas trmicas aprovechando la red neumtica del laboratorio de hidrulicas.
Equipo, material e instrumentos utilizados:
Se usaran dos tipos de manmetros de Bourdn; uno que corresponde a un regulador de presin
(instrumento) y otro propiamente dicho (patrn o el de lectura verdadera), que puede medir sobre
presiones y depresiones (vacuometro).
Los equipos y materiales que se usaran en el laboratorio son:
o
o
o
o
o
o
o
Compresor.
Red neumtica.
Regulador de presin.
Mangueras de presin.
Conector Cnico.
Manmetro vacumetro.
Cinta Mtrica
A continuacin damos a conocer las fichas tcnicas de los instrumentos, sistemas o equipos
que se usaron en la realizacin del presente laboratorio
Fichas tcnicas.
Regulador de presin
Accesorios
Ficha tcnica del medidor de
flujo:
Fig.
MATERIAL
Nombre del instrumento
Tipo
Marca del instrumento
Industria
Color
Unidad de medicin
Rango de medicin
Sensibilidad
Incertidumbre
DESCRIPCIN
Medidor de flujo
Diafragma
East sea
Naranja (carcasa)
-------------------------------------------------------------------------
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 23 de ...
LABORATORIO N1
Ficha tcnica del Manmetro:
MATERIAL
Nombre del instrumento
Tipo
Marca del instrumento
Industria
Color
Unidad de medicin
Rango de medicin
Sensibilidad
Incertidumbre
DESCRIPCIN
Manmetro
Bourdn
Ashcroft
USA
Plateado (carcasa)
Psi
0 - 30
0.5
0.25
Fig.
Ficha tcnica de la Manguera de presin:
MATERIAL
Nombre del instrumento
Tipo
Marca del instrumento
Industria
Color
Unidad de medicin
Rango de medicin
Sensibilidad
Incertidumbre
DESCRIPCIN
Manguera de presin
-----------------Argentina
Verde
--------------------------------------------------------------------
Fig.
Ficha tcnica del manmetro vacuo metro:
Nombre del Manmetro vacuometro
instrument
o
Tipo
Vacuometro
Fig.
Marca
---------------------------
industria
Color
Unidad
de
medicin
Alcance
Mnimo
Alcance
Mximo
Sensibilidad
Incertidumbre
USA
Negro (carcasa)
In Hg
Cm Hg
Psi
kPa
30
70
10
0.5
0.5
0.5
0.5
0.25
0.25
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 24 de ...
LABORATORIO N1
Ficha tcnica del compresor alternativo:
Fig.
MATERIAL
Nombre del instrumento
Tipo
Marca del instrumento
Industria
Color
Unidad de medicin
DESCRIPCIN
Compresor alternativo
Envase
Shwenninen
Alemn
Guindo
Longitud
Permetro
36 in
37in
MATERIAL
Nombre del instrumento
Tipo
Marca del instrumento
Industria
Color
Unidad de medicin
Rango de medicin
Sensibilidad
Incertidumbre
DESCRIPCIN
Cinta mtrica
kg
cm2
Ficha tcnica de la cinta mtrica
Fig.
Montaje del equipo:
Wyteface
USA
Plateado (carcasa)
Inch pies
0 50
0.125 in.
0.0625 in.
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 25 de ...
LABORATORIO N1
Descripcin del experimento:
- Inicialmente se realiz un reconocimiento de los manmetros y del tipo de compresor sacando una
ficha tcnica de cada uno de los mencionados.
- Despus se hizo la verificacin de las vlvulas abriendo la vlvula del compresor.
- Posteriormente se procedi a regular la presin y posteriormente a conectar el manmetro patrn a
la red neumtica.
- Se hicieron las mediciones de las lecturas de presin del manmetro patrn como es del manmetro
regulador.
- Se procedi al cierre de las vlvulas, el despresurizado de las mangueras y retirado de las
mangueras.
- Se hicieron las mediciones del dimetro, longitud del compresor con la ayuda de una cinta mtrica.
- Finalmente se procedi al recojo de los instrumentos utilizados.
Registro de datos:
PATRON
PATRON
REGULADOR
psi( 0.5)
kPa ( 2.5)
psi ( 0.25)
2.5
20
3.5
35
6.5
45
6.5
45
6.5
Tabla 2.4: resultados
obtenidos de la
velocidad media
cuadrtica
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
LABORATORIO N1
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 26 de ...
Clculos:
Aplicando la teora de propagacin de la incertidumbre calcular la velocidad media cuadrtica de las
molculas de aire.
Datos:
T= temperatura
T 7 0C 0.10 C
Transformando a grados kelvin
T 280.150K 273.250K
R= Constante del aire
R 287 J
0
Kg* K
P=presin del sistema
P 2.5 bar
Z= altura de la ciudad de Oruro
Z= 3706 (m)
3P
(2.1)
P
R *T
.. (2.2)
T0 T prom
z
. (2.3)
g
*T
Patm P
T *Z
.... (2.4)
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 27 de ...
LABORATORIO N1
Patm Patms Pman
. (2.5)
Usando el mtodo de casos frecuentes hallamos las siguientes ecuaciones
2
1
P
T
P
2
R *T
R *T
(2.6)
3* P
3
P 2
v
2
3
4
*
*
p
4
*
.. (2.7)
Hallando la presin atmosfrica en Oruro
De la ecuacin (2.3):
T0 T prom
z
0
293.15 280.15
3.507 * 10 3 K
m
3706
De la ecuacin (2.4):
g
*T
T *Z
Patm P
293.15 (3.507 *10 3 * 3706)
101.325
293.15
9.81
287*3.507*103
65.121 kPa 65127.242 N
Transformando la presin manomtrica a pascales
5kPa *1000 Pa
5000 Pa
1kPa
P1
Transformando la incertidumbre
P1
0.25kPa *1000 Pa
250 Pa
1kPa
Los resultados faltantes se muestran en la siguiente tabla:
Manmetro PATRON
P kPa 0.25 kPa
Tabla 2.1:
transformacin de
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 28 de ...
LABORATORIO N1
P N
1
2
3
4
5
5 0.25
20 0.25
35 0.25
45 0.25
45 0.25
m2
250 N m
2
5000 250
20000 250
35000 250
45000 250
45000 250
Obteniendo la presin absoluta
De la ecuacin (2.5) para la presin 1
Patm Patms Pman 65127.242 5000 70127.242 N
N
o
1
2
3
4
5
P N
PATRON
m2
250 N m
Patm Patms Pman
5000 250
20000 250
35000 250
45000 250
45000 250
70127.242
85127.242
100127.242
110127.242
110127.242
Tabla 2.2:
presin
Calculando la densidad y la velocidad media cuadrtica
Obteniendo la densidad para cada presin que se ejerce en el compresor
De la ecuacin (2.2) para la densidad 1
P
70127.242
0.8722 Kg 2
m
R * T 287 * 280.15
De la ecuacin (2.6)
2
1
P
P
T
R
*
T
R
*
T2
1
70127.242
2
0.12 0.003
250
2
287 * 280.15
287 * 28015
PATRON
Tabla 2.3:
resultados
obtenidos de la
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 29 de ...
LABORATORIO N1
N
o
1
2
3
4
5
P
Kg 3 Kg 3
m
m
R *T
0.872 0.003
1.058 0.003
1.245 0.003
1.369 0.003
1.369 0.003
De la ecuacin (2.1) para la velocidad 1
v
3P
3 * 70127.242
497.185 m
s
0.872
De la ecuacin (2.7)
3* P
3
P 2
v
2
3
4
*
*
p
4
*
3 * 70127.242
2
2
* 250
* 0.003 1.217 m s
3
4 * 0.872 * 70127.242
4 * 0.872
PATRON
N
o
1
2
3
4
5
3P
v m v m
s
s
491.185 1.217
491.306 1.217
491.193 1.217
491.254 1.217
491.254 1.217
Tabla 2.4: resultados
obtenidos de la
velocidad media
cuadrtica
2.Cual es la capacidad de almacenamiento del compresor del laboratorio para cada una de las
presiones ledas en el manmetro patrn (kPa)?
Convirtiendo unidades de la tabla .
Usando los siguientes factores de conversin convertimos las unidades a [m]
1 [ft] = 0.3048 [m]
1 [in] = 0.0254 [m]
1 [mm] = 0.001 [m]
MEDIDAS DEL COMPRESOR
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
LABORATORIO N1
Longitud
Permetro
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 30 de ...
36.0000 0.0625 [in]
37.0000 0.0625 [in]
0.9144000 0.0015875 [m]
0.9398000 0.0015875 [m]
Tabla 2.4: resultados
obtenidos de la
velocidad media
cuadrtica
D=
Perimetro
( )
V=
D L
()
4
Para el clculo de la incertidumbre usaremos la siguiente ecuacin.
V=
2
2
V
V
D +
L (.)
D
L
)(
Hallando el dimetro del compresor y la incertidumbre de la misma usando la ecuacin ... tenemos
D=
0.9398000
=0.2991476 [ m ]
D=
0.0015875
=0.0005053 [ m ]
D=0.2991476 [ m ] 0.0005053 [ m ]
Hallando el volumen por la ecuacin ()
V=
0.2991476 20.9144000
=0.0642683 [ m3 ]
4
Hallando la incertidumbre del volumen puede ser calculada por la ecuacin ()
Donde
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 31 de ...
LABORATORIO N1
V 0.91440000.2991476
=
=0.4296765
D
2
V 0.2991476 2
=
=0.0702847
L
4
V = ( 0.42967650.0005053 ) + ( 0.07028470.0015875 )
2
V =0.002441
V =0.0642683 [ m 3 ] 0.002441 [ m3 ]
Calculando la capacidad para cada una de las presiones ledas.
2
P=
V
3
2
P1=
491.185 0.872
=70.127026[kPa]
3
P2=
491.30621.058
=85.127239[kPa]
3
P3=
491.19321.245
=100.12728[kPa]
3
P4 =
491.25421.369
=110.127148[ kPa]
3
P5=
491.254 21.369
=110.127148 [ kPa]
3
Resultados:
Los principales resultados obtenidos son:
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
LABORATORIO N1
v =491.238
[ ]
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 32 de ...
[ ]
m
m
1.217
s
s
V =0.0642683 [ m 3 ] 0.002441 [ m3 ]
3. Discusin e interpretacin de los resultados:
Se verifica que cuando se hace el tratamiento de magnitudes ms propiamente en la ley de los
gases ideales no importando el estado del mismo la relacin de las magnitudes que
involucran dicha ley permanecen constante es decir, si observamos la parte del clculo en el
cual se observa la velocidad media cuadrtica se tiene la expresin de la relacin entre la
presin y la densidad, y si a esto agregamos que se trabaja con el criterio de que la
temperatura permanece constante se tiene que observar que la ecuacin de los gases ideales
se reduce solo a esta relacin de variables debido a que todas las dems magnitudes sern
constantes.
v m1
3 p1
v m1 491.185 1.217 [m/s]
vm 2
3 p2
v m 2 491.306 1.217 [m/s]
vm3
3 p3
v m3 491.193 1.217 [m/s]
vm4
3 p4
v m 4 491.254 1.217 [m/s]
v m5
3 p4
v m 4 491.254 1.217 [m/s]
Entonces las dos variantes para cada estado por el enunciado de la ley de los gases indican
que su relacin deber permanecer constante. Lo cual se verifica en el extracto de clculos
anteriormente visto.
UNIVERSIDAD TECNICA DE ORURO
FACULTAD NACIONAL DE INGENIERIA
CARRERA DE INGENIERIA MECANICA-ELECTROMECANICA
LABORATORIO DE MAQUINAS TRMICAS
TERMODINAMICA TECNICA I
MEC 2244 A
MEDICIONES EN EL SISTEMA NEUMATICO DEL
LABORATORIO Pagina 33 de ...
LABORATORIO N1
4. Conclusiones:
Despus de realizar este trabajo experimental se puede decir que:
En la industria los instrumentos para medir presiones ms usados son los manmetros de Bourdon,
por ser de buena calidad, precisos, bastante prcticos (Fciles de usar) ya que muchas empresas
manejan el rango de 0 70 kPa en sus sistemas neumticos.
La precisin es inversamente proporcional a la temperatura y directamente proporcional al volumen.
La primera ley en termodinmica se aplica a todos los tipos de energa existentes y es una base para
el entendimiento de este campo de estudio.
A partir de los datos obtenidos en laboratorio, calcular la velocidad media cuadrtica de las
molculas del aire, la capacidad de almacenamiento del compresor del laboratorio para cada una de
las presiones ledas:
=503.424
m
s
1.759
m
s
5. Bibliografa:
Yunus Cengel, termodinmica, Mc Graw Hill, Mxico, 2008
Villca Tudela Juan Adres, Expresin de la incertidumbre, edit. Laboratorio de Trmicas,
Ing. Mecnica Electromecnica, FNI, Oruro 2007
Fsica lab, https://www.fisicalab.com/apartado/primer-principio-termo#contenidose, 16
agosto 2015
M. Sc. Ing. Pearanda Muoz Edgar S., Laboratorio Trmicas,
http://docentes.uto.edu.bo/epenarandam/, 14 agosto 2015
Vous aimerez peut-être aussi
- Lab2 2441 II 2020Document5 pagesLab2 2441 II 2020Brayan Altamirano Zubieta0% (2)
- Inf.3 Nivel Goniometrico2Document37 pagesInf.3 Nivel Goniometrico2Piter WellsPas encore d'évaluation
- Ind 2204Document5 pagesInd 2204Sayui JuanezPas encore d'évaluation
- TERMODINAMICA1Document110 pagesTERMODINAMICA1Benjamin Neciosup PaucarPas encore d'évaluation
- Maquinas y MecanismosDocument32 pagesMaquinas y MecanismosGerman Ortiz MonroyPas encore d'évaluation
- Informe Final 1Document30 pagesInforme Final 1brad floresPas encore d'évaluation
- Practica 2 de TermicasDocument5 pagesPractica 2 de TermicasRomer BaltazarPas encore d'évaluation
- Laboratorio de Procesos de ManufacturaDocument18 pagesLaboratorio de Procesos de ManufacturaAlvaroPas encore d'évaluation
- Informe 1 Medicion de TemperaturaDocument17 pagesInforme 1 Medicion de TemperaturaRaul LaraPas encore d'évaluation
- Transferencia Lab 2Document31 pagesTransferencia Lab 2pedro saul zutaraPas encore d'évaluation
- Silabo MC 216-2021-1-PROCESOS DE MANUFACTURA (PERALDO ANITA)Document3 pagesSilabo MC 216-2021-1-PROCESOS DE MANUFACTURA (PERALDO ANITA)Dennis FernandezPas encore d'évaluation
- Listado de Los Valores de Entrada para La Resolución Del Ciclo Mediante El CoolpackDocument8 pagesListado de Los Valores de Entrada para La Resolución Del Ciclo Mediante El CoolpackffPas encore d'évaluation
- 3 - Guia Prácticade RadiaciónDocument15 pages3 - Guia Prácticade RadiaciónAndrea DíazPas encore d'évaluation
- Guia 5 Tratamientos TermicosDocument9 pagesGuia 5 Tratamientos TermicosMauricio Colque ZevallosPas encore d'évaluation
- Practica 2 MEC 3330 Castelo Arguellas CristofferDocument7 pagesPractica 2 MEC 3330 Castelo Arguellas CristofferCristoffer Castelo ArgüellasPas encore d'évaluation
- Ensayo de MetalografiaDocument11 pagesEnsayo de MetalografiaNedas AsefrePas encore d'évaluation
- Exa Entrada Termodinámica 1 2020Document1 pageExa Entrada Termodinámica 1 2020Dilman LimaPas encore d'évaluation
- 2 Proyecto Camara Frigorifica para LacteosDocument46 pages2 Proyecto Camara Frigorifica para LacteosDiego Alejandro Mercado QuintanillaPas encore d'évaluation
- Limadora-Laboratorio de MaterialesDocument10 pagesLimadora-Laboratorio de Materialesleidy mendozaPas encore d'évaluation
- Lab Procesos TornoDocument12 pagesLab Procesos TornoVillafuerte Julca AlcidesPas encore d'évaluation
- Ensayo de AtraccionDocument24 pagesEnsayo de AtraccionMilagros Valeria Silva ChávezPas encore d'évaluation
- Fluidos de CorteDocument73 pagesFluidos de CortePaolo TorreZzPas encore d'évaluation
- Guia 5 Ensayo de Dureza RockwellDocument8 pagesGuia 5 Ensayo de Dureza RockwellArnol CallataPas encore d'évaluation
- Reporte de Practica 8 Medición de Acabado Superficial Con El Rugosímetro Equipo4Document9 pagesReporte de Practica 8 Medición de Acabado Superficial Con El Rugosímetro Equipo4Shamed AngelPas encore d'évaluation
- Problemas ManuDocument5 pagesProblemas ManuTony ChavezPas encore d'évaluation
- Laboratorio de Fisica III Informe #2Document21 pagesLaboratorio de Fisica III Informe #2Brian WilliamsPas encore d'évaluation
- Diseno de Una Cortadora de AlfalfaDocument20 pagesDiseno de Una Cortadora de Alfalfacesar salles lozanoPas encore d'évaluation
- MandrinadoDocument12 pagesMandrinadoKevin DPas encore d'évaluation
- Tema N°4 - Ingeniería Del ProyectoDocument57 pagesTema N°4 - Ingeniería Del ProyectoDanitza Mendoza Chambi0% (1)
- Procesos de ManufacturaDocument58 pagesProcesos de Manufacturasmok_sk8Pas encore d'évaluation
- Presentacion de TesisDocument42 pagesPresentacion de Tesisc_kelly_janeth2738Pas encore d'évaluation
- Esab Boletin-Tecnico-Nº134Document36 pagesEsab Boletin-Tecnico-Nº134Jose Luis PizarroPas encore d'évaluation
- 2do Exam II06Document12 pages2do Exam II06JuanDanielPuentesGuzman0% (2)
- Calculo Del Tiempo Principal en El TaladradoDocument5 pagesCalculo Del Tiempo Principal en El TaladradoKaryq MarinPas encore d'évaluation
- Calderón Rodríguez, Eder EduardoDocument200 pagesCalderón Rodríguez, Eder EduardoYURIPas encore d'évaluation
- Ensayo MicrograficoDocument1 pageEnsayo MicrograficoMaite ZuritaPas encore d'évaluation
- Cálculo de Carga de Enfriamiento para Un Restaurante de Comida RápidaDocument10 pagesCálculo de Carga de Enfriamiento para Un Restaurante de Comida RápidaAngel MansillaPas encore d'évaluation
- Equipamiento de Una Fresadora de Control NuméricoDocument44 pagesEquipamiento de Una Fresadora de Control NuméricoVictor Hugo Valqui LopezPas encore d'évaluation
- Mec 102 - AcabadosDocument29 pagesMec 102 - AcabadosTobi Obito100% (1)
- 17 InstrumentacionDocument14 pages17 InstrumentacionJose Antonio P BPas encore d'évaluation
- Amasadora Dic 23Document29 pagesAmasadora Dic 23Manuel Blanco MendozaPas encore d'évaluation
- Informe #2 - MetrologíaDocument10 pagesInforme #2 - MetrologíaLuis Gregory QRPas encore d'évaluation
- Práctica N°2Document21 pagesPráctica N°2Arturo YosepPas encore d'évaluation
- Informe N°3-Instrumentos de MediciónDocument23 pagesInforme N°3-Instrumentos de MediciónAlexandra GaldosPas encore d'évaluation
- Que Son Las Normas ASTMDocument12 pagesQue Son Las Normas ASTMJunge AkademischPas encore d'évaluation
- Plantilla Excel Analisis Modo Efecto FallaDocument1 pagePlantilla Excel Analisis Modo Efecto Fallajose adan alvarez ortegaPas encore d'évaluation
- Congelamiento de Pescado Transferencia de CalorDocument12 pagesCongelamiento de Pescado Transferencia de CalorAlejandro RamirezPas encore d'évaluation
- Conformado de PLÁSTICOS PDFDocument54 pagesConformado de PLÁSTICOS PDFjuan miguel calzada100% (1)
- Tif - Adiestramiento 1a - Segunda Parte - Procesos de Soldadura en La Construcción de Aviones y Barcos PDFDocument69 pagesTif - Adiestramiento 1a - Segunda Parte - Procesos de Soldadura en La Construcción de Aviones y Barcos PDFAony H.Q.Pas encore d'évaluation
- Problemas de Procesos Mecánicos de Fabricación IDocument31 pagesProblemas de Procesos Mecánicos de Fabricación IJhon HaylerPas encore d'évaluation
- Calculos Despulpadora de FrutasDocument36 pagesCalculos Despulpadora de FrutasJoseLuisRodriguezMirandaPas encore d'évaluation
- 01 Ejercicios de Conducción en Paredes Ticoman 2015Document5 pages01 Ejercicios de Conducción en Paredes Ticoman 2015Adrian CardePas encore d'évaluation
- Unidad 9 MC 115 2018 1 Antifricc.Document34 pagesUnidad 9 MC 115 2018 1 Antifricc.Lides Fernandez Saldivar100% (1)
- Los 10 Primeros Países Con Reservas de Combustibles Fósiles (2016)Document6 pagesLos 10 Primeros Países Con Reservas de Combustibles Fósiles (2016)energia21Pas encore d'évaluation
- 214 Guia 1Document4 pages214 Guia 1AlbaroMamaniVenizPas encore d'évaluation
- Guia Lab 1Document4 pagesGuia Lab 1CARLOS DAVID POMA RAMÍREZPas encore d'évaluation
- Laboratorio 1Document5 pagesLaboratorio 1monchoPas encore d'évaluation
- Resumen: M 0.354 KG 0.008 (KG)Document40 pagesResumen: M 0.354 KG 0.008 (KG)GUARACHI MUÑOZ ROLY FERNANDOPas encore d'évaluation
- Equilibrios de Fases y Transiciones de Fases: Parte ID'EverandEquilibrios de Fases y Transiciones de Fases: Parte IPas encore d'évaluation
- Flujo de fluidos e intercambio de calorD'EverandFlujo de fluidos e intercambio de calorÉvaluation : 1 sur 5 étoiles1/5 (1)
- ORGANIGRAMADocument2 pagesORGANIGRAMAAlvaroFloresPas encore d'évaluation
- Introducción Lab 1Document39 pagesIntroducción Lab 1AlvaroFloresPas encore d'évaluation
- Dimensionado de Bombas CentrifugasDocument50 pagesDimensionado de Bombas CentrifugasAlvaroFloresPas encore d'évaluation
- Conceptos Demanda OfertaDocument4 pagesConceptos Demanda OfertaAlvaroFloresPas encore d'évaluation
- Practica 2 3216 CDocument2 pagesPractica 2 3216 CAlvaroFloresPas encore d'évaluation
- FORMULASDocument6 pagesFORMULASAlvaroFloresPas encore d'évaluation
- Ejercicio de CogeneracionDocument7 pagesEjercicio de CogeneracionAlvaroFloresPas encore d'évaluation
- INFORME DE LABORATORIO I ReparadoDocument38 pagesINFORME DE LABORATORIO I ReparadoAlvaroFloresPas encore d'évaluation
- Conceptos Engranajes CorreasDocument17 pagesConceptos Engranajes CorreasAlvaroFloresPas encore d'évaluation
- Empresa GuabiraDocument10 pagesEmpresa GuabiraAlvaroFloresPas encore d'évaluation
- Practica 1 Mec 3343Document4 pagesPractica 1 Mec 3343AlvaroFloresPas encore d'évaluation
- Practica N°1 Mec-3343 14Document2 pagesPractica N°1 Mec-3343 14AlvaroFloresPas encore d'évaluation
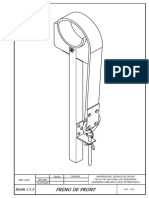
- Freno de Prony PDFDocument1 pageFreno de Prony PDFAlvaroFloresPas encore d'évaluation
- Generadores de VaporDocument67 pagesGeneradores de VaporLuiXs GR100% (1)
- TORNO MECANICO - Hecho Con Piezas Corrientes - Mi Mecánica PopularDocument14 pagesTORNO MECANICO - Hecho Con Piezas Corrientes - Mi Mecánica PopularMariainmaculada Maria Maria100% (2)
- EP1 Reporte de Práctica de Laboratorio Viscosímetro Por Caída de Bola.Document22 pagesEP1 Reporte de Práctica de Laboratorio Viscosímetro Por Caída de Bola.Elizabeth L H LopezPas encore d'évaluation
- Manual de Uso PDFDocument16 pagesManual de Uso PDFezequielpasqualiPas encore d'évaluation
- PrácticaDocument7 pagesPrácticaanthony sanchezPas encore d'évaluation
- IN005SPDocument32 pagesIN005SPMarcosPas encore d'évaluation
- 01 FluidosDocument38 pages01 Fluidoscesar muñoz100% (1)
- Presentación FinalDocument11 pagesPresentación FinalEstefaniaFernandezPas encore d'évaluation
- Informe Estabilidad Vehiculos Lanzadores Francisco Patitucci PerezDocument27 pagesInforme Estabilidad Vehiculos Lanzadores Francisco Patitucci PerezfranciscoPas encore d'évaluation
- Tarea 12 - Cálculo de Relaciones de TransmisiónDocument2 pagesTarea 12 - Cálculo de Relaciones de TransmisiónJr StevenPas encore d'évaluation
- Valvula de Alivio - Retroexcavadora - Probar y AjustarDocument3 pagesValvula de Alivio - Retroexcavadora - Probar y AjustarTeobaldo Silva CascaPas encore d'évaluation
- Manual Captiva Suspénsion PDFDocument142 pagesManual Captiva Suspénsion PDFdarwinPas encore d'évaluation
- U7 Codigo Asme Ix Art III WelderDocument38 pagesU7 Codigo Asme Ix Art III WelderDi No100% (1)
- Diseño Rib LocDocument16 pagesDiseño Rib LocArturo Rafael Olguin NoriegaPas encore d'évaluation
- Procesos de Transferencia de Calor de Donald Kern SolucionarioDocument3 pagesProcesos de Transferencia de Calor de Donald Kern SolucionarioXochitl De JesusPas encore d'évaluation
- Tipos de CargaDocument30 pagesTipos de CargaJohan Macías ÁlavaPas encore d'évaluation
- Fundamentos de CPDPDocument129 pagesFundamentos de CPDPAlfonso LockherupPas encore d'évaluation
- Manual CABALLETEDocument4 pagesManual CABALLETESofia GonzalezPas encore d'évaluation
- Ejercicios 2Document9 pagesEjercicios 2Joseph CruzPas encore d'évaluation
- Ejercicios de Dinámica4Document2 pagesEjercicios de Dinámica4Carmen VelayosPas encore d'évaluation
- Libro de Ingenieria Sismica 2do ParcDocument24 pagesLibro de Ingenieria Sismica 2do ParcAlejandro Triviño De La CruzPas encore d'évaluation
- Puente de Manómetro - TeamsDocument27 pagesPuente de Manómetro - TeamsManuela García FernándezPas encore d'évaluation
- Capitulo 70-80 para InstruccionDocument45 pagesCapitulo 70-80 para InstruccionAndres Parra NavarroPas encore d'évaluation
- Memoria de Calculo - FA20149 - Edificio ZEPITA - R0Document31 pagesMemoria de Calculo - FA20149 - Edificio ZEPITA - R0Dante Carbajal CruzPas encore d'évaluation
- Práctica 2 - 1 2 - 2Document15 pagesPráctica 2 - 1 2 - 2Fabricio Cabrera RPas encore d'évaluation
- Pa2 DinamicaDocument15 pagesPa2 DinamicaMIGUEL ANGEL ALARCON CRUZPas encore d'évaluation
- LubricacionDocument88 pagesLubricacionEdgar Pangol RodríguezPas encore d'évaluation
- Base de Datos - Ferreteria ProveedoresDocument85 pagesBase de Datos - Ferreteria ProveedoresANTONELLAPas encore d'évaluation
- 2021 - Sept - Tarea - 2 - Parcial - 2Document10 pages2021 - Sept - Tarea - 2 - Parcial - 2Ana Paola SámanoPas encore d'évaluation
- Ayudantias Mecanica de Fluidos 2011Document119 pagesAyudantias Mecanica de Fluidos 2011Gonzalo Ferrer NorambuenaPas encore d'évaluation