Académique Documents
Professionnel Documents
Culture Documents
Gases Shlom
Transféré par
Gerson FloresCopyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Gases Shlom
Transféré par
Gerson FloresDroits d'auteur :
Formats disponibles
UNMSM Ingeniera Qumica
Laboratorio de Fisicoqumica I
Gases
Contenido
I. INTRODUCCION..................................................................................................................................2
II. RESUMEN............................................................................................................................................3
III. PRINCIPIOS TEORICOS...................................................................................................................4
IV. PROCEDIMIENTO EXPERIMENTAL..............................................................................................7
V.TABULACION DE DATOS..................................................................................................................9
VI. EJEMPLO DE CALCULOS.............................................................................................................11
VII.ANALISIS Y DISCUSION DE RESULTADOS..............................................................................16
V.CONCLUSIONES................................................................................................................................17
IX.RECOMENDACIONES....................................................................................................................18
X. BIBLIOGRAFIA................................................................................................................................19
XI. APENDICE.......................................................................................................................................20
Gases
UNMSM Ingeniera Qumica
Laboratorio de Fisicoqumica I
I. INTRODUCCION
Los gases reales son los que en condiciones ordinarias de temperatura y
presin se comportan como gases ideales; pero si la temperatura es muy baja
o la presin muy alta, las propiedades de los gases reales se desvan en forma
considerable de las de los gases ideales.
Para estudiar los gases reales con mayor exactitud, es necesario modificar la
ecuacin del gas ideal, tomando en cuenta las fuerzas intermoleculares y los
volmenes moleculares finitos.
Es por esto que existen una serie de ecuaciones, llamadas ecuaciones de
estado, para predecir el comportamiento de un gas tratado como gas real,
entre las ms utilizadas tenemos: la ecuacin de Van Der Walls y la ecuacin
de Berthelot
Gases
UNMSM Ingeniera Qumica
Laboratorio de Fisicoqumica I
II. RESUMEN
El presente trabajo aborda de manera experimental la teora de Gases
reales. El estudio de los gases reales es ciertamente ms complejo que el de
los gases ideales. Es as, que la determinacin de sus propiedades, no se
puede hacer usando las ecuaciones propias de los gases ideales. Se recurrir
entonces a otras relaciones, algunas de las cuales involucran la correccin
de sus semejantes ideales.
El objetivo del presente trabajo es estudiar las principales propiedades de los
gases reales, analizando para este propsito: la capacidad calorfica y la
densidad de los gases.
Bajo condiciones tales como: temperatura de 22C, presin de 756 mmHg y
92% de humedad relativa, se realizan los experimentos en mencin.
El clculo de la densidad de los gases se hace usando el mtodo de Vctor
Meyer que permite determinar condiciones importantes en un gas tales como
la presin, el volumen, la masa, la temperatura, del gas entre otros.
Estableciendo una analoga con las condiciones normales, es posible
determinar el volumen de la sustancia, lo cual finalmente nos permite obtener
la densidad del gas a condiciones normales, siguiendo la muy conocida
relacin entre la densidad, la masa y el volumen.
Posteriormente realizamos el clculo de la relacin entre las capacidades
calorficas (Cp y Cv) para un gas, que en nuestro experimento es el aire. Para
este propsito usamos el mtodo de Clement y Desormes, segn el cual es
posible determinar la relacin entre las capacidades calorficas de un gas a
partir de ciertas relaciones que involucran presiones.
Los detalles experimentales de estos mtodos son explicados de manera
concisa, as como el anlisis de los resultados obtenidos, respecto al margen
de error de los experimentos, adems de las conclusiones y las
recomendaciones respectivas que permitan la obtencin de mejores
resultados asi como la reduccin del porcentaje de error.
Gases
UNMSM Ingeniera Qumica
Laboratorio de Fisicoqumica I
III. PRINCIPIOS TEORICOS
CONDENSACIN Y CONDICIONES CRTICAS
El trmino "punto crtico" a veces se utiliza para denotar especficamente el
lquido-vapor de puntos crticos de un material. El lquido-vapor punto crtico
indica las condiciones a partir del cual distintos lquidos y de gases de fases
no existen.
El lquido-vapor de puntos crticos de presin-temperatura diagrama de fase
est en la temperatura extrema alta de la fase gaseosa lmite-lquido. La lnea
verde de puntos da el comportamiento anmalo del agua.
Como se muestra en el diagrama de fase especies puras a la derecha, este es
el punto en que el lmite de fase entre lquido y gas termina. En el agua, el
punto crtico se produce en torno a 647 K (374 C o 705 F ) y 22,064 MPa
(3200 PSIA o 218 atm ) [1] .
A medida que la temperatura crtica se plantea, las propiedades del gas y el
enfoque de fases lquidas entre s, resultando en una sola fase en el punto
crtico: una homognea fluido supercrtico . El calor de vaporizacin es cero
en y ms all de este punto crtico, lo que no hay distincin entre las dos
fases. Por encima de la temperatura crtica de un lquido no puede ser
formado por un aumento en la presin , pero con la suficiente presin un slido
puede ser formado. La presin crtica es la presin de vapor a la temperatura
crtica. En el diagrama que muestra la termodinmica las propiedades de una
determinada sustancia, el punto en que la temperatura crtica y presin crtica
cumplir se llama el punto crtico de la sustancia. La crtica volumen molar es el
volumen de un mol de material a la temperatura crtica y la presin.
propiedades crticas varan de un material a otro, como es el caso del punto
de fusin y punto de ebullicin . Propiedades crticas para muchas sustancias
puras estn fcilmente disponibles en la literatura.
La obtencin de
propiedades crticas para las mezclas es algo ms problemtica.
UNMSM Ingeniera Qumica
Laboratorio de Fisicoqumica I
Gases
Definicin matemtica
Para sustancias puras, no hay un punto de inflexin en la crtica isoterma en
un diagrama pV. Esto significa que en el punto crtico:
Esta relacin se puede utilizar para evaluar dos parmetros para una
ecuacin de estado en trminos de las propiedades crticas.
A veces, un conjunto de propiedades reducidas se definen en trminos de las
propiedades crticas, es decir: [2]
donde r T es la temperatura reducida, r p es la presin reducida, r V es el
volumen reducido, y R es la constante universal de los gases
Como puede verse en la figura 1(b), el volumen y la presin a la que ocurre el
cambio de fase depende de la temperatura, esto es, de la isoterma en la que
nos estemos moviendo. Como puede apreciarse en la grfica, conforme
aumenta la temperatura la coexistencia lquido-vapor tiene lugar a mayor
presin y volumen, y cada vez tiene lugar durante un intervalo de volumen ms
pequeo.
Gases
UNMSM Ingeniera Qumica
Laboratorio de Fisicoqumica I
Diferencia entre cp y cv (capacidad calorfica a presin
constante y a volumen constante)
La diferencia entre C P y C V es que C P se aplica si el trabajo se hace para el sistema
que provoca un cambio en el volumen (por ejemplo, al mover un pistn para comprimir
el contenido de un cilindro), o si el trabajo es realizado por el sistema que cambia su
temperatura (por ejemplo, calentando el gas en un cilindro de causar un pistn para
moverse). V C se aplica slo si P d V - es decir, el trabajo realizado - es cero. Tenga en
cuenta la diferencia entre la adicin de calor al gas con un pistn bloqueado, y la
adicin de calor con un pistn libre para moverse, para que la presin permanece
constante. En el segundo caso, el gas y ampliar tanto el calor, haciendo que el pistn
para hacer el trabajo mecnico en la atmsfera. El calor que se aade al gas va slo
en parte en calentar el gas, mientras que el resto se transforma en trabajo mecnico
realizado por el pistn. En el, de volumen constante el primer caso (llave de pistn) no
hay ningn movimiento externo, y por ende no se realiza trabajo mecnico en la
atmsfera; C V se utiliza. En el segundo caso, el trabajo adicional se realiza como los
cambios de volumen, por lo que la cantidad de calor necesaria para elevar la
temperatura del gas (la capacidad calorfica especfica) es ms alto para este caso una
presin constante.
Relaciones cp y cv en gases ideales
Para un gas ideal, la capacidad calorfica es constante con la temperatura. En
consecuencia, podemos expresar la entalpa como H C P T = y el interior de la energa
como U C T = V. Por lo tanto, tambin se puede decir que la relacin entre capacidad
trmica es la relacin entre la entalpa de la energa interna:
Por otra parte, las capacidades calorficas se puede expresar en trminos de capacidad
de relacin de calor () y la constante de los gases (R):
Puede ser bastante difcil encontrar informacin tabulada para C V, ya que C P es ms
comnmente tabulados. La siguiente relacin, se puede utilizar para determinar C V:
Cv = C P - R
Relaciones de cp y cv en gases Reales
A medida que aumenta la temperatura, mayor energa y vibracin estados de rotacin se
hacen accesibles a los gases moleculares, lo que aumenta el nmero de grados de
libertad y la reduccin de . Para un gas real, tanto C P y C V aumentan al aumentar la
temperatura, sin dejar de se diferencian entre s por una constante fija (como arriba, C P
= C + V R), que refleja la relativamente constante P * V diferencia en el trabajo realizado
durante la expansin, para una presin constante contra las condiciones de volumen
constante. As, la proporcin de los dos valores, , disminuye al aumentar la
temperatura. Para obtener ms informacin sobre los mecanismos de almacenamiento
de calor de los gases, vea la seccin de gas de capacidad calorfica especfica .
Gases
UNMSM Ingeniera Qumica
Laboratorio de Fisicoqumica I
IV. PROCEDIMIENTO EXPERIMENTAL
PRIMERA PARTE:
Determinacin del la densidad de gases por el Mtodo de Vctor Meyer.
1. Instalar el equipo compuesto por un vaso, una bureta, una pera, tubo de ensayo
con desprendimiento lateral (tubo de vaporizacin), estufa tal como se muestra a
continuacin.
2. El vaso deber contener agua (aproximadamente 2/3 de su volumen). El agua
contenida en la bureta deber igualar sus extremos tanto en la pera como en la
bureta. Para ellos se deber abrir la llave de la bureta.
3. Pese en la balanza analtica electrnica la masa de cloroformo que aparece
contenido en una ampolla de vidrio. Para este propsito deber pesar primero el
frasco con la sustancia en su interior, y posteriormente el frasco sin la sustancia,
para obtener por diferencia la masa de cloroformo en cuestin.
4. Para evitar errores en los clculos coloque el tapn al tubo de vaporizacin de
manera que se produzcan variaciones en los niveles del lquido. Este
procedimiento deber repetirse hasta que tal variacin de niveles no sea mayor
de 0.2 ml, entonces podremos iniciar el experimento.
5. Vierta el cloroformo en el tubo de vaporizacin y coloque inmediatamente el tapn
de manera que no permita la fuga de vapor de cloroformo.
6. A medida que decrezca el nivel del agua en la bureta iguale el nivel de la pera
(coloque la pera a una altura menor) hasta que el nivel de agua detenga su
descenso.
7. El cloroformo que ha pasado a estado gaseoso ejerce presin en el lquido, al
cual ha desplazado ocupando un cierto volumen. Cierre la llave de la bureta.
Luego de 10 minutos aproximadamente, realice una recopilacin de los siguientes
datos: temperatura del agua en la pera, y variacin de nivel de agua en la bureta.
Ello constituye todo el proceso.
7
UNMSM Ingeniera Qumica
Laboratorio de Fisicoqumica I
Gases
SEGUNDA PARTE:
Determinacin de la capacidad calorfica (Cp y Cv) por el mtodo de
Clement y Desormes.
1. Instale el equipo tal como se muestra en la figura.
2. Inicie el experimento suministrando aire al equipo con el inflador. Esto con el
objetivo de provocar en el manmetro que contiene agua, una diferencia de nivel
de 10 cm. Observe que existe un orificio abierto (O), por esta razn, para evitar la
fuga de gas, debe mantenerlo cerrado mientras se ingresa aire al equipo (tpelo
con el dedo).
3. Una vez logrado el desnivel requerido, obstruya (presione con los dedos) el tubo
(en el punto E, por ejemplo) con el objetivo de no permitir que el aire escape.
Es posible que al suministrar aire al equipo no consiga exactamente la diferencia
de niveles que usted desea. En caso que haya logrado menos de lo que usted
desea, deber bombear ms aire. En tanto, si ha excedido la diferencia de nivel
que usted requera deber ir soltando un poco del aire (soltando el tubo por un
pequeo instante) con mucho cuidado hasta lograr el desnivel objetivo.
4. Una vez lograda la diferencia de alturas de aproximadamente10 cm. Mida con
exactitud de cuanto realmente es la diferencia de alturas. Esta altura inicial la
caracterizaremos como h1.
5. El siguiente paso requiere de cierta habilidad para su realizacin. Una vez medido
el desnivel inicial, deber retirar el dedo que obstrua el orificio (O) para permitir la
salida de aire. Ello ocasionar que el agua en el manmetro se mueva buscando
su posicin original. En el instante en el que el extremo superior se cruce con el
extremo inferior, debe obstruirse nuevamente el orificio (O). Una vez que el lquido
se haya estabilizado, mida la nueva diferencia de alturas,
la cual
caracterizaremos como h2. Ello constituye todo el proceso.
6. Debe repetir esta experiencia varias veces. Primero con una diferencia de alturas
inicial de 10 cm (4 medidas que sern promediadas), posteriormente con
diferencias iniciales de 15, 20 y 25 cm.
Gases
UNMSM Ingeniera Qumica
Laboratorio de Fisicoqumica I
V.TABULACION DE DATOS
Condiciones ambientales
P (mmHg)
756
TC
22
HR (%)
92
a) Experimento: Densidad de gases.
Datos experimentales obtenidos
TC agua en la pera
24
Volumen en la bureta (ml)
17.5
Datos tericos
P vapor H2O (mmHg)
19.83
Tc CHCl3 (K)
536.55
Pc CHCl3 (atm)
53.79
Resultados obtenidos
P (P baromtrica corregida)
754.41
R (Constante corregida)
Densidad terica del CHCl3
(CN)
0.08
Densidad Experimental CHCl3
(CN)
5.47
6.49
Error Experimental
Error %
18.6
b) Experimento: Capacidad Calorfica
9
Gases
UNMSM Ingeniera Qumica
Laboratorio de Fisicoqumica I
Datos experimentales obtenidos
H2 (cm)
H1 (cm)
4.6
4.0
4.1
3.9
5.5
4.8
5.5
5.2
8.5
8.6
8.0
8.4
15
20
30
Datos tericos
Y aire
1.4
Cp Aire
6.93
Cv Aire
4.95
Resultados obtenidos
Y promedio
1.38
Cp
7.26
Cv
5.26
Error Experimental
Error % Cp
6.26
Error % Cv
4.76
10
Gases
UNMSM Ingeniera Qumica
Laboratorio de Fisicoqumica I
VI. EJEMPLO DE CALCULOS
A)
Calculo de las densidades:
Para los gases reales se establecen las siguientes relaciones.
A partir de la siguiente relacin:
Se puede establecer la densidad (elegimos a condiciones ambientales: T= 273.15 k, P= 1 atm):
. (2)
Para calcular el valor del R corregido se usa la ecuacin de Berthelot:
(3)
De donde se deduce que:
(4)
Donde: P y T estn a CN y Pc, Tc deben ser extrados de handbooks como datos tericos.
Tc= 536.55 K
Pc=53.79 atm
R= 0.082 atm.L/Mol.k
Reemplazando en la expresin y resolviendo se obtiene:
R=0.08
Reemplazamos los datos respectivos en la expresin (2)
Asi obtenemos:
D teorica= 5.47 g/L
Asi mismo, es posible determinar la densidad de manera experimental (con el mtodo usado en
laboratorio)
Usamos la siguiente relacin:
11
Gases
UNMSM Ingeniera Qumica
Laboratorio de Fisicoqumica I
(3)
Para obtener el Volumen del CHCl3 a condiciones normales usaremos esta relacin:
. (4)
Se necesita entonces obtener el valor de Pb corregido, para ello usamos la siguiente relacin:
Donde:
Pb= Patmosferica= 756 mmHg
H= humedad relativa= 92
F= Presion de vapor=19.83 mmHg
Reemplazando en la expresin se obtiene:
Pb = 754.41 mmHg
Ello reemplazando en la expresin (4) da como resultado
VCN= 15.97 ml
Finalmente podemos determinar la densidad reemplazando los valores obtenidos en la
expresin (3):
D= 0.1037g
0.01597 L
D exp= 6.49 g/L
Podemos determinar el porcentaje de error en nuestro experimento comparando los valores
experimentales con los tericos:
I%EI= (5.47-6.49) x 100 = 18.6 %
5.74
12
Gases
UNMSM Ingeniera Qumica
Laboratorio de Fisicoqumica I
B)
Calculo de las capacidades calorficas:
Para poder determinar las capacidades calorficas cp y cv hacemos uso de ciertas
relaciones. Es posible determinar la relacin entre las capacidades calorficas Cp y Cv.
Esta relacin viene representada por :
(1)
As mismo se puede establecer la siguiente frmula para determinar dicha relacin:
... (2)
Donde h1: Diferencia de alturas iniciales
H2: Diferencia de alturas finales.
Tambin ocurre:
(3)
El procedimiento es simple: Hallar experimentalmente a partir de la relacin (2).
Luego, segn la relacin (3), podemos expresar Cp en funcin de Cv (R es conocido) o
expresar cv en funcin de cp, como se desee. Ello reemplazndolo en la expresin 1.
Nos permitir conocer el valor de cp y luego por la relacin 3 el valor de cv (o
viceversa).
Segn lo detallado, el clculo se har de la siguiente manera:
1) De acuerdo a la relacin (2) hallaremos el valor de :
Para h= 15 cm:
1 = 15
= 1.44
15 4.6
2 = 15
= 1.36
15-4.0
As determinamos para el primer caso un
3 =
15
= 1.38
15-4.1
4 = 15
= 1.35
15-3.9
promedio:
= 1.38
13
Gases
UNMSM Ingeniera Qumica
Laboratorio de Fisicoqumica I
Para h= 20 cm:
1 = 20
= 1.38
20 5.5
3 =
20
= 1.38
20 5.5
2 = 20
= 1.32
20 4.8
4 =
20
= 1.35
20 5.2
3 =
30
= 1.36
30-8.0
Promedio:
=1.36
Para h= 30 cm:
1 = 30
= 1.40
30 8.5
2 = 30
= 1.40
30 8.6
Promedio:
4 =
25
30-8.4
= 1.39
=1.39
A partir de estos valores de , obtenemos un valor promedio:
=1.38
2) De acuerdo a las relaciones:
Es posible establecer la siguiente relacin:
Dnde: R=2 cal/molg.K
Reemplazando en la expresin el
obtenido y el R, podremos obtener el valor de Cv.
= 2 + Cv = 1.38
Cv
Cv = 5.26 cal/k
Luego, de acuerdo a la relacin (3), es posible determinar el valor de Cp:
Cp= Cv+ R= 5.26+2 = 7.26 cal /k
14
Gases
UNMSM Ingeniera Qumica
Laboratorio de Fisicoqumica I
3)
Finalmente, estos datos experimentales podrn ser comparados con los tericos
para as determinar el porcentaje de error en nuestro experimento.
Considerando al aire (mezcla de gases compuesta en un 78% por N2 y 21% por O2 )
como un gas diatmico es posible establecer las siguientes relaciones:
Cp= 7R
2
Cv= 5R
2
Donde R= 2 cal /mol.g K
Asi, para el aire, tericamente se establece:
Cp= 6.93(2)
2
Cv= 4.95(2)
2
Cp= 6. 93
Cv= 4.95
Calculo del error experimental:
Dados:
Cv exp= 5.26
Cv teor= 4.95
Cp exp = 7.26
Cp teor= 6.93
I%EI= (4.95 5.26) x100
4.95
%E Cv= 6.26 %
I%EI= (6.93 -7.26) x100
6.93
%E Cp= 4.76 %
15
UNMSM Ingeniera Qumica
Laboratorio de Fisicoqumica I
Gases
VII.ANALISIS Y DISCUSION DE RESULTADOS
Los resultados obtenidos en el experimento de Meyer para determinacin de la
densidad del cloroformo son similares a los tericos lo cual nos demuestra que
este mtodo es efectivo para tal propsito. Se registro aun as, un porcentaje
de error considerable. Este error probablemente se deba a la medicin de la
masa del cloroformo (problemas con la balanza) o a la mala medicin de otros
datos importantes como: la temperatura de la pera o el volumen desplazado en
la bureta. Tambin pueden haber propagado un error de este tipo el considerar
valores arbitrarios como el de la presin atmosfrica (asumimos 756 mmHg
pero dicho valor deba ser determinado usando cierto tipo de instrumentos con
los cuales no cuenta el laboratorio) o la humedad relativa
Respecto al experimento relacionado a las capacidades calorfica, pese a la simpleza
del mtodo de Desormes, los resultados obtenidos experimentalmente con este
mtodo corresponden muy bien a los datos tericos (considerando al aire, que est
compuesto en un 79% por Nitrgeno y 21 % de oxigeno, en estas condiciones como
un gas ideal diatmico)
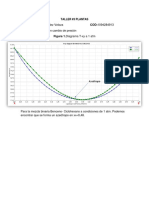
A diferentes medidas de alturas iniciales se determino respectivas alturas posteriores,
de tal manera que la relacin Y se presento prcticamente constante para todos estos
casos. Si realizramos una grafica h1 vs h1-h2 esta determinara una recta cuya
pendiente seria: Y
16
Gases
UNMSM Ingeniera Qumica
Laboratorio de Fisicoqumica I
V.CONCLUSIONES
El mtodo de Meyer para la determinacin de la densidad de gases es
efectivo.
Para poder determinar la densidad de gas real es necesario considera la
ecuacin de los gases reales (similar a la de los gases ideales pero con R
corregido). Es preciso determinar el valor de dicho R para lo cual se usa
una relacin planteada por Berthelot. Adems de asumir condiciones
normales para facilitar los clculos. Asi mismo debemos usar relacion
conocidas como la de la densidad respecto a la masa y el volumen.
Es necesario corregir la presin baromtrica del gas dado que se trata de
un gas hmedo.
La aplicacin de las relaciones para gases reales relativas a la capacidad
calorfica son correctas, ello fue comprobado experimentalmente.
As mismo, hemos comprobado experimentalmente que el mtodo de
Desormes y Clement para el clculo de la relacin de capacidades
calorficas, aunque no es el ms indicado o preciso, es efectivo para su
propsito permitindonos obtener resultado muy cercanos a los reales.
17
Gases
UNMSM Ingeniera Qumica
Laboratorio de Fisicoqumica I
IX.RECOMENDACIONES
Para la obtencin de mejores resultados as como la reduccin del porcentaje
de error, se hacen las siguientes recomendaciones:
A)
Para el experimento de determinacin de densidad de gases
Realizar un pesado correcto de la sustancia en anlisis (cloroformo en
nuestro experimento)
Nivelar adecuadamente el liquido en la bureta tal como lo indica el
proceso, hasta que la diferencia no supere los 0.2 ml
Tener cuidado con la temperatura que puede adquirir el agua del vaso,
recordar que la temperatura de ebullicin del agua es mayor que la del
cloroformo.
Cuidar que no haya fugas en el tapn del tupo de vaporizacin o al
cerrar la llave de la bureta.
Esperar como indica el proceso,10 minutos para realizar la toma de
datos ( temperatura de pera y variacin de volumen en la bureta)
Cuidado en los clculos matemticos, cambio de unidades, etc. Los
clculos involucran formulas un tanto complejas que pueden provocar
errores sistemticos y propagacin de errores.
B)
Para el experimento de determinacin de capacidades calorficas.
Asegurar que no exista fugas en los conductos, ya que ello provocara
una fuga del aire y un error considerable en las mediciones de alturas y
por propagacin, en los clculos experimentales.
Se recomienda la participacin de 3 personas para una realizacin ms
cmoda de este experimento. Una persona que bombee el aire al
sistema, otra que se encargue de obstruir el orificio y la manguera
cuando sea necesario, y otra persona que se encargue de medir las
diferencias de alturas y tomar los apuntes respectivos.
Precisin en el procedimiento, especficamente en la parte de abrir la
salida de aire para la determinacin del h1, dado que este paso requiere
de cierta habilidad y reflejos. De obtenerse medidas que difieran mucho
de las otras estas debern ser reemplazadas por otras ms exactas.
Tambin precisin en la medicin de las diferencias de altura h1 y h2,
se recomienda: Esperar que el lquido se estabilice para poder hacer la
medicin.
Luego de ingresar aire al sistema presionar con firmeza el conducto a
fin de no dejar escapar aire, lo cual inducira a errores en los clculos.
Evitar los errores de clculo. Aunque las formulas que se usan para la
determinacin de capacidades calorficas no son muy complejas, no
est de ms tener cierto cuidado en los clculos matemticos.
18
Gases
UNMSM Ingeniera Qumica
Laboratorio de Fisicoqumica I
X. BIBLIOGRAFIA
MARON Y PRUTTON, "Fundamentos de FISICOQUMICA", Editorial:
Noriega Limusa, Mxico, D.F., 1990 Pginas: 237-238,239-243, 245.252253.
HILL Graham, HOLMAN John. Chemistry in context. Estados Unidos,
Editorial Nelson thornes. quinta edicion, pag 143
AGUILAR S.A. FisicoQuimica Ediciones(7ma. edicin, Espaa, 1972 Pg.
283
PONS MUZZO: Fisicoqumica Editorial Universo S.A. (2da. Edicin,
Lima - Per, 1973) Pg. 24-27,capitulo 2,pag70, capitulo 3.pag.119.
BURNS, RALPH A.Fundamentos de Qumica ,2 edicin 1996Editorial
Prentice Hall Capitulo 12, Pgs. 343-370.
SHOEMAKER, DAVID P. y GARLAND, CARL W.Experimentos de
Fisicoqumica. 1 edicin en espaol - 1968Editorial Hispanoamericano,
Pags. 60-85
19
Gases
UNMSM Ingeniera Qumica
Laboratorio de Fisicoqumica I
XI. APENDICE
CUESTIONARIO
1.-En
qu consiste el mtodo de Regnault para la determinacin de los
pesos moleculares de las sustancias gaseosas?
Este mtodo se usa para determinar los pesos moleculares de las sustancias
gaseosas a la temperatura ambiente, y se realiza as: un matraz de vidrio de
unos 300 o 500 c.c de capacidad, provisto de llave, se evac y pesa,
llenndolo a continuacin con el gas cuyo peso molecular se busca a una
temperatura y presin, procediendo a pesarlo de nuevo. La diferencia de
pesos representa el peso del gas W en el matraz cuyo volumen se determina
llenndolo y pesndolo con agua o mercurio, cuyas densidades se
conocen.Con los datos obtenidos se deduce el peso molecular buscado
mediante la ecuacin:
P.V= n.R.T = (W/M).R.T
M =(W.R.T)/(P.V)
2.-Explicar que es la temperatura boyle
20
Vous aimerez peut-être aussi
- Exposiciones Flujo CompresibleDocument4 pagesExposiciones Flujo CompresibleAbel Bullon ChuquipulPas encore d'évaluation
- Definición de Viscosidad y Propiedades ColigativasDocument3 pagesDefinición de Viscosidad y Propiedades ColigativasPablo CalderònPas encore d'évaluation
- Dest Extracti - Cam PresionDocument8 pagesDest Extracti - Cam PresionMaria Del Mar MedinaPas encore d'évaluation
- GasesDocument18 pagesGasesDayanaKarolyneSalcedoCornejo100% (1)
- Propiedades Del Aceite NegroDocument10 pagesPropiedades Del Aceite NegroAngel magaña castilloPas encore d'évaluation
- Problema Resuelto Ciclo de OTTODocument4 pagesProblema Resuelto Ciclo de OTTOChristian HunterPas encore d'évaluation
- LABORATORIO Nº5 FISICA II UNAPDocument13 pagesLABORATORIO Nº5 FISICA II UNAPWilliam Taipe100% (1)
- Ejercicios RestantesDocument7 pagesEjercicios RestantesHermes BravoPas encore d'évaluation
- 1212 TermodinamicaDocument2 pages1212 TermodinamicaEduardo BaronPas encore d'évaluation
- Correlacion de Duns y RosDocument52 pagesCorrelacion de Duns y RosMiguel CondayaPas encore d'évaluation
- Compresores NeverCOMPRESORES NEVERAS ELECTROLUXas ElectroluxDocument4 pagesCompresores NeverCOMPRESORES NEVERAS ELECTROLUXas ElectroluxJesus Grillet100% (1)
- FORMULARIO VENTILACIÓN DE MINAS CorregidoDocument3 pagesFORMULARIO VENTILACIÓN DE MINAS CorregidoAnonymous xw3hvRgZPas encore d'évaluation
- Carnot InversoDocument32 pagesCarnot InversoBrandon AC100% (1)
- Ecuacion de EstadoDocument13 pagesEcuacion de EstadoROSARIOMARTINEZ25Pas encore d'évaluation
- Constante Universal de Los Gases "R"Document4 pagesConstante Universal de Los Gases "R"AmairaniPas encore d'évaluation
- Procesos TermodinamicosDocument11 pagesProcesos TermodinamicosNavarro José LuisPas encore d'évaluation
- 5 El Estado Gaseoso y Sus LeyesDocument20 pages5 El Estado Gaseoso y Sus LeyesTito Condori PairumaniPas encore d'évaluation
- Tension SuperficialDocument4 pagesTension SuperficialAndres MirandaPas encore d'évaluation
- Velocidades Recomendadas de FluidosDocument4 pagesVelocidades Recomendadas de Fluidoschipiloo100% (1)
- Diagrama de Moody y Monograma de TuberiaDocument9 pagesDiagrama de Moody y Monograma de TuberiaYerson GarciaPas encore d'évaluation
- Guía de Los Gases y Sus Leyes Ii. 7°Document4 pagesGuía de Los Gases y Sus Leyes Ii. 7°XIMENA MORENO AYVARPas encore d'évaluation
- Semana 3 M - Termo - Mar-Jun 2021Document7 pagesSemana 3 M - Termo - Mar-Jun 2021chucho 2112Pas encore d'évaluation
- Ley de LussacDocument6 pagesLey de LussacallanPas encore d'évaluation
- Equilibrio Líquido-VaporDocument8 pagesEquilibrio Líquido-Vaporbrendads89100% (1)
- Taller FinalDocument8 pagesTaller Finalarialdo jose pertuzPas encore d'évaluation
- Gases Ideales y Procesos de Los GasesDocument9 pagesGases Ideales y Procesos de Los GasesBeacker Huaquisto RaimePas encore d'évaluation
- Introduccion A La Termodinamica 2Document250 pagesIntroduccion A La Termodinamica 2laura gomez0% (1)
- PROBLEMAS DE MÉTODOS DE DESTILACIÓN EjemplosDocument11 pagesPROBLEMAS DE MÉTODOS DE DESTILACIÓN EjemplosJorge Bahena ArteagaPas encore d'évaluation
- Correción Parcial - Natalia Osorio y Pedro BedoyaDocument4 pagesCorreción Parcial - Natalia Osorio y Pedro BedoyaNataliaOsorioHenaoPas encore d'évaluation
- Ecuaciones de EstadoDocument15 pagesEcuaciones de EstadocesarcarrionpascualPas encore d'évaluation