Académique Documents
Professionnel Documents
Culture Documents
05 Primera Ley Masa de Control
Transféré par
fatamariCopyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
05 Primera Ley Masa de Control
Transféré par
fatamariDroits d'auteur :
Formats disponibles
PONTIFICIA UNIVERSIDAD CATOLICA DEL PERU
MECANICA
FACULTAD DE CIENCIAS E INGENIERIA
ENERGIA
SECCION INGENIERIA
AREA DE
TERMODINAMICA
PRIMERA LEY DE LA TERMODINAMICA
CONSERVACION DE LA MASA
Uno de los conceptos ms fundamentales de la ciencia es que la masa no puede crearse ni
destruirse (una excepcin a este principio es la teora de la relatividad de Einstein).
CONSERVACION DE LA ENERGIA
LA ENERGIA NO SE CREA NI SE DESTRUYE SLO SE TRANSFORMA
De forma semejante, se postula que la energa se conserva en cualquier proceso que tenga
lugar en un sistema: masa de control o volumen de control.
Es decir:
EENTRA - ESALE = ESISTEMA
PRIMERA LEY: CICLO
El calor neto agregado a un sistema que opera cclicamente
es igual en magnitud al trabajo desarrollado por ste
Q W
QNETO = W NETO
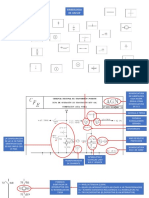
PRIMERA LEY MASA DE CONTROL
Este principio axiomtico postula la existencia de una propiedad extensiva del sistema (E) ;
esto es, que un cambio en su valor, entre dos estados cualesquiera, es numricamente igual a
la diferencia entre el calor neto agregado a un sistema y el trabajo neto desarrollado por ste
durante el proceso. Esta propiedad se conoce como Energa del sistema
dE Q W
Q dE W
siendo E = U + EC + EP
Q dU dEC dEP W
Q12 = U + EC + EP + W 12
q12 =
ec
ep
+ w12
ENTALPIA (H) (h)
Es una propiedad sumamente importante en los anlisis termodinmicos. Esta propiedad
termodinmica extensiva se define como :
H = U + pV
h = u + pv
Esta propiedad termodinmica no tiene ninguna interpretacin fsica y constituye simplemente
una agrupacin de propiedades que se presentan frecuentemente en los anlisis
termodinmicos.
CALORES ESPECIFICOS (Cp) (Cv)
PROF. JAVIER TAMASHIRO H.
TERMODINAMICA
Dos propiedades termodinmicas de gran importancia estn relacionadas con la entalpa y la
energa interna de una sustancia. Estas propiedades se conocen como calor especfico a
presin constante (Cp) y calor especfico a volumen constante (Cv) y estn definidas mediante
las siguientes expresiones:
u
Cp
Cv
Cada uno de los calores especficos denota la razn de cambio de una propiedad con
respecto a la temperatura, mientras otra se mantiene constante.
Las definiciones de los calores especficos implica que:
h = f(T,p)
Cp = f(T,p)
u = f(T,v)
Cv = f(T,v)
Sin embargo, cuando los gases estn a presiones relativamente bajas, los calores especficos
dependen nicamente de la temperatura. En el caso de los lquidos y los slidos, los calores
especficos Cp y Cv son esencialmente iguales en magnitud y tambin dependen nicamente
de la temperatura.
EXPERIMENTO DE JOULE
Este experimento que lleva el nombre de James Joule, quien lo realiz por primera vez en
1843, requiere el uso del aparato mostrado en la figura.
Los tanques A y B estn sumergidos en un bao de agua. Inicialmente el tanque A contiene
aire a 22 atm de presin y el tanque B est totalmente vaco. Cuando el equilibrio trmico ha
sido alcanzado, se abre la vlvula hasta que las presiones en A y en B se igualen. Se registra
la temperatura durante el proceso y se encuentra que aquella no vara. Debido a que no hubo
variacin de la temperatura del bao de agua, Joule concluy que no existi transferencia de
calor alguna entre el agua y el aire; y como el trabajo realizado por el aire es cero (expansin
libre) determin, a partir de la primera Ley, que no hubo cambio de la energa interna del aire
durante el proceso. Adems observ que durante el proceso la presin y el volumen del aire
se modificaron, mientras que la temperatura y la energa interna permanecieron invariables. A
partir de estas observaciones concluy que: LA ENERGIA INTERNA DE UN GAS IDEAL ES
SOLO FUNCION DE LA TEMPERATURA (esto se conoce como la Ley de Joule).
Por extensin: la ENTALPIA de un gas ideal tambin depende slo de la temperatura.
TERMOMETRO
PARED ADIABATICA
AIRE
vaco
AGUA
PROF. JAVIER TAMASHIRO H.
TERMODINAMICA
ii
PONTIFICIA UNIVERSIDAD CATOLICA DEL PERU
MECANICA
FACULTAD DE CIENCIAS E INGENIERIA
ENERGIA
SECCION INGENIERIA
AREA DE
RELACIONES ENTRE LOS CALORES ESPECIFICOS
Cp Cv = R
k = Cp / Cv
Cp = (k R) / (k 1)
Cv = R / (k 1)
CAMBIO DE ENERGIA INTERNA Y ENTALPIA (masa constante)
Sustancia pura:
Gases ideales (Cp y Cv constantes):
U12 = U2 U1 = m (u2 u1)
U = m Cv (T2 T1)
H12 = H2 H1 = m (h2 h1)
H = m Cp (T2 T1)
u12 = u2 u1
u = Cv (T2 T1)
h12 = h2 h1
h = Cp (T2 T1)
CALOR PARA DIFERENTES PROCESOS
Considerando que el nico trabajo presente es el de cambio de volumen, que las energas
cintica y potencial son despreciables y que el proceso es sin friccin, la ecuacin de la
primera ley quedara expresada:
q = u + p dv
Proceso
ISCORO
ISOBRICO
Primera ley (sustancia pura/gas ideal)
q u u2 - u1
q u p v h h2 - h1
pv=C
q u p v ln
p vn = C
q u
PROF. JAVIER TAMASHIRO H.
v2
v1
p 2 v 2 p1 v1
1 - n
TERMODINAMICA
iii
Proceso
Primera ley para gas ideal
(con calores especficos constantes)
ISOCORO
q u u2 - u1 = Cv (T2 - T1)
ISOBARICO
ISOTERMICO
pv=C
q u p v h Cp (T2 - T1 )
q p v ln
v2
v
R T ln 2
v1
v1
q u
p 2 v 2 p1 v1
1 - n
Cp - n Cv
1 n
T2 T1
POLITROPICO
p vn = C
k - n
1- n
q Cv
T2 - T1
q = Cn (T2 T1)
k - n
k - 1
PROF. JAVIER TAMASHIRO H.
wV
TERMODINAMICA
iv
Vous aimerez peut-être aussi
- MapaConceptual TransductoresDocument4 pagesMapaConceptual Transductoresmarieth ruiz lopezPas encore d'évaluation
- Unidad 4Document22 pagesUnidad 4EMILIOPas encore d'évaluation
- Unidad 2 - MantenimientoDocument29 pagesUnidad 2 - MantenimientoOctavio GamasPas encore d'évaluation
- Termodinamica Unidad 2 Gases Ideales y Sustancia PuraDocument55 pagesTermodinamica Unidad 2 Gases Ideales y Sustancia PuraLee-hoo Transe Beeath100% (2)
- Cp3 - Ciclo Brayton Ideal y RealDocument17 pagesCp3 - Ciclo Brayton Ideal y RealNelzon Mamani100% (1)
- 1.6 Elementos de Control EléctricoDocument9 pages1.6 Elementos de Control EléctricoyeseniaPas encore d'évaluation
- Examen Unidad 4 ResueltoDocument2 pagesExamen Unidad 4 ResueltoDann De JesusPas encore d'évaluation
- Ingeniería Electromecánica.: Máquinas Y Equipos Térmicos 1. Complemento de La Unidad 1Document13 pagesIngeniería Electromecánica.: Máquinas Y Equipos Térmicos 1. Complemento de La Unidad 1Kevin PerezPas encore d'évaluation
- Unidad No. 1 Componentes de Un Sistema Neumatico e Hid.Document21 pagesUnidad No. 1 Componentes de Un Sistema Neumatico e Hid.gonzalezlazaro5100% (1)
- Problemas de Ciclo Rankine Ideal de VaporDocument33 pagesProblemas de Ciclo Rankine Ideal de VaporManuel Xool HerreraPas encore d'évaluation
- Máquina de Fluidos IncompresiblesDocument6 pagesMáquina de Fluidos IncompresiblesLuis MenaPas encore d'évaluation
- Las Condiciones de Diseño para Las Principales Ciudades de MéxicoDocument8 pagesLas Condiciones de Diseño para Las Principales Ciudades de Méxicokevinmc 181Pas encore d'évaluation
- Tema 3 Aire Acondicionado y Confort Parte IIDocument11 pagesTema 3 Aire Acondicionado y Confort Parte IICarlos BarbaPas encore d'évaluation
- Unidad V Transmisiones HidráulicasDocument4 pagesUnidad V Transmisiones HidráulicasRoberto Tapia LópezPas encore d'évaluation
- Practica 5 Elec PotenciaDocument12 pagesPractica 5 Elec PotenciaAdriana NavarretePas encore d'évaluation
- Sistemas de Refrigeracion Ciclo de AireDocument3 pagesSistemas de Refrigeracion Ciclo de AireDavid BeltranPas encore d'évaluation
- Ensayo Mantenimiento Preventivo Wuisbely PortilloDocument6 pagesEnsayo Mantenimiento Preventivo Wuisbely PortilloJose Barboza100% (1)
- Analisis de Masa y Energia para Volumen de ControlDocument20 pagesAnalisis de Masa y Energia para Volumen de ControlPatricio Torrejon50% (2)
- Experimentos Condensación Tipo Gota y PelículaDocument16 pagesExperimentos Condensación Tipo Gota y PelículaDavid Acosta100% (1)
- Unidad 6-Maquina de Fluidos CompresiblesDocument21 pagesUnidad 6-Maquina de Fluidos Compresibles97QUITOPas encore d'évaluation
- Reporte de Residencias VeronicaDocument37 pagesReporte de Residencias VeronicaJuan Pedro LopezPas encore d'évaluation
- U4. - Autómatas ProgramablesDocument33 pagesU4. - Autómatas Programableserik vazquez jimenezPas encore d'évaluation
- Pastor Nolo BorresDocument26 pagesPastor Nolo BorresJose Alfredo Pastor HernandezPas encore d'évaluation
- Concepto de Energía Interna y Entalpía PDFDocument3 pagesConcepto de Energía Interna y Entalpía PDFJanda210711Pas encore d'évaluation
- Desplazamiento Angular y LinealDocument6 pagesDesplazamiento Angular y LinealDavid SantillánPas encore d'évaluation
- PROBLEMAS Diaz David y Vasquez MaritzaDocument1 pagePROBLEMAS Diaz David y Vasquez MaritzamariitzaPas encore d'évaluation
- El Ciclo de Rankine SobrecalentadoDocument12 pagesEl Ciclo de Rankine SobrecalentadoJean Pierre Rivera Baldeon100% (1)
- TermoDocument9 pagesTermoChiani HernandezPas encore d'évaluation
- Tarea Refrigeracion2Document10 pagesTarea Refrigeracion2Guillermo PadillaPas encore d'évaluation
- 5.7 Temperaturas A Punto de RocioDocument5 pages5.7 Temperaturas A Punto de RocioMarlon BrandonPas encore d'évaluation
- Ciclos de Potencia A Vapor PDFDocument39 pagesCiclos de Potencia A Vapor PDFCQ StalinPas encore d'évaluation
- 3.3 Flexibilidad Del Personal de MantenimientoDocument9 pages3.3 Flexibilidad Del Personal de MantenimientoMaresa AntonioPas encore d'évaluation
- Marco Teórico Turbomaquinas Por Kelvin Ariel Yanes SortoDocument4 pagesMarco Teórico Turbomaquinas Por Kelvin Ariel Yanes SortoLuis Alonso Argueta MartínezPas encore d'évaluation
- Arrastre Debido A Fricción y PresiónDocument10 pagesArrastre Debido A Fricción y PresiónDaniel NúñezPas encore d'évaluation
- 4 Turbinas de GasDocument21 pages4 Turbinas de GasDaniel SGPas encore d'évaluation
- Ciclos TermodinámicosDocument7 pagesCiclos TermodinámicosKeven ChavarríaPas encore d'évaluation
- Práctica 9 - Corrección Del Factor de Potencia Rev2 PDFDocument3 pagesPráctica 9 - Corrección Del Factor de Potencia Rev2 PDFAndrea Flores MaldonadoPas encore d'évaluation
- Unidad 3 Mantenimiento PreventivoDocument12 pagesUnidad 3 Mantenimiento PreventivoAldo SalazarPas encore d'évaluation
- Ciclo Brayton Con InterenfriamientoDocument7 pagesCiclo Brayton Con InterenfriamientoEdy AlmengorPas encore d'évaluation
- Investigación 1 Máquinas y Equipos Térmicos IIDocument26 pagesInvestigación 1 Máquinas y Equipos Térmicos IICarlos Martinez VazquezPas encore d'évaluation
- Unidad V Aplicacion de La Normatividad VigenteDocument14 pagesUnidad V Aplicacion de La Normatividad Vigentejavier50% (4)
- Amef TurbinaDocument2 pagesAmef TurbinaDaniel López100% (1)
- Separata toleranciasProfAltunaDocument7 pagesSeparata toleranciasProfAltunajulitomonkdaPas encore d'évaluation
- UNIDAD 5 EntropiaDocument37 pagesUNIDAD 5 EntropiaCamila Paz Cuadra RiosPas encore d'évaluation
- La Función de TransferenciaDocument3 pagesLa Función de TransferenciaGabrielle PotterPas encore d'évaluation
- Conducción en Régimen TransitorioDocument4 pagesConducción en Régimen TransitorioerikaPas encore d'évaluation
- 4.1 Higiene y Seguridad IndustrialDocument4 pages4.1 Higiene y Seguridad IndustrialCarlos A-v Skate SibajaPas encore d'évaluation
- REPORTE #4 Labview PDFDocument6 pagesREPORTE #4 Labview PDFJesús EHPas encore d'évaluation
- Transferencia de Calor Con Cambio de FaseDocument20 pagesTransferencia de Calor Con Cambio de FaseAbraham LeyvaPas encore d'évaluation
- Investigación de La Unidad 5, Métodos Numéricos (Método de Euler)Document8 pagesInvestigación de La Unidad 5, Métodos Numéricos (Método de Euler)Jesús Alexander MejíazPas encore d'évaluation
- Ecuaciones de Estado Del Gas IdealDocument30 pagesEcuaciones de Estado Del Gas IdealSneider CastañedaPas encore d'évaluation
- Cálculos y Selección de Formulas de VentiladoresDocument3 pagesCálculos y Selección de Formulas de VentiladoresHomero Uc MayPas encore d'évaluation
- SIMBOLOGIADocument9 pagesSIMBOLOGIADani SosaPas encore d'évaluation
- Primera Ley de La Termodinámica Unidad 3Document12 pagesPrimera Ley de La Termodinámica Unidad 3Juan Obdulia Villagrana100% (1)
- Análisis de Masa y Energía de Volúmenes de Control TermodinamicaDocument7 pagesAnálisis de Masa y Energía de Volúmenes de Control TermodinamicajosePas encore d'évaluation
- Factores de SuciedadDocument1 pageFactores de SuciedadBrenda BecerrilPas encore d'évaluation
- Montajes y Tecnicas de AlimentacionDocument25 pagesMontajes y Tecnicas de AlimentacionVictor LopezPas encore d'évaluation
- Conceptos Fundamentales de Circuitos de Corriente DirectaDocument1 pageConceptos Fundamentales de Circuitos de Corriente Directajimmy hurtadoPas encore d'évaluation
- Marco TeoricoDocument6 pagesMarco TeoricoMarysabel SánchezPas encore d'évaluation
- La Identidad TermodinámicaDocument8 pagesLa Identidad TermodinámicaFrancoDavidHuamanQuispePas encore d'évaluation
- Cinema de Velocidades y AceleracionesDocument2 pagesCinema de Velocidades y AceleracionesfatamariPas encore d'évaluation
- RM2 Lab5 Ajuste Por Contraccion 2018-1Document3 pagesRM2 Lab5 Ajuste Por Contraccion 2018-1fatamariPas encore d'évaluation
- RM2 Lab3 Vigas Continuas 2018-1Document7 pagesRM2 Lab3 Vigas Continuas 2018-1fatamariPas encore d'évaluation
- RM2 Lab1 Resortes 2018-1Document6 pagesRM2 Lab1 Resortes 2018-1fatamariPas encore d'évaluation
- 01 Objetivos - Quinta UnidadDocument2 pages01 Objetivos - Quinta UnidadfatamariPas encore d'évaluation
- Termo-Informe Balance de MotorDocument41 pagesTermo-Informe Balance de MotorfatamariPas encore d'évaluation
- Solucionario de Problemas de FisicaDocument32 pagesSolucionario de Problemas de Fisicaelcaminanteblue126457% (44)
- P-090-AR-tcm68-9748 Bombas Vacio KaeserDocument2 pagesP-090-AR-tcm68-9748 Bombas Vacio KaeserLENDPas encore d'évaluation
- Practica 3 - PolimerizacionDocument3 pagesPractica 3 - PolimerizacionRodolfo Perez MendezPas encore d'évaluation
- AtmosfericaDocument11 pagesAtmosfericaYaneth Patarroyp100% (1)
- Dinamica Practica-7 XDDocument8 pagesDinamica Practica-7 XDRoderick Cervantes100% (1)
- Manual Entrenamiento KSB CSBDocument226 pagesManual Entrenamiento KSB CSBFrancisco Javier Rivero Moreno100% (1)
- Modulo Extracción PDFDocument106 pagesModulo Extracción PDFMige Angel CastroPas encore d'évaluation
- Clase 5 - SolucionesDocument63 pagesClase 5 - Solucionesapi-3702222100% (5)
- Propiedades de La MateriaDocument4 pagesPropiedades de La MateriaSalas Castro J MPas encore d'évaluation
- Como Se Produce La Energía Eléctrica en VenezuelaDocument26 pagesComo Se Produce La Energía Eléctrica en VenezuelaAida OstoPas encore d'évaluation
- Sonido en El MarDocument1 pageSonido en El MarJose EnriquePas encore d'évaluation
- Jose - Silva - Tarea - Semana - 5Document7 pagesJose - Silva - Tarea - Semana - 5Miguel Angel Barrera MuñozPas encore d'évaluation
- Tarea Fisica U5Document5 pagesTarea Fisica U5Andrea JoselynPas encore d'évaluation
- Dilatación TermicaDocument11 pagesDilatación Termicagustavo adolfoPas encore d'évaluation
- 2019 Cuestionario Unidad 3 PDFDocument4 pages2019 Cuestionario Unidad 3 PDFJennifer A. PatiñoPas encore d'évaluation
- Acondicionamiento Ambiental / PortafolioDocument17 pagesAcondicionamiento Ambiental / PortafolioTamara CadilloPas encore d'évaluation
- ¿Qué Voy A Aprender?: SABERES PREVIOS: ¿Qué Causa Que Un Cuerpo Cambie Su Velocidad? Piensa y RespondeDocument16 pages¿Qué Voy A Aprender?: SABERES PREVIOS: ¿Qué Causa Que Un Cuerpo Cambie Su Velocidad? Piensa y RespondeTatianaFrancoPas encore d'évaluation
- Pala HidraulicaDocument6 pagesPala HidraulicaMaria Mïly ChuctayaPas encore d'évaluation
- Tostacion Concentrados Cobre Alto Contenido ArsenicoDocument7 pagesTostacion Concentrados Cobre Alto Contenido ArsenicoRichard ApazaPas encore d'évaluation
- Declinacion MagneticaDocument8 pagesDeclinacion MagneticaRodrigo AlejoPas encore d'évaluation
- Digital Heat PipeDocument4 pagesDigital Heat PipeRobin GomezPas encore d'évaluation
- Tema 2 de HidraulicaDocument7 pagesTema 2 de HidraulicamarlinPas encore d'évaluation
- Asignacion 2 Control 2021Document1 pageAsignacion 2 Control 2021Rigoberto GonzalezPas encore d'évaluation
- Proyecto Unidad 4Document18 pagesProyecto Unidad 4Jose MarianoPas encore d'évaluation
- Principios de Bioenergética 1a ClaseDocument33 pagesPrincipios de Bioenergética 1a ClaseGabriel GuerreroPas encore d'évaluation
- Trabajo 10Document3 pagesTrabajo 10Heverth Fabian Romero MartinezPas encore d'évaluation
- 6 Portico TraslacionalDocument19 pages6 Portico TraslacionalYleyam Q AicragPas encore d'évaluation
- Asig. Nº25, Termo Ii, Grupo Nº1, 2020-IiiDocument10 pagesAsig. Nº25, Termo Ii, Grupo Nº1, 2020-IiirubiPas encore d'évaluation
- 3ro de Secundaria SolucionDocument3 pages3ro de Secundaria SolucionKaterin FrancoPas encore d'évaluation
- Dilatacion TermicaDocument13 pagesDilatacion TermicaPaula CampoPas encore d'évaluation