Académique Documents
Professionnel Documents
Culture Documents
FISICOQUÍMICA II-Orden reacción métodos
Transféré par
LaArlequinaTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
FISICOQUÍMICA II-Orden reacción métodos
Transféré par
LaArlequinaDroits d'auteur :
Formats disponibles
FISICOQUMICA II
Dra. Luz M. Rodrguez Valdez
PROBLEMAS 2
OBJETO DE ESTUDIO 3
Determinacin del orden de reaccin: Mtodo de Integracin y Diferencial.
1. El ciclobutano se descompone a etileno, de acuerdo con la ecuacin
Determine el orden de reaccin y la constante de rapidez basndose en las presiones siguientes, que
se registraron cuando se realiz la reaccin a 430C en un recipiente de volumen constante.
Tiempo/s
PC4H8/mmHg
400
2000
316
4000
248
6000
196
8000
155
10000
122
2. Para la descomposicin de la glucosa en solucin acuosa se obtuvieron los siguientes resultados:
[glucosa]
mmol dm-3
56.0
55.3
54.2
52.5
49.0
tiempo
min
0
45
120
240
480
Demustrese que la reaccin es de primero orden y calclese la constante de velocidad para el proceso y el
tiempo de vida media para la glucosa bajo estas condiciones.
3. Slater [J Chem. Soc. 85 (1904), 286] obtuvo los siguientes datos cinticos para la reaccin entre el
tiosulfato sdico y el yoduro de metilo a 25C, estando expresadas las concentraciones en unidades
arbitrarias.
0
4.75
10.0
20.0
35.0
55.0
[Na2S2O3]
35.35
30.5
27.0
23.2
20.3
18.6
17.1
[CH3I]
18.25
13.4
9.9
6.1
3.2
1.5
Tiempo /min
Demustrese que la reaccin es de segundo orden.
4. La saponificacin del acetato de etilo en disolucin de hidrxido sdico a 30C.
CH3CO2C2H5 + NaOH CH3CO2Na + C2H5OH
fue estudiada por Smith y Lorenson [J. Am. Chem. Soc. 61 (1939) 117]. Las concentraciones iniciales de
ster y lcali fueron ambas de 0.05 mol dm -3 y se midi la variacin de la concentracin de ster X en los
siguientes tiempos:
103 X / mol dm-3
5.91
11.42
16.30
22.07
27.17
31.47
36.44
Tiempo / min
15
24
37
53
83
Determine el orden y la constante de velocidad para la reaccin.
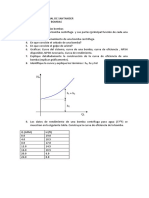
5. Los siguientes datos fueron obtenidos para la hidrlisis de un azcar en disolucin acuosa a 23C.
Tiempo / min
Concentracin de azcar
Mol dm-3
60
130
180
1.000
0.807
0.630
0.531
Demuestre que la reaccin es de primer orden y calclese la constante de velocidad para la hidrlisis.
6. La reaccin entre la trietilamina y el yoduro de metilo da una amina cuaternaria:
(C2H5)3N + CH3I CH3(C2H5)3NI
A 20C con concentraciones iniciales [amina] 0=[CH3I]0=0.224 mol dm-3 en disolucin en tetracloruro de
carbono, se sigue la reaccin por medio de la determinacin de la amina que no ha reaccionado
potenciomtricamente, obtenindose los siguientes resultados:
Tiempo / min
Concentracin de amina
Mol dm-3
10
40
90
150
300
0.212
0.183
0.149
0.122
0.084
Demuestre que la reaccin es de orden total dos y calcule la constante de velocidad.
7. Dos sustancias A y B se transforman mediante una reaccin bimolecular. La siguiente tabla da las
concentraciones de A en varios tiempos para un experimento llevado a cabo a temperatura
constante de 17C.
104 [A] / mol dm-3
Tiempo / min
10.00
7.94
6.31
5.01
3.98
10
20
30
40
La concentracin inicial de B es 2.5 mol dm -3. Calclese la constante de velocidad de segundo orden para la
reaccin.
Vous aimerez peut-être aussi
- P4 - Analisis Granulometrico de Un Material Polidisperso A Traves de La Técnica de TamizadoDocument5 pagesP4 - Analisis Granulometrico de Un Material Polidisperso A Traves de La Técnica de TamizadoJORGE ANDRES ARIAS BATALLASPas encore d'évaluation
- Ley de ErgùnDocument3 pagesLey de Ergùncoreano63Pas encore d'évaluation
- Filtracion A PresionDocument9 pagesFiltracion A Presionyudmily chambi callohuancaPas encore d'évaluation
- Reporte de Laboratorio 1 PSM115 2Document17 pagesReporte de Laboratorio 1 PSM115 2Stefany Mariela Pineda AyalaPas encore d'évaluation
- Informe 4Document5 pagesInforme 4Nunciely Rando Rodriguez100% (1)
- Proc Ind CristlizacionDocument9 pagesProc Ind CristlizacionFiorella0% (2)
- Difusion +ebull+condensDocument4 pagesDifusion +ebull+condensZhakaDeVirgoPas encore d'évaluation
- Práctica de Evaporador de Película AscendenteDocument7 pagesPráctica de Evaporador de Película AscendenteEsperanza ArellanoPas encore d'évaluation
- Inmovilizacion de Enzimas Por El Método de Atrapamiento en AgarDocument3 pagesInmovilizacion de Enzimas Por El Método de Atrapamiento en AgarRober Paredes100% (1)
- Métodos de estructura electrónica y química computacionalDocument11 pagesMétodos de estructura electrónica y química computacionalSandra SalazarPas encore d'évaluation
- PRACTICA PROPUESTA - Filtración Continúa en Un Filtro Tambor Rotatorio.Document4 pagesPRACTICA PROPUESTA - Filtración Continúa en Un Filtro Tambor Rotatorio.Marco Sanchez OlayaPas encore d'évaluation
- Lab DifusividadDocument26 pagesLab DifusividadJhon0% (1)
- Unidad 8 Flujo de Fluidos Compresibles 8 Marzo 2016Document68 pagesUnidad 8 Flujo de Fluidos Compresibles 8 Marzo 2016Samantha Elizabeth Borjón CastroPas encore d'évaluation
- El Punto IsoeléctricoDocument9 pagesEl Punto IsoeléctricoDainer SalgadoPas encore d'évaluation
- Aplicaciones DisolucionesDocument13 pagesAplicaciones DisolucionesAdrián PilataxiPas encore d'évaluation
- Lab 1Document26 pagesLab 1Samuel RomeroPas encore d'évaluation
- 05 Fluidos de Perforación y CompletaciónDocument1 page05 Fluidos de Perforación y Completaciónivan martinez olivares0% (1)
- Practica 7Document9 pagesPractica 7CesarPas encore d'évaluation
- Asignación Destilación FINALDocument34 pagesAsignación Destilación FINALJAMIT GUZMAN MARTINEZPas encore d'évaluation
- Informe Reactor DiscontinuoDocument24 pagesInforme Reactor DiscontinuoPABLOPas encore d'évaluation
- QuimiostatoDocument33 pagesQuimiostatoMarco Antonio0% (1)
- Bfde U2 Ea EmmgDocument5 pagesBfde U2 Ea EmmgEmmanuel Mendoza GonzalezPas encore d'évaluation
- Problemas de FluidizacionDocument6 pagesProblemas de FluidizacionJose Luis Chumpitaz ZáratePas encore d'évaluation
- Probl Res IADocument46 pagesProbl Res IArobertoam15100% (2)
- Procesos de transporte. Parte 2Document4 pagesProcesos de transporte. Parte 2Iza AlegríaPas encore d'évaluation
- Extracción Sólido-Líquido PDFDocument23 pagesExtracción Sólido-Líquido PDFAle BernalPas encore d'évaluation
- 3 TrabajoDocument4 pages3 TrabajoMilagrosCabanillasInfantes100% (1)
- Practica 8 2017Document3 pagesPractica 8 2017oniatrdPas encore d'évaluation
- Parcial FinalDocument3 pagesParcial FinalSebastian OcampoPas encore d'évaluation
- Intercambiadores de Tubo en TuboDocument16 pagesIntercambiadores de Tubo en TuboJosseline ScarPas encore d'évaluation
- Problemas Manejo MecánicoDocument11 pagesProblemas Manejo MecánicoLiliana OliverosPas encore d'évaluation
- Problema de Lecho FluidizadoDocument1 pageProblema de Lecho FluidizadoDiana Cueva MillaPas encore d'évaluation
- Tarea 3 SeguridadDocument12 pagesTarea 3 SeguridadAlejandra Fabiola CadenasPas encore d'évaluation
- Operación de filtración en ingeniería agroindustrialDocument19 pagesOperación de filtración en ingeniería agroindustrialFlor Elena Valles Rojas100% (1)
- Agitación en fermentación: transferencia de oxígeno y suspensión de célulasDocument4 pagesAgitación en fermentación: transferencia de oxígeno y suspensión de célulasMary Anel Cuervo MedinaPas encore d'évaluation
- Balance de Materia Con Reaccion QuimicaDocument7 pagesBalance de Materia Con Reaccion QuimicaDysarth Peraza Magallanes100% (1)
- ING Biorreactores Mezclado, Trans Calor y MasaDocument2 pagesING Biorreactores Mezclado, Trans Calor y MasaDaniel Alberto Velázquez VillarrealPas encore d'évaluation
- Ejercicios de Estequiometría - 3 - 6 - 7-8-9Document8 pagesEjercicios de Estequiometría - 3 - 6 - 7-8-9María Sánchez MontesPas encore d'évaluation
- Reduccion de Tamao 160213185543Document19 pagesReduccion de Tamao 160213185543manoloPas encore d'évaluation
- Lem V PDFDocument61 pagesLem V PDFChinno Moya RamirezPas encore d'évaluation
- Metodos Numericos TP T1Document13 pagesMetodos Numericos TP T1Xhare GarciaPas encore d'évaluation
- Caracterización de SólidosDocument8 pagesCaracterización de SólidosJesicaCarrascalPas encore d'évaluation
- Actividad Transf de MasaDocument6 pagesActividad Transf de Masalissette alvaradoPas encore d'évaluation
- Ecología Proyecto III Canastas de PET FMADocument7 pagesEcología Proyecto III Canastas de PET FMAJosee MaayaPas encore d'évaluation
- CROMATOGRAFIADocument4 pagesCROMATOGRAFIAalvaro zapPas encore d'évaluation
- Clase de Repaso para El Primer Parcial Clase 6Document5 pagesClase de Repaso para El Primer Parcial Clase 6lolaPas encore d'évaluation
- 08-1 GUIA Cap. 11 EsferasDocument4 pages08-1 GUIA Cap. 11 EsferasElza PatoPas encore d'évaluation
- Bombas Centrífugas: Funcionamiento, Curvas y Prevención de CavitaciónDocument4 pagesBombas Centrífugas: Funcionamiento, Curvas y Prevención de Cavitaciónmaria julianaPas encore d'évaluation
- TAMARINDO Primer SeminarioDocument22 pagesTAMARINDO Primer SeminarioBelen Brito MuñozPas encore d'évaluation
- Ejercicio 1Document5 pagesEjercicio 1Daniel LautaroPas encore d'évaluation
- Coeficiente difusión CO2 aire 20°CDocument5 pagesCoeficiente difusión CO2 aire 20°CJesús BuenoPas encore d'évaluation
- Ecuación de Monod para cinética microbiana en reactoresDocument2 pagesEcuación de Monod para cinética microbiana en reactoresAle SuaznabarPas encore d'évaluation
- Ejercicios Conducción Calor UnidimensionalDocument4 pagesEjercicios Conducción Calor UnidimensionalDiego Alejandro Castaño BarragánPas encore d'évaluation
- Operaciones de SeparaciónDocument13 pagesOperaciones de SeparaciónfepafuPas encore d'évaluation
- Determinación de Los Parámetros de Transferencia de Calor Durante El Freido de Carne de HamburguesaDocument3 pagesDeterminación de Los Parámetros de Transferencia de Calor Durante El Freido de Carne de HamburguesaMeli CastañoPas encore d'évaluation
- Informe 2 TecnologiasDocument17 pagesInforme 2 TecnologiasCamila RodriguezPas encore d'évaluation
- Equilibrio de fases: Un enfoque basado en competenciasD'EverandEquilibrio de fases: Un enfoque basado en competenciasPas encore d'évaluation
- Objeto 3-PROBLEMAS DE CINETICADocument2 pagesObjeto 3-PROBLEMAS DE CINETICADaniela TPas encore d'évaluation
- Tema 2Document9 pagesTema 2Pepe Pertíñez0% (1)
- Química Tarea 1Document2 pagesQuímica Tarea 1Laura LantiguaPas encore d'évaluation
- Evaluación sumativa de Química 3° y 4° MedioDocument7 pagesEvaluación sumativa de Química 3° y 4° Mediotpp 11Pas encore d'évaluation
- Introduccion MagnesioDocument1 pageIntroduccion MagnesioAimee Sangronis100% (1)
- Materiales de ImpresionDocument31 pagesMateriales de ImpresionAndrea Montero100% (1)
- Revista ION 0120-100X: Issn: Revistaion@uis - Edu.coDocument13 pagesRevista ION 0120-100X: Issn: Revistaion@uis - Edu.coEdwin RojasPas encore d'évaluation
- Muestreo - 4Document9 pagesMuestreo - 4Hans JaramilloPas encore d'évaluation
- Determinación de Carbonato y Bicarbonato en Una Muestra de AguaDocument2 pagesDeterminación de Carbonato y Bicarbonato en Una Muestra de Agualeandro raimundoPas encore d'évaluation
- P1 - Equilibrio QuímicoDocument8 pagesP1 - Equilibrio QuímicosantiagoPas encore d'évaluation
- Biomoléculas y funcionesDocument7 pagesBiomoléculas y funcionesRobinson Gonzalez GomezPas encore d'évaluation
- Informe de TP de Química OrgánicaDocument22 pagesInforme de TP de Química OrgánicaGrafi PackPas encore d'évaluation
- Q - AUNI - Dir - Sem 35Document3 pagesQ - AUNI - Dir - Sem 35Elizabeth Lucero Huanaco HuaytaPas encore d'évaluation
- IntroducciónDocument11 pagesIntroducciónwolowitz_8Pas encore d'évaluation
- Practica 11. Obtencion de n-BUTIRALDEHIDDocument5 pagesPractica 11. Obtencion de n-BUTIRALDEHIDLuis AngelPas encore d'évaluation
- Desnaturalización de ProteínasDocument6 pagesDesnaturalización de Proteínasvanesa aldaoPas encore d'évaluation
- Extracción aceite almendras dulcesDocument1 pageExtracción aceite almendras dulcesAlejandro Torres FloresPas encore d'évaluation
- BIOMOLÉCULAS INORGÁNICAS-TaniaDocument2 pagesBIOMOLÉCULAS INORGÁNICAS-TaniaPaola ÁngelesPas encore d'évaluation
- Alimentos y Golosinas Información NutricionalDocument18 pagesAlimentos y Golosinas Información NutricionalJulioPas encore d'évaluation
- Grupo FuncionalDocument4 pagesGrupo FuncionalIrene CuevasPas encore d'évaluation
- NMX-AA - 047 Determinacion de MercurioDocument4 pagesNMX-AA - 047 Determinacion de MercuriorrollerPas encore d'évaluation
- Sintesis Del Complejo de CoordinacionDocument2 pagesSintesis Del Complejo de CoordinacionesliPas encore d'évaluation
- Acetato IsoamiloDocument7 pagesAcetato IsoamiloRomario SansoresPas encore d'évaluation
- Sales - QUIMICADocument4 pagesSales - QUIMICAJames ArredondoPas encore d'évaluation
- QUÍMICA INORGANICA HidrogenoDocument21 pagesQUÍMICA INORGANICA HidrogenoFederico David FloresPas encore d'évaluation
- Medidas de Seguridad en El LaboratorioDocument5 pagesMedidas de Seguridad en El LaboratorioalexanderPas encore d'évaluation
- Acido Acetico A Partir de Alcohol EtilicoDocument3 pagesAcido Acetico A Partir de Alcohol EtilicoRicardo Martinez CastillejosPas encore d'évaluation
- Funciones Químicas: Práctica #4Document6 pagesFunciones Químicas: Práctica #4DANIEL JOEL RAMIREZ REYESPas encore d'évaluation
- 7 LipidosDocument49 pages7 LipidosValePas encore d'évaluation
- Historia Critica de BoliviaDocument7 pagesHistoria Critica de BoliviaCarlos Cornelio Choque QuispePas encore d'évaluation
- PAUAcido Base Es EnuncDocument5 pagesPAUAcido Base Es Enuncrsanchez349Pas encore d'évaluation
- Dioxido de CobreDocument6 pagesDioxido de CobreLander Chavez MedranoPas encore d'évaluation
- Informe Técnico Manejo de Sustancias Controladas SICOQDocument17 pagesInforme Técnico Manejo de Sustancias Controladas SICOQSandra Pita100% (3)