Académique Documents
Professionnel Documents
Culture Documents
Exp 7
Transféré par
Gonzalvus Sandoval RiquelmeDescription originale:
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Exp 7
Transféré par
Gonzalvus Sandoval RiquelmeDroits d'auteur :
Formats disponibles
UNIVERSIDAD TCNICA FEDERICO SANTA MARA
CAMPUS SANTIAGO
LABORATORIO FIS 130
PRIMER SEMESTRE 2016
CALOR LATENTE
Emilio Luchsinger, Rol 201341504-0, emilio.luchsinger.13@sansano.usm.cl, 363 A
Gonzalo Sandoval, Rol 201410523-1, gonzalo.sandoval.14@sansano.usm.cl, 363 A
1. Resumen
En el presente experimento se masar una cantidad de
agua dada, agua que tiene una temperatura en un rango de
30 a 45 [ ] y esta agua estar dispuesta en un
calormetro, donde se medir la temperatura del agua, ya
que est descender hasta alcanzar el equilibrio trmico
con el calormetro. Luego se tomar un trozo de hielo a una
temperatura, que debe ser medida en el laboratorio, y ser
masado; e inmediatamente introducido al sistema, se
espera que se derrita completamente el trozo de hielo, y en
ese instante se mide la temperatura del agua, que es la del
sistema en equilibrio trmico. Todo esto para encontrar el
calor latente de un cuerpo, en este caso el calor latente de
fusin del hielo, este proceso es llamado mtodo de
mezclas.
2. Objetivos
Utilizar el mtodo de mezclas para obtener el calor
latente de un cuerpo.
Determinar el calor latente de fusin del hielo.
3. Introduccin
En los meses de verano, en algunas regiones del
planeta se registran altas temperaturas, los seres humanos
suelen refrescarse consumiendo bebestibles a bajas
temperaturas.
Este
concepto
de
bajas
temperaturas, no es ms que entrega o quitar
energa al sistema, en este caso el bebestible
debe ceder energa o calor, para bajar su
temperatura, para esto es comn ocupar hielo,
para que el bebestible y el hielo logren llegar a
un equilibrio trmico el lquido deber ceder
energa necesariamente y bajo este simple
concepto los seres humanos logramos
refrescarnos. El concepto de calor latente es
til para conocer cuanta energa o calor ceder
el lquido y por eso es importante este
concepto fsico.
4. Marco Terico
Cambios de fase
El trmino fase ser usado para describir un estado
especfico de la materia. Una transicin de una fase a otra
es un cambio de fase. Para un proceso isobrico, es decir, a
presin constante, los cambios de fase se dan a una
temperatura definida, generalmente acompaada por
absorcin o emisin de calor, y un cambio de volumen y
densidad.
Para convertir 1 [ kg ] de agua en fase liquida a
0 [ ] y a presin atmosfrica normal, se requieren
3,34 10 5 [ J ]
de calor. El calor requerido por unidad
de masa se llama calor latente de fusin, denotado por
Lf . Para el agua a presin atmosfrica normal, el color
de fusin es:
Lf =3,34 105
[ ]( )
J
1
kg
De forma ms general, para fundir una masa m
Lf se
de material con un calor latente de fusin
requiere una cantidad de calor Q dada por:
Q=m Lf ( 2 )
El proceso de fundir un material es reversible. Para
lograr esto se debe quitar calor, la magnitud es la misma,
pero ahora Q es negativa por que se quita calor en vez
de agregar. Para incluir ambas posibilidades e incluir otros
tipos de cambio de fase, esto es:
Q= m L ( 3 )
5. Montaje Experimental
Los materiales e instrumentos utilizados durante la
experiencia fueron los siguientes:
Instrumento
Resolucin
Sensor de
temperatura acero
inoxidable
0,1 [ ]
Rango
40, 135,0
[ ]
Marca
Vernier
UNIVERSIDAD TCNICA FEDERICO SANTA MARA
CAMPUS SANTIAGO
LABORATORIO FIS 130
PRIMER SEMESTRE 2016
Calormetro MSJ07051
N/a
N/a
N/e
Hervidor Inox Boil
HE 1000
N/a
N/a
Somela
Balanza electrnica
FEJ-1500
0,1 [ g ]
0,1 1500 [g]
N/e
Tabla 1: Especificaciones de los materiales utilizados durante la
experiencia, donde N/a significa no aplica y N/e no especificado.
Para el desarrollo de la experiencia se deber realizar
el siguiente montaje:
Por ltimo, se debe calcular el calor latente de fusin
del hielo por medio de la ecuacin (YX).
6. Resultados
Se tomaron medidas para el estudio del fenmeno
en tres oportunidades, por lo que los resultados sern
obtenidos como un promedio de las medidas obtenidas.
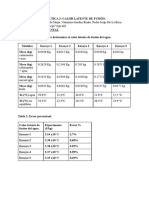
Masa de agua
Masa hielo
T o inicial
T o equilibrio
89,8
34,6
43,4
10,2
119,8
17,7
45,8
29,7
129,8
31,7
45,1
20,4
0,1 [ g ]
ma=113,1
0,1 [ g ]
mh=28,3
0,1 [ ]
t i =44,8
0,1 [ ]
te=63,3
Tabla 2: Mediciones obtenidas en el laboratorio, se indica el
promedio de ellas.
Adems, la masa del calormetro es igual a
28,9 0,1 [ g ] y la temperatura del hielo es igual a
7,7 0,1 [ ] .
Por ltimo, se obtuvieron los valores para el calor
latente de fusin del hielo, los cuales fueron:
Esquema 1: Montaje del calormetro con agua y el hielo.
Lf =3,23 105
A continuacin se describirn los pasos a seguir para
realizar la experiencia.
Lf =3,78 105
Primero se debe masar el contenedor del calormetro,
para luego llenarlo hasta la mitad aproximadamente con
agua previamente entibiada en el hervidor, lo que debe ser
masado nuevamente para obtener una medida indirecta de
la masa de agua.
Luego, es necesario registrar la temperatura del agua
en el calormetro. Y en el menor tiempo posible masar un
cubo de hielo e introducirlo en el calormetro.
El hielo comenzar a derretirse, lo cual puede ser
acelerado con el agitador del calormetro. Una vez que el
hielo se haya derretido, se registra nuevamente la
temperatura del sistema.
Los pasos anteriores se deben repetir tres veces, para
as obtener un mejor estimado del resultado. Adems, se
debe medir la temperatura del hielo.
Lf =3,65 105
[ ]
[ ]
[ ]
J
kg
J
kg
J
kg
Luego el promedio de los tres resultados es:
Lf =3,55 105
Los
errores
posteriormente.
[ ]( )
J
4
kg
asociados
sern
calculados
7. Anlisis
UNIVERSIDAD TCNICA FEDERICO SANTA MARA
CAMPUS SANTIAGO
LABORATORIO FIS 130
PRIMER SEMESTRE 2016
Como es posible observar en la ecuacin ( 2 ) , el
calor que absorbe un cuerpo al cambiar de estado es
proporcional a su masa por el calor latente, en este caso,
calor latente de fusin. Y como se sabe, el calor absorbido
o cedido por un cuerpo tambin puede ser expresado como:
un 17
de diferencia. Y adems el nuevo resultado
tiene un error porcentual con respecto al valor esperado
igual a 6,7 , lo que claramente indica que al considerar
al calormetro en el sistema, el resultado es ms cercano al
esperado.
Q=m c T ( 5 )
Como se puede apreciar, es muy simple obtener el
calor latente de fusin, simplemente al sumar ( 2 ) con
( 5 ) , lo que es igual a cero. Por lo tanto, la ecuacin
final queda de la siguiente forma:
mHielo Lf +m Hielo c T +magua c T =0 ( 6 )
donde no se toma en cuenta el efecto del calormetro en el
sistema y c es el calor especifico del agua.
Con lo anterior, es claro que mientras mayor sea la
masa de agua, la temperatura de equilibrio ser ms
cercana a su temperatura inicial, y del mismo modo con el
hielo.
En cuanto al resultado obtenido ( 4 ) , se puede
calcular el error de propagacin Lf , ya que proviene
de varias mediciones. El detalle del clculo se encuentra en
el apndice. Error
Lf =0,17 10 5
[ ]
J
kg
Adems, es posible comparar el resultado del calor
latente de fusin obtenido, con el valor esperado
[ ]
J
. De donde se obtiene un
kg
error porcentual de 12,45 .
Lf esperado =3,34 105
Como todos los datos anteriores fueron calculados sin
considerar el efecto del calormetro en el sistema, se
analizar la diferencia que se produce al considerarlo en
los clculos.
Entonces, considerando la ecuacin
ltima toma de datos, se obtiene que:
Lf =
(6)
y la
mHielo c T + m Agua c T +mcal c Al T
(7 )
m Hielo
Donde c y c Al estn en el apndice. De la
ecuacin anterior se obtiene un calor latente de fusin
Lf =3,58 105
[ ]
J
kg
Como se puede apreciar, el nuevo resultado dista
bastante del resultado original, de hecho, entre ellos existe
8. Discusin
Como bien se sabe, el calormetro utilizado no es
ideal, y a pesar de hacer un buen trabajo al aislar el sistema
del medio, esto no se logra completamente.
Por lo anterior, es que se esperan errores de algn tipo
en los resultados, y este caso no es la excepcin.
Para el primer caso, en el que se calcul el calor
latente de fusin sin considerar el calormetro de aluminio
en el sistema, se obtuvo un error para nada despreciable de
12,45 . Estos errores fueron inducidos en parte por lo
anteriormente mencionado, pero en gran medida, por no
considerar al calormetro en el sistema, ya que tambin
participa en el intercambio de energa (calor) que se
produce cuando el sistema busca encontrar el equilibrio
trmico. En cuanto a lo anterior, tambin se produce un
intercambio de calor con la tapa del calormetro, el
agitador, el termmetro y el aire que contiene. Factores que
tampoco son considerados dentro del sistema, debido a la
complejidad que este adoptara.
Como se mostr en el apartado anterior, el valor
calculado al considerar el calormetro en el sistema ( 7 )
, se acerca bastante ms al valor esperado de
3,34 10 5
[ ]
J
kg
que
el
valor
calculado
sin
considerarlo.
Adems se debe tener en consideracin que el agua
utilizada, no es agua pura, ms bien es agua con algn
porcentaje de minerales, lo cual influye ya que el calor
especfico de esta no sera el mismo.
9. Conclusin
Por medio del mtodo de mezclas se pudo obtener el
valor experimental del calor latente de un cuerpo, en esta
experiencia se trata del calor latente de fusin del hielo.
Considerando que en el sistema que se considera
existe un cambio de fase y recordando la teora y
considerando que el sistema logra el equilibrio trmico se
obtiene lo siguiente:
mHielo Lf +m Hielo c T +magua c T =0 ( 6 )
UNIVERSIDAD TCNICA FEDERICO SANTA MARA
CAMPUS SANTIAGO
LABORATORIO FIS 130
PRIMER SEMESTRE 2016
Esto es despreciando al pote de aluminio que se
encuentra al interior del calormetro, obteniendo:
[ ]
J
Lf =3,55 10
(4 )
kg
5
Luego se realiza un clculo considerando los mismos
datos pero ahora considerando el pote de aluminio del
calormetro. Esto en ecuacin se ve de la siguiente forma:
mHielo c T + m Agua c T +mcal c Al T
(7 )
m Hielo
Obteniendo un nuevo valor para el calor latente de
fusin del hielo
I. Suma y resta:
Q= A+ B C
que es el promedio de tres mediciones, y tiene un error
asociado al compararlo con el valor esperado de
12,45 .
Lf =
Error de propagacin por hiptesis estadstica:
Lf =3,58 105
[ ]
J
kg
. Y con un
nuevo error al compararlo con el valor esperado de
6,7 .
Claramente es siempre mejor el modelo que se acerca
ms a la realidad, pero a las vez la complejidad del
problema aumenta, ya que aumenta el nmero de variables
en juego.
10. Bibliografa
Q2= A 2+ B2 C 2
Sears, F. W., Zemansky, M. W., & Young, H. D.
(1972). University physics. Reading, MA: AddisonWesley.
11. Apndice
Error porcentual (error %):
|valorexperimental valor terico|
valorexperimental
100
(6)
(8)
II. Multiplicacin, divisin, potenciacin y radicacin:
Q=
Am Bn
Cp
(9)
Q
A
B
C
=m
+ n
+ p
Q
A
B
C
( ) (
)( )(
(10)
Para conocer el error de propagacin del valor Q
calculado, se despeja Q de la ecuacin (10), como
se muestra a continuacin.
Q=Q
A 2
B 2
C
+ n
+ p
A
B
C
) ( )(
(11)
Esta nueva ecuacin es equivalente a la frmula general
para determinar errores de propagacin, es decir, para una
funcin F(x, y,) el diferencial total F se expresar de la
siguiente manera.
F=
(7)
| |
df
df
x2 +
y 2 +
dx
dy
(12)
Contantes utilizadas
[
[
]
]
J
kg
J
c hielo =2090
kg
J
c Aluminio=909
kg
c agua =4186
Vous aimerez peut-être aussi
- Informe N° 3Document2 pagesInforme N° 3Carolina Alejandra Cardenas JametPas encore d'évaluation
- Calor LatenteDocument6 pagesCalor LatenteJose Manuel RojasPas encore d'évaluation
- Ingeniería química. Soluciones a los problemas del tomo ID'EverandIngeniería química. Soluciones a los problemas del tomo IPas encore d'évaluation
- 3 Medida Del Calor Latente de Fusión Del HieloDocument10 pages3 Medida Del Calor Latente de Fusión Del HieloNicole Machado TubiñezPas encore d'évaluation
- Informe Quimica 4Document9 pagesInforme Quimica 4Felipe Ignacio Ã�lvarezPas encore d'évaluation
- Informe 2 Pancho-Nico Fis130Document7 pagesInforme 2 Pancho-Nico Fis130Nico RebolledoPas encore d'évaluation
- Práctica Calor Latente de Fusión 2362Document5 pagesPráctica Calor Latente de Fusión 2362Juan Lozano AngaritaPas encore d'évaluation
- Taller de Calor LatenteDocument2 pagesTaller de Calor LatenteMaria VirginiaPas encore d'évaluation
- Calor Latente de Fusion Del HieloDocument7 pagesCalor Latente de Fusion Del HieloeliasrtPas encore d'évaluation
- Documento de HDocument9 pagesDocumento de Hcristian albarracinPas encore d'évaluation
- Informe N°3 Calor Latente de Vaporizacion Del AguaDocument7 pagesInforme N°3 Calor Latente de Vaporizacion Del AguaAntonio Jose Salcedo MartinezPas encore d'évaluation
- Lab de Fisica Calor Ondas 3Document5 pagesLab de Fisica Calor Ondas 3yirisPas encore d'évaluation
- Calor Latente de Fusion CompletoDocument4 pagesCalor Latente de Fusion CompletoJose Eduardo Villanueva FerrerPas encore d'évaluation
- 1 CalorimetroDocument4 pages1 CalorimetroAndrea ParedesPas encore d'évaluation
- Informe 2 FisicaDocument5 pagesInforme 2 FisicaElena A. GarayPas encore d'évaluation
- INFORME de Entalpia de Fusion Del HieloDocument5 pagesINFORME de Entalpia de Fusion Del HieloJuan Pablo Toro Rojas0% (1)
- TP 5 Calorimetría y TermoquímicaDocument14 pagesTP 5 Calorimetría y TermoquímicaRamiroClericiPas encore d'évaluation
- Practica 14 Laboratorio de Fisica UCMDocument7 pagesPractica 14 Laboratorio de Fisica UCMMarina Guerrero LorentePas encore d'évaluation
- Experimento N°9-CalorimetríaDocument15 pagesExperimento N°9-CalorimetríaJesus AndradesPas encore d'évaluation
- Trabajo de Laboratorio CalorimetriaDocument7 pagesTrabajo de Laboratorio CalorimetriaWalter LunaPas encore d'évaluation
- Informe 7 Calor de DisolucionDocument5 pagesInforme 7 Calor de DisolucionArilu2010100% (2)
- Fisico Quimica Informe FinalDocument12 pagesFisico Quimica Informe FinalMaria FernandaPas encore d'évaluation
- Informe de Laboratorio No 6 UaoDocument4 pagesInforme de Laboratorio No 6 UaoJuancarl000zzzPas encore d'évaluation
- Guia de TP N 3 Con ExplicacionesDocument7 pagesGuia de TP N 3 Con ExplicacionesaleinPas encore d'évaluation
- Practica 8Document6 pagesPractica 8320518980Pas encore d'évaluation
- Práctica de Laboratorio - Calor LatenteDocument6 pagesPráctica de Laboratorio - Calor LatenteSergio Luis Castaño RodriguezPas encore d'évaluation
- Reporte de TermodinamicaDocument5 pagesReporte de TermodinamicaMauricio Baltazar PerezPas encore d'évaluation
- Informe Lab Física Calor EspecíficoDocument3 pagesInforme Lab Física Calor EspecíficoMartin EliasPas encore d'évaluation
- Efecto JouleDocument7 pagesEfecto JouleVictor Parra0% (1)
- Imforme Practca PresencialDocument24 pagesImforme Practca PresencialNataly Fernanda CaranquiPas encore d'évaluation
- Determinacion Del Calor Especifico Del EtanolDocument5 pagesDeterminacion Del Calor Especifico Del EtanolEder Terres LeonPas encore d'évaluation
- Calorimetro Informe.Document7 pagesCalorimetro Informe.Joseantonio Garcia MorronPas encore d'évaluation
- U1901 Guia de Trabajos Prácticos Módulo III y IV 2020Document22 pagesU1901 Guia de Trabajos Prácticos Módulo III y IV 2020Sebastian Lizarazo SotoPas encore d'évaluation
- Práctica 8 CAMBIO DE ENTALPÍA DE FUSIÓN DE HIELODocument7 pagesPráctica 8 CAMBIO DE ENTALPÍA DE FUSIÓN DE HIELOJohann RojasPas encore d'évaluation
- Informe Fqmca #2Document12 pagesInforme Fqmca #2JUAN FELIPE SERRATO BUITRAGOPas encore d'évaluation
- Calor Latente de Fusion Del Hielo 01Document2 pagesCalor Latente de Fusion Del Hielo 01John AndradePas encore d'évaluation
- Informe 1 Qca FisicaDocument6 pagesInforme 1 Qca FisicaMatilde Santibáñez MéndezPas encore d'évaluation
- Equivalencia Del H2O en Un Calorimetro Lab VDocument4 pagesEquivalencia Del H2O en Un Calorimetro Lab VJulian PadiernaPas encore d'évaluation
- Calor de Fusión Del HieloDocument5 pagesCalor de Fusión Del HieloJuan Felipe Giraldo100% (1)
- Informe Final Fisicoquimica PDFDocument18 pagesInforme Final Fisicoquimica PDFwendys joplyPas encore d'évaluation
- Equivalente Mecanico Del CalorDocument4 pagesEquivalente Mecanico Del CalorRubiany Gonzalez QuiñonezPas encore d'évaluation
- Capacidad Calorífica y Entalpía de FusiónDocument8 pagesCapacidad Calorífica y Entalpía de FusiónVanessa Campos75% (4)
- Reporte CalorimetriaDocument10 pagesReporte CalorimetriaGibran Meza CastrejonPas encore d'évaluation
- Calor de Combusti NDocument10 pagesCalor de Combusti NXiomara Lizeth Velez DiazPas encore d'évaluation
- Calor AbsorbidoDocument18 pagesCalor AbsorbidoSandy CisnerosPas encore d'évaluation
- Entalpía de Vaporización de Un Líquido Info MateDocument8 pagesEntalpía de Vaporización de Un Líquido Info MateMaria Paula DiazPas encore d'évaluation
- 4 Calor Latnte de Fusion Del Agua NDocument6 pages4 Calor Latnte de Fusion Del Agua Npriscila92004Pas encore d'évaluation
- Informe de Práctica 8 Calor LatenteDocument6 pagesInforme de Práctica 8 Calor LatentezkdifyPas encore d'évaluation
- P3 G12 B1 Calorimetria 2023-2Document18 pagesP3 G12 B1 Calorimetria 2023-2Sospek Bloquerl PockerPas encore d'évaluation
- Título de Un Vapor HúmedoDocument6 pagesTítulo de Un Vapor HúmedoKarinita No MásPas encore d'évaluation
- Medida Del Calor Latente de Fusión Del HieloDocument7 pagesMedida Del Calor Latente de Fusión Del Hielojorgenitalesthe3rdPas encore d'évaluation
- Informe Calorimetria 3Document15 pagesInforme Calorimetria 3vaudevilleePas encore d'évaluation
- Calor de Fusion Del HieloDocument10 pagesCalor de Fusion Del HieloFranciscoLopezMartinezPas encore d'évaluation
- Práctica 7 TermodinámicaDocument10 pagesPráctica 7 TermodinámicaFDGH133333100% (1)
- Lab Calor EspecificoDocument5 pagesLab Calor Especificoفيفيان فيفيان مار مارPas encore d'évaluation
- Practica 8 Calor LatenteDocument7 pagesPractica 8 Calor LatenteFDGH133333Pas encore d'évaluation
- Ley de EnfriamientoDocument9 pagesLey de EnfriamientoJorge CastrejonPas encore d'évaluation
- TP 5 TermodinámicaDocument12 pagesTP 5 TermodinámicaOriana FarfanPas encore d'évaluation
- Parcial - Escenario 4 - PRIMER BLOQUE-TEORICO-PRACTICO - VIRTUAL - MATEMÁTICAS FINANCIERAS - (GRUPO B02)Document9 pagesParcial - Escenario 4 - PRIMER BLOQUE-TEORICO-PRACTICO - VIRTUAL - MATEMÁTICAS FINANCIERAS - (GRUPO B02)angie perezPas encore d'évaluation
- Clase 02 Medicion de PresionDocument33 pagesClase 02 Medicion de PresionWilliam Yoel CcalloPas encore d'évaluation
- Costos Unitarios CementerioDocument9 pagesCostos Unitarios CementerioEtefano Javier Arutaype SuniPas encore d'évaluation
- Cotizacion 005JS-2023-XCMGDocument1 pageCotizacion 005JS-2023-XCMGGiuliano Salvatore Mori GodoyPas encore d'évaluation
- 2-Analisis de Muda y Balance de CargasDocument34 pages2-Analisis de Muda y Balance de CargasElba Margarita Cruz RiosPas encore d'évaluation
- COLANTADocument13 pagesCOLANTASebastián AgudeloPas encore d'évaluation
- Final TALLER JUDICIAL UBADocument18 pagesFinal TALLER JUDICIAL UBAVirginia RomeroPas encore d'évaluation
- Track While Scan - FinalizadoDocument7 pagesTrack While Scan - FinalizadoJorge Andres Pino CapchaPas encore d'évaluation
- Introducción A La DFIDocument5 pagesIntroducción A La DFIjorgeluistineocorzoPas encore d'évaluation
- Taller Facturacion ElectronicaDocument6 pagesTaller Facturacion Electronicaluisa fernanda garcia sabogalPas encore d'évaluation
- Trabajo Final HT4Document11 pagesTrabajo Final HT4Carlos MortadelaPas encore d'évaluation
- Ejercicios Distribucion de Probabilidad Listos-1.Docx CompletoDocument26 pagesEjercicios Distribucion de Probabilidad Listos-1.Docx CompletoOlga Sorany Jaramillo LoaizaPas encore d'évaluation
- Actividad 1 de Gestion de CalidadDocument5 pagesActividad 1 de Gestion de CalidadedinsonPas encore d'évaluation
- ArrozDocument12 pagesArrozEduardo FriasPas encore d'évaluation
- Proceso Contravencional y Coactivo FCMDocument14 pagesProceso Contravencional y Coactivo FCMANGELA MORAPas encore d'évaluation
- Anabi SacDocument4 pagesAnabi SacBorisGuzmanPas encore d'évaluation
- Inyectores Semana 4Document48 pagesInyectores Semana 4Roy Enrrique Julca PaucarPas encore d'évaluation
- Comisiones: Cuenta Sueldo / Cuenta Previsional Concepto Precio (1) Periodicidad de CobroDocument5 pagesComisiones: Cuenta Sueldo / Cuenta Previsional Concepto Precio (1) Periodicidad de Cobroastolfo buñueloPas encore d'évaluation
- ChequesDocument6 pagesChequesJuan C. ReynosoPas encore d'évaluation
- Especificaciones IRB120Document50 pagesEspecificaciones IRB120Sonia Sanchez MansoPas encore d'évaluation
- Manual de Normas Técnicas Colombianas Gas NaturalDocument119 pagesManual de Normas Técnicas Colombianas Gas NaturalREDEGAS INGENIERIA100% (1)
- Documentos para Validar Evaluaciones Quimestrales. 2023.Document5 pagesDocumentos para Validar Evaluaciones Quimestrales. 2023.Miriam RiosPas encore d'évaluation
- Codificacion y Difusion Informacion MultimediaDocument53 pagesCodificacion y Difusion Informacion MultimediaFree MusicPas encore d'évaluation
- Infografía Historia Clínica GA3-230101280-AA1-EV02Document5 pagesInfografía Historia Clínica GA3-230101280-AA1-EV02gloria pizarroPas encore d'évaluation
- Guía Práctica #14Document14 pagesGuía Práctica #14Mitssy Navarro Quispe25% (8)
- Normas TFG ETSIT 2018 19Document6 pagesNormas TFG ETSIT 2018 19Alba Rubio FernándezPas encore d'évaluation
- Resumen de Cómo Funciona El InternetDocument3 pagesResumen de Cómo Funciona El InternetIsabel PechPas encore d'évaluation
- Como Se Origina Una NormaDocument2 pagesComo Se Origina Una NormaAntonio Gil0% (1)
- Icon-R - Checklist Tractor OrugaDocument3 pagesIcon-R - Checklist Tractor OrugaDIEGO PEDRO ROLLY CARRERA URBINAPas encore d'évaluation
- Administracion y Gestion EducativaDocument83 pagesAdministracion y Gestion EducativaElmer GarcíaPas encore d'évaluation