Académique Documents
Professionnel Documents
Culture Documents
Extraccion de La Caseina y Determinacion Del Punto Isoelectrico
Transféré par
Greily Yulieth ArdilaDescription originale:
Titre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Extraccion de La Caseina y Determinacion Del Punto Isoelectrico
Transféré par
Greily Yulieth ArdilaDroits d'auteur :
Formats disponibles
EXTRACCION DE LA CASEINA Y DETERMINACION DEL PUNTO ISOELECTRICO
EXTRACTION AND DETERMINATION CASEIN ISOELECTRIC POINT
Ardila Greilly (05242097)
Corporacin tecnolgica de Bogot, Tecnologa en Qumica Industrial
Bogot, Colombia
12/11/2015
RESUMEN
Se llev a cabo el procedimiento de
extraccin y separacin de la casena de una
muestra de leche comn, La casena es una
protena conjugada de la leche del tipo
fosfoprotena que se separa de la leche por
acidificacin y forma una masa blanca. Se
realiz la determinacin experimental del
punto isoelctrico de la protena separada
(5,2) haciendo preparacin de soluciones a
diferentes concentraciones y medida su
absorbancia en el espectrofotmetro.
Palabras clave: Protena, casena, extraccin,
Punto isoelctrico.
ABSTRACT
Carried out the process of extraction and
separation of casein from a sample of regular
milk, Casein is a milk protein conjugate of
the type phosphoprotein which is separated
from milk by acidification and forms a white
mass. Experimental determination of the
isoelectric point of the separated protein
(5.2 ) was performed by preparing solutions
at different concentrations and the absorbance
measured in a spectrophotometer .
INTRODUCCION
Una caracterstica de las protenas y otros
biopolmeros es que la carga total que
adquieren depende del pH del medio. De la
misma manera las protenas tienen una carga
neta dependiendo del pH del medio en el que
se encuentren y de los aminocidos que la
componen. La casena es una protena
conjugada de la leche del tipo fosfoprotena
que se separa de la leche por acidificacin y
forma una masa blanca. Las fosfoproteinas
son un grupo de protenas que estn
qumicamente unidas a una sustancia que
contiene cido fosfrico. En la casena la
mayora de los grupos fosfato estn unidos
por los grupos hidroxilo de los aminocidos
serina y treonina. La casena en la leche se
encuentra en forma de sal clcica (caseinato
clcico). La casena
representa cerca del 77% al 82% de las
protenas presentes en la leche y el 2,7% en
composicin de la leche lquida.
MATERIALES Y METODOS
Extraccin de la casena:
A una mezcla de agua destilada y leche
caliente se le agreg 1 mL de cido actico
1M hasta formar un precipitado, se filtr y se
agreg etanol para volver a filtrar.
Determinacin del punto isoelctrico:
A 50 mg de casena se le adicion agua
destilada, Hidrxido de potasio y se prepar
una solucin de 10 mL, los cuales se
distribuyeron los 10 tubos de ensayo (1 mL
en cada uno), a los cuales se les agreg los
volmenes correspondientes a la tabla No. 1,
y se midi la absorbancia de cada uno de
ellos a 640 nm para realizar la posterior
grfica (Grfica No. 1) de absorbancia Vs pH
RESULTADOS
TESULTADOS
ANALISIS
DE
Extraccin de la casena:
Al adicionar el cido actico a la leche se
observa un cambio en su composicin,
evidencindose una precipitacin completa,
ya que la fase lquida es traslcida y la fase
slida completamente blanca. Se puede
explicar ya que de acuerdo al cambio de pH
experimentado por la leche, inicialmente
entre 6,5 y 6,7, all la protena (casena) se
encuentra cargada negativamente solubilizada
con sal clcica, al acidificarse el pH se acerca
al punto isoelctrico de la protena, al llegar a
pH aproximado a 4,2 y 4,7 se neutraliza la
casena (los grupos fosfatos se protonan), as
se precipita debido a que hay menos
repulsiones intermoleculares, evidencindose
la separacin de estos compuestos por medio
de densidad ya que la densidad del agua es 1
g/ml quedando arriba por tener densidad ms
baja que la casena que es de 1.3g/ml, esta
separacin se da debido a que cuando las
protenas en este caso la casena se encuentra
a pH de punto isoelctrico son menos
solubles en agua y se da la separacin de la
protena y el agua.
Ca2 + Caseinato + CH3COOH
CaCOOH
Casena +
Despus de precipitada la casena, se procede
a lavado para eliminar el suero y grasas
forzando a la parte soluble de la casena con
la lactosa a cristalizar.
Determinacin del punto isoelctrico:
Con la preparacin previa de las siguientes
soluciones se prepararon la solucin para
medir su correspondiente absorbancia:
acetat
o de
sodio
0.1m
Tubo
cido
actic
o 0.1
m
cido
actic
o
0.01
m
pH
apro
x.
1
0.5
9.5
3.2
2
1
9
3.6
3
1.5
8.5
3.8
4
2
8
4
5
3
7
4.2
6
4
6
4.5
7
6
4
5
8
8
2
5.1
9
6
4
5.5
10
8
2
6.1
BLANC
2
8
4
O
Tabla No. 1. Fraccin para preparacin de
soluciones segn sus componentes a pH
aproximado.
Se obtuvieron los siguientes resultados
correspondientes a la medicin de la
absorbancia de la muestra de casena a
diferentes pH en diferentes tubos de ensayo
(10) a 640 nm:
pH
Experimenta Absorbancia
l
1
2,81
0,081
2
3,01
0,058
3
3,12
0,004
4
3,21
0,002
5
3,35
-0,004
6
3,54
0,008
7
3,85
0,010
8
4,18
0,014
9
5,20
0,040
10
7,5
0,011
Tabla No. 2 Medidas de las absorbancias de
la casena a diferentes pH en solucin.
Tubo
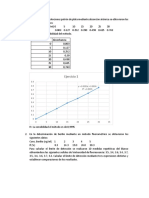
Con los anteriores datos se realiz una grfica
pH Vs Absorbancia, en la que se muestra el
comportamiento de las soluciones:
alejados a su punto isoelctrico, en el tubo
que se observa una ligera precipitacin est
indicando que la protena se ha
insolubilizado.
pH Vs absorbancia
0.1
0.05
0
-0.05
Grfica No 1. PH Vs absorbancia
Se observa la disminucin de la actividad de
la protena (casena) con referencia a su pH
debido a que cuanto est a pH alejados de su
punto isoelctrico se comporta diferente,
igual se puede notar en su inestabilidad
despus de pasar por el punto en que sus
cargas son neutras.
Derivada de absorbancia
15
10
5
0
Grfica No. 2 derivada de absorbancia
Segn la grfica el punto isoelctrico se
encuentra en (5,2), ya que se puede observar
un aumento de la absorbancia por respecto al
pH.
Al utilizar un porcentaje de error
tenemos que:
de error=
teoricoexperimental
teorico
de error=
4,75,2
100=10,6
4,7
La prueba para determinar el punto
isoelctrico de la casena no es aceptable, ya
que el porcentaje indica que se hicieron
errores en el proceso pero que son aceptables,
ya que estn cerca del rango en que precipita
la casena. las soluciones de acetato de sodio
y cido actico al 0.1 y 0.01 se usaron como
soluciones amortiguadoras que permitieron
identificar la protena ya que la casena se
solubiliza fcilmente en valores de pH
CONCLUSIONES
Se logr la debida separacin de la protena
de la leche (casena) con el proceso de
acidificacin.
Se determin el punto isoelctrico
experimental de la casena (5,2) con la
interpretacin de la grfica de pH Vs
Absorbancia
Se evidenci error en el procedimiento de
medicin de las absorbancias ya que el
porcentaje de error alcanza el 10%.
Se adoptaron conocimientos tericos y
prcticos con respecto a las protenas.
BIBLIOGRAFIA
Lehninger principios de bioqumica. Nelson,
David L., Michael M. Cox.
Fisicoqumica de molculas. Extraccin de
casena
y
determinacin
de
punto
isoelctrico. Licenciatura de Biotecnologa.
Vous aimerez peut-être aussi
- Propiedades de Las Proteínas de Origen Vegetal Obtención de Gluten o SeitánDocument3 pagesPropiedades de Las Proteínas de Origen Vegetal Obtención de Gluten o SeitánAraceli Molina RodriguezPas encore d'évaluation
- Influencia de Los Activadores e InhibidoresDocument1 pageInfluencia de Los Activadores e InhibidoresAndrés SánchezPas encore d'évaluation
- CLASE Nro. 4 ANALISIS ORGANICO - RESOLCION DE EJERCICIOSDocument14 pagesCLASE Nro. 4 ANALISIS ORGANICO - RESOLCION DE EJERCICIOSLuz IzaPas encore d'évaluation
- Practica 13Document4 pagesPractica 13PAO Escobedo0% (1)
- Laboratorio CaseínaDocument9 pagesLaboratorio CaseínaMaria Alejandra Diaz MejiaPas encore d'évaluation
- Variacion pH soluciones amortiguadorasDocument27 pagesVariacion pH soluciones amortiguadorasStefany XiomAra B SPas encore d'évaluation
- PRACTICA DE LABORATORIO No 1 CarbohidratDocument20 pagesPRACTICA DE LABORATORIO No 1 CarbohidratEdwin MontañoPas encore d'évaluation
- Práctica 2 MezcladoDocument11 pagesPráctica 2 MezcladoIlsePas encore d'évaluation
- Determinación del punto isoeléctrico de la insulina mediante análisis de solubilidad a diferentes pHDocument8 pagesDeterminación del punto isoeléctrico de la insulina mediante análisis de solubilidad a diferentes pHNathan Ulises Reyes JimenezPas encore d'évaluation
- Determinacion de Acido Fosforico en Coca Cola Mediante Titulaciones Potenciometricas PDFDocument7 pagesDeterminacion de Acido Fosforico en Coca Cola Mediante Titulaciones Potenciometricas PDFGaby Quispe AyalaPas encore d'évaluation
- Practica 1. Reacciones de CarbohidratosDocument10 pagesPractica 1. Reacciones de CarbohidratosGar AraPas encore d'évaluation
- Informe de NitraciónDocument6 pagesInforme de Nitraciónandres guerreroPas encore d'évaluation
- 8 AEDT Formacion de ComplejosDocument4 pages8 AEDT Formacion de ComplejosHéctor Fabio Hernández SánchezPas encore d'évaluation
- Síntesis de benzocaína y acetilación de amina primariaDocument7 pagesSíntesis de benzocaína y acetilación de amina primariaIsberto Martínez0% (1)
- Diagrama de Flujo Cromatografia - Diagrama de FlujoDocument1 pageDiagrama de Flujo Cromatografia - Diagrama de FlujoJosé Daniel BotinaPas encore d'évaluation
- Determinación de masa en sobres de azúcarDocument3 pagesDeterminación de masa en sobres de azúcarKatheryn RamirezPas encore d'évaluation
- Informe CaseinaDocument4 pagesInforme CaseinaVALENTINA JARAMILLO SALAZARPas encore d'évaluation
- Taller Potenciometría - Química AnalíticaDocument9 pagesTaller Potenciometría - Química AnalíticaGUSTAVO GABRIEL GÓMEZ BARBIERIPas encore d'évaluation
- Reporte Curva de Titulación de AminoácidosDocument5 pagesReporte Curva de Titulación de AminoácidosJonathan CortesPas encore d'évaluation
- Práctica Desnaturalizacion de Proteínas.Document2 pagesPráctica Desnaturalizacion de Proteínas.Karen MonserratePas encore d'évaluation
- Método Bradford proteínasDocument7 pagesMétodo Bradford proteínasjaliPas encore d'évaluation
- Informe Fosfolipasa A2Document3 pagesInforme Fosfolipasa A2MARÍA JOSÉ DAVID PUERTAPas encore d'évaluation
- Determinacion Del Isoterma de Adsorcion Practica # 3 InformeDocument4 pagesDeterminacion Del Isoterma de Adsorcion Practica # 3 InformeJose David Castro0% (1)
- Practica 4Document3 pagesPractica 4CAROLINA HERRERAPas encore d'évaluation
- Problemario MC Equipo 6Document13 pagesProblemario MC Equipo 6Andrea Renteria GuzmanPas encore d'évaluation
- Curvas de Titulación de AminoácidosDocument3 pagesCurvas de Titulación de AminoácidosGuaris Abreu Hernández100% (14)
- Bitacora No.8 PeroxisomasDocument6 pagesBitacora No.8 PeroxisomasSponja75Pas encore d'évaluation
- Articulo Del Polimorfismo Del ChocolateDocument9 pagesArticulo Del Polimorfismo Del ChocolateMarjhory AylingPas encore d'évaluation
- Titulacion de AminoacidosDocument8 pagesTitulacion de AminoacidosCharly Gonzalez100% (1)
- L11 Informe Grupo 3 BQ1 2020-2Document16 pagesL11 Informe Grupo 3 BQ1 2020-2DavidOchoaPas encore d'évaluation
- Laboratorio 1. Fraccionamiento de Tejidos (Versión Final) - Agroindustrial PDFDocument4 pagesLaboratorio 1. Fraccionamiento de Tejidos (Versión Final) - Agroindustrial PDFAndres Hurtado Saenz0% (4)
- Unidad # 6 Potenciometria DirectaDocument25 pagesUnidad # 6 Potenciometria DirectaDarkcacherPas encore d'évaluation
- Estudio Cinetico de Oxidacion de Vitamina C Con Ferrocianuro de PotasioDocument8 pagesEstudio Cinetico de Oxidacion de Vitamina C Con Ferrocianuro de PotasioDaniela AlvarezPas encore d'évaluation
- Cuestionario 1Document2 pagesCuestionario 1Iraiz VelazquezPas encore d'évaluation
- Determinacion Del Peso Molecular de Un Vapor Condensable Por Los Metodos de Dumas y de Victor MeyerDocument11 pagesDeterminacion Del Peso Molecular de Un Vapor Condensable Por Los Metodos de Dumas y de Victor MeyerSEBASTIAN ALZATE ALZATEPas encore d'évaluation
- La Deshidrogenasa SuccínicaDocument6 pagesLa Deshidrogenasa SuccínicaMercedes MolinaPas encore d'évaluation
- Informe 4 Cuanti 2Document6 pagesInforme 4 Cuanti 2Less ÁvilaPas encore d'évaluation
- Análisis de plata y berilio mediante absorción atómica y fluorometríaDocument2 pagesAnálisis de plata y berilio mediante absorción atómica y fluorometríaNatasha VargasPas encore d'évaluation
- Práctica. - No.8.1 Determinación de Colesterol en La Yema de HuevoDocument1 pagePráctica. - No.8.1 Determinación de Colesterol en La Yema de HuevoEvelyn Jim 3295100% (1)
- Condensacion Aldolica Informe 1Document40 pagesCondensacion Aldolica Informe 1Laura PerdomoPas encore d'évaluation
- Informe Resultados. Cuantitativa Carbohidratos FINALDocument4 pagesInforme Resultados. Cuantitativa Carbohidratos FINALANDRÉS STEVEN ÁLVAREZ GONZÁLEZPas encore d'évaluation
- Informe Caseina PDFDocument8 pagesInforme Caseina PDFMoni AntolinezPas encore d'évaluation
- Proceso de Extracción Del Omeprazol FinalDocument12 pagesProceso de Extracción Del Omeprazol FinalJuan DavidPas encore d'évaluation
- Cuestionario Dra. NigdDocument9 pagesCuestionario Dra. NigdChristiansito AndresitoPas encore d'évaluation
- INFORMEDocument11 pagesINFORMENatalia Ortega100% (1)
- Determinacion Gravimetrica Del HierroDocument5 pagesDeterminacion Gravimetrica Del HierroJhonny G. Mendoza Perez100% (1)
- Introducción a las azlactonasDocument3 pagesIntroducción a las azlactonasJohn Gerardo Razuri100% (1)
- Síntesis de DibenzalacetonaDocument5 pagesSíntesis de DibenzalacetonaDaniela Rios100% (1)
- Formacion de OsazonasDocument4 pagesFormacion de OsazonasPao Fonseca100% (1)
- Cuestionario 2 (8-10)Document1 pageCuestionario 2 (8-10)Heydi Vargas100% (1)
- 1014Document3 pages1014Jhoan RiveraPas encore d'évaluation
- AminoácidoDocument7 pagesAminoácidoBetty LopezPas encore d'évaluation
- Guía de Laboratorio Proteina Bruta Método KjeldahlDocument2 pagesGuía de Laboratorio Proteina Bruta Método KjeldahlFabianHPasquelPas encore d'évaluation
- Practica de LaboratorioDocument2 pagesPractica de LaboratorioMarcos Ulises OrellanaPas encore d'évaluation
- Extraccion de La Caseina y Determinacion Del Punto IsoelectricoDocument4 pagesExtraccion de La Caseina y Determinacion Del Punto IsoelectricoAnonymous T6KNhV100% (4)
- Determinación del punto isoeléctrico de la caseínaDocument3 pagesDeterminación del punto isoeléctrico de la caseínaDarien Molina100% (1)
- Extraccion de La Caseina y Determinacion Del PiDocument5 pagesExtraccion de La Caseina y Determinacion Del PiChristian RPas encore d'évaluation
- Determinación del punto isoeléctrico de la caseínaDocument13 pagesDeterminación del punto isoeléctrico de la caseínaAlejandra Gutierrez SaavedraPas encore d'évaluation
- Determinación del punto isoeléctrico de la caseína mediante extracción y precipitaciónDocument13 pagesDeterminación del punto isoeléctrico de la caseína mediante extracción y precipitaciónAlejandra Gutierrez SaavedraPas encore d'évaluation
- Laboratorio 2 BioquimicaDocument5 pagesLaboratorio 2 BioquimicaWendy Paola Chica SimancaPas encore d'évaluation
- Historia de La EmpresaDocument3 pagesHistoria de La EmpresaJuan Esteban Castro MenaPas encore d'évaluation
- Historia económica: evolución población, energía y desarrolloDocument103 pagesHistoria económica: evolución población, energía y desarrolloMara RicciPas encore d'évaluation
- Acupuntura ReductIvaDocument3 pagesAcupuntura ReductIvaAnselmo Franco MirandaPas encore d'évaluation
- Panificacion en ColombiaDocument112 pagesPanificacion en ColombiaAlejo AlvaresPas encore d'évaluation
- Santa Cruz y Sus ProvinciasDocument61 pagesSanta Cruz y Sus ProvinciasFernandoCardozoCastañoPas encore d'évaluation
- Guia de Aprendizaje BpaDocument4 pagesGuia de Aprendizaje BpaYuliet CastañoPas encore d'évaluation
- Proceso productivo del shampoo Sedal HidrataciónDocument25 pagesProceso productivo del shampoo Sedal Hidrataciónrafa GonzalesPas encore d'évaluation
- 19 en EsDocument8 pages19 en Essteve oliverPas encore d'évaluation
- Requerimiento Agroclimatico Del Esparrago 2005Document10 pagesRequerimiento Agroclimatico Del Esparrago 2005Angel LuisPas encore d'évaluation
- Comidas típicas de mi comunidadDocument9 pagesComidas típicas de mi comunidadGloria Delina Castro Zorrilla0% (1)
- Bioindicación de Calidad Del AguaDocument39 pagesBioindicación de Calidad Del AguaHair LimaPas encore d'évaluation
- Formulas de CosmeticosDocument67 pagesFormulas de Cosmeticoseduardo100% (7)
- Proyecto de Diseño NectarDocument43 pagesProyecto de Diseño NectarXiomi Senmache Cornejo100% (1)
- Yurany Rojas - Entrevista CalidadDocument4 pagesYurany Rojas - Entrevista Calidadyuranyrojas83Pas encore d'évaluation
- Razonamiento matemático: Problemas de prácticaDocument2 pagesRazonamiento matemático: Problemas de prácticaJesus GuerraPas encore d'évaluation
- M4t01636#i01-312!1!7531 Horas - Verificar - Todos Lo Sos. Rojo - Noregistra Pm3 7000 HDocument6 pagesM4t01636#i01-312!1!7531 Horas - Verificar - Todos Lo Sos. Rojo - Noregistra Pm3 7000 HJherry Huaripata ChávezPas encore d'évaluation
- Purificación proteínas espinacaDocument6 pagesPurificación proteínas espinacaDaniela Ramirez MartinezPas encore d'évaluation
- Propagación in vitro de tomate con 2,4-DDocument9 pagesPropagación in vitro de tomate con 2,4-DKarenSamanezHernandezPas encore d'évaluation
- Edicion 28-10-2019Document16 pagesEdicion 28-10-2019Pagina web Diario elsigloPas encore d'évaluation
- NOM-144-SCFI-2000 Charanda.Document9 pagesNOM-144-SCFI-2000 Charanda.Edgar GarciaPas encore d'évaluation
- Raíces y Tubérculos: Cultivos Alimenticios ClaveDocument21 pagesRaíces y Tubérculos: Cultivos Alimenticios ClaveYadira Perez MangualPas encore d'évaluation
- La papa, un alimento peruanoDocument2 pagesLa papa, un alimento peruanoMaria ChambiPas encore d'évaluation
- Trucos de Belleza para El Cuidado de La PielDocument8 pagesTrucos de Belleza para El Cuidado de La Pielleila sanchezPas encore d'évaluation
- Plan de Alimentación para Aumento de Peso FDocument4 pagesPlan de Alimentación para Aumento de Peso FJuli AcostaPas encore d'évaluation
- SEMANA1nnACTn1 575f2c2cc621f4eDocument3 pagesSEMANA1nnACTn1 575f2c2cc621f4eCristian ParraPas encore d'évaluation
- Coliformes TotalesDocument6 pagesColiformes TotalesNANCY ANDREA GOMEZ ORTEGAPas encore d'évaluation
- Proyecto FinalDocument32 pagesProyecto FinalAlejandro YupanquiPas encore d'évaluation
- Artículo OrgánicaDocument8 pagesArtículo OrgánicaVerónica ArévaloPas encore d'évaluation
- Diapositiva Practica Docente IDocument13 pagesDiapositiva Practica Docente IElieser Estefan Mejia GuillandeauxPas encore d'évaluation
- Importancia e Significado de Los TriglicéridosDocument3 pagesImportancia e Significado de Los TriglicéridosRichard Pol0% (1)