Académique Documents
Professionnel Documents
Culture Documents
Elementos de Termodinamíca PDF
Transféré par
Alina Diaz GallegosTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Elementos de Termodinamíca PDF
Transféré par
Alina Diaz GallegosDroits d'auteur :
Formats disponibles
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
UNIDAD 02
2. 2.ELEMENTOS
ELEMENTOS DE TERMODINAMICA
DE TERMODINMICA
2.1. CONCEPTOS BSICOS
2.1.1. Sistema termodinmico
Segn Abbott y Van Ness (1991), un sistema puede ser cualquier objeto, cualquier cantidad
de materia, cualquier regin del espacio, etc., seleccionado para estudiarlo y aislarlo
(mentalmente) de todo lo dems, lo cual se convierte entonces en el entorno del sistema. El
sistema y su entorno forman el universo.
La envoltura imaginaria que encierra un sistema y lo separa de sus inmediaciones (entorno) se
llama frontera del sistema y puede pensarse que tiene propiedades especiales que sirven para:
a) aislar el sistema de su entorno o para b) permitir la interaccin de un modo especfico
entre el sistema y su ambiente.
Segn Thellier y Ripoll (1992), sistema, o medio interior, es la porcin del espacio limitado
por una superficie real o ficticia, donde se sita la materia estudiada. El resto del universo es
el medio exterior. La distincin entre sistema y entorno es arbitraria: el sistema es lo que el
observador ha escogido para estudiar.
Figura 2.1: Sistema y su entorno
2.1.2. Sistemas aislados, cerrados y abiertos
Sistema aislado es el sistema que no puede intercambiar materia ni energa con su entorno.
Sistema cerrado es el sistema que slo puede intercambiar energa con su entorno, pero no
materia. Sistema abierto es el sistema que puede intercambiar materia y energa con su
entorno.
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 27
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
Materia
AISLADOS Energa
SISTEMAS CERRADOS Materia
Materia
ABIERTOS Energa
Figura 2.2: Formas de sistema
2.1.3. Sistema Homogneo y heterogneo
Si anteriormente se clasific al sistema como responsable del intercambio de materia y
energa, ahora desde una situacin de presentacin a la vista humana, los sistemas puedes ser
Homogneo, cuando es completamente uniforme, tal como un gas o una mezcla gaseosa, un
lquido o un slido, y tambin una solucin donde se haya disuelto algn otro cuerpo y
Heterognea cuando el sistema no es uniforme, sino que consiste en dos o ms partes
homogneas, que son separadas unas de otras por definidas superficies delimitatorias (PONS
MUZZO, 1981)
2.1.4. Propiedades de un sistema
Las propiedades fsicas de un sistema se consideran en dos grupos, las propiedades
intensivas que son caractersticas de cada sustancia e independientes de su cantidad, como
ejemplos se tienen la temperatura, presin, densidad, el ndice de refraccin, la viscosidad y la
tensin superficial. Y segundo las propiedades extensivas que dependen de la cantidad de
materia del sistema, siendo el volumen el ejemplo ms simple de este tipo de propiedad
2.1.5. Estado termodinmico y funcin de estado
Llamado tambin el estado de un sistema, queda definido cuando se dan el nmero mnimo de
propiedades termodinmicas que fijan el sistema. El estado termodinmico de un sistema se
puede definir completamente mediante cuatro propiedades: Composicin, presin, volumen y
temperatura. El valor de cualquiera de estas propiedades depende pues de los valores de las
otras dos, denominndose una ecuacin de estado a la relacin entre las tres propiedades
citadas. Las propiedades que como variables independientes, determinan el estado
termodinmico del sistema, se les llama los parmetros termodinmicos.
En la siguiente figura se ha representado un gas encerrado en un recipiente y las variables
termodinmicas que describen su estado.
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 28
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
Figura 2.3: Descripcin de estados termodinmicos
2.1.6. Proceso termodinmico
Un proceso termodinmico es un cambio de estado en el cual se da informacin adicional
sobre el mecanismo o cmo la presin, temperatura u otra propiedad vara cuando acontece el
cambio. Los procesos ms conocidos son los siguientes:
a) Isotrmico, cuando el cambio ocurre a temperatura constante.
b) Isobrico, si la presin se mantiene constante
c) Isocrico, cuando la restriccin del proceso es que el parmetro V = constante.
d) Adiabtico, cuando no hay intercambio de calor entre el sistema y los sistemas
limitantes.
e) Reversible, si est constituido de una serie de estados de equilibrio, y
f) Cclico, cuando el sistema retorna a su estado inicial despus de realizar una serie
de cambios.
2.1.7. Equilibrio termodinmico
En Termodinmica se dice que un sistema se encuentra en equilibrio termodinmico cuando
las variables intensivas que describen su estado no varan a lo largo del tiempo. El equilibrio
termodinmico comprende a tres equilibrios diferentes que deben existir simultneamente.
Primero el sistema debe estar en equilibrio trmico, tal que la temperatura sea la misma en
todo el sistema; segundo, si el sistema consiste de ms de una sustancia, debe haber tambin
un equilibrio qumico, tal que su composicin no vara con el tiempo; y finalmente, el
sistema debe estar en equilibrio mecnico
2.2. DEFINICIONES DEL PRIMER PRINCIPIO DE LA TERMODINMICA
El primer principio de la termodinmica es el enunciado cuantitativo del Principio General de
Conservacin de Energa. Se conoce por las definiciones sencillas siguientes:
- La energa no se crea ni se destruye, solo se transforma en el curso de los fenmenos
- Las energas se convierten de una forma a otra en cantidades equivalentes;
- Para realizar un trabajo debe gastarse una cantidad equivalente de otra energa; y
- Un aumento en el contenido de energa de un sistema requiere una correspondiente
disminucin en el contenido de energa de algn otro sistema.
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 29
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
2.3. ENERGA INTERNA
La energa interna se representa por los smbolos U E. El valor absoluto de la energa
interna de un sistema no es fcil de determinar, pues depende de muchos factores. La energa
interna se refiere a la energa de las molculas constitutivas de la sustancia, que se encuentran
en movimiento continuas y poseen energa cintica de traslacin y a excepcin de las
molculas monoatmicas, tambin cuentan con energa cintica de rotacin y vibracin
interna.
La energa interna es una funcin de estado: su variacin entre dos estados es independiente
de la transformacin que los conecte, slo depende del estado inicial y del estado final.
Figura 2.4: Ciclo Termodinmico
2.4. TRABAJO
El trabajo de expansin-compresin, W, es la transferencia de energa debida a una diferencia
de presiones. Es funcin de la trayectoria, es decir, depende del camino seguido, del nmero
de etapas en que se realiza. Su expresin matemtica puede obtenerse partiendo de la
definicin general:
dW Fdz
F
Pext
A
dW Pext Adz
dV Adz
dW Pext dV , integrando
V2
W P dV (2.1)
V1
Donde Pext es la presin externa de oposicin, es decir, la presin que ejerce el medio sobre el
sistema.
Fundamentos de Qumica (1 Grado en Fsica) 2011/2012 TERMOQUMI
En estas ecuaciones el signo menos se incluye para que stas cumplan con la convencin del
signo adoptada para el trabajo. Cuando el pistn se mueve dentro del cilindro comprimiendo
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 30
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
al fluido, la fuerza aplicada y su desplazamiento estn en la misma direccin, por tanto, el
trabajo es positivo. El signo menos es necesario debido a que el cambio en el volumen es
negativo. Para un proceso de expansin, la fuerza aplicada y su desplazamiento tienen
direcciones opuestas. En este caso el cambio en el volumen es positivo y se requiere del signo
menos para hacer que el trabajo sea negativo.
2.5. PRIMERA LEY DE LA TERMODINMICA
Una vez que se reconocieron el calor y la energa interna como formas de energa fue posible
generalizar la ley de la conservacin de energa mecnica. Para formular la primera ley de la
termodinmica, teniendo en cuenta la aplicacin de la ley de conservacin de energa
mecnica aplicndolo mediante las formas de energas cintica y potencial externas, mas aun
extenderse a otras formas de energa tales como: energas superficial, elctrica y magntica.
Por lo que se lleg a establecer una ley natural, conocida como la primera ley de la
termodinmica, cuyo enunciado es la siguiente: La cantidad total de energa es constante aunque
adopte diferentes presentaciones; cuando desaparece una forma de energa, surge simultneamente con otra
apariencia
Qin 0
Win 0
Sistema
U
Wout 0 Qout 0
Figura 2.5: Principio de conservacin de energa
Como la energa sufre transformaciones, se deduce que la energa interna es igual al calor
transferido al sistema ms el trabajo hecho sobre el sistema .
U = Q + W (2.2)
De acuerdo a la convencin de signos en el lado derecho de la ecuacin (2.2) el valor
numrico del calor y trabajo ser positivo cuando se transfiere de los alrededores al sistema.
Esta ecuacin se aplica a procesos que implican cambios finitos en el sistema. Para cambios
diferenciales, la ecuacin se escribe:
dU = dQ + dW (2.3)
La ecuacin (2.3) es til cuando U, Q y W se expresan en funcin de las variables de proceso.
Esta relacin representa la Primera ley de la Termodinmica
Despejando dQ de la ecuacin (2.3) se tiene:
dQ dU dW , y
Reemplazando la ecuacin (2.1) en la anterior resulta:
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 31
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
dQ dU PdV (2.4)
Con respecto a los procesos cclicos se ha dicho que, cuando un sistema retorna a su estado
original, su contenido de energa es incambiable, tal que U = 0, de la ecuacin 2.3 resulta
dU dQ dW 0 , entonces esta ecuacin queda:
dQ dW
Integrando da:
Q W (2.5)
2.6. PROCESOS REVERSIBLES
En termodinmica constituye un proceso reversible aquel proceso que realizndose bajo
condicin de fuerzas opuestas balanceadas, la fuerza impelente es en todo tiempo solo
infinitamente ms grande que la fuerza opositora, pudindose invertir exactamente el proceso
aumentando la fuerza opositora por una cantidad infinitesimal. (PONS MUZZO, 1981)
2.6.1. Expansin isotrmica reversible de un gas
Cuando el proceso se expande a temperatura constante, donde no hay flujo mecnicamente
reversible, el sistema siempre est virtualmente en equilibrio mecnico con los alrededores
por lo que la presin externa va a ser igual a la presin del gas:
P ext = P gas ideal (caso gas ideal)
n R T
Pext Pgas (*)
V
Integrando la ecuacin (2.3) resulta:
V2
W Pext dV
V1
Luego reemplazando la ecuacin (*) en la ltima:
V2 n R T V2 dV
W dV n R T , que integrando da:
V1 V V1 V
V2 (2.6)
W n R T ln
V1
La ecuacin (2.6) depende solamente de los volmenes V1 y final V2, aparte de la temperatura
constante, y es independiente del camino considerando que el trabajo se ha efectuado de
manera reversible. En este caso, el trabajo reversible isotrmico ser tambin el trabajo
mximo.
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 32
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
Como el gas es ideal y a temperatura constante, por la ley de Boyle: V2/V1 = P1/P2, que
sustituyendo en la anterior expresin se tiene:
P1
W n R T ln (2.7)
P2
En la expansin de un gas ideal no se necesita un gasto para vencer las fuerzas de atraccin de
sus molculas. Por consiguiente para un gas ideal U = 0 para cualquier expansin o
compresin isotrmica de este. Sustituyendo este valor de U en la ecuacin (2.1), tenemos
que Q = -W
As combinando este resultado con los valores de las ecuaciones (2.6) y (2.7), se tienen:
V2
W Q n R T ln (2.8)
V1
P1
W Q n R T ln (2.9)
P2
P ext = P gas real (caso gas real)
n R T a n2
Pext Pgas 2 (Ec. de Van der Walls)
V nb V
Luego:
n R T a n2 dV dV
W VV12 2 dV n R T VV12 a n 2 VV12 2 , que integrando da:
V n b V V nb V
V n b 2 V1 V2
W n R T ln 2 an (2.10)
V1 n b V2 V1
2.7. PROCESOS IRREVERSIBLES
2.7.1. Trabajo irreversible de expansin o contraccin isoterma del proceso
Cuando el proceso es irreversible la presin externa va a ser constante, luego:
V2 V2
W Pext dV Pext dV , que integrando da:
V1 V1
W Pext V2 V1 (2.11)
Ejercicio 2.1: Una muestra de gas ideal se expande al doble de su volumen inicial de 0,1 m3
en un proceso para el cual P = aV2, con a=2 atm/m6. a) Bosqueje un grfico en el diagrama
PV. b) Calcular el trabajo realizado por el gas durante la expansin
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 33
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
Solucin
El diagrama Presin volumen es el siguiente
P atm
0,1 0,2 V m3
Usando la definicin de trabajo termodinmico
V2
W PdV (1)
V1
Como P = aV2, reemplazando en (1) se tiene:
V2
W aV 2 dV , integrando
V1
a 3
W (V2 V1 ) , remplazando valores
3
W
2 atm
3 m 6
(0,2m 3 ) 3 (0,1m 3 ) 3
1,013 105 Pa
W 4,67 103 atm m 3
1 atm
2
1N /m
W 472,73 Pa m 3
1 Pa
1J 1 kJ
W 472,73 N m
N m 1000 J
W 0,47273 kJ
Ejercicio 2.2: Tres moles de un gas ideal a 27 C se expanden isotrmica y reversiblemente
desde 20 hasta 60 L. Calcular W y Q
Solucin
Como en esta expansin, T es constante y la P es variable, usaremos la ecuacin (2.8)
V
W Q n R T ln 2
V1
L atm 60 L
W Q 3 mol 0,082 300,15 K ln
mol K 20 L
W 81,12 L atm
Q 81,12 L atm
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 34
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
De acuerdo a la convencin de signos Q es positivo debido a que el calor es absorbido por la
expansin y W es negativo porque es trabajo hecho por el sistema
Ejercicio 2.3: Tres moles de un gas ideal se expanden isotrmicamente contra una presin de
oposicin de 1 atm desde 20 hasta 60 L. Calcular W y Q
Solucin
Como la presin externa es constante, usaremos la ecuacin (2.11)
W Pext V2 V1
W 1 atm 60 L 20 L
W 40 L atm
Para un proceso isotrmico, la ecuacin de la primera ley est dado por W = - Q
Luego:
Q 40 L atm
Ejercicio 2.4: Tres moles de Nitrgeno experimentan una expansin isotrmica y
reversiblemente a 27 C desde 20 hasta 60 L. Calcular el W, si el Nitrgeno se comporta
como gas Van der Waals, a = 5,49 L-atm-mol-1; b = 0,064 L/mol
Solucin
Se utilizar la ecuacin (2.10)
V n b 2 V1 V2
W n R T ln 2 an
V1 n b V2 V1
L atm 60 L 3 mol 0,064 L/mol
W 3 mol 0,082 300,15K ln
mol K 20 L 3 mol 0,064 L/mol
L atm 20 L 60 L
5,46 (3 mol)2
mol 60 L 20 L
W 79,947 L atm
2.8. ENTALPA
Se define a la funcin entalpa por la siguiente expresin matemtica:
H U PV (2.12)
Donde:
U = energa total interna
P = presin absoluta
V = volumen
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 35
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
H es una nueva funcin de estado, porque U, P y V son funciones de estado y es propiedad
intensiva por serlo U y V
Esta funcin tiene diferencial total exacta, puesto que es una combinacin lineal de funciones
que son a su vez diferenciables exactamente. La forma diferencial de la ecuacin (2.12) se
escribe como:
dH dU d ( P V ) (2.13)
Integrando la ecuacin (2.13) se tiene el siguiente resultado:
H U PV (2.14)
La ecuacin (2.14) es otra forma de expresar el primer principio de la termodinmica para
sistemas cerrados.
2.9. PROCESOS TERMODINMICOS CON GASES IDEALES
2.9.1. Procesos a Volumen constante
Para un proceso a volumen constante se tiene:
dU dQ dW (2.2)
Donde Q y W siempre representan el calor y el trabajo totales. El trabajo en un proceso
reversible mecnicamente y para un sistema cerrado esta dado por:
dW PdV (2.15)
Por tanto la ecuacin (2.2) queda:
dU dQ PdV (2.16)
Esta es la ecuacin general de la primera ley para un proceso reversible mecnicamente, en un
sistema cerrado.
Si este proceso ocurre a volumen constante dV 0 , entonces la ecuacin (2.16) queda:
dQV dU (2.17)
Integrando da:
QV U (2.18)
As, en un sistema cerrado, para un proceso a volumen constante, reversible mecnicamente,
la transferencia de calor es igual al cambio en la energa interna del sistema.
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 36
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
2.9.2. Procesos de Presin constante
De la primera ley para sistemas cerrados se tiene:
dQ dU PdV (a)
La ecuacin (2.12), que define la entalpa, puede escribirse:
H U PV
Diferenciando la ecuacin anterior:
dH dU VdP PdV , despejando dU:
dU dH VdP PdV (b)
Reemplazando la ecuacin (b) en (a) se obtiene:
dQ dH VdP PdV PdV
Simplificando la ecuacin anterior queda:
dQ dH VdP (2.19)
Como el proceso ocurre a presin constante dP 0 , entonces la ecuacin anterior queda:
dQP dH (2.20)
Integrando da:
QP H (2.21)
En los procesos a P = cte, la variacin de la entalpa es igual al calor intercambiado, esta
caracterstica de la entalpa, la convierte en una de las propiedades ms tiles de la ingeniera.
2.10. CAPACIDADES CALORFICAS A VOLUMEN CONSTANTE Y PRESIN
CONSTANTE
2.10.1. Capacidad Calorfica
La capacidad calorfica, C, de un sistema es la relacin entre el q entregado o cedido por el
sistema por el cambio de temperatura del mismo. Por lo tanto:
dQ
C (2.22)
dT
Capacidad calorfica a volumen constante
La determinacin de Cv es a partir de:
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 37
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
dQV
CV (2.23)
dT
De la ecuacin (2.23) se despeja dQv
dQV CV dT (a)
Del primer principio y por la ecuacin (2.17) para un proceso a volumen constante
dV 0 , se tiene que dQv = dU, y reemplazando esta ecuacin en (a) tenemos:
dU V CV dT
Despejando CV de la ecuacin anterior queda:
U (2.24)
CV
T V
Capacidad calorfica a presin constante
La determinacin de CP es a partir de:
dQP
CP (2.25)
dT
De la ecuacin (2.25) se despeja dQP
dQP CP dT (a)
Del primer principio:
dQP = dH (b)
Reemplazando (b) en (a)
dH C P dT
Despejando CP, de la ecuacin anterior queda:
H
CP (2.26)
T P
Estas definiciones son vlidas tanto para capacidades calorficas molares como para
capacidades calorficas especficas (comnmente llamados calores especficos), dependiendo
de si U y H son propiedades molares o especficas.
Si se tiene un proceso a volumen constante, la ecuacin (2.24) puede escribirse
dU CV dT (V constante) (2.27)
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 38
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
Integrando da:
T2
U
T1
CV dT (V constante) (2.28)
Para un proceso a presin constante la ecuacin (2.26) se escribe
dH CP dT (P constante) (2.29)
De donde integrando da
T2
H
T1
C P dT (P constante) (2.30)
Integrando la ecuacin (2.30) con CP = constante
H C P (T2 T1 ) (2.31)
Si CP no es constante por tener dependencia con la temperatura, CP toma el siguiente valor:
CP a b T c T 2 d T 3 ... (2.32)
Relaciones de Mayer (solo para gases ideales)
Partiendo de la ecuacin (2.12) H U PV , donde se sustituye el trmino PV por su
equivalente RT de la ecuacin de gases ideales para un mol.
H U RT
Diferenciado esta ecuacin con respecto a T se obtiene:
dH dU dT
R , simplificando:
dT dT dT
dH dU
R (2.33)
dT dT
Reemplazando (2.24) y (2.26) en (2.33) se tiene;
Cp Cv R Cp Cv R (2.34)
2.11. PROCESOS ADIABTICO
2.11.1. Proceso adiabtico reversible
Son procesos donde no hay intercambio de calor con los alrededores, entonces Q 0
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 39
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
dU dQ dW
Como Q 0 , esta ecuacin queda:
dU dW (2.35)
En esta etapa infinitesimal de una expresin adiabtica reversible el trabajo dW vale -PdV,
reemplazando en (2.35)
dU PdV
dU dW PdV (2.36)
La variacin de dU en un proceso infinitesimal en el que interviene n moles de gas ideal es:
dU nCv dT (a)
Reemplazando esta ecuacin en la (2.36) da:
nCv dT dW
T2
W n Cv dT , si Cv = cte
T1
W n Cv T2 T1 (2.37)
Comparando nuevamente la ecuacin (a) con (2.36)
nCv dT PdV (2.38)
n
Para un gas ideal P RT , reemplazando en (2.38)
V
dV
nCv dT nRT , simplificando n y suponiendo Cv independiente
V
de la temperatura, integrando esta ecuacin da:
T2 V
Cv ln R ln 1 (2.39)
T1 V2
Esta ecuacin se puedes escribir as:
Cv R
T V
ln 2 ln 1 , eliminando logaritmos:
T1 V2
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 40
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
Cv R
T2 V
1 , despejando:
T1 V2
R
T2 V1 Cv
, pero R=Cp-Cv
T1 V2
CpCv
T2 V1 Cv
, simplificando
T1 V2
Cp
1
T2 V1 Cv Cp
, como , queda la ecuacin anterior como:
T1 V2 Cv
1
T2 V1
(2.40)
T1 V2
Para un gas ideal PV = nRT aplicado para una misma masa de gas en dos estados, produce la
relacin siguiente:
P1 V1 P2 V2 T P V
2 2 2 (b)
T1 T2 T1 P1 V1
Reemplazando (b) en (2.40)
1
P2 V2 V1
, despejando:
P1 V1 V2
1 1
P2 V1 V1
, simplificando
P1 V2 V2
P2 V1
(2.41)
P1 V2
P2 V2 P1 V1
P1 V1 P2 V2 P3 V3 cte
P V cte (2.42)
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 41
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
PRCTICA 03: PRIMERA LEY DE LA TERMODINMICA
1) Un gas ideal dentro de un cilindro cuya rea es de 18,8 pulg2 es comprimido una
distancia de 20 pulgadas, mediante una presin exterior constante igual a 13,5 lbf/pulg2.
Qu trabajo fue realizado en lb f pi ?
2) Tres moles de gas (modelo ideal) a 27C se expanden desde 20 L hasta 60 L,
manteniendo la temperatura constante. Calcular el trabajo realizado en Julios, a) si el
proceso es reversible y b) si el proceso es irreversible, manteniendo una presin de
oposicin constante de 1 atm.
3) Dos moles de un gas ideal experimentan una comprensin isotrmica desde 60 L hasta 20
L utilizando una presin constante de 5 atm. Calclense Q y W.
4) 3 moles de un gas ideal experimentan una expansin isotrmica contra una presin de
oposicin constante de 100 kPa desde 20dm3 hasta 60dm3. Calclese W, Q, U y H.
5) Un mol de gas de van der Waals a 27C se expande isotrmica y reversiblemente desde
10 hasta 30 litros. Calcular el trabajo producido. Para este gas las constantes a y b de van
der Waals son, respectivamente: 5,49 atm L2/mol y 0,064 L/mol.
6) Un mol de gas ideal est confinado bajo una presin constante Pop = P = 200 kPa. La
temperatura se cambia de 100C a 25 C. Cv = 3/2R. Calcular Q, W, U y H.
7) Un mol de un gas ideal, Cv=20,8 J/K mol, se transforma a volumen constante desde 0C
hasta 75C. Calclese Q, W, U y H.
8) Un mol de gas de van der Waals a 300 K realiza una expansin isotrmica reversible de
20 dm3 a 60 dm3 (a=0,556 m6 Pa mol-2; b=0,064 dm3 mol-1). Calcular W, Q, U y H,
a) si el proceso es reversible,
b) si el proceso es irreversible y la presin de oposicin es igual a la presin final.
9) Obtener la expresin para el trabajo reversible realizado por un gas de Berthelot. La
nRT an 2
ecuacin de estado es: P
V nb TV 2
10) Calcule el cambio de entalpa, en Joule, al expandir reversiblemente un mol de un gas
ideal, desde un volumen inicial V1 hasta dos veces su volumen (V2 = 2V1) desde una
temperatura inicial de 273,15 K hasta una temperatura final de 543,15 y a una presin
constante de 1,0 atm.
11) Una muestra de 32 g de metano inicialmente a 1 atm y 27C se caliente hasta 277C. La
ecuacin emprica para la capacidad calorfica molar del metano a presin constante es:
Cp = 3 + 2 x 10-2 T cal/mol K.
Considerando modelo ideal, calcular Q, W, U y H:
a) Para un proceso isobrico reversible.
b) Para un proceso isocrico reversible.
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 42
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
12) Una muestra de argn a 1,0 atm de presin y 25C, se expande reversiblemente y
adiabticamente desde 0,50 dm3 a 1,00 dm3. Calcular su temperatura final, el trabajo
efectuado durante la expansin y el cambio en la energa interna considerando
comportamiento ideal.
13) Un mol de fluoruro de carbono se expande reversible y adiabticamente hasta duplicar su
volumen. Calcular el valor de Cv para este gas si se sabe que la temperatura desciende de
25C a 24,71C. Evaluar tambin el valor de la exponente adiabtica gamma; si la
presin cambia de 1522,2 mmHg a 613,85 mmHg. Finalmente calcular U y H para el
sistema. Considerar comportamiento ideal.
14) Cinco moles de un gas monoatmico realizan el siguiente ciclo reversible:
Calcular W, Q, U, H para cada proceso y para el ciclo.
2.12. SEGUNDA LEY DE LA TERMODINMICA, ENTROPIA Y APLICACIONES
2.12.1. Enunciados de la Segunda ley
El Segundo Principio se ocupa de predecir la direccin en que se va a realizar un determinado
proceso, de estudiar las condiciones en las que se alcanza el equilibrio, de determinar la
mxima cantidad de trabajo que se puede obtener en un proceso y de estudiar los factores que
impiden conseguir esa cantidad de trabajo mxima. Dado que hay diferentes aspectos en los
que interviene el Segundo Principio, existen diferentes formulaciones, pero todas ellas son
equivalentes entre s.
a) El postulado de Clausius puede enunciarse diciendo: El calor no puede pasar por s mismo
(es decir en forma espontanea) de un cuerpo a menor temperatura a otro a mayor temperatura . En otras
ocasiones se formula diciendo que el calor no puede transmitirse espontneamente de un cuerpo fro a
otro caliente. El enunciado de Clausius no dice que no pueda transferirse energa de un cuerpo
fro a otro caliente, sino que eso es imposible espontneamente, es decir, es necesario que
exista otro efecto. En las mquinas frigorficas ocurre exactamente eso, se transfiere calor de
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 43
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
un foco fro a otro caliente, pero para ello es necesario aportar un trabajo desde el exterior por
lo que la transmisin de calor no es el nico efecto o, dicho de otra manera, La transmisin de
calor no es espontnea. Se puede concluir que el concepto deducido intuitivamente es
totalmente correcto e interpreta el proceso natural como es debido, con lo que para hacer lo
contrario se debe usar una ayuda externa, y ya no es "por s mismo".
b) El postulado de Kelvin-Planck puede enunciarse diciendo: Es imposible que un
dispositivo funcione en un ciclo y produzca trabajo al intercambiar calor nicamente con un foco trmico.
De otra manera podemos expresarlo diciendo que Es imposible que un dispositivo funcione en un
ciclo en el que se absorba calor de un solo foco y produzca una cantidad equivalente de trabajo . La
equivalencia de las formulaciones de Clausius y Kelvin-Planck puede demostrarse viendo que
cuando se viola cada una de las formulaciones, se viola la otra.
c) El postulado de Carnot puede enunciarse diciendo: Es imposible construir una mquina
que operando cclicamente no produzca otro efecto que la absorcin de calor de un depsito y su conversin a
una cantidad equivalente de trabajo. La frase operando cclicamente quiere decir que la
mquina debe volver a su estado original cada cierto nmero de etapas a fn de que pueda
funcionar continuamente
2.13. Entropa
Es una de las propiedades de estado ms importantes de la termodinmica, fue sugerida por
CLAUSIUS en 1854, viene dada de una palabra griega que quiere decir cambio y se
representa por la letra S
La entropa es precisamente til debido a que es una funcin de estado o propiedad. Debe su existencia a la
segunda ley, a partir de la cual aparece de la misma manera en que la energa interna aparece de la primera
ley
Por tanto, puede inferirse la existencia de una propiedad del sistema cuyos cambios
diferenciales estn dados por estas cantidades. Esta propiedad es la entropa y sus cambios
diferenciales son:
dQrev
dS (2.43)
T
Donde dS que est definida por la ecuacin anterior es una diferencial exacta, ya que dQ tiene
un valor definido para un proceso isotrmico reversible.
El cambio de entropa de cualquier sistema que experimenta un proceso reversible es
integrando la ecuacin (2.43):
T2
dQrev
S ( S 2 S1 )
T1
T
(2.44)
Cuando un sistema experimenta un proceso irreversible de un punto de equilibrio a otro, el
cambio de entropa del sistema AS debe ser evaluado con la aplicacin de la ecuacin (2.44)
para un proceso reversible elegido arbitrariamente que produzca el mismo cambio de estado
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 44
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
que el proceso real. La integracin no se realiza sobre la trayectoria irreversible. Puesto que la
entropa es una funcin de estado, los cambios de entropa de los procesos reversible e
irreversible son los mismos.
Cuando un proceso es reversible y adiabtico, dQ = 0; entonces, de acuerdo con la ecuacin
(2.43), dS = 0. Por tanto, la entropa de un sistema es constante durante un proceso adiabtico
reversible, y se dice entonces que el proceso es isentrpico.
2.13.1. Cambios de entropa de un gas ideal
La primera ley, escrita para n moles o unidad de masa de fluido, es:
dU = dQ + dW (2.45)
dQ = dU + PdV (2.46)
dividiendo la ecuacin (2.46) entre T
dQrev dU P
dV
T T T
dU P
dS dV (2.47)
T T
Ahora como dU nCvdT y por la ecuacin de gases ideales P nRT / V ,
dT dV
dS nCv nR (2.48)
T V
Suponiendo que Cv es independiente de la temperatura, la integracin de la ecuacin (2.48)
dar:
T2 V
S nCv ln nR ln 2 (2.49)
T1 V1
Para un proceso isotrmico, la ecuacin (2.49) se convierte en:
V2
S nR ln (2.50)
V1
Para un proceso isocrico a volumen constante la ecuacin (2.48) se convierte en:
dT
dS nCv (2.51)
T
Integrando la ecuacin (2.51) da:
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 45
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
T2
dT
S n Cv (2.52)
T1
T
El anlisis de la ecuacin (2.52) es si Cv es o no independiente de la Temperatura.
Para procesos donde interviene la entalpa el procedimiento es a partir de la ecuacin de la I
ley:
dU = dQ + dW
dU = dQ PdV (2.53)
Ahora como H U PV , diferenciando esta ecuacin:
dH dU VdP PdV (a)
Reemplazando la ecuacin (2.53) en (a), tenemos que:
dH dQrev PdV VdP PdV , simplificando esta ecuacin se convierte:
dH dQrev VdP , despejando dQrev y dividiendo entre T esta ecuacin se
tiene:
dQrev dH V
dP
T T T
dH V
dS dP (2.54)
T T
Ahora como dH nCpdT y por la ecuacin de gases ideales V nRT / P ,
dT dP
dS nCp nR (2.55)
T P
Suponiendo que Cp es independiente de la temperatura, la integracin de la ecuacin (2.55)
dar:
T2 P
S nCp ln nR ln 2 (2.56)
T1 P1
Para un proceso isotrmico, la ecuacin (2.56) se convierte en:
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 46
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
P2
S nR ln (2.57)
P1
Para procesos a Presin constante la ecuacin (2.55) se convierte
dT
dS nCp (2.58)
T
Integrando la ecuacin (2.58) da:
T2
dT
S n Cp (2.59)
T1
T
El anlisis de la ecuacin (2.59) es si Cp es o no independiente de la Temperatura.
2.13.2. Energa Libre y la Funcin Helmholtz
La energa libre de Gibbs (o entalpa libre) es un potencial termodinmico, es decir, una
funcin de estado extensiva con unidades de energa, que da la condicin de equilibrio y de
espontaneidad para una reaccin qumica (a presin y temperatura constantes).
La energa libre de Hemholtz tambin llamada funcin de Helmholtz o funcin trabajo. Es
una magnitud extensiva del sistema, funcin de estado termodinmico, por tanto, no depende
del proceso sufrido, sino del estado nal e inicial del sistema.
Por definicin total:
Funcin Hemholtz : A = U TS (2.60)
Energa Libre de Gibbs : G = H TS (2.61)
Donde A es el smbolo de la funcin Helmholtz, es la inicial de arbeit que quiere decir
trabajo en alemn y G smbolo de energa libre es en memoria de GIBBS, famoso
termodinmico norteamericano.
La funcin A esta relacionada a G, como U est relacionada a H
En trmicos de incrementos finitos las ecuaciones (2.60) y (2.61), se expresan como:
A = U TS (2.62)
G = H TS (2.63)
Con relacin a cualquier proceso reversible que ocurre a temperatura y presin constante, el
estado de equilibrio se define por la ecuacin:
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 47
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
dG = 0 (2.64)
2.13.3. Variacin de la Energa Libre con la Presin
De acuerdo a la primera ley:
dU = TdS PdV (2.65)
Por definicin de entalpa H = U + PV, la cual diferenciando produce:
dH dU VdP PdV (a)
Remplazando (2.65) en (a), se obtiene:
dH TdS PdV VdP PdV , simplificando
dH TdS VdP (2.66)
De acuerdo a la ecuacin (2.61) G = H TS, la cual diferenciando es:
dG dH TdS SdT (2.67)
Sustituyendo (2.66) en (2.67), se tiene:
dG TdS VdP TdS SdT , simplificando
dG VdP SdT (2.68)
La ecuacin de la Energa libre esta dado por la relacin entre las variables P y T de
acuerdo: G G( P, T ) mediante esta relacin definimos los diferenciales en funcin de ellas
como diferencial total de acuerdo a:
G G
dG dP dT (2.69)
P T T P
Aplicando el criterio de igualacin entre las ecuaciones (2.68) y (2.69), resulta:
G
V (2.70)
P T
G
S (2.71)
T P
Operando la ecuacin (2.70) para el caso de un gas ideal, donde V = nRT/P,
dP
dG nRT , integrando da:
P
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 48
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
P2
G nRT ln (2.72)
P1
2.14. TERCERA LEY DE LA TERMODINMICA
A la temperatura del cero absoluto la entropa de cualquier sustancia cristalina perfecta es
cero. Esta Ley permite calcular la entropa absoluta de cualquier sustancia a
una temperatura y presin de referencia. As, la entropa absoluta estndar: ST ser la
entropa de un sistema a 1 atm de presin y a la temperatura T, calculada a partir de la tercera
Ley de la termodinmica.
dT H f
Tf T
dT
S T Cp S Cpl (2.73)
0
T Tf Tf
T
Para el agua a 25C y 1 atm de presin: S298
dT H f
273 298
dT
S 298
0
Cp S
T
Tf
Cpl
273
T
Los trminos que se consideran en el clculo de la entropa absoluta para el agua a 25C y 1
atm son: El primer trmino considera la capacidad calrica a presin constante del agua
slida, el segundo trmino corresponde al cambio de estado donde Hf es el calor de fusin y
Tf la temperatura de fusin del agua a 1 atm de presin. El tercer trmino corresponde a la
capacidad calrica del agua lquida a presin constante. En esta ecuacin se est despreciando
el efecto de la presin sobre la entropa para el sistema slido y lquido.
Las leyes de la termodinmica permiten modelar los intercambios de energa entre los
sistemas y los alrededores y valorar la prdida de calidad energtica en ellos para permitir al
ingeniero hacer propuestas de los mejores caminos por los que se puede dar un proceso
disminuyendo el deterioro acelerado del medio ambiente.
PRCTICA 04: SEGUNDA LEY DE LA TERMODINMICA
1) Un nmero n de moles de un gas ideal experimentan una expansin libre y adiabtica en
el vaco (experimento de Joule). Expresar en trminos de la temperatura y volumen
inicial y final el incremento de entropa del sistema. Calcular cunto vale la entropa
molar si el volumen final es doble que el volumen inicial.
2) Un cilindro vertical de paredes adiabticas y provistas de un pistn no conductor del
calor, est dividido por una pared fija y diatrmica. La parte superior contiene 10 moles
de un gas ideal y la inferior una mezcla en equilibrio a 1,013 bar de 100 g de agua y 100
g de hielo. Se introduce lentamente el pistn hacia dentro hasta que la presin del gas se
duplica. Cul es la variacin de entropa del gas, de la mezcla y del universo en este
proceso?
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 49
ELEMENTOS DE TERMODINAMICA NOTAS DE FISICOQUMICA
3) Un mol de gas de van der Waals realiza una expansin isotrmica de 0,0015m3a
0,035m3. La temperatura es de 398.15 K. Calcular el cambio de entropa para el gas, los
alrededores y el total, a) si el proceso es reversible; b) si el proceso es irreversible y la
presin externa es 94.6 kPa. Para este gas
2 6 1
a 3,7 Pa m m b 0,052 10 Pa m m
6 3
4) Un mol de un gas ideal monoatmico se calienta reversiblemente de 298,15 K a 398,15
K. Calcular el cambio de entropa del sistema, de los alrededores y el total.
a) Si el proceso se realiza a volumen constante
b) Si el proceso se realiza a presin constante
5) Cinco moles de nitrgeno son enfriados reversiblemente desde 1000 hasta 300 K.
Calcular el cambio de entropa para el sistema, para los alrededores y el total
considerando que depende de la temperatura, Cv
a) Si el proceso se realiza a volumen constante
b) Si el proceso se realiza a presin constante.
6) Un mol de gas ideal monoatmico recorre un ciclo de Carnot reversible, como el indicado
en la figura, con V1 = 20 L, V2 = 40 L, T1 = 300 K y T3 = 200 K. Calclense P, V,
T, U, H y S en cada etapa del ciclo.
7) Calcular S cuando se mezcla 1 mol de N2 con 3 moles de O2 a 25C y una atmsfera de
presin, siendo la presin final de una atmsfera.
8) Un mol de gas ideal que se encuentra inicialmente a 25C se expande:
a) isotrmicamente y reversiblemente desde 20 hasta 40 L, y
b) isotrmicamente e irreversiblemente contra una presin de oposicin nula (expansin
de Joule) desde 20 hasta 40 L.
Calcular S, Q y W para ambos procesos. Obsrvese la relacin entre S y Q en ambos
procesos.
Sol. a) U=0 Q=1717J W=-1717J S=5,76J/K b) U=0 Q=0 W=0 S=5,76J/K
9) Derive la relacin entre la energa libre de Helmholtz con la entropa y la temperatura.
M.Sc. Ing. Ali Epifanio Diaz Cama Pgina 50
Vous aimerez peut-être aussi
- Resumen Difusión Molecular y Transferencia de MasaDocument7 pagesResumen Difusión Molecular y Transferencia de MasaAlina Diaz GallegosPas encore d'évaluation
- Analisis Parametricos y No ParametricosDocument19 pagesAnalisis Parametricos y No ParametricosHarold VargasPas encore d'évaluation
- Perdidas DarcyDocument45 pagesPerdidas DarcyDieggo92% (13)
- Ciclos de Potencia y RefrigeraciónDocument41 pagesCiclos de Potencia y RefrigeraciónAlina Diaz GallegosPas encore d'évaluation
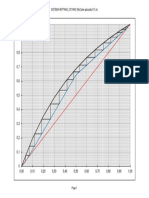
- Sistema Heptano - Octano (Mccabe-Aplazados17)Document1 pageSistema Heptano - Octano (Mccabe-Aplazados17)Alina Diaz GallegosPas encore d'évaluation
- SISTEMA HEPTANO - OCTANO (McCabe Aplazados17 Desarollo)Document1 pageSISTEMA HEPTANO - OCTANO (McCabe Aplazados17 Desarollo)Alina Diaz Gallegos100% (1)
- Sistemas de RefrigeraciónDocument37 pagesSistemas de RefrigeraciónAlina Diaz GallegosPas encore d'évaluation
- Intercambiador de Calor de Doble TuboDocument6 pagesIntercambiador de Calor de Doble TuboAlina Diaz GallegosPas encore d'évaluation
- La NaturalezaDocument14 pagesLa NaturalezaAlina Diaz GallegosPas encore d'évaluation
- Embarazo Aborto Adolescente (T)Document60 pagesEmbarazo Aborto Adolescente (T)Alina Diaz GallegosPas encore d'évaluation
- "La Sopa de PiedraDocument2 pages"La Sopa de PiedraAlina Diaz Gallegos100% (1)
- Triptico DilucionesDocument2 pagesTriptico DilucionesAlina Diaz GallegosPas encore d'évaluation
- La NaturalezaDocument14 pagesLa NaturalezaAlina Diaz GallegosPas encore d'évaluation
- INTRODUCCIONDocument1 pageINTRODUCCIONAlina Diaz GallegosPas encore d'évaluation
- 1 Epidemiologia de La Violencia y Maltrato InfantilDocument30 pages1 Epidemiologia de La Violencia y Maltrato InfantilAlina Diaz GallegosPas encore d'évaluation
- 0ESN Control de La Tuberculosis 2013Document30 pages0ESN Control de La Tuberculosis 2013Jaime RamirezPas encore d'évaluation
- La NaturalezaDocument14 pagesLa NaturalezaAlina Diaz GallegosPas encore d'évaluation
- La Sopa de PiedraDocument2 pagesLa Sopa de PiedraAlina Diaz GallegosPas encore d'évaluation
- Análisis de Situación de Salud en El PerúDocument32 pagesAnálisis de Situación de Salud en El PerúAlexia Villegas PamoPas encore d'évaluation
- La NaturalezaDocument14 pagesLa NaturalezaAlina Diaz GallegosPas encore d'évaluation
- Modelo de Abordaje Promocion de La SaludDocument38 pagesModelo de Abordaje Promocion de La SaludPercy Martínez Ponce100% (1)
- Situacion Nacional de La Anemia 2012Document21 pagesSituacion Nacional de La Anemia 2012Alina Diaz GallegosPas encore d'évaluation
- Autoestima e Inteligencia EmocionalDocument68 pagesAutoestima e Inteligencia EmocionalDAKARPAPas encore d'évaluation
- Evaluacion Del CrecimientoDocument20 pagesEvaluacion Del CrecimientoAlina Diaz GallegosPas encore d'évaluation
- Norma Técnica MINSA - Tuberculosis 2013Document128 pagesNorma Técnica MINSA - Tuberculosis 2013Paul PereyraPas encore d'évaluation
- Paradigmas Cientc3adficosDocument10 pagesParadigmas Cientc3adficosAmelia Kely Garcia MendozaPas encore d'évaluation
- Hip OcratesDocument2 pagesHip OcratesAlina Diaz GallegosPas encore d'évaluation
- 0ESN Salud Ocular 2013Document18 pages0ESN Salud Ocular 2013JOSCARDIPas encore d'évaluation
- Capitulo 5Document28 pagesCapitulo 5Alina Diaz Gallegos100% (1)
- Folleto Alcohol y DrogasDocument3 pagesFolleto Alcohol y DrogasJavi PedrazaPas encore d'évaluation
- Lamina Electroforjada - RejillasDocument12 pagesLamina Electroforjada - RejillasofingjbrmPas encore d'évaluation
- Bioquimica Ii Informe 3 Mañana FB7M2Document19 pagesBioquimica Ii Informe 3 Mañana FB7M2Francesca RojasPas encore d'évaluation
- ES2273904T3Document11 pagesES2273904T3Maria PazPas encore d'évaluation
- Informe Final Intervención CLP-9 (YPFB) PDFDocument29 pagesInforme Final Intervención CLP-9 (YPFB) PDFAlegil90Pas encore d'évaluation
- Plantas de Tratamiento-Busbanzá-Terminado 2Document15 pagesPlantas de Tratamiento-Busbanzá-Terminado 2Henry Eduardo RodriguezPas encore d'évaluation
- Nuevo de CromatografiaDocument42 pagesNuevo de CromatografiaYoPas encore d'évaluation
- Geologia General y FisicaDocument302 pagesGeologia General y FisicaAlexandra Guamann MendozaPas encore d'évaluation
- Diccionario Del Petroleo Español-Ingles PDFDocument34 pagesDiccionario Del Petroleo Español-Ingles PDFNaly Cas67% (3)
- Resumen Macromoléculas 2Document5 pagesResumen Macromoléculas 2Constanza LanzaPas encore d'évaluation
- NEREACLEP2Document2 pagesNEREACLEP2Ariel FragaPas encore d'évaluation
- EncuestaDocument2 pagesEncuestaArman HalePas encore d'évaluation
- Valvulas en Mineria - CatalogoDocument12 pagesValvulas en Mineria - CatalogoManuel Uturunco AguilarPas encore d'évaluation
- Pracrica 5Document3 pagesPracrica 5GeorginaMitjansDomenechPas encore d'évaluation
- Comparación de Instrumentos Rotatorios Entre Una Aleación NovedosaDocument17 pagesComparación de Instrumentos Rotatorios Entre Una Aleación NovedosaKelyn Ticona CanaveraPas encore d'évaluation
- La Matriz Extracelular - El Ecosistema de La CélulaDocument11 pagesLa Matriz Extracelular - El Ecosistema de La CélulaDanielAntonioValderramaMerejildoPas encore d'évaluation
- 13 05 17 Exp Tec CocinaDocument20 pages13 05 17 Exp Tec Cocinatomás quispePas encore d'évaluation
- Cyperkill Ficha Tecnica PDFDocument1 pageCyperkill Ficha Tecnica PDFPamela GaticaPas encore d'évaluation
- Amistar ZtraDocument11 pagesAmistar ZtraYony Alexander QuinteroPas encore d'évaluation
- Informacion Conductores para TripticoDocument4 pagesInformacion Conductores para TripticoRooldaan RoldanPas encore d'évaluation
- Mecanica de Fluidos y AlimentosDocument9 pagesMecanica de Fluidos y AlimentosCarolina ChávezPas encore d'évaluation
- PDF Pozo Perforado ProcedimientosDocument22 pagesPDF Pozo Perforado ProcedimientosnaghibPas encore d'évaluation
- Laboratorio 5 de OrganicaDocument14 pagesLaboratorio 5 de OrganicaJuniorZeladaPas encore d'évaluation
- Reporte Prueba de AcidezDocument21 pagesReporte Prueba de AcidezJonathan Alexander Escalera ChanPas encore d'évaluation
- 2018.02.26 - Equilibrios en Disolucion - IntroduccionDocument4 pages2018.02.26 - Equilibrios en Disolucion - IntroduccionTorrez ElvisPas encore d'évaluation
- Resolucion Guia 4Document15 pagesResolucion Guia 4CamilaAmapolaGonzalezPas encore d'évaluation
- IntroducciónDocument2 pagesIntroducciónCésar Augusto JuárezPas encore d'évaluation
- TejasDocument51 pagesTejasTotta OteroPas encore d'évaluation
- Irimo EsDocument164 pagesIrimo EsSantiagoYacobPas encore d'évaluation
- Proceso de La Exportacion Del CarbonDocument6 pagesProceso de La Exportacion Del CarbonsuryPas encore d'évaluation