Académique Documents
Professionnel Documents
Culture Documents
Guia de Laboratorio
Transféré par
Valeria Piovesan GalindoTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Guia de Laboratorio
Transféré par
Valeria Piovesan GalindoDroits d'auteur :
Formats disponibles
GUIA DE LABORATORIO DE BIOQUIMICA APLICADA EMI
LABORATORIO # 1
MEDIDAS DE BIOSEGURIDAD
OBJETIVO:
Al finalizar esta prctica el estudiante ser capaz de:
Aplicar las medidas de bioseguridad y de proteccin necesaria para para el desempeo
correcto de las prcticas laboratoriales de Bioqumica Aplicada.
INTRODUCCION
Todas las personas que trabajan con reactivos qumicos deben estar conscientes de los peligros
potenciales asociados a estos agentes, adems deben estar entrenadas en las prcticas y tcnicas
requeridas para manejar estos materiales de una manera segura.
Es por ello que antes de comenzar con las actividades prcticas, todas las personas involucradas
(estudiantes y profesores) tenemos la obligacin de conocer cules son las normas de seguridad a
seguir en el laboratorio de manera tal que el trabajo se realice con un riesgo mnimo de
exposicin, tanto para las personas que lo ejecutan como para el medio ambiente.
BIOSEGURIDAD - CONCEPTO
Conjunto de medidas preventivas que tienen como objetivo proteger la salud y la seguridad del
personal, de los usuarios y de la comunidad, frente a diferentes riesgos producidos por agentes
biolgicos, fsicos, qumicos y mecnicos
El reglamento interno de laboratorio, son un conjunto de reglas que se establecen para un mejor
desarrollo y mayor aprovechamiento de las practicas laboratoriales.
MEDIDAS DE BIOSEGURIDAD
Las siguientes normas deben ser observadas y cumplidas estrictamente en todas las secciones de
prctica de Bioqumica.
El estudiante debe tomar consciencia del riesgo al que est expuesto al manipular material
qumico, sospechar y tomar como peligrosa todas las sustancias analizadas.
No comer, ni ingerir, ningn lquido en laboratorio
No fumar en el laboratorio
Est prohibido que el estudiante realice experimentos por su propia cuenta, sin
supervisin del docente.
Cuando caliente algo, asegrese que la boca del recipiente que lo contiene no est dirigida
hacia otra persona. El lquido puede ser inflamable y salpicar.
Lic. VICTORIA MORON LAZARTE 1
GUIA DE LABORATORIO DE BIOQUIMICA APLICADA EMI
No se debe correr, gritar o jugar en laboratorio, este siempre atento a las indicaciones
para evitar cualquier tipo de accidente.
Leer claramente la etiqueta de todos los reactivos que est utilizando, para evitar
cualquier confusin.
Considere peligroso todas las sustancias qumicas del laboratorio, no los pruebe, ni las
toque sin autorizacin previa.
Uso obligatorio de elementos de proteccin personal como mandil blanco, manga larga,
correctamente abotonado, zapatos cerrados, y ocasionalmente guantes, barbijo y gorro.
REGLAMENTO INTERNO PARA EL LABORATORIO DE BIOQUIMICA
El cabello debe estar recogido totalmente, para evitar contaminacin con material
infeccioso, reactivos o quemaduras
Mantener las uas cortas para evitar el acumulo de material contaminado debajo de ellas.
El ingreso a laboratorio es a las 14:15 a.m. con una tolerancia mxima de 10 minutos, el
estudiante no podr ingresar despus de este tiempo.
Debe registrar en su libreta de apuntes todas sus observaciones, y elaborar con estos
datos y con la ayuda de su gua de laboratorio un informe que debe ser presentado al
inicio de la prxima prctica.
El estudiante que no estuvo presente en la prctica de laboratorio, no tiene derecho a
presentar su informe y pierde su nota.
Al inicio y al final de cada prctica debe desinfectarse adecuadamente los mesones de
trabajo, primero con una esponja y detergente neutro, luego enjuagar con agua y
finalmente pasar con un algodn embebido en alcohol por toda la superficie.
Los materiales de trabajo deben ser lavados primero con detergente neutro, enjuagar 3
veces con agua de grifo y luego pasarles etanol para su secado, antes de su uso y al
finalizar la prctica. No devolver materiales ni equipos sucios.
Al finalizar la prctica debe lavarse bien las manos con agua y jabn y desinfectarse con
alcohol.
CUESTIONARIO
1. Disear una etiqueta de laboratorio, con los datos correctos que debe contener.
2. Buscar pictogramas de bioseguridad para reactivos, peligrosos, nocivos, inflamables,
corrosivos, venenosos, etc. (Por lo menos 10 pictogramas)
Lic. VICTORIA MORON LAZARTE 2
GUIA DE LABORATORIO DE BIOQUIMICA APLICADA EMI
3. Que cuidados debe tener al manipular cidos concentrados.
4. Indique las medidas de primeros auxilio en caso de accidente con: cidos concentrados,
lcalis concentrados y sustancias orgnicas peligrosas.
5. Indique el sistema de clasificacin de sustancias qumicas peligrosas por colores.
BIBLIOGRAFIA
El estudiante colocara la bibliografa consultada para la elaboracin de este informe.
Lic. VICTORIA MORON LAZARTE 3
GUIA DE LABORATORIO DE BIOQUIMICA APLICADA EMI
LABORATORIO # 2
EL AGUA COMO ELECTROLITO Y pH
1.- OBEJTIVOS
- Verificar la conductividad elctrica del agua y otras sustancias qumicas.
- Determinar el pH de electrolitos dbiles y fuertes explicando el grado de disociacin para
cada sustancia.
2.- FUNDAMENTO TEORICO
Debido a su polaridad el agua puede solubilizar sustancias polares e inicas que actan como
electrolitos fuertes o dbiles y que actan como conductores elctricos.
3.- DESARROLLO DE LA PRCTICA
EXPERIENCIA # 1
CONDUCTIVIDAD ELECTRICA
Preparar las siguientes soluciones, y determinar si son conductores buenos, malos, o no conducen
la electricidad, explique en su conclusin cada uno de los resultados.
- 50ml de solucin de HCl 1 M
- 50 ml de solucin de CH3COOH (g)
- 50 ml de solucin de CH3COOH 1M
- 50 ml de solucin de NaOH 1 M
- 50 ml de solucin de NH3 1 M
- 50 ml de solucin de NaCl 1 M
- 50 ml de solucin de CH3COONa 1 M
- 50 ml de solucin de sacarosa al 5%
- 50 ml de H2O (d)
- 50 ml de mezcla de H2O (d) + CH3COOH (g)
EXPERIENCIA # 2
DETERMINACION DE pH
Determinar el pH de las soluciones preparadas anteriormente
Lic. VICTORIA MORON LAZARTE 4
GUIA DE LABORATORIO DE BIOQUIMICA APLICADA EMI
Colocar una gota de cada solucin sobre papel pH universal y leer en la escala de pHmetro.
Calcular el pH terico de cada solucin preparada tomando en cuenta que
Ka CH3COOH 1,8X10-5
EXPERIENCIA # 3
PREPRARACION DE UNA SOLUCION BUFFER
- Preparar 50 ml de la siguiente solucin tampn: 22 ml, CH3COOH 1M /28 ml, CH3COONa
1M
- Al tampn preparado medir el pH
- Adicionar 1 ml de una solucin de HCl 1M, luego medir el pH. Continuar la adicin hasta
verificar que el tampn se hubiese roto, finalmente dibujar la curva de titulacin.
4.- CONCLUSION
El estudiante debe realizar una conclusin por cada experiencial.
5.- BIBLIOGRAFIA
El estudiante colocara la bibliografa que consulto para la elaboracin del informe.
Lic. VICTORIA MORON LAZARTE 5
GUIA DE LABORATORIO DE BIOQUIMICA APLICADA EMI
LABORATORIO N 3
IDENTIFICACION DE PROTEINAS
1.- OBJETIVOS
Identificar protenas azufradas, aromticas
2.- FUNDAMENTO TEORICO
Las protenas son macromolculas compuestas por C, O, H y N. La mayora contiene
tambin S y P. Estos compuestos forman en primer lugar a los aminocidos, que son
los monmeros que conforman a las protenas. Los aminocidos presentan un
Carbono en el centro, un grupo amino (NH2), en uno de sus extremos, un grupo
carboxilo (-COOH) en otro y un grupo R de longitud y composicin variable. Dos
aminocidos se unen mediante enlace peptdico de tipo amida, con la correspondiente
perdida de agua. La unin de aminocidos da origen a los pptidos y a las protenas.
Identificacin de protenas azufradas
Las protenas que contienen azufre en su composicin pueden ser fcilmente
identificadas mediante la formacin de precipitados de sulfuro con la adicin de algn
metal al medio. Los precipitados de azufre son precipitados oscuros, marrn o
negruzcos en su mayora.
Reaccin xantoproteica
Es un mtodo que se puede utilizar para determinar la presencia de protenas solubles
en una solucin, empleando cido ntrico concentrado. La prueba da resultado positivo
en aquellas protenas con aminocidos portadores de grupos aromticos,
especialmente en presencia de tirosina. Si una vez realizada la prueba se neutraliza
con un lcali, se torna color amarillo oscuro a naranja.
La reaccin xantoproteica se puede considerar como una sustitucin electroflica
aromtica de los residuos de tirosina de las protenas por el cido ntrico dando un
compuesto coloreado amarillo a pH cido.
Lic. VICTORIA MORON LAZARTE 6
GUIA DE LABORATORIO DE BIOQUIMICA APLICADA EMI
La reaccin es cualitativa, no cuantitativa. Por ende determina la presencia o no de
protenas
Reaccin de Biuret
Es aquella que detecta la presencia de protenas, pptidos cortos y otros compuestos
con dos o ms enlaces peptdicos.
El reactivo de Biuret contiene hidrxido potsico (KOH) y sulfato cprico (CuSO4),
junto con tartrato de sodio y potasio (KNaC4H4O64H2O). El reactivo, de color azul,
cambia a violeta en presencia de protenas, y vira a rosa cuando se combina con
polipptidos de cadena corta. El hidrxido de potasio no participa en la reaccin, pero
proporciona el medio alcalino necesario para que tenga lugar.
Se usa normalmente en el ensayo de Biuret, un mtodo colorimtrico que permite
determinar la concentracin de protenas de una muestra mediante espectroscopia
ultravioleta-visible a una longitud de onda de 560 nm (para detectar el ion Cu2+).
Coagulacin de protenas
Las protenas debido a su gran tamao, forman con el agua sustancias coloidales.
Estas soluciones pueden precipitar con formacin de coagulo a temperaturas
superiores a 70C o al ser tratadas con soluciones salinas, acidas o alcohol, etc. La
coagulacin de protenas, es un proceso irreversible, y se debe a su desnaturalizacin
por los agentes indicados, que al contacto con la protena destruye su estructura
secundaria, terciaria y cuaternaria.
3.- DESARROLLO DE LA PRCTICA
EXPERIENCIA # 1
IDENTIFICACION DE AMINOACIDOS AZUFRADOS
Procedimiento
- Colocar en un tubo de ensayo 1 ml de albumina (de huevo).
- Adicionar 1ml de NaOH al 20%
- Con ayuda de una pipeta pasteur aadir 5 gotas de Pb(CH3COO)2 al 5%
- Observar el resultado obtenido.
Lic. VICTORIA MORON LAZARTE 7
GUIA DE LABORATORIO DE BIOQUIMICA APLICADA EMI
EXPERIENCIA # 2
REACCION XANTOPROTEINICA
Procedimiento
- En un tubo de ensayo colocar 2 ml de albumina (de huevo).
- Anadir 10 gotas de HNO3 concentrado.
- Llevar a bao mara, hasta ebullicin.
- Enfriar
- Adicionar 10 gotas de NaOH al 20%
- Observar el precipitado formado
EXPERIENCIA # 3
REACCION DE BIURET
Procedimiento
- En un tubo colocar 2 ml de albumina (de leche)
- Adicionar 2 ml de NaOH al 20% y agitar
- Adicionar 5 gotas de CuSO4 al 1%
- Observar los resultados
EXPERIENCIA # 4
DESNATURALIZACION DE PROTEINAS
Procedimiento
- En un tubo de ensayo colocar 2 ml de albumina (de huevo) diluida
- Calentar a un mechero
- Observar la desnaturalizacin de las protenas
4.- CUESTIONARIO
1.- Investigue las caractersticas de los precipitados de sulfuro
2.- En la reaccin de biuret, cual es el compuesto que se forma al final de la reaccin.
3.- Explique el proceso de desnaturalizacin de protenas
4.- Para qu tipo de aminocidos se utiliza la reaccin xantoproteinica.
Lic. VICTORIA MORON LAZARTE 8
GUIA DE LABORATORIO DE BIOQUIMICA APLICADA EMI
LABORATORIO # 4
IDENTIFICACION DE CARBOHIDRATOS
1.- OBJETIVOS
- Identificar la presencia de azcares reductores mediante la reaccin de Fehling
- Demostrar que el almidn es un polisacrido compuesto por muchas molculas de
azcares sencillos (glucosa).
- Comprobar la existencia de amilasa en la saliva.
2.- FUNDAMENTO TEORICO
Los carbohidratos son compuestos orgnicos formados por carbono, hidrgeno y
oxgeno. Estos forman parte e intervienen en una gran cantidad de procesos de los
seres vivientes. Los ms importantes son de tres tipos: energticos, de reserva y
estructurales. Desde el punto de vista energtico uno de los carbohidratos ms
sencillos, la glucosa constituye el material de ms rpido aprovechamiento en el
organismo y su oxidacin satisface las necesidades energticas y calricas del
mismo.
Como materiales de reserva, los carbohidratos existen en reino vegetal en forma de
almidones y en el reino animal en forma de glucgenos; tanto uno como el otro son
susceptibles de convertirse en glucosa para poder ser utilizados. Y en el aspecto
estructural, los carbohidratos llevan a cabo una importante funcin en los vegetales
debido a que la clula, que es su estructura leosa o esqueleto, est constituida por
cadenas de azcares simples. En los animales tambin sucede lo anterior, as
tenemos que el exoesqueleto de muchos artrpodos est constituido tambin por
cadenas de carbohidratos simples.
Los monosacridos y la mayora de los disacridos (excepto la sacarosa) son
azcares reductores debido a la presencia de un grupo carbonilo libre capaz de
oxidarse y pasar a cido. En medio alcalino, reducen con facilidad a agentes
oxidantes suaves como los iones metlicos Cu2+, Fe3+, Ag+. Estas reacciones redox
constituyen la base de las pruebas de Fehling y Benedict, que permiten identificar, e
incluso cuantificar, la presencia de azcares reductores en un material biolgico y han
sido frecuentemente utilizadas en la determinacin del contenido de glucosa en
sangre y orina para el diagnstico de la diabetes mellitus.
Si el azcar es reductor se oxida al reaccionar con el reactivo de Fehling, el carbono
carbonlico se oxida a cido carboxlico, mientras que el in cprico (Cu+2), antes de
color azul intenso, se reduce a in cuproso (Cu+2) que precipita de la disolucin en
forma de xido cuproso (Cu2O) de color rojo ladrillo.
La glucosa es un monosacrido y por tanto reductor. La reaccin positiva se
manifiesta con la formacin de un precipitado de color rojo de xido cuproso. Con el
zumo de uva la reaccin es positiva, contiene azcares reductores (la glucosa y la
fructosa abundan en estado libre en las frutas). La sacarosa no tiene grupo carbonilo
libre por lo que no da reaccin positiva con el Fehling.
Lic. VICTORIA MORON LAZARTE 9
GUIA DE LABORATORIO DE BIOQUIMICA APLICADA EMI
3.- DESARROLLO DE LA PRCTICA
EXPERIENCIA # 1
CAPACIDAD REDUCTORA DE AZUCARES
- Preparar 50 ml de solucin de glucosa al 3%
- Preparar 50 ml de solucin de sacarosa al 3%
- Preparar 50 ml de solucin de almidn al 0,1%
- Colocar en un tubo de ensayo 3ml de glucosa
- Aadir 1ml de Reactivo de Fehling A
- Aadir 1ml de Reactivo de Fehling B
- Llevar el tubo a Bao Mara o calentamiento directo por unos 2 minutos,
hasta la aparicin de un color rojo ladrillo si la reaccin es positiva.
- Repetir el mismo procedimiento con solucin de sacarosa y almidn.
EXPERIENCIA # 2
IDENTIFICACION DE ALMIDON
- Colocar en un tubo de ensayo 3ml de solucin de almidn
- Aadir 2 a 3 gotas de lugol
- Observar los resultados, se formara un complejo azul oscuro si al reaccin
es positiva.
- Repetir este mismo procedimiento con solucin de sacarosa y glucosa.
- Explicar los resultados obtenidos.
- Llevar este tubo a bao mara por unos minutos.
- Observar y explicar los resultados.
EXPERIENCIA # 3
IDENTIFICACION DE AMILASA EN LA BOCA
- Colocar en un tubo de ensayo 5 ml de saliva
- Aadir 3 ml de solucin de almidn
- Agitar vigorosamente
- Aadir 2 a 3 gotas de solucin de lugol
- Observar y explicar los resultados.
4.- CONCLUSION
El estudiante redactara una conclusin de acuerdo a los resultados obtenidos para cada
experiencia.
5.- CUESTIONARIO
1.- Explique por qu la glucosa es un azcar reductor mientras que sacarosa y el almidn
no lo son.
2.- Explique el fundamento de la reaccin de Fehling
3.- Cual es la diferencia estructural entre almidn y celulosa. Por qu los seres humanos
no podemos usar celulosa como fuente energtica.
4.- Cual es la composicin qumica del lugol, como se prepara en laboratorio.
Lic. VICTORIA MORON LAZARTE 10
GUIA DE LABORATORIO DE BIOQUIMICA APLICADA EMI
LABORATORIO N 5
EXTRACCION E IDENTIFICACION DEL ALMIDON
1.- OBJETIVOS
Extraer el almidn proveniente de diferentes fuentes naturales (cereales y
tubrculo)
Determinar el origen vegetal del almidn segn sus caractersticas microscpicas
por comparacin con datos bibliogrficos.
Identificar qumicamente el almidn.
2.- FUNDAMENTO TEORICO
2.1.- Caractersticas qumicas
El almidn, es un polisacrido de reserva de vegetales. Se trata de un polmero de
glucosa, formado por dos tipos de molculas: amilosa (20 a 30%), ligadas a travs de un
enlace (1 - 4) para formar un polmero lineal, que se encuentra enrollado en forma de
hlice, y amilopectina (80 a 70%), formado por enlaces (1 4) y (1 6) formando un
polmero altamente ramificado. El almidn da una coloracin azul intenso con soluciones
de yodo. Puede ser hidrolizado mediante la accin enzimtica (amilasa) o en presencia de
soluciones acidas, dando molculas de glucosa, que fcilmente puede ser identificado con
el reactivo de fehling, Tollens y otros.
2.2.- Propiedades fsicas
El almidn se presenta en masas irregulares, angulosos, en forma de polvo blanco. Es
insoluble en agua fra, pero forma una solucin coloidal por ebullicin, por enfriamiento se
forma una jalea traslcida conocido como engrudo de almidn. El engrudo de almidn se
colorea en azul intenso con solucin de yodo, color que desaparece por calentamiento a
93 C, reapareciendo por enfriamiento.
2.3.- Caractersticas Microscpicas
El almidn formado en la clula vegetal, se acumula en forma de granos que van
creciendo a partir de un punto o hilo, que puede ser central o excntrico. Los granos con
Lic. VICTORIA MORON LAZARTE 11
GUIA DE LABORATORIO DE BIOQUIMICA APLICADA EMI
hilo excntricos suelen ser ms largos que anchos.
El grano de almidn se forma a partir de capas sucesivas que giran alrededor del hilo,
pudiendo observarse claramente la presencia de anillos o estriaciones concntricas,
siendo estas importantes para la caracterizacin e identificacin. El aspecto final del grano
de almidn es variable y caracterstico de un vegetal, como se puede detallar a
continuacin:
a) Almidn de Papa
Proveniente del tubrculo Solanum tuberosum L. (Solanceas). Son granos aislados de
forma ovoide, tamao variable, hilo excntrico situado en la parte ms estrecha del grano
y estras visibles.
b) Almidn de Maz
Proveniente de los frutos del Zea mays L. (Gramneas). Son granos aislados o en grupos
de 2 a 3, forma polidrica, tamao ms o menos uniforme (15 ), con hilo central y sin
estras visibles.
c) Almidn de Arroz
Proveniente de Oryza sativa L. (Gramneas). Son granos aislados o compuestos, estos
granos compuestos se disocian fcilmente frotando ligeramente el cubre sobre el
portaobjeto. Forma polidrica, tamao alrededor de 5 , hilo central, sin estras visibles.
d) Almidn de Trigo
Proveniente de Triticum sativum L. (Gramneas). Son granos aislados de forma ms o
menos redondeada, tamao variable, granos pequeos de 2 20 y granos grandes de
alrededor de 30 , hilo central, estriaciones concntricas pero bien dbiles.
Lic. VICTORIA MORON LAZARTE 12
GUIA DE LABORATORIO DE BIOQUIMICA APLICADA EMI
e) Almidn de Yuca
Proveniente del tubrculo Manihot utilsima (Eurphorbiaceae). Son granos de 2 a 7
corpsculos reunidos. La superficie de contacto de unos con otros son planas, la mayora
son subesfricas o redondas-polidricas, presenta hilo punteado o hendido y estriaciones
concntricas.
f) Almidn de Leguminosas
Granos de forma generalmente arrionada y estratificaciones concntricas muy visibles.
En el centro presentan una gran hendidura de la cual parten hacia la periferia del grano
una serie de ranuras radiales, cortas y anchas tomando el aspecto de palo bifurcado,
todas las leguminosas tienen el mismo tipo de almidn diferencindose solo en el tamao.
Figura 1: Grnulos de almidn A) Papa; B) Maz; C) Avena; D) Trigo
3. PARTE PRCTICA
EXPERIENCIA N 1
EXTRACCION DEL ALMIDON
PROCEDIMIENTO
1. Si se parte de cereales, triturar a polvo grueso, si es a partir de tubrculos,
primeramente y rallar para hacer como especie de papilla.
2. En primer caso (polvo triturado), tamizar.
3. El polvo obtenido, o la papilla, se deja remojar en agua destilada, para que los
granos de almidn (parte solida) pase a la fase liquida (agua destilada).
4. Dejar en reposo durante media hora para completar la disolucin de los granos de
almidn en la fase liquida.
5. Lavar con tres aguas, las aguas del lavado se guardan, debido a que los granos se
encuentran sobrenadando en este medio.
Lic. VICTORIA MORON LAZARTE 13
GUIA DE LABORATORIO DE BIOQUIMICA APLICADA EMI
6. Dejar reposar durante media hora, los granos de almidn sedimentan como polvo
blanco.
7. Decantar toda el agua.
8. Se recoge todo el polvo blanco obtenido en papel filtro.
9. Se deja secar.
EXPERIENCIA N 2
IDENTIFICACION MICROSCOPICA
Los almidones pueden ser caracterizados mediante un examen microscpico. Los granos
de almidn tienen un tamao, forma y estructura determinada, segn su procedencia. Por
lo que es posible distinguir los almidones procedentes de especies distintas segn sus
caractersticas.
a) Se debe observar las siguientes caractersticas:
b) Estado del grano (aislado o en masas de formas definidas).
c) Forma y dimensin.
d) Presencia o ausencia de hilo, su forma y posicin.
e) Presencia o ausencia de estras.
PROCEDIMIENTO
1. Realizar un montaje con agua
2. En un portaobjeto, colocar una gota de agua destilada
3. Suspender en esta gota una pequea porcin de la muestra
4. Cubrir con un cubreobjeto, evitando la formacin de burbujas de aire
5. Observar al microscopio con objetivo 40 X
6. Describir las caractersticas observadas
EXPERIENCIA N 3
CARACTERIZACION QUIMICA
La amilosa reacciona con el yodo formando un complejo de color azul intenso, mientras
que la amilopectina presenta coloracin azul-violeta en presencia de yodo.
Lic. VICTORIA MORON LAZARTE 14
GUIA DE LABORATORIO DE BIOQUIMICA APLICADA EMI
HIDRLISIS ACIDA DEL ALMIDON
La hidrlisis acida del almidn tiene lugar utilizando cidos inorgnicos; esta degradacin
acida, da lugar a varios compuestos intermedios, antes de obtener la glucosa.
Durante el proceso de la hidrlisis tanto la amilosa como la amilopectina se van
desdoblando o rompiendo los enlaces (1-4) en el primer caso, y los enlaces (1-6) en el
segundo caso, dando lugar a la formacin de polisacridos de cadena corta pero
ramificadas las llamadas dextrina, que segn el color que dan al reaccionar con el yodo
en solucin de Lugol, se denomina:
Amilodextrina + I2 = Rojo violeta
Eritrodextrina + I2 = Rojo
Acrodextrina + I2 = Amarillo (color del lugol)
PROCEDIMIENTO
1. Tomar 1g de almidn obtenido, preparar una suspensin en 10 ml de agua,
obtenindose una suspensin lechosa.
2. Llevar a ebullicin 200 ml de agua, verter los 10 ml de suspensin del almidn,
hasta que se torne transparente la suspensin.
3. Tomar de esta solucin 5 ml y dividir en dos tubos, en el primer tubo se aade 1
gota de lugol, al segundo tubo 0.5 ml del reactivo de fehling (Fehling A: CuSO4
disuelto en H2O y Fehling B: NaOH y tartrato Na-K disuletos en agua), observar
las reacciones (fehling reacciona en medio bsico).
4. Al resto de la solucin que continua en ebullicin se agrega 5 ml de HCl
concentrado, pasados 5 minutos se procede a tomar 5 ml. Se divide en dos tubos
y se siguen los mismos pasos indicados en la anterior etapa.
5. Continuar con los pasos ya indicados hasta observar en el tubo con la solucin de
lugol un color amarillo y el tubo con el reactivo de fehling aparece un precipitado
anaranjado o rojo ladrillo, que indican que se llev a cabo la hidrlisis total, dando
por consiguiente la siguiente reaccin.
CuSO4 + 2NaOH Cu(OH)2 + Na2SO4 (azul)
Cu (OH)2 + RCOH Cu2O + RCOOH+H2O(rojo ladrillo)
Esta reaccin indica la presencia de molculas de glucosa; dando lugar por
Lic. VICTORIA MORON LAZARTE 15
Vous aimerez peut-être aussi
- Manual de practicas de laboratorio de MicrobiologíaD'EverandManual de practicas de laboratorio de MicrobiologíaÉvaluation : 4 sur 5 étoiles4/5 (7)
- Manual de Practicas de Quimica OrganicaDocument69 pagesManual de Practicas de Quimica OrganicaShandira Itzel Idiaquez RiosPas encore d'évaluation
- Guia de Practica Bioquimica Unid PDFDocument49 pagesGuia de Practica Bioquimica Unid PDFSara Underwood0% (1)
- Practicas de Bioquimica 2023Document89 pagesPracticas de Bioquimica 2023Aldo Iván QUPas encore d'évaluation
- Manual MicroDocument74 pagesManual MicroJuan DuartePas encore d'évaluation
- Guion Toxicologia VeterinariaDocument83 pagesGuion Toxicologia VeterinariaDiana Patricia Molano PerezPas encore d'évaluation
- Estudio de Equilibrios Ácido-BaseDocument5 pagesEstudio de Equilibrios Ácido-BaseClaudia HerreraPas encore d'évaluation
- Manual de Practicas Quimica Inorganica 2022Document61 pagesManual de Practicas Quimica Inorganica 2022El salado del PesPas encore d'évaluation
- Practicas de Bioquímica 2009Document38 pagesPracticas de Bioquímica 2009george_mtm28Pas encore d'évaluation
- Manual Química Orgánica Ciclo I - 2022Document30 pagesManual Química Orgánica Ciclo I - 2022Toloza VladimirPas encore d'évaluation
- GUÍAS DE QUÍMICA GENERAL Semestre A 2017Document41 pagesGUÍAS DE QUÍMICA GENERAL Semestre A 2017luis miguel erazo zamudioPas encore d'évaluation
- Guía de Práctica Química InorganicaDocument62 pagesGuía de Práctica Química InorganicaBrigite de la CruzPas encore d'évaluation
- Guía de Práctica Química InorganicaDocument62 pagesGuía de Práctica Química InorganicaBrigite de la CruzPas encore d'évaluation
- Práctica 1 BI-244Document17 pagesPráctica 1 BI-244CN Kenyu AlexPas encore d'évaluation
- Primer Practica QUIMICADocument11 pagesPrimer Practica QUIMICAyair muñozPas encore d'évaluation
- José Ivan Trejo RojasDocument11 pagesJosé Ivan Trejo RojasAngel Baez BaezPas encore d'évaluation
- Universidad Autonoma de Baja California PDFDocument28 pagesUniversidad Autonoma de Baja California PDFTaciturnoait NihilistaPas encore d'évaluation
- Manual de Practicas Bioq. I Sem - B - 22Document40 pagesManual de Practicas Bioq. I Sem - B - 22pamsPas encore d'évaluation
- Guion Fundamentos Toxicologia PDFDocument83 pagesGuion Fundamentos Toxicologia PDFAlejandro GonzaloPas encore d'évaluation
- Guion Prácticas Bioquímica 23-24Document20 pagesGuion Prácticas Bioquímica 23-24hugoieslaniaPas encore d'évaluation
- Guia P. Biologia Celular y MolecularDocument36 pagesGuia P. Biologia Celular y MolecularNathan OrtizPas encore d'évaluation
- Guía de BioquimicaDocument103 pagesGuía de BioquimicaMARICIELO CCALLO HUAMANIPas encore d'évaluation
- FileDocument33 pagesFileALEJANDRO PALOMINO FIGUEROA0% (1)
- Guia de Practica QuimicaDocument82 pagesGuia de Practica QuimicaGreciaPas encore d'évaluation
- QUÍMICA Guía de Práctica 2023 I IDocument80 pagesQUÍMICA Guía de Práctica 2023 I IAshly Saravia jimenezPas encore d'évaluation
- Practicas de Bioquimica 2020 A-1-13Document13 pagesPracticas de Bioquimica 2020 A-1-13Andres Delgado TorresPas encore d'évaluation
- Practicas de BromatologiaDocument30 pagesPracticas de BromatologiaAdela Velasco100% (1)
- Informe de Laboratorio 1Document18 pagesInforme de Laboratorio 1ivan cipriano ricaldiPas encore d'évaluation
- Guia 2008 Lab QuimDocument100 pagesGuia 2008 Lab Quimapi-3711222100% (2)
- Manual Fisicoquimica - Barceló PDFDocument97 pagesManual Fisicoquimica - Barceló PDFGerardo JimenezPas encore d'évaluation
- Guía de Práctica de Química-2020 IDocument73 pagesGuía de Práctica de Química-2020 IRODRIGO RAULPas encore d'évaluation
- QUÍMICA Guía de Práctica 2019. Modificada 1Document82 pagesQUÍMICA Guía de Práctica 2019. Modificada 1Wendy Jhasmin HuallpaPas encore d'évaluation
- Manual de Lab Quimica Orgánica Aplicada CorregidoDocument69 pagesManual de Lab Quimica Orgánica Aplicada CorregidoOscar Lora GuerreroPas encore d'évaluation
- Guia BioquimicaDocument107 pagesGuia Bioquimicaraul_mestasPas encore d'évaluation
- Biotecnologia MetalurgicaDocument20 pagesBiotecnologia MetalurgicaFrank León La CruzPas encore d'évaluation
- Guía de Práctica Presencial Escuela Profesional de EnfermeríaDocument19 pagesGuía de Práctica Presencial Escuela Profesional de EnfermeríaDenzel RMPas encore d'évaluation
- Practica 5Document104 pagesPractica 5Luis Miguel FloresPas encore d'évaluation
- Manual de Química Analítica Upao - 2022Document87 pagesManual de Química Analítica Upao - 2022MARICIELO ISABEL SANCHEZ FERNANDEZ100% (2)
- PracticaDocument30 pagesPracticashaneriPas encore d'évaluation
- Química Orgánica-Guía de LaboratorioDocument140 pagesQuímica Orgánica-Guía de LaboratorioMary Cielo CalderonPas encore d'évaluation
- Guias Lab BioquimicaDocument44 pagesGuias Lab BioquimicaDiego QuinteroPas encore d'évaluation
- Manual de Práctica de Bioquímica-2022-2Document94 pagesManual de Práctica de Bioquímica-2022-2Marcos Javier Palomino CusiPas encore d'évaluation
- Guía Recomendaciones para El LaboratorioDocument4 pagesGuía Recomendaciones para El LaboratorioRAUL ANDRES DIAZ CHACONPas encore d'évaluation
- Practicas de Laboratorio de BioquimicaDocument45 pagesPracticas de Laboratorio de BioquimicaKaysser Alberto Villar CaleroPas encore d'évaluation
- Guia de Practicas Bioquimica 2019-IDocument54 pagesGuia de Practicas Bioquimica 2019-IAnonymous s1iqsr0i6TPas encore d'évaluation
- Guía de Práctica Química OrgánicaDocument120 pagesGuía de Práctica Química OrgánicaDaniela Melanie Pecho GrandaPas encore d'évaluation
- Guias Lab Química OrgánicaDocument26 pagesGuias Lab Química OrgánicaAngie ParraPas encore d'évaluation
- Manual de Práctica de Bioquímica-2022-2 PDFDocument94 pagesManual de Práctica de Bioquímica-2022-2 PDFMishelle PastorPas encore d'évaluation
- Guía de Laboratorio Quimica 1Document66 pagesGuía de Laboratorio Quimica 1Alan ValenzuelaPas encore d'évaluation
- Química OrgánicaDocument140 pagesQuímica OrgánicaRONALDPas encore d'évaluation
- Manual de Laboratorio Evaluacion Sensorial II - 2020Document35 pagesManual de Laboratorio Evaluacion Sensorial II - 2020STIVEN ORTEGA QUINTEROPas encore d'évaluation
- Mediciones y métodos de uso común en el laboratorio de QuímicaD'EverandMediciones y métodos de uso común en el laboratorio de QuímicaÉvaluation : 4.5 sur 5 étoiles4.5/5 (3)
- Guiones experimentales para la enseñanza y aprendizaje del laboratorio de Toxicología (clave 1614)D'EverandGuiones experimentales para la enseñanza y aprendizaje del laboratorio de Toxicología (clave 1614)Pas encore d'évaluation
- Laboratorio de microbiología para optómetrasD'EverandLaboratorio de microbiología para optómetrasPas encore d'évaluation
- Métodos analíticos de microbiología general y aplicadaD'EverandMétodos analíticos de microbiología general y aplicadaÉvaluation : 5 sur 5 étoiles5/5 (1)
- Dominando las Tinciones: Manual para el Laboratorio MicrobiológicoD'EverandDominando las Tinciones: Manual para el Laboratorio MicrobiológicoPas encore d'évaluation
- Manual de prácticas de laboratorio en microbiología veterinariaD'EverandManual de prácticas de laboratorio en microbiología veterinariaPas encore d'évaluation
- EMI Realidad NacionalDocument2 pagesEMI Realidad NacionalValeria Piovesan GalindoPas encore d'évaluation
- Resumen 1Document9 pagesResumen 1Valeria Piovesan GalindoPas encore d'évaluation
- Delimitación y Codificación Unidades Hidrográficas Dpto - Santa CruzDocument70 pagesDelimitación y Codificación Unidades Hidrográficas Dpto - Santa CruzbeidarongPas encore d'évaluation
- Trabajo 'Practico 2Document2 pagesTrabajo 'Practico 2Valeria Piovesan GalindoPas encore d'évaluation
- Sintesis 4Document2 pagesSintesis 4Valeria Piovesan GalindoPas encore d'évaluation
- P2 GeoreferenciaDocument6 pagesP2 GeoreferenciaValeria Piovesan GalindoPas encore d'évaluation
- Tema 7Document29 pagesTema 7Vladi Chamorro PajueloPas encore d'évaluation
- Procesos Hidrologicos - Geomorfologia de La CuencaDocument64 pagesProcesos Hidrologicos - Geomorfologia de La CuencaValeria Piovesan GalindoPas encore d'évaluation
- Ley 2066Document39 pagesLey 2066Valeria Piovesan GalindoPas encore d'évaluation
- MGA 001 Manual Del SGA PDFDocument27 pagesMGA 001 Manual Del SGA PDFIvan R BarajasPas encore d'évaluation
- (P7) EscurrimientoDocument27 pages(P7) EscurrimientoValeria Piovesan GalindoPas encore d'évaluation
- Sintesis 1Document6 pagesSintesis 1Valeria Piovesan GalindoPas encore d'évaluation
- Aprendiendo A Vivir FelizAJAJJAJAJDocument6 pagesAprendiendo A Vivir FelizAJAJJAJAJValeria Piovesan GalindoPas encore d'évaluation
- Ejercicios para RepasarDocument30 pagesEjercicios para RepasarValeria Piovesan GalindoPas encore d'évaluation
- Impieza NoviembreDocument1 pageImpieza NoviembreValeria Piovesan GalindoPas encore d'évaluation
- CARATULAemi OficialDocument1 pageCARATULAemi OficialValeria Piovesan GalindoPas encore d'évaluation
- Dietas HipocalóricasDocument14 pagesDietas HipocalóricasCrisD.AlbuernePas encore d'évaluation
- MMDocument2 pagesMMValeria Piovesan GalindoPas encore d'évaluation
- Dietas HipocalóricasDocument14 pagesDietas HipocalóricasCrisD.AlbuernePas encore d'évaluation
- Geopolitica en BoliviaDocument14 pagesGeopolitica en BoliviaValeria Piovesan Galindo100% (2)
- P2 GeoreferenciaDocument6 pagesP2 GeoreferenciaValeria Piovesan GalindoPas encore d'évaluation
- MMDocument2 pagesMMValeria Piovesan GalindoPas encore d'évaluation
- Good MorningDocument1 pageGood MorningValeria Piovesan GalindoPas encore d'évaluation
- MMDocument2 pagesMMValeria Piovesan GalindoPas encore d'évaluation
- MMDocument2 pagesMMValeria Piovesan GalindoPas encore d'évaluation
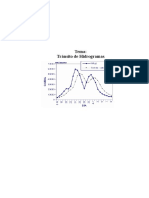
- (T7.2) Transito PDFDocument10 pages(T7.2) Transito PDFValeria Piovesan GalindoPas encore d'évaluation
- 3 Abril - Ses - Expreso Lo Q Siento - TutoriaDocument5 pages3 Abril - Ses - Expreso Lo Q Siento - TutoriaRosa Edita Flores CastroPas encore d'évaluation
- Ento CamelidoDocument1 pageEnto CamelidopatchparchePas encore d'évaluation
- Aperturas Falso SelfDocument27 pagesAperturas Falso SelfMaría José LamasPas encore d'évaluation
- Manejo DefensivoDocument22 pagesManejo DefensivoEnrique Roldan Montes100% (1)
- Taller 1 HigieneDocument4 pagesTaller 1 Higieneninfa paredesPas encore d'évaluation
- ¡Usted y La Seguridad!Document1 page¡Usted y La Seguridad!Richard Cristian Mendoza GarciaPas encore d'évaluation
- Cinco Tibetan OsDocument17 pagesCinco Tibetan OsJuliana Rozo100% (1)
- CAPÍTULO I Cancer de ProstataDocument7 pagesCAPÍTULO I Cancer de ProstatajrgoferPas encore d'évaluation
- Formato de Valoracion MedicaDocument2 pagesFormato de Valoracion MedicaTerrazas Flowers Days75% (4)
- 3° MEDIO Guía 1 Classroom. Aplicación de Cuidados BásicosDocument5 pages3° MEDIO Guía 1 Classroom. Aplicación de Cuidados BásicosjatsiryPas encore d'évaluation
- PanfletoDocument6 pagesPanfletoLudin LeivaPas encore d'évaluation
- Resumen de ClinicaDocument15 pagesResumen de ClinicaKaren Salas100% (1)
- Avance 3 - CRMDocument7 pagesAvance 3 - CRMFabiola Vega0% (1)
- Tesina CalculoDocument66 pagesTesina CalculoFred GoicocheaPas encore d'évaluation
- AccidentesDocument94 pagesAccidentesJuana Tacora CarbajalPas encore d'évaluation
- Clinica 2 OcredDocument157 pagesClinica 2 OcredToni CrespoPas encore d'évaluation
- Cronologia de Las Amputaciones PDFDocument14 pagesCronologia de Las Amputaciones PDFSERGIO PEÑAPas encore d'évaluation
- Abs SubjtivasDocument6 pagesAbs SubjtivasCARLOS ANDRES SALAZAR PRIETOPas encore d'évaluation
- Derrame Pleural y NeumotóraxDocument23 pagesDerrame Pleural y Neumotóraxfrazao13Pas encore d'évaluation
- Anexo 3 - Acuerdo 097-ADocument7 pagesAnexo 3 - Acuerdo 097-AERICK ALEXANDER RAMOS VELASTEGUIPas encore d'évaluation
- Metodos de Evalución de Trabajos RepetitivosDocument4 pagesMetodos de Evalución de Trabajos Repetitivoskaren lorena caballero guerreroPas encore d'évaluation
- Neuropsicologia Del Envejecimiento Normal y Deterioro Cognitivo LeveDocument25 pagesNeuropsicologia Del Envejecimiento Normal y Deterioro Cognitivo LeveEdinson MaxPas encore d'évaluation
- Intervención Policial en Tiempos de PandemiaDocument20 pagesIntervención Policial en Tiempos de PandemiaNelly Medali Barturen FloresPas encore d'évaluation
- Manual para La Implementación Del Sistema de Gestión en Seguridad y Salud en El TrabajoDocument50 pagesManual para La Implementación Del Sistema de Gestión en Seguridad y Salud en El TrabajoSunafil90% (101)
- Presentacion CotrimoxazolDocument35 pagesPresentacion CotrimoxazolBel Zeballos RadaPas encore d'évaluation
- Taller #2 - Antígenos y AnticuerposDocument2 pagesTaller #2 - Antígenos y AnticuerposAngela Chamorro100% (1)
- Complicaciones en La HemiartroplastiaDocument7 pagesComplicaciones en La HemiartroplastiaC Martin TraumatoPas encore d'évaluation
- Acta de Autorizacion A Clases PresencialesDocument1 pageActa de Autorizacion A Clases PresencialesYudi Paola Díaz RojasPas encore d'évaluation
- Madres Que Matan Preguntas y ContextosDocument24 pagesMadres Que Matan Preguntas y ContextosSandra MarinPas encore d'évaluation
- 1 PBDocument11 pages1 PBLuis MGamboaPas encore d'évaluation