Académique Documents
Professionnel Documents
Culture Documents
2015 Fenilcetonuria
Transféré par
Belle AmoreTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
2015 Fenilcetonuria
Transféré par
Belle AmoreDroits d'auteur :
Formats disponibles
Qumica Biolgica Patolgica Tema 11: Fenilcetonuria Ao: 2015
HIPERFENILALANINEMIA y FENILCETONURIA
1-INTRODUCCION
La fenilcetonuria (phenylketonuria o PKU) es una enfermedad gentica que sigue un
patrn de herencia autosmico recesivo (OMIM 261600). Se debe a una deficiencia
en la funcin de la fenilalanina hidroxilasa (fenilalanina 4-monooxigenasa, PAH,
EC.1.14.16.1), primera enzima limitante en el catabolismo de la fenilalanina. Su
deficiencia da lugar a una acumulacin de fenilalanina en sangre y tejidos
(hiperfenilalaninemia) y a un aumento en la eliminacin de sus metabolitos en orina
(fenilcetonuria).
La fenilalanina (Phe) es un aminocido esencial que compone aproximadamente el
5% de las protenas de origen natural y que se absorbe a nivel intestinal de forma
competitiva con otros aminocidos neutros. La hidroxilacin de la fenilalanina
consume aproximadamente el 60-75% de la Phe procedente de la dieta y de la
degradacin tisular de protenas, mientras que el 25-40% restante se utiliza para la
regeneracin de protenas endgenas.
Hiperfenilalaninemia es un trmino genrico dado a una concentracin de
fenilalanina plasmtica elevada de forma persistente sobre la distribucin normal de
los valores en plasma. Los valores normales de la fenilalanina en plasma,
independientemente de la edad, son aproximadamente de 60 mol/L (1mg/dl). Los
niveles varan a lo largo del da pero dentro de lmites muy estrechos. Los niveles de
la fenilalanina en sangre y los distintos tejidos tienen escasas diferencias y se
encuentran siempre en equilibrio homeosttico. Los individuos con un defecto en el
sistema de hidroxilacin de la fenilalanina tienen niveles en sangre superiores a 120
mol/L (2mg/dl), siendo ms elevados cuanto menor sea la actividad residual de las
enzimas implicadas. Los niveles elevados de fenilalanina actan por diferentes
mecanismos como txicos cerebrales produciendo muerte o apoptosis neuronal
progresiva, dando lugar a diferentes grados de alteracin en el desarrollo cognitivo de
las personas afectadas. La manifestacin clnica ms importante de la
hiperfenilalanimemia es por tanto el retraso mental moderado-severo. Tambin se
puede acompaar de palidez de piel, eccemas pruriginosos y un olor caracterstico a
ratones o paja mojada de las secreciones corporales cuando los niveles de fenilalanina
son extremadamente elevados y se trasforman en fenilactico.
Cualquier defecto en la actividad del sistema de hidroxilacin de la fenilalanina puede
dar lugar a una hiperfenilalaninemia, pero aproximadamente el 98% de las
rea de Qumica Biolgica 1
Qumica Biolgica Patolgica Tema 11: Fenilcetonuria Ao: 2015
hiperfenilalaninemias estn asociadas a deficiencias en la funcin de la fenilalanina
hidroxilasa.
La incidencia de esta enfermedad es dependiente de la zona geogrfica de estudio,
para Europa es de 1:10000 recin nacidos (Scriver and Kaufman 2001) y la
estimacin de portadores por lo tanto es 1 de cada 50 individuos. Algunas
caractersticas de la enfermedad se encuentran recogidas en la Tabla 1.
La primera descripcin de la enfermedad fue hecha por Asbjrn Flling en 1934, al
estudiar dos hermanos con retraso mental que excretaban en orina cantidades
elevadas de cido fenilpirvico, por lo que llam a esta patologa oligofrenia
fenilpirvica. En 1939 Penrose confirm la enfermedad, a la que rebautiz como
Fenilcetonuria, y describi su herencia autosmica recesiva. En 1947, Jervis postul
que el defecto metablico de la fenilcetonuria consista en la imposibilidad de oxidar
la fenilalanina a tirosina, y en 1953 demostr la deficiencia de fenilalanina hidroxilasa
en el hgado de un paciente. Ese mismo ao Bickel consigui un hidrolizado de
protenas bajo en fenilalanina y pudo tratar a varios pacientes con una dieta que
redujo los niveles de fenilalanina en sangre. Esta dieta consigui una mejora del
desarrollo mental y del comportamiento de los pacientes, incluso previniendo
totalmente el dao neurolgico si el tratamiento se iniciaba en el periodo neonatal. A
partir de ese momento se inician los programas de deteccin precoz de la
hiperfenilalaninemia y se extiende su tratamiento mediante dietas limitadas en
rea de Qumica Biolgica 2
Qumica Biolgica Patolgica Tema 11: Fenilcetonuria Ao: 2015
fenilalanina. La cantidad de fenilalanina que cada paciente tolera en su dieta fue el
parmetro utilizado por Gttler en 1980 para determinar la severidad de cada caso y
clasificarlos en distintos fenotipos.
2- SISTEMA DE HIDROXILACION DE FENILALANINA
El trmino de hiperfenilalaninemia se refiere a niveles de fenilalanina en sangre
superiores de forma persistente a 2,5 mg/dl (> 150 mol/L), y que son secundarios a
una alteracin en la reaccin enzimtica de hidroxilacin de fenilalanina.
El sistema de hidroxilacin de fenilalanina (Figura 1) consta de dos enzimas,
fenilalanina hidroxilasa (PAH: EC 1.14.16.1) y dihidropterina reductasa (DHPR: EC
1.6.99.10), y un cofactor no proteico llamado tetrahidrobiopterina (BH4). La BH4 se
sintetiza a partir de guanosin trifosfato (GTP) a travs de tres reacciones enzimticas,
guanosin trifosfato ciclohidrolasa (GTP-CH: EC3.5.4.16), 6-piruvoil
tetrahidrobiopterina sintasa (PTPS: EC 4.6.1.10) y sepiapterina reductasa (SR: EC
1.1.1.153). La PAH cataliza la hidroxilacin de fenilalanina convirtindola en tirosina,
siendo el donador de electrones la BH4 que, a su vez, se oxida convirtindose en
dihidrobiopterina (qBH2). La qBH2 se reduce de nuevo a BH4, a travs de la reaccin
catalizada por la dihidropterina reductasa (DHPR: EC 1.6.99.7). La oxidacin de
qBH2 a BH4, se facilita in vivo con una deshidratasa, carbinolamina deshidratasa
(PCD: EC 4.2.1.96) que hace perder una molcula de agua a un compuesto intermedio
denominado carbinolamina.
a) Si el defecto enzimtico se encuentra en la PAH, se afecta exclusivamente la
hidroxilacin heptica de la fenilalanina, dando lugar a un grupo de enfermedades
conocidas como Hiperfenilalaninemias por deficiencia de PAH en las que la
concentracin de fenilalanina en fluidos y tejidos, especialmente en el sistema
nervioso central, aumenta cuanto menor es la actividad PAH residual heptica. Si la
fenilalaninemia es superior a 600 micromoles/L (>10 mg/dl), se produce dao
cerebral y apoptosis neuronal, que es mayor cuanto mayor es la concentracin de
fenilalanina, condicionando un fenotipo de retraso mental grave.
b) Cuando el defecto enzimtico se encuentra en alguna de las enzimas de los
sistemas de sntesis y/o de reciclaje de BH4, no solo se afecta el sistema de
hidroxilacin de fenilalanina, sino que tambin lo hace el sistema de hidroxilacin de
rea de Qumica Biolgica 3
Qumica Biolgica Patolgica Tema 11: Fenilcetonuria Ao: 2015
tirosina y de triptofano, dando lugar a un defecto de sntesis de LDOPA (3-5
dihidroxifenilalanina) y de 5-hidroxitriptofano (5HT) precursor de la serotonina
(Figs. 1 y 2). Es decir, se afecta la sntesis de neurotransmisores dopaminergicos y
serotoninergicos dando lugar a un grupo de enfermedades conocidas como
hiperfenilalaninemias por defecto del cofactor BH4.
Estas diferencias en su fisiopatologa hacen indispensable el diagnostico diferencial
de la causa de una hiperfenilalaninemia persistente para establecer el tratamiento
adecuado.
El sistema de hidroxilacin de la fenilalanina es la primera etapa en el catabolismo de
este aminocido. La enzima PAH cataliza la parahidroxilacin del aminocido L-
fenilalanina para dar L-tirosina, en presencia de tetrahidrobiopterina (BH4) como
cofactor y de oxgeno molecular como cosustrato (Figura 1).
Figura 1- Sistema de hidroxilacin de la fenilalanina. El ciclo cataltico de la fenilalanina hidroxilasa (PAH) en
presencia de su cofactor natural BH4 se expresan en rojo, las rutas principales de biosntesis de BH4 en azul, y las
de reduccin del cofactor oxidado en verde. Las enzimas implicadas se muestran en recuadros. Se indica
activacin (+) ejercida por la L-Phe y la inhibicin (-) ejercida por la BH4 sobre la etapa limitante en la biosntesis
del cofactor.
rea de Qumica Biolgica 4
Qumica Biolgica Patolgica Tema 11: Fenilcetonuria Ao: 2015
Figura 2. Sntesis de neurotransmisores dopaminrgicos y serotoninrgicos a nivel del sistema nervioso central, a
partir de la oxidacin del triptfano y de la tirosina con tetrahidrobiopterina (BH4).
AADC: decarboxilasa de aminocidos aromticos; COMT: catecolamina metil transferasa; MAO: monoamino
oxidasa; 5HIAA: 5 hidroxi indol actico; HVA: homovanlico. La carbidopa inhibe a la AADC, la selegilina inhibe a
la MAO y la entacapona inhibe a la COMT.
La PAH requiere una adecuada concentracin de BH4 (Km), por lo que su actividad
depende del funcionamiento de las dos enzimas que regeneran el cofactor a partir de
su forma reducida, la 4-carbinolamin-deshidratasa (PCD) y la dihidropterina
reductasa (DHPR), as como de la actividad de las distintas enzimas que componen la
ruta de biosntesis intracelular de BH4. La primera enzima de esta ruta de biosntesis
es la GTP-ciclohidrolasa (GTPCH), que es activada por la Phe e inhibida por su
producto final, la BH4 (Figura 1).
El acmulo de fenilalanina activa otras rutas metablicas alternativas que producen
unos metabolitos indetectables en condiciones normales y que se eliminan por orina
y distintos fluidos corporales. Uno de ellos es el cido fenilactico, que da el olor
caracterstico de los pacientes, y otro el cido fenilpirvico detectado por Flling.
3- ESTRUCTURA, FUNCION Y REGULACION DE LA PAH
La enzima PAH forma parte de la familia de las hidroxilasas de aminocidos
aromticos, que utilizan la BH4 como cofactor y que requieren un tomo de hierro en
su estructura para ser funcionales. Debido a que la PAH humana es difcil de estudiar
por su rpida degradacin post-mortem, la mayora de los estudios de estructura y
rea de Qumica Biolgica 5
Qumica Biolgica Patolgica Tema 11: Fenilcetonuria Ao: 2015
funcin se han realizado en PAH purificada de hgado de rata, con la que guarda una
similitud del 92%. En humanos se expresa fundamentalmente en el hgado, aunque
algunos estudios indican que tambin se expresa minoritariamente en el rin y en
los melanocitos. Distintos estudios han demostrado la existencia de tres dominios
funcionales en la protena (Figura 3):
1) Dominio regulador (residuos 1-110 desde el extremo amino-terminal): dada la
importancia fisiolgica del sistema de hidroxilacin de la Phe, la enzima est
fuertemente regulada y tiene como activador alostrico los niveles de Phe y como
inhibidor los niveles de BH4, dependiendo adems de la fosforilacin-defosforilacin
del residuo Ser16.
2) Dominio cataltico (residuos 111-410): en l se halla el centro activo de la enzima,
con el tomo de hierro y los sitios de unin del sustrato y el cofactor.
3) Dominio de oligomerizacin (residuos 411-452): para su actividad, la enzima debe
ensamblarse en forma de dmero y sobre todo en forma de tetrmero, que tiene una
actividad cinco veces superior. La formacin de estos tetrmeros se ve favorecida en
presencia de BH4.
rea de Qumica Biolgica 6
Qumica Biolgica Patolgica Tema 11: Fenilcetonuria Ao: 2015
Figura 3- Organizacin estructural del gen y la protena PAH. A) Estructura del gen PAH; B) Estructura primaria
de la protena PAH, donde se localizan los dominios funcionales, el tomo de hierro y el sitio de fosforilacin
(Ser16); C) y D) Modelos tridimensionales propuestos para la PAH en forma monomrica (C) y tetramrica (D).
Tomado de: Pey, 2004; Erlandsen y Stevens, 1999; Konecki y Lichter-Konecki, 2001; Scriver y Kaufman, 2001.
4- GEN PAH. EXPRESION DE MUTACIONES. RELACION GENOTIPO/
FENOTIPO
El gen PAH se localiza en humanos en la regin q22-q24.1 del cromosoma 12. Tiene
una longitud total de 171 kb y contiene 13 exones (Figura 3). Su transcripcin est
regulada por mltiples factores como los glucocorticoides, el AMPc, hormonas y el
HNF-1 mediante secuencias especficas presentes en la regin del promotor. Hasta el
momento se han identificado a nivel mundial 532 mutaciones asociadas a PKU,
aunque continuamente se hallan nuevas variantes allicas. La mayora son
mutaciones puntuales de cambio de aminocido (missense), aunque tambin las hay
de tipo unin intrn-exn (splice), sin sentido o stop (nonsense) y silentes, as como
mayores mutaciones como deleciones o inserciones (http://www.pahdb.mcgill.ca).
rea de Qumica Biolgica 7
Qumica Biolgica Patolgica Tema 11: Fenilcetonuria Ao: 2015
Se han identificado mutaciones en todos los exones, pero la mayora se localiza en el
exn 7, probablemente por tratarse de una regin altamente conservada del dominio
cataltico de la enzima. Existe un porcentaje entre el 1 y el 10% de alelos PKU que no
han podido ser caracterizados y que afectan a la regin del promotor, a seales de
poliadenilacin, a regiones intrnicas o son deleciones no detectables por las tcnicas
habituales de estudio de mutaciones. El mecanismo ms frecuente a travs del cual
las mutaciones del gen PAH ejercen sus efectos patognicos es la inestabilidad
conformacional de la protena, lo que la confiere menor solubilidad, menor
estabilidad trmica y mayor predisposicin a la degradacin proteoltica. Los estudios
de expresin in vitro han permitido en muchos casos correlacionar el defecto
funcional de las mutaciones con el fenotipo de los pacientes. Las mutaciones que
confieren una actividad residual alta in vitro estn generalmente asociadas a los
fenotipos ms suaves. La presencia en homocigosis de mutaciones con actividad
residual in vitro nula o muy reducida se correlaciona con los fenotipos ms graves de
la enfermedad. Sin embargo, existen mutaciones para las que no se observa una
relacin entre la actividad residual observada in vitro y el fenotipo del paciente.
Tambin hay que tener en cuenta que la mayora de los pacientes son heterocigotos
para distintas mutaciones, y que el fenotipo clnico y bioqumico final depende de la
interaccin entre las protenas resultantes de ambos alelos. Adems se han descrito
pacientes, incluso hermanos, con un mismo genotipo pero diferentes fenotipos
clnicos. Esta inconsistencia genotipo-fenotipo impide, hasta ahora, predecir con total
fiabilidad la gravedad del fenotipo en los pacientes PKU a partir del genotipo.
5- MANIFESTACIONES CLINICAS DE LA DEFICIENCIA DE
FENILALANINA HIDROXILASA
5.1.- Clnica de la Fenilcetonuria
La manifestacin clnica ms importante de la PKU es una alteracin en el desarrollo
cognitivo que puede llegar a ser extremadamente intensa, con automutilaciones y
trastornos psiquitricos semejantes a la esquizofrenia. Los mecanismos a travs de
los cuales el incremento en los niveles de fenilalanina causan la muerte neuronal no
se conocen con exactitud, aunque existen evidencias en animales que sugieren que se
puede producir una alteracin en la mielinizacin y en la diferenciacin celular, as
como una inhibicin en el trasporte proteico a travs de la barrera hematoenceflica
rea de Qumica Biolgica 8
Qumica Biolgica Patolgica Tema 11: Fenilcetonuria Ao: 2015
que ralentizara la sntesis de protenas y neurotrasmisores a nivel del sistema
nervioso central.
El dao producido por la hiperfenilalaninemia no se manifiesta de forma aguda, sino
que es necesario un acmulo prolongado o reiterativo para que se puedan observar
las alteraciones neurolgicas. Por este motivo los pacientes PKU son clnicamente
normales hasta el final de la lactancia, en la que se comienza a apreciar su retraso
psicomotor. Asimismo, en pacientes que abandonan el tratamiento, no se producen
descompensaciones agudas y los sntomas neurolgicos no se expresan hasta meses o
aos despus. En la resonancia magntica cerebral (RMC) slo se aprecian las
lesiones tpicas de hiperintensidad en sustancia blanca periventricular en T2 cuando
los niveles de fenilalanina se han mantenido por encima de 660 mol/L (11 mg/dl) al
menos durante 6 meses.
El grado de afectacin del sistema nervioso central es muy variable y depende de los
niveles de fenilalanina que tenga el paciente y que son el resultado del grado de
actividad residual de PAH, del tipo de dieta que siga el paciente, de la absorcin de
fenilalanina a nivel intestinal, del grado en el que cruza la barrera hematoenceflica,
de la presencia de procesos intercurrentes, etc. Los resultados son tambin
heterogneos ya que no se pueden olvidar todos los dems factores genticos y
ambientales implicados en el desarrollo cognitivo de una persona.
Los niveles de fenilalanina a partir de los cuales hay riesgo de dao neurolgico han
sido y son motivo de controversia. Muchos grupos utilizan niveles de 600 mol/L (10
mg/dl) como corte por encima del cual se debe tratar a los pacientes, pero se han
descrito alteraciones cognitivas menores tales como hiperactividad o dificultades en
el aprendizaje en pacientes con valores de fenilalanina inferiores. Actualmente se
tiende a intentar mantener los niveles de fenilalanina lo ms cerca posible de la
normalidad (<120 mol/L), sobre todo durante la infancia temprana. Posteriormente
se admiten como aceptables niveles ms altos con el fin de permitir cierta relajacin
de la dieta. Cada pas ha desarrollado su propio protocolo para el seguimiento de la
fenilcetonuria. Como se puede observar en la Tabla 2, no hay consenso en cuanto a
los valores mximos de fenilalanina que se consideran adecuados a cada edad, y estos
pueden ser muy variables.
rea de Qumica Biolgica 9
Qumica Biolgica Patolgica Tema 11: Fenilcetonuria Ao: 2015
Niveles de Fenilalanina
Inicio tratamiento >360 umol/L (>6mg/dl)
0-6 aos <360 umol/L (<6mg/dl)
6-9 aos <540 umol/L (<9mg/dl)
9-12 aos <630 umol/L (<10,5mg/dl)
> 12 aos <630 umol/L (<10,5mg/dl)
Embarazo <240 umol/L (<4mg/dl)
Tabla 2: Niveles plasmticos de fenilalanina utilizados como referencia para tomar la decisin de tratar y
posteriormente mantener a lo largo de la vida segn las indicaciones de los protocolos utilizados en distintos
pases, se muestra los valores consensuados en Espaa.
En nuestro pas, el Ministerio de Salud de la Nacin (MSN), recomienda que un buen
control metablico implica mantener concentraciones plasmticas entre 2 y 6mg/dl
(120-360 uM/L) en los primeros aos de vida, en los nios mayores hasta 8mg/dl
(485 uM/L) y en adultos hasta 10mg/dl (600 uM/L).
Se ha establecido que todo nio que presente concentraciones de Fenilalanina por
encima de 10mg/dl, tirosina normal o disminuida y que est recibiendo alimentacin
normal, debe iniciar dieta restringida en Fenilalanina. Nios con concentraciones
entre 6 y 10mg/dl y que persisten luego de 1 mes de dieta normal, tambin requieren
de restriccin dietaria.
La edad a la que se produce el acmulo de fenilalanina parece tener tambin una
importancia crucial para determinar el grado de afectacin neurolgica. Los primeros
meses de vida el cerebro humano completa su proceso de crecimiento y
diferenciacin, y es en este periodo en el que la hiperfenilalninemia produce mayores
trastornos, produciendo retrasos cognitivos que pueden llegar a ser muy severos. En
nios mayores y adolescentes, dejar el tratamiento los predispone a sufrir dificultades
en el aprendizaje. En cambio, un paciente adulto puede abandonar la dieta sin sufrir
sntomas o reducindose stos a falta de concentracin o irritabilidad, aunque
ocasionalmente se han descrito cambios importantes del comportamiento y
paranoias. Para evitar los sntomas se recomienda mantener el tratamiento durante
toda la vida.
Asimismo, la capacidad de recuperacin del dao cerebral depende de la edad a la
que se instaure el tratamiento, consiguiendo mayores beneficios cuanto ms precoz
sea. Para evitar completamente la afectacin neurolgica es necesario comenzar el
tratamiento durante el periodo neonatal. Cuanto el diagnstico es tardo se observa
rea de Qumica Biolgica 10
Qumica Biolgica Patolgica Tema 11: Fenilcetonuria Ao: 2015
cierta mejora de la capacidad intelectual, el comportamiento y la sociabilidad si se
trata a estos pacientes, pero en estos casos siempre se mantiene alguna limitacin.
Actualmente se tiende a iniciar el tratamiento incluso en pacientes de edades
avanzadas. Las lesiones observadas en la resonancia magntica desaparecen si se
mantiene el tratamiento durante al menos un ao, aunque puedan persistir las
secuelas neurolgicas.
Las alteraciones cutneas y el olor a ratones se presentan cuando los niveles de
fenilalanina en sangre son superiores a 900 mol/L (15mg/dl), y son rpidamente
reversibles al disminuir esas cifras.
5.2.- Hiperfenilalaninemia Benigna (Hyperphenylalaninemia o HPA, Mild
Hyperphenylalaninemia o MHP)
Antes de disponer del diagnstico gentico se describi esta enfermedad como una
entidad diferenciada de la fenilcetonuria. Se trata de pacientes que tienen niveles de
fenilalanina en sangre ligeramente elevados por encima de la normalidad (entre 120 y
600 mol/L), a pesar de lo cual su desarrollo psicomotor es normal y no requieren
tratamiento diettico. Posteriormente se ha visto que en realidad se trata de pacientes
con mutaciones en el gen PAH, pero cuyas enzimas resultantes mantienen una alta
actividad residual. Esto permite un catabolismo de la fenilalanina cercano a la
normalidad, impidiendo el acmulo excesivo de fenilalanina y su neurotoxicidad. En
muchas clasificaciones sigue apareciendo por tradicin esta entidad como una
enfermedad diferenciada, pero ya que se trata de una deficiencia en la funcin de la
PAH, nosotros la denominaremos fenilcetonuria con fenotipo benigno.
A pesar de su aparente benignidad, se ha descrito en estos pacientes alteraciones
menores del comportamiento tales como hiperactividad con mayor frecuencia que en
la poblacin normal. Asimismo, la falta de diagnstico de estos casos puede dar lugar
a sndromes de hiperfenilalaninemia materna en los hijos de las mujeres afectadas.
Tambin es necesario realizar el diagnstico de estos nios para poder dar a sus
familias un consejo gentico adecuado, ya que pueden ser portadores de mutaciones
ms severas y tener en su descendencia o entre sus familiares casos de fenilcetonuria
clsica.
rea de Qumica Biolgica 11
Qumica Biolgica Patolgica Tema 11: Fenilcetonuria Ao: 2015
5.3.- Sndrome de Hiperfenilalaninemia Materna
Unos niveles elevados de fenilalanina en la sangre de la madre durante el desarrollo
intrauterino de sus hijos no slo tienen efectos devastadores a nivel cerebral, sino que
pueden dar lugar a malformaciones cardiacas y renales. Tambin son frecuentes en
estas mujeres los abortos de repeticin. La homeostasis de la fenilalanina hasta la
semana 27 de gestacin depende exclusivamente de la capacidad materna para
metabolizarla, y por lo tanto son los hijos de madre PKU los que pueden verse
afectados por este sndrome, independientemente de su propia capacidad funcional.
Para evitar estas importantes complicaciones las madres deben seguir, desde el
momento de la concepcin, un estricto tratamiento que evite niveles superiores a 180
mol/L (3mg/dl). Se utilizan estos niveles porque se supone que el feto puede llegar a
doblar los niveles maternos.
El Sndrome de Hiperfenilalaninemia Materna debe entrar en el diagnstico
diferencial de todo paciente con retraso mental de cualquier grado y/ microcefalia.
Es importante tener en cuenta que para diagnosticarlo la nica prueba til es la
determinacin de los niveles de fenilalanina en la madre, y no en el nio.
6- DIAGNOSTICO DIFERENCIAL DE LA HIPERFENILALANINEMIA.
DETECCION NEONATAL
La fenilcetonuria era una de las causas ms frecuentes de retraso mental. En el
momento en que se encontr un tratamiento para prevenir las alteraciones cognitivas
si se iniciaba de forma precoz exista una razn para buscar de forma masiva
pacientes PKU durante el periodo neonatal. Con este fin Guthrie y Susi desarrollaron
en 1963 un mtodo que permita la determinacin de fenilalanina con muestras de
sangre del taln de recin nacidos. Los programas de deteccin precoz de esta
enfermedad junto con los de hipotiroidismo congnito, son los ms extendidos en
pases desarrollados. El mtodo utilizado es variable, y se utilizan ensayos
microbiolgicos, cromatogrficos, colorimtricos, fluoromtricos, etc.
En nuestro pas, en los hospitales pblicos se utiliza un kit cubano de SUMA:
UMTEST PKU. Ver folleto adjunto.
La fenilalanina se acumula en sangre y tejidos cuando existe una disfuncin en su
sistema de hidroxilacin. Como ya se ha comentado anteriormente, la gran mayora
de los casos se deben a deficiencias de la enzima PAH, pero un pequeo porcentaje de
rea de Qumica Biolgica 12
Qumica Biolgica Patolgica Tema 11: Fenilcetonuria Ao: 2015
pacientes sufren hiperfenilalaninemia como consecuencia de alteraciones en la
sntesis o regeneracin de su cofactor, la BH4. La tetrahidrobiopterina acta no slo
como donante de electrones para la PAH, sino tambin para la tirosina hidroxilasa, la
triptfano hidroxilasa y otra serie de enzimas (Figura 4), y su deficiencia afecta
directamente la sntesis de neurotrasmisores dopaminrgicos y serotoninrgicos .
Los pacientes con alteraciones en la sntesis o reciclaje de la BH4 tienen una
afectacin neurolgica ms severa que los pacientes fenilcetonricos, con distonas,
alteraciones de motilidad ocular, hipoglucemias y trastornos del control de
temperatura desde el periodo neonatal, y no responden clnicamente aunque s
disminuyen los niveles de fenilalnina en sangre al tratamiento diettico habitual de la
fenilcetonuria.
Histricamente se denomin a estos procesos en conjunto Hiperfenilalaninemia
Maligna. Su tratamiento consiste en aportes exgenos de BH4, L-Dopa y 5-OH-
Triptfano pero su evolucin no es tan satisfactoria como el de la fenilcetonuria. Los
protocolos de diagnstico diferencial de la hiperfenilalaninemia deben ir
encaminados a la diferenciacin de cada defecto enzimtico para poder instaurar un
tratamiento acertado a cada caso de forma precoz, poder predecir la evolucin de los
pacientes con mayor precisin y poder ofrecer un consejo gentico adecuado.
Figura 4: Reacciones enzimticas mediadas por BH4: 1) Fenilalanina hidroxilasa; 2) Tirosina hidroxilasa; 3)
Triptfano hidroxilasa; 4) Oxido ntrico cintaza; 5) Gliceril-eter-monooxigenasa. BH4: tetrahidrobiopterina.
q-BH2: quinonoil dihidrobiopterina (tomado de Blau et al, 2001).
rea de Qumica Biolgica 13
Qumica Biolgica Patolgica Tema 11: Fenilcetonuria Ao: 2015
Figura 5a: Diagnstico diferencial de la hiperfenilalaninemia. En recuadro se representan las sustancias medidas
para realizar dicho diagnstico: fenilalanina y tirosina en plasma, actividad DHPR en sangre, cidos orgnicos
derivados del exceso de fenilalanina en orina, as como las pterinas. Estas ltimas son subproductos de la sntesis
de BH4 y se dividen en neopterinas (procedentes de la degradacin de la 7,8-DHNP) y biopterinas (procedentes
de la degradacin de sepiapterina, BH4 y BH2). Los pacientes con deficiencia de la PCD presentan un aumento de
la excrecin de primapterina (procedentes de la degradacin de la HO-BH4)
Figura 5b: Estructuras qumicas de los productos excretados por orina
rea de Qumica Biolgica 14
Qumica Biolgica Patolgica Tema 11: Fenilcetonuria Ao: 2015
7- TRATAMIENTO DE LA FENILCETONURIA
El objetivo del tratamiento de la fenilcetonuria es mantener los niveles de
fenilalanina plasmticos por debajo de unos niveles considerados peligrosos para el
desarrollo y funcin cognitiva del paciente (ver tabla 2). En 1993 el Medical Research
Council Working Party on Phenylketonuria de Inglaterra y la Asociacin Espaola
para el Estudio de los Errores Congnitos del Metabolismo (AECOM), establecen que
todo paciente con unos valores en sangre superiores a 360 mol/L (6 mg/dl) debe ser
tratado. Como ya hemos comentado con anterioridad, los niveles tomados como
referencia en los distintos pases para tomar la decisin de tratar o no pueden diferir.
En Espaa, los pacientes con niveles mantenidos entre 120 y 360 mol/L (2-6 mg/dl)
se considera que tienen un fenotipo benigno y que no requieren tratamiento aunque
s deben ser monitorizados para valorar la aparicin de alteraciones neurolgicas
menores o evitar el sndrome de hiperfenilalaninemia materna.
El tratamiento habitual de la fenilcetonuria consiste en una limitacin en la ingesta
de fenilalanina. Ya que la fenilalanina es un aminocido esencial, la restriccin de su
ingesta reduce la cantidad que llega al sistema catablico donde acta la PAH, pero es
indispensable abastecer adecuadamente al organismo para la biosntesis de protenas
endgenas. Para que el tratamiento tenga xito debe iniciarse en los primeros meses
de la vida y mantenerse durante el desarrollo hasta la madurez, aunque actualmente
se recomienda mantenerlo durante toda la vida. La dieta, los niveles de fenilalanina, y
el desarrollo psicomotor y general de cada paciente debe monitorizarse de forma
individual y prolongada, ya que las necesidades teraputicas se deben adaptar a cada
etapa evolutiva.
La cantidad de fenilalanina que cada paciente puede tolerar en su dieta depende de la
actividad residual de PAH que tenga. En 1980 Gttler estableci unos fenotipos
segn la tolerancia a fenilalanina que se han mantenido con escasas variaciones hasta
la actualidad. Segn esta clasificacin, los pacientes fenilcetonricos que requieren
tratamiento pueden tener un fenotipo suave, moderado y severo (o grave). En la
Tabla 3 se especifican los distintos fenotipos, con su tolerancia, y la frecuencia de
cada uno de ellos en la poblacin espaola. Esta clasificacin utiliza la tolerancia a
fenilalanina a los 5 aos de edad, ya que los requerimientos de fenilalanina varan
segn las necesidades para el crecimiento y por lo tanto disminuyen
rea de Qumica Biolgica 15
Qumica Biolgica Patolgica Tema 11: Fenilcetonuria Ao: 2015
progresivamente. Esto supone que hasta que el paciente no alcanza los 5 aos, no
puede ser catalogado adecuadamente.
Tabla 3- Clasificacin de los pacientes con deficiencia de PAH segn la tolerancia a fenilalanina a los 5 aos de
edad, junto con la frecuencia de estos fenotipos en la poblacin espaola.
La fenilalanina forma parte de todas las protenas de origen natural, de las cuales
supone aproximadamente un 5%. La mayora de los grupos recomienda restringir
todas las protenas naturales en mayor o menor grado, segn la tolerancia de cada
paciente
La restriccin en la ingesta de protenas naturales para evitar un incremento en los
niveles de fenilalanina conlleva una restriccin en la ingesta de otros aminocidos,
vitaminas y oligoelementos. Para evitar la aparicin de patologa carencial secundaria
es necesario suplementar la dieta de los pacientes con productos industriales que
contengan estos nutrientes. Con este fin se han desarrollado mltiples frmulas de
aminocidos exentas de fenilalanina y enriquecidas en tirosina que cumplen todos los
requisitos
8- SEGUIMIENTO CLINICO Y BIOQUIMICO DE LOS PACIENTES
FENILCETONURICOS
Todos los pacientes deben ser evaluados clnica y bioqumicamente de forma
peridica para adaptar la dieta a sus niveles de fenilalanina, permitir un adecuado
crecimiento y desarrollo psicomotor y evitar la aparicin de patologa carencial. Es
importante realizar peridicamente una evaluacin neurolgica y psicolgica
completa y valorar la realizacin de pruebas de imagen y de neurofisiologa.
El nmero de controles clnicos y analticos debe hacerse de forma individualizada,
dependiendo de la evolucin de cada paciente. En los primeros aos de la vida y en
mujeres embarazadas se debe realizar un seguimiento exhaustivo, mientras que en
fenotipos suaves y en adultos puede no ser tan estricto. En Espaa se siguen las
rea de Qumica Biolgica 16
Qumica Biolgica Patolgica Tema 11: Fenilcetonuria Ao: 2015
directrices del Protocolo de Diagnstico, Tratamiento y Seguimiento de las
Hiperfenilalaninemias propuesto por la AECOM y que se expone de forma resumida
en la Tabla 4.
Tabla 4.- Controles clnicos y bioqumicos recomendados por la AECOM (Espaa) para el seguimiento de
pacientes PKU. Los controles pueden verse modificados segn la evolucin de cada paciente.
9- RESPUESTA A TETRAHIDROBIOPTERINA (BH4) EN PACIENTES
PKU
La tetrahidrobiopterina es un cofactor perteneciente al grupo de las pterinas,
estructuralmente est constituida por una cadena de pteridina con las sustituciones
2-amino, 4 oxo y 5,6,7,8 tetrahidro. En humanos la BH4 se encuentra en todos los
tejidos y fluidos biolgicos y puede ser tanto reciclada como sintetizada de novo a
partir de GTP, (Figura 1). La BH4 acta como cofactor de la oxido ntrico sintasa y de
la gliceril eter monooxigenasa aunque la funcin mejor establecida y ms estudiada
para la BH4 en humanos es su actuacin como cofactor de tres enzimas implicadas en
la hidroxilacin de aminocidos aromticos; la fenilalanina-4-hidroxilasa, la tirosina-
3- hidroxilasa y la triptfano-5-hidroxilasa, estas enzimas son claves en la biosntesis
de aminas bigenas.
En las hiperfenilalalinemias para distinguir las deficiencias producidas por defectos
en la sntesis o regeneracin del cofactor BH4 (Figura 5) de las debidas a defectos en
el gen de la PAH se realiza un test de sobrecarga oral con BH4, aunque para un
diagnstico exacto es necesario adems el anlisis de los niveles de pterinas en la
orina y la actividad dihidropterina reductasa en eritrocitos. En general, los pacientes
con alteraciones en las enzimas implicadas en la sntesis y regeneracin de la BH4
presentan una normalizacin de los niveles de L-Phe plasmtica muy rpida (4-8
horas despus de la sobrecarga) tras la ingesta oral de dosis moderadas de este
cofactor (Figura 6).
rea de Qumica Biolgica 17
Qumica Biolgica Patolgica Tema 11: Fenilcetonuria Ao: 2015
Figura 6: Niveles de fenilalanina plasmtica antes y despus de una sobrecarga en un paciente con deficiencia en
PAH, uno con deficiencia en PTPS y un caso de deficiencia en DHPR. Considerando niveles plasmticos en rango
teraputico (Scriver and Kaufman 2001) normalmente por debajo de 7 mg/dl (400 M).
PAH: Fenilalanina hidroxilasa;
DHPR: dihidropteridina reductasa;
PTPS: 6-piruvoil-5,6,7,8-tetrahidropterina sintasa
La tetrahidrobiopterina acta como cofactor de la enzima PAH induciendo cambios
conformacionales en su centro activo y regulador. En el ao 1983, los laboratorios
Shircks, en Suiza, comenzaron a producir una tetrahidrobiopterina sinttica (6-metil-
tetrahidrobiopterina), con capacidad para interactuar con el centro activo pero sin
inhibir el centro regulador debido a las diferencias en su cadena lateral. Este
producto estaba pensado para el tratamiento de los pacientes con deficiencia del
cofactor, y era el utilizado en las sobrecargas orales de BH4 en neonatos.
Histricamente, la realizacin de sobrecargas orales de BH4 estaba restringido a
aquellos casos en los que era necesario hacer un diagnstico diferencial entre las
deficiencias de PAH y los defectos en la sntesis del cofactor. Los pacientes con
defectos en la sntesis de BH4 tienen una rpida normalizacin de los niveles de
fenilalanina plasmtica tras la ingesta oral de dosis moderadas de BH4
(aproximadamente 4 horas despus de la administracin de 2,5-10 mg/Kg). Sin
embargo, ante posibles errores en el diagnstico de pacientes con deficiencia de
DHPR y coincidiendo con una mejora en la comercializacin del producto, se
recomend a partir de 1993 la administracin de dosis de superiores de BH4 (hasta
20 mg/kg) en los protocolos diagnsticos.
La heterogenicidad en la clasificacin de los pacientes y en el tipo de protocolo
utilizado para valorar la respuesta a BH4 (dosis, edad, tiempo de observacin, dieta
rea de Qumica Biolgica 18
Qumica Biolgica Patolgica Tema 11: Fenilcetonuria Ao: 2015
concomitante, grado de respuesta considerado positivo, etc) hace difcil establecer
comparaciones entre los estudios disponibles.
En algunos casos el tratamiento exclusivo con BH4 permite seguir una dieta
completamente normal. Salvo un caso de irritacin local tras su administracin
sublingual, no se han descrito efectos secundarios. Tambin se ha postulado su
utilidad para evitar el sndrome de hiperfenilalaninemia materna, pero la falta de
experiencia obliga a ser cautos en cuanto a los posibles efectos teratognicos de la
BH4. En el nico caso descrito de su utilizacin en una mujer embarazada, se ha
utilizado con xito.
En los ltimos aos, la implicacin de la tetrahidrobiopterina en el metabolismo del
xido ntrico ha hecho que se proponga como tratamiento en campos tan dispares
como la sepsis, las miocardiopatas y las alteraciones del endotelio vascular,
enfermedades neurodegenerativas como el Parkinson o el Alzheimer, enfermedades
genitourinarias como la criptorquidia, etc. La tetrahidrobiopterina sinttica utilizada
comercialmente es el dihidroclorato de sapropterina.
10- ALGORITMO
Un algoritmo aconsejable para el diagnstico diferencial es el de la figura 7 y tabla 5.
rea de Qumica Biolgica 19
Qumica Biolgica Patolgica Tema 11: Fenilcetonuria Ao: 2015
Figura 7: Algoritmo diagnstico diferencial entre la deficiencia de PKU y BH4 (modificada de Opladen y col.). Las
manchas de sangre secas y muestras de orina puede ser usadas para la determinacin diferencial basados en los
niveles de neopterina (Neo), biopterina (Bio), y primapterina (Pri) y la actividad de la enzima Dihidropteridina
reductasa (DHPR) en MSP.
En la Deficiencia de GTP ciclohidrolasa (GTPCH): Hay niveles bajos o no detectables de Neopterina y
Biopterina.
En la deficiencia de 6- piruvoil tetrahidropterina sintasa (PTPS): Hay altos niveles de Neopterina y bajos o no
detectables de Biopterina.
En la Deficiencia de dihidropteridina reductasa (DHPR): Hay niveles normal de neopterina y normal o elevado
de biopterina y ausencia de actividad de DHPR.
En la deficiencia de 4carbinolamina tetrahidrobipterina deshidratasa (PCD): hay niveles elevados de
neopterina y primapterina y bajo-normal de biopterina.
rea de Qumica Biolgica 20
Qumica Biolgica Patolgica Tema 11: Fenilcetonuria Ao: 2015
Tabla 5: Parmetros bioqumicos para el diagnstico diferencial de la deficiencia PKU
y BH4
Neopterina Biopterina Primapterina Actividad DHPR Phe
PKU n- n- n n
GTPCH n n a
PTPS n n
PCD -n n
DHPR n n- a n
El programa de fortalecimiento de la deteccin precoz de enfermedades congnitas,
del ministerio de salud de la nacin no presenta algoritmo para la pesquisa de
fenilcetonuria.
Pero las recomendaciones que resalta son:
rea de Qumica Biolgica 21
Qumica Biolgica Patolgica Tema 11: Fenilcetonuria Ao: 2015
BIBLIOGRAFIA:
- Charles R. Scriver: The PAH gene, phenylketonuria, and a paradigm shift. 2007.
Human Mutation 28(9), 831-845.
- Nenad Blau, Julia B. Hennermann, Ulrich Langenbeck, Uta Lichter-Konecki
(2011) Diagnosis, classification, and genetics of phenylketonuria and tetrahydrobiopterin
(BH4) deficiencies. Molecular Genetics and Metabolism 104 S2S9
- Martnez-Pardo M; Blanger-Quintana A; Garca Muoz MJ; Desviat L; Prez
B; Ugarte M. FENILCETONURIA. Protocolo de diagnstico, tratamiento y seguimiento
de las hiperfenilalaninemias. AECOM.
- Charles R. Scriver. 2008. Garrods Croonian Lectures (1908) and the charter Inborn
Errors of Metabolism: Albinism, alkaptonuria, cystinuria, and pentosuria at age 100 in
2008. J Inherit Metab Dis 31: 580598
- Charles R. Scriver, Paula J. Waters. 1999. Monogenic traits are not simple: lessons
from phenylketonuria. TIG 15, (7): 267-272.
- PESQUISA NEONATAL ARGENTINA. Programa Nacional de Fortalecimiento de la
Deteccin Precoz de Enfermedades Congnitas: Manual de procedimientos. Ministerio de
Salud. Presidencia de la Nacin. 2011. Pginas: 1-138.
rea de Qumica Biolgica 22
Vous aimerez peut-être aussi
- Atencion de Personas Con QuemaduraDocument18 pagesAtencion de Personas Con QuemaduraBelle AmorePas encore d'évaluation
- SoapieDocument22 pagesSoapieBelle Amore80% (5)
- Pae IctericiaDocument19 pagesPae IctericiaBelle AmorePas encore d'évaluation
- Cuadros e Interpretacion de Uso de Videojuegos en Adolescentes San JuanDocument88 pagesCuadros e Interpretacion de Uso de Videojuegos en Adolescentes San JuanBelle AmorePas encore d'évaluation
- Estrategias Sanitaria de Prevención de Accidentes de Transito OriginalDocument11 pagesEstrategias Sanitaria de Prevención de Accidentes de Transito OriginalBelle AmorePas encore d'évaluation
- Hipopituitarismo Congénito: Reporte de Caso y Revisión de La LiteraturaDocument9 pagesHipopituitarismo Congénito: Reporte de Caso y Revisión de La LiteraturaVane LévanoPas encore d'évaluation
- Genomica Nutricional y Sus Prespectivas PDFDocument32 pagesGenomica Nutricional y Sus Prespectivas PDFCynthia RodriguezPas encore d'évaluation
- Concurso Microbiología GBS. Mención de Honor 2006 (1) - Meritxell Mas.Document18 pagesConcurso Microbiología GBS. Mención de Honor 2006 (1) - Meritxell Mas.concursogbsPas encore d'évaluation
- GametogénesisDocument4 pagesGametogénesisAndrea Mesa Arrieta100% (1)
- GUIA DE NaturalesDocument2 pagesGUIA DE NaturalesCristina RipollPas encore d'évaluation
- APB01 TareaDocument4 pagesAPB01 TareaRamón75% (4)
- Clase 2 Codigo GeneticoDocument16 pagesClase 2 Codigo GeneticoCarlos BareiroPas encore d'évaluation
- Preguntas Del IbmDocument5 pagesPreguntas Del IbmHeber FallenPas encore d'évaluation
- Diagnóstico Microbiológico Texto Y Atlas Color KonemanDocument59 pagesDiagnóstico Microbiológico Texto Y Atlas Color KonemanJade A Avilez EscamillaPas encore d'évaluation
- Carpeta Con Gancho Natu 5 BonDocument26 pagesCarpeta Con Gancho Natu 5 Bonfeder tuiran garciaPas encore d'évaluation
- Hospedero o Incidental PDFDocument1 pageHospedero o Incidental PDFCoasaca Céspedes Javier JesúsPas encore d'évaluation
- 0000001566cnt 2019 09 - Guia para La Utilizacion de Pruebas Rapidas de Sifilis PDFDocument19 pages0000001566cnt 2019 09 - Guia para La Utilizacion de Pruebas Rapidas de Sifilis PDFSebastian Ramirez Useche100% (1)
- Vía AereaDocument6 pagesVía AereaKarla ChpPas encore d'évaluation
- Sesión de Aprendizaje 1Document4 pagesSesión de Aprendizaje 1Patricia FloresPas encore d'évaluation
- Fisiologia Cultivos Fase 1Document5 pagesFisiologia Cultivos Fase 1Andres Zuñiga BambaguePas encore d'évaluation
- Funciones RenalesDocument2 pagesFunciones RenalesIsaac PillapaPas encore d'évaluation
- Genética de PoblacionesDocument9 pagesGenética de PoblacionesAGUDELO & GUTIÉRREZ INGENIERÍAPas encore d'évaluation
- Lesiones Benignas de Glándulas SalivalesDocument12 pagesLesiones Benignas de Glándulas SalivalesEduardo VenturaPas encore d'évaluation
- Investigación FisiologíaDocument3 pagesInvestigación FisiologíaLuis Humberto Valdivieso NeriPas encore d'évaluation
- Alineamiento de en ParesDocument47 pagesAlineamiento de en ParesMANUEL CHEPEPas encore d'évaluation
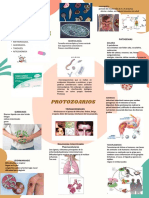
- PROTOZOARIOS InfoDocument1 pagePROTOZOARIOS InfoEsmeralda Miguel carreraPas encore d'évaluation
- Tarea #1Document13 pagesTarea #1tokio JaponPas encore d'évaluation
- Paracitologia 2Document6 pagesParacitologia 2Luz AguilarPas encore d'évaluation
- Reproducción Continuación de La Unidad IIDocument24 pagesReproducción Continuación de La Unidad IIherrera0210Pas encore d'évaluation
- Informe ConejosDocument12 pagesInforme ConejosmichellePas encore d'évaluation
- Efecto Prebiótico de Sacáridos Comerciales Sobre Bacterias Probióticas Aisladas de Productos Comerciales.Document10 pagesEfecto Prebiótico de Sacáridos Comerciales Sobre Bacterias Probióticas Aisladas de Productos Comerciales.JUDITHPas encore d'évaluation
- Seminario "Introducción A La Osteología Humana" - Dictado Por Las Dras. Carolina Barboza y Carolina PíccoliDocument12 pagesSeminario "Introducción A La Osteología Humana" - Dictado Por Las Dras. Carolina Barboza y Carolina PíccolibioantropologiaPas encore d'évaluation
- LocomotorDocument6 pagesLocomotormayerli pedrazaPas encore d'évaluation
- Propiedades EmergentesDocument8 pagesPropiedades EmergentesChristian ThiagoPas encore d'évaluation
- Unidad 3 Proteinas HemicasDocument11 pagesUnidad 3 Proteinas HemicasErica Monterrey MoraPas encore d'évaluation