Académique Documents
Professionnel Documents
Culture Documents
QA PROB-2DOCUAT2014 Parte1 ConRespuestasVerificadas
Transféré par
Anonymous qKeDFDCopyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
QA PROB-2DOCUAT2014 Parte1 ConRespuestasVerificadas
Transféré par
Anonymous qKeDFDDroits d'auteur :
Formats disponibles
Qumica Analtica Serie de Problemas
QUIMICA ANALITICA 2c2014 GUIA DE PROBLEMAS
SERIE 1
Objetivos:
1- Manejar las expresiones usadas en la expresin de resultados analticos en
las unidades comnmente usadas.
2- Expresin de balances de masa y carga.
3- Familiarizarse con el uso de factores de conversin gravimtricos.
Con los conceptos cubiertos en esta seccin se espera un manejo gil de la
conversin de datos y resultados en trminos de diversas unidades de
concentracin y la expresin de una composicin en trminos de una sustancia
tipo. Tambin se debera ser capaz de escribir balances masa y carga en
cualquier sistema qumico donde se conozca las especies presentes.
SOLUCIONES. PARMETROS ANALTICOS
a) Expresiones de concentracin. Diluciones.
1- Definir y escribir las unidades (cuando corresponda):
a) Unidad de masa.
b) Unidad de cantidad de materia.
c) Densidad.
d) Concentracin.
2- Definir y escribir las unidades:
a) porcentaje en peso (%p/p)
b) porcentaje peso/volumen (% p/v)
c) "partes por milln" (ppm)
d) molaridad.
3- Encontrar los factores para convertir:
a) % p/p en % p/v
b) % p/p en molaridad (sc = 1 g/cm3).
c) molaridad en ppm
4- Calcular las concentraciones finales si 10 mL de una solucin de HCl 5 M se
llevan a:
a) 20 mL. b) 50 mL. c) 100 mL. d) 1000 mL.
Qu dilucin se practic en cada caso?
5- Se tiene una solucin 5.10-3 M en NaOH. Calcule la concentracin final si se
practican las siguientes diluciones:
a)1:2 b) 1+1 c) 1:5 d) 1+9.
6- Qu volumen de una solucin 0,600 M en HCl debe tomar para preparar
100 mL de una solucin 0,150 M? Qu dilucin ha practicado?
1 2do cuatrimestre de 2014
Qumica Analtica Serie de Problemas
7- Cuntos mL de HCl concentrado (densidad 1,19 g/ml y 37% p/p) se
requieren para hacer 20 L de una solucin 0,160 M?
Dato: Mr HCl = 36,500.
b) Balance de masa. Condicin de electroneutralidad.
8- Exprese la condicin de electroneutralidad en cada una de las siguientes
soluciones, en trminos de las concentraciones molares de los iones, sin tener
en cuenta las posibles hidrlisis.
a) 0,5 M en NaNO3. b) 0,35 M en BaCl2.
c) 0,01 M en Na2SO4. d) 0,05 M en NaOH.
e) 0,01 M en HNO3 y 0,1 M en KNO3. f) 0,1 M en Al2(SO4)3
g) 0,45 M en NaClO4 y 0,3 M en HClO4. h) 10-3 M en H3PO4
9- a) Un litro de HCl 3,3 M se agita con cido benzoico, disolvindose 0,0152
moles del cido. Exprese el balance de masa para la solucin.
b) 0,1 milimoles de KH2PO4 se agregan a una cantidad de agua suficiente
como para obtener 4 mL de solucin. Exprese los balances de masa y la
condicin de electroneutralidad para la solucin.
c) Se prepara una solucin disolviendo 0,1 moles de H2SO4 en una cantidad tal
que se obtienen 250 mL de solucin. Exprese el balance de masa y el balance
de carga para la solucin obtenida.
10- Exprese el balance de masa y la condicin de electroneutralidad para una
solucin que resulta de mezclar 500 mL de AgNO3 0,01M con 500 mL de
Na2S2O3 0,02 M, admitiendo que no aparece precipitado.
(Las especies presentes en solucin son: Ag+, Na+, S2O32-, Ag(S2O3)23-, H+, OH-
, AgS2O3-, HS2O3- y NO3-)
c) Clculos en gravimetras.
11- 0,50 g de un sulfato soluble dieron 0,65 g de BaSO4. Cul es el %S en
la muestra?
Datos: Ar S = 32.064; Ar O = 15,999; Ar Ba = 137,00.
12- 500 mL de agua corriente dieron un residuo de 0,10 g de CaO. Calcular
el contenido de calcio en agua expresado en ppm de CaCO3.
Datos: Ar O = 15,999. Ar C = 12,011. Ar Ca = 40,08.
13- Indique los factores gravimtricos para convertir segn las reacciones
correspondientes:
a) Mg2P2O7 en MgO
b) Fe3O4 en Fe2O3
2 2do cuatrimestre de 2014
Qumica Analtica Serie de Problemas
c) U3O6 en U
d) B2O3 en Na2B4O7.10 H2O
e) (NH4)2PtCl4 en NH3.
14- Se precipit una muestra de cido oxlico de 1,000g con exceso de
cloruro de calcio y se calcin el precipitado lavado, hasta xido de calcio. El
residuo pes 0,4402g. Calcular el porcentaje de H2C2O4 en la muestra.
Datos: Ar Ca = 40,08; Ar C = 12,011; Ar O = 15,999; Ar H = 1,008
Reacciones:
15- Se precipita 1,000 g de Fe como Fe2O3 hidratado. En la calcinacin se
convierte el 90,00% del Fe en Fe2O3, pero el resto (impropiamente) se
convierte en Fe3O4. Cuntos gramos pesa el precipitado mal calcinado?
Cunto pesara si todo el Fe estuviera como Fe2O3? Cul sera el error
porcentual de la determinacin?
Datos: Mr Fe2O3 =159,70; Mr Fe3O4 =231,55; Ar Fe = 55.851
Respuestas
4- a) [HCl] = 2,5 M Dilucin: 1:2 o 1+1
b) [HCl] = 1 M Dilucin: 1:5 o 1+4
c) [HCl] = 0,5 M Dilucin: 1:10 o 1+9
d) [HCl] =0,05 M Dilucin: 1:100 o 1+99
5- a) 2,5 x 10-3 M
b) 2,5 x 10-3 M
c) 1,0 x 10-3 M
d) 5,0 x 10-4 M
6- V = 25mL Dilucin: 1:4 o 1+3
7- V = 265 mL
9- a) BM) [HA] + [A-] = 0,0152 M [Cl-] = 3,3 M BC) [H+] = [OH-] + [A-]
b) BM) [H3PO4] + [H2PO4-] + [HPO42-] + [PO43-] = 0,025 M [K+] = 0,025 M
BC) [K+] + [H+] = [H2PO4-] + 2[HPO42-] + 3[PO43-] + [OH-]
c) BM) [HSO4-] + [SO42-] = 0,4 M BC) [HSO4-] + 2[SO42-] + [OH-] = [H+]
10- BM) [Ag+] + [Ag(S2O3)-] + [Ag(S2O3)23-] = 0,005 M [Na+] = 0,02 M
[NO3-]= 0,005 M [S2O33-] + 2[Ag(S2O3)23-] + [Ag(S2O3)-] + [HS2O3-] = 0,01 M
3 2do cuatrimestre de 2014
Qumica Analtica Serie de Problemas
BC) [Ag+] + [Na+] + [H+] = [OH-] + [HS2O3-] + [Ag(S2O3)-] + 3 [Ag(S2O3)23-] +
2 [S2O32-] + [NO3-]
11- %S = 17,9 %
12- [CaCO3] = 357 ppm
13-
2 M r MgO
a) FG =
M r Mg 2 P2O7
6 M r Fe2O3
b) FG =
4 M r Fe3O4
3M rU
c) FG =
M rU 3O6
M r Na2 B4O7 .10 H 2 O
d) FG =
2 M r B2O3
2 M r NH 3
e) FG =
M r ( NH 4 ) 2 PtCl4
14- %H2C2O4 = 70,67%
15- m precipitado impuro = 1,4249 g m precipitado puro = 1,4297 g error % = - 0,34 %
4 2do cuatrimestre de 2014
Qumica Analtica Serie de Problemas
SERIE 2 - MUESTREO
Objetivos:
1- Revisin de los conceptos estadsticos de poblacin, media y varianza e
intervalo de confianza.
2- Impacto del error de muestreo en la varianza total de un resultado.
3- Comprender la estadstica del proceso de toma de muestras y elegir el
tamao de muestra adecuada.
Luego de manejar los conceptos de esta seccin se debera ser capaz de
disear procedimientos de muestreo sencillos de acuerdo al tipo de pregunta
que origine el trabajo analtico.
1- Un anlisis cuantitativo para un analito da una concentracin media de 14,5
partes por milln. Se sabe que la desviacin estndar del mtodo es de 1,3
ppm y que la desviacin estndar del muestreo es de 2,5 ppm.
a) Cul es la varianza total del anlisis?
b) Cunto cambiara la varianza total si el desvo estndar del mtodo
analtico mejorase con una reduccin de un 10 %?
c) Cunto cambiara la varianza total (del tem a)) si el desvo estndar del
muestreo mejorase con una reduccin de un 20 %?
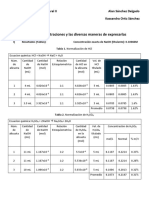
2- Dados los resultados de anlisis sobre una serie de muestras en condiciones
donde hay errores aleatorios de muestreo y de anlisis (columna I) y resultados
obtenidos mediante repetidos anlisis sobre una nica muestra de laboratorio
bien homogeneizada (columna II).
Estime la contribucin del muestreo a la varianza total. Conviene mejorar la
precisin del mtodo usado en el anlisis?
I Porcentaje de analito II Porcentaje de analito
0,114 0,105
0,102 0,103
0,100 0,101
0,105 0,107
0,099 0,103
0,095 0,104
0,105 0,103
0,095
0,106
3- Se desea muestrear un material slido donde el analito a determinar se
encuentra presente en 1x10-6 % de las partculas del material. Las partculas
del material a muestrear son aproximadamente esfricas con un dimetro
medio de 0,05 mm. La densidad de las partculas es de 2,0 g/cm3 sin importar
si contienen el analito.
a) Cuntas partculas debera tomar para que la varianza relativa de muestreo
sea del 1 %?
b) Qu masa de material debe tomar para conseguir dicha varianza relativa?
c) Si la muestra presentara un dimetro 10 veces menor (0,005 mm), a cunto
se reducira la cantidad de partculas a muestrear? En base a este resultado
explique la conveniencia de moler una muestra.
5 2do cuatrimestre de 2014
Qumica Analtica Serie de Problemas
4- El resultado de un anlisis de alimento balanceado para pollos dio como
resultado los siguientes valores de carbonato de magnesio:
Masa de alimento balanceado % p/p de MgCO3 en alimento balanceado
1,0431 g 1,43
0,9908 g 1,36
0,9967 g 1,33
0,9992 g 1,29
1,0073 g 1,25
Si las incertezas del mtodo son despreciables respecto a las de muestreo:
a) Determine la constante de muestreo Ks y utilcela para estimar cuanta masa
de muestra se necesitara para lograr una desviacin estndar de muestreo de
2,5 %.
b) Cul sera la desviacin estndar relativa porcentual y la desviacin
estndar absoluta si se utilizaran muestras de 4 gramos?
5- Para un anlisis de vitamina B en comprimidos se muele un nmero
representativo de los mismos, se homogeneiza y cuartea. Se sabe que se
necesitan 1,6 g de muestra homogeneizada para lograr una desviacin
estndar de muestreo de 2,0 %.
Cuntas muestras son necesarias para que el error relativo porcentual de
muestreo sea como mximo 0,9 %, a un intervalo de confianza del 95 %?
Nota: Deber utilizar una tabla de estadstico t.
6- En un procedimiento de toma de muestra se determin una constante de
muestreo Ks = 36 g.
a) Qu masa dara una desviacin estndar de 5%?
b) Si el mtodo analtico usado en la medicin tiene una desviacin estndar
insignificante comparada con la del muestreo, cuntas muestras de 1,0 gramo
sern necesarias para que el error relativo porcentual de la determinacin sea
del 4 %, a un intervalo de confianza del 95 %?
Nota: Deber utilizar una tabla de estadstico t.
7- Para que un dado procedimiento analtico de fertilizantes sea
econmicamente rentable se requiere una exactitud de un 3 % en no ms de 8
repeticiones con un 95 % de probabilidad. Con este requerimiento una empresa
desea un protocolo de muestreo y determinacin de fosfato en muestras de
guano. El mismo est compuesto de una mezcla de partculas de dimetro
medio 0,25 cm, conteniendo un 40 % de fosfato de calcio ((Ca3(PO4)2 )= 3,21
g/cm3) y un 60 % de carbonato de calcio ((CaCO3)= 2,85 g/cm3).
a) Obtenga un valor estimado para la constante de muestreo (Ks) para el lote
de guano explicando su razonamiento.
b) Cuntas repeticiones del procedimiento analtico (muestreo-determinacin)
sern necesarias si se deseara que la media experimental no difiera del valor
verdadero en ms de un 2 % con una probabilidad del 95 %? Considere que el
procedimiento analtico tiene un desvo estndar relativo porcentual del 2 %.
c) Cul deber ser el mximo desvo estndar relativo porcentual que podr
tener el mtodo de anlisis (determinacin) para que con muestras de m = Ks
gramos de guano sea posible cumplir con el requerimiento de rentabilidad?
6 2do cuatrimestre de 2014
Qumica Analtica Serie de Problemas
8- (OPTATIVO DESPUS DE LA SERIE DE PRECIPITACIN)
Para disear un protocolo para titulacin por mtodo de Mohr de muestras de
25,00 mL de cloruros de concentraciones cercanas a 0,05 M se opta por titular
con AgNO3 0,025M.
a) Si el pH de las muestras es regulado en 5,0 Cul es la mnima
concentracin de K2CrO4 que deber usarse en la titulacin para que el error
por viraje del indicador sea menor al 1 %?
b) Considerando que el desvo estndar total no sea mayor al 2 %, cuntas
muestras deberan tomarse si se deseara que la media poblacional no difiera
en ms del 1,5 % con un nivel de confianza del 95 %?
[CrO4 2 ][ H + ] 6 [Cr2O7 2 ]
Datos: Ka2 =
= 1.25 x10 ; K= 2 2 + 2
= 3.2 x10+14 ;
[ HCrO4 ] [CrO4 ] [ H ]
Kps ( Ag 2CrO4 ) = [CrO4 2 ][ Ag + ]2 = 1.2 x1012
----------------------------------------------------------------------------------------------------------
Tabla del estadstico t
n t (95%) n t (95%) n t (95%) n t (95%)
1 12,706 9 2,2622 17 2,1098 25 2,0595
2 4,3027 10 2,2281 18 2,1009 26 2,0555
3 3,1824 11 2,2010 19 2,0930 27 2,0518
4 2,7765 12 2,1788 20 2,0860 28 2,0484
5 2,5706 13 2,1604 21 2,0796 29 2,0452
6 2,4469 14 2,1448 22 2,0739 30 2,0423
7 2,3646 15 2,1315 23 2,0687 1,9600
8 2,3060 16 2,1199 24 2,0639
n representa los grados de libertad, en nuestro caso el nmero de muestras
menos 1.
Respuestas
1- a) 7,94 ppm2; b) 7,62 ppm2 (se reduce 4 %); c) 6,75 ppm2 (se reduce15 %)
2- Smuestreo = 5,7 x 10-3; S2muestreo = 3,2 x 10-5
Contribucin del muestreo = 90 %
3- a) 1 x 1012 partculas b) 130,9 kg c) 130,9 g
4- a) Ks = 26,9 g mmuestra = 4,3083 g
b) R% = 2,59 % SDabsoluta = 0,0345 %
5- a) Nmuestra = 21
6- a) masa = 1,44 g b) Nmuestra = 11
7- a) Ks = 367 g; b) N = 7; c) Srel % de anlisis = 3,45 %.
7 2do cuatrimestre de 2014
Qumica Analtica Serie de Problemas
SERIE 3 SISTEMAS CIDO BASE
Objetivos:
1- Clculo riguroso de las concentraciones de todas las especies presentes en
una solucin de cidos fuertes o dbiles. Aprender a verificar si las
aproximaciones fueron suficientes para una exactitud cercana al 1%.
2- Poder esquematizar curvas de titulacin y comprender el efecto de las
constantes de disociacin y el efecto de las concentraciones del titulante y del
titulado en las mismas.
3- Estimacin del error de titulacin cuando se utilizan indicadores visuales.
Con esta seccin se espera obtener un manejo fluido del clculo de pH y
concentraciones en soluciones de cidos y anfolitos haciendo uso de
expresiones aproximadas pero a la vez rigurosas. Es importante alcanzar la
capacidad de decidir cundo un clculo simple es suficiente y cundo es
necesario llevar cabo un clculo ms complicado utilizando menos
aproximaciones para lograr mayor exactitud. Se deber poder esquematizar
curvas de titulacin razonablemente exactas calculando unos pocos puntos
importantes.
EQUILIBRIO CIDO BASE. TITULACIN
a) Equilibrio cido-base.
1- El producto inico del agua a 0 C es 1,1 x 10-15, a 25 C es 1,0 x 10-14 y a
una temperatura de 60 C es 9,6 x 10-14.
Calcule el pH del agua pura a las temperaturas mencionadas. Discuta, en
funcin de estos valores, la validez de la segunda cifra decimal en la medicin
experimental del pH.
2- Calcule la [OH-] y la [H+] de las siguientes soluciones acuosas de KOH:
a) 5 x 10-3 M; b) 9,9 x 10-8 M; c) 10-10 M.
Dato: Kw = 10-14.
3- La constante de ionizacin del cido lctico es 1,4 x 10-4. Calcule el grado de
ionizacin y la concentracin de HL sin disociar en una solucin:
a) 1,00 M; b) 0,01 M.
4- Calcule el pH de una solucin 0,05 M de H2S.
Datos: Kas H2S = 1,0 x 10-7; 1,2 x 10-15.
5- Calcule las concentraciones de todas las especies presentes en:
a) Una solucin 0,1 M en H3PO4
b) Una solucin 0,1 M en cido ctrico.
Datos: Kas H3PO4: 7,1 x 10-3; 6,3 x 10-8; 4,4 x 10-13
Kas c. Ctrico: 7,4 x 10-4; 1,7 x 10-5; 4,0 x 10 -7
6- Se disuelven 1,20 g de HAcO en 200 mL de agua y 0,74 g de cido
propinico en 50 mL.
8 2do cuatrimestre de 2014
Qumica Analtica Serie de Problemas
Al mezclar ambas soluciones el volumen final es de 250 mL. Calcule el pH.
Discuta la necesidad de usar una ecuacin cbica para el clculo de la [H+],
teniendo en cuenta la precisin del dato obtenido.
Datos:
Mr HAcO = 60,000; Ka HAcO = 1,8 x 10-5; Mr HPr = 74,000; Ka HPr = 1,4 x 10-5
7- a) Calcular el pH de una solucin acuosa 0,1 M de NaHCO3.
b) Calcular el pH de una solucin acuosa 0,001 M de NaH2PO4
c) Calcular el pH de una solucin acuosa 0,1 M de NaHS
Datos: Ka1 H2CO3 = 4 x 10-7; Ka2 H2CO3 = 5 x 10-11
Kas H3PO4: 7,1 x 10-3; 6,3 x 10-8; 4,4 x 10-13
Kas H2S = 1,0 x 10-7; 1,2 x 10-15.
8- Calcule el pH de una solucin 0,1 M de (NH4)2SO3.
Datos: Ka1 = 1,3 x 10-2; Ka2 = 6,2 x 10-6; Kb NH3 = 1,78 x 10-5.
b) Curvas de titulacin.
9- Dibuje la curva de titulacin pH vs. grado de avance () en el mismo grfico,
para los siguientes sistemas titulado-titulante:
a) 25,00 mL de HCl 0,1 M con NaOH 0,1 M
b) 10,0 mL de HAcO 0,1 M con NaOH 0,1 M
c) 10,00 mL de NH3 0,1 M con HCl 0,1 M
Indique qu cambios observara en las curvas si:
i) diluyera 10 veces el titulante
ii) diluyera 10 veces el titulado
iii) diluyera 10 veces ambos
Seleccione un indicador de punto final para cada propuesta y calcule el error de
titulacin cometido, a partir de los correspondientes valores de pKa.
Datos: pKa HAcO = 4,75 ; Kb NH3 = 10-5;
Anaranjado de Metilo: 3,14,4 Azul de Bromotimol: 6,0 7,6
Fenolftalena: 8,2 9,8
10- Represente grficamente pH vs. para los tres sistemas del problema 9.
Compare el grfico, por superposicin, con la curva de titulacin.
11- Se titulan 50 mL del cido dbil HA 0,1 M con una base fuerte de
concentracin 0,1 M.
a) Calcule el valor mnimo de Ka para que, cuando se hayan adicionado 49,95
mL de titulante, la reaccin entre HA y OH- sea esencialmente completa,
(99,9%) y que el pH cambie en 2,00 unidades con la adicin de 2 gotas ms
(0,10 mL) de titulante.
b) Repita el clculo para pH = 0,10 unidades.
c) Qu puede decir de la titulacin en el caso b) con un indicador visual?
12- a) Dibuje superpuestas las curvas de titulacin que se obtienen en los
siguientes casos:
(i) NaBO2 0,1 M con HCl 0,1 M y (ii) HBO2 0,1 M con NaOH 0,1 M. Justifique la
forma de las curvas obtenidas con un grfico vs pH.
9 2do cuatrimestre de 2014
Qumica Analtica Serie de Problemas
b) Calcule el error de titulacin cometido si cada una de las titulaciones se
detuvieran una unidad de pH antes del punto equivalente. Comente los
resultados obtenidos.
Dato: pKa HBO2 = 9,5
13- Una muestra de 1,600 g que contiene un cido dbil HA (Mr = 62,0) se
disuelve en 60 mL de agua y se titula con NaOH 0,250 M. Cuando la mitad del
cido se ha neutralizado, el pH es de 5,00 y en el punto de equivalencia es de
9,00. Calcule el porcentaje de HA en la muestra.
14- Qu cantidad en gramos debe pesarse de cada una de las siguientes
sustancias patrn, para valorar una solucin 0,1 N de NaOH o HCl, y gastar
20,0 mL?
a) HgO [
b) Brax [ ]
c) KH(IO3)2 [ ]
d) Na2CO3 [ ]
e) cido benzoico [ ]
f) Biftalato de potasio [ ]
15- Una muestra de 2,020 g de ZnO impuro se pone en digestin con 100,0
mL de H2SO4 0,5000 N, y el exceso de cido se neutraliza con 2,96 mL de
NaOH 0,1372 N. Calcular el % de pureza de la muestra, suponiendo que slo
contiene impurezas inertes.
Dato: Mr ZnO = 81,37.
16- Una muestra de 3,500 g que contiene NaOH y Na2CO3 se disolvi en
250,0 mL. Una alcuota de 50,00 mL requiere 41,70 mL de HCl 0,0860 N para
virar la fenolftalena. Una segunda alcuota de 50,00 mL se trat con BaCl2,
para precipitar el carbonato. La solucin necesit 7,60 mL de cido para virar la
fenolftalena. Calcular el % de cada componente en la muestra.
Datos: Mr Na2CO3 = 106,00 Mr NaOH = 40,00
17- Se entregan a un qumico para su anlisis diversas muestras,
advirtindole que contienen NaOH, Na2CO3, NaHCO3 o mezclas compatibles
de esas sustancias, junto con impurezas inertes. A partir de los datos que se
indican a continuacin, identificar las sustancias y calcular el % de cada una de
ellas. En todos las casos se emplean muestras de 1,0000 g y HCl 0,2500 N.
Muestra 1: con fenolftalena se consumen 24,32 mL. Una segunda muestra
requiri 48,64 mL con naranja de metilo.
Muestra 2: Con el agregando fenolftalena la muestra permanece incolora, y
con naranja de metilo se consumen 36,47 mL.
Muestra 3: se consumieron 15,29 mL para que se produjera el viraje en fro de
la fenolftalena, y hubo que agregar 33,19 mL mas para la neutralizacin
completa.
Muestra 4: se valor con cido hasta desaparicin del color violeta de la
fenolftalena, consumindose 39,96 mL. Agregando un exceso de cido,
hirviendo y valorando por retorno con lcali, se comprob que el lcali era
exactamente equivalente al exceso de cido agregado.
10 2do cuatrimestre de 2014
Qumica Analtica Serie de Problemas
Muestra 5: se valora en fro con el cido, empleando fenolftalena como
indicador; la solucin vira a incoloro despus de adicionar 30,00 mL de cido.
Se agrega a continuacin naranja de metilo, y se requieren 5,00 mL ms del
cido para el viraje.
Datos: Mr Na2CO3 = 106,00; Mr NaOH = 40,00; Mr NaHCO3 = 84,00
18- Una muestra que se sabe contiene Na3PO4, Na2HPO4, NaH2PO4,
mezclas compatibles de estas sustancias, junto con impurezas inertes, pesa
2,00 g. Al valorar esta muestra con HCl 0,500 N, en presencia de naranja de
metilo, se consumen 32,0 mL. Valorando el mismo peso de muestra con igual
cido, en presencia de fenolftalena, se consumen 12,0 mL. Calcular la
composicin porcentual de la muestra.
19- Se sabe que una solucin contiene: a) HCl y H3PO4; b) H3PO4 y
NaH2PO4, o c) los tres componentes por separado. Una muestra valorada con
NaOH consume A mL en presencia de naranja de metilo, y el mismo peso de la
muestra consume B mL del NaOH con fenolftalena. Qu relacin matemtica
debe existir entre A y B en el caso de tener la mezcla a), la b) o una muestra c)
con H3PO4 puro?
Datos: Mr HCl = 36,45; Mr H3PO4 = 98,00 ; Mr NaH2PO4 = 120,00
Kas H3PO4: 7,1 x 10-3; 6,3 x 10-8; 4,4 x 10-13
Anaranjado de Metilo: 3,14,4 Fenolftalena: 8,2 9,8
20- Se desean analizar dos muestras de medicamento que contienen
mezclas compatibles de fosfatos. El protocolo consta de disolver una cierta
cantidad de muestra slida y llevarse a 100,0 mL finales (Solucin A). Se toma
una alcuota de 25,00 mL de A y se la titula con HCl 0,0200 M (f = 0,9847)
hasta viraje de fenolftalena (8,2 9,8). Otra alcuota de 10,00 mL de A se
valora con el mismo HCl hasta viraje de la heliantina (3,1 - 4,4).
A continuacin se informan los datos registrados para cada muestra:
Muestra 1 Muestra 2
Masa de muestra 1,0049g 0.9987g
Vol HCl (fenolftalena) 23,3mL 17,6mL
Vol HCl (heliantina) 18,7mL 20,5mL
a) En base a los valores obtenidos en las titulaciones justifique cul de las
posibles mezclas compatibles se encuentra en cada muestra.
b) Calcule la composicin porcentual de las muestras expresada en funcin de
cada componente. Qu muestra posee mayor porcentaje de fsforo total?
c) Grafique la curva de titulacin de una mezcla 0,1 M de HPO42- y 0,2 M PO43-
con ambos indicadores titulando con HCl 0,1 M. Justifique brevemente los
puntos importantes.
21- Se sabe que dos muestras podran contener Na3AsO4, Na2HAsO4,
NaH2AsO4 o sus mezclas compatibles. Se desea conocer la composicin de las
mismas para lo cual se lleva a cabo el siguiente protocolo:
Muestra 1: se toma una masa de 2,0321 g de muestra y se disuelven en 40 mL
de agua. Se filtra y se eliminan impurezas y el remanente se lleva a un volumen
final de 100 mL (solucin A).
11 2do cuatrimestre de 2014
Qumica Analtica Serie de Problemas
La titulacin de una alcuota de 25,00 mL de la solucin A consume 19,55 mL
de HCl 0,100M para virar la fenolftalena y otra alcuota de 25,00 mL de la
solucin A consume 39,10 mL del mismo cido para virar el rojo de metilo.
Muestra 2: se pesan 2,1038 g de muestra y se procede como para la muestra 1
(solucin B).
La titulacin de una alcuota de 25,00 mL de la solucin B consume 7,60 mL
del mismo HCl para virar la fenolftalena y otra alcuota de 25,00 mL de la
solucin B consume 32,20 mL para virar el rojo de metilo.
a) Indique cuales son las posibles especies compatibles presentes en las
muestras. Justifique.
b) Calcule la composicin porcentual de la muestra 1 y la muestra 2 en base a
los datos volumtricos. Justifique.
c) Grafique la curva de titulacin observada para 25,00 mL de una muestra de
agua que tiene una concentracin de H3AsO4 de 0,1 M y que se titula con una
solucin de NaOH 0,1 M. Calcule analticamente el pH para = 0; 0,5 y 1,0.
Justifique estrictamente la validez de sus aproximaciones.
Datos: Kas H3AsO4: 2,5 x 10-4 ; 4,5 x 10-8 ; 3,2 x 10-13; Mr H3AsO4 = 141,92;
Mr NaH2AsO4 = 163,91; Mr Na2HAsO4 = 185,90; Mr Na3AsO4 = 207,89
Intervalos de viraje: Fenolftalena: 8,2 9,8 Rojo de Metilo: 4,2 5,5
22) Discuta la veracidad de las siguientes afirmaciones. Justifique su respuesta
sin realizar clculos
a) Una mezcla equimolar de H3PO4 e Ca(OH)2 tiene pH 7,0.
b) Cuando se titula una solucin de NaHCO3 con HCl y se utiliza heliantina
como indicador de punto final (IV: 4,0-5,0) se consume el mismo
volumen que si se utiliza fenolftalena como indicador (IV: 8,5-10).
c) El error de titulacin cometido en la determinacin de cido fosfrico
utilizando heliantina (pKa = 4,5) como indicador del punto final es el
mismo independientemente que se utilice NaOH o NH3 como reactivo
titulante.
d) Cuando se titula HCl 0,10 M con NaOH de igual concentracin
i) el pH del punto equivalente es MENOR que cuando se utiliza NH3
0,10 M como titulante.
ii) el volumen del punto equivalente es MENOR que cuando se
utiliza NH3 0,10 M como titulante.
iii) el error de titulacin que se comete a pH = 9 ES EL MISMO que
cuando se utiliza NH3 0,10 M como titulante.
iv) el error de titulacin que se comete a pH = 4 ES EL MISMO que
cuando se utiliza NH3 0,10 M como titulante.
e) El volumen de NaOH 0,1 M que se consume para titular una solucin de
H2SO4 0,1 M es el doble que el que se requiere para titular NaHSO4 de
idntica concentracin.
Datos: Utilice todos los datos que considere necesarios de los problemas
precedentes
12 2do cuatrimestre de 2014
Qumica Analtica Serie de Problemas
Respuestas
1- T = 0 C pH = 7,479
T = 25 C pH = 7,000
T = 60 C pH = 6,509
2- a) [H+] = 2 x 10-12 M; [OH-] = 5 x 10-3 M.
b) [H+] = 6,21 x 10-8 M; [OH-] = 1,61 x 10-7 M.
c) [H+] = 1 x 10-7 M = [OH-]
3- a) [HL] = 0,988 M L- = 1,18 x 10-2
b) [HL] = 8,88 x 10-3 M L- = 0,112
4- pH = 4,15
5- a) [H3PO4] = 7,67 x 10-2 M; [H2PO4-] = 2,33 x 10-2 M; [HPO42-] = 6,3 x 10-8 M;
[PO43-] = 1,19 x 10-18 M; [OH-] = 4,29 x 10-13 M; [H+] = 2,33 x 10-2 M.
b) [OH-] = 1,12 x 10-12 M; [H+] = 8,24 x 10-3 M; [H3A] = 0,092 M; [H2A-] = 8,24 x
10-3 M; [HA2-] = 1,7 x 10-5 M; [A3-] = 8,25 x 10-10 M.
6- [H+] = 1,41 x 10-3 M pH = 2,85
7- a) pH = 8,35 b) pH = 5,13 c) pH = 10,00
8- pH = 7,08
9-
a) b) c)
pH pH pH
0 1,00 0 2,87 0 11,13
0,5 1,48 0,5 4,74 0,5 9,25
1 7,00 1 8,72 1 5,28
1,5 12,30 1,5 12,30 1,5 1,70
11- a) Kamn = 2 x 10-5; b) Kamn = 2,51 x 10-7.
12-
a) b)
pH pH
0 11,25 0 5,25
0,5 9,50 0,5 9,50
1 5,40 1 11,10
1,5 1,70 1,5 12,30
13- %HA = 38,8 %.
13 2do cuatrimestre de 2014
Qumica Analtica Serie de Problemas
14- a) m HgO = 0,2166g; b) m borax = 0,3814g; c) m KH(IO3)2 = 0,7798g; d) m
Na2CO3 = 0,1060g (naranja de metilo) o m Na2CO3 = 0,2120g (fenolftalena); e)
m c. benzoico = 0,2442 g; f) m kbift = 0,4084g.
15- % Pureza = 99,88 %.
16- % NaOH = 3,7 %; % Na2CO3 = 44,5 %.
17- muestra 1: %Na2CO3 = 64,45%; muestra 2: %NaHCO3 = 76,59%; muestra
3: %NaHCO3 = 37,59% + %Na2CO3 = 40,52%; muestra 4: %NaOH = 39,96%;
muestra 5: %NaOH = 25,0% + %Na2CO3 = 13,25%.
18- %Na3PO4 = 49,2% + %Na2HPO4 = 28,4%.
19- a) A< B < 2A b) B>2A c) B = 2A
20- a) muestra 1: fosfato; muestra 2: fosfato + fosfato cido.
b) muestra 1: % fosfato = 0,183 mol/g x Mr fosfato
muestra 2: % fosfato = 0,139 mol/g x Mr fosfato; % fosfato cido = 0,134 mol/g
x Mr fosfato cido. La muestra 2 tiene mayor porcentaje de fsforo total.
c) pH inicial = 12,47; VHCl = 2 Vmuestra (viraje fenolftalena): pH = 9,73; VHCl = 3,5
Vmuestra (buffer HPO42-/H2PO4-): pH = 7,20; VHCl = 5 Vmuestra (viraje heliantina): pH
= 4,70.
21- a) muestra 1: Na3AsO4; muestra 2: Na3AsO4 + Na2HAsO4.
b) muestra 1: % Na3AsO4 = 80 %;
muestra 2: % Na3AsO4 = 30,04 % + % Na2HAsO4 = 60,09 %.
c) = 0: pH = 2,31; = 0,5: pH = 3,61; = 1: pH = 5,48; = 1,5: pH = 7,35; =
2: pH = 9,78.
14 2do cuatrimestre de 2014
Qumica Analtica Serie de Problemas
SERIE 4 SISTEMAS REGULADORES
Objetivos:
Conocer el impacto del poder regulador de un sistema en las titulaciones cido
- base.
1- Calcule el pH de las siguientes soluciones acuosas:
a) 0,20 M en HAcO y 0,10 M en NaAcO. pKa HAcO = 4,75
b) 0,10 M en HF y 0,20 M en KF. pKa HF = 3,16
c) 0,10 M en NH3 y 0,05 M en NH4Cl. pKa NH4 = 9,27
d) 0,05 M en HCl y 0,50 M en NH3. Kb NH3 = 2 x 10-5
e) 0,01 M en NaAcO y 0,01 M en NH3. Ka HAcO = 2 x 10-5
2- Obtenga la expresin del poder regulador de una base fuerte. En qu se
diferencia de la correspondiente a un cido fuerte? A que pH es mnimo su
valor? Cul es el poder regulador del agua pura?
3- Calcular la variacin de pH causada por la adicin de 0,5 mL de NaOH 0,2 M
a 100 mL de (considere despreciable el cambio de volumen)
a) Agua destilada
b) Solucin de HCl 1 M
c) Solucin de HCl 10-4 M
d) Solucin 0,002 M en HAcO y 0,002 M en NaAcO
e) Solucin 0,2 M en HAcO y 0,2 M en NaAcO
f) Solucin 0,39 M en HAcO y 0,01 M en NaAcO
Datos: pKa HAcO = 4,75
4- Se quieren preparar 500 mL de una solucin reguladora de pOH = 8,6. Se
parten de 50 mL de una solucin 1 M en piridina. Qu volumen de HCl 1 M es
necesario agregar a esta solucin? Calcule, adems, el poder regulador.
Dato: pKb piridina = 8,8
5- Se desean preparar 100,0 mL de una solucin de pH = 7,0 por adicin de
una cantidad adecuada de alguna de las siguientes sustancias a 10,0 mL de
arseniato disdico 1,00 M.
i) NaOH 0,2 M; ii) HCl 0,1 M; iii) arseniato trisdico 1,00 M.
a) Indique cual de ellas seleccionara y qu volumen se requerir. Justifique su
respuesta.
b) Calcule la capacidad reguladora de la solucin resultante. Ser buena
reguladora a ese pH si se requiere una variacin no mayor de 0,01 unidades
por adicin de 0,5 milimoles de NaOH?
Datos: Kas H3AsO4 = 2,5 x 10-4; 4,5 x 10-8; 3,2 x 10-13.
6- Se mezclan volmenes iguales de una solucin 0,100 M en HBO2 y 0,020 M
en NH3.
Calcule el pH y el poder regulador de la solucin resultante (admita que los
volmenes son aditivos).
Datos: Ka HBO2 = 1,0 x 10-10; Kb NH3 = 2,0 x 10-5
15 2do cuatrimestre de 2014
Qumica Analtica Serie de Problemas
7- Se desea preparar una solucin reguladora de pH = 9,25 para utilizar 10 mL
de la misma en un sistema de 50 mL de volumen total, en dnde se liberan
0,53 mmol de H+. Para la preparacin del mismo se dispone de las siguientes
soluciones:
i) HCl 1 M ii) NH3 1 M iii) H3BO3 1 M iv) NaOH 1 M
a) Indique todas las posibles soluciones buffer que podra realizar. Justifique
realizando grficos cualitativos de poder regulador en funcin del pH. De
encontrar ms de una opcin, comprelas e indique cul resultara mejor
utilizar en este caso.
b) Si se desea que el pH del sistema a regular no vare en ms de 0,10
unidades, utilizando el buffer elegido en el item a), indique el/los volumen/es
necesario/s de solucin/es para preparar 100 mL del buffer.
Nota: Considere en el caso de mezclas que los volmenes son aditivos.
Datos: pKa (NH4+) = 9,25; pKa (H3BO3) = 9,30
8- Las bacterias del grupo Acetobacter producen cido actico a partir de la
fermentacin aerbica de insumos comunes como malta, cereal, arroz, etc. La
reaccin qumica general es:
C2H5OH + O2 CH3COOH + H2O
Una cepa de Acetobacter se siembra en un medio de cultivo en presencia de
un buffer NaH2PO4 / Na2HPO4 0,1 M.
a) Calcule el pH final del medio de cultivo si las bacterias sembradas producen
un equivalente a 5,0 x 10-3 moles de protones en 50 mL. Justifique.
b) Se desean preparar 100,0 mL de una solucin de pH = 7,0 por adicin de
una cantidad adecuada de alguna de las siguientes sustancias a 10,0 mL de
Na2HPO4 1,00 M.
NaOH 0,2 M ; HCl 0,1 M ; NaH2PO4 1,00 M.
Indique cul de ellas seleccionara y qu volumen se requerir. Justifique su
respuesta.
Calcule la capacidad reguladora de la solucin resultante. Ser buena
reguladora a ese pH si se requiere una variacin no mayor de 0,01 unidades
por adicin de 0,5 milimoles de NaOH?
Datos: pKas H3PO4: 2,15; 7,20; 12,36.
9) Discuta la veracidad de las siguientes afirmaciones. Justifique su respuesta
sin realizar clculos.
a) El poder regulador de una solucin 1,0 M de NH4CN a su propio pH es
0,575.
b) El poder regulador de una solucin 1,0 M de NH4AcO a su propio pH es
0,575
c) Cuando se mezclan volmenes iguales de H3AsO4 con NaOH, ambos 1
M, se obtiene un excelente regulador de pH.
d) Una solucin formada mezclando cantidades adecuadas de acetato de
sodio 0,1 M y cido Actico 0,1 M regula mejor el pH en un valor 4,22 que
otra solucin preparada mezclando iguales cantidades de cido benzoico
0,001 M y benzoato de sodio 0,001 M.
Datos: pKa cido benzico = 4,22, el resto puede extraerse de los
problemas precedentes.
16 2do cuatrimestre de 2014
Qumica Analtica Serie de Problemas
Respuestas
1- a) pH = 4,45; b) pH = 3,46; c) pH = 9,57; d) pH = 10,25; e) pH = 10,64.
C Ka (H + )
2- = 2,303 ( H + ) + (OH ) +
(( K a + ( H + )) 2
pHmin = 7,00
agua pura = 4,606 x 10-7.
3- a) pH = 4; b) pH = 4,35 x 10-4; c) pH = 6,95; d) pH = 0,48; e) pH = 4,34
x 10-3; f) pH = 0,03.
4- VHCl = 19,3 mL = 0,0546 M
5- a) solucin de HCl 0,1 M VHCl = 69,1 mL
b) = 0,0493 M
6- pH = 9,13 = 1,76 x 10-2 M
7- a) solucin 1: NH3 + HCl (buffer NH3/NH4+); solucin 2: H3BO3 + NaOH
(buffer H3BO3/H2BO2-); solucin 3: NH3 + H3BO3 (buffer NH3/NH4+ y
H3BO3/H2BO2-). La mejor es NH3 + H3BO3 (mayor a pH = 9,25).
b) VH3BO3 = 47,3 mL, VNH3 = 44,6 mL.
8- a) pH = 4,68; b) se elige NaH2PO4 1,00 M, VNaH2PO4 = 15,85 mL; bpH=7 =
0,141 M; pH = 0,035 (no es buena reguladora a ese pH).
17 2do cuatrimestre de 2014
Qumica Analtica Serie de Problemas
SERIE 5 - EQUILIBRIO DE PRECIPITACIN
Objetivos:
1- Efectuar clculos de solubilidades relacionadas con precipitacin cuantitativa
y selectiva de analitos.
2- Describir curvas de titulacin por precipitacin calculando los puntos mas
importantes de las mismas.
3- Clculos rigurosos de solubilidades de sales de cidos dbiles en funcin del
pH de la solucin o en presencia de iones comunes.
Con esta seccin se pretende poder elegir las condiciones necesarias para la
precipitacin cuantitativa de un analito, permitiendo su separacin y saber si
ser posible separar dicho analito de una mezcla donde podran precipitar mas
de un slido.
Debera poder decidirse si las condiciones de una muestra dada son tales que
un mtodo de volumetra por precipitacin seria aplicable.
a) Equilibrio de precipitacin
1- Calcule la solubilidad del AgCl y del Ag2CrO4 en NaNO3 0,04 M (sin tener en
cuenta procesos de hidrlisis) si:
a) El factor de actividad es 0,70 para todos los iones.
b) El factor de actividad se considera igual a 1,0.
Datos: pKps AgCl = 9,70; pKps Ag2CrO4 = 11,50.
2- Para eliminar impurezas de 1,35 g de un precipitado de PbI2 se dispone de
250 mL de agua destilada y 250 mL de solucin de NH4I 0,1 M Cul de los
dos lquidos utilizara como solucin de lavado? Qu fraccin de precipitado
se perdera concluido el lavado?
Datos: solubilidad PbI2 en agua = 1,2 x 10-5 M; Mr PbI2 = 461,00.
3- Se tienen dos porciones de 50 mL de solucin 0,02 M en Ag2SO4. A una de
ellas se agregan 50 mL de K2SO4 2 M, y a la otra 50 mL de AgNO3 2 M. En
cul de ellas es ms pronunciado el efecto de ion comn? Considere que los
volmenes son aditivos y que los procesos de hidrlisis son despreciables.
Datos: Kps Ag2SO4 = 2 x 10-5
4- Se agregan 25 mL de una solucin 0,5 M en KI a 25 mL de una solucin
0,25 M en AgNO3 y 0,05 M en Pb(NO3)2. Cul es la concentracin de Pb y de
Ag en el equilibrio?
Datos: Kps PbI2 = 1,4 x 10-8; Kps AgI = 1,5 x 10-16
5- Una solucin es 10-2 M en BaCl2 y 10-2 M en SrCl2. Si se mezclan 100 mL de
la misma con 200 mL de Na2SO4 2 x 10-2 M, qu fraccin de cada in
precipita?
Datos: Kps SrSO4 = 3,2 x 10-7; Kps BaSO4 = 1,1 x 10-10
6- Qu concentracin de Na2CO3 sera necesaria como mnimo para
transformar 10-3 moles de BaSO4 en BaCO3 si se usa un volumen de 100 mL?
Despreciar hidrlisis del carbonato.
18 2do cuatrimestre de 2014
Qumica Analtica Serie de Problemas
Datos: Kps BaCO3 = 5,1 x 10-9. Kps BaSO4 = 1,1 x 10-10
b) Precipitacin - acidez
7- Un litro de solucin contiene 0,5 moles de Mn (II). Calcule la concentracin
de protones mnima necesaria para impedir la precipitacin del MnS cuando la
solucin se satura con H2S (g). Considere que la concentracin de H2S en una
solucin saturada es 0,1M.
Datos: Kps MnS = 10-13 pKas H2S = 7,0 y 14,9
8- Se desean mezclar 100 mL de NH3 0,1 M con igual volumen de una solucin
0,02 M en MnCl2. Calcule el nmero mnimo de moles de NH4Cl que se deben
agregar para impedir la precipitacin del Mn(OH)2.
Datos: Kps Mn(OH)2 = 2 x 10-13 Kb NH3= 2 x 10-5.
9- Calcule la solubilidad molar del BaSO4 en:
a) agua
b) solucin 10-3 en H2SO4
c) solucin 0,2 M en CH3COOH
d) solucin 10-3 en Na2SO4
Comente los resultados obtenidos.
Datos: Ka HSO4- = 2 x 10-2; Ka HAcO = 2 x 10-5; Kps BaSO4 = 9 x 10-11.
10- El uranio se presenta en la naturaleza como distintas especies, y una de las
ms importantes son los complejos de su forma oxidada con la especie
carbonato.
a) Calcule la solubilidad del UO2CO3 en un medio acuoso donde pCO2 = 0,1
atm y a los siguientes valores de pH = 4, 5, 7 y 8.
b) Explique cualitativamente, en funcin de los equilibrios y las especies
presentes, las variaciones de solubilidad observadas a cada valor de pH (en
menos de 10 renglones).
Datos: Kps UO2CO3 = 4 x 10-15
Ka2 = .9x10-19
Ke = .4x1016
c) Volumetra por precipitacin
11- Los elementos metlicos como Ba y Sr deben formar especies voltiles
para producir los colores caractersticos en los fuegos artificiales. Para eso se
utilizan los denominados "dadores de cloro", compuestos que contienen
tomos de Cl para generar a altas temperaturas especies emisoras como el
SrCl (rojo). Se quiere analizar el contenido de Cl en hexacloroetano (C2Cl6)
presente en una bengala. Para eso se toma 4,1094 g del contenido de la
bengala previamente homogeneizado, se disuelve convenientemente y se
eliminan las posibles interferencias, llevando a un volumen final de 100,0 mL
con agua destilada. Se toma una alcuota de 5,00mL, se lleva a 25,00mL con
agua destilada, se agrega 1 mL de solucin de K2CrO4 al 5% y se titula con
solucin valorada de AgNO3 0,100 M, agitando constantemente, hasta alcanzar
el punto final. Paralelamente se realiza un blanco utilizando CaCO3 para
19 2do cuatrimestre de 2014
Qumica Analtica Serie de Problemas
simular el precipitado, y se anota el volumen de AgNO3 requerido para
observar el mismo punto final.
Si la titulacin consumi 6,30 mL de solucin de AgNO3, y el blanco 0,05 mL,
calcule el porcentaje de hexacloroetano en la bengala.
Datos: Mr C2Cl6 = 236,72
12- Una muestra de 2,2886g de un plaguicida que contiene DDT, di-(p-
clorofenil)- tricloroetano, se mineraliza y la disolucin resultante se enrasa a
100,0 mL. A una alcuota de 25,0 mL se le aaden 10,0 mL de una disolucin
de AgNO3. En la valoracin del exceso de Ag+ se consumen 3,75 mL de SCN-.
Para determinar la concentracin de la disolucin de AgNO3, se pesan 0,1226
g de NaCl, se disuelven en agua y se valoran por el mtodo de Mohr con la
disolucin de AgNO3 requiriendo 21,4 mL de la misma. Si 17,7 mL de SCN-
consumen 19,7 mL de esa misma disolucin de Ag+, calcular el porcentaje de
DDT en el plaguicida.
Datos: Mr DDT = 354,50
13. Discuta la veracidad de las siguientes afirmaciones. Justifique su
respuesta sin realizar clculos.
a) El punto equivalente de la titulacin de Na2C2O4 con AgNO3 en medio
neutro se alcanza cuando la [C2O4=] = (Kps/4)1/3.
b) El punto equivalente de la titulacin anterior realizada a pH = 5,0 se
alcanza a la misma concentracin de oxalato indicada en b).
c) Cuando de una solucin equimolar de Ca y Ba se precipitan ambos
como oxalatos, el FS Ca/Ba en la solucin es igual al cociente entre sus
Kps independientemente del pH al que se regule tal solucin.
d) Cuando de una solucin equimolar de sulfato y oxalato se precipitan
ambos como sales de Ba(II), el FS sulfato/oxalato definido en la
solucin depende del pH al cual se regula el medio.
e) La constante de producto de solubilidad (Kps) del BaSO4 en agua pura
es MAYOR que en una solucin 0,010 M en Na2SO4.
f) Al agregar I- a una solucin que contiene Pb2+, el producto (I-)2.(Pb2+) es
una constante.
g) La solubilidad del AgCl en la titulacin de NaCl con AgNO3 (ambos 0,1
M) en = 0,1 es mayor que en = 1,0.
Datos:
pKps Ag2C2O4 = 8,0; pKps CaC2O4 = 10,0 pKps BaC2O4 = 12,2; pKps BaSO4 =
9,75; pKas H2C2O4 = 1,0 y 5,0, pKps AgCl = 10.
Respuestas
1- a) SAgCl = 2,02 x 10-5 M; SAg2CrO4 = 1,32 x 10-4 M
b) SAgCl = 1,41 x 10-5 M; SAg2CrO4 = 9,25 x 10-5 M
2- Uso NH4I. Se perdern 7,97 x 10-11 g.
3- S(Ag2SO4 en H2O) = 0,017 M; S(Ag2SO4 en K2SO4) = 2,24 x 10-3 M;
S(Ag2SO4 en AgNO3) = 2 x 10-5 M.
20 2do cuatrimestre de 2014
Qumica Analtica Serie de Problemas
4- [Pb2+] = 2,50 x 10-6 M [Ag+] = 2 x 10-15 M
5- % Ba precipitado = 100 % % Sr precipitado = 98,56 %
6- [Na2CO3] = 0,474 M
7- [H]mnima = 7,89 x 10-6 M
8- n NH4Cl mn = 4,47 x 10-2 mol
9- a) S = 9,49 x 10-6 M; b) S = 9,89 x 10-8 M; c) S = 9,95 x 10-6 M;
d) S = 9 x 10-8 M.
11- % C2Cl6 = 12,0 %
12- % DDT = 7,08 %
21 2do cuatrimestre de 2014
Vous aimerez peut-être aussi
- QA Problemas de QuímicaDocument22 pagesQA Problemas de Químicagr4ndeunicornPas encore d'évaluation
- Guia de Quimica Analitica e Instrumental 2018Document46 pagesGuia de Quimica Analitica e Instrumental 2018marito67% (3)
- Cuestionarios 1er ParcialDocument7 pagesCuestionarios 1er ParcialBrandon obando chavarriaPas encore d'évaluation
- Ejercicios VOLUMETRIADocument4 pagesEjercicios VOLUMETRIANALENY MORAYMA RUIZ CRUZPas encore d'évaluation
- 1 IntroduccionDocument16 pages1 IntroduccionesajuaniPas encore d'évaluation
- Serie 3. Equilibrio QuímicoDocument5 pagesSerie 3. Equilibrio QuímicolucianaramirezmalikPas encore d'évaluation
- Serie III (2019)Document3 pagesSerie III (2019)alejandro caztañonPas encore d'évaluation
- Guía Analítica 1Document4 pagesGuía Analítica 1Francisca Ignacia Espinoza CastroPas encore d'évaluation
- Errores P.propuestosDocument5 pagesErrores P.propuestosJUAN MIGUEL VELEZ GARCIAPas encore d'évaluation
- EspectrofotometriaDocument21 pagesEspectrofotometriaEdson DiazPas encore d'évaluation
- Preguntas Controles Quimica AnaliticaDocument13 pagesPreguntas Controles Quimica AnaliticaMaite Valentina Ríos OlavarríaPas encore d'évaluation
- Analítica Informe 1Document4 pagesAnalítica Informe 1Camilo OrtizPas encore d'évaluation
- Taller TermodinamicaDocument15 pagesTaller TermodinamicaCarolina LeonPas encore d'évaluation
- Guía de Ejercicios Primera ParteDocument4 pagesGuía de Ejercicios Primera ParteAnaPas encore d'évaluation
- III EXAMEN DE ANALISIS QUÍMICO (QU-244) Grupo 1Document2 pagesIII EXAMEN DE ANALISIS QUÍMICO (QU-244) Grupo 1CN Kenyu AlexPas encore d'évaluation
- Práctica 3 Quimica 2Document4 pagesPráctica 3 Quimica 2Abril1094Pas encore d'évaluation
- TAREA#1Document3 pagesTAREA#1Roberth Intriago CedeñoPas encore d'évaluation
- SinghDocument9 pagesSinghgino MamaniPas encore d'évaluation
- 100 Problemas Concentraciones Química AnalíticaDocument8 pages100 Problemas Concentraciones Química AnalíticaHabacuc Lorenzo Márquez50% (2)
- Taller Estequiometria y DisolucionesDocument5 pagesTaller Estequiometria y DisolucionesValenzuela C PazPas encore d'évaluation
- Reporte Practica 14 LEY DE LA CONSERVACIÓN DE LA MATERIADocument7 pagesReporte Practica 14 LEY DE LA CONSERVACIÓN DE LA MATERIAThe Edward WorldPas encore d'évaluation
- Ejercicios EspectrofotometriaDocument3 pagesEjercicios EspectrofotometriaJaviera M. Valdés100% (1)
- I Taller de Quimica Analitica GeneralDocument2 pagesI Taller de Quimica Analitica GeneralDaniel Hernandez PeñaPas encore d'évaluation
- Finales Quimica Analitica FBCB UNLDocument66 pagesFinales Quimica Analitica FBCB UNLRecoHitsPas encore d'évaluation
- Evaluacion Diagnostica Estequiometria 2º Medio Con SolucionarioDocument5 pagesEvaluacion Diagnostica Estequiometria 2º Medio Con SolucionarioValeria ApablazaPas encore d'évaluation
- 2bachillerato QuimicaDocument146 pages2bachillerato QuimicaIsel Nufio40% (5)
- 4° Medio QuímicaDocument7 pages4° Medio QuímicaMarcela YusefPas encore d'évaluation
- 2do Examen de Quimica Analitica CuantitativaDocument6 pages2do Examen de Quimica Analitica Cuantitativacarmen geraldoPas encore d'évaluation
- Guia Ejercicios Analisis Instrumental N1-2022RDocument6 pagesGuia Ejercicios Analisis Instrumental N1-2022RChasconaPas encore d'évaluation
- Análisis Químico - Practica #01-1 PDFDocument4 pagesAnálisis Químico - Practica #01-1 PDFJosué ZNPas encore d'évaluation
- Análisis Químico - Practica #01Document4 pagesAnálisis Químico - Practica #01FRONDPas encore d'évaluation
- Ejercicios Cálculos Elementales en QuímicaDocument6 pagesEjercicios Cálculos Elementales en Químicaisabella cajarPas encore d'évaluation
- Resolución 2 Parcial QAIIDocument6 pagesResolución 2 Parcial QAIIRo AguileraPas encore d'évaluation
- Cuestionario Practica 6Document5 pagesCuestionario Practica 6luis caisaluisaPas encore d'évaluation
- Guia de Ejercicios 2023 PDFDocument15 pagesGuia de Ejercicios 2023 PDFailuPas encore d'évaluation
- Ejercicios Resueltos. Unidad 8 - QuímicaDocument7 pagesEjercicios Resueltos. Unidad 8 - QuímicaMax ChazzPas encore d'évaluation
- Prueba II Esteq + Soluciones + GasesDocument5 pagesPrueba II Esteq + Soluciones + Gasespemp1996Pas encore d'évaluation
- Guia de Repaso y Conceptos BasicosDocument5 pagesGuia de Repaso y Conceptos BasicosVanina RecaldePas encore d'évaluation
- Modelos de Examenes Quimica AnaliticaDocument37 pagesModelos de Examenes Quimica AnaliticajoseluiswubPas encore d'évaluation
- Modelos de Exámenes QAIDocument46 pagesModelos de Exámenes QAIMiilenne100% (1)
- 05 - Guiìa #2, EstequiometriìaDocument13 pages05 - Guiìa #2, EstequiometriìavivithepPas encore d'évaluation
- Examen Diciembre 2012 PDFDocument2 pagesExamen Diciembre 2012 PDFmarinacocoPas encore d'évaluation
- Problemario 2Document5 pagesProblemario 2Chico Pedroza Ingrid AbigailPas encore d'évaluation
- Ejercicios y Problemas Capitulos 1,2,3Document5 pagesEjercicios y Problemas Capitulos 1,2,3Annie Diana Yumpiri AguilarPas encore d'évaluation
- Informe 5 ESTEQUIOMETRIADocument6 pagesInforme 5 ESTEQUIOMETRIAVictor Alessander Calle FernandezPas encore d'évaluation
- Bibp1 U1 A1 JochDocument4 pagesBibp1 U1 A1 JochJosue CruzPas encore d'évaluation
- Bibp1 U1 A1 JochDocument4 pagesBibp1 U1 A1 JochJosue CruzPas encore d'évaluation
- Ejercicios y Prob de Estequiometru00EDaDocument2 pagesEjercicios y Prob de Estequiometru00EDafioriPas encore d'évaluation
- Ejercicios UV Visible 2019Document4 pagesEjercicios UV Visible 2019Felipe Bayona100% (1)
- Practica 2Document5 pagesPractica 2Alex RamosPas encore d'évaluation
- Guia 1y2Document4 pagesGuia 1y2Ivan PortugalPas encore d'évaluation
- Calidad del agua para estudiantes de ciencias ambientalesD'EverandCalidad del agua para estudiantes de ciencias ambientalesPas encore d'évaluation
- Técnicas analíticas básicas: En el control de la calidad del agua según normatividadD'EverandTécnicas analíticas básicas: En el control de la calidad del agua según normatividadPas encore d'évaluation
- Ingeniería química. Soluciones a los problemas del tomo ID'EverandIngeniería química. Soluciones a los problemas del tomo IPas encore d'évaluation
- Modelado fenomenológico del proceso de combustión por difusión diéselD'EverandModelado fenomenológico del proceso de combustión por difusión diéselPas encore d'évaluation
- Problemas resueltos de Hidráulica de CanalesD'EverandProblemas resueltos de Hidráulica de CanalesÉvaluation : 4.5 sur 5 étoiles4.5/5 (7)
- Casos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSD'EverandCasos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSÉvaluation : 4.5 sur 5 étoiles4.5/5 (7)
- Obtención Del Ácido Bórico A Partir Del Mineral de UlexitaDocument93 pagesObtención Del Ácido Bórico A Partir Del Mineral de UlexitaBernie_Garcia__988650% (2)
- Valoraciones PotenciometricasDocument8 pagesValoraciones PotenciometricasAndres Felipe Franco HerreraPas encore d'évaluation
- Validacion y Verificacion de Metodos de PDFDocument8 pagesValidacion y Verificacion de Metodos de PDFAnonymous qKeDFDPas encore d'évaluation
- Validación de Métodos AnalíticosDocument184 pagesValidación de Métodos AnalíticosAnonymous qKeDFDPas encore d'évaluation
- Método Electrométrico para La Determinación de Boro en AguasDocument44 pagesMétodo Electrométrico para La Determinación de Boro en AguasAnonymous qKeDFDPas encore d'évaluation
- Boro en Siembra de UvasDocument25 pagesBoro en Siembra de UvasAnonymous qKeDFDPas encore d'évaluation
- Determinación de Microcantidades de Plata en Presencia de Plomo Utilizando Técnicas Volumétricas PDFDocument20 pagesDeterminación de Microcantidades de Plata en Presencia de Plomo Utilizando Técnicas Volumétricas PDFAnonymous qKeDFDPas encore d'évaluation
- Anexo 4 Guia DidacticaDocument35 pagesAnexo 4 Guia DidacticafakzimakyPas encore d'évaluation
- Guia Validación Metodos MicrobiologicosDocument17 pagesGuia Validación Metodos MicrobiologicosJose Alfredo DiazPas encore d'évaluation
- TD VILLERO SALAS Jose Maria PDFDocument334 pagesTD VILLERO SALAS Jose Maria PDFRenzo QuispePas encore d'évaluation
- Gluconato de CalcioDocument1 pageGluconato de CalcioLopez1980Pas encore d'évaluation
- 1 PBDocument20 pages1 PBYoelito LipaPas encore d'évaluation
- Validacion y Verificacion de Metodos de PDFDocument8 pagesValidacion y Verificacion de Metodos de PDFAnonymous qKeDFDPas encore d'évaluation
- 7-Equilibrios Acido Base IIDocument37 pages7-Equilibrios Acido Base IICristian Calcina GutierrezPas encore d'évaluation
- Dimensionamiento de SedimentadoresDocument56 pagesDimensionamiento de SedimentadoresMary100% (1)
- Validación para La Determinación de BoroDocument8 pagesValidación para La Determinación de BoroAnonymous qKeDFD100% (1)
- Determinación Volumétrica de Ag en Presencia de Cu, Ni y FeDocument11 pagesDeterminación Volumétrica de Ag en Presencia de Cu, Ni y FeRoque VirgilioPas encore d'évaluation
- Espesado Centrifugacion2Document13 pagesEspesado Centrifugacion2Jocelyn Karina Dorantes SolísPas encore d'évaluation
- Metodología para El Dimensionamiento de La Unidad de Espesamiento de Lodos en Las Plantas de Tratamiento de Agua PotableDocument130 pagesMetodología para El Dimensionamiento de La Unidad de Espesamiento de Lodos en Las Plantas de Tratamiento de Agua PotableAnonymous qKeDFDPas encore d'évaluation
- Síntesis de Ácido BóricoDocument4 pagesSíntesis de Ácido Bóricopaula murciaPas encore d'évaluation
- Compendium Final 25 de MayoDocument172 pagesCompendium Final 25 de MayoAlejandro Torres100% (1)
- Vida Util PDFDocument140 pagesVida Util PDFAnonymous qKeDFDPas encore d'évaluation
- Aplicación de La Microbiología Predictiva en La Determinación de La Vida Útil de Los AlimentosDocument15 pagesAplicación de La Microbiología Predictiva en La Determinación de La Vida Útil de Los AlimentosjudamoroPas encore d'évaluation
- Determinación de BoroDocument8 pagesDeterminación de BoroAnonymous qKeDFDPas encore d'évaluation
- Dimensionamiento de SedimentadoresDocument256 pagesDimensionamiento de SedimentadoresAnonymous qKeDFD100% (1)
- Informe FrackingDocument30 pagesInforme FrackingchristianPas encore d'évaluation
- Metodología Determinación Contaminación AtmosféricaDocument12 pagesMetodología Determinación Contaminación AtmosféricaAnonymous qKeDFDPas encore d'évaluation
- 143 (H2o B2o3)Document29 pages143 (H2o B2o3)Anonymous qKeDFDPas encore d'évaluation
- Monitoreo Calidad Del AireDocument9 pagesMonitoreo Calidad Del AireAnonymous qKeDFDPas encore d'évaluation
- Li2 (SO) 4 Na2SO4Document11 pagesLi2 (SO) 4 Na2SO4Anonymous qKeDFDPas encore d'évaluation
- HipotermiaDocument5 pagesHipotermiaMarvin VelasquezPas encore d'évaluation
- Actividad Individual FASE 3 Linda PalaciosDocument27 pagesActividad Individual FASE 3 Linda Palacioslinda giselld palacios rodriguezPas encore d'évaluation
- CASTILLA LA MANCHA Reserva A 2010 PDFDocument2 pagesCASTILLA LA MANCHA Reserva A 2010 PDFPianistasenderistaPas encore d'évaluation
- TERMOMETRIADocument12 pagesTERMOMETRIAAnonymous LNHGiVz8Pas encore d'évaluation
- Memoria Descriptiva de Los SS - HH Pronoei MalcaDocument5 pagesMemoria Descriptiva de Los SS - HH Pronoei MalcaAnonymous E7zQQpPas encore d'évaluation
- Determinacionde Aceites y Grasas en AguaDocument3 pagesDeterminacionde Aceites y Grasas en AguaJonathan Arley Valencia DurangoPas encore d'évaluation
- Ejercicios Eta 2 ExcelenciaDocument4 pagesEjercicios Eta 2 ExcelenciaAlfonso MendozaPas encore d'évaluation
- ProyectoDocument45 pagesProyectoErnesto gomezPas encore d'évaluation
- Poleas para Correas PlanasDocument1 pagePoleas para Correas PlanasCristïan SæzPas encore d'évaluation
- Ejercicio Resuelto FisicaDocument7 pagesEjercicio Resuelto FisicajuandavidPas encore d'évaluation
- Shou GangDocument16 pagesShou GangKatherin Carhuas QuispePas encore d'évaluation
- Mecanica de Fluidos 2Document8 pagesMecanica de Fluidos 2Julieth Fernanda VegaPas encore d'évaluation
- Construcción de Una Inyectora de PlásticosDocument5 pagesConstrucción de Una Inyectora de PlásticosLuis TorresPas encore d'évaluation
- Fisica Estatica 1Document1 pageFisica Estatica 1César Tipo RamosPas encore d'évaluation
- Dibujo de Proyecto - Tipos de LosasDocument9 pagesDibujo de Proyecto - Tipos de LosasYurelys MoyaPas encore d'évaluation
- 3 Tesis Sobre El Movimiento de BergsonDocument6 pages3 Tesis Sobre El Movimiento de BergsonClubS100% (1)
- Problemas Grupo-01 PDFDocument2 pagesProblemas Grupo-01 PDFHiro Manuel Lozada NisshiokaPas encore d'évaluation
- Informe Bioquimica Lab 3 I UnidadDocument22 pagesInforme Bioquimica Lab 3 I UnidadJhosleyArandaUlloa100% (1)
- Ferro NíquelDocument1 pageFerro Níquelpepitop18Pas encore d'évaluation
- La Luna No Tiene Cuatro FasesDocument2 pagesLa Luna No Tiene Cuatro FasesAnthony Abad VmPas encore d'évaluation
- El EstañoDocument10 pagesEl EstañoMiguel CoitaPas encore d'évaluation
- AntimonioDocument10 pagesAntimonioAnonymous Vw0azEPas encore d'évaluation
- Formulario de Metodos NumericosDocument2 pagesFormulario de Metodos NumericosJerson Torres CardenasPas encore d'évaluation
- 2.8.-FB5032 - QUIMICA INORGANICA 2019-Revisado Julio AutoguardadoDocument51 pages2.8.-FB5032 - QUIMICA INORGANICA 2019-Revisado Julio AutoguardadoAlejandra Gutierrez ʚïɞ100% (1)
- Configuracion ElectronicaDocument21 pagesConfiguracion ElectronicaPaty JamaicaPas encore d'évaluation
- Lenguaje Formal L' de PredicadosDocument4 pagesLenguaje Formal L' de PredicadosverlonPas encore d'évaluation
- Transformar A Latex 1Document14 pagesTransformar A Latex 1diego pintaPas encore d'évaluation
- Anteproyecto de Metodologia - Tejada Arbildo Daniel AgustinDocument38 pagesAnteproyecto de Metodologia - Tejada Arbildo Daniel AgustinDaniel A. TejadaPas encore d'évaluation
- Probabilidad CondicionalDocument7 pagesProbabilidad CondicionalVanneDelaRosaPas encore d'évaluation
- EXAMENDocument11 pagesEXAMENJose Luis TenPas encore d'évaluation