Académique Documents
Professionnel Documents
Culture Documents
Quimica Taller 1
Transféré par
bryggyttDescription originale:
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Quimica Taller 1
Transféré par
bryggyttDroits d'auteur :
Formats disponibles
1
QUIMICA 2
TALLER
1.- Definir:
Equilibrio qumico :
Sistema homogneo:
Stefany Caballero Castelo
2
QUIMICA 2
Sistema Heterogneo :
Stefany Caballero Castelo
3
QUIMICA 2
Constante de Equilibrio :
Stefany Caballero Castelo
4
QUIMICA 2
Principio de Le Chatelier :
Stefany Caballero Castelo
5
QUIMICA 2
2.- Cules son los factores que afectan el equilibrio dinmico?
3.- Escriba la expresin para la constante de equilibrio de las reacciones:
a. CO(g) + CL 2(g) COCL2(g)
b. H2(g) +I2(g) 2HI
c. CaCO3(g) CaO + CO2(G)
d. 2HCL(g) H2(g) + CL 2(g)
e. Na2SO4(ac) + BaCl2(ac) BaSO4(S) + 2NaCl(ac)
Stefany Caballero Castelo
6
QUIMICA 2
4.- Formule la ecuacin de la constante de equilibrio (Kc, Kp) Segn el caso para cada reaccin:
a) H2O H2O(g)
b) H2O(g) +CO( g) H2(g)+ CO2(g)
c) PCL5 PCl3(g) +Cl 2(g)
4.- Para la reaccin N2O4 2NO2 (g)
Las concentraciones de las sustancias en las mezclas en equilibrio a 25C son: [N2O4] = 4.27x10-1
mol/litro Cul es el valor de K a esta temperatura?
5.-El cido fluorhdrico en una solucin 0.400 M se encuentra ionizado 13.4% Calcular Kc para HF
Stefany Caballero Castelo
7
QUIMICA 2
6.-El valor de Kc para HI (g) se coloca en un recipiente de 1.0 litro y se le permite alcanzar el equilibrio a
450C. Cules son las concentraciones que las especies presentes cuando alcanza el equilibrio con
0.50 mol /lit de HI (g) .
7.- Para la reaccin H2 (g) + CO2 (g) H2O (g) + CO (g)
K es 0.771 a 750C, si 0.0100 moles de H2 y 0.100 moles CO2 se mezclan en un recipiente de 1 litro de
750C Cules son las concentraciones de todas las sustancias presentes en equilibrio?
Stefany Caballero Castelo
8
QUIMICA 2
8.- Calcule la concentracin de Ion Hidrogeno y el porcentaje de ionizacin a 25C de una solucin de cido
actico 0.102 M .La K para el cido es 1.76 x 10 -5 25 C
9.- En el equilibrio las presiones parciales se expresan en atmosfera, las concentraciones se expresan en
moles/litros, R es 0.08206 atm /K.Mol, T es la temperatura absoluta en K para la reaccin:
PCl5 (g) PCL3+ Cl2 (g)
Cul es el valor de n?
Cul es el valor de Kp?
10.- Para la reaccin H2 (g) + I2(g) 2HI(g)
a) Calcule el valor de n
b) Cul es el valor de Kp
Stefany Caballero Castelo
9
QUIMICA 2
12.- Para el sistema
2NO2 (g) 2NO(g) + O3(g)
13.- Ordenar las siguientes reacciones segn su tendencia creciente ha transcurrido a 298K y 1 atm. En
el sentido en el que estn escritas.
a) H2O(g) H2O(l) Kc = 782
b) F2(g) 2F(g) Kc = 4.9X 10-21
c) C(grafito)+O2(g) CO2(g) Kc = 1.3 x1053
d) H2(g) + C2H4(g) C2H6(g) Kc= 9.8X 1018}
14.- A una determinada temperatura y en fase gaseosa, el valor de la contante de equilibrio
correspondiente a la ecuacin: N2 +2O2 2NO2 es 100 cul de las siguientes ecuaciones tendrn
menor constante de equilibrio a la temperatura T?
a) 2NO2 N2 + 2O2
b) NO2 N2 + O2
c) O2 + N2 NO2
Stefany Caballero Castelo
10
QUIMICA 2
15.- Dadas las siguientes ecuaciones en las que A, B, C, D son metales hipotticos
a) A(g) + B+2 B(g) + A+2(ac) Kc = 1.2 x10 30 a 25C
b) B(s) + C+2 B (s) +C (s) Kc = 5.0 x 10-80 a 25C
c) D(g) + B+2 B(s) + D+2(ac) Kc = 2.5 x 10-20 a 25C
Cul de los metales A, C,D eliminara ms completamente a los iones B+2 de una disolucin en las
mismas condiciones ?
Stefany Caballero Castelo
11
QUIMICA 2
16.- Cual es el valor Kc para la reaccin:
N2 (g) + 3H2 (g) 2NH3 (g)
A 500C si el Kp es de 1.50 x10-5/atm -2 a esta temperatura
17.- Para la reaccin:
C(s) + CO2 (g) 2CO2 (g)
Kp en 167.5 atm a 1000C Cul es la presin parcial CO (g) es un sistema de equilibrio en el cual la
presin parcial de CO2 (g) es 0.100 atm?
Stefany Caballero Castelo
12
QUIMICA 2
Stefany Caballero Castelo
Vous aimerez peut-être aussi
- Problemas Equilibrio QuímicoDocument4 pagesProblemas Equilibrio QuímicoKerly West100% (1)
- PD Equilibrio QuimicoDocument2 pagesPD Equilibrio QuimicoUwOPas encore d'évaluation
- TALLER 6 Equilibrio PDFDocument2 pagesTALLER 6 Equilibrio PDFSAMUEL OROZCO RESTREPOPas encore d'évaluation
- 2 QEquilibrio ACTDocument28 pages2 QEquilibrio ACTIria Díaz BarrigaPas encore d'évaluation
- Problemas Equilibrio QuímicoDocument16 pagesProblemas Equilibrio QuímicogsofiaedithPas encore d'évaluation
- Cap5 Proble SolDocument8 pagesCap5 Proble SolAngel Fernan Pro 12Pas encore d'évaluation
- QuimicaDocument6 pagesQuimicaAndrea PintoPas encore d'évaluation
- Equilibrio Químico-PreguntasDocument10 pagesEquilibrio Químico-PreguntasStiven AlvarezPas encore d'évaluation
- (Completo) Ejercicios Sobre Equilibrio Químico PDFDocument35 pages(Completo) Ejercicios Sobre Equilibrio Químico PDFRuth Mayli100% (1)
- Guia Ejercicios EquilibrioDocument11 pagesGuia Ejercicios Equilibriojose contrerasPas encore d'évaluation
- Ejercicios Equilibrio QuimicoDocument21 pagesEjercicios Equilibrio Quimicoyaissa.jalilPas encore d'évaluation
- TP3 EQUILIBRIO QUIMICO I - 2020 Funda2Document5 pagesTP3 EQUILIBRIO QUIMICO I - 2020 Funda2fanny torresPas encore d'évaluation
- T Sem21 QuímicaDocument3 pagesT Sem21 QuímicaAllison Maravi RamosPas encore d'évaluation
- Tarea Grupal 2Document21 pagesTarea Grupal 2EsliDavidMolerosIngunza100% (1)
- PROBLEMAS DE EQUILIBRIO QUIMICO Tema 1 PDFDocument15 pagesPROBLEMAS DE EQUILIBRIO QUIMICO Tema 1 PDFabelardoPas encore d'évaluation
- Taller Resuelto Equilibrio Quimico 6Document15 pagesTaller Resuelto Equilibrio Quimico 6capl930100% (1)
- Ejercicios - EQUILIBRIO QUÍMICODocument5 pagesEjercicios - EQUILIBRIO QUÍMICOIrene HolmesPas encore d'évaluation
- Equilibrio Químico (Bloque III-2)Document13 pagesEquilibrio Químico (Bloque III-2)AngieCristinaBarreraPas encore d'évaluation
- Ejercicios PAU de Cinetica y EquilibrioDocument13 pagesEjercicios PAU de Cinetica y Equilibriofaltriquera100% (1)
- Equilibrio QuímicoDocument5 pagesEquilibrio QuímicoNerea OlmoPas encore d'évaluation
- Problemas de Parcial EQUILIBRIO QUÍMICODocument1 pageProblemas de Parcial EQUILIBRIO QUÍMICOSamantha HDzPas encore d'évaluation
- Ejercicios Propuestos - Equilibrio QuímicoDocument2 pagesEjercicios Propuestos - Equilibrio QuímicoWiliams KevinPas encore d'évaluation
- Guà A N° 9 Equilibrio Quà Mico (1496)Document2 pagesGuà A N° 9 Equilibrio Quà Mico (1496)Aguss ValentePas encore d'évaluation
- Equilibrio Químico (Bloque III-2)Document13 pagesEquilibrio Químico (Bloque III-2)Jonathan BrunoPas encore d'évaluation
- Taller Equilibrio QcoDocument4 pagesTaller Equilibrio QcoDani CVPas encore d'évaluation
- Ejercicios PAU de Cinetica y EquilibrioDocument14 pagesEjercicios PAU de Cinetica y Equilibriocarlos vallePas encore d'évaluation
- No 1 Equilibrio QuimicoDocument38 pagesNo 1 Equilibrio QuimicoDonnys ValenciaPas encore d'évaluation
- Serie QG IIDocument6 pagesSerie QG IIroy ito100% (2)
- 2da Práctica Virtual de Química General EQUILIBRIODocument4 pages2da Práctica Virtual de Química General EQUILIBRIOCami xdPas encore d'évaluation
- Guía de Seminarios 2022-2Document52 pagesGuía de Seminarios 2022-2Alvaro GamboaPas encore d'évaluation
- Tarea 10 - Equilibrio QuímicoDocument4 pagesTarea 10 - Equilibrio QuímicoCuau SuarezPas encore d'évaluation
- S5 Sol. Equivalencias IiDocument3 pagesS5 Sol. Equivalencias IiAriana adrioteroPas encore d'évaluation
- Equilibrio QcoDocument3 pagesEquilibrio QcoklingsorPas encore d'évaluation
- Hoja de Trabajo #1 EQUILIBRIO QUIMICODocument2 pagesHoja de Trabajo #1 EQUILIBRIO QUIMICObarbathos0% (1)
- Equilibrio QuímicoDocument5 pagesEquilibrio QuímicoJosé Carlos Torres VarillasPas encore d'évaluation
- Hoja 2 EquilibrioDocument4 pagesHoja 2 EquilibrioA A Asdasd DfPas encore d'évaluation
- Taller 5.0 - Equilibrio QuìmicoDocument4 pagesTaller 5.0 - Equilibrio QuìmicoJL SilvaPas encore d'évaluation
- Mentoría Unidad 16-Equilibrio JSTR 2020 - v2Document4 pagesMentoría Unidad 16-Equilibrio JSTR 2020 - v2Lesly Yohana Carmona SarabiaPas encore d'évaluation
- Ejercicios Sobre Equilibrio Quimico. PrimeraDocument3 pagesEjercicios Sobre Equilibrio Quimico. Primeragjra1982100% (1)
- Equilibrio Químico 13-14 PDFDocument4 pagesEquilibrio Químico 13-14 PDFAngelaPas encore d'évaluation
- 9 - Unidad 8Document6 pages9 - Unidad 8LGM proPas encore d'évaluation
- Guia de PROBLEMAS 2da PARTE - 2022Document66 pagesGuia de PROBLEMAS 2da PARTE - 2022rPas encore d'évaluation
- Equilibrio GaseosoDocument2 pagesEquilibrio GaseosoEnriqueGarridoPas encore d'évaluation
- Equilibrio Quã Mico - EBAU 4Document18 pagesEquilibrio Quã Mico - EBAU 4P M RPas encore d'évaluation
- P 5 - Equilibrio Quimico MarcelaDocument3 pagesP 5 - Equilibrio Quimico MarcelaDiego MiguelPas encore d'évaluation
- Taller Equilibrio - QuimicoDocument2 pagesTaller Equilibrio - QuimicoMaria Camila Alvarez100% (1)
- Taller Equilibrio QuimicoDocument2 pagesTaller Equilibrio QuimicoMaria Camila AlvarezPas encore d'évaluation
- HE Equilibrio QuímicoDocument1 pageHE Equilibrio QuímicoVivi TambascoPas encore d'évaluation
- Semana N°09 Quimica DocentesDocument4 pagesSemana N°09 Quimica DocentesLuis felipe Martínez RomanPas encore d'évaluation
- Ejercicios DW Equilibrio QuimicoDocument2 pagesEjercicios DW Equilibrio Quimicoantonio santiago hermitañoPas encore d'évaluation
- Guía de Seminarios 2024-1Document56 pagesGuía de Seminarios 2024-1Piero Carlos Tacsa QuispePas encore d'évaluation
- Transferencia S15 ABDocument5 pagesTransferencia S15 ABJuan José Aldana CarranzaPas encore d'évaluation
- 4.-HOJA DE TRABAJO Equilibrio QuímicoDocument1 page4.-HOJA DE TRABAJO Equilibrio QuímicoCesar Erick Sotomayor VilchezPas encore d'évaluation
- Guía de Seminarios 2023-1Document56 pagesGuía de Seminarios 2023-1DanuskaPas encore d'évaluation
- Tarea 2-Ejercicios Sobre Equilibrio QuímicoDocument8 pagesTarea 2-Ejercicios Sobre Equilibrio QuímicocarmenPas encore d'évaluation
- GUIA N°2-Equilibrio Quimico-Factores Que ModificanDocument5 pagesGUIA N°2-Equilibrio Quimico-Factores Que ModificanJuan GervasoniPas encore d'évaluation
- Trabajo Práctico Nº4 FisicoquímicaDocument3 pagesTrabajo Práctico Nº4 FisicoquímicaPaez LamaPas encore d'évaluation
- Ejercicios y Problemas Sobre Equilibrio QuímicoDocument1 pageEjercicios y Problemas Sobre Equilibrio QuímicoMario MartinPas encore d'évaluation
- Problemas resueltos de Hidráulica de CanalesD'EverandProblemas resueltos de Hidráulica de CanalesÉvaluation : 4.5 sur 5 étoiles4.5/5 (7)
- Ope 2 ExtraccionDocument34 pagesOpe 2 Extraccionbryggytt0% (1)
- Convergencia AceleradaDocument3 pagesConvergencia AceleradabryggyttPas encore d'évaluation
- Laboratorio Metalurgia ExtractivaDocument12 pagesLaboratorio Metalurgia ExtractivabryggyttPas encore d'évaluation
- Ope 2 Extraccion LaedDocument13 pagesOpe 2 Extraccion LaedbryggyttPas encore d'évaluation
- Balance Macroscopico de MateriaDocument10 pagesBalance Macroscopico de MateriabryggyttPas encore d'évaluation
- Ejemplos de Sistemas de ControlDocument2 pagesEjemplos de Sistemas de ControlbryggyttPas encore d'évaluation
- Cascara de HuevoDocument4 pagesCascara de HuevobryggyttPas encore d'évaluation
- Degradación de Polietileno de Baja Densidad Por Asociaciones Microbianas Autora: Patricia Noemí Martínez LoveraDocument6 pagesDegradación de Polietileno de Baja Densidad Por Asociaciones Microbianas Autora: Patricia Noemí Martínez LoverabryggyttPas encore d'évaluation
- Matriz de Perfil de PuestoDocument4 pagesMatriz de Perfil de PuestobryggyttPas encore d'évaluation
- TH-F-01 Perfil de PuestoDocument4 pagesTH-F-01 Perfil de PuestobryggyttPas encore d'évaluation
- Iperc Base - Ssoma - MacdesaDocument24 pagesIperc Base - Ssoma - MacdesabryggyttPas encore d'évaluation
- Matriz IPERCDocument3 pagesMatriz IPERCbryggyttPas encore d'évaluation
- Transformaciones en Estado SolidoDocument24 pagesTransformaciones en Estado SolidobryggyttPas encore d'évaluation
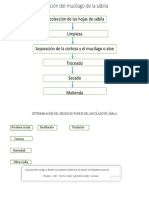
- Obtención Del Mucílago de La SábilaDocument2 pagesObtención Del Mucílago de La SábilabryggyttPas encore d'évaluation
- Nitracion de BencenoDocument9 pagesNitracion de BencenobryggyttPas encore d'évaluation
- Cuestionario Residuos SolidosDocument20 pagesCuestionario Residuos SolidosbryggyttPas encore d'évaluation
- Laboratorio de AmbientalDocument2 pagesLaboratorio de AmbientalbryggyttPas encore d'évaluation
- Tecnicas de Reclutamiento EficacesDocument13 pagesTecnicas de Reclutamiento EficacesbryggyttPas encore d'évaluation
- Qué Son Las Competencias TransversalesDocument40 pagesQué Son Las Competencias TransversalesbryggyttPas encore d'évaluation
- Operaciones Unitarias IIDocument9 pagesOperaciones Unitarias IIbryggyttPas encore d'évaluation
- Problemas de Rectas Paralelas y Perpendiculares (En El Plano)Document10 pagesProblemas de Rectas Paralelas y Perpendiculares (En El Plano)Edgar Abarca QuezadaPas encore d'évaluation
- Informe 1Document11 pagesInforme 1Emerson Chavez HuanshaPas encore d'évaluation
- Codigos Error Canon Ir 1600 o 2000Document4 pagesCodigos Error Canon Ir 1600 o 2000jlsfarinas100% (1)
- 116 Examen Sustitutorio Modulo Vii, Viii y IxDocument2 pages116 Examen Sustitutorio Modulo Vii, Viii y Ixoscarariagna100% (1)
- Ciclo RankineDocument15 pagesCiclo RankineAnonymous tofQlvPas encore d'évaluation
- Resolución Ministerial 0079 2023 MidagriDocument3 pagesResolución Ministerial 0079 2023 MidagriMARIA AVALOSPas encore d'évaluation
- EdafosferaDocument23 pagesEdafosferaFer MartellPas encore d'évaluation
- Trabajo en EquipoDocument12 pagesTrabajo en EquipoFelipe Trujillo GomezPas encore d'évaluation
- Interpretacion ConductorDocument8 pagesInterpretacion ConductorAgp SolucionesPas encore d'évaluation
- Buzones Tipicos 1Document6 pagesBuzones Tipicos 1Lucia JuanaPas encore d'évaluation
- Planificación Anual - Biología 2° Año - Ciclo 2020 - Profesora Jimena RomanoDocument4 pagesPlanificación Anual - Biología 2° Año - Ciclo 2020 - Profesora Jimena Romanojimena romanoPas encore d'évaluation
- ENFOQUESDocument3 pagesENFOQUESHector Armando Vargas FigueroaPas encore d'évaluation
- CITADODocument21 pagesCITADOFel GonzalezPas encore d'évaluation
- 08 Diseño Sismorresistente Sistemas Armonicos 1GLDocument14 pages08 Diseño Sismorresistente Sistemas Armonicos 1GLAlejandro Cortijo CastilloPas encore d'évaluation
- Actividad de Puntos Evaluables - Escenario 2 Ciencias Basicas Probabilidad Grupo b01Document4 pagesActividad de Puntos Evaluables - Escenario 2 Ciencias Basicas Probabilidad Grupo b01leoniPas encore d'évaluation
- Caso Worlwide Chemical CompanyDocument2 pagesCaso Worlwide Chemical CompanyLucho DomínguezPas encore d'évaluation
- Grupo 2 Primer ParcialDocument18 pagesGrupo 2 Primer ParcialAriel CalbertoPas encore d'évaluation
- Blog Diagnostico FinancieroDocument3 pagesBlog Diagnostico FinancieroLucas MolinaPas encore d'évaluation
- Nicomar Propc 1000Document1 pageNicomar Propc 1000José Luis Gualotuña P.0% (1)
- Evaluacion de La Inteligencia Tarea VDocument8 pagesEvaluacion de La Inteligencia Tarea Vnenyr_2Pas encore d'évaluation
- PDF Boletaeb01 5220607862312Document1 pagePDF Boletaeb01 5220607862312Rolando Herrera MatosPas encore d'évaluation
- Marco Teorico Pendulo SimpleDocument2 pagesMarco Teorico Pendulo SimplePaola Andrea Colque GonzalesPas encore d'évaluation
- Hambre Traduccion de Kirsti Baggethun - Knut HamsunDocument134 pagesHambre Traduccion de Kirsti Baggethun - Knut HamsunMauro Rojas33% (3)
- Información Preinscripción: Fecha Versión: 5/06/2014 Versión: 0.1 Página: 1 de 2 Código: 01Document2 pagesInformación Preinscripción: Fecha Versión: 5/06/2014 Versión: 0.1 Página: 1 de 2 Código: 01Eliecer Manuel Noble GuerraPas encore d'évaluation
- Guia - Planes de Saneamiento BasicoDocument6 pagesGuia - Planes de Saneamiento BasicoLuz Katerine Martinez CrespoPas encore d'évaluation
- Proceso de Adquisición de Materiales 8 02 2023Document1 pageProceso de Adquisición de Materiales 8 02 2023gerson chavarroPas encore d'évaluation
- Lección #5 PHA HAZID HAZOPDocument36 pagesLección #5 PHA HAZID HAZOPSSOMA AlmaqPas encore d'évaluation
- Guía PrimeraDocument29 pagesGuía PrimeraPao CarreroPas encore d'évaluation
- Tema 5 Ingind2Document21 pagesTema 5 Ingind2Laura CeciliaPas encore d'évaluation
- Programa de Cursos - ICCAEDocument4 pagesPrograma de Cursos - ICCAEEmerson GomezPas encore d'évaluation