Académique Documents
Professionnel Documents
Culture Documents
Transféré par
Karina OchoaCopyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Transféré par
Karina OchoaDroits d'auteur :
Formats disponibles
https://www.thrombosisadviser.com/es/trombosis/cascada-de-coagulacion/index.
php
La cascada de coagulación
Resumen del contenidoEl proceso de coagulación que lleva a la hemostasia consiste
en un conjunto complejo de reacciones de proteasas en el que
participan aproximadamente 30 proteínas diferentes. Estas reacciones convierten fibrinógeno en fibrina,
la cual, con las plaquetas, forma un trombo estable. Se han
propuesto varios modelos de cascada de coagulación, incluyendo el modelo de
la vía intrínseca y extrínseca, y el más reciente modelo celular
de la coagulación. A partir de estos modelos, la investigación en
curso ha dilucidado otros componentes del proceso de coagulación, incluyendo micropartículas
y la proteína selectina P. Se denomina trombofilia a un desequilibrio
heredado o adquirido en el sistema de coagulación que lleva a
un mayor riesgo de trombosis. Aproximadamente uno de cada tres pacientes
con tromboembolia venosa (ETV) tiene una trombofilia heredada.
La cascada de coagulaciónBookmark this page
El proceso de coagulación que lleva a la hemostasia consiste en un conjunto complejo de reacciones
de proteasas en el que participan aproximadamente 30 proteínas diferentes. [22] Estas reacciones convierten fibrinógeno,
una proteína soluble, en filamentos insolubles de fibrina, que, con las plaquetas, forman un trombo
estable.
Se han propuesto varios modelos de cascada de coagulación, incluyendo el modelo de la vía intrínseca
y extrínseca, y el más reciente modelo celular de la coagulación.
El modelo de la vía intrínseca y extrínseca
El modelo de la vía intrínseca y extrínseca. [19] La vía extrínseca se considera que es
la responsable de la generación inicial del factor X activado (factor Xa), mientras que la
vía intrínseca lleva a la amplificación de la generación del factor Xa. El factor Xa
desempeña un papel central en la cascada de coagulación debido a que ocupa un punto
en el que convergen la vía intrínseca y la extrínseca.
El modelo celular de la coagulación
El modelo celular de la coagulación explica mejor el mecanismo de la hemostasia en vivo e
incluye las importantes interacciones entre las células directamente implicadas en la hemostasia (esto es, células
portadoras de factor tisular [FT] y plaquetas) y los factores de coagulación. Este modelo representa
con mayor precisión la interacción entre la actividad celular y las proteínas de la coagulación
que conduce a la formación de trombos y a la hemostasia. [23]
El modelo celular de la coagulación identifica las membranas de las células portadoras de factor tisular
y de las plaquetas como las zonas en donde se produce la activación de factores
de coagulación específicos. [23] Este modelo describe un proceso en tres fases:
° Iniciación
° Amplificación
° Formación de fibrina
La iniciación ocurre tras una lesión vascular, cuando las células portadoras de factor tisular se unen
al factor VII y lo activan. Esto lleva a la producción de una pequeña cantidad
de trombina que, a continuación, activa las plaquetas y los cofactores durante la fase de
amplificación. El complejo protrombinasa (que comprende el factor Xa y los cofactores unidos a las
plaquetas activadas) es responsable de la explosión de la producción de trombina que lleva a
la tercera fase de formación de fibrina.
El paso final de la serie de reacciones de proteasas que lleva a la formación de
trombos, supone la conversión de la proteína soluble fibrinógeno en filamentos insolubles de fibrina por
la trombina. La trombina también activa el factor XIII, que estabiliza el trombo entrecruzando la
fibrina. La malla de fibrina resultante atrapa y mantiene los componentes celulares del trombo (plaquetas
y/o eritrocitos). [19]
https://www.thrombosisadviser.com/es/trombosis/cascada-de-coagulacion/index.php
El papel central del factor Xa en la formación
del trombo
El factor Xa desempeña un papel central en el proceso de coagulación que lleva a la
hemostasia, tanto en el antiguo modelo extrínseco/intrínseco como en el más reciente modelo celular de
la coagulación.El factor Xa, con el factor V activado (factor Va) como cofactor, propaga la
coagulación mediante la conversión de protrombina (factor II) en trombina (factor IIa) [23] El factor
Xa es un sitio crucial de amplificación en el proceso de coagulaciónUna molécula de factor
Xa cataliza la formación de aproximadamente 1.000 moléculas de trombina [24] El desarrollo de medicamentos
que inhiban el factor Xa es, por tanto, un área atractiva de investigación farmacéutica. [25]
Fibrinólisis: restaurar el flujo sanguíneo
La fibrinólisis es el proceso que disuelve la fibrina. Al disolver la fibrina, la fibrinólisis lleva
a la disolución del trombo.
El plasminógeno es el precursor de la plasmina, que rompe la fibrina en el trombo. Durante
la formación inicial del trombo, los activadores del plasminógeno están inhibidos. Una vez se ha
restablecido la integridad estructural del vaso sanguíneo, las células endoteliales empiezan a secretar activadores del
plasminógeno tisular para comenzar a disolver el trombo. La fibrinólisis debe producirse para que se
restablezca el flujo sanguíneo normal.
Los medicamentos que convierten plasminógeno en plasmina se utilizan para tratar trastornos trombóticos agudos potencialmente mortales
como el infarto de miocardio (IM) y el accidente cerebrovascular isquémico. [26]
Más allá de las células y los factores de
coagulación: el papel de las micropartículas y la
selectina P
La investigación en curso ha dilucidado otros componentes del proceso de coagulación. Estos componentes incluyen las
micropartículas y la selectina P.
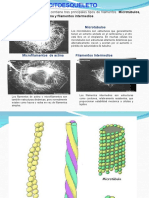
Las micropartículas son vesículas de forma irregular más pequeñas que las plaquetas (esto es, con un
diámetro inferior a 1 μm). Estas vesículas surgen de la membrana plasmática de las células
del torrente circulatorio durante la activación celular, la muerte celular programada o la exposición a
fuerzas de cizallamiento. [27] La selectina P es una molécula de adhesión celular que se
encuentra en la superficie interior de los vasos sanguíneos y en las plaquetas activadas. [28]
Tanto las micropartículas como la selectina P promueven la trombosis durante la fase de amplificación de
la coagulación. [28] Durante la formación del trombo, las plaquetas se acumulan en el sitio
de la lesión vascular, se activan y expresan selectina P. [28] La selectina P, a
su vez, se une a las micropartículas portadoras de factor tisular. Uno de los efectos
de esta unión es hacer que dichas micropartículas se unan a las plaquetas activadas a
través de la selectina P unida a las plaquetas. El factor tisular de las micropartículas
se une entonces al factor VII y lo activa. Las micropartículas portadoras de factor tisular
están también implicadas en la trombosis asociada a la diabetes, el síndrome metabólico, tumores malignos
específicos (p. ej., cáncer de colon, páncreas, mama, ovario y pulmón) y trastornos inflamatorios y
hematológicos. [27]
Desequilibrios en el sistema de coagulación
La «trombofilia» es un desequilibrio heredado o adquirido en el sistema de coagulación que conlleva un
mayor riesgo de trombosis.
La trombofilia puede esperarse en:
° Pacientes con ETV recurrente o ETV potencialmente mortal
° Pacientes de
° Pacientes con ETV y antecedentes familiares de ETV
° Pacientes que desarrollan ETV sin factores aparentes que expongan al riesgo
° Mujeres que experimentan múltiples abortos espontáneos o muertes fetales [
https://www.thrombosisadviser.com/es/trombosis/cascada-de-coagulacion/index.php
Aproximadamente uno de cada tres pacientes con ETV tiene trombofilia heredada. [30]
° Las formas comunes implican mutaciones genéticas que afectan al factor V (conocido como factor V Leiden)
° y a la protrombina (factor II)
° Entre las causas poco comunes, se incluyen las deficiencias de los anticoagulantes naturales proteína C, proteína
° S y antitrombina [
Artículos seleccionados
19 Colman RW, Clowes AW, George JN et al. Overview of hemostasis. In Hemostasis and Thrombosis:
Basic Principles and Clinical Practice. 5th edn. Colman RW, Clowes AW, George JN et al.
(editors). Philadelphia: Lippincott, Williams & Wilkins; 2006. p. 1–16.
22 Colman RW, Clowes AW, George JN et al. Overview of coagulation, fibrinolysis and their regulation.
In Hemostasis and Thrombosis: Basic Principles and Clinical Practice. 5th edn. Colman RW, Clowes AW,
George JN et al. (editors). Philadelphia: Lippincott, Williams & Wilkins; 2006. p. 17–20.
23 Hoffman M, Monroe DM. Coagulation 2006: a modern view of hemostasis. Hematol Oncol Clin North
Am 2007;21:1–11.
24 Mann KG, Brummel K, Butenas S. What is all that thrombin for? J Thromb Haemost
2003;1:1504–1514.
25 Turpie AGG. Oral, direct Factor Xa inhibitors in development for the prevention and treatment of
thromboembolic diseases. Arterioscler Thromb Vasc Biol 2007;27:1238–1247.
26 Mackman N. Triggers, targets and treatments for thrombosis. Nature 2008;451:914–918.
27 Davizon P, Lopez JA. Microparticles and thrombotic disease. Curr Opin Hematol 2009;16:334–341.
28 Furie B, Furie BC. Mechanisms of thrombus formation. N Engl J Med 2008;359:938–949.
29 Seligsohn U, Lubetsky A. Genetic susceptibility to venous thrombosis. N Engl J Med 2001;344:1222–1231.
30 Merli GJ. Pathophysiology of venous thrombosis, thrombophilia, and the diagnosis of deep vein thrombosis-pulmonary embolism
in the elderly. Clin Geriatr Med 2006;22:75–92, viii-ix.
Vous aimerez peut-être aussi
- Proteínas de La LecheDocument16 pagesProteínas de La LecheManuel AlejandroPas encore d'évaluation
- Citoesqueleto y Motilidad Celular. Filamentos 14-07-2016Document63 pagesCitoesqueleto y Motilidad Celular. Filamentos 14-07-2016Beto BarcelonaPas encore d'évaluation
- Tp01 de Bioquímica UNLPDocument5 pagesTp01 de Bioquímica UNLPAlyson GuilhermePas encore d'évaluation
- Wuolah-Free-Tema 6 - CitoesqueletoDocument8 pagesWuolah-Free-Tema 6 - CitoesqueletoCarlos MartínezPas encore d'évaluation
- Tema 2 Aminoácidos y Proteínas 2023 4 CRDocument52 pagesTema 2 Aminoácidos y Proteínas 2023 4 CRrosbeidyPas encore d'évaluation
- Taller 3Document4 pagesTaller 3Carolina Cumbicus TorresPas encore d'évaluation
- Expresión Génica UADEDocument10 pagesExpresión Génica UADEMilagros CastromanPas encore d'évaluation
- Blgo. Ms. Pablo Chuna MogollónDocument24 pagesBlgo. Ms. Pablo Chuna MogollónAnonymous aeyMBcNDfPas encore d'évaluation
- Tema4.3 CitoesqueletoDocument38 pagesTema4.3 CitoesqueletoJose BarajasPas encore d'évaluation
- Diapositiva Mesa - A3Document48 pagesDiapositiva Mesa - A3FABIAN RODAS MENDOZAPas encore d'évaluation
- Hemostasia y TrombosisDocument61 pagesHemostasia y TrombosisLorena ZepedaPas encore d'évaluation
- Biomoleculas SIV "A"Document35 pagesBiomoleculas SIV "A"Sergio Ivan ViramontesPas encore d'évaluation
- 1151 Problemas Proteinas1Document2 pages1151 Problemas Proteinas1magyPas encore d'évaluation
- Lectura Obligatoria de Semana 12Document55 pagesLectura Obligatoria de Semana 12Mariabel Garcia CanalesPas encore d'évaluation
- Práctica de Aula Nº13 ProteinasDocument3 pagesPráctica de Aula Nº13 ProteinasFer VrgsNyrPas encore d'évaluation
- Tema 24. Plaquetas. Hemostasia y CoagulaciónDocument7 pagesTema 24. Plaquetas. Hemostasia y Coagulaciónmontserrat collaoPas encore d'évaluation
- IsoenzimasDocument4 pagesIsoenzimasRaziel CabreraPas encore d'évaluation
- Graficos Cinetica EnzimaticaDocument6 pagesGraficos Cinetica EnzimaticaGEYSEEL AGUILERAPas encore d'évaluation
- Principios de Lehninger Del Banco de Pruebas de Bioquímica Capítulo 4Document9 pagesPrincipios de Lehninger Del Banco de Pruebas de Bioquímica Capítulo 4BRYAN ALEXIS ORDOÑEZ RECINOSPas encore d'évaluation
- Receptores EsteroideosDocument6 pagesReceptores Esteroideosaismara bojorquezPas encore d'évaluation
- Resumen CitoesqueletoDocument14 pagesResumen CitoesqueletoAmaury de la CruzPas encore d'évaluation
- Los Factores Generales de Transcripción Del ARN Polimerasa IIDocument21 pagesLos Factores Generales de Transcripción Del ARN Polimerasa IIcsos csosPas encore d'évaluation
- Transportadores de Glucosa e Insulina (Esquemas)Document8 pagesTransportadores de Glucosa e Insulina (Esquemas)ROGGER CERNAPas encore d'évaluation
- Las Enzimas Clase-1Document37 pagesLas Enzimas Clase-1Kate ́s FilmPas encore d'évaluation
- El CitoesqueletoDocument18 pagesEl CitoesqueletoStephanie Soria SanchezPas encore d'évaluation
- Modificaciones PostraduccionalesDocument15 pagesModificaciones PostraduccionalesDaniel Ovando100% (1)
- Citoesqueleto: FuncionesDocument14 pagesCitoesqueleto: Funcioneskarina ramos100% (1)
- FISIOLOGIA DE LA HEMOSTASIA - Cap LibroDocument17 pagesFISIOLOGIA DE LA HEMOSTASIA - Cap LibroAdriana Lucía LópezPas encore d'évaluation
- TEMA 2bDocument67 pagesTEMA 2bJaime SnchzPas encore d'évaluation
- Coagulación PDFDocument19 pagesCoagulación PDFLuis CarrizoPas encore d'évaluation