Académique Documents
Professionnel Documents
Culture Documents
EJERCICIOS - BRAYAN Fisiocquimica
Transféré par
Abraham S. AroDescription originale:
Titre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
EJERCICIOS - BRAYAN Fisiocquimica
Transféré par
Abraham S. AroDroits d'auteur :
Formats disponibles
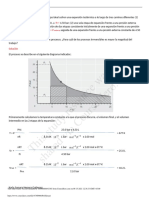
11.
Las densidades en gramos por centímetro cúbico del éter metílico líquido y
gaseoso, a distintas temperaturas, son las siguientes:
Tabla.- Densidad del éter metílico líquido y gaseoso a diferentes temperaturas
ºC 30 50 70 100 120
ρl, (g/L) 0,6455 0,6116 0,5735 0,4950 0,4040
ρl, (g/L) 0,0142 0,0241 0,0385 0,0810 0,1465
Calcular la densidad y temperatura critica:
Densidad y temperatura corregida:
ºK 303,15 K 323,15 K 343,15 K 373,15 K 393,15 K
ρl, (g/cm3) 6,45 x 10-4 6,116 x 10-4 5,735 x 10-4 4,95 x 10-4 4,04 x 10-4
ρl, (g/cm3) 1,42 x 10-5 2,41 x 10-5 3,85 x 10-5 8,1 x 10-5 1,465 x 10-4
Densidad media:
ºK 303,15 K 323,15 K 343,15 K 373,15 K 393,15 K
ρm, (g/cm3) 3,2985x10-4 3,1785x10-4 3,06x10-4 2,88x10-4 2,7525x10-4
Valores de A y B:
A = 5,1326 x10-4
B= -6,0456 x10-7
o Temperatura Critica:
ρm = ρ0 – aTC
o Densidad:
ρm = m / Vc
ρm =
12. Dosis altas de calcio pueden ayudar a las mujeres que sufren de problemas
agudos durante la menstruación. La dosis diaria recomendada es de 0,6 a 1,3 g de
calcio. El porcentaje de calcio presente en la leche es 0,27%. Si esta fuera la única
fuente de calcio, ¿cuántos mililitros de leche diarios se tendría que tomar una
mujer para ingerir el mínimo de la dosis recomendada? La densidad de la leche
es de 0,97 g/mL.
DATOS:
o 0,6 – 1,3 g Ca
o Leche 0,27%
o Densidad 0,97 g/ml
13. Una forma de obtener alcohol etílico, C2H5OH, es fermentando frutas que
contengan glucosa, C6H12O6. La reacción de fermentación es la siguiente:
𝐶6𝐻12𝑂6→𝐶2𝐻5𝑂𝐻+𝐶𝑂2
¿Qué masa de alcohol etílico se puede obtener con la fermentación de 3 kg de
manzanas? Las manzanas contienen 13% de glucosa.
DATOS:
o 3 kg manzanas
o 13 % de glucosa en las manzanas
o Masa de alcohol etílico: ¿?
3 kg = 3000 g
3000 g 100%
Xg 13% Xg = 390 g
𝐶6𝐻12𝑂6 → 2𝐶2𝐻5𝑂𝐻+ 2𝐶𝑂2 Balanceo de la reacción.
180 g/mol 𝐶6𝐻12𝑂6 92 g/mol 𝐶2𝐻5𝑂𝐻
390 g 𝐶6𝐻12𝑂6 X g/mol 𝐶2𝐻5𝑂𝐻 199,3 g 𝐶2𝐻5𝑂𝐻
Obtendría 199,3 g de alcohol etílico de 3 kg de manzanas.
APORTE: BRAYAN QUISPE ARAPA CUI: 20162837
14. Las mascarillas de oxígeno que se utilizan en situaciones de emergencia
contienen KO2 (superóxido de potasio) que reacciona con el CO2 y el agua del
aire exhalado para dar oxígeno, según la siguiente reacción:
𝐾𝑂2+𝐻2𝑂+𝐶𝑂2→𝐻𝐶𝑂3+𝑂2
Considerando que una persona exhala 0,95 kg de CO2 por día y que una mascarilla
contiene 100 g de KO2, ¿cuántos minutos podrá ser utilizada?
DATOS:
o 0,95 kg CO2 = 950 g CO2
o 100 g KO2
o Minutos: ¿?
20𝐾𝑂2 + 𝐻2𝑂 + 20𝐶𝑂2→ 20 K𝐻𝐶𝑂3 + 10𝑂2
1421,942 g/mol 𝐾𝑂2 880, 19 g/mol 𝐶𝑂2
100 g 𝐾𝑂2 X g/mol 𝐶𝑂2 61,90055572 g 𝐶𝑂2
1 dia = 1440 min
950 g CO2 1440 min
61,90055572 g 𝐶𝑂2 X min 93,82 min 94 min
Esta mascarilla podrá ser utiliza alrededor de 94 min.
15. El ahumado es una técnica utilizada en la conservación de alimentos debido a
la acción secante y bactericida del humo. Uno de los componentes del humo es
el formaldehído (CH2O), que se sospecha es carcinógeno. ¿Cuál es la presión
parcial de 1,2 g de formaldehído, que están contenidos en 4,5 L de humo a
temperatura y presión estándar?
DATOS:
o 4,5 L
o 273,15K
o 1 atm
o Presión Parcial de formaldehido: ¿?
PV 1 atm ×4,5 L
nmezcla = RT atmxL 0,20 mol
0,082 X273,15K
molxK
Pformaldehido = X formaldehido x Pmezcla
Pformaldehido Presión Parcial
X formaldehido Fracción Mol
Pmezcla Presión Total
masa 1,2 g
nmol formaldehido = Peso Molecular g = 0,04 mol
30
mol
nformaldehido 0,04 mol
X formaldehido = nmezcla
0,20 mol
= 0,2 mol
El formaldehido contribuye a la presión total que es 1 atm, con 0,2
atm y los demás gases con 0,8 atm.
16. (a) ¿Podrían 25 g de gas argón en un tanque de 1,5 dm3 de volumen ejercer
una presión de 2,0 bar a 30ºC si se comportara como un gas ideal? Si no, ¿qué
presión ejercería? (b) ¿Qué presión ejercería si se comportara como un gas de
van der Waals? a = 1,337 dm6 atm mol-2 , b = 3,20 x10-2 dm3 mol
DATOS:
o 25 g Ar
o 40 g/mol peso molecular Ar
o 2,0 bar = 1,97 atm
o 1,5 dm3 = 1,5 L
o 30ºC = 303,15 K
Parte “A”
o PV = nRT
APORTE: BRAYAN QUISPE ARAPA CUI: 20162837
25 g atm L
o 1,97 atm x 1,5L = g x 0,082 X 303,15 K
40 mol K
mol
atm L
o P x 1,5L = 0,625 mol x 0,082 mol K
X 303,15 K
o P = 10,36 atm
No ejercería ya que la presión es más alta estimando lo
obtenido.
La presión ejercida es de 10,36 atm.
Parte “B”
𝑎𝑛2
(𝑃 + ) (𝑉 − 𝑛𝑏) = 𝑛𝑅𝑇
𝑉2
1,337 𝑑𝑚6 atm 𝑚𝑜𝑙 −2 𝑥 (0,625 𝑚𝑜𝑙)2
(𝑃 + ) (1,5 𝐿 − 0,625 𝑚𝑜𝑙 𝑥 3,20 x 10−2 𝑑𝑚3 mol )
(1,5 𝑑𝑚3 )2
atm L
= 0,625 𝑚𝑜𝑙 𝑥 0,082 𝑥 303,15 𝐾
mol K
1,337 𝑑𝑚6 atm 𝑚𝑜𝑙 −2 𝑥 0,390𝑚𝑜𝑙 2
(𝑃 + ) ( 1,48 𝑑𝑚3 ) = 15, 536 𝑎𝑡𝑚
2,25 𝑑𝑚6
(𝑃 + 0,2317 𝑎𝑡𝑚)( 1,48) = 15, 536
𝑃 = 10,2655973 𝑎𝑡𝑚
La presión ejercida es 10,2655973 𝑎𝑡𝑚
17. Un neumático de automóvil fue inflado a una presión de 24 lb pulg-2 (1,00 atm
= 14,7 lb pulg-2) en un día de invierno cuando la temperatura era de -5ºC. ¿Qué
presión tendrá, asumiendo que no hay pérdidas y que el volumen es constante,
en un posterior día de verano cuando la temperatura es de 35ºC? ¿Qué
complicaciones habría que tener en cuenta en la práctica?
DATOS:
o 24 lb pulg-2 considerando (1,00 atm = 14,7 lb pulg-2) =1,632653061 atm
o TI = -5ºC ↔ TI = 268,15 k
o TF = 35ºC ↔ TF = 308,15 k
𝑃1 𝑥 𝑉1 𝑃 𝑥𝑉
= 2 2
𝑇1 𝑇2
1,632653061 atm 𝑋
268,15 𝐾
= 308,15 𝐾
𝑋
6,088581246 𝑥 10−3 = 308,15
1,876196311 𝑎𝑡𝑚 = 𝑋
La presión que tendría seria 1,876196311 𝑎𝑡𝑚
Se debería tener en cuenta que el volumen en la práctica
no va a ser constante, debido a que poco a poco se irá
perdiendo un determinado volumen.
18. Un propietario utiliza 4,00 x 103 m3 de gas natural en un año para calentar su
casa. Asuma que el gas natural es todo metano, CH4, y que el metano es un gas
ideal para las condiciones de este problema, las cuales son 1,00 atm y 20ºC ¿Cuál
es la masa de gas usado?
DATOS:
o 4,00 x 103 m3 de gas natural.
o Metano CH4 : 16 g/mol
o 1 atm
o 20 ºC : 293,15K
o Masa de metano: ¿?
1000L
4,00x103 m3 x m3 = 4x106 L
APORTE: BRAYAN QUISPE ARAPA CUI: 20162837
PV = nRT
m atm L
1 atm x 4x106 L = g x 0,082 mol K
X 293,15 K
16
mol
m
4x106 L = 16 g X 24,0383
24,0383 x m
4x106 L = 16 g
64x106 g = 24,0383 x m
2662417,891 g = m ↔ 2662, 417891 kg
El propietario emplea 2662, 417891 kg de gas de metano.
19. Las densidades del aire a -85ºC, 0ºC y 100ºC son 1,877 g dm-3, 1,294 g dm-3 y
0,946 g dm-3, respectivamente. De estos datos y asumiendo que el aire obedece la
ley de Charles, determine un valor para el cero absoluto de temperatura en grados
Celsius.
20. Dado que la densidad del aire a 0,987 bar y 27ºC es 1,146 kg m-3, calcule la
fracción molar y la presión parcial del nitrógeno y el oxígeno asumiendo que (a)
el aire consiste sólo en esos dos gases, (b) el aire también contiene 1,00 mol por
ciento de Ar.
DATOS:
o 1,146 kg m-3 = 1,146 g/L
o 0,987 bar = 0,974 atm
o 27ºC = 300,15 K
Parte “A”
Suponiendo que es un gas ideal
RT RT
V= Vm =
P P
atm L
0,082 mol K x 300,15 K
Vm = Vm = 25,2847 L
0,974 atm
m
ρ= m= ρ v m= (1.146)(25.2847) m= 28.9762 g
v
o Entonces un mol de aire= 28.9762g
o Sabiendo que M de Oxigeno= 32 y de nitrógeno=28 Si decimos
que:
o X es la fracción molar del Nitrógeno y (1-X) es la fracción molar del
Oxígeno, Entonces:
28x+32(1-x)=28.9762
28x+32-32x=28.9762
-4x=28.9762-32
-4x=-3.0238
x= -3.0238 / -4
x= 0.7559
o La fracción molar del Nitrógeno, entonces
Frm (N2 ) = 75.59%
o La fracción molar del Oxígeno es 1- x. Entonces
Frm (O2 ) = 24.40%
o Para sacar la presión parcial, tenemos:
Pp = PT (Frm )
o La presión total, 0.974 atm, Entonces:
Pp (N2 ) = 0.974(0.7559)
Pp (N2 ) = 73.62%
Pp(O2 ) = 0.974(0.244)
Pp (O2 ) = 23.76%
APORTE: BRAYAN QUISPE ARAPA CUI: 20162837
Parte “B”
o Cuando el aire contiene 1% molar de Argón
o Se hace el mismo arreglo algebraico que el anterior, solamente se
cambia el 1 por 0.99, ya que el argón está ocupando el 1%
28x + 32(0.99-x)=28.9762
28x+31.68-32x=28.9762
28x-32x=28.9762-31.68
-4x=-2.7038
x=0.6759
o Entonces, sabiendo que x es la fracción molar del Nitrógeno:
𝐹𝑟𝑚 (𝑁2 ) = 67.59%
o Y sabiendo que el oxígeno es (1-.99)
𝐹𝑟𝑚 (𝑂2 ) = 31.41%
𝐹𝑟𝑚 (𝐴𝑟) = 1%
o Y para conocer las presiones parciales se utiliza la misma fórmula:
𝑃𝑝 (𝑁2 ) = 0.974(0.6759)
𝑃𝑝 (𝑁2 ) = 65.83%
𝑃𝑝 (𝑂2 ) = 0.974(0.3141)
𝑃𝑝 (𝑂2 ) = 30.5933%
𝑃𝑝 (𝐴𝑟) = 0.974(0.1)
𝑃𝑝 (𝐴𝑟) = 0.0974%
APORTE: BRAYAN QUISPE ARAPA CUI: 20162837
Vous aimerez peut-être aussi
- ProblemasDocument2 pagesProblemasJoseph Sulca MartinezPas encore d'évaluation
- Fisico QuimicaDocument3 pagesFisico Quimicamarco antonioPas encore d'évaluation
- Gases IdealesDocument21 pagesGases Idealesraul medinaPas encore d'évaluation
- Problemas 1° Ley TermodinamicaDocument7 pagesProblemas 1° Ley TermodinamicaEduardo MartinezPas encore d'évaluation
- Tarea 4 Gases Reales Luis Nieto LemusDocument36 pagesTarea 4 Gases Reales Luis Nieto LemusJimena MoralesPas encore d'évaluation
- Solucion Taller EntropiasDocument4 pagesSolucion Taller EntropiasGabriela100% (1)
- Fisicoquimica TypeoDocument26 pagesFisicoquimica TypeoKevin Peredo HidalgoPas encore d'évaluation
- Problemas Resueltos SEM7Document9 pagesProblemas Resueltos SEM7ESTHIVEN KIM CRUZ AYTEPas encore d'évaluation
- Post3 - Termo2 Equilibrio Liquido Vapor en Un Sistema No IdealDocument7 pagesPost3 - Termo2 Equilibrio Liquido Vapor en Un Sistema No IdealRaquel DíazPas encore d'évaluation
- Práctica 5: Determinación de La Solubilidad Del Ca (OH) 2. Efecto Del Ion Común.Document18 pagesPráctica 5: Determinación de La Solubilidad Del Ca (OH) 2. Efecto Del Ion Común.Enrique DelgadoPas encore d'évaluation
- EstequiometríaDocument11 pagesEstequiometríaJOSE ANTONIO SIERRA CONEOPas encore d'évaluation
- Tarea 1 - MasDocument21 pagesTarea 1 - MasDiana AvilaPas encore d'évaluation
- Practica 6 QADocument5 pagesPractica 6 QAAdolfo Rodriguez Hernandez100% (1)
- Práctica Gel. BalanceDocument6 pagesPráctica Gel. BalanceYol MorenoPas encore d'évaluation
- AnaliticaDocument12 pagesAnaliticaJhonny Carrasco Taipe100% (1)
- Serie de Ecuación de Gases Reales 21-IDocument6 pagesSerie de Ecuación de Gases Reales 21-IDaniela Gonzalez100% (2)
- Problemas de Gravimetria Ayres 15-1 Al 15-3Document8 pagesProblemas de Gravimetria Ayres 15-1 Al 15-3Néstor Juan Sánchez AlfaroPas encore d'évaluation
- Ejercicios de DimensionesDocument4 pagesEjercicios de DimensionesMiguel Alejandro Gomez NavarroPas encore d'évaluation
- Datos: M: 131g Xe, V 1,0dm 1,0L, R 0,0821 T 25°C+273 298°KDocument3 pagesDatos: M: 131g Xe, V 1,0dm 1,0L, R 0,0821 T 25°C+273 298°Kluis cardenasPas encore d'évaluation
- P YodoanilinaDocument10 pagesP YodoanilinaAlex Sean100% (1)
- Tarea Unidad 1Document8 pagesTarea Unidad 1Valery Suarez100% (1)
- 2 PrimeraLey Termoquimica PDFDocument4 pages2 PrimeraLey Termoquimica PDFnathaPas encore d'évaluation
- Determinacion Del Naoh y Na2co3Document14 pagesDeterminacion Del Naoh y Na2co3Carla Flores DiasPas encore d'évaluation
- Taller Propiedades PeriodicasDocument12 pagesTaller Propiedades PeriodicasSandra NarváezPas encore d'évaluation
- Problema 3Document16 pagesProblema 3pekeiaaf2100% (1)
- Problemario BalanceDocument10 pagesProblemario BalanceEdwin CastañedaPas encore d'évaluation
- Soluciones y Propiedades ColigativasDocument53 pagesSoluciones y Propiedades ColigativasRUBEN DARIO ROMERO ROMERO100% (1)
- Práctica No.3Document8 pagesPráctica No.3Paams Mart100% (1)
- FQ - Aplicaciones de Beta y Kappa - MCBVDocument2 pagesFQ - Aplicaciones de Beta y Kappa - MCBVMARIA DEL CARMEN BARAJAS VALDIVIAPas encore d'évaluation
- Ejercicios Unidad IiiDocument3 pagesEjercicios Unidad IiiRoosvel Soto DiazPas encore d'évaluation
- Tarea Equlibrio Acido-BaseDocument2 pagesTarea Equlibrio Acido-BaseKatia LealPas encore d'évaluation
- Practica No.4 Volumenes Molares ParcialesDocument10 pagesPractica No.4 Volumenes Molares ParcialesAldo Ilyan Perez MendezPas encore d'évaluation
- Seminarios Equilibrios SolucionesDocument46 pagesSeminarios Equilibrios SolucionesGustavoPas encore d'évaluation
- Segunda Tarea Cinética FormalDocument1 pageSegunda Tarea Cinética FormalEdward AlexanderPas encore d'évaluation
- Problemas 3, 4 y 5Document4 pagesProblemas 3, 4 y 5Isabel OropezaPas encore d'évaluation
- Taller (2) (Autoguardado)Document3 pagesTaller (2) (Autoguardado)Alvaro A. Gomez Castro100% (1)
- Tarea 23Document5 pagesTarea 23ODALYSPas encore d'évaluation
- Ejercicios SolubilidadDocument37 pagesEjercicios SolubilidadVania Millan0% (1)
- Cuestionario Práctica 2. Quimica Organica IIDocument2 pagesCuestionario Práctica 2. Quimica Organica IIKarla Alonso100% (1)
- Ejercicio 11.13Document5 pagesEjercicio 11.13Andrea Sarahi Izquiy VPas encore d'évaluation
- TeoriaDocument4 pagesTeoriaChristian Noe Esp. Her.100% (1)
- Ilovepdf MergedDocument18 pagesIlovepdf MergedJulia BarrosPas encore d'évaluation
- Ejercicios de FisicoquímicaDocument1 pageEjercicios de FisicoquímicaLuce Dávila FernandezPas encore d'évaluation
- Ejercicios Resueltos de Análisis ElectroanalíticoDocument8 pagesEjercicios Resueltos de Análisis ElectroanalíticoRENATO JAIR COSTA MINGAPas encore d'évaluation
- TAREA No. 7 SOLUCIONES IÓNICAS ASIVDocument14 pagesTAREA No. 7 SOLUCIONES IÓNICAS ASIVAndrea Sarahi Izquiy VPas encore d'évaluation
- CALCULODECALOR2Document8 pagesCALCULODECALOR2Layla LópezPas encore d'évaluation
- Problemas SustitucionDocument24 pagesProblemas Sustitucionloper100% (3)
- Capitulo II CastellanDocument24 pagesCapitulo II CastellanLéo AyolPas encore d'évaluation
- Fenómenos de Transporte Presentes en Los BiofiltrosDocument2 pagesFenómenos de Transporte Presentes en Los BiofiltrosIrene CuevasPas encore d'évaluation
- Práctica 6 de Orgánica, Obtención de FluoresceínaDocument10 pagesPráctica 6 de Orgánica, Obtención de FluoresceínaBryan LujanPas encore d'évaluation
- BalanceDocument4 pagesBalanceLarissa Andrade0% (1)
- Información Previa Al Experimento Práctica 7 Complejos Metálicos Con Ligantes DitiocarbamatoDocument8 pagesInformación Previa Al Experimento Práctica 7 Complejos Metálicos Con Ligantes DitiocarbamatoDanny Elle GonzagaPas encore d'évaluation
- Guiatiii - 2020Document7 pagesGuiatiii - 2020yoPas encore d'évaluation
- TAREA3 (Recuperado Automáticamente)Document16 pagesTAREA3 (Recuperado Automáticamente)Fernando Mendoza JuarezPas encore d'évaluation
- Reporte Q.A 1.2Document10 pagesReporte Q.A 1.2MisaelPas encore d'évaluation
- 12Document3 pages12Elias MaytaPas encore d'évaluation
- Ejrcicios de Gas IdealDocument32 pagesEjrcicios de Gas Idealgustavo_castro_17Pas encore d'évaluation
- Ejercios en Clase Pro ColigativasDocument18 pagesEjercios en Clase Pro ColigativasFlores Gamarra DeylisPas encore d'évaluation
- Taller 1Document4 pagesTaller 1Aracelli Coayla MurilloPas encore d'évaluation
- Trabajo de Quimica - Daniela PulidoDocument7 pagesTrabajo de Quimica - Daniela PulidoJhon CaroPas encore d'évaluation
- Primer Examen GestionDocument3 pagesPrimer Examen GestionAbraham S. AroPas encore d'évaluation
- Informe Final IMPRIMIRDocument22 pagesInforme Final IMPRIMIRAbraham S. AroPas encore d'évaluation
- Breve Reseña de Pandemias en El Mundo PDFDocument4 pagesBreve Reseña de Pandemias en El Mundo PDFAbraham S. AroPas encore d'évaluation
- Evaluacion Continua Iii, Abraham Aro Mixto PDFDocument3 pagesEvaluacion Continua Iii, Abraham Aro Mixto PDFAbraham S. AroPas encore d'évaluation
- Sesión 4 Derecho AmbientalDocument66 pagesSesión 4 Derecho AmbientalAbraham S. AroPas encore d'évaluation
- Contaminacion Del AguaDocument27 pagesContaminacion Del AguaAbraham S. AroPas encore d'évaluation
- CuestionarioDocument2 pagesCuestionarioAbraham S. AroPas encore d'évaluation
- Informe de La Practica 1. MineriaDocument10 pagesInforme de La Practica 1. MineriaAbraham S. AroPas encore d'évaluation
- Diagrama de Flujo Del Tratamiento de Cascara de PlatanoDocument2 pagesDiagrama de Flujo Del Tratamiento de Cascara de PlatanoAbraham S. AroPas encore d'évaluation
- Diagrama de Flujo Del Tratamiento de Cascara de PlatanoDocument2 pagesDiagrama de Flujo Del Tratamiento de Cascara de PlatanoAbraham S. AroPas encore d'évaluation
- Rol Servicio Diaconos 2018 2do TrimestreDocument1 pageRol Servicio Diaconos 2018 2do TrimestreAbraham S. AroPas encore d'évaluation
- QUINUADocument18 pagesQUINUAAbraham S. AroPas encore d'évaluation
- Curva de CalibraciónDocument1 pageCurva de CalibraciónAbraham S. AroPas encore d'évaluation
- Reporte 2 AnálisisDocument5 pagesReporte 2 AnálisisAbraham S. AroPas encore d'évaluation
- Espectroscopia Visible Cuestionario Desarrollado AbrahamDocument3 pagesEspectroscopia Visible Cuestionario Desarrollado AbrahamAbraham S. Aro100% (1)
- Crucigrama de Quimica Analitica I Abraham AroDocument6 pagesCrucigrama de Quimica Analitica I Abraham AroAbraham S. AroPas encore d'évaluation
- 4to y 5to Trabajo de Investigacion de Temas Desarrolados en ClaseDocument17 pages4to y 5to Trabajo de Investigacion de Temas Desarrolados en ClaseAbraham S. AroPas encore d'évaluation
- Practica de Quimica Laboratorio 1Document3 pagesPractica de Quimica Laboratorio 1Abraham S. AroPas encore d'évaluation
- Quimica General Universidad Cientifica Del SurDocument19 pagesQuimica General Universidad Cientifica Del Surrehavor725Pas encore d'évaluation
- Pdfslide - Tips Extraccion de MescalinaDocument5 pagesPdfslide - Tips Extraccion de MescalinasorgintxokoPas encore d'évaluation
- Cinética QuímicaDocument1 pageCinética Químicaconstanza.salas.1Pas encore d'évaluation
- TERMODINÁMICADocument3 pagesTERMODINÁMICAvalenzua97Pas encore d'évaluation
- 5 Fórmulas de TermologíaDocument2 pages5 Fórmulas de TermologíaGARCIA MARTINEZ OSCAR ALBERTO (DOCENTE PL 10 SAN JUAN DEL RIO)Pas encore d'évaluation
- Sintesis de NitrobencenoDocument5 pagesSintesis de NitrobencenoAdrizz FrancoPas encore d'évaluation
- Uso Del Diagrama de Stüve en Sondeo AtmosféricoDocument9 pagesUso Del Diagrama de Stüve en Sondeo Atmosféricoagustina villana ramirezPas encore d'évaluation
- Solucionario de La 1ra Practica de Química de CEPU Invierno 2024-IIDocument9 pagesSolucionario de La 1ra Practica de Química de CEPU Invierno 2024-IIsalcedomaniaPas encore d'évaluation
- Que Es El Modelo AtómicoDocument3 pagesQue Es El Modelo AtómicoVictoria Conejo LucioPas encore d'évaluation
- Teoria de Soluciones Productos Quimicos PDFDocument23 pagesTeoria de Soluciones Productos Quimicos PDFhslscribdPas encore d'évaluation
- Bomba de VacioDocument20 pagesBomba de VacioSaul ZLPas encore d'évaluation
- Practica Conductividad ElectricaDocument4 pagesPractica Conductividad ElectricaProfesor Andres PintorPas encore d'évaluation
- Unidad 1. FUNDAMENTOS DE PROCESOS INDUSTRIALES PDFDocument39 pagesUnidad 1. FUNDAMENTOS DE PROCESOS INDUSTRIALES PDFCésar Muñoz MairaPas encore d'évaluation
- TAREADocument2 pagesTAREAandrea UrgilesPas encore d'évaluation
- 3.semiconductores DoctoradoDocument30 pages3.semiconductores DoctoradoEduardo HernándezPas encore d'évaluation
- Capitulo 1Document26 pagesCapitulo 1lisseth callePas encore d'évaluation
- Clase #2 Piro Revision Conceptos TermodinámicosDocument20 pagesClase #2 Piro Revision Conceptos TermodinámicosBraulio ala andiaPas encore d'évaluation
- Quiz Martha Quimica 2Document10 pagesQuiz Martha Quimica 2Deisy Lliiana Vasquez Gallego100% (1)
- Ejercicios de KC y Kps ModificadaDocument3 pagesEjercicios de KC y Kps ModificadaJosé MuñozPas encore d'évaluation
- Cuadro Comparativo Modelos Atómicos - 004454Document4 pagesCuadro Comparativo Modelos Atómicos - 004454Melissa CalzadaPas encore d'évaluation
- 003 Guia Reposicion MaquinasDocument3 pages003 Guia Reposicion MaquinasPioe FranPas encore d'évaluation
- Taller 1Document4 pagesTaller 1Andres G FelipePas encore d'évaluation
- 8 Trabajo ColaborativoDocument13 pages8 Trabajo ColaborativoyanPas encore d'évaluation
- Tarea Semana 8 - Versión 3Document2 pagesTarea Semana 8 - Versión 3Fabian Fernández Bout50% (2)
- Práctica 3 - Cinética QuímicaDocument15 pagesPráctica 3 - Cinética QuímicaJUAN FRANCISCO GOMEZ HERNANDEZPas encore d'évaluation
- 10 Osmosis y DialisisDocument52 pages10 Osmosis y DialisisAbigailPas encore d'évaluation
- Factores Que Modifican La SolubilidadDocument2 pagesFactores Que Modifican La SolubilidadAiedail666Pas encore d'évaluation
- Produccion de BicarbonatoDocument12 pagesProduccion de BicarbonatoDarkinfire WesternPas encore d'évaluation
- Practica 4 Eyc PDFDocument11 pagesPractica 4 Eyc PDFRicardo CruzPas encore d'évaluation
- Ejercicios ExamenDocument10 pagesEjercicios ExamenJorge Luis Cdn100% (1)