Académique Documents
Professionnel Documents
Culture Documents
Semana 2 Uniones y Enlace Quimico
Transféré par
Eder Hernández0 évaluation0% ont trouvé ce document utile (0 vote)
80 vues17 pagesEste documento trata sobre los diferentes tipos de enlaces químicos, incluyendo enlaces iónicos, covalentes, covalentes múltiples y metálicos. Explica la regla del octeto y cómo los átomos alcanzan estabilidad mediante la pérdida, ganancia o compartición de electrones. También cubre la electronegatividad y cómo esta determina el carácter polar o no polar de los enlaces covalentes. Por último, resume las fuerzas intermoleculares como las fuerzas de dipolo-dipolo y dispersión.
Description originale:
uuuuuuuuuuuuuuu
Titre original
Semana 2 Uniones y Enlace Quimico (1)
Copyright
© © All Rights Reserved
Formats disponibles
PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentEste documento trata sobre los diferentes tipos de enlaces químicos, incluyendo enlaces iónicos, covalentes, covalentes múltiples y metálicos. Explica la regla del octeto y cómo los átomos alcanzan estabilidad mediante la pérdida, ganancia o compartición de electrones. También cubre la electronegatividad y cómo esta determina el carácter polar o no polar de los enlaces covalentes. Por último, resume las fuerzas intermoleculares como las fuerzas de dipolo-dipolo y dispersión.
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PDF, TXT ou lisez en ligne sur Scribd
0 évaluation0% ont trouvé ce document utile (0 vote)
80 vues17 pagesSemana 2 Uniones y Enlace Quimico
Transféré par
Eder HernándezEste documento trata sobre los diferentes tipos de enlaces químicos, incluyendo enlaces iónicos, covalentes, covalentes múltiples y metálicos. Explica la regla del octeto y cómo los átomos alcanzan estabilidad mediante la pérdida, ganancia o compartición de electrones. También cubre la electronegatividad y cómo esta determina el carácter polar o no polar de los enlaces covalentes. Por último, resume las fuerzas intermoleculares como las fuerzas de dipolo-dipolo y dispersión.
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 17
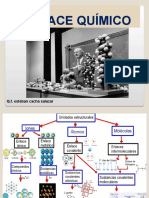
Semana 2
Unión y Enlace
Químico, Fuerzas
Intermoleculares
Ing. Q. Rosangela Juárez
Enlace Químico
O Un enlace químico es la interacción física responsable
de las fusiones entre átomos, moléculas e iones, que
tiene una estabilidad en los compuestos.
O Debido a los enlaces químicos presentes en las
sustancias se debe las propiedades físicas y químicas.
O Los tipos de enlaces químicos pueden ser:
O IÓNICOS
O COVALENTES (POLAR, NO POLAR Y PURO)
Ing. Q. Rosangela Juárez
Regla del Octeto
O Los átomos tienen la capacidad de interaccionar para
modificar el numero de electrones que tienen en su
capa mas externa, y buscan tener la configuración
electrónica de un gas noble, que en su nivel mas
externo tiene 8 electrones. Ne, Ar, Kr, Xe.
O Excepto el H y He, que son estables con 2 electrones.
Ing. Q. Rosangela Juárez
O Los átomos alcanzan estabilidad cuando tienen 8
electrones en su nivel mas externo, para cumplir
con la regla del octeto los átomos pueden:
O Perder electrones (metales -M)
O Ganar electrones( No metales - nM)
O Compartir electrones
Ing. Q. Rosangela Juárez
Enlace Iónico
O En este tipo de enlace químico hay transferencia de
electrones de un Metal a un No metal.
Ing. Q. Rosangela Juárez
Enlace Covalente
O En este tipo de enlace químico dos átomos comparten
electrones. Generalmente para cumplir con la regla
del octeto.
O Este tipo de enlace se da entre dos átomos No
metales. H2, Cl2, I2.
Ing. Q. Rosangela Juárez
Enlaces Covalentes Múltiples
O Sencillo: Se comparte un par de electrones HCl
O Doble: Se comparten dos pares de electrones CH2 CH2
O Triple: Se comparten tres pares de electrones N2
Ing. Q. Rosangela Juárez
Enlace covalente dativo
O En este tipo de enlace los átomos comparten
electrones pero este par de electrones han sido
aportados solo por un átomo. SO3
Ing. Q. Rosangela Juárez
O Enlace Covalente Polar: Se da cuando los pares de
electrones se comparte de una manera desigual,
entre átomos diferentes. HCl
O Enlace Covalente No Polar: Se da cuando los pares de
electrones se comparten de una manera igual, entre
átomos diatomicos. Cl2 , I2 , H2 , C2
Ing. Q. Rosangela Juárez
O Enlace Metálico: es un enlace químico que
mantiene unidos los átomos de los metales entre
sí.
Ing. Q. Rosangela Juárez
Electronegatividad
O Es la capacidad que tiene un átomo para atraer
electrones hacia el.
O Los que tienen mayor electronegatividad son los no
metales, eje. Flúor.
Ing. Q. Rosangela Juárez
Tipos de enlace químico según la
diferencia de electronegatividad.
>
>
Si el valor es 0 es enlace Puro
Ing. Q. Rosangela Juárez
O Pasos para establecer el tipo de enlace según la
diferencia de electronegatividad para el P2S3
O Busque la electronegatividad de los dos elementos
O P=2.19 S= 2.58
O No se toman en cuenta los subíndices
O Se resta el mayor menos el menor
O La Diferencia= 2.58-2.19= 0.39 por lo tanto es un
tipo de enlace covalente No Polar
Ing. Q. Rosangela Juárez
Ing. Q. Rosangela Juárez
O Busque el tipo de enlace según la diferencia de
electronegatividad:
Ing. Q. Rosangela Juárez
Fuerzas Intermoleculares
O Fuerza Dipolo-Dipolo: La interacción dipolo-
dipolo consiste en la atracción electrostática entre el
extremo positivo de una molécula polar y el negativo
de otra. El enlace de hidrógeno es un tipo especial de
interacción dipolo-dipolo.
O Fuerza de Dispersión: Las fuerzas de dispersión de
London son un tipo de fuerza intermolecular, surgen
entre moléculas no polares, en las que pueden
aparecer dipolos instantáneos. Son más intensas
cuanto mayor es la molécula, ya que los dipolos se
pueden producir con más facilidad.
Vous aimerez peut-être aussi
- De la estructura atómica a la quiralidad.: Algunos conceptos de la químicaD'EverandDe la estructura atómica a la quiralidad.: Algunos conceptos de la químicaÉvaluation : 5 sur 5 étoiles5/5 (1)
- Semana 2, Uniones y Enlace QuimicoDocument20 pagesSemana 2, Uniones y Enlace QuimicoDarwin VasquezPas encore d'évaluation
- Clase 8 Cup Quimica 2021Document23 pagesClase 8 Cup Quimica 2021Flores Alcocer Walter JhimmyPas encore d'évaluation
- Enlaces QuimicosDocument29 pagesEnlaces Quimicosplanetashop976Pas encore d'évaluation
- Enlaces QuimicoDocument22 pagesEnlaces Quimicomandrake1233Pas encore d'évaluation
- Enlace Quimico IDocument3 pagesEnlace Quimico IAngelitoLeónPas encore d'évaluation
- Taller de Nivelación de QuímicaDocument11 pagesTaller de Nivelación de QuímicaRocio Yaqueline Rivero EscobarPas encore d'évaluation
- Enlaces QuimicosDocument15 pagesEnlaces QuimicosMoisesito EspinozaPas encore d'évaluation
- Enlaces QuimicosDocument8 pagesEnlaces QuimicosJosé Carlo Vallecillo LizardoPas encore d'évaluation
- Química General T4Document11 pagesQuímica General T4John Ramos JapaPas encore d'évaluation
- Teoría Atómica y Enlaces AtómicosDocument7 pagesTeoría Atómica y Enlaces AtómicosMeredith YanesPas encore d'évaluation
- Glosario Nº3Document8 pagesGlosario Nº3Nicolas CocoPas encore d'évaluation
- Enlace Químico Ionico, Covalente y MetalicoDocument35 pagesEnlace Químico Ionico, Covalente y MetalicoalfonsojimenesPas encore d'évaluation
- Unidad N°4. Enlaces QuimicosDocument13 pagesUnidad N°4. Enlaces QuimicosIván RJ GimenezPas encore d'évaluation
- Practica Modulo III-1Document15 pagesPractica Modulo III-1Erick Henry Trujillo EustaquioPas encore d'évaluation
- Enlace QuimicoDocument44 pagesEnlace QuimicoStephanieChávezPas encore d'évaluation
- Enlace Quimico Interacciones MolecularesDocument22 pagesEnlace Quimico Interacciones MolecularesKiara MarroquínPas encore d'évaluation
- Grupo 6 - Química General - Capitulo - 8Document13 pagesGrupo 6 - Química General - Capitulo - 8GabrielaPas encore d'évaluation
- Tarea de Quimica 2Document5 pagesTarea de Quimica 2yader daniel pozo liraPas encore d'évaluation
- Unidad 3. Enlace QuimicoDocument28 pagesUnidad 3. Enlace QuimicoalfonsojimenesPas encore d'évaluation
- Nomenclatura y Notación Química (2) - 1Document78 pagesNomenclatura y Notación Química (2) - 1LetiziaPas encore d'évaluation
- Enlace Quimico UnmsmDocument42 pagesEnlace Quimico UnmsmWilber Milla TrujilloPas encore d'évaluation
- Resumen Unidad No. 3 Quimica Basica 2Document22 pagesResumen Unidad No. 3 Quimica Basica 2Addy PujolsPas encore d'évaluation
- 2-Enlaces Quimicos MBDocument6 pages2-Enlaces Quimicos MBferhumanistaPas encore d'évaluation
- 10 Guia Taller 1 Enlaces QuímicosDocument6 pages10 Guia Taller 1 Enlaces Químicosnn CastroPas encore d'évaluation
- Los Covalentes, Enlaces Iónicos, Enlace Metálico, Electronegatividad y ElectropositividadDocument11 pagesLos Covalentes, Enlaces Iónicos, Enlace Metálico, Electronegatividad y ElectropositividadCristina PerezPas encore d'évaluation
- Química CalmecacDocument84 pagesQuímica CalmecacDanae RamirezPas encore d'évaluation
- Enlaces QuímicosDocument5 pagesEnlaces QuímicosLucia SalinasPas encore d'évaluation
- Práctica 1 ESIMEDocument17 pagesPráctica 1 ESIMEElaine AlbiterPas encore d'évaluation
- Quimica-013-Electronegatividad Enlaces Quimicos Clasificacion PDFDocument11 pagesQuimica-013-Electronegatividad Enlaces Quimicos Clasificacion PDFDavid EstradaPas encore d'évaluation
- Capítulo 4 - Enlaces Químicos y Fuerzas IntermolecularesDocument33 pagesCapítulo 4 - Enlaces Químicos y Fuerzas IntermolecularesLeoCorleonePas encore d'évaluation
- Quimica-012-Clasificacion de Los Elementos en GruposDocument11 pagesQuimica-012-Clasificacion de Los Elementos en GruposMoroni45Pas encore d'évaluation
- Enlace Quimico Ionico, Covalente y MetalicoDocument35 pagesEnlace Quimico Ionico, Covalente y MetalicoMagdalena AvilaPas encore d'évaluation
- Uniones QuímicasDocument15 pagesUniones QuímicasFelipe Alejandro JaraPas encore d'évaluation
- Práctica 5Document17 pagesPráctica 5MoramoretonPas encore d'évaluation
- Bloque 2 - Unidad 4 El EnlaceDocument8 pagesBloque 2 - Unidad 4 El EnlaceMarcos Campayo FernándezPas encore d'évaluation
- Institución Educativa "Alfonso López Pumarejo"Document4 pagesInstitución Educativa "Alfonso López Pumarejo"Jeanca ManosalvaPas encore d'évaluation
- Guia de PracticaDocument15 pagesGuia de PracticaElmer Cadillo LimasPas encore d'évaluation
- EnlacesDocument28 pagesEnlacesCamilo SolanoPas encore d'évaluation
- Uniones Químicas - Fisicoquímica 3°Document14 pagesUniones Químicas - Fisicoquímica 3°Silvia SianoPas encore d'évaluation
- Enlaces QuimicosDocument18 pagesEnlaces QuimicosEdgar MeléndezPas encore d'évaluation
- Electronegatividad y Enlaces QuímicosDocument18 pagesElectronegatividad y Enlaces QuímicosDayana Vázquez gordilloPas encore d'évaluation
- Compuestos Quimicos Guia de EstudioDocument2 pagesCompuestos Quimicos Guia de EstudioLanzus RSPas encore d'évaluation
- Uniones y Enlace QuimicoDocument25 pagesUniones y Enlace QuimicoDanielaPas encore d'évaluation
- CLASE 7-Enlace QuímicoDocument59 pagesCLASE 7-Enlace Químicojhonnatan loyolaPas encore d'évaluation
- PPP Enlaces QuimicosDocument13 pagesPPP Enlaces Quimicosjaneln_1Pas encore d'évaluation
- Enlace Quimico - OK PDFDocument35 pagesEnlace Quimico - OK PDFYves Olivier Brard AracenaPas encore d'évaluation
- GLOSARIODocument8 pagesGLOSARIOGiani CerveraPas encore d'évaluation
- 1.6 Enlaces Quimicos INGENIERIAS PDFDocument11 pages1.6 Enlaces Quimicos INGENIERIAS PDFAndres FloresPas encore d'évaluation
- Ensayo Enlaces QuimicosDocument13 pagesEnsayo Enlaces QuimicosMiguel Ángel VillamaresPas encore d'évaluation
- Uniones QuimicasDocument6 pagesUniones QuimicasMaria Celina MoyanoPas encore d'évaluation
- Resumen para Teórico N°2Document11 pagesResumen para Teórico N°2estefanisPas encore d'évaluation
- Unidad 4. Enlaces Químicos y Fuerza Intermoleculares.Document31 pagesUnidad 4. Enlaces Químicos y Fuerza Intermoleculares.BRANDON MARTINEZ RIOSPas encore d'évaluation
- T3. El Enlace Quã MicoDocument24 pagesT3. El Enlace Quã MicoAppPas encore d'évaluation
- En Lace Covalent Ecor Regi DoDocument10 pagesEn Lace Covalent Ecor Regi DoLilian MonterrosoPas encore d'évaluation
- Enlaces QuímicosDocument24 pagesEnlaces QuímicosKatia VelásquezPas encore d'évaluation
- TeamsDocument5 pagesTeamsELIZABETH QUINCHO MARTINEZPas encore d'évaluation
- Guia Enlaces Quimicos Septimo PDFDocument10 pagesGuia Enlaces Quimicos Septimo PDFJacson Ivan Torres VasquezPas encore d'évaluation
- Guia 3 - U1 - Enlaces QuimicosDocument16 pagesGuia 3 - U1 - Enlaces QuimicosRocio OrtizPas encore d'évaluation
- Resumen Del Acuerdo de Paz.Document12 pagesResumen Del Acuerdo de Paz.Eder HernándezPas encore d'évaluation
- Todos Los InstrumentosDocument10 pagesTodos Los InstrumentosEder HernándezPas encore d'évaluation
- Marco TeóricoDocument11 pagesMarco TeóricoEder Hernández0% (1)
- ContabilidadDocument12 pagesContabilidadEder HernándezPas encore d'évaluation
- Instrumentos Autóctonos de GuatemalaDocument4 pagesInstrumentos Autóctonos de GuatemalaEder HernándezPas encore d'évaluation
- Matriz de Evaluación de SoftwareDocument38 pagesMatriz de Evaluación de SoftwareEder Hernández0% (1)
- Glosario de EtimologíaDocument26 pagesGlosario de EtimologíaEder Hernández0% (1)
- Tipos de MatrimonioDocument2 pagesTipos de MatrimonioEder HernándezPas encore d'évaluation
- Limpieza en El CasaDocument4 pagesLimpieza en El CasaEder HernándezPas encore d'évaluation
- La Diferencia Entre Un Texto Narrativo y Un DescriptivoDocument2 pagesLa Diferencia Entre Un Texto Narrativo y Un DescriptivoEder Hernández100% (1)
- Poema A La Marimba de GuatemalaDocument2 pagesPoema A La Marimba de GuatemalaEder Hernández100% (2)
- Instrumentos Musicales de GuatemalaDocument6 pagesInstrumentos Musicales de GuatemalaEder HernándezPas encore d'évaluation
- Guia TP Quimica General - 2014Document115 pagesGuia TP Quimica General - 2014Ina GigliPas encore d'évaluation
- Quimica Enlace Químico I: CH CH CHDocument6 pagesQuimica Enlace Químico I: CH CH CHWalsen Helian Evangelista VidalPas encore d'évaluation
- Tarea2 401582 26Document20 pagesTarea2 401582 26JefferssonFlorezMeneses100% (1)
- Megatarea 02Document13 pagesMegatarea 02allan130Pas encore d'évaluation
- Enlance QuímicoDocument140 pagesEnlance Químicofernando ramirez100% (1)
- DETALLES EXPERIMENTALES A y BDocument5 pagesDETALLES EXPERIMENTALES A y BerickPas encore d'évaluation
- CuestionarioDocument3 pagesCuestionarioKaren Rodriguez RiveraPas encore d'évaluation
- Informe de Laboratorio Enlace QuimicoDocument12 pagesInforme de Laboratorio Enlace QuimicoMariana Delgadillo ObregonPas encore d'évaluation
- Química Paes 2023Document43 pagesQuímica Paes 2023ROSA MUÑOZ100% (3)
- Informe de Compuestos de CoordinaciónDocument7 pagesInforme de Compuestos de Coordinaciónoscar morales riosPas encore d'évaluation
- Enlace QuimicoDocument5 pagesEnlace Quimicodragonrojo12Pas encore d'évaluation
- OAQ Intercolegial - Examen Niveles I1-3 - Respuestas - 2018Document19 pagesOAQ Intercolegial - Examen Niveles I1-3 - Respuestas - 2018Lucas Vicente Fano CostasPas encore d'évaluation
- Tema 1 - Principios de Bioquimica IDocument6 pagesTema 1 - Principios de Bioquimica Ijhordy illaconza lizarbePas encore d'évaluation
- Examen Bases BiologicasDocument48 pagesExamen Bases Biologicastruyts.medPas encore d'évaluation
- Examen Simulacro Preuniversitario Academia La NacionalDocument8 pagesExamen Simulacro Preuniversitario Academia La NacionalAnonymous Z0vRagJv1HPas encore d'évaluation
- Qui MicaDocument3 pagesQui MicaLia MendezPas encore d'évaluation
- Resumen de Libro Ciencia de MaterialesDocument25 pagesResumen de Libro Ciencia de MaterialesDariela Catunta LópezPas encore d'évaluation
- Quimica General ResumenDocument40 pagesQuimica General ResumenLala Lalalal80% (5)
- Unidad 5.1 5Document23 pagesUnidad 5.1 5Lucía Ibán LlorentePas encore d'évaluation
- Qu Mica (1) QuimicaDocument82 pagesQu Mica (1) Quimicachicho6404100% (3)
- Guia 10 Periodo 4 Quimica PDFDocument33 pagesGuia 10 Periodo 4 Quimica PDFMARIA DE LOS ANGELES MEDINA MARTINEZPas encore d'évaluation
- Ingeniería de Materiales - Apunte de ClasesDocument57 pagesIngeniería de Materiales - Apunte de ClasesRodrigo MoralesPas encore d'évaluation
- 03 - Qca JunioDocument5 pages03 - Qca JunioMax Peña ReyesPas encore d'évaluation
- Tema 3 Enlace Quimico en PDFDocument8 pagesTema 3 Enlace Quimico en PDFesquezombi20073Pas encore d'évaluation
- 1 Uniones QuímicasDocument129 pages1 Uniones QuímicasGabriela ArteroPas encore d'évaluation
- Guia 3Document4 pagesGuia 3Jesica SalazarPas encore d'évaluation
- Taller QuimicaDocument6 pagesTaller QuimicaMauricio Perdomo PPas encore d'évaluation
- Cuestionario Materiales DentalesDocument7 pagesCuestionario Materiales DentalesLuz Adriana Zue IIPas encore d'évaluation
- TESIS González FelipeDocument270 pagesTESIS González FelipeMarco CossioPas encore d'évaluation
- Apuntes de QuimicaDocument9 pagesApuntes de QuimicaMartin PiotrovskiPas encore d'évaluation