Académique Documents
Professionnel Documents
Culture Documents
Tabletas Feum PDF
Transféré par
Salvador Jeronimo SolanoTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Tabletas Feum PDF
Transféré par
Salvador Jeronimo SolanoDroits d'auteur :
Formats disponibles
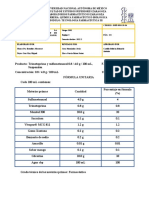
EL TEXTO EN COLOR ROJO HA SIDO MODIFICADO Tabletas recubiertas, con excepción de las tabletas recu-
Con fundamento en el numeral 4.11.1 de la Norma Oficial biertas con una película y que contengan 25 mg
Mexicana NOM-001-SSA1-2010, se publica el presente o más de un principio activo que constituya el 25 % o
proyecto a efecto de que los interesados, a partir del 1º de más de la masa total de la tableta.
febrero y hasta el 31 de marzo de 2016, lo analicen, evalúen y Suspensiones, emulsiones o geles en envases de dosis
envíen sus observaciones o comentarios en idioma español y única o en cápsulas blandas, destinadas exclusivamente
con el sustento técnico suficiente ante la CPFEUM, sito en Río para administración sistémica y no para los fármacos
Rhin número 57, colonia Cuauhtémoc, código postal 06500, destinados para administración externa, cutánea.
México, D.F. Fax: 5207 6890 Sólidos (estériles o no) en envases de dosis única con
Correo electrónico: consultas@farmacopea.org.mx. sustancias agregadas, ya sean activas o inactivas cuando
no se cumplen los requisitos establecidos para Variación
de masa (véase tabla 0299.1).
Soluciones para inhalación envasadas en frasco ámpula
MGA 0299. UNIFORMIDAD DE DOSIS de vidrio o de plástico, destinadas para uso en nebú-
lizadores.
Para los fines de este método, los términos “unidad” y “unidad A menos que se indique algo diferente en la monografía
de dosis” se consideran como sinónimos y se definen como individual, los aerosoles e inhaladores y unidades de dosificación
formas farmacéuticas que contienen una única dosis o parte de de dosis fija o medida (con válvula de dosificación), e
una dosis de un fármaco en cada unidad. inhaladores de polvos secos que contengan polvos de inhalación
La uniformidad de dosis se puede demostrar por los métodos en reservorios, deben cumplir con los requisitos establecidos,
de Variación de masa o el de Uniformidad de contenido. Los según corresponda, de Uniformidad de dosis liberada o de
requisitos se aplican individualmente para cada ingrediente Uniformidad de dosis liberada en todo el contenido del MGA
activo del producto tanto en unidades de dosis que contengan 0021. Aerosoles, atomizadores e inhaladores. Uniformidad de
un solo ingrediente activo como en aquellas que contengan dos o dosis, propiedades fisicoquímicas y aerodinámicas de sus
más ingredientes activos, a menos que se especifique otra cosa componentes.
en la monografía individual.
El método de Variación de masa se basa en la medición de la PROCEDIMIENTOS PARA VARIACIÓN DE MASA
masa individual de las unidades de dosis en prueba y el cálculo Para determinar la uniformidad de dosis en una preparación
de la variación entre ellas, relacionada al contenido del principio por este método, seleccionar 10 unidades y proceder como se
activo, y suponiendo una distribución homogénea. indica a continuación para cada preparado farmacéutico.
Se aplica para las siguientes formas farmacéuticas: Nota: se pueden utilizar las unidades que se hayan destinado
Cápsulas duras y tabletas que contengan 25 mg o más de un para la valoración del principio activo.
principio activo y si éste constituye el 25 % o más de
la masa total de la unidad de dosis o del contenido de la cápsula Tabletas sin recubrimiento y tabletas recubiertas con
película. Pesar con exactitud 10 tabletas individualmente.
en el caso de cápsulas duras.
Calcular el contenido del principio activo en cada una de las
Soluciones orales en envases de dosis única y en 10 tabletas expresado como el porcentaje de la cantidad
cápsulas blandas. Sólidos (estériles o no) en envases de declarada, relacionando la masa de cada tableta con el
dosis única sin sustancias agregadas, ya sean activas o resultado de la valoración del principio activo obtenido como
inactivas. se indica en la monografía individual del producto. Calcular el
Sólidos (estériles o no) en envases de dosis única con o valor de aceptación.
sin sustancias agregadas, ya sean activas o inactivas, que
hayan sido preparados a partir de soluciones verdaderas Cápsulas duras, sólidos y sólidos estériles, en envases de
y liofilizados en el envase final y cuyas etiquetas dosis única. Pesar con exactitud 10 unidades individualmente
indiquen este método de preparación. para obtener el peso bruto, identificar cada unidad, vaciar el
Nota: en el caso de que en una forma farmacéutica existan dos contenido de cada cápsula o envase por un método adecuado
o más principios activos y alguno de ellos no cumple y pesar con exactitud cada cápsula o envase vacío. Calcular el
los requisitos para Variación de masa, para dicho principio activo peso neto individual por diferencia del peso bruto menos el peso
deberá realizarse la prueba de Uniformidad de contenido. de las cápsulas o envases vacíos correspondientes y relacionar
El método de Uniformidad de contenido se basa en la deter- el resultado de la valoración del principio activo obtenido
minación cuantitativa del contenido individual del principio como se indica en la monografía individual del producto con el
activo en un cierto número de unidades de formas farma- peso neto individual, para calcular el contenido del principio
céuticas de dosis única, para determinar si la variación de los activo en cada una de las 10 unidades, expresado como
contenidos individuales está dentro de los límites establecidos. porcentaje de la cantidad declarada. Calcular el valor de
Se puede aplicar a todas las formas farmacéuticas y es aceptación.
necesario en los casos que se describen a continuación:
+52 55 5207 8187 CONSULTA A USUARIOS DE LA FEUM 2016-1 Río Rhin 57
+52 55 5207 6887 Métodos Generales de Análisis col. Cuauhtémoc
www.farmacopea.org.mx 1 06500, del. Cuauhtémoc
consultas@farmacopea.org.mx México D. F., México.
Cápsulas blandas. Pesar individualmente con exactitud individual del producto, y del peso neto del contenido del
10 cápsulas intactas, para obtener el peso bruto; identificar envase individual calcular el contenido del principio activo en
cada cápsula. Abrir las cápsulas cortando con tijeras o navaja el líquido drenado de cada una de las 10 unidades, expresado
y vaciar el contenido lavando la cápsula con un disolvente que como porcentaje de la cantidad declarada. Calcular el valor de
no disuelva la cápsula y sí elimine totalmente el contenido. aceptación.
Dejar evaporar el disolvente de la cápsula a temperatura
ambiente durante 30 min, evitando que la cápsula adquiera o Cálculo del valor de aceptación. Calcular el valor de acepta-
pierda humedad. Pesar individualmente las cápsulas vacías y ción como se indica en el Procedimiento para Uniformidad de
calcular el contenido neto por diferencia del peso bruto menos contenido, reemplazando el contenido individual de las
el peso de las cápsulas vacías. Relacionar el resultado de la unidades dosis por el contenido estimado individualmente,
valoración del principio activo obtenido como se indica en la xi : x1, x2, …, xn = Contenido estimado individual de las unida-
monografía individual del producto con el peso neto des analizadas.
individual, para calcular el contenido del principio activo en
cada una de las cápsulas, expresado como porcentaje de la 𝑥𝑖 = 𝑚1 𝐴⁄𝑚
̅
cantidad declarada. Calcular el valor de aceptación. Donde:
m1, m2, …, mn = Masas individuales de las unidades analizadas.
Soluciones orales y jarabes en envases de dosis única. Pesar A = Contenido de principio activo (porcentaje de la cantidad
con exactitud la cantidad de líquido que drene, en no más de declarada) determinado como se describe en
5 s, de cada uno de 10 envases individuales. Si es necesario la valoración.
calcular el volumen equivalente después de determinar la ̅ = Media de las masas individuales (m1, m2, …, mn)
𝑚
densidad del producto, como se indica en el MGA 0251
Densidad relativa. A partir del resultado de la valoración del Tabla 0299.1. Requisitos para pruebas de uniformidad de
principio activo, obtenido como se indica en la monografía contenido (UC) y variación de masa (VM).
Dosis y proporción de
fármaco
Forma farmacéutica Tipo Subtipo
≥ 25 mg y < 25 mg y
≥ 25 % < 25 %
Sin cubierta ---- VM UC
Tabletas Películas VM UC
Recubiertas
Otras UC UC
Rígidas ---- VM UC
Suspensión,
Cápsula UC UC
Blandas emulsión o gel
Soluciones VM VM
Componente único ---- VM VM
Solución liofilizada
Sólidos en envases de dosis única VM VM
Varios componentes en envase final
Otros UC UC
Suspensión, emulsión o gel para uso sistémico exclu-
---- ---- UC UC
sivamente, envasado en envases de dosis única.
Soluciones orales envasadas en recipientes de dosis
---- ---- VM VM
única y cápsulas blandas.
Inhalaciones envasadas en unidades de dosificación
previamente medida, incluyendo las soluciones para
---- ---- UC UC
inhalación envasadas en frasco ámpula de vidrio o
de plástico, destinadas para uso en nebulizadores.
Sistemas transdérmicos ---- ---- UC UC
Supositorios ---- ---- UC UC
Otros ---- ---- UC UC
+52 55 5207 8187 CONSULTA A USUARIOS DE LA FEUM 2016-1 Río Rhin 57
+52 55 5207 6887 Métodos Generales de Análisis col. Cuauhtémoc
www.farmacopea.org.mx 2 06500, del. Cuauhtémoc
consultas@farmacopea.org.mx México D. F., México.
Soluciones para inhalación, envasadas en frasco ámpula de Calcular el contenido de principio activo equivalente a una unidad
vidrio o de plástico, destinadas para uso en nebulizadores. de dosis promedio utilizando los resultados obtenidos con:
Pesar con exactitud 10 envases individualmente para obtener el a) el método de la valoración del principio activo y,
peso bruto; identificar cada envase. Retirar el contenido de cada b) el método especial de la Uniformidad de contenido
envase por un medio adecuado. Pesar individualmente con exac- Calcular el factor de corrección F, por medio de la siguiente
titud los envases vacíos y calcular el peso neto de cada envase por fórmula:
diferencia del peso bruto menos el peso de los envases vacíos.
𝐹 = 𝐴 ⁄𝑃
Relacionar el resultado de la valoración del principio activo
Donde:
obtenido como se indica en la monografía individual del
A = Contenido de principio activo en una unidad de dosis
producto con el peso neto individual, para calcular el
promedio obtenido con el método de la valoración del
contenido del principio activo en cada uno de los envases,
principio activo.
expresado como porcentaje de la cantidad declarada.
P = Contenido de principio activo en una unidad de dosis
Nota: para estas formas farmacéuticas no se requiere el cálculo
promedio obtenido con el método especial de la
de valores de aceptación.
Uniformidad de contenido.
PROCEDIMIENTOS PARA UNIFORMIDAD DE Si (100 A - P / A) 10, no es válido el uso de un factor de
CONTENIDO corrección, por lo tanto deberá repetirse la prueba.
Seleccionar no menos de 30 unidades dosis y proceder como El factor de corrección sólo se podrá aplicar si F no es menor
se indica a continuación para cada preparado farmacéutico. que 1.030, ni mayor que 1.100, o no es menor que 0.900 ni
Cuando la cantidad del o los principios activos en cada unidad mayor que 0.970.
de dosis difiere de la requerida para la valoración, ajustar el Si F se encuentra entre 0.970 y 1.030 la corrección no es
grado de dilución de las soluciones y/o el volumen de las necesaria.
alícuotas, hasta que la concentración de los principios activos Si F se encuentra entre 1.030 y 1.100 o entre 0.900 y 0.970,
en la solución final sea igual que la del procedimiento para la calcular el contenido de principio activo en cada unidad de
valoración o en el caso de análisis por titulación, si es dosis, multiplicando por F cada uno de los contenidos
necesario se puede utilizar una solución volumétrica de una obtenidos con el método especial.
concentración diferente para tener un gasto adecuado en la
titulación. Si se realiza alguna de las modificaciones antes Tabletas, cápsulas, soluciones orales, suspensiones orales,
mencionadas, hacer las correcciones necesarias para efectuar jarabes, emulsiones orales, o geles orales, sólidos y sólidos
los cálculos. estériles en envases de dosis única. Analizar individualmente
Cuando se indique un método de análisis especial para la 10 unidades de dosis como se indica en la Valoración del
Uniformidad de contenido, corregir los resultados como se principio activo de la monografía individual del producto, a
indica a continuación: menos que se indique otra cosa en el Procedimiento para la
Preparar una muestra con un número suficiente de unidades de Uniformidad de contenido. Calcular el valor de aceptación.
dosificación para obtener una mezcla homogénea que Para soluciones orales, suspensiones orales, jarabes, emul-
proporcione la cantidad de muestra requerida para la cuantifi- siones orales o geles orales en envases de dosis única,
cación del principio activo por el método indicado en la mezclar bien y realizar la valoración del principio activo en la
valoración, más la cantidad de muestra requerida para cantidad del material, que drene desde el envase individual en
cuantificar el principio activo por el método indicado en la no más de 5 s y para productos con valores altos
Uniformidad de contenido según se describe en la monografía de viscosidad, realizar la valoración sobre la cantidad de
individual del producto. Para lo cual se debe triturar hasta material bien mezclado que se obtiene retirando en forma
polvo fino una cantidad de tabletas, o mezclar los contenidos cuantitativa el contenido de un envase individual. Expresar los
de cápsulas, las soluciones orales, los jarabes, las resultados como dosis liberada.
suspensiones, emulsiones, geles o sólidos en envases de dosis Cálculo del valor de aceptación (VA). Calcular el valor de
única Si no se obtiene una mezcla homogénea de esta manera, aceptación mediante la fórmula:
usar disolventes adecuados u otros procedimientos para
|𝑀 − 𝑋̅ | + 𝑘𝑠
preparar una solución que contenga todo el principio activo y
usar alícuotas adecuadas de esta solución para el (los) Donde los términos son los definidos en la tabla 0299.2.
procedimiento(s) especificado (s).
Supositorios y sistemas transdérmicos
Valorar por separado, una cantidad exactamente medida, de la Analizar 10 unidades individualmente como se indica en la
mezcla homogénea de cápsulas, tabletas, soluciones orales, Valoración en la monografía individual del producto, a menos
jarabes, suspensiones, inhalaciones o sólidos en envases de que otra cosa se indique en el Procedimiento para Uniformidad
dosis única, como se indica en (a) la valoración del principio de contenido.
activo y (b) utilizando el procedimiento de análisis descrito en Expresión de resultados. Aplicar los siguientes criterios a menos
el método especial para Uniformidad de contenido descrito en que otra cosa se especifique en la monografía individual.
la monografía del producto correspondiente.
+52 55 5207 8187 CONSULTA A USUARIOS DE LA FEUM 2016-1 Río Rhin 57
+52 55 5207 6887 Métodos Generales de Análisis col. Cuauhtémoc
www.farmacopea.org.mx 3 06500, del. Cuauhtémoc
consultas@farmacopea.org.mx México D. F., México.
Nota: para estas formas farmacéuticas no se requiere el cálculo Supositorios
de valor de aceptación. (A) Si el promedio de los límites especificados en la valoración
del principio activo en la monografía individual del producto
Tabletas, cápsulas, soluciones orales, suspensiones orales, no es mayor que 100 %:
jarabes, emulsiones orales, o geles orales, sólidos y sólidos A menos que se indique otra cosa en la monografía individual
estériles en envases de dosis única. Se cumplen los requisitos de del producto, los requisitos para la uniformidad de dosis se
uniformidad de dosis si el valor de aceptación de las primeras 10 cumplen si la cantidad de principio activo en cada una de las
unidades de dosificación no es mayor que L1 %. Si el valor de 10 unidades de dosis, determinada por el método de Unifor-
aceptación es mayor que L1 %, analizar las siguientes 20 midad de contenido, se encuentra dentro del intervalo de 85.0
unidades y calcular el valor de aceptación. Se cumplen los a 115.0 % de la cantidad declarada en el marbete, y si el
requisitos si el valor de aceptación final de las 30 unidades de coeficiente de variación no es mayor que 6.0 %.
dosificación no es mayor que L1 %, y si el contenido individual Si una unidad de dosis se encuentra fuera del intervalo de 85.0
de ninguna unidad de dosificación es menor que [1- (0.01) (L2)] a 115.0 % y ninguna fuera del intervalo de 75.0 %
M; ni mayor que [1 + (0.01) (L2)] M como se especifica en a 125.0 % de la cantidad declarada en el marbete, o si el
Cálculo del valor de aceptación en Uniformidad de contenido o coeficiente de variación es mayor que 6.0 %, o si ambas
en Variación de masa. A menos que se indique otra cosa en la condiciones se presentan, probar 20 unidades de dosis
monografía individual, L1 = 15.0 y L2 = 25.0. adicionales. Los requisitos se cumplen si no más de una de las
30 unidades de dosis se encuentra fuera del intervalo
de 85.0 a 115.0 % y ninguna fuera del intervalo de 75.0 a
125.0 % de la cantidad declarada en el marbete, y si el
coeficiente de variación de las 30 unidades de dosis no es
mayor que 7.8 %.
Tabla 0299.2. Variables para el cálculo del valor de aceptación.
Variable Definición Condiciones Valor
Media de los contenidos indivi-
duales (x1, x₂,…, xn) expresados
𝑋̅
como el porcentaje de la cantidad
declarada.
Contenido individual de las uni-
xi = x1, x₂, … dades probadas, expresado como
,en el porcentaje de la cantidad
declarada.
Tamaño de la muestra (número
n
de unidades en una muestra).
k Constante de Aceptabilidad. Si n = 10, entonces k = 2.4
Si n = 30, entonces k = 2.0
s Desviación estándar de la ∑(𝑥𝑖 − 𝑋̅)2
(DE) muestra. 𝐷𝐸 = √
𝑛−1
Coeficiente de variación (la desvia-
ción estándar de la muestra
CV (100 𝑆)⁄𝑋̅
expresada como un porcentaje de
la media).
M (caso 1) a
Si 98.5 % ≤ 𝑋̅ ≤ 101.5 %, 𝑀 = 𝑋̅
aplicar cuando 𝑇 ≤ Valor de referencia.
entonces (𝑉𝐴 = 𝑘𝑠)
101.5T
𝑀 = 98.5 %
Si 𝑋̅ < 98.5 %, entonces
(𝑉𝐴 = 98.5 − 𝑋̅ + 𝑘𝑠)
𝑀 = 101.5 %
Si 𝑋̅ > 101.5 %, entonces
(𝑉𝐴 = 𝑋̅ − 101.5 + 𝑘𝑠)
+52 55 5207 8187 CONSULTA A USUARIOS DE LA FEUM 2016-1 Río Rhin 57
+52 55 5207 6887 Métodos Generales de Análisis col. Cuauhtémoc
www.farmacopea.org.mx 4 06500, del. Cuauhtémoc
consultas@farmacopea.org.mx México D. F., México.
Tabla 0299.2. Variables para el cálculo del valor de aceptación.
Variable Definición Condiciones Valor
M (caso 2) a
𝑀 = 𝑋̅
aplicar cuando 𝑇 > Valor de referencia. Si 98.5 % ≤ 𝑋̅ ≤ 𝑇, entonces
(𝑉𝐴 = 𝑘𝑠)
101.5
𝑀 = 98.5 %
Si X < 98.5 %, entonces
(𝑉𝐴 = 98.5 − 𝑋̅ + 𝑘𝑠)
𝑀=𝑇%
Si X >T, entonces
(𝑉𝐴 = 𝑋̅ − 𝑇 + 𝑘𝑠)
Fórmula general:
|𝑀 − 𝑋̅| + 𝑘𝑠
Valor de
(Los cálculos especifi-
aceptación
cados anteriormente
(VA)
son para los distintos
casos).
L1 = 15.0 a menos que
Máximo valor de aceptación se especifique algo
L1
permitido en porcentaje. diferente en la
monografía individual.
En el lado del valor menor, ningún
resultado de unidad de dosificación
Máximo intervalo permitido L2 = 25.0 a menos
puede ser menor que [1– (0.01) (L2)]
para la desviación de cada que se especifique
M, mientras que en el lado del valor
L2 unidad de dosificación probada algo diferente en la
superior ningún resultado de unidad
a partir del monografía
de dosificación puede ser mayor que
valor calculado de M. individual.
[1+ (0.01) (L2)] M. (Esto está basado
en un valor de L2 de 25.0).
Valor deseado en el momento de la
fabricación. Para los efectos de esta
Farmacopea, a menos que se
especifique algo diferente en la
T monografía individual, T es 100 % y
para los efectos de fabricación, T es el
valor asignado del fármaco, aprobado
por el fabricante, en el momento de la
fabricación.
(B) Si el promedio de los límites especificados en la valoración los límites establecidos en la valoración del principio activo de
del principio activo en la monografía individual el producto es la monografía individual del producto, aplicar las
mayor que 100 %, aplicar las siguientes interpretaciones: interpretaciones del inciso (A), excepto que los porcentajes no
1. Si el contenido promedio del principio activo en las se calculan con respecto a la cantidad declarada en el marbete,
unidades de dosis probadas es del 100 % o menor, aplicar la sino que se computarizan con respecto al valor obtenido al
interpretación del inciso (A). multiplicar la cantidad declarada en el marbete por el
2. Si el contenido promedio del principio activo en las unidades contenido promedio del principio activo de las unidades de
de dosis probadas no es menor que el promedio de los límites dosis probadas, expresado como un porcentaje de la cantidad
establecidos en la valoración del principio activo de la declarada en el marbete, dividido entre 100.
monografía individual del producto, aplicar la interpretación
del inciso (A), excepto que los porcentajes no se calculan con Sistemas transdérmicos
respecto a la cantidad declarada en el marbete, sino que se (A) Si el promedio de los límites especificados en la valoración
computarizan con respecto al valor obtenido al multiplicar la del principio activo en la monografía individual del producto
cantidad declarada en el marbete por el promedio de los límites no es mayor que 100 %:
establecidos en la valoración del principio activo en la A menos que se indique otra cosa en la monografía individual del
monografía individual del producto y dividida entre 100. producto, los requisitos para la uniformidad de dosis se
3. Si el contenido promedio del principio activo de las unidades cumplen si la cantidad del principio activo en no menos de 9
de dosis probadas se encuentra entre 100 % y el promedio de de las 10 unidades de dosis, determinada por el método de
+52 55 5207 8187 CONSULTA A USUARIOS DE LA FEUM 2016-1 Río Rhin 57
+52 55 5207 6887 Métodos Generales de Análisis col. Cuauhtémoc
www.farmacopea.org.mx 5 06500, del. Cuauhtémoc
consultas@farmacopea.org.mx México D. F., México.
Uniformidad de contenido, se encuentren dentro del intervalo de de la masa promedio, y ninguna unidad dosis, se desvía más
85.0 a 115.0 % y ninguna fuera del intervalo de 75.0 a 125.0 % del 20 % de la masa promedio.
de la cantidad declarada en el marbete y el coeficiente de
variación no es mayor que 6.0 %. VARIACIÓN DE MASA DE VITAMÍNICOS
Si 2 ó 3 unidades de dosis se encuentran fuera del intervalo de Las siguientes pruebas aplican a preparados farmacéuticos
85.0 a 115.0 %, pero no fuera del intervalo de 75.0 a 125.0 % utilizados en nutriología y proporcionan los límites para las
de la cantidad declarada en el marbete, o si el coeficiente de variaciones permisibles en la masa de las tabletas o cápsulas
variación es mayor que 6.0 %, o si ambas condiciones se individuales, expresados en función de la desviación permitida
presentan, probar 20 unidades de dosis adicionales. Los del peso promedio de una muestra.
requisitos se cumplen si no más de 3 de las 30 unidades de
dosis se encuentran fuera del intervalo de 85.0 a 115.0 % y CÁPSULAS. Las cápsulas cumplen con los requisitos de la si-
ninguna fuera del intervalo de 75.0 a 125.0 % de la cantidad guiente prueba, en cuanto a la variación de masa del contenido.
declarada en el marbete y el coeficiente de variación de las
30 unidades de dosis no es mayor que 7.8 %. Cápsulas duras. Pesar individualmente 20 cápsulas intactas y
determinar la masa promedio. Los requisitos se cumplen si
(B) Si el promedio de los límites especificados en la valoración cada peso individual esta entre los 90 y 110 % de la masa
del principio activo en la monografía individual del producto promedio.
es mayor que 100 %, aplicar las siguientes interpretaciones: Si no todas las cápsulas están dentro de los límites mencio-
1. Si el contenido promedio del principio activo en las nados, pesar individualmente las 20 cápsulas, teniendo
unidades de dosis probadas es del 100 % o menor, aplicar cuidado de conservar la identidad de cada cápsula y retirar el
la interpretación del inciso (A). contenido de cada cápsula con la ayuda de un pequeño cepillo
2. Si el contenido promedio del principio activo en las o trozo de algodón. Pesar individualmente las cubiertas vacías
unidades de dosis probadas no es menor que el promedio de calcular para cada cápsula el peso neto de su contenido restando
los límites establecidos en la valoración del principio activo de el peso de la cubierta del peso bruto respectivo. Determinar el
la monografía individual del producto, aplicar la interpretación contenido neto promedio a partir de la suma de los pesos netos
del inciso (A), excepto que los porcentajes no se calculan con individuales. Luego determinar la diferencia entre cada contenido
respecto a la cantidad declarada en el marbete, sino que se neto individual y el contenido neto promedio: los requisitos se
calculan con respecto al valor obtenido al multiplicar la cumplen si (a) no más de 2 de las diferencias son mayores que 10
cantidad declarada en el marbete por el promedio de los límites % del contenido neto promedio y (b) en ningún caso la
establecidos en la valoración del principio activo en la diferencia es mayor que 25 %.
monografía individual del producto y dividida entre 100. Si más de 2 pero no más de 6 cápsulas se apartan del promedio en
3. Si el contenido promedio del principio activo de las 10 a 25 %, determinar el contenido neto de 40 cápsulas
unidades de dosis probadas se encuentra entre 100 % y el adicionales y determinar el contenido promedio de las
promedio de los límites establecidos en la valoración del 60 cápsulas. Determinar las 60 desviaciones del promedio
principio activo de la monografía individual del producto, nuevo: los requisitos se cumplen si (a) en no más de 6 de las
aplicar las interpretaciones del inciso (A), excepto que los 60 cápsulas la diferencia excede el 10 % del contenido neto
porcentajes no se calculan con respecto a la cantidad declarada en promedio y (b) en ningún caso la diferencia excede el 25 %.
el marbete, sino que se calculan con respecto al valor obtenido
al multiplicar la cantidad declarada en el marbete por el Cápsulas blandas. Proceder según se indica en Cápsulas
contenido promedio del principio activo de las unidades de duras, pero determinar el peso neto del contenido de las
dosis probadas, expresado como un porcentaje de la cantidad cápsulas individuales del siguiente modo. Pesar las cápsulas
declarada en el marbete, dividido entre 100. intactas individualmente para obtener sus pesos brutos,
procurando preservar la identidad de cada cápsula. Luego,
Uniformidad de dosis por variación de masa de las prepa- cortar y abrir las cápsulas con un instrumento cortante
raciones en envases multidosis adecuado, limpio y seco, como por ejemplo una tijera o una
La prueba aplica para formas farmacéuticas de administración cuchilla afilada, y retirar el contenido por lavado con un
oral, como granulados, polvos, y líquidos envasados en disolvente adecuado. Dejar que el disolvente ocluido se
presentaciones multidosis, que contienen un dispositivo evapore de las cubiertas a temperatura ambiente durante un
dosificador integrado. periodo de aproximadamente 30 min, tomando precauciones
A menos que se especifique otra cosa en la monografía del para evitar la absorción o la pérdida de humedad. Pesar las
producto, determinar la masa individual de 20 unidades dosis cubiertas individuales y calcular el contenido neto. Los
seleccionadas al azar de uno o más envases, utilizando el dispo- requisitos son los que se indican para Cápsulas duras.
sitivo dosificador integrado y calcular la masa promedio.
Interpretación. Los requisitos se cumplen si la masa indivi- TABLETAS. Las tabletas se ajustan a los criterios de la tabla
dual de no más de dos unidades dosis se desvía más del 10 % 0299.3 adjunta.
+52 55 5207 8187 CONSULTA A USUARIOS DE LA FEUM 2016-1 Río Rhin 57
+52 55 5207 6887 Métodos Generales de Análisis col. Cuauhtémoc
www.farmacopea.org.mx 6 06500, del. Cuauhtémoc
consultas@farmacopea.org.mx México D. F., México.
Tabletas sin cubierta y tabletas recubiertas con película.
Pesar individualmente 20 tabletas enteras y calcular la masa
promedio. Los requisitos se cumplen si el peso de no más
de 2 de las tabletas difiere de la masa promedio en más del
porcentaje especificado en la tabla adjunta y ninguna tableta
difiere en masa en más del doble de ese porcentaje.
Tabletas recubiertas (a excepción de las tabletas recu-
biertas con película). Pesar individualmente 20 tabletas
enteras y calcular la masa promedio. Si las tabletas no se
ajustan a los criterios de la tabla adjunta, colocar 20 tabletas
en un vaso de precipitados con agua a 37 °C y agitar por
rotación moderada durante no más de 5 min. Examinar las
partes centrales para ver si existen indicios de desintegración
y repetir el procedimiento durante un periodo más breve en
caso de haber comenzado la desintegración. Secar los núcleos a
50 °C durante 30 min. Pesar con exactitud los núcleos de
20 tabletas individuales y calcular la masa promedio.
Los requisitos se cumplen si los pesos de no más de 2 de las
tabletas difieren del peso promedio en más del porcentaje
especificado en la tabla adjunta y ninguna tableta difiere en
peso en no más del doble de ese porcentaje.
Criterios. Véase tabla 0299.3.
Tabla 0299.3. Tolerancias para la Variación de masa
de tabletas con o sin recubrimiento.
Peso promedio de las Diferencia
tabletas, miligramos porcentual
130 o menos 10
De 130 a 324 7.5
Más de 324 5
+52 55 5207 8187 CONSULTA A USUARIOS DE LA FEUM 2016-1 Río Rhin 57
+52 55 5207 6887 Métodos Generales de Análisis col. Cuauhtémoc
www.farmacopea.org.mx 7 06500, del. Cuauhtémoc
consultas@farmacopea.org.mx México D. F., México.
Vous aimerez peut-être aussi
- Pruebas de Calidad CápsulasDocument6 pagesPruebas de Calidad CápsulasGaby NRmz0% (1)
- Instituto Politécnico Nacional: Escuela Nacional de Ciencias BiológicasDocument30 pagesInstituto Politécnico Nacional: Escuela Nacional de Ciencias BiológicasMónica MedinaPas encore d'évaluation
- Pruebas para La Determinación de La Calidad de GlicerinaDocument5 pagesPruebas para La Determinación de La Calidad de GlicerinaKadirAmethMontalvoMurilloPas encore d'évaluation
- L Sistema de Inyección de Combustible Del Chevrolet OptraDocument20 pagesL Sistema de Inyección de Combustible Del Chevrolet Optrakelvisert57% (7)
- Uniformidad de DosisDocument7 pagesUniformidad de DosisEder VillanuevaPas encore d'évaluation
- Práctica 1. Estudio de Algunos Factores Que Afectan La Solubilidad de Un Fármaco Primer CurseDocument19 pagesPráctica 1. Estudio de Algunos Factores Que Afectan La Solubilidad de Un Fármaco Primer CurseEduardo Romero CanoPas encore d'évaluation
- PNO MGA 0041 Determinación Agua Por Karl FischerDocument10 pagesPNO MGA 0041 Determinación Agua Por Karl FischerJude LizowskyPas encore d'évaluation
- Tema 4 Modelo Monocompartimental-Adm Intrav Dosis ÚnicaDocument11 pagesTema 4 Modelo Monocompartimental-Adm Intrav Dosis ÚnicaRosa María Soto PérezPas encore d'évaluation
- Mga 0001 Determinacion Del Indice de AcidezDocument49 pagesMga 0001 Determinacion Del Indice de Acidezhatziry moreno100% (1)
- PTE - Monitoreo de Calidad Ambiental (Proyecto No Especificado)Document6 pagesPTE - Monitoreo de Calidad Ambiental (Proyecto No Especificado)EnmanuelPas encore d'évaluation
- Fundamento Del Proceso de Extraccion. Trabajo en LaboratorioDocument2 pagesFundamento Del Proceso de Extraccion. Trabajo en LaboratorioAle Alegria100% (2)
- Informe 5 Análisis de Control de Calidad de Amoxicilina Cápsulas 500MGDocument8 pagesInforme 5 Análisis de Control de Calidad de Amoxicilina Cápsulas 500MGMadeleine RodriguezPas encore d'évaluation
- Manual Mantencion PAB06Document477 pagesManual Mantencion PAB06Eduardo Campos100% (1)
- Práctica - Propiedades Reológicas de Los PolvosDocument6 pagesPráctica - Propiedades Reológicas de Los PolvosAngelinatorPoPas encore d'évaluation
- Mga 0221-2Document5 pagesMga 0221-2Maria Rene Torres50% (2)
- Mezclado de LiquidosDocument11 pagesMezclado de LiquidosBrayanm Quispe MolinaPas encore d'évaluation
- Ácido Acetilsalicílico, TabletasDocument3 pagesÁcido Acetilsalicílico, TabletasEvelyn Jim 3295Pas encore d'évaluation
- UDC. Uniformidad de Unidades de Dosificación 2016 PDFDocument21 pagesUDC. Uniformidad de Unidades de Dosificación 2016 PDFKaoru SumeragiPas encore d'évaluation
- Reporte F.A (Polvos) .Document8 pagesReporte F.A (Polvos) .Adriana MarinPas encore d'évaluation
- Reologia de PolvosDocument3 pagesReologia de PolvosAdriana MarinPas encore d'évaluation
- Lecho FluidoDocument4 pagesLecho FluidoMauricio GonzalezPas encore d'évaluation
- Ciclos de CompresiónDocument3 pagesCiclos de CompresiónYessi LopzPas encore d'évaluation
- Pnoac - DisolutorDocument7 pagesPnoac - DisolutorKaren Belen Labastida EspinosaPas encore d'évaluation
- VANIAprevreologiadepolvosDocument3 pagesVANIAprevreologiadepolvosAdriana MarinPas encore d'évaluation
- ExamenDocument4 pagesExamenomar barreraPas encore d'évaluation
- Informe 1Document15 pagesInforme 1Oscar Ramirez BermeoPas encore d'évaluation
- Reporte DepuracionDocument6 pagesReporte DepuracionJose Raul Lizardi ResendizPas encore d'évaluation
- Efecto de La Concentración de Tensoactivos en La Solubilidad Del Ácido BenzoicoDocument8 pagesEfecto de La Concentración de Tensoactivos en La Solubilidad Del Ácido BenzoicoSantiago BaezPas encore d'évaluation
- Práctica 1Document8 pagesPráctica 1Andrea Cordova CedilloPas encore d'évaluation
- 1 Biofarmacia Introducción OkDocument27 pages1 Biofarmacia Introducción OkCornelioTaipeSaldivarPas encore d'évaluation
- Disolucion y Teorias CineticasDocument23 pagesDisolucion y Teorias CineticasGiss Arroyo100% (1)
- Granulación HúmedaDocument23 pagesGranulación HúmedaSergioPas encore d'évaluation
- Jonathan Urbina Soto-Validación Del Método Analítico de Valoración de Ácido SalicílicoDocument16 pagesJonathan Urbina Soto-Validación Del Método Analítico de Valoración de Ácido SalicílicoJonathan UrbinaPas encore d'évaluation
- CápsulasDocument9 pagesCápsulasValery.Pas encore d'évaluation
- Practica de CromatografiaDocument14 pagesPractica de CromatografiaHernann von HelmholtzPas encore d'évaluation
- Guia 1 FarmacotecniaDocument4 pagesGuia 1 FarmacotecniaSantiago Ocampo GutierrezPas encore d'évaluation
- Guía Práctica 9Document5 pagesGuía Práctica 9Nicolas CastilloPas encore d'évaluation
- Orden Maestra de Fabricacion Trimetoprima y SulfametoxazolDocument9 pagesOrden Maestra de Fabricacion Trimetoprima y SulfametoxazolEduardo A. Castillo BeltránPas encore d'évaluation
- Protocolo de Perfil de Disolucion 2Document2 pagesProtocolo de Perfil de Disolucion 2admtzmontanoPas encore d'évaluation
- Practica 11Document3 pagesPractica 11Adriana MarinPas encore d'évaluation
- Practica 3 Obtencion de EmulsinaDocument4 pagesPractica 3 Obtencion de EmulsinaRob HBPas encore d'évaluation
- Informe HPLC AcetaminofenDocument7 pagesInforme HPLC AcetaminofenPatricia MunozPas encore d'évaluation
- Problemario FisSisAmb CinéticaDocument1 pageProblemario FisSisAmb CinéticaLucía MargaritaPas encore d'évaluation
- Farma Practica 11 ReporteDocument4 pagesFarma Practica 11 ReporteNancy SánchezPas encore d'évaluation
- 08 Detectores en HPLC PDFDocument12 pages08 Detectores en HPLC PDFJuan Diego Morales DuranPas encore d'évaluation
- Potencia Microbiologica de Ampicilina SoDocument14 pagesPotencia Microbiologica de Ampicilina Socarolinepacheco14Pas encore d'évaluation
- Mga 0521Document22 pagesMga 0521jesusPas encore d'évaluation
- TF1 Operacion Unitaria - ReologiaDocument24 pagesTF1 Operacion Unitaria - ReologiaAdelheint BernsteinPas encore d'évaluation
- Obtención de Ácido Cítrico Con HongosDocument6 pagesObtención de Ácido Cítrico Con HongosDaniela BarreraPas encore d'évaluation
- Inyectores HPLCDocument37 pagesInyectores HPLCEdgar Flores0% (1)
- REologia 1Document2 pagesREologia 1vvveeeePas encore d'évaluation
- Defectos Del RecubrimientoDocument6 pagesDefectos Del RecubrimientoNubia Patricia Ponce Cárdenas100% (2)
- MGA 0271 DesintegracionDocument2 pagesMGA 0271 DesintegracionbethPas encore d'évaluation
- AP Practica 3 - Filtro RotatorioDocument4 pagesAP Practica 3 - Filtro RotatorioAkiraPas encore d'évaluation
- Tfii P2Document6 pagesTfii P2Cristian PintaPas encore d'évaluation
- Ejercicio Desarrollo AnaliticoDocument1 pageEjercicio Desarrollo AnaliticoJuan Volta BellamyPas encore d'évaluation
- Mga 261Document4 pagesMga 261ALONDRA GARCIA ZEPEDAPas encore d'évaluation
- Caso de Hechos 2 Monjaras Elias G40Document4 pagesCaso de Hechos 2 Monjaras Elias G40FATIMA ITZEL MONJARAS ELIASPas encore d'évaluation
- Fabricación de Tabletas RecubiertasDocument8 pagesFabricación de Tabletas RecubiertasBernardo Colorado Dubois50% (2)
- Métodos Generales de AnálisisDocument3 pagesMétodos Generales de AnálisisItz CorPas encore d'évaluation
- Pno SedimentacionDocument5 pagesPno SedimentacionAreli SanchezPas encore d'évaluation
- Protocolo para El Estudio de Estabilidad Del AcetaminofenDocument6 pagesProtocolo para El Estudio de Estabilidad Del AcetaminofenHarold Betancourt PerezPas encore d'évaluation
- Uniformidad de Dosis DFGSFDocument41 pagesUniformidad de Dosis DFGSFFINEES HIDAI LUGO ALEGRIA50% (2)
- Cosavet DF X 25 KG Sulphur Mills LimitedDocument1 pageCosavet DF X 25 KG Sulphur Mills LimitedCésar Jesús Bautista HernándezPas encore d'évaluation
- Conceptos de Lodo de PerforaciónDocument7 pagesConceptos de Lodo de PerforaciónAnonymous HAIlShM100% (1)
- Principalesplagasdelcultivodemelonysusenemigosnaturales 100531164308 Phpapp01Document120 pagesPrincipalesplagasdelcultivodemelonysusenemigosnaturales 100531164308 Phpapp01Vera Cieza EynerPas encore d'évaluation
- Almidón Agrio de YucaDocument14 pagesAlmidón Agrio de YucaSamario SamarioPas encore d'évaluation
- Actividadn1nnnMatriznestablecimientosnfarmacennuticosn 995f3d3a357c234Document2 pagesActividadn1nnnMatriznestablecimientosnfarmacennuticosn 995f3d3a357c234Yovany MillánPas encore d'évaluation
- Diagrama Protocolo Trementina Simple - StandardDocument1 pageDiagrama Protocolo Trementina Simple - StandardVictor Andres Fierro SouzaPas encore d'évaluation
- Evaluacion II Bimetre 4TODocument2 pagesEvaluacion II Bimetre 4TOJose LuisPas encore d'évaluation
- Triptico Acido FosforicoDocument3 pagesTriptico Acido FosforicoDIANA GARCÉSPas encore d'évaluation
- 2021 05 31 16 37 22 1118362234 Quimica - Guia 2.2Document10 pages2021 05 31 16 37 22 1118362234 Quimica - Guia 2.2Jhon Esneider Brand PimentelPas encore d'évaluation
- Taller 1 Sobre Esfuerzo, Deformación.Document2 pagesTaller 1 Sobre Esfuerzo, Deformación.Julio Mario Zuñiga EcheverriaPas encore d'évaluation
- Informe 2Document7 pagesInforme 2JeanPas encore d'évaluation
- Mesón de CocinaDocument7 pagesMesón de CocinaBlanca AstudilloPas encore d'évaluation
- Actividad AA7-1Document24 pagesActividad AA7-1Natalia CamachoPas encore d'évaluation
- 2,5 - Dimetilfurano Como Biocomponente Energético para La Formulación de Biocombustibles.Document34 pages2,5 - Dimetilfurano Como Biocomponente Energético para La Formulación de Biocombustibles.Gian Percy Lozano Flores0% (1)
- Tipos de SuelosDocument31 pagesTipos de SuelosJorge Andrés RíosPas encore d'évaluation
- Ciclo Del FosforoDocument25 pagesCiclo Del FosforoAleejandra Raya100% (1)
- BIOLOGIADocument80 pagesBIOLOGIAFa GaviñoPas encore d'évaluation
- FichaTécnica EscamaBlancaDocument10 pagesFichaTécnica EscamaBlancaMauricio RocketPas encore d'évaluation
- CalorimetríaentalpiaDocument12 pagesCalorimetríaentalpiaNataly Neira GuzmánPas encore d'évaluation
- Cuestionario Sobre Estructura y Energética Del EcosistemaDocument5 pagesCuestionario Sobre Estructura y Energética Del EcosistemaCeci ArteagaPas encore d'évaluation
- Pimienta PDFDocument2 pagesPimienta PDFhosin humiriPas encore d'évaluation
- Recetas Muy AntiguasDocument18 pagesRecetas Muy AntiguasFernandez JuanPas encore d'évaluation
- El PlomoDocument14 pagesEl Plomosurvive dotaPas encore d'évaluation
- ATMOSFERADocument10 pagesATMOSFERAFidel VladimiroPas encore d'évaluation
- OsmolaridadDocument2 pagesOsmolaridadCarla penalozaPas encore d'évaluation