Académique Documents
Professionnel Documents
Culture Documents
3 - Determinación Del Calor Integral y Calor Diferencial de Solución
Transféré par
Barbara Zamora YustiDescription originale:
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
3 - Determinación Del Calor Integral y Calor Diferencial de Solución
Transféré par
Barbara Zamora YustiDroits d'auteur :
Formats disponibles
1
DETERMINACIÓN EXPERIMENTAL DEL CALOR INTEGRAL Y EL CALOR
DIFERENCIAL DE SOLUCIONES DE CLORURO DE POTASIO
Hincapié, María Mercedes (1237208); Valdez, Julio Cesar (1435462); Zamora, Bárbara (1439083).
23 de marzo de 2018. Departamento de Química – Universidad del Valle.
Resumen. Se llevó a cabo la determinación experimental del calor diferencial de solución empleando como soluto. Para
esto, se empleó un calorímetro para registrar mediciones de temperatura, tras adiciones sucesivas de soluto en 200 mL de
agua. Con los datos obtenidos se obtuvo por medio de: 1) la pendiente del grafico vs moles de soluto y 2) el
gráfico de vs molalidad. Para una de las soluciones estudiadas, los valores de y encontrados
experimentalmente fueron de 82,87 J 12356,32 J/mol, respectivamente, que representan errores relativos del 3,82% y 23,40%
con respecto a lo reportado en la literatura.
Palabras clave: calor integral de solución, calor diferencial de solución, molalidad.
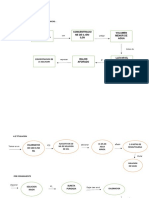
Introducción. La dilución de un soluto en un solvente implica procedimiento llevado a cabo para determinar el calor
cambios energéticos que determinan si la reacción producida es diferencial y el calor integral de solución para en agua.
exotérmica o endotérmica; la cantidad de calor absorbido o
liberado en el proceso se puede calcular mediante calorimetría Metodología. En primer lugar, se realizó la calibración del
adiabática. Para lo anterior se utiliza la siguiente ecuación: calorímetro que se utilizaría para la determinación experimental
en cuestión; para esto se utilizó agua, sustancia con capacidad
∫ calorífica conocida, a dos temperaturas diferentes. Después, se
El cambio en la entalpía por mol de soluto disuelto varía con la procedió a realizar la determinación de interés midiendo la
dilución y con la temperatura del solvente y, por tanto, es temperatura de la solución contenida en el calorímetro, tras
esencial expresar el cambio entálpico con referencia a la adiciones sucesivas de sobre 200 mL de agua.
concentración de la solución y especificar la temperatura.
Ahora, el calor integral de solución es el cambio entálpico Resultados y discusión. Mediante la ecuación 1 es posible
debido a la disolución de 1 mol de soluto B en un solvente puro obtener los valores para las entalpías de las soluciones de ,
A, para producir una solución de cierta concentración [1], es dichos valores se presentan en la tabla 1. Para ello es necesario
decir: conocer la capacidad calorífica del calorímetro, cuyo valor es
Tabla 1. Entalpías de solución para las soluciones de .
Por otra parte, el calor diferencial de solución se define como el
Entalpía de solución [1] 82,87 J
calor de solución de 1 mol de soluto en una gran cantidad de
Entalpía de solución [2] 175,69 J
solución de concentración conocida, tal que la adición de 1 mol
Entalpía de solución [3] 290,05 J
de solución no altera la concentración apreciablemente. [1]
Entalpía de solución [4] 414,35 J
( ) Entalpía de solución [5] 580,09 J
Una definición análoga viene dada por la diferencia de entalpía
Los números 1, 2, 3, 4 y 5 representan las soluciones cuyos
molar parcial del soluto en la solución menos la entalpía molar
gramos de soluto son 0.5, 1.51, 3.01, 5.01 y 7.51,
del solvente puro:
respectivamente.
( )
Según lo reportado en literatura, la entalpía de solución para
Sin embargo, debido a que resulta imposible medir una molalidad correspondiente a la de la solución [1] es 86,17 J
directamente esta magnitud, se puede demostrar que la a 308.15 K, lo que representa un porcentaje de error relativo del
siguiente fórmula proporciona un método indirecto para dicha 3,82%.[4]
determinación:
( ) Por otro lado, los calores integrales de solución para las
soluciones correspondientes se muestran en la tabla 2.
Para el estudio de modelos de soluciones electrolíticas, el
conocimiento de la dependencia de la concentración con la Tabla 2. Calores integrales de las soluciones de
entalpía de solución es necesario.[2] Sin embargo, se encuentra Calor integral de solución [1] 12356,32 J/mol
una deficiencia de información acerca del comportamiento Calor integral de solución [2] 8673,97 J/mol
termodinámico de soluciones acuosas de cloruros de metales Calor integral de solución [3] 7183,91 J/mol
alcalinos, particularmente, de entalpías de solución Calor integral de solución [4] 6165,83 J/mol
experimentales en ciertos rangos de molalidad.[3] Por todo lo Calor integral de solución [5] 5758,60 J/mol
anterior, este documento expone, de forma detallada, el
2
De forma análoga, el calor integral para una molalidad Los valores de calor diferencial de solución calculados
correspondiente a la de la solución [1] es 16130 J/mol a 308.15 mediante las Ec. 4 para el primer método se presentan en la
K, lo que representa un porcentaje de error relativo del Tabla 3 y los calculados mediante las Ec. 5 para el segundo
23,40%.[4] método en la Tabla 4.
Lo anterior podría ser consecuencia de la dependencia de la Tabla 3. Calores diferenciales de las soluciones de calculados a
entalpía de solución con las variables iniciales, es decir con la partir del método 1.
Calor diferencial [1] 6152,13 J/mol
concentración y con la temperatura del solvente.
Calor diferencial [2] 5877,28 J/mol
Sanahuja reporta una serie de calores integrales para soluciones Calor diferencial [3] 5469,07 J/mol
Calor diferencial [4] 4924,81 J/mol
de en un rango de molalidades entre 0,01 y 0,07 mol/Kg a
Calor diferencial [5] 4244,47 J/mol
308.15 K, el rango de esta magnitud varía entre 15790,00 y
16330,00 J/mol y, por tanto, podría esperarse que, a
Tabla 4. Calores diferenciales de las soluciones de calculados a
concentraciones cercanas a las reportadas, el valor del calor partir del método 2.
integral de solución encontrado experimentalmente sea cercano Calor diferencial [1] 8888,06 J/mol
a los valores de dicho rango. Para la solución [2] se realizaron Calor diferencial [2] 6145,67 J/mol
medidas repetidas y el calor integral promedio calculado fue de Calor diferencial [3] 5108,29 J/mol
15514,52 KJ/mol, que es un valor relativamente cercano al Calor diferencial [4] 4371,66 J/mol
valor más pequeño del rango reportado en la literatura. Lo Calor diferencial [5] 4160,58 J/mol
anterior deja claro que, además de la dependencia de las
magnitudes termodinámicas estudiadas con las condiciones En la Figura 2 se puede observar que para molalidades
iniciales, los datos son muy sensibles y, por tanto, fluctúan pequeñas, la pendiente de la gráfica cambia bruscamente y, por
mucho de experimento a experimento y para obtener valores tanto, también lo hace el calor diferencial de solución, lo que
con errores más pequeños resulta conveniente realizar varias evidencia experimentalmente que, en efecto, las variables
medidas. iniciales desarrollan un papel importante en el tratamiento
matemático para los datos obtenidos.
Finalmente se calculó el calor diferencial de solución mediante
dos métodos de aproximación, siendo el primero una relación Nótese que el ajuste realizado en la Figura 1 se realizó
entre la entalpia de solución y moles de soluto y el segundo una mediante un polinomio de grado 2 y no uno de grado 1, pues al
relación entre el calor integral de solución y la molalidad. A analizar el cambio de una de las variables graficadas con
continuación de muestran las gráficas con cada uno de los respecto a la otra se habría obtenido una constante y, en
ajustes realizados: términos de interpretación, esto significaría que el calor
diferencial es constante.
Conclusiones. Al determinar experimentalmente los calores
integrales y diferenciales de soluciones de se evidenció que
las principales fuentes de error se relacionan con la
dependencia de la entalpía de solución con la concentración y
la temperatura del solvente; además, se verificó que es posible
realizar la determinación experimental siguiendo el protocolo
empleado en la práctica, pero tomando las debidas precauciones
que permitan minimizar las fuentes de error mencionadas y
realizando medidas repetidas.
Figura 1. Representación gráfica de la entalpía de solución vs. moles Referencias.
de soluto con el ajuste polinómico correspondiente. [1] Tyagi, P. Thermochemistry; Discovery Pub. House, India.
20-21
[2] Chmarzyński, A. Differential enthalpies of solution of LiCl·
H2O, NaCl, KCl, MgCl2· 6H2O, CaCl2· 6H2O, and BaCl2·
2H2O in water at 298.15 K, near the saturation concentration.
Journal of thermal analysis. 45 (1995). 791-798.
[3] Sanahuja, A; Cesari, E. Enthalpy of Solution of KCl and
NaCl in Water at 298.15 K. J. Chem. Thermodyn. 16 (1984),
1195–1202.
[4] Sanahuja, A. Enthalpy of Solution of KCl in Water at
308.15 and 313.15 K. J. Chem. Thermodyn. 17 (1985), 1063–
1066.
Figura 2. Representación gráfica del calor integral de solución vs.
molalidad con el ajuste polinómico correspondiente.
Vous aimerez peut-être aussi
- Calor IntegralDocument5 pagesCalor IntegralMaiira ZeaPas encore d'évaluation
- Calor Integral y Diferencial de Una SoluciónDocument3 pagesCalor Integral y Diferencial de Una SoluciónMarce OrtegaPas encore d'évaluation
- Laboratorio CALOR DIFERENCIAL Y CALOR INTEGRALDocument3 pagesLaboratorio CALOR DIFERENCIAL Y CALOR INTEGRALISABELLA OROZCO SANTAPas encore d'évaluation
- Determinacion Del Coeficiente de Difusion en Un Gel de Azul de BromofenolDocument5 pagesDeterminacion Del Coeficiente de Difusion en Un Gel de Azul de BromofenolSebastian ViverosPas encore d'évaluation
- Informe ConductimetriaDocument12 pagesInforme ConductimetriaRoslianaPas encore d'évaluation
- Practica 9 Ley de HessDocument10 pagesPractica 9 Ley de Hessaida13012002Pas encore d'évaluation
- Urea ReporteDocument4 pagesUrea ReporteEduardo SuarezPas encore d'évaluation
- Adsorcion de Sustancia DisueltaDocument2 pagesAdsorcion de Sustancia DisueltaLeonardo Medina GermanottaPas encore d'évaluation
- INFORME 5 Ley de HessDocument12 pagesINFORME 5 Ley de HessLinaMarHernandezPerez100% (2)
- Informe 2Document6 pagesInforme 2tata1234-33Pas encore d'évaluation
- Laboratorio de Fisicoquimica IIDocument18 pagesLaboratorio de Fisicoquimica IIluis alvarezPas encore d'évaluation
- Práctica 6. Predicciòn de La Espontaniedad de Las Reacciones RedoxDocument3 pagesPráctica 6. Predicciòn de La Espontaniedad de Las Reacciones RedoxIrving GarciaPas encore d'évaluation
- Informe de Haluros de AlquiloDocument11 pagesInforme de Haluros de AlquiloFiorella Juarez ArevaloPas encore d'évaluation
- Determinación de La Constante de Equilibrio para Una Reacción HomogéneaDocument4 pagesDeterminación de La Constante de Equilibrio para Una Reacción HomogéneaÓscar Eduardo Castro100% (1)
- Laboratorio 1 Calor Integral y Calor Diferencial de SolucionDocument3 pagesLaboratorio 1 Calor Integral y Calor Diferencial de SolucionDANNA VALENTINA CARDENAS CALDERONPas encore d'évaluation
- Cálculos Coeficiente de ParticiónDocument6 pagesCálculos Coeficiente de ParticiónHolly CastroPas encore d'évaluation
- Masa Molecular de Una Sustancia VolátilDocument16 pagesMasa Molecular de Una Sustancia VolátilKevin CPas encore d'évaluation
- CompletoDocument439 pagesCompletoJuan Carlos Vazquez80% (5)
- Lab.1.Fq - Determinacion Del Peso Molecularde La Urea Utilizando Propiedades ColigativasDocument4 pagesLab.1.Fq - Determinacion Del Peso Molecularde La Urea Utilizando Propiedades ColigativasElbaArauz0% (1)
- FQ2 Tarea 3Document27 pagesFQ2 Tarea 3Brenda GallegosPas encore d'évaluation
- Cristal VioletaDocument8 pagesCristal VioletaMelissa QuinteroPas encore d'évaluation
- Problema 3 AnalisisDocument3 pagesProblema 3 AnalisisRAMO ZENITRAMPas encore d'évaluation
- Fuerza Iónica y Coeficiente de Actividad de ElectrolitosDocument23 pagesFuerza Iónica y Coeficiente de Actividad de ElectrolitosYesika Almanza100% (1)
- Reporte P3. Punto de Fusión y Sublimación - Equipo 6 - 1101 - BQD - Lab. QO IDocument22 pagesReporte P3. Punto de Fusión y Sublimación - Equipo 6 - 1101 - BQD - Lab. QO Ileonardo Ibañez PardinesPas encore d'évaluation
- VALORACION CON DOS INDICADORES (Grupo 2)Document8 pagesVALORACION CON DOS INDICADORES (Grupo 2)SOFIA MELENDEZ RODRIGUEZPas encore d'évaluation
- Bromo Por ElectrolisisDocument8 pagesBromo Por ElectrolisisDaira Torrico MeleanPas encore d'évaluation
- Practica 3 FisicoquimicaDocument7 pagesPractica 3 FisicoquimicaQuique RosasPas encore d'évaluation
- Articulo 3. Determinacion de La Curva de Solubilidad para Nitrato de Potasio y Otra SalDocument11 pagesArticulo 3. Determinacion de La Curva de Solubilidad para Nitrato de Potasio y Otra SalCristian Sair Garcés NaranjoPas encore d'évaluation
- Analisis Elemental Cualitativo ValenDocument5 pagesAnalisis Elemental Cualitativo ValenCatalina Duque HenaoPas encore d'évaluation
- Práctica 20. Eficiencia de AntiacidosDocument4 pagesPráctica 20. Eficiencia de AntiacidosOxana ShtefanPas encore d'évaluation
- Informe Destilaccion Sencilla y FraccionadaDocument8 pagesInforme Destilaccion Sencilla y FraccionadaJess Lozada PantojaPas encore d'évaluation
- Determinación de La Constante de EquilibrioDocument7 pagesDeterminación de La Constante de EquilibrioSOFIA MELENDEZ RODRIGUEZPas encore d'évaluation
- 16 ProblemarioDocument8 pages16 ProblemarioLEONEL CRUZ ORTIZPas encore d'évaluation
- Reporte Bromuro de N-ButiloDocument4 pagesReporte Bromuro de N-ButiloEduardo Hernández HuertaPas encore d'évaluation
- Reporte, Practica 2 (Polvos) .Document8 pagesReporte, Practica 2 (Polvos) .Adriana MarinPas encore d'évaluation
- Determinación Espetrofotométrica de Una Constante de EquilibrioDocument8 pagesDeterminación Espetrofotométrica de Una Constante de EquilibrioAlvaro Etcheverry67% (3)
- Informe de Fuerza IonicaDocument16 pagesInforme de Fuerza IonicaKriz Tinita MirandaPas encore d'évaluation
- Determinación de La Constante de EquilibrioDocument12 pagesDeterminación de La Constante de EquilibrioAndrea GonzálezPas encore d'évaluation
- Practica 1.-Determinacion de La Tensión Superficial PDFDocument13 pagesPractica 1.-Determinacion de La Tensión Superficial PDFerikaPas encore d'évaluation
- AASDocument2 pagesAASJorge WhitePas encore d'évaluation
- Estudio de La Influencia de La Concentración Del Ion Hidronio en La Velocidad de Reacción Del Magnesio Con Los Ácidos HCL y H2so4 WuuuDocument17 pagesEstudio de La Influencia de La Concentración Del Ion Hidronio en La Velocidad de Reacción Del Magnesio Con Los Ácidos HCL y H2so4 WuuuwillaimPas encore d'évaluation
- 4. Complejos Con Ligandos Areno Π-EnlazadosDocument2 pages4. Complejos Con Ligandos Areno Π-EnlazadosYesica NarvaezPas encore d'évaluation
- Cinetica de Reaccion Entre Un Ester Con El Ion HidroxiloDocument3 pagesCinetica de Reaccion Entre Un Ester Con El Ion HidroxiloLeonardo Medina GermanottaPas encore d'évaluation
- Practica 2.determinación de La Masa Molar de Un Líquido VolátilDocument5 pagesPractica 2.determinación de La Masa Molar de Un Líquido VolátilabruPas encore d'évaluation
- Analisis Cualitativo Marcha de CationesDocument10 pagesAnalisis Cualitativo Marcha de CationesAna C. Ramirez0% (1)
- Taller 8 EdtaDocument2 pagesTaller 8 EdtaSEBASTIAN GRAJALES HENAOPas encore d'évaluation
- Practica No.4 Volumenes Molares ParcialesDocument10 pagesPractica No.4 Volumenes Molares ParcialesAldo Ilyan Perez MendezPas encore d'évaluation
- Medidas y Evaporación de Solución SalinaDocument11 pagesMedidas y Evaporación de Solución SalinaCatalina Suarez MurciaPas encore d'évaluation
- Diagrama de Flujo-DisolucionesDocument2 pagesDiagrama de Flujo-DisolucionesLisbeth Camila MosqueraPas encore d'évaluation
- Practica 5 - Lab II - FENOLDocument8 pagesPractica 5 - Lab II - FENOLJulio BarrancoPas encore d'évaluation
- Serie 5 SqiDocument4 pagesSerie 5 SqiEduardo ValenzuelaPas encore d'évaluation
- Informe 4 OrgánicaDocument8 pagesInforme 4 OrgánicaAldair ArenaPas encore d'évaluation
- Problemas TermoelectroquímicaDocument15 pagesProblemas TermoelectroquímicaIsmael Cristóbal MarcosPas encore d'évaluation
- Tarea 1 - MasDocument21 pagesTarea 1 - MasDiana AvilaPas encore d'évaluation
- Problemario 1Document3 pagesProblemario 1JorgePas encore d'évaluation
- Sintesis de Cloruro de Ter ButiloDocument7 pagesSintesis de Cloruro de Ter ButiloValentinaToroPas encore d'évaluation
- Informe 3 Lab Quimica UnivalleDocument5 pagesInforme 3 Lab Quimica Univallejuanpis100% (2)
- Informe 6 - Calor Diferencial de SoluciónDocument4 pagesInforme 6 - Calor Diferencial de SolucióndarlellyPas encore d'évaluation
- SolubilidadDocument7 pagesSolubilidadMariaPas encore d'évaluation
- Informe 11 - G2Document9 pagesInforme 11 - G2Jaime Beltran RamirezPas encore d'évaluation
- Manual Condiciones Del Servicio EcocapitalDocument12 pagesManual Condiciones Del Servicio EcocapitalJorge Alonso Medina BustosPas encore d'évaluation
- Semana 10 - PAE en Trastornos o Complicaciones de OtorrinolaringologiaDocument4 pagesSemana 10 - PAE en Trastornos o Complicaciones de OtorrinolaringologiaAriana LizbethPas encore d'évaluation
- Sílabo Cátedra Integrado V Ciclo.Document32 pagesSílabo Cátedra Integrado V Ciclo.FREDY CERDAPas encore d'évaluation
- Ejercicios Sistemas OperativosDocument7 pagesEjercicios Sistemas OperativosJuan Antonio Muñoz Platero100% (1)
- Sistema de Control EscolarDocument4 pagesSistema de Control EscolarfubuolarsPas encore d'évaluation
- La Arquitectura BarrocaDocument36 pagesLa Arquitectura BarrocaPérezPas encore d'évaluation
- Pme 2019Document42 pagesPme 2019enidfuentealba966650% (2)
- Triptico ProteinasDocument2 pagesTriptico ProteinasFrank GraterolPas encore d'évaluation
- El Verbo para Segundo de PrimariaDocument5 pagesEl Verbo para Segundo de PrimariaSusana SenaPas encore d'évaluation
- Tecnotray Carola Tipo MallaDocument16 pagesTecnotray Carola Tipo MallaRicardo Juárez RuizPas encore d'évaluation
- Figaro On-Line (Materias)Document4 pagesFigaro On-Line (Materias)Julieta BlancoPas encore d'évaluation
- Entre VistaDocument1 pageEntre VistaSabriMarconiPas encore d'évaluation
- Plan de NegocioDocument30 pagesPlan de Negociochewicr7Pas encore d'évaluation
- Eurocodigo 5 1995-1997Document110 pagesEurocodigo 5 1995-1997Andrés Zardo García100% (7)
- Nellie Bly, Periodista y ReporteraDocument50 pagesNellie Bly, Periodista y ReporteraRed Ética Segura - FNPI100% (1)
- Estudio Evaluativo de Los Hábitos de Hidratación en Estudiantes de Educación FisicaDocument11 pagesEstudio Evaluativo de Los Hábitos de Hidratación en Estudiantes de Educación FisicaMauricio Hernández MartínezPas encore d'évaluation
- Paul Washer Libro Escato - 15Document13 pagesPaul Washer Libro Escato - 15Franklin Moreira100% (2)
- EWAN PTAct 7 2 8-InstructorDocument4 pagesEWAN PTAct 7 2 8-InstructorlinkeanPas encore d'évaluation
- Protocolo de Presentación de Tesis v4.3Document45 pagesProtocolo de Presentación de Tesis v4.3jhosmerPas encore d'évaluation
- D - Sector 03Document66 pagesD - Sector 03Carlos Esteban VictorioPas encore d'évaluation
- Tarea 2Document4 pagesTarea 2Velkis MadridPas encore d'évaluation
- SGI-For-V01-020 - Cuestionario de Evaluación de Riesgos Psicosociales en El Trabajo (CoPsoQ)Document7 pagesSGI-For-V01-020 - Cuestionario de Evaluación de Riesgos Psicosociales en El Trabajo (CoPsoQ)KynderNorabuenaFigueroaPas encore d'évaluation
- Eje 3 Actividad EvaluativaDocument6 pagesEje 3 Actividad EvaluativaDiego mayorgaPas encore d'évaluation
- Cronograma Plan Salud OcupacionalDocument2 pagesCronograma Plan Salud OcupacionalAlex Orozco100% (1)
- TAREADocument14 pagesTAREAgladys castilloPas encore d'évaluation
- Silabo Inv Cuali PDFDocument9 pagesSilabo Inv Cuali PDFbethsy liliana serrano mariñoPas encore d'évaluation
- Rúbrica para Evaluar DispositivoDocument1 pageRúbrica para Evaluar DispositivoDennis Mendez100% (1)
- Construcción de Terraplenes PDFDocument5 pagesConstrucción de Terraplenes PDFDaniel HuancaPas encore d'évaluation
- Ejer Cici OsDocument24 pagesEjer Cici OsKaren GarayPas encore d'évaluation
- Triptico Beneficios Del Jengibre Al MetabolismoDocument2 pagesTriptico Beneficios Del Jengibre Al MetabolismoJesúsPas encore d'évaluation