Académique Documents
Professionnel Documents
Culture Documents
Anexo 28 PO06 SS LABS P002 Control de Datos PDF
Transféré par
ca_rl_4Titre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Anexo 28 PO06 SS LABS P002 Control de Datos PDF
Transféré par
ca_rl_4Droits d'auteur :
Formats disponibles
LABORATORIOS CÓDIGO: PO06-SS-LABS-P002
INSTITUTO NACIONAL DE VIGILANCIA
DE MEDICAMENTOS Y ALIMENTOS
INVIMA VERSIÓN: 01
CONTROL DE DATOS VIGENTE: 2015-11-23
1. OBJETIVO
Establecer y documentar los requisitos que permitan garantizar el control y protección de los
datos, la seguridad de la información electrónica derivada de actividades analíticas y la validación
del software desarrollado internamente (Hojas de Cálculo en Excel), asegurando la confiabilidad y
trazabilidad de los datos emitidos por los Laboratorios de la Oficina de Laboratorios y Control de
Calidad.
2. ALCANCE
Aplica para la información electrónica derivada de actividades analíticas y la validación de los
software desarrollados (Hojas de Cálculo en Excel) por los laboratorios del INVIMA.
3. DEFINICIONES Y ABREVIATURAS
DATO: Es una representación simbólica (numérica, alfabética, algorítmica, etc.), un atributo o una
característica, que no tiene valor semántico (sentido) en sí mismo, pero que si recibe un
tratamiento y/o procesamiento apropiado, se puede utilizar en la realización de cálculos o toma de
decisiones.
DATO DE PRUEBA: Dato o conjunto de datos, con el que se verifica o valida la hoja de cálculo,
este dato de prueba puede corresponder a un dato que previamente ha sido trabajado en la hoja
de cálculo, o a datos no trabajados pero que son de similar orden para los que fue diseñada la hoja
de cálculo.
EQUIPO AUTOMATIZADO: Equipo de medición al que se le ha adaptado un programa de
computador para el recibo de la señal del detector, procesar los datos y producir un informe que
contenga la información resultante.
EVIDENCIA OBJETIVA: Datos que respaldan la existencia o veracidad de algo.
FUENTE DE DATOS: Identificación del ítem de ensayo.
INFORMACIÓN: Datos que poseen significado.
PRUEBA DE ESCRITORIO: Prueba manual que se realiza para comparar los resultados arrojados
por la hoja de cálculo y los datos obtenidos de forma manual.
SOFTWARE: Se conoce como software al equipamiento lógico o soporte lógico de una
computadora digital; comprende el conjunto de los componentes lógicos necesarios que hacen
posible la realización de tareas específicas.
lcifuentesf/mrochas/merazor/kdiaza/ avelar/jterrerosv/ediazs/
REVISÓ: APROBÓ:
loteroc/orodriguezr/mprietom jfonsecaf/olopezl/dmesal
Código:PO06-SS-LABS-P002 Versión:01 Página 1 de 6
SOFTWARE DESARROLLADO EN EL LABORATORIO: Corresponde a las Hojas de cálculo en
Excel, u otro programa, creado según las indicaciones y requisitos del laboratorio.
TRANSFERENCIA DE DATOS: Está representado por el traspaso de información de un
determinado soporte a otro, por medio físico y/o magnético. De igual forma, puede corresponder al
envío y/o recepción de datos a través de algún medio en una red o a través de un puerto.
TRAZABILIDAD: Propiedad del resultado de una medida o del valor de un estándar donde éste
pueda estar relacionado con referencias especificadas, usualmente estándares nacionales o
internacionales, a través de una cadena continúa de comparaciones todas con incertidumbres
especificadas.
VALIDACIÓN DE SOFTWARE: Documento evidencia que provee un alto grado de aseguramiento
que los sistemas computarizados de análisis, controles y datos grabados correctamente y que los
datos procesados cumplan con especificaciones predeterminadas.
VERIFICACIÓN DE SOFTWARE: Aplicación de métodos, procedimientos, test y otras
evaluaciones, para determinar el cumplimiento de los principios de validación.
4. REFERENCIAS
INSTITUTO COLOMBIANO DE NORMAS TÉCNICAS Y CERTIFICACIÓN. 2005. Requisitos
generales para la competencia de los laboratorios de ensayo y calibración – NTC-ISO/IEC
17025:2005Numeral 5.4.7.ICONTEC. Bogotá, Colombia.
NTC-ISO 9000. Sistemas de Gestión de la Calidad. Fundamentos y Vocabulario. 2000-12-15
Garfield, F. Principios de Garantía de calidad para laboratorios analíticos. AOAC Internacional 1993
Pág. 57-60.
ENGL (EUROPEAN NETWORK OF GMO LABORATORIES). 2011. Guía de verificación de
métodos analíticos para evaluar OGM´s cuando se implementan métodos validados por
interlaboratorio.
INSTITUTO COLOMBIANO DE NORMAS TECNICAS Y CERTIFICACIÓN. 2009 Norma Técnica
de Calidad en la Gestión Pública (NTCGP 1000:2009) ICONTEC. Bogotá, Colombia.
INSTITUTO NACIONAL DE VIGILANCIA DE MEDICAMENTOS Y ALIMENTOS. INVIMA. 2010.
Control de Datos. PA06-GM-403-P002.Versión 03. INVIMA. Bogotá, Colombia
INSTITUTO NACIONAL DE VIGILANCIA DE MEDICAMENTOS Y ALIMENTOS. INVIMA. 2012.
Control de Datos.PO06-SS-603-P002.Versión 02. INVIMA. Bogotá, Colombia
INSTITUTO NACIONAL DE VIGILANCIA DE MEDICAMENTOS Y ALIMENTOS. INVIMA. 2014.
Control de Datos.PO06-SS-LABS-P002.Versión 00. INVIMA. Bogotá, Colombia
Technical Considerations for the Validation of Electronic Spreadsheets for Complying with 21 CFR
Part 11.Tuan T Phan, Pharmaceutical TechnologyJANUARY 2003.
ORGANIZACION MUNDIAL DE LA SALUD. OMS. Informe 40, informe de expertos de la OMS, en
especificaciones para preparaciones farmacéuticas: guía suplementaria y buenas prácticas de
fabricación: validación de sistemas computarizados. Apéndice 5 anexo 4, serie de informes
técnicos 937. Ginebra-Suiza.
Código:PO06-SS-LABS-P002 Versión:01 Página 2 de 6
5. RESPONSABILIDADES
Es responsabilidad del Coordinador y/o Líder Técnico de cada Laboratorio de la Oficina de
Laboratorios y Control de Calidad velar por el cumplimiento de este procedimiento. Igualmente los
profesionales del laboratorio y los facilitadores de calidad tienen la responsabilidad de seguir los
lineamientos descritos en este procedimiento.
6. CONDICIONES PREVIAS
Para la aplicación de este procedimiento se hace necesario seguir el procedimiento PE02-GC-
LABS-P002 Control de Registros.
La confidencialidad e integridad de los datos generados como producto de las actividades del
laboratorio se asegura mediante los lineamientos establecidos en el procedimiento PE01-GD-
LABS-P002 Confidencialidad, Protección de la Información Confidencial, Imparcialidad e
Integridad.
Se requiere conocer los manuales de uso, instructivos o guías operativas del manejo de los
equipos automatizados y su software. El software de manejo de los equipos automatizados debe
haberse adquirido de manera legal con las licencias de fábrica, garantizando que ha sido validado
y es adecuado para el uso.
Adicionalmente, los representantes autorizados por los fabricantes de los equipos deben garantizar
la realización del mantenimiento preventivo, correctivo, calibración y/o la calificación del equipo,
computador (cuando aplique) y que se realice una verificación del funcionamiento del software.
Los equipos automatizados solamente se pueden operar por personal autorizado o con acceso
permitido para su manejo.
Las instalaciones del laboratorio deben proveer las condiciones ambientales y de operación
adecuadas para preservar la integridad de los datos.
Se realizan mantenimientos preventivo, correctivos y las calificaciones de los equipos, incluidos el
computador (cuando aplique) y el software con proveedores autorizados de acuerdo con la
frecuencia estipulada en el PA06-GM-LABS-F003 Plan de Control de Equipos o Instrumentos.
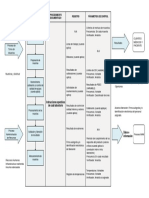
7. PROCEDIMIENTO
No. Descripción Responsable
1 Inicio
CONTROL DE DATOS, SEGURIDAD Y RESGUARDO DE LA INFORMACIÓN:
La integridad y confidencialidad de la entrada o recopilación de
los datos, almacenamiento y backup, se encuentran definidos Analistas,
bajo los lineamientos del PE02-GC-LABS-P002 Procedimiento Líder técnico,
2 de control de registros. Facilitador de Calidad,
Coordinación de
Laboratorio
Todo registro electrónico, donde la pérdida o modificación de
su información coloque en duda el cumplimiento o la
demostración de las actividades relacionadas con el mismo,
Código:PO06-SS-LABS-P002 Versión:01 Página 3 de 6
No. Descripción Responsable
son responsabilidad del personal que diligencie este tipo de
registro.
La transferencia de los datos del cuaderno o formatos de datos
primarios analíticos a las hojas de cálculo, o de las hojas de
cálculo a los formatos o cuaderno, según corresponda, debe
ser revisada por el Líder Técnico, de acuerdo a lineamientos de
cada laboratorio.
Los archivos con datos de métodos, curvas de calibración y
lectura de muestras en equipos automatizados son
responsabilidad de los profesionales que hagan uso de esta
información y deben archivar el soporte en carpeta; el Líder
técnico tiene a su cargo el seguimiento al cumplimiento de
dichas actividades.
Los registros de datos que se han diligenciado en su totalidad,
pueden ser impresos o escaneados para evitar que la
información consignada sea alterada.
Cuando se empleen hojas de cálculo como registro de datos,
se debe realizar protección y/o bloqueo interno de las celdas
que incluyen las fórmulas de cálculo, celdas que no sean
requeridas para diligenciamiento y de aquellas ya diligenciadas,
de tal manera que no se puedan modificar.
Los datos de análisis que se almacenan en los equipos de
cómputo y software de manejo de los equipos se deben
organizar de tal manera que para impresiones de pantallazos
(cuando corresponda) permitan su fácil ubicación y
recuperación, manteniendo la trazabilidad de los datos y
muestras. La organización de los archivos depende de las
características del software y por tanto, es específica para cada
equipo.
PROTECCIÓN DE EQUIPOS AUTOMATIZADOS
Todos los equipos automatizados en cuanto sea técnicamente
posible, deben protegerse con una clave de acceso. En los
casos donde el software no permita la inclusión de clave de
acceso, el ingreso al equipo se controla con la clave de acceso
del computador.
Solo la persona designada por cada laboratorio puede acceder Líder
3 al sistema como administrador; el personal analista puede Técnico/Analista/Personal
acceder al equipo a través de las cuentas de usuario con designado
acceso limitado con el fin de evitar la modificación de
resultados. Las cuentas de usuario son creadas por el perfil de
administrador.
Las claves de administrador y acceso de usuarios deben ser
registradas en el Listado de claves de acceso.
Código:PO06-SS-LABS-P002 Versión:01 Página 4 de 6
No. Descripción Responsable
Para el caso de los laboratorios de Productos Farmacéuticos y
otras Tecnologías y de Productos Biológicos, la adquisición de
equipos automatizados que procesen o emitan información que
afecten los resultados analíticos debe incluir un ítem en los
requisitos o características técnicas, que establezca el
cumplimiento con la norma CFR 21 parte 11. Si el equipo es un
Cromatógrafo de Gases o HPLC, adicionalmente se incluye
que el software cuente con la opción AUDIT TRAIL activada.
Así mismo, en el momento de la instalación se requiere al
proveedor crear cuentas de administrador y de usuarios.
VALIDACIÓN DE HOJAS DE CÁLCULO EN EXCEL
El Líder Técnico asigna a los profesionales analistas, la
validación o verificación de las hojas de cálculo.
Definir en el alcance de validación de la hoja de cálculo, el
conjunto de datos de prueba (mínimo tres conjuntos de datos).
La validación de las hojas de cálculo se realiza cuando se crea
la hoja de cálculo y cada vez que se requiera un cambio de
versión del formato.
Validación:
Ingresar los datos de prueba en la hoja de cálculo en Líder técnico/ Analistas
4 Excel a validar.
Para dejar evidencia de las fórmulas, condicionales,
gráficos, cartas de control, celdas protegidas, accesos,
protecciones, almacenamiento de información incluida
en la hoja de cálculo, etc., imprimir pantallazos, cuando
aplique.
Imprimir las hojas de cálculo, con los resultados.
Realizar los cálculos en forma manual, (por medio de
calculadora) y compararlos con los arrojados por la hoja
de cálculo.
Si los resultados generados durante la validación,
arrojan el concepto no cumple, informar al Líder
Técnico, quien decide las acciones a tomar.
VERIFICACIÓN DE HOJAS DE CALCULO EN EXCEL
De acuerdo a las necesidades del laboratorio se debe
probar/examinar un dato de prueba para verificar que la fórmula
no ha sido modificada, se realiza mínimo una vez al año una
prueba de escritorio para comprobar que se obtiene el mismo
Analistas
5 resultado que con la hoja de cálculo.
Estas actividades las ejecuta un analista autorizado en la
metodología respectiva.
Código:PO06-SS-LABS-P002 Versión:01 Página 5 de 6
No. Descripción Responsable
ELABORACIÓN DE INFORME DE VALIDACION/VERIFICACION
La validación o verificación de la hoja de cálculo en Excel se
registra en el formato PO06-SS-LABS-F002 Informe de
validación/verificación de hojas de cálculo donde se especifica:
- Identificación de la actividad a desarrollar (validación o
verificación)
- Identificación de la hoja de cálculo (Código, nombre y
versión del formato de la hoja de cálculo)
- Fecha de realización de la actividad
- Realizado por
- Fuente de los datos
6 Líder técnico/analistas
- Cálculos correspondientes de la hoja de cálculos,
(pruebas de escritorio) Ver Anexo
- Conclusión de la validación ó verificación (cumple o no
cumple)
- Actividades a desarrollar en caso de que no cumpla
- Observaciones si aplican
- Firma de los responsables de la actividad y fecha
- Firma de los responsables de aprobación y fecha
- Impresiones de pantallazos (cuando corresponda).
Nota: El Líder Técnico es el responsable de aprobar el informe.
7 Fin
8. REGISTROS Y DOCUMENTOS ASOCIADOS
PE02-GC-LABS-P002 Control de Registros
PA06-GM-LABS-F003 Plan de Control de Equipos o Instrumentos.
PO06-SS-LABS-F002 Informe de validación/verificación de hojas de cálculo
9. ANEXOS
Cuadernos de analistas o formatos de datos primarios y hojas de trabajo.
Informe de validación/verificación
Código:PO06-SS-LABS-P002 Versión:01 Página 6 de 6
Vous aimerez peut-être aussi
- Verificación de Balanza. Cuestionario.Document4 pagesVerificación de Balanza. Cuestionario.Kiiaf100% (1)
- Plan de Validación de Método de Ensayo QELAB S.a.C FinalDocument24 pagesPlan de Validación de Método de Ensayo QELAB S.a.C FinalBiSOPPas encore d'évaluation
- Ensayos Aptitud MAACDocument8 pagesEnsayos Aptitud MAACoswaldo morales resendizPas encore d'évaluation
- Manual de Calidad Lab PereiraDocument28 pagesManual de Calidad Lab PereiraMartha BallesterosPas encore d'évaluation
- Procedimiento para La Gestión de Los Riesgos y OportunidadesDocument4 pagesProcedimiento para La Gestión de Los Riesgos y OportunidadesluisPas encore d'évaluation
- 001 Intervalos de CalibracionDocument3 pages001 Intervalos de CalibracionFabian Andres ContrerasPas encore d'évaluation
- EMA - Políticas de Trazabilidad 2016Document18 pagesEMA - Políticas de Trazabilidad 2016Luis TrejoPas encore d'évaluation
- Diagrama FlujoDocument1 pageDiagrama FlujoJesus DominguezPas encore d'évaluation
- FR Programacion GestionDocument3 pagesFR Programacion GestionGuillermo Cortes Silva100% (1)
- Validacion Métodos Analíticos-FMDocument88 pagesValidacion Métodos Analíticos-FMmanuelsnic2820100% (2)
- Validacion en Metodos de MedicionDocument9 pagesValidacion en Metodos de Medicionbyenar0% (1)
- Calibracion Volumen Metodo Gravimetrico Cenam PDFDocument33 pagesCalibracion Volumen Metodo Gravimetrico Cenam PDFJuan Carlos MejiaPas encore d'évaluation
- Resultado intercomparación laboratorios voltaje AC y tiempoDocument7 pagesResultado intercomparación laboratorios voltaje AC y tiempoJuan Manuel PascagazaPas encore d'évaluation
- ISO 17025 procedimientosDocument5 pagesISO 17025 procedimientosGaby RiveraPas encore d'évaluation
- G-EnAC 14 Guia InterlaboratoriosDocument18 pagesG-EnAC 14 Guia InterlaboratoriosPaula Andrea Restrepo OchoaPas encore d'évaluation
- Criterios para Evaluac y Acreditac de Provee de Ensayos de Aptitud Norma 17043 V01Document6 pagesCriterios para Evaluac y Acreditac de Provee de Ensayos de Aptitud Norma 17043 V01Isis MartinezPas encore d'évaluation
- Intervalos de Calibración PDFDocument2 pagesIntervalos de Calibración PDFjennijohanaPas encore d'évaluation
- Curso Aseguramiento de La Calidad Metodo Icp-MsDocument140 pagesCurso Aseguramiento de La Calidad Metodo Icp-Mswilson50% (2)
- P-Sa-85 Guia para La Validacion de Metodos de Ensayo V1-OkDocument26 pagesP-Sa-85 Guia para La Validacion de Metodos de Ensayo V1-OkOLGA MARÍNPas encore d'évaluation
- Informacion Guia M-17025Document9 pagesInformacion Guia M-17025Clau ArandaPas encore d'évaluation
- ML - DIM, ISOTERMOS Y TEMP - MÓDULO 3 - Medios IsotermosDocument41 pagesML - DIM, ISOTERMOS Y TEMP - MÓDULO 3 - Medios IsotermosAndres Felipe Bermudez Rosero - Gr. Reg Ciencias Forenses - Reg. OccidentePas encore d'évaluation
- MP-CA006 Politica TrazabilidadDocument18 pagesMP-CA006 Politica TrazabilidadDaniel CastilloPas encore d'évaluation
- Estimacion de La IncertidumbreDocument11 pagesEstimacion de La IncertidumbrerayPas encore d'évaluation
- Manual de Gestion de Calidad Cap 5Document16 pagesManual de Gestion de Calidad Cap 5Luis AuquillaPas encore d'évaluation
- Manual de Calidad - Stark LabDocument32 pagesManual de Calidad - Stark LabRosmery Elvira Atuncar RojasPas encore d'évaluation
- Calibración de comparadores con bloques patronesDocument8 pagesCalibración de comparadores con bloques patronesCésar Soto SoriaPas encore d'évaluation
- Guia para La Validacion de Metodos de Ensayo PDFDocument11 pagesGuia para La Validacion de Metodos de Ensayo PDFIngeniero Biomédico Rodrigo RodríguezPas encore d'évaluation
- Politica para La Validacion de Metodos de Laboratorios de Ensayo y CalibracionDocument49 pagesPolitica para La Validacion de Metodos de Laboratorios de Ensayo y CalibracionMiriam100% (1)
- 7.2 Seleccion, Verificacion y Validacion de MetodosDocument1 page7.2 Seleccion, Verificacion y Validacion de MetodosDiana ReyPas encore d'évaluation
- Procedimiento de CalibracionDocument12 pagesProcedimiento de Calibracionluisefedj100% (2)
- MC-DT-P-002 Procedimiento Estimacion IncertidumbreDocument8 pagesMC-DT-P-002 Procedimiento Estimacion IncertidumbreDireccion TecnicaPas encore d'évaluation
- Procedimiento de Recepción y Manipulación de Ítem Bajo CalibraciónDocument3 pagesProcedimiento de Recepción y Manipulación de Ítem Bajo CalibraciónJesse Watson50% (4)
- Procedimientos Documentados ISO 17025Document3 pagesProcedimientos Documentados ISO 17025adiazcalidadPas encore d'évaluation
- ESTABILIZACIÓN PLANCHAS CALENTAMIENTODocument5 pagesESTABILIZACIÓN PLANCHAS CALENTAMIENTOErick Michael GarciaPas encore d'évaluation
- Evaluar la incertidumbre de mediciones químicasDocument6 pagesEvaluar la incertidumbre de mediciones químicasPaola FrancoPas encore d'évaluation
- Aseguramiento de La Validez de Los ResultadosDocument14 pagesAseguramiento de La Validez de Los Resultadosdaimerjosetorresgale100% (1)
- Verificación de MicropipetasDocument8 pagesVerificación de MicropipetasANGIE GERALDINE ROJAS AMADOPas encore d'évaluation
- Pd-A-Apv-19 Procedimiento de Validación de MetodosDocument10 pagesPd-A-Apv-19 Procedimiento de Validación de MetodosCecilia AvilaPas encore d'évaluation
- INTERLABORATORIODocument138 pagesINTERLABORATORIOharold david gil muñozPas encore d'évaluation
- Procedimiento para Trazabilidad de Las MedicionesDocument9 pagesProcedimiento para Trazabilidad de Las MedicionesNairo vianchaPas encore d'évaluation
- Criterios Generales de Balanzas y Pesas, Interpretación de Certificados de CalibraciónDocument44 pagesCriterios Generales de Balanzas y Pesas, Interpretación de Certificados de CalibraciónPaul CruzPas encore d'évaluation
- 8.9 Revision Por La DirecciónDocument2 pages8.9 Revision Por La Direcciónkarla aguilarPas encore d'évaluation
- Procedimiento para Control de Trabajos de Ensayo No ConformeDocument5 pagesProcedimiento para Control de Trabajos de Ensayo No ConformeFrancisco VargasPas encore d'évaluation
- Cálculos de validación de métodos analíticos en ExcelDocument33 pagesCálculos de validación de métodos analíticos en ExcelAida SayaPas encore d'évaluation
- Ensayos InterlaboratorioDocument36 pagesEnsayos InterlaboratorioDiego PuentesPas encore d'évaluation
- InterpretaciDocument22 pagesInterpretaciSofia RodriguezPas encore d'évaluation
- CalibracionDocument48 pagesCalibracionorozco_guerrero_fcoPas encore d'évaluation
- Validacion y Verificacion de Metodos de PDFDocument8 pagesValidacion y Verificacion de Metodos de PDFAnonymous qKeDFDPas encore d'évaluation
- Cursos AI ISO IEC 17025 2005 AL Rev 2013 03Document122 pagesCursos AI ISO IEC 17025 2005 AL Rev 2013 03Diego Fernado AvendañoPas encore d'évaluation
- Cea-3 0-02 Trazabilidad Metrológica V5 1 PDFDocument21 pagesCea-3 0-02 Trazabilidad Metrológica V5 1 PDFrugthier.connie5611Pas encore d'évaluation
- PRO - 13 Evaluación de La Calidad de Los Ensayos v4Document10 pagesPRO - 13 Evaluación de La Calidad de Los Ensayos v4resp 4922Pas encore d'évaluation
- Interpretacion Certificados y Determinacion Intervalos de CalibracionDocument43 pagesInterpretacion Certificados y Determinacion Intervalos de CalibracionDiamirPas encore d'évaluation
- Aseguramiento de la calidad en laboratorios de ensayoDocument18 pagesAseguramiento de la calidad en laboratorios de ensayoBiSOPPas encore d'évaluation
- Manual de Validación de MétodosDocument14 pagesManual de Validación de MétodosLaboratorio100% (1)
- TF CIE 01 Cronometros y TemporizadoresDocument15 pagesTF CIE 01 Cronometros y TemporizadoresAKCHPas encore d'évaluation
- VerifPipetasBuretasFiolasDocument2 pagesVerifPipetasBuretasFiolasExson LaricoPas encore d'évaluation
- Procedimiento para Estimar La Incertidumbre de La MediciónDocument20 pagesProcedimiento para Estimar La Incertidumbre de La MediciónAnonymous YwFJrk0yCPas encore d'évaluation
- Procedimiento para Control de Datos PDFDocument7 pagesProcedimiento para Control de Datos PDFesuarezc_atlPas encore d'évaluation
- ResultadosAnálisisInvimaDocument4 pagesResultadosAnálisisInvimaJhonny BosmedianoPas encore d'évaluation
- 37 Procedimiento para Calibracion de Instrumentos de MedicionDocument12 pages37 Procedimiento para Calibracion de Instrumentos de MedicionYolanda gelvez tarazona100% (1)
- Libro de EmbrioDocument98 pagesLibro de EmbrioGabriel Nicolas Rodriguez NeyraPas encore d'évaluation
- Medición Gravimetrica de HRDocument8 pagesMedición Gravimetrica de HRVer OnischPas encore d'évaluation
- Proteínas - Enzimas - Membrana 54Document108 pagesProteínas - Enzimas - Membrana 54Ver OnischPas encore d'évaluation
- Tutorial - Cómo Proteger Un PendriveDocument2 pagesTutorial - Cómo Proteger Un PendriveVer OnischPas encore d'évaluation
- Amd Apuntes Termodinamica v3 - 0 PDFDocument157 pagesAmd Apuntes Termodinamica v3 - 0 PDFJahira PoncePas encore d'évaluation
- La Guia MetAs 08 09 Termometros Liquido en VidrioDocument8 pagesLa Guia MetAs 08 09 Termometros Liquido en VidrioRawi MontillaPas encore d'évaluation
- Spa 01 ADocument7 pagesSpa 01 AFelelico SalinasPas encore d'évaluation
- Mapeo de Temperatura en AlmacenDocument10 pagesMapeo de Temperatura en AlmacenLeonardo Blanco Caselles100% (1)
- Integracion Fluidos-CompartimientosDocument51 pagesIntegracion Fluidos-CompartimientosGiulliana PaolaPas encore d'évaluation
- Isotherm - KGW Catalogo GeneralDocument22 pagesIsotherm - KGW Catalogo GeneralVer OnischPas encore d'évaluation
- Capurro PDFDocument86 pagesCapurro PDFErika BoniPas encore d'évaluation
- Traduccion Guia DKD R 5 7 Calibracion de Camaras Climaticas 2019Document45 pagesTraduccion Guia DKD R 5 7 Calibracion de Camaras Climaticas 2019vanessa ArenasPas encore d'évaluation
- Gonzalo Martín Vivaldi - Curso de RedacciónDocument561 pagesGonzalo Martín Vivaldi - Curso de RedacciónAnonymous LKmYete100% (1)
- Aleman pdf1 PDFDocument93 pagesAleman pdf1 PDFsoy yo o noPas encore d'évaluation
- Apuntes Guia Tiempos Verbales AlemánDocument9 pagesApuntes Guia Tiempos Verbales AlemánDavid BastidasPas encore d'évaluation
- Metrologia para No Metro LogosDocument146 pagesMetrologia para No Metro Logosjljimenez196995% (20)
- Taller sobre Metrología para países hispanohablantes de la OMMDocument4 pagesTaller sobre Metrología para países hispanohablantes de la OMMVer OnischPas encore d'évaluation
- Udla Ec Tpu 2008 06 2 (S) PDFDocument154 pagesUdla Ec Tpu 2008 06 2 (S) PDFVer OnischPas encore d'évaluation
- Tutorial - Cómo Proteger Un PendriveDocument2 pagesTutorial - Cómo Proteger Un PendriveVer OnischPas encore d'évaluation
- aulaMAS PDFDocument20 pagesaulaMAS PDFTavico CipriPas encore d'évaluation
- Capitulo5 LeydecoulombycampoelectDocument83 pagesCapitulo5 LeydecoulombycampoelectVer OnischPas encore d'évaluation
- Guia Quimica Uba Cap 1 Al 5 - DobleDocument17 pagesGuia Quimica Uba Cap 1 Al 5 - DobleVer OnischPas encore d'évaluation
- Verificación máquinas ensayos ISO normasDocument1 pageVerificación máquinas ensayos ISO normasVer OnischPas encore d'évaluation
- Taller sobre Metrología para países hispanohablantes de la OMMDocument4 pagesTaller sobre Metrología para países hispanohablantes de la OMMVer OnischPas encore d'évaluation
- INFORME Maquinas EnsayoDocument50 pagesINFORME Maquinas EnsayoVer OnischPas encore d'évaluation
- INFORME 2 Maquinas EnsayoDocument4 pagesINFORME 2 Maquinas EnsayoVer OnischPas encore d'évaluation
- Ensayo A TraccionDocument9 pagesEnsayo A Traccionosfa10Pas encore d'évaluation
- Verificación máquinas ensayos ISO normasDocument1 pageVerificación máquinas ensayos ISO normasVer OnischPas encore d'évaluation
- Implantacion Calidad en El Laboratorio de DimenisonalDocument262 pagesImplantacion Calidad en El Laboratorio de DimenisonalVer OnischPas encore d'évaluation
- Site Survey ENodes LTE Huawei Instalar Regiones - 1Document10 pagesSite Survey ENodes LTE Huawei Instalar Regiones - 1carlos chopitePas encore d'évaluation
- Cursor EuskaltelDocument185 pagesCursor EuskaltelSamuel RamosPas encore d'évaluation
- Ataque Lado Del ClienteDocument2 pagesAtaque Lado Del Clientejekatats26Pas encore d'évaluation
- Volquete CA 3256Document46 pagesVolquete CA 3256Heber Arcana67% (3)
- Idioma ChinoDocument10 pagesIdioma Chinoclaudia47Pas encore d'évaluation
- La Escritura Como Plurisistema o Teoría de L1 de Nina Catach PDFDocument11 pagesLa Escritura Como Plurisistema o Teoría de L1 de Nina Catach PDFDaniel Lerena Amilivia100% (2)
- Foro 2 2BDocument3 pagesForo 2 2BDome ObandoPas encore d'évaluation
- Servicio de Voz Sobre IP PDFDocument14 pagesServicio de Voz Sobre IP PDFRafael CarlosPas encore d'évaluation
- PROYECTODocument9 pagesPROYECTOJulio CésarPas encore d'évaluation
- ESItronicDocument0 pageESItronicMarĭo Isaac Manrĭquéz LealPas encore d'évaluation
- Acoplamientos y LevasDocument21 pagesAcoplamientos y LevasDonald Askeland PhulePas encore d'évaluation
- Configuracion DMZDocument112 pagesConfiguracion DMZßùttêŕŦlŷ ŤöẁmPas encore d'évaluation
- Cap. 1 Soldaura Tuberias (Rev)Document22 pagesCap. 1 Soldaura Tuberias (Rev)Erick100% (1)
- Aplicador de BarraDocument1 pageAplicador de BarraRicardo L.Pas encore d'évaluation
- Cotizacion COMUNIDAD ERASMO ESCALA V1.0 - P19112021Document2 pagesCotizacion COMUNIDAD ERASMO ESCALA V1.0 - P19112021Axel Igor Villalonga EscaratePas encore d'évaluation
- Indicador de Peso Indicador de Peso: Descripción Descripción Funciones Principales Funciones PrincipalesDocument3 pagesIndicador de Peso Indicador de Peso: Descripción Descripción Funciones Principales Funciones PrincipalesWilfredo Bravo VidartePas encore d'évaluation
- Mensajes CamelDocument9 pagesMensajes CamelmarcoPas encore d'évaluation
- Une-En - 61386-1 2008Document42 pagesUne-En - 61386-1 2008estiben montoya100% (2)
- 1.2sistemas de MedidaDocument5 pages1.2sistemas de MedidaJuan Jo Z. CHPas encore d'évaluation
- Optix Metro 500 - Hardware DescriptionDocument30 pagesOptix Metro 500 - Hardware DescriptionCarlos AngaritaPas encore d'évaluation
- Técnicas de Interpretación de Lengua de Signos Resumen Tema 10Document6 pagesTécnicas de Interpretación de Lengua de Signos Resumen Tema 10RecursosilsePas encore d'évaluation
- Wp3Pronosticos 2012090507Document7 pagesWp3Pronosticos 2012090507Neal Aro LaraPas encore d'évaluation
- Solera Tarifa Nacional 2022Document131 pagesSolera Tarifa Nacional 2022VEMATELPas encore d'évaluation
- GE Security Incendio y Protección de Vida Vigilant. Innovación. Serie V Sistemas Inteligentes de Protección de VidaDocument6 pagesGE Security Incendio y Protección de Vida Vigilant. Innovación. Serie V Sistemas Inteligentes de Protección de VidaESTEBAN PORRASPas encore d'évaluation
- Migracion WinServer2008to2012Document26 pagesMigracion WinServer2008to2012GeovannyCepedaPas encore d'évaluation
- Iec 62271-100 2014Document358 pagesIec 62271-100 2014juliancansen100% (15)
- Ética en contabilidad y toma de decisionesDocument2 pagesÉtica en contabilidad y toma de decisionesmeli EspinosaPas encore d'évaluation
- Manual Chery Grand Tiggo PDFDocument375 pagesManual Chery Grand Tiggo PDFCristian Troncoso Alarcón86% (14)
- Estructura de La Trama STM 1Document4 pagesEstructura de La Trama STM 1royPas encore d'évaluation
- Términos ISO 9000:2015Document2 pagesTérminos ISO 9000:2015Daluis Gioanni Garcia SanchezPas encore d'évaluation