Académique Documents
Professionnel Documents
Culture Documents
Eva Bim Fís 10° Ivp
Transféré par
Diego Andres GarciaDescription originale:
Titre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Eva Bim Fís 10° Ivp
Transféré par
Diego Andres GarciaDroits d'auteur :
Formats disponibles
DOCENTE: DIEGO ANDRÉS GARCÍA MURCIA FECHA: 20 DE NOVIEMBRE PERIODO: IV
ESTUDIANTE: ASIGNATURA: FÍSICA GRADO: DÉCIMO
DESEMPEÑO(S): REVISADO:
Predice los cambios que pueden suceder en un cuerpo o un sistema al ser expuesto a variaciones de
temperatura y/o transferencia de calor de acuerdo a las leyes de la Termodinámica.
Describe las propiedades de los fenómenos oscilatorios y ondulatorios comprendidos desde las leyes
de la cinemática, dinámica y conservación de energía.
ACTIVIDAD: PRUEBA BIMESTRAL IV PERIODO FECHA: 20 DE NOVIEMBRE
PARTE I. SOLUCIÓN DE PROBLEMAS
1. En un calorímetro ideal 25Kg de agua a 80°C se mezclan con 5Kg. de hielo a –8°C. Determinar la temperatura final de la mezcla.
(Valor 1.0)
2. Un recipiente de vidrio de capacidad 2000 cm³ está lleno de mercurio. Si la temperatura se incrementa en 100°C, el recipiente alcanza
un volumen de 2010cm³. Calcule el volumen de mercurio que se derrama. (Valor 1.0)
3. Una muestra de gas de 100cm3 a la presión de 100Kpa, se calienta isocóricamente desde el punto A hasta el punto B hasta que su
presión es de300Kpa. Después se expande isobáricamente hasta el punto C, donde su volumen es de 400cm 3. La presión disminuye
hasta 100Kpa en el punto D, sin cambio de volumen. Por último regresa a su estado original en el punto A. (Valor 1.0)
A. Construya el diagrama PV.
B. ¿Cuál es el trabajo neto realizado en todo el ciclo?
5. Un gas ideal está encerrado en un cilindro con un émbolo movible sobre él. El émbolo tiene una masa de 8000g. y un área de 5cm2 y
está libre para subir y bajar, manteniendo constante la presión del gas. ¿Cuánto trabajo se realiza sobre el gas cuando la temperatura
de 0.2mol del gas se eleva de 20°C a 300°C? (Valor 1.0)
PARTE II. PREGUNTAS TIPO PRUEBA SABER (Valor 2.0)
1. Cierta cantidad de gas es sometida al siguiente ciclo 3. A un recipiente cerrado que contiene un gas ideal se le
termodinámico. suministra calor por medio de un mechero; si todo el calor se
convierte en energía térmica del gas, se sabe que éste es un
proceso:
A. Isotérmico. B. Isovolumétrico.
C. Adiabático. D. Isobárico.
4. Se tiene un gas encerrado en un recipiente al cual se le
transfiere 400J de calor. Si el gas se expande según el proceso
de 1 a 2, ¿cuál es la su energía interna (J) en el estado 2, si en
el estado 1 es de 100J?
¿Qué cantidad de trabajo se produce en cada realización del
ciclo?
A. 5 PV B. 15 PV C. 20 PV D. 30 PV
2. Un gas se somete a un ciclo termodinámico como se muestra
en la figura.
A.400 B.300 C.200 D.-200 E.-100
5. La primera ley de la termodinámica relaciona las cantidades
físicas de energía interna (ΔE), calor (Q) y trabajo (W = PΔV)
mediante la ecuación Q = ΔE + PΔV, donde P y V son presión y
volumen, respectivamente. A un recipiente cerrado que contiene
un gas ideal se le aísla del exterior y se disminuye su
temperatura, se sabe que éste:
¿Cómo es el valor del trabajo en cada proceso? A. No realiza trabajo porque es un proceso isotérmico.
A. W12 > 0, W23 > 0, W34 < 0, W41 = 0. B. No realiza trabajo porque es un proceso isovolumétrico.
B. W12 > 0, W23 < 0, W34 > 0, W41 = 0. C. Realiza trabajo porque es un proceso adiabático.
C. W12 = 0, W23 < 0, W34 > 0, W41 > 0. D. Realiza trabajo porque es un proceso isobárico.
D. W12 > 0, W23 < 0, W34 < 0, W41 > 0.
6. Dos bloques de masas iguales, calores específicos distintos e De lo anterior se puede afirmar que:
inicialmente a temperaturas distintas, están en contacto térmico A. El calor específico del material A es menor que el del material
y aislados térmicamente del exterior. En relación con esta B puesto que Ce y Q son directamente proporcional.
situación se hacen las siguientes afirmaciones: B. La cantidad de calor es tanto mayor cuanto mayor es la masa
I. Todo el calor que cede el bloque más caliente lo absorbe el a la cual se le está suministrando energía.
más frío. C. Los calores específicos son iguales puesto que alcanzan la
II. La temperatura del bloque más caliente disminuye tanto misma T.
como aumenta la del más frío. Respecto a estas afirmaciones se D. No es posible afirmar cual es mayor puesto que no hay
puede decir que: valores de Q y de T.
A. Solo la II es correcta B. Las dos son incorrecta
C. Ambas son correctas D. Sólo la I es correcta.
8. De la primera ley de la termodinámica se puede concluir que
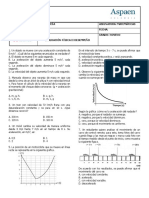
7. La siguiente gráfica representa la variación de la temperatura, durante la compresión, la energía interna del gas permanece
T, para dos cuerpos, A y B del mismo material y de diferentes constante porque:
masas, en función del calor Q que se les suministra. A. Todo el calor que absorbe el sistema se transforma en energía
potencial intermolecular.
B. El trabajo hecho sobre el sistema se convierte en energía
potencial intermolecular.
C. Todo el calor que absorbe el sistema se transforma en
trabajo.
D. El trabajo hecho sobre el sistema es cedido al exterior en
forma de calor.
PARTE III. PROFUNDIZACIÓN (Valor 1.0)
7. Suponga que una partícula de 0.2 kg de masa, sobre la que actúa un resorte, experimenta movimiento armónico simple de tal manera
que oscila entre las coordenadas x=-0,20 m y x=0,20 m. El periodo del movimiento es 1,6 segundos. En t=0 la partícula está en
t= 0,20 m y su velocidad es 0.
a. ¿Cuál es la energía total de este movimiento?
b. ¿En qué tiempo la energía cinética es cero? ¿En qué tiempo la energía potencial es cero?
c. ¿En qué tiempo la energía cinética es igual a la energía potencial?
d. Escriba las ecuaciones del movimiento.
Vous aimerez peut-être aussi
- Factores de La Enseñanza Que Favorecen El Aprendizaje AutónomoDocument3 pagesFactores de La Enseñanza Que Favorecen El Aprendizaje AutónomoEdnithaa VazquezPas encore d'évaluation
- Guía LapbookDocument3 pagesGuía LapbookJuana Diaz EspinozaPas encore d'évaluation
- CuestionarioDocument5 pagesCuestionarioMichael Alexander Baltazar CondorPas encore d'évaluation
- T - Bim - Fis - 10° - Iii PeriodoDocument5 pagesT - Bim - Fis - 10° - Iii PeriodoDiego Andres Garcia100% (1)
- Material para Trabajar Cada DíaDocument6 pagesMaterial para Trabajar Cada DíaDiego Andres GarciaPas encore d'évaluation
- 1 - Prueba de Matemáticas - Día 2Document10 pages1 - Prueba de Matemáticas - Día 2Diego Andres Garcia100% (1)
- Material Especial 11Document2 pagesMaterial Especial 11Diego Andres GarciaPas encore d'évaluation
- Quiz Didáctico Leyes de NewtonDocument2 pagesQuiz Didáctico Leyes de NewtonDiego Andres GarciaPas encore d'évaluation
- Evaluación de Matematicas Grado 10Document1 pageEvaluación de Matematicas Grado 10Diego Andres GarciaPas encore d'évaluation
- Prueba de Sociales Grado 8Document4 pagesPrueba de Sociales Grado 8Diego Andres Garcia100% (2)
- Taller Física PierreDocument12 pagesTaller Física PierreDiego Andres GarciaPas encore d'évaluation
- Trabajo de Física Grado 10 - TermodinámicaDocument6 pagesTrabajo de Física Grado 10 - TermodinámicaDiego Andres GarciaPas encore d'évaluation
- Temas de Tercer PeriodoDocument2 pagesTemas de Tercer PeriodoDiego Andres GarciaPas encore d'évaluation
- Plan de Estudio.Document3 pagesPlan de Estudio.Diego Andres GarciaPas encore d'évaluation
- Evaluación de Física - MaterialDocument6 pagesEvaluación de Física - MaterialDiego Andres GarciaPas encore d'évaluation
- Curso Especial - Día 1 - AmDocument5 pagesCurso Especial - Día 1 - AmDiego Andres GarciaPas encore d'évaluation
- Curso Especial - Prueba 04Document4 pagesCurso Especial - Prueba 04Diego Andres GarciaPas encore d'évaluation
- EvaluaciónDocument1 pageEvaluaciónDiego Andres GarciaPas encore d'évaluation
- Especial de FísicaDocument3 pagesEspecial de FísicaDiego Andres GarciaPas encore d'évaluation
- Curso Especial - Día 4 - PMDocument6 pagesCurso Especial - Día 4 - PMDiego Andres Garcia100% (1)
- Curso Especial - Día 2 - AmDocument5 pagesCurso Especial - Día 2 - AmDiego Andres GarciaPas encore d'évaluation
- Curso Especial-Prueba 1Document4 pagesCurso Especial-Prueba 1Diego Andres GarciaPas encore d'évaluation
- Curso Especial - Día 2 - AmDocument5 pagesCurso Especial - Día 2 - AmDiego Andres GarciaPas encore d'évaluation
- Mat - 9 Reme 2Document5 pagesMat - 9 Reme 2Diego Andres GarciaPas encore d'évaluation
- Problemas de Investigación OperativaDocument7 pagesProblemas de Investigación OperativamestadisticoPas encore d'évaluation
- Poder y Estudios de Las Danzas en El PeruDocument78 pagesPoder y Estudios de Las Danzas en El PeruJonathan Cahuana TacuriPas encore d'évaluation
- Practica Final de MatematicaDocument6 pagesPractica Final de MatematicaCesar FelizPas encore d'évaluation
- Ep4 CRMY SCMDocument4 pagesEp4 CRMY SCMiluminacion LEDPas encore d'évaluation
- Prehistoria y Edad Media de EnfermeriaDocument5 pagesPrehistoria y Edad Media de EnfermeriaHenry Fernando ILTW0% (1)
- Trabajo - Eticacolaborativo Tarea 3 EticaDocument3 pagesTrabajo - Eticacolaborativo Tarea 3 EticaAura MariaPas encore d'évaluation
- Heidegger - IntroduccionDocument2 pagesHeidegger - IntroduccionAlejandra DominguezPas encore d'évaluation
- Sistema Hidroneumático - Res. Dama-Din B-3 (500 X 353 MM)Document1 pageSistema Hidroneumático - Res. Dama-Din B-3 (500 X 353 MM)Grupo Urbaniza, C.A.Pas encore d'évaluation
- WencdorDocument30 pagesWencdorKevin SilvaPas encore d'évaluation
- Destilador CaseroDocument7 pagesDestilador CaseroDaniel Achoy100% (1)
- Ensayo-Plan Cuaternal GRCDocument8 pagesEnsayo-Plan Cuaternal GRCLucy GallardoPas encore d'évaluation
- Tipos de Editores de TextoDocument7 pagesTipos de Editores de Textoleo081989Pas encore d'évaluation
- Producto Integrador Bloque 3Document4 pagesProducto Integrador Bloque 3Tania Salgado NajeraPas encore d'évaluation
- Anteproyecto CompletoDocument50 pagesAnteproyecto CompletoBetzabeth SanllorentePas encore d'évaluation
- TrigonometriaDocument12 pagesTrigonometriaJosep BezerraPas encore d'évaluation
- 9 Junquera PDFDocument38 pages9 Junquera PDFna77aquenoPas encore d'évaluation
- CinematicaDocument22 pagesCinematicaCamy ZambranoPas encore d'évaluation
- Negociar Con Un Proveedor ExtranjeroDocument2 pagesNegociar Con Un Proveedor ExtranjeroGabriela JaraPas encore d'évaluation
- Mpaa SinopticDocument4 pagesMpaa SinopticAzalea Ramiréz GallardoPas encore d'évaluation
- Trabajo Final Asignatura DER-104Document2 pagesTrabajo Final Asignatura DER-104elizabeth pujolsPas encore d'évaluation
- Electronica de Potencia-Lab3Document4 pagesElectronica de Potencia-Lab3Andres Felipe Vasquez RojasPas encore d'évaluation
- Sena - Induccion Procesos Pedagogicos Taller Semana 3Document3 pagesSena - Induccion Procesos Pedagogicos Taller Semana 3Anita SanOroPas encore d'évaluation
- U1 Comunicacion Efectiva Guia OKDocument20 pagesU1 Comunicacion Efectiva Guia OKjavier donayre100% (1)
- 2 Plan OracionDocument7 pages2 Plan OracionJohaniita FuentezPas encore d'évaluation
- Discriminacion LaboralDocument8 pagesDiscriminacion LaboralEmiliano Montañez CardenasPas encore d'évaluation
- Calidad Del Concreto, Mezclado Y Colocación: F'CR F'C F'CDocument7 pagesCalidad Del Concreto, Mezclado Y Colocación: F'CR F'C F'CalfredoPas encore d'évaluation
- Concentracion de Las SolucionesDocument20 pagesConcentracion de Las SolucionesMIGUEL100% (1)