Académique Documents
Professionnel Documents
Culture Documents
Resumen Edición in Vivo de Ryr2. Corrección de Taquicardia Polimórfica Ventricular Catecolaminérgica.
Transféré par
Kathia Jaz0 évaluation0% ont trouvé ce document utile (0 vote)
25 vues3 pagesLa taquicardia polimórfica ventricular catecolaminérgica (CPVT) es una arritmia cardiaca hereditaria con alta tasa de mortalidad. El estudio utilizó la edición genética CRISPR/Cas9 para corregir la mutación genética que causa la CPVT en ratones, eliminando con éxito la secuencia mutada y restaurando la función cardiaca normal. Los resultados demostraron que el enfoque de edición génica in vivo es efectivo y seguro para tratar esta enfermedad.
Description originale:
genómica
Titre original
resumen Edición in vivo de Ryr2. Corrección de Taquicardia Polimórfica Ventricular Catecolaminérgica.
Copyright
© © All Rights Reserved
Formats disponibles
PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentLa taquicardia polimórfica ventricular catecolaminérgica (CPVT) es una arritmia cardiaca hereditaria con alta tasa de mortalidad. El estudio utilizó la edición genética CRISPR/Cas9 para corregir la mutación genética que causa la CPVT en ratones, eliminando con éxito la secuencia mutada y restaurando la función cardiaca normal. Los resultados demostraron que el enfoque de edición génica in vivo es efectivo y seguro para tratar esta enfermedad.
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PDF, TXT ou lisez en ligne sur Scribd
0 évaluation0% ont trouvé ce document utile (0 vote)
25 vues3 pagesResumen Edición in Vivo de Ryr2. Corrección de Taquicardia Polimórfica Ventricular Catecolaminérgica.
Transféré par
Kathia JazLa taquicardia polimórfica ventricular catecolaminérgica (CPVT) es una arritmia cardiaca hereditaria con alta tasa de mortalidad. El estudio utilizó la edición genética CRISPR/Cas9 para corregir la mutación genética que causa la CPVT en ratones, eliminando con éxito la secuencia mutada y restaurando la función cardiaca normal. Los resultados demostraron que el enfoque de edición génica in vivo es efectivo y seguro para tratar esta enfermedad.
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 3
Introducción a la Genómica. Tarea 5.
González Simón Kathia Jazmín
Artículo: Edición in vivo de Ryr2. Corrección de Taquicardia Polimórfica
Ventricular Catecolaminérgica.
Resumen.
Taquicardia Polimórfica Ventricular Catecolaminérgica (CPVT): Arritmia cardiaca
hereditaria. Tiene una taza de mortalidad de hasta el 50% durante los primeros 8
años luego de su diagnóstico. Debido a la ineficiencia de los tratamientos (algunos
incluso dolorosos como los desfibriladores implantables) se busca, mediante la
terapia génica, hacer un cambio en la salud de quienes padecen esta enfermedad.
Fisiopatología de CPVT: Resultado de mutaciones autosómicas dominantes en el
gen codificante del receptor rianodina 2 (RYR2) (generalmente causado por
mutaciones de sentido erróneo, ganancia de función), gen que codifica para el
canal RyR2 que se activa por la entrada de Ca2+ (dependiente de voltaje), el
retículo sarcoplasmático inicia a través de RyR2 la contracción del miocito. Al
tener una subunidad mutada se producen liberaciones espontáneas de Ca2+ del
Retículo al citoplasma, y se obtiene una polarización de la célula cardiaca que,
junto a una deficiente despolarización de esta, ocasiona graves arritmias.
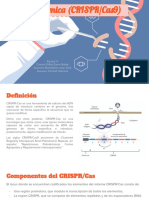
Del tratamiento: Se utilizó el sistema CRISPR/Cas9 (Repeticiones Palindrómicas
Cortas Agrupadas y Regularmente Interespaciadas), que utiliza una nucleasa
guiada por ARN (Cas9) para hacer roturas específicas en la doble cadena de DNA
lo que da como resultado mutaciones de deleción/inserción. Con la edición
CRISPR/Cas9 se pueden eliminar alelos mutados al introducir un codón de alto
prematuro, anomalías de splicing y/o degradación del ARN mensajero mediada
por mutación terminadora. Y debido a que en la taquicardia (CPVT), la mutación
consiste en el cabio de un codón que codifica para un aminoácido diferente, es
posible utilizar esta técnica.
Del método:
- Se utilizaron ratones hembra con mutación en heterocigosis (R176Q/+).
- El sistema CRISPR/Cas9 fue inyectado mediante un vector AVV dirigido
específicamente por ARNg al alelo mutado.
Para monitorear los resultados se utilizaron:
- Un programa de estimulación intracardiaca, para el estudio
electrofisiológico in vivo de los ratones.
- Se cuantificó a tiempo real un PCR en tejidos ventriculares, (primers
corriente arriba: exón 3-6 y corriente abajo: Exón 11-13), utilizando el
equipo iTaq Universal SYBR Green Supermix.
- Se realizó un Análisis Western Blot.
- Se utilizó también un equipo de próxima generación para la secuenciación y
cuantificación de CRISPR/Cas9 at On-/Off-Target Sites .
- Imagen celular de Ca2+
- Y finalmente para tratamiento de datos, se realizó un análisis estadístico.
Resultados: Se demostró que el vector AAV9 junto con SaCAS9 y gRNA, editan
eficientemente los cardiomiocitos un vivo (eliminando la secuencia target de 22pb
en exón 8), reduciendo los niveles de mutación en la subunidad RyR2, se
normalizó en manejo de Ca2+ intracelular en los ratones R176Q/+, restaurando así
la función cardiaca. No se afectan los flujos de Ca2+ más allá del causante de la
enfermedad, por lo que se demuestra que el enfoque de edición de genes in vivo
es efectivo y seguro.
Comentario.
Elegí el artículo debido a que con anterioridad había leído acerca del tratamiento
génico con CRISPR/Cas9 y la conmoción que había causado por la implicación
moral que generaba en el público en general, así que quería saber más acerca de
este tema y analizar por mí misma lo que se comentaba en las redes sociales.
Primero que nada, me sorprendí de que pudiera leer un artículo con esta temática
con relativa facilidad, los conocimientos adquiridos de la materia y el estudio
propio me permitieron entender términos muy técnicos y saber a qué se referían
exactamente, palabras como PCR o Western Blot (técnicas de identificación de
secuencias de DNA o proteínas, que revisamos en clase), sólo aumentaron mi
interés con respecto al trabajo que hay detrás de la investigación. Sucedió lo
mismo al comenzar el artículo y leer la fisiopatología de la enfermedad, ya no sólo
es un mecanismo a nivel celular, sino a nivel génico, que desde mi perspectiva
aumenta la dificultad; tuve un poco de problemas para entender esta parte de la
fisiopatología, ya que me parece que la página donde encontré el artículo no
redacta de manera adecuada éste mecanismo: “Con solo una subunidad mutada
en el homotetrámero que forma, ya es suficiente para que se produzcan
liberaciones espontáneas de Ca2+ al citoplasma, incluso tras concluir la
despolarización, que ocasionan graves arritmias de resultado posiblemente
mortal.” Cuando el artículo menciona algo diferente, desde mi entendimiento, no
es la polarización (la entrada de calcio genera el cambio en el voltaje) de la célula
cardiaca lo que genera la arritmia, sino la deficiente despolarización.
Al ser una técnica bastante desconocida para mí (CRISPR/Cas9), existieron cosas
en la explicación del artículo que no comprendí, como la técnica de próxima
generación para la secuenciación y cuantificación de CRISPR/Cas9 at On-/Off-
Target Sites, pero en general, el funcionamiento se basa en mutaciones que se
revisaron en clase, como la mutación deleción/inserción, y mutaciones como la de
codón de alto prematuro.
Es cierto que falta mayor conocimiento para entender un artículo, con técnicas y
temas nuevos, pero la clase de Introducción a la Genómica da cierto alcancé para
comprender el panorama general del tema.
Me gustó mucho el artículo, primero porque era un tema que me interesaba, y
segundo, porque comprobé que, al tener mayor conocimiento respecto al tema, se
puede dejar de malignizar, algo que podría ser benéfico para la salud de las
personas.
Bibliografía:
Aguilar Ballester, María, Aplicado por primera vez de manera exitosa el sistema
CRISPR-Cas como terapia génica personalizada en un modelo animal de
enfermedad cardiaca hereditaria, Genética Médica News, Enero 2019, publicado
en: https://genotipia.com/genetica_medica_news/crispr-enfermedades-cardiacas/
Link del artículo original:
https://www.ahajournals.org/doi/pdf/10.1161/CIRCRESAHA.118.313369
Vous aimerez peut-être aussi
- Taller de SinapsisDocument4 pagesTaller de Sinapsismatacurie100% (1)
- ABO y DiscrepanciasDocument58 pagesABO y DiscrepanciasRomina Angulo Rivera100% (1)
- 8va Clase - Preguntas Sobre Pruebas MolecularesDocument8 pages8va Clase - Preguntas Sobre Pruebas Molecularesalberto rengifo ramirez100% (1)
- Acceso a Universidad para Mayores de 25 años. Biología 2013-2017.: Solucionario Pruebas 2013-2017D'EverandAcceso a Universidad para Mayores de 25 años. Biología 2013-2017.: Solucionario Pruebas 2013-2017Pas encore d'évaluation
- BTMAV INFORME Practicas Diseño de Primers para PCRDocument20 pagesBTMAV INFORME Practicas Diseño de Primers para PCRAndrea Pignatelli100% (1)
- GenéticaDocument52 pagesGenéticaSebastianPinoPas encore d'évaluation
- Farmacologia Del Sistema Nervioso Autonomo Parasimpatico-5b26c197d8520Document11 pagesFarmacologia Del Sistema Nervioso Autonomo Parasimpatico-5b26c197d8520javiera_chingPas encore d'évaluation
- Taller Moleculas de La HerenciaDocument8 pagesTaller Moleculas de La HerenciasergioPas encore d'évaluation
- Seminario Genetica - MutacionesDocument51 pagesSeminario Genetica - MutacionesIvan MolinaPas encore d'évaluation
- Ciencias Taller #1Document5 pagesCiencias Taller #1Juan Andres Quintero ClaroPas encore d'évaluation
- Taller Moleculas de La HerenciaDocument8 pagesTaller Moleculas de La HerenciasergioPas encore d'évaluation
- Genetic ADocument10 pagesGenetic AAngela VasquezPas encore d'évaluation
- Taller GeneticaDocument9 pagesTaller GeneticaFrk AlexxPas encore d'évaluation
- HT Módulo IV - MutacionesDocument4 pagesHT Módulo IV - MutacionesBRIANNA ALVAREZ CHINCHILLAPas encore d'évaluation
- 5 Dra Mezaa ClaseDocument59 pages5 Dra Mezaa ClaseJimena RamírezPas encore d'évaluation
- TSA 10 GeneticaDocument5 pagesTSA 10 GeneticaKatty HornaPas encore d'évaluation
- Tarea 4 - AnalizarDocument13 pagesTarea 4 - AnalizarPaula TorresPas encore d'évaluation
- Unidad 3 AnalizarDocument15 pagesUnidad 3 AnalizarMaria Alejandra Zambrano OrtegaPas encore d'évaluation
- Examen FinalDocument6 pagesExamen FinalYenifer EncarnacionPas encore d'évaluation
- CRISPRCas 9Document17 pagesCRISPRCas 9omar barreraPas encore d'évaluation
- Reacción en Cadena de La Polimerasa y Diseño de IniciadoresDocument44 pagesReacción en Cadena de La Polimerasa y Diseño de IniciadoresValeria Gutierrez RuizPas encore d'évaluation
- Tarea 4 - AnalizarDocument11 pagesTarea 4 - Analizarpaola lopezPas encore d'évaluation
- 14 ACN3 Actividad de Complementación y Nivelación 2023-10Document16 pages14 ACN3 Actividad de Complementación y Nivelación 2023-10evalerap1Pas encore d'évaluation
- Act. 1.trabajo ColaborativoDocument8 pagesAct. 1.trabajo ColaborativoAnonymous IG3Pj6AwPas encore d'évaluation
- Taller3 2022Document51 pagesTaller3 2022LucasPas encore d'évaluation
- Semana 09 - Edicion GenicaDocument61 pagesSemana 09 - Edicion GenicaJorge Janampa CamposPas encore d'évaluation
- Bases Moleculares de La Genã - TicaDocument17 pagesBases Moleculares de La Genã - TicaRafaelPas encore d'évaluation
- Mutacion y ReparacionDocument45 pagesMutacion y ReparacionMaritza Elizabeth Ramos Castro0% (1)
- Tema15 TranscripcionDocument11 pagesTema15 TranscripcionIrene PG100% (1)
- Práctica 13 - Codigo GeneticoDocument4 pagesPráctica 13 - Codigo GeneticoMarycielo Graviel SánchezPas encore d'évaluation
- CUESTIONARIO GENÉTICA MOLECULAR CorrectoDocument5 pagesCUESTIONARIO GENÉTICA MOLECULAR CorrectoElizabeth Maldonado LimaPas encore d'évaluation
- La Tecnología CRISPR2019 - 3 - 16P15 - 48 - 34Document9 pagesLa Tecnología CRISPR2019 - 3 - 16P15 - 48 - 34GUADALUPE FERNáNDEZPas encore d'évaluation
- Biolo MoleDocument8 pagesBiolo Molelola loPas encore d'évaluation
- Repeticiones Palindrómicas CortasDocument4 pagesRepeticiones Palindrómicas CortasJoe PertuPas encore d'évaluation
- CrisprDocument41 pagesCrisprMarta DonoPas encore d'évaluation
- Laboratorio Biologia Celular NeuronasDocument4 pagesLaboratorio Biologia Celular NeuronasPaulaPas encore d'évaluation
- Aula 16 Herramientas de Biología Molecular - MartesDocument5 pagesAula 16 Herramientas de Biología Molecular - MartesCarolina Bailon TrujilloPas encore d'évaluation
- Tarea 3 BiologiaDocument11 pagesTarea 3 BiologiaSandra RodriguezPas encore d'évaluation
- Taller Enzimas de Restricción y Aplicaciones 2023 ARRDocument5 pagesTaller Enzimas de Restricción y Aplicaciones 2023 ARRJean Carlos Manrique EspinosaPas encore d'évaluation
- ¿Qué Es La Tecnología CRISPR - Cas9 y Cómo Nos Cambiará La Vida - Dciencia PDFDocument6 pages¿Qué Es La Tecnología CRISPR - Cas9 y Cómo Nos Cambiará La Vida - Dciencia PDFJose Gregorio Ochoa HidalgoPas encore d'évaluation
- Terapia Genica Mediante Sistemas CRISPRCas Garcia Torres DanielDocument42 pagesTerapia Genica Mediante Sistemas CRISPRCas Garcia Torres Danielnorbe.1108timaure83Pas encore d'évaluation
- Repaso Primer Semestre MedicinaDocument2 pagesRepaso Primer Semestre MedicinaFelipe Smith0% (1)
- 2da Parte BancoDocument3 pages2da Parte BancoNicol ArtunduagaPas encore d'évaluation
- Semana 12 - PrácticaDocument14 pagesSemana 12 - PrácticaAldrin Arias CarbajalPas encore d'évaluation
- DISEÑO EXPERIMENTAL ARNi Y CRISPR CASDocument8 pagesDISEÑO EXPERIMENTAL ARNi Y CRISPR CASMafe MolinaPas encore d'évaluation
- 31 - Técnicas de Biología Molecular y Laboratorio ClínicoDocument38 pages31 - Técnicas de Biología Molecular y Laboratorio ClínicoMedia SolutionsPas encore d'évaluation
- CRISPRCas 9Document11 pagesCRISPRCas 9kyriephobiaPas encore d'évaluation
- Trabajo BiologíaDocument8 pagesTrabajo BiologíaDarwinPas encore d'évaluation
- Informe Gye Semana 10Document8 pagesInforme Gye Semana 10KIARA ANALY SHOCUSH ARMASPas encore d'évaluation
- Simulación de La Aplificacion Del ADN - Adriana ArandaDocument6 pagesSimulación de La Aplificacion Del ADN - Adriana ArandaAdriana SwanPas encore d'évaluation
- Reporte BioloDocument5 pagesReporte BioloTiti PortalesPas encore d'évaluation
- Qué Es La Tecnología CrisprDocument8 pagesQué Es La Tecnología CrisprJRIISSPas encore d'évaluation
- Uees-Escribe-José Ignacio Guerra SwettDocument22 pagesUees-Escribe-José Ignacio Guerra SwettANNELIESE VELEZ NAVARRETEPas encore d'évaluation
- Guia para Principiantes de Biologia Molecular Aplicada A La AcuiculturaDocument53 pagesGuia para Principiantes de Biologia Molecular Aplicada A La AcuiculturaJorge Chavez AraizaPas encore d'évaluation
- Taller de Recuperacion Biologia Celular y MolecularDocument7 pagesTaller de Recuperacion Biologia Celular y MolecularJuanEstebanMoraPas encore d'évaluation
- Laboratorio CRISPR-Cas9Document2 pagesLaboratorio CRISPR-Cas9PerejiloPas encore d'évaluation
- GENETICA Seminario 3 BQIIDocument7 pagesGENETICA Seminario 3 BQIILucia RamirezPas encore d'évaluation
- PCR ConvencionalDocument3 pagesPCR Convencionalcassievw314Pas encore d'évaluation
- Pre y Post Laboratorio 5 y Anexo MolecularDocument6 pagesPre y Post Laboratorio 5 y Anexo MolecularJulieth PeñalozaPas encore d'évaluation
- Preguntas Sobre Pruebas MolecularesDocument8 pagesPreguntas Sobre Pruebas MolecularesNats OCPas encore d'évaluation
- Informe G&e-S10Document8 pagesInforme G&e-S10MARIA FERNANDA PINEDO AZA�EROPas encore d'évaluation
- Taller de Recuperacion BiologíaDocument6 pagesTaller de Recuperacion BiologíaJuanEstebanMoraPas encore d'évaluation
- MIcro P3Document1 pageMIcro P3Kathia JazPas encore d'évaluation
- Cuestionario Analítica ExperimentalDocument1 pageCuestionario Analítica ExperimentalKathia JazPas encore d'évaluation
- Micro P1 PDFDocument1 pageMicro P1 PDFKathia JazPas encore d'évaluation
- Análisis de Medicamentos EjerciciosDocument4 pagesAnálisis de Medicamentos EjerciciosKathia JazPas encore d'évaluation
- Interpretación IR VainillinaDocument2 pagesInterpretación IR VainillinaKathia JazPas encore d'évaluation
- 1 Conductimetria AASDocument4 pages1 Conductimetria AASKathia JazPas encore d'évaluation
- Artículo Introducción A La Espectrometría de Masas para La Caracterización de Péptidos y Proteínas en ProteómicaDocument20 pagesArtículo Introducción A La Espectrometría de Masas para La Caracterización de Péptidos y Proteínas en ProteómicaKathia JazPas encore d'évaluation
- Qo P1 PDFDocument2 pagesQo P1 PDFKathia JazPas encore d'évaluation
- Trabajo de CienciasDocument18 pagesTrabajo de CienciasLeider Mendoza PoloPas encore d'évaluation
- Laboratorio Estraccion de Adn ConnieDocument18 pagesLaboratorio Estraccion de Adn ConnieHyalette EsturainPas encore d'évaluation
- Taller MeiosisDocument3 pagesTaller MeiosisAlfredo AlvearPas encore d'évaluation
- Sistema Basico de PischingerDocument32 pagesSistema Basico de PischingerEstela PonisioPas encore d'évaluation
- Unidad Educativa Liceo Cristiano de Guayaquil: Taller 1 de Biologia: TemaDocument12 pagesUnidad Educativa Liceo Cristiano de Guayaquil: Taller 1 de Biologia: TemaDeisy JTigrePas encore d'évaluation
- Quimica Biomolecular.Document25 pagesQuimica Biomolecular.Lazaro FerreyraPas encore d'évaluation
- Antigenos de HistocompatibilidadDocument26 pagesAntigenos de HistocompatibilidadMao NgPas encore d'évaluation
- ADN Cuarto Medio Comun 2013 Salvavida de PlomoDocument5 pagesADN Cuarto Medio Comun 2013 Salvavida de Plomooliver1125Pas encore d'évaluation
- ¿Que Hace Que Ocurra Dominancia Actual?: Auxinias, Giberelinas Y CitocininasDocument4 pages¿Que Hace Que Ocurra Dominancia Actual?: Auxinias, Giberelinas Y CitocininasRODRIGOI50% (8)
- Retículo Endoplásmico GARCIA MEJIA Alvaro Eduardo 1°ADocument20 pagesRetículo Endoplásmico GARCIA MEJIA Alvaro Eduardo 1°AÁlvaro GarciaPas encore d'évaluation
- Clasificación de Los BiocompuestosDocument2 pagesClasificación de Los BiocompuestosNicol Fernanda Varela gilPas encore d'évaluation
- Trensa Cientifica PDFDocument1 pageTrensa Cientifica PDFSERIES Y MASPas encore d'évaluation
- Mapa ConceptualDocument2 pagesMapa Conceptualfaty hdezPas encore d'évaluation
- Transportadores de Glucosa e Insulina (Esquemas)Document8 pagesTransportadores de Glucosa e Insulina (Esquemas)ROGGER CERNAPas encore d'évaluation
- Clase 2Document8 pagesClase 2Victor AlvaradoPas encore d'évaluation
- Citoesqueleto 2023Document18 pagesCitoesqueleto 2023Maricielo LRPas encore d'évaluation
- Final Bioquimica FMED UBA 14-2-19 TEMA ADocument2 pagesFinal Bioquimica FMED UBA 14-2-19 TEMA ACande AmiconePas encore d'évaluation
- Mtra. Nora Rodríguez CangalayaDocument20 pagesMtra. Nora Rodríguez CangalayaJonathan StPas encore d'évaluation
- Bioquimica Evaluación 1cDocument3 pagesBioquimica Evaluación 1cRominaPas encore d'évaluation
- Grupos Funcionales de Los BiomoleculasDocument35 pagesGrupos Funcionales de Los BiomoleculasLuigimom Orobio MartinezPas encore d'évaluation
- Regulación Molecular Del Desarrollo Del RiñónDocument2 pagesRegulación Molecular Del Desarrollo Del Riñónyuri gallardo0% (1)
- FarmacodinamiaDocument12 pagesFarmacodinamiaMarihelena CortezPas encore d'évaluation
- CITOCINASDocument20 pagesCITOCINASValeria Padilla LopezPas encore d'évaluation
- Tarea de CatalizadoresDocument2 pagesTarea de CatalizadoresDavis CarbajalPas encore d'évaluation
- 1 Biologia Molecular y Celular en OrtopediaDocument44 pages1 Biologia Molecular y Celular en OrtopediaCristian MarquezPas encore d'évaluation
- Celulas Animal VegetalDocument10 pagesCelulas Animal VegetalJarov TijerinoPas encore d'évaluation
- 2 Mitosis y MeiosisDocument15 pages2 Mitosis y MeiosisJadher PradaPas encore d'évaluation