Académique Documents
Professionnel Documents
Culture Documents
H
Transféré par
Angiie Vanessa Martiinez Cuadros0 évaluation0% ont trouvé ce document utile (0 vote)
43 vues2 pagesH
Copyright
© © All Rights Reserved
Formats disponibles
PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentH
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PDF, TXT ou lisez en ligne sur Scribd
0 évaluation0% ont trouvé ce document utile (0 vote)
43 vues2 pagesH
Transféré par
Angiie Vanessa Martiinez CuadrosH
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 2
En la siguiente lista se encuentran las fórmulas y nombres tradicionales
de los ácidos oxácidos más importantes y que se deben aprender de memoria:
HCLO : Ácido hipocloroso H6 TeO6 : Ácido ortotelúrico
HClO2 : Ácido cloroso H2 N2 O2 : Ácido hiponitroso
HClO3 : Ácido clórico HNO2 : Ácido nitroso Las fórmulas de la mayoría de los elementos se
HClO4 : Ácido perclórico HNO3 : Ácido nítrico representan por su símbolo simple
HBrO : Ácido hipobromoso HPH2 O2 : Ácido fosfínico
HBrO2 : Ácido bromoso H2 PHO3 : Ácido fosfónico
Entre los pocos elementos que se representan por su
HBrO3 : Ácido brómico HPO3 : Ácido metafosfórico
HBrO4 : Ácido perbrómico H4 P2 O7 : Ácido piro o difosfórico molécula y que se deben aprender de memoria se
HIO : Ácido hipoyodoso H3 PO4 : Ácido (orto)fosfórico encuentran:
HIO3 : Ácido yódico H3 AsO3 : Ácido arsenioso
HIO4 : Ácido metaperyódico H3 AsO4 : Ácido arsénico
H5 IO6 : Ácido ortoperyódico H2 CO3 : Ácido carbónico
H2 SO2 : Ácido sulfoxílico H2 SiO3 : Ácido metasilícico
H2 = Hidrógeno F2 = Flúor
H2 SO3 : Ácido sulfuroso H4 SiO4 : Ácido ortosilícico N2 = Nitrógeno Cl2 = Cloro
H2 S2 O5 : Ácido disulfuroso HBO2 : Ácido metabórico
H2 SO4 : Ácido sulfúrico H3 BO3 : Ácido (orto)bórico O2 = Oxígeno Br2 = Bromo
H2 S2 O7 : Ácido disulfúrico H2 CrO4 : Ácido crómico O3 = Ozono I2 = Yodo
H2 SeO3 : Ácido selenioso H2 Cr2 O7 : Ácido dicrómico
H2 SeO4 : Ácido selénico HmnO4 : Ácido permangánico
El concepto de valencia (o valor de combinación) tiene relación con la
proporción en que se unen los átomos para formar los compuestos. Se toma como Dividimos la nomenclatura de este tipo de compuesto en 2 partes:
referencia al H, al que se da valencia 1, y a los demás átomos se le asigna la A) Los de nometal con valencias 1 y 2: se pueden nombrar como ácidos
valencia por el número de H con los que se une. Por ejemplo, decimos que la hidrácidos (terminación hídrico) o como compuestos binarios
valencia del Al es 3 porque forma el AlH 3. Cuando a la valencia se le pone un signo,
+ ó -, se le denomina ESTADO DE OXIDACIÓN. El sentido que tienen los estados Ácido fluorhídrico Ácido cianhídrico
de oxidación es que el nº de cargas positivas y negativas de los átomos de un
HF Fluoruro de hidrógeno HCN Cianuro de hidrógeno
Ácido clorhídrico Ácido sulfhídrico
compuesto deben ser iguales, para que la fórmula resulte en su conjunto HCl Cloruro de hidrógeno
H2S Sulfuro de hidrógeno
eléctricamente neutra.
Ácido bromhídrico Ácido selenhídrico
HBr Bromuro de hidrógeno
H2Se Seleniuro de hidrógeno
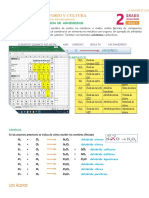
ESTADOS DE OXIDACIÓN MÁS FRECUENTES DE LOS Ácido yodhídrico Ácido telurhídrico
ELEMENTOS MÁS IMPORTANTES HI Yoduro de hidrógeno
H2Te Telururo de hidrógeno
METALES NO METALES
+1: Li, Na, K, Rb, Cs, Fr, Ag, -1, +1: H B) Los de nometal con valencias 3 y 4: aunque podrían nombrarse como
NH4+ (ion amonio) compuestos binarios, lo cierto es que la comunidad científica acepta sus nombres
vulgares y que, además de H2O son:
+2: Be, Mg, Ca, Sr, Ba, Ra, Zn, Cd -2: O
+3: Al -1: F
+1, +2: Cu, Hg -1, +1, +3, +5, +7: Cl, Br, I NH3 : Amoniaco CH4: Metano
+1, +3: Au -2, +2, +4, +6: S, Se, Te
+2, +3: Fe, Co, Ni -3, +1, +3, +5, N, P, As, Sb PH3: Fosfina SiH4 : Silano
+2, +4: Sn, Pb, Pt -4, +4: C, Si AsH3: Arsina BH3 : Borano
- 3, +3: B
+2, +3, +4, +5 (metal), +6 (no metal): Cr SbH3: Estibina
+2, +3, +4, +5 (metal), +6, +7 8no metal): Mn Fijarse en la distinta posición del NOMETAL y el H en los grupos A) y B)
Vous aimerez peut-être aussi
- Problemas resueltos de Química Analítica CuantitativaD'EverandProblemas resueltos de Química Analítica CuantitativaÉvaluation : 5 sur 5 étoiles5/5 (3)
- Ensayo Sobre El DeporteDocument5 pagesEnsayo Sobre El DeporteDaniel Leal45% (11)
- Sesion 3 Función Hidruros, Ácidos y SalesDocument30 pagesSesion 3 Función Hidruros, Ácidos y SalesAnthony Esquivel AraujoPas encore d'évaluation
- Cómo Identificar Tus Creencias LimitantesDocument12 pagesCómo Identificar Tus Creencias LimitantesRoser84100% (4)
- Acidos HidracidosDocument3 pagesAcidos HidracidosNidia Millán SalazarPas encore d'évaluation
- Capitulo II Química General - Nomenclatura Química Inorgánica II PDFDocument16 pagesCapitulo II Química General - Nomenclatura Química Inorgánica II PDFLourdesPas encore d'évaluation
- GUIA #10 QCA I Con Respuesta Nomenclatura Binaria Compuestos Hidrogenados 2023Document5 pagesGUIA #10 QCA I Con Respuesta Nomenclatura Binaria Compuestos Hidrogenados 2023Anita Ortiz LiberonaPas encore d'évaluation
- GUIA #10 QCA I Con Respuesta Nomenclatura Binaria Compuestos Hidrogenados 2023Document5 pagesGUIA #10 QCA I Con Respuesta Nomenclatura Binaria Compuestos Hidrogenados 2023Anita Ortiz LiberonaPas encore d'évaluation
- CLASE 5 - F. HIDRUROS y ÁCIDOSDocument39 pagesCLASE 5 - F. HIDRUROS y ÁCIDOSMilagros RabanalPas encore d'évaluation
- Tema 3 Química 5to SecundariaDocument14 pagesTema 3 Química 5to SecundariaCRISTHIAN JESUS PANEZ MORENOPas encore d'évaluation
- Sesion 5 Función Ácidos e HidrurosDocument28 pagesSesion 5 Función Ácidos e HidrurosAlejandra Ramírez VigoPas encore d'évaluation
- Nomenclatura de Compuestos Inorganicos-BDocument27 pagesNomenclatura de Compuestos Inorganicos-BCarlos SantanaPas encore d'évaluation
- NegroDocument7 pagesNegroSabelli CameliaPas encore d'évaluation
- Funciones Quimicas para Primero de SecundariaDocument5 pagesFunciones Quimicas para Primero de SecundariaCesar JulcamoroPas encore d'évaluation
- Nomenclatura en Química InorgánicaDocument10 pagesNomenclatura en Química InorgánicaTania MendezPas encore d'évaluation
- Ciencia y TecnologíaDocument4 pagesCiencia y TecnologíaChio Vásquez GeldresPas encore d'évaluation
- Química - Nomenclatura Inorgánica Ii (5° Uni)Document25 pagesQuímica - Nomenclatura Inorgánica Ii (5° Uni)kjdisjifsPas encore d'évaluation
- FormulaciónDocument6 pagesFormulaciónbelenPas encore d'évaluation
- U2 - Clase 4 - S3 H14Document4 pagesU2 - Clase 4 - S3 H14OliPas encore d'évaluation
- Nomenclatura Inorgánica II Sm-IntegralDocument13 pagesNomenclatura Inorgánica II Sm-IntegralDanna Paola Portilla NeiraPas encore d'évaluation
- Que Es Un Acido para Quinto de SecundariaDocument3 pagesQue Es Un Acido para Quinto de SecundariaLeivf CastPas encore d'évaluation
- Tema 26 B1 CTS 2do Los AcidosDocument6 pagesTema 26 B1 CTS 2do Los AcidosVictor Raul Torres PerezPas encore d'évaluation
- Ácidos OxoácidosDocument17 pagesÁcidos OxoácidosrubenPas encore d'évaluation
- Taller Aprende en Casa Química 11° - ABRIL PDFDocument5 pagesTaller Aprende en Casa Química 11° - ABRIL PDFJUAN ESTEBAN LASPRILLA CASTILLOPas encore d'évaluation
- Nomenclatura de Compuestos Inorganicos-2021Document28 pagesNomenclatura de Compuestos Inorganicos-2021Fernanda ManzanoPas encore d'évaluation
- Ácidos y BasesDocument4 pagesÁcidos y BasesTony Tony Luis MarioPas encore d'évaluation
- Quimica Tema 8 Nomenclatura Inorganica IiDocument3 pagesQuimica Tema 8 Nomenclatura Inorganica IiViviendo VenciendoPas encore d'évaluation
- Pre Presentacion 14 7s Nomenclatura 2 2023 1Document30 pagesPre Presentacion 14 7s Nomenclatura 2 2023 1Nicolle Campos chamorroPas encore d'évaluation
- Deber 13 de QuimicaDocument5 pagesDeber 13 de Quimicaivanna salazarPas encore d'évaluation
- 5to. QUIM - Nomenclatura Inorgánica IIDocument4 pages5to. QUIM - Nomenclatura Inorgánica IIMauricio Rivera VerdePas encore d'évaluation
- Nomenclatura Quimica de Los Compuestos InorganicosDocument26 pagesNomenclatura Quimica de Los Compuestos InorganicosSaen ab100% (1)
- Nomenclatura de Compuestos Inorganicos-2021Document28 pagesNomenclatura de Compuestos Inorganicos-2021angela bazalduaPas encore d'évaluation
- 7127 - Propuesta Nomenclatura Inorgánica - Ja Dominguez y F MonzónDocument20 pages7127 - Propuesta Nomenclatura Inorgánica - Ja Dominguez y F MonzónwallterBrianPas encore d'évaluation
- Filemd9181-2023-09-16 11-55-26Document26 pagesFilemd9181-2023-09-16 11-55-26erickelderestradaarenasPas encore d'évaluation
- Compuestos Quimicos. Formulación y Nomenclatura. Parte IIDocument25 pagesCompuestos Quimicos. Formulación y Nomenclatura. Parte IIlissethPas encore d'évaluation
- Guia de Nomenclatura de Compuestos InorgánicosDocument13 pagesGuia de Nomenclatura de Compuestos InorgánicosWilmer LopezPas encore d'évaluation
- Funciones Quimicas para Primero de SecundariaDocument5 pagesFunciones Quimicas para Primero de SecundariaAnonymous wQ4ReuHPas encore d'évaluation
- Tipos de Ácidos para Tercer Grado de SecundariaDocument3 pagesTipos de Ácidos para Tercer Grado de SecundariaJosé MorenoPas encore d'évaluation
- Nomenclatura Inorgánica 2021Document11 pagesNomenclatura Inorgánica 2021Barbie KenPas encore d'évaluation
- Acidos y Bases ArrheniusDocument13 pagesAcidos y Bases ArrheniusValeria RoblesPas encore d'évaluation
- Nomenclatura IiDocument20 pagesNomenclatura IiRoy Melendrez AlbercaPas encore d'évaluation
- s1 Ficha de Hidroxidos Vs Acidos OxacidosDocument6 pagess1 Ficha de Hidroxidos Vs Acidos OxacidosPaola Grisell Esquía FernándezPas encore d'évaluation
- 2actividad de AplicacionDocument2 pages2actividad de Aplicacionandy valdiviezoPas encore d'évaluation
- Nomenclatura de Compuestos Inorganicos-HidracidosDocument19 pagesNomenclatura de Compuestos Inorganicos-HidracidosCarlos SantanaPas encore d'évaluation
- AcidosDocument7 pagesAcidospatricia vargasPas encore d'évaluation
- Clase 9, Compuestos TernariosDocument14 pagesClase 9, Compuestos TernariosHenrry CacPas encore d'évaluation
- 5to. QUIM - Guía #2 - Nomenclatura Inorgánica IIDocument3 pages5to. QUIM - Guía #2 - Nomenclatura Inorgánica IICarlos LopezPas encore d'évaluation
- Tipos de Ácidos para Tercer Grado de SecundariaDocument3 pagesTipos de Ácidos para Tercer Grado de SecundariaIsrael BackusPas encore d'évaluation
- Taller Hidróxidos y Ácidos GMSF 2021Document2 pagesTaller Hidróxidos y Ácidos GMSF 2021adriYT100% (1)
- Guía 1 - Teoría HidrurosDocument10 pagesGuía 1 - Teoría HidrurosSergio OrtegaPas encore d'évaluation
- Radicales de Acidos Hidracidos y OxacidosDocument10 pagesRadicales de Acidos Hidracidos y OxacidosSergio Driss Melèndez MartìnezPas encore d'évaluation
- TP 4 ResueltoDocument7 pagesTP 4 ResueltoCecilia GaticaPas encore d'évaluation
- Nomenclatura #2Document6 pagesNomenclatura #2Hügô MïrãPas encore d'évaluation
- 3 Nomenclatura InorganicaDocument24 pages3 Nomenclatura InorganicaNicolas Patricio SitjaPas encore d'évaluation
- 3 HidroxidosyOxoacidosv 2Document15 pages3 HidroxidosyOxoacidosv 2Alvaro Ramos BarbaPas encore d'évaluation
- 901, 902 y 903 Química-Guia 11 - J.T. Isabel Pérez.Document6 pages901, 902 y 903 Química-Guia 11 - J.T. Isabel Pérez.Bryan Fabian LopezPas encore d'évaluation
- Función HidróxidoDocument5 pagesFunción Hidróxidocesar coilaPas encore d'évaluation
- Filemd7485-2023-06-28 10-02-29Document35 pagesFilemd7485-2023-06-28 10-02-29Renzo BabilonioPas encore d'évaluation
- CQ 4Document14 pagesCQ 4nazarethPas encore d'évaluation
- Acidos para Primero Grado de SecundariaDocument4 pagesAcidos para Primero Grado de SecundariaANGIE GIERESH HUAMAN MENDOZAPas encore d'évaluation
- Nom Quim Inorg Parte IIDocument8 pagesNom Quim Inorg Parte IIromarioPas encore d'évaluation
- Guia Riesgo Biológico Empresas PDFDocument87 pagesGuia Riesgo Biológico Empresas PDFMonica UrreaPas encore d'évaluation
- Guia Riesgo Biológico para Ips - Eps PDFDocument57 pagesGuia Riesgo Biológico para Ips - Eps PDFDianaVanessaSilvaPas encore d'évaluation
- Matriz Identificación de Peligros VillavicencioDocument10 pagesMatriz Identificación de Peligros VillavicencioMonica Guerra DuranPas encore d'évaluation
- Vector EsDocument29 pagesVector EsJame'z ValDivia0% (1)
- Taller 1.2Document7 pagesTaller 1.2Angiie Vanessa Martiinez CuadrosPas encore d'évaluation
- Angie Vanessa Martinez CuadrosDocument11 pagesAngie Vanessa Martinez CuadrosAngiie Vanessa Martiinez CuadrosPas encore d'évaluation
- Re Acci Ones Organic AsDocument25 pagesRe Acci Ones Organic AsAndrea VukasovicPas encore d'évaluation
- El Arte de Amar PDFDocument10 pagesEl Arte de Amar PDFCarlos Mikael LópezPas encore d'évaluation
- Re Acci Ones Organic AsDocument25 pagesRe Acci Ones Organic AsAndrea VukasovicPas encore d'évaluation
- El Efecto Del Deporte en La SaludDocument5 pagesEl Efecto Del Deporte en La SaludAngiie Vanessa Martiinez CuadrosPas encore d'évaluation
- HDocument2 pagesHAngiie Vanessa Martiinez CuadrosPas encore d'évaluation
- Ecorregiones PerúDocument16 pagesEcorregiones PerúRosa de AméricaPas encore d'évaluation
- Las Mascotas en El Sistema Familiar. Legitimidad, Formación y Dinámicas de La Familia Humano-AnimalDocument21 pagesLas Mascotas en El Sistema Familiar. Legitimidad, Formación y Dinámicas de La Familia Humano-AnimalCarolina GarridoPas encore d'évaluation
- Perforación Radicular Durante El Procedimiento Endodóntico - Artículos - IntraMedDocument7 pagesPerforación Radicular Durante El Procedimiento Endodóntico - Artículos - IntraMednallejazxPas encore d'évaluation
- Cannabis Sativa. (II)Document28 pagesCannabis Sativa. (II)Ruben Kapa TiconaPas encore d'évaluation
- CervicalgiaDocument175 pagesCervicalgiawww.pacourgencias.blogspot.com/100% (3)
- 308 - Chapter N.2 Maquinaria Moderna en Agricultura - SPAINDocument8 pages308 - Chapter N.2 Maquinaria Moderna en Agricultura - SPAINGarcía-Hernández Raúl VidalPas encore d'évaluation
- InformeDocument25 pagesInformeCEFACUNDOSPas encore d'évaluation
- Principio 90 10Document3 pagesPrincipio 90 10wolverinei3Pas encore d'évaluation
- Laboratorio de Biología 10Document8 pagesLaboratorio de Biología 10Keila MartinezPas encore d'évaluation
- PROTOCOLOS BANERJI (Homeopatía de La Evidencia)Document96 pagesPROTOCOLOS BANERJI (Homeopatía de La Evidencia)Guido AB0% (1)
- Bioprocesos BiolixiviacionDocument5 pagesBioprocesos BiolixiviacionAbel AdrianPas encore d'évaluation
- Tricologia ExpoDocument14 pagesTricologia ExpoBrandon J. Salinas MamaniPas encore d'évaluation
- Ipa LiquenesDocument6 pagesIpa LiquenesLaura PérezPas encore d'évaluation
- Guía #9 Placenta.Document9 pagesGuía #9 Placenta.KatePas encore d'évaluation
- Medicina LegalDocument217 pagesMedicina LegalFranchesca OrtizPas encore d'évaluation
- 09 CEyEDocument14 pages09 CEyEClaudia PadillaPas encore d'évaluation
- Entrevista Joe DispenzaDocument7 pagesEntrevista Joe Dispenzaapi-3698923100% (4)
- Bioq Tema 3 - ATP y Transferencia de Energia 2022-2Document17 pagesBioq Tema 3 - ATP y Transferencia de Energia 2022-2Gianella Xiomara Valverde GómezPas encore d'évaluation
- Informe de FarmacognosiaDocument23 pagesInforme de FarmacognosiaMARISOL ESTHER SANTIAGO AMAOPas encore d'évaluation
- Nutrición DeportivaDocument115 pagesNutrición DeportivafredyaronescastilloPas encore d'évaluation
- Transferencia Embrionaria PorcinosDocument9 pagesTransferencia Embrionaria PorcinosJohanita ArangoPas encore d'évaluation
- Producción Industrial de Enzimas de Origen BacterianoDocument20 pagesProducción Industrial de Enzimas de Origen BacterianoLuis GbPas encore d'évaluation
- Analisis de Laboratorio Del Nitrogeno en El SueloDocument5 pagesAnalisis de Laboratorio Del Nitrogeno en El SueloGabriel Jima NarvaezPas encore d'évaluation
- P5.acidez de Los Cationes MetalicosDocument3 pagesP5.acidez de Los Cationes MetalicosjoelPas encore d'évaluation
- Anatomia y Fisiologia Humana IDocument82 pagesAnatomia y Fisiologia Humana IRicardo Vega GarcíaPas encore d'évaluation
- VERRUGAS - DescodificacionDocument6 pagesVERRUGAS - DescodificacionLuciano GilPas encore d'évaluation
- Presupuesto Casa de La Cultura Troje 123Document16 pagesPresupuesto Casa de La Cultura Troje 123Saúl Andrade MartinezPas encore d'évaluation
- EndosporasDocument5 pagesEndosporasMaria Camila Cabarcas RamosPas encore d'évaluation
- Ap14 Ufv PDFDocument2 pagesAp14 Ufv PDFdeandaevaPas encore d'évaluation