Académique Documents
Professionnel Documents
Culture Documents
Cues Ti On A Rio
Transféré par
anon-6721210 évaluation0% ont trouvé ce document utile (0 vote)
44 vues2 pagesTitre original
Cues Ti on a Rio
Copyright
© Attribution Non-Commercial (BY-NC)
Formats disponibles
DOC, PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Attribution Non-Commercial (BY-NC)
Formats disponibles
Téléchargez comme DOC, PDF, TXT ou lisez en ligne sur Scribd
0 évaluation0% ont trouvé ce document utile (0 vote)
44 vues2 pagesCues Ti On A Rio
Transféré par
anon-672121Droits d'auteur :
Attribution Non-Commercial (BY-NC)
Formats disponibles
Téléchargez comme DOC, PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 2
Cuestionario
Tabla Periódica de los elementos y enlaces químicos
1. ¿Cuáles eran triada de Döbenier? ¿De qué modo condujeron a
desarrollos posteriores de la periodicidad?
2. ¿Cuál crees que es la base de la Ley de las Octavas de Newlans?
3. Desde el punto de vista de la estructura electrónica, ¿qué tienen
en común los elementos del bloque s?
4. ¿Qué quiere decir el termino periodicidad aplicado a los elementos?
5. ¿En que se diferencia la tabla periódica moderna de la tabla de
Mendeleev?
6. ¿Cómo varía el tamaño de los átomos de los elementos en el tercer
periodo de izquierda a derecha?
7. Escribe los símbolos de los elementos que tienen siete electrones
en su nivel exterior de energía?
8. ¿Cómo se relacionan entre sí los elementos de un grupo?
9. ¿Qué tienen en común las estructuras electrónicas de los metales
alcalinos?
10. Escribe los símbolos de los elementos de la familia de los metales
alcalinos en orden de tamaño atómico creciente.
11. ¿Cómo se relacionan entre si los elementos de un periodo?
12. Escriba las estructuras de Lewis para el Cs, Ba, Ti, Pb, Po, At y
Rn. Menciona como se relacionan estas estructuras con el grupo en el
que está cada elemento.
13. Clasifica los siguientes elementos como metal, no metal y
metaloide: Potasio, Plutonio, Azufre, Antimonio, Yodo, Tugsteno,
Molibdeno y Germanio.
14. ¿En qué periodo o grupo aparece primero un electrón en un
orbital d?
15. ¿Qué elemento en cada uno de los siguientes pares tiene la
mayor radio atomico?
a) Na o K b) O o F c) Na o Mg d) Ti o Zr e) Br o I
16. ¿En cuales zonas generales de la tabla periódica se encuentran
los elementos con la mayor y menor electronegatividad?
17. Busca la tabla de valores de electronegatividad, indica cual de los
siguientes elementos es positivo y cual negativo?
a) H2O b) NO c) CCl4 d) NaF e)CH4
f) IBr g) NH3 h) HCl i) MgH2 j) PbS
k) LiH l) OF2
18. Clasifique el enlace entre los siguientes pares de elementos como
principalmente iónicos o principalmente covalentes, y menciona cual
es el símbolo
a) Sodio y cloro
b) Carbono e hidrógeno
c) Cloro y carbono
d) Calcio y oxígeno
e) Hidrógeno y azufre
f) Bario y oxígeno
g) Flúor y flúor
h) Potasio y flúor
19. Explique por qué, en general la energía de ionización disminuye al
ir de arriba y hacia abajo en una familia de elementos en la tabla
periódica.
20. Explique la diferencia entre afinidad electrónica y energía de
ionización.
21. Con las estructura de Lewis, indique la transferencia de electrones
en la formación de los siguientes compuestos iónicos a partir de sus
átomos.
a) MgF2 b) K2O c) CaO d) NaBr
22. ¿Qué son los electrones de valencia?
23. ¿Cuántos electrones de valencia hay en cada uno de los
siguientes átomos? H, K, Mg, He, Al, Si, N, P, O, Cl.
24. ¿Quién fue el científico que publico independientemente el
ordenamiento de los elementos basada en masas atómicas crecientes
semejante a la ordenación de Mendeleev.
25. En el grupo VA, cuál es el elemento que tiene el radio atómico
menor.
26. En el grupo IVA, cuál es el elemento que presenta mayor carácter
metálico.
27. ¿Por qué se dice que el sodio es un metal muy activo?
28. ¿Qué nombre recibe la energía necesaria para sacar o apartar un
electrón de un átomo?
29. ¿Qué nombre recibe el enlace que ocurre entre un ión positivo y
un ión negativo?
30. ¿A qué se llama ión poliatómico?
31. A media que disminuye la diferencia en electronegatividad entre
dos elementos, la tendencia de esos elementos para formar un enlace
covalente es:
32. ¿Qué es un enlace covalente?
Vous aimerez peut-être aussi
- Método de Rentabilidad o Capitalización de RentaDocument62 pagesMétodo de Rentabilidad o Capitalización de RentaDiego AcuñaPas encore d'évaluation
- IntroductionDocument28 pagesIntroductionalberPas encore d'évaluation
- Planta Arquitectonica - Parque Industrial Tala 01 23-02-21Document1 pagePlanta Arquitectonica - Parque Industrial Tala 01 23-02-21Javier Gonzalez RuizPas encore d'évaluation
- Reporte de Practica No. 7 - Arranque Por Autotransformador de Un Motor de Inducción 3Document14 pagesReporte de Practica No. 7 - Arranque Por Autotransformador de Un Motor de Inducción 3Ernesto Sotelo GarciaPas encore d'évaluation
- Espectrofotometría de Absorción AtómicaDocument78 pagesEspectrofotometría de Absorción AtómicaNahomi Mina RomeroPas encore d'évaluation
- Energia VaporDocument123 pagesEnergia Vaporzagl660802Pas encore d'évaluation
- Ad Astra Rocket CompanyDocument9 pagesAd Astra Rocket CompanyTravis BrockPas encore d'évaluation
- Seminario N°1 Estructura Atomica - 2023 - 2CDocument2 pagesSeminario N°1 Estructura Atomica - 2023 - 2Cayerhoy1612Pas encore d'évaluation
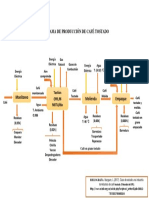
- Diagrama de Producción de Café TostadoDocument1 pageDiagrama de Producción de Café TostadoGuadalupe Castillo100% (1)
- NRF-044 Aisladores de Susp Sinteticos para LT de 161 A 400 KVDocument39 pagesNRF-044 Aisladores de Susp Sinteticos para LT de 161 A 400 KVdarkneoss100% (1)
- Estudio Sobre Fijacion de Carbono en PlantacionesDocument86 pagesEstudio Sobre Fijacion de Carbono en PlantacionesdfavendaPas encore d'évaluation
- Factura - 2021 07 09Document2 pagesFactura - 2021 07 09Gabriel ManPas encore d'évaluation
- PLANILLA DE DESVIACIONES HAZOP-lunesDocument10 pagesPLANILLA DE DESVIACIONES HAZOP-lunesEstefanny ArispePas encore d'évaluation
- Ficha Tec. Autotrol AmericanaDocument6 pagesFicha Tec. Autotrol AmericanaSalvador HuarancaPas encore d'évaluation
- 11 Patrones de Margorit GordonDocument3 pages11 Patrones de Margorit GordonRoDo ReYeZ0197Pas encore d'évaluation
- LORTIDocument169 pagesLORTILenin Camargo EnríquezPas encore d'évaluation
- Unidad HidraulicaDocument4 pagesUnidad HidraulicaJonathan Cortes FaundezPas encore d'évaluation
- Como Hacer Una Turbina Eólica CaseraDocument4 pagesComo Hacer Una Turbina Eólica Caserajose silveraPas encore d'évaluation
- Circuitos ResonantesDocument19 pagesCircuitos ResonantesSaritaStefiGuerreroPas encore d'évaluation
- Marco Teorico MotoresDocument5 pagesMarco Teorico MotoresDaniel MartinezPas encore d'évaluation
- Tarea de Capacitancia y DieléctricosDocument29 pagesTarea de Capacitancia y DieléctricosAles PeresPas encore d'évaluation
- Especificaciones Tecnicas - EstructuraDocument40 pagesEspecificaciones Tecnicas - EstructuraGregory Epifania PinedaPas encore d'évaluation
- Efecto MagnusDocument20 pagesEfecto MagnuscyanhidricoPas encore d'évaluation
- Practica 02Document1 pagePractica 02Oscar Joao Perez MoralesPas encore d'évaluation
- Ct-Terra Clima - Piura PDFDocument2 pagesCt-Terra Clima - Piura PDFProyectos2 aym insistecPas encore d'évaluation
- AbonadorasDocument12 pagesAbonadoraszztrieleroPas encore d'évaluation
- Autoclaves y EsterilizadoresDocument17 pagesAutoclaves y EsterilizadoresRosy Hernandez SanchezPas encore d'évaluation
- Hormi 2Document9 pagesHormi 2Xavier TravezPas encore d'évaluation
- IC-OPE-27.3.R01 - Muestreo de Emisiones GaseosasDocument6 pagesIC-OPE-27.3.R01 - Muestreo de Emisiones GaseosasYOMIRA ALARCON DURANPas encore d'évaluation