Académique Documents
Professionnel Documents
Culture Documents
AMINOÁCIDOS
Transféré par
Adrian Alejandro Ramirez LemusCopyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
AMINOÁCIDOS
Transféré par
Adrian Alejandro Ramirez LemusDroits d'auteur :
Formats disponibles
AMINOCIDOS.
Los aminocidos son sustancias compuestas por carbono, oxgeno, hidrgeno y nitrgeno. Son compuestos cristalinos que contienen un grupo cido dbil, carboxilo (-COOH) y un grupo bsico dbil, amina (-NH2), unido al carbono a (el carbono a de un cido orgnico es aquel inmediato al carboxilo). Se les denomina, por tanto, a-aminocidos y se considera que son neutros. Estas son las caractersticas generales, naturalmente aparecen excepciones como el que en la molcula existe algn tipo de cidos ms, que da lugar a los denominados aminocidos cidos, o que prestan algn grupo amino ms, los denominados aminocidos bsicos, o que incluso incorporan en la estructura molecular otros elementos, como el azufre (S) y que se denominan aminocidos azufrados, o que en lugar de tener una estructura molecular lineal tenga una configuracin cclica en la que se sitan los aminocidos aromticos y los denominados aminocidos de cadena, as como tambin, que la posicin del grupo no sea en a. Finalmente la prolina, que en realidad no es un a-aminocido, pues el carbono adyacente al de la funcin carboxilo posee un grupo imino (=NH); por tanto, la prolina es un iminocido. Las estructuras de los aminocidos son pticamente activas, es decir, que pueden rotar el plano de luz polarizada en diferente direccin dependiendo del estereoismero que se trate. Entre ellos hay que distinguir entre los que rotan el plano hacia la izquierda, levorrotatorios, levgiros o L, y los que lo hacen hacia la derecha, dextrorrotatorios, dextrgiros o D. En la naturaleza encontramos una mezcla de ambos que se denomina racmica, pero los aminocidos que forman las protenas son, la gran mayora, L.
Figura 1: Esquema de los aminocidos como precursores de otras molculas. Tomado de "Bioqumica" (E. Herrera)
Los aminocidos son los precursores de otras molculas de gran importancia biolgica que son las protenas. La unin de aminocidos da lugar a la formacin de pptidos que se denominan dipptidos, tripptidos, tetrapptidos, pentapptidos, octapptidos o polipptidos, si en su formacin intervienen, 2, 3, 4, 5, 8 o un nmero cualquiera superior. La unin de polipptidos entre s da lugar a la formacin de protenas.
Funciones de los aminocidos
Los aminocidos son los componentes bsicos de las protenas, pero para cada protena, la secuencia, es decir el orden en que van ordenados los aminocidos, es diferente. El nmero de secuencias posibles es tan grande que se explica la gran cantidad de protenas diferentes.
Tabla 1: Funciones de las protenas
En general, todos los nombres de aminocidos tienen la terminacin -ina lo que indica una relacin con el grupo amina. Algunos aminocidos conocidos, como por ejemplo, la fenilalanina, forman parte esencial de los neurotransmisores, tanto en el cerebro como fuera de l. La metionina y el triptofano son componentes esenciales del hgado. La tirosina y la glutamina, son segregadas por la glndula tiroides.
Biosntesis de los aminocidos
Cada organismo vivo sintetiza sus propias protenas a partir de los aminocidos. Las plantas superiores sintetizan a su vez todos los aminocidos necesarios. Hay que destacar que los animales carecen de esa capacidad. Cada especie animal puede sintetizar slo algunos aminocidos que necesita y, por lo tanto, depende de la dieta para incorporar aquellos aminocidos que debe sintetizar para formar protenas. Esos aminocidos se los considera esenciales y no porque sean los nicos necesarios para la vida de la especie, sino porque deben estar incluidos en la dieta. Cada especie, tiene su grupo de aminocidos esenciales propios. La mayora de los aminocidos que ingerimos se encuentran en forma de protenas, sin embargo slo los aminocidos pueden incorporarse a las diferentes rutas metablicas. Para ello, las protenas y pptidos ingeridos sufren un proceso de hidrolizacin por medio de enzimas proteolticas (secretadas por el estmago, pncreas e intestino delgado) en el tracto gastrointestinal. Despus de la accin de las enzimas los aminocidos quedan libres y son absorbidos y transportados a la corriente sangunea por medio de la que llegan al hgado donde ocurre su metabolismo y distribucin.
Las protenas endgenas tambin se degradan despus de un tiempo y adquieren unas seales que van a indicar a las enzimas de degradacin cuando deben comenzar su proceso. Los aminocidos libres que provienen de este proceso de digestin de las protenas son absorbidos por las paredes del intestino y conducidos por medio del sistema porta-heptico. Una vez que llegan al hgado, a travs de la corriente sangunea, son distribuidos por las clulas para su posterior utilizacin.
Implicaciones funcionales de los aminocidos
En los perodos en que el organismo atraviesa crisis funcionales (desnutricin aguda o crnica, traumatismos o trastornos articulares y/o musculares, alteraciones en el tracto gastrointestinal, hepatitis, afecciones renales, deficiencias cerebrales o nerviosas, etc.) o demandas extras por razones mecnicas (atletas, etc.) o cerebrales (estrs, exmenes, etc.) se produce aumento en el consumo de los aminocidos, por lo que muchas veces conviene completar la dieta habitual por medio de la administracin exogna de los mismos. Por las mismas razones, la ingesta de alimentos que contienen aminocidos significa adems un extraordinario recurso preventivo, por cuanto incorpora al organismo mecanismos de fortalecimiento ante previsibles compromisos extra, sean stos derivados de circunstancias especiales o de inevitables decadencias de las funciones orgnicas derivadas de la edad. El organismo no almacena el exceso de aminocidos que provienen de la dieta, lo que ocurre es que los transforma en intermediarios metablicos comunes como son el piruvato, oxalacetato y a-cetoglutarato, es decir, que los aminocidos van a ser precursores de la glucosa, cidos grasos y cuerpos cetnicos, es decir, actan como combustible y precursores metablicos.
Figura 2: Esquema sobre la visin general del metabolismo de los aminocidos. Tomado de "Bioqumica" (E. Herrera)
Clasificacin de los aminocidos
Como ya hemos comentado de los 20 aminocidos proteicos conocidos, 8 son esenciales para la vida humana y 2 semiesenciales. Son estos 10 aminocidos los que requieren ser incorporados al organismo en su cotidiana alimentacin y, especialmente, en los momentos en que el organismo ms los necesita cuando se da una situacin de disfuncin o enfermedad. Los ocho aminocidos esenciales son treonina, metionina, lisina, valina, triptfano, leucina, isoleucina y fenilalanina (adems puede aadirse la histidina como esencial durante el crecimiento, pero no para el adulto). Tambin existe otros aminocidos pero son poco frecuentes, son derivados de los aminocidos corrientes. Entre ellos encontramos a la 4-hidroxiprlina e hidroxilisina presentes en el colgeno y de la desmosina e isodesmosina presentes en la protena fibrosa elastina. Por otro lado tambin estn los aminocidos no proteicos que son un grupo formado por 150 aminocidos. Se presentan en diferentes clulas y tejidos en forma libre o combinada, pero nunca en las protenas y actan como precursores en el metabolismo. Por ejemplo, la b-alanina, precursor de la vitamina cido pantotnico, la homocisteina y homoserina, intermediarios en el metabolismo de los aminocidos. La citrulina, ornitina, cido-g-aminobutrico, D-alanina, Dserina. En hongos y plantas superiores abundan la canavanina y la b-cianolanina. Por otro lado, los aminocidos se pueden clasificar siguiendo varios criterios en funcin de sus propiedades qumicas y fsicas.
Tabla 2: Tipos de aminocidos en funcin de la cadena R.
Los aminocidos, como ya hemos comentado, son materia prima de protenas y pptidos que cumplen diferentes funciones en nuestro organismo. No obstante, tambin pueden utilizarse como materia prima del metabolismo energtico, de hecho, alrededor del 30% de los
aminocidos, pasan a una ruta metablica que, despus de eliminar el nitrgeno de la molcula, enva los productos desaminados al ciclo de Krebs. La eliminacin de nitrgeno ocurre de dos maneras diferentes, el grupo amino sera transferido a otra molcula o es eliminado para convertirlo en urea, en el caso del hombre.
Lista de Aminocidos (Esenciales y no esenciales) y funcin de cada una de ellos:
Alanina: Funcin: Interviene en el metabolismo de la glucosa. La glucosa es un carbohidrato simple que el organismo utiliza como fuente de energa. Arginina: Funcin: Est implicada en la conservacin del equilibrio de nitrgeno y de dixido de carbono. Tambin tiene una gran importancia en la produccin de la Hormona del Crecimiento, directamente involucrada en el crecimiento de los tejidos y msculos y en el mantenimiento y reparacin del sistema inmunolgico. Asparagina: Funcin: Interviene especficamente en los procesos metablicos del Sistema Nervioso Central (SNC). Acido Asprtico: Funcin: Es muy importante para la desintoxicacin del Hgado y su correcto funcionamiento. El cido L- Asprtico se combina con otros aminocidos formando molculas capases de absorber toxinas del torrente sanguneo. Citrulina: Funcin: Interviene especficamente en la eliminacin del amonaco. Cistina: Funcin: Tambin interviene en la desintoxicacin, en combinacin con los aminocidos anteriores. La L - Cistina es muy importante en la sntesis de la insulina y tambin en las reacciones de ciertas molculas a la insulina. Cistena: Funcin: Junto con la L- cistina, la L- Cistena est implicada en la desintoxicacin, principalmente como antagonista de los radicales libres. Tambin contribuye a mantener la salud de los cabellos por su elevado contenido de azufre. Glutamina: Funcin: Nutriente cerebral e interviene especficamente en la utilizacin de la glucosa por el cerebro. Acido Glutminico: Funcin: Tiene gran importancia en el funcionamiento del Sistema Nervioso Central y acta como estimulante del sistema inmunolgico. Glicina: Funcin: En combinacin con muchos otros aminocidos, es un componente de numerosos tejidos del organismo. Histidina: Funcin: En combinacin con la hormona de crecimiento (HGH) y algunos aminocidos asociados, contribuyen al crecimiento y reparacin de los tejidos con un papel especficamente relacionado con el sistema cardio-vascular. Serina: Funcin: Junto con algunos aminocidos mencionados, interviene en la desintoxicacin del organismo, crecimiento muscular, y metabolismo de grasas y cidos grasos. Taurina: Funcin: Estimula la Hormona del Crecimiento (HGH) en asociacin con otros aminocidos, esta implicada en la regulacin de la presin sangunea, fortalece el msculo cardiaco y vigoriza el sistema nervioso. Tirosina: Funcin: Es un neurotransmisor directo y puede ser muy eficaz en el tratamiento de la depresin, en combinacin con otros aminocidos necesarios. Ornitina: Funcin: Es especfico para la hormona del Crecimiento (HGH) en asociacin con otros aminocidos ya mencionados. Al combinarse con la L-Arginina y con carnitina (que se sintetiza en el organismo, la L-Ornitina tiene una importante funcin en el metabolismo del exceso de grasa corporal. Prolina: Funcin: Est involucrada tambin en la produccin de colgeno y tiene gran importancia en la reparacin y mantenimiento del msculo y huesos.
Los Ocho (8) Esenciales Isoleucina: Funcin: Junto con la L-Leucina y la Hormona del Crecimiento intervienen en la formacin y reparacin del tejido muscular. Leucina: Funcin: Junto con la L-Isoleucina y la Hormona del Crecimiento (HGH) interviene con la formacin y reparacin del tejido muscular. Lisina: Funcin: Es uno de los ms importantes aminocidos porque, en asociacin con varios aminocidos ms, interviene en diversas funciones, incluyendo el crecimiento, reparacin de tejidos, anticuerpos del sistema inmunolgico y sntesis de hormonas. Metionina: Funcin: Colabora en la sntesis de protenas y constituye el principal limitante en las protenas de la dieta. El aminocido limitante determina el porcentaje de alimento que va a utilizarse a nivel celular. Fenilalanina: Funcin: Interviene en la produccin del Colgeno, fundamentalmente en la estructura de la piel y el tejido conectivo, y tambin en la formacin de diversas neurohormonas. Triptfano: Funcin: Est inplicado en el crecimiento y en la produccin hormonal, especialmente en la funcin de las glndulas de secrecin adrenal. Tambin interviene en la sntesis de la serotonina, neurohormona involucrada en la relajacin y el sueo. Treonina: Funcin: Junto con la con la L-Metionina y el cido Asprtico ayuda al hgado en sus funciones generales de desintoxicacin. Valina: Funcin: Estimula el crecimiento y reparacin de los tejidos, el mantenimiento de diversos sistemas y balance de nitrgeno.
Protenas
En animales superiores, las protenas son los compuestos orgnicos ms abundantes, pues representan alrededor del 50% del peso seco de los tejidos. Desde el punto de vista funcional, su papel es fundamental. No existe proceso biolgico alguno que no dependa de la presencia y/o actividad de este tipo de sustancias; las protenas cumplen diferentes funciones: enzimas, hormonas, trasportadores, los anticuerpos, receptores de muchas clulas, etc. Todas las protenas contienen carbono, hidrgeno, oxgeno y nitrgeno y casi todas poseen tambin azufre. Si bien hay ligeras variaciones en diferentes protenas, el contenido de nitrgeno representa, trmino medio, el 16% de la masa total de la molcula, lo cual permite calcular la cantidad de protena existente en una muestra, por medicin del N de la misma. Las protenas son molculas polimricas (poli: muchos; meros: partes) de enorme tamao; pertenecen a la categora de macromolculas, constituidas por gran nmero de unidades estructurales que forman largas cadenas. Debido a su gran tamao, cuando se dispersa a estas molculas en un solvente adecuado, forman obligadamente soluciones coloidales, con caractersticas especiales que las distinguen de las soluciones de molculas pequeas. Por medio de la hidrlisis, las molculas protenicas son escindidas en sus monmeros, los aminocidos. Y cientos o miles de estos aminocidos pueden participar en la formacin de la gran molcula polimrica de una protena. Las protenas resultan de la unin de molculas de aminocidos por medio de enlaces peptdicos. Por esto, se pueden clasificar en dos grandes categoras, protenas globulares y protena fibrosas.
Tabla 3: Categoras de protenas.
Estructura molecular
La estructura de las protenas es muy compleja, razn por la cual resulta conveniente describirla considerando distintos niveles de organizacin:
Estructura Primaria
Se refiere al nmero e identidad de los aminocidos que componen la molcula y al ordenamiento o secuencia de esas unidades en la cadena polipeptdica. La unin peptdica slo permite formar estructuras lineales; por ello, las cadenas no presentan ramificaciones.
Estructura Secundaria
A medida que la longitud de las cadenas va aumentando y en funcin de las condiciones fsicoqumicas del medio, se conforma la estructura secundaria, que es la disposicin espacial regular, repetitiva, que puede adoptar la cadena polipeptdica, generalmente mantenida por enlaces de hidrgeno. En este caso suelen darse dos tipos de enlace: Hlice a: las cadenas de aminocidos tienen varios centros polares y, debido a esto, la fibra suele enrollarse dando lugar a una hlice que se estabiliza formando enlaces intramoleculares con puentes de hidrgeno. Lmina b: las cadenas de pptidos se unen formando filas paralelas que se estabilizan de manera intermolecular mediante puentes de hidrgeno.
Estructura Terciaria
Es la estructura de la mayora de las protenas globulares, aparece a partir de que la hlice a se vuelve a enrollar. Es una arquitectura tridimensional completa que se debe a las fuerzas de atraccin o repulsin electrosttica, a enlaces de hidrgeno, a fuerzas de Van der Walls y a puentes disulfuro.
Estructura Cuaternaria
Son estructuras de carcter oligomrico, que estn compuestos por varias cadenas separadas pero entrelazadas en estructura terciaria. Se aplica slo a protenas constituidas por dos o ms cadenas polipeptdicas y se refiere a la disposicin espacial de esas cadenas y a los enlaces que se establecen entre ellas (puentes de hidrgeno, atracciones electrostticas, interacciones
hidrofbicas, puentes disulfuro entre cistenas de cadenas diferentes, etc.). Un ejemplo de este tipo de estructura es la hemoglobina que est compuesta por cuatro subunidades de mioglobina.
Defectos del metabolismo de los aminocidos Alcaptonuria Cistinuria Encefalopata glicina, la CME - no cetsica hiperglicinemia, NKH Histidinemia Homocistinuria Hyperlysinemia De jarabe de arce Enfermedad de la orina, esta enfermedad Aciduria metilmalnica Fenilcetonuria La tirosinemia tipo I -tirosinosis Tipo II Tyrosinnemia -Richner-Hanhart sndrome La tirosinemia tipo III
Aminocido
Familia
Enzima catalizadora
Sustrato original
Intermediarios Producto final
Lugar donde se lleva a cabo
Alanina Arginina Asparagina Aspartato Cistena Glicina Glutamato Glutamina Histidina Prolina Serina Tirosina
Instrucciones: 1. Por medio de grficos, describe la reaccin qumica que se produce para obtener aspargina. 2. Por medio de grficos, describe la reaccin qumica por la cual se forma aspartato a partir del glutamato y oxalacetato. 3. Especfica las enzimas que participan en las reacciones anteriores y describe la funcin que desempean. Entrega la tarea a tu profesor, en formato de reporte.
Vous aimerez peut-être aussi
- El Efecto FotoelectricoDocument23 pagesEl Efecto FotoelectricoDavidSuarezPas encore d'évaluation
- 3° y 4° Semana 3Document4 pages3° y 4° Semana 3Nela Puma SotoPas encore d'évaluation
- HDS EstirenoDocument8 pagesHDS Estirenopaloma aspePas encore d'évaluation
- B Proceso de Manufactura - Soldadura de GasDocument8 pagesB Proceso de Manufactura - Soldadura de GasFrank SorianoPas encore d'évaluation
- Índices de MillerDocument4 pagesÍndices de MillerFernando GarciaPas encore d'évaluation
- Administracion y Logistica 2ed Bowersox.Document11 pagesAdministracion y Logistica 2ed Bowersox.Paula RamirezPas encore d'évaluation
- Práctica 1. Ejemplos de Mezcla Homogénea y Heterogénea.Document3 pagesPráctica 1. Ejemplos de Mezcla Homogénea y Heterogénea.Ángel ArriagaPas encore d'évaluation
- 7.0 PLANO DE CRP TIPO 7 A2-Cr-07Document1 page7.0 PLANO DE CRP TIPO 7 A2-Cr-07Javier Xavi CMPas encore d'évaluation
- Red Contra IncendiosDocument14 pagesRed Contra IncendiosDaniel LojanoPas encore d'évaluation
- Quimica QuânticaDocument31 pagesQuimica QuânticaPedro RosárioPas encore d'évaluation
- EXPLOSIVOSDocument30 pagesEXPLOSIVOSGenoveva Cruz Juarez100% (1)
- Manual Prevencion Incendios DemsaDocument238 pagesManual Prevencion Incendios Demsaoscar palenciaPas encore d'évaluation
- Informe Esterificación de FischerDocument7 pagesInforme Esterificación de FischerLuisafcaPas encore d'évaluation
- Exposición de Biomateriales y Biosensores - CianoacrilatoDocument26 pagesExposición de Biomateriales y Biosensores - CianoacrilatoLuis Rios CarrilloPas encore d'évaluation
- Revision 1 Catabolismo 1 2Document2 pagesRevision 1 Catabolismo 1 2liss alvaradoPas encore d'évaluation
- BioelementosDocument14 pagesBioelementosFernanda Chuquillanqui RuizPas encore d'évaluation
- Erosion CorrosionDocument9 pagesErosion CorrosionCesar Perez SerratoPas encore d'évaluation
- Guía de Laboratorio AMCDocument24 pagesGuía de Laboratorio AMCGeraldine MargaretPas encore d'évaluation
- S01 S2-EjerciciosDocument4 pagesS01 S2-EjerciciosLuisW.NoriegaPas encore d'évaluation
- Zinc Acetil AcetonaDocument3 pagesZinc Acetil AcetonaJose Antonio Cubillos BokaPas encore d'évaluation
- Actividad 3 Toxicologia MatrizDocument3 pagesActividad 3 Toxicologia MatrizElver HUERTAS RAMIREZPas encore d'évaluation
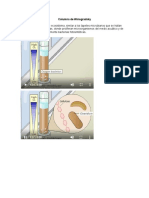
- Columna de WinogradskyDocument6 pagesColumna de WinogradskyNataliaPas encore d'évaluation
- Tesis 2Document97 pagesTesis 2Fran velazquezPas encore d'évaluation
- Flujograma de Procedimiento de Preparación de Un JarabeDocument4 pagesFlujograma de Procedimiento de Preparación de Un JarabeLidia Escobar100% (1)
- Prueba HidrocarburosDocument4 pagesPrueba HidrocarburosNicole Alejandra Abarca CamposPas encore d'évaluation
- Factores Que Influyen en El Crecimiento yDocument8 pagesFactores Que Influyen en El Crecimiento yAnthony BaltazarPas encore d'évaluation
- Guia de Problemas - Reactores IdealesDocument4 pagesGuia de Problemas - Reactores IdealesDianaMenchacaPas encore d'évaluation
- Gases Arteriales PaulaDocument12 pagesGases Arteriales PaulaCarolina Montaño RuizPas encore d'évaluation
- Ejercicios Propiedades Coligativas y EquilibrioDocument1 pageEjercicios Propiedades Coligativas y EquilibrioMICHELL NATALIA HERNANDEZ GARCÍAPas encore d'évaluation
- Recocido de Aisi 1020Document2 pagesRecocido de Aisi 1020Johan Medina TovarPas encore d'évaluation