Académique Documents
Professionnel Documents
Culture Documents
NIA
Transféré par
Carmen RomeroCopyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
NIA
Transféré par
Carmen RomeroDroits d'auteur :
Formats disponibles
EL potencial de accin de Na
Sirvindonos del programa informtico Neurons in action pretendemos con este trabajo conocer en profundidad el potencial de accin del sodio. Concretamente llevaremos a cabo las siguientes tareas: -Observar el potencial de accin y las corrientes inicas que conlleva, as como los cambios en la conductancia en un patch de la membrana. -Experimentar con la temperatura, analgsicos y toxinas y observar sus efectos en el potencial de accin. -Examinar el periodo refractario que tiene lugar tras un potencial de accin y las consecuencias de este en la excitabilidad de la membrana
Comprender la forma de la corriente de sodio
Tras haber estimulado un axn y haber disparado un potencial de accin, los canales de sodio dependientes de voltaje se abren originando esto una corriente de iones de sodio. Como sabemos, con unos milisegundos de posterioridad tendr lugar la apertura de los canales de potasio, lo que igualmente dar lugar a una corriente de iones de potasio. Comparando ambas corrientes, observamos una clara diferencia en la forma de las grficas: en el curso temporal de la corriente de sodio aparecen dos fases (Grfica 2).
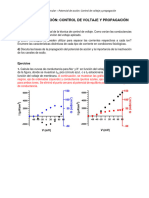
Grfica 1: Potencial de accin de membrana En rojo: Potencial de equilibrio del sodio En verde: Estmulo (20mV) En negro: Potencial de accin En azul: Potencial de equilibrio del potasio Eje X: tiempo (ms) Eje Y: voltaje
Grfica 2: Corrientes inicas de sodio y potasio En rojo: Corriente inica de iones de sodio En azul: Corriente inica de iones de potasio Eje X: tiempo (ms) Eje Y: corriente de membrana (mA/cm^2)
Para explicar la causa del ciclo temporal de la corriente de sodio nos apoyaremos en el concepto de fuerza de conduccin (Grfica 3). La fuerza de conduccin es la diferencia entre el potencial de membrana y el potencial de equilibrio del in del cual estemos midiendo la fuerza de conduccin (Fuerza de conduccin= Vm- ENa); su incremento implica un aumento de la cantidad de iones que atraviesa la membrana [INa = GNa( Vm- ENa)]. Como observamos en la grfica 3 la fuerza de conduccin es mayor al principio (-120mV), y decrece casi hasta 0 durante el potencial de accin, para luego volver a crecer hasta un valor de -130mV.
Grfica 3: Fuerza de conduccin del sodio En rojo: Potencial de equilibrio del sodio En negro: Potencial de accin En marrn: Fuerza de conduccin de los iones de sodio Eje X: tiempo (ms) Eje Y: voltaje (mV)
Pues bien, la razn para la anomala en la corriente del sodio se debe a que mientras que el potencial de accin se acerca al potencial de equilibrio (ENa), la fuerza conductora de iones de sodio se acerca a 0, la corriente de de sodio es reducida. Como estamos muy cerca de un potencial en el que no hay corriente de iones de sodio esta es muy pequea. Mientras el potencial de accin se aleja del equilibrio del sodio en su fase de caida(falling phase), la corriente de sodio se incrementa de nuevo fluyendo hacia adentro, hacia canales abiertos que no han sido an inactivados. Es decir la cada del potencial de accin implica un alejamiento del ENa, los iones no se encuentran ya en su potencial y de reposo, y lo que tienden es a desplazarse.
Obsrvese como ese primer pico (kink) aparece en el mismo momento (X=1.3ms) que la fuerza de conduccin llega a 0, y que el potencial de accin se aproxima y casi alcanza el potencial de equilibrio del sodio. Esto nos da evidencia de la veracidad de nuestro razonamiento.
Utilizacin de agentes analgsicos, bloqueadores tanto de canales de Na+ como de K+ (procana y lidocana).
Esta simulacin de Neurons in Actions consiste en observar y analizar como vara un potencial de accin al aplicar diferentes frmacos a la clula que lo sufre. En esta ocasin se le suministrar procana y lidocana, agentes analgsicos locales que actan como bloqueadores tanto de canales de Na+ como de K+, es decir, inhiben el paso de iones Na+ al medio intracelular e inhiben el paso de iones K+ al medio extracelular, y por tanto, tambin inhiben la generacin de un potencial de accin, que tiene como consecuencia el bloqueo de la propagacin del impulso nervioso. Como el programa de simulacin virtual Neurons in Actions no tiene la posibilidad de aplicar frmacos, se conseguir un efecto similar a la aplicacin de estos variando la densidad de los canales de Na+ y K+ de una clula hipottica. A menor densidad de canales de Na+ y K+ mayor cantidad de analgsico suministrado.
A continuacin se procede a observar y comentar cada una de las situaciones que se nos han mostrado a la hora de realizar la simulacin: 1- Al aplicar una densidad de canales de Na+ de 0,06 S/cm y una densidad de canales de K+ de 0,018 S/cm, es decir, al aplicar una cierta cantidad de procana y lidocana, observamos que se produce un potencial de accin de 40 mV aproximadamente, por lo que habr que suministrar ms cantidad de analgsicos o bien disminuir la densidad de canales de Na+ y K+ para que el potencial de accin no se produzca. 2- Al disminuir la densidad de canales de Na+ a 0,03 S/cm y la densidad de canales de K+ a 0,009 S/cm, es decir, al aplicar una mayor cantidad de procana y lidocana que la inicial, observamos que se sigue produciendo un potencial de accin de 30 mV aproximadamente, es decir, menor que el anterior potencial de accin, por lo que se deber seguir suministrando mayor cantidad de analgsicos hasta que el potencial de accin cese. 3- Al seguir disminuyendo la densidad de canales de Na+ a 0,01 S/cm y la densidad de canales de K+ a 0,004 S/cm, o bien, al suministrar una cantidad de dichos analgsicos an mayor que la anterior, podemos observar que el potencial de accin se ha visto reducido notablemente a 5mV aproximadamente, pero todava se sigue produciendo por lo que se tiene que aumentar an ms la cantidad de dichos frmacos. 4- Finalmente, al reducir la densidad de canales de Na+ a 0,005 S/cm y la cantidad de canales de K+ a 0,003 S/cm observamos que ya no se produce el potencial de accin, debido a que hemos suministrado la cantidad precisa de procana y lidocana para que dicho potencial de accin no se genere.
Podemos observar que a medida que se aumenta la cantidad de analgsicos suministrados disminuye la densidad de canales de Na+ y K+ por lo que la despolarizacin del potencial de accin ( entrada de iones Na+ al medio intracelular) y la repolarizacin de dicho potencial ( salida de iones K+ del medio intracelular al extracelular) tardan ms tiempo en producirse, debido a que al disminuir el nmero de canales de Na+ y K+ activos, cada vez entran menos iones Na+, lo que provoca que la despolarizacin se produzca ms lentamente, y cada vez salen menos iones K+ del medio intracelular al extracelular por lo que la repolarizacin tambin se producir con mayor lentitud (tardarn en producirse ms milisegundos).
Aplicacin de tetrodotoxina (TTX), bloqueador altamente especfico de canales de Na+.
En esta ocasin suministraremos a una clula hipottica un frmaco conocido como tetrodotoxina o TTX. La TTX es extrada del pez globo y acta como un bloqueador altamente especfico de canales de Na+, al igual que otros frmacos como la saxitoxina (STX) o la batracotoxina (BTX). Como slo utilizaremos la TTX, en el programa de simulacin virtual Neurons in Actions slo modificaremos la densidad de canales de Na+, dejando la densidad de canales de K+ en su valor inicial, ya que en este caso no se van a utilizar bloqueantes de canales de K+.
A continuacin se procede a observar y a comentar cada una de las situaciones que se nos han mostrado a la hora de realizar la simulacin:
1- Al aplicar una densidad de canales de Na+ de 0,06 S/cm, es decir, al suministrar una cierta cantidad de TTX observamos que se produce un potencial de accin de 32 mV aproximadamente, por lo que habr que suministrar una mayor cantidad de TTX o bien disminuir la densidad de canales de Na+ hasta que el potencial de accin no se produzca.
2- Al disminuir la densidad de canales de Na+ a 0,005 S/cm y 0,004 S/cm, es decir, al aplicar una mayor cantidad de TTX que en el caso anterior, se producen potenciales de accin de 25 mV y 15 mV respectivamente, por lo que podemos observar, que dicho potencial de accin ha disminuido pero se tendr que aplicar an ms TTX o bien reducir todava ms la densidad de canales de Na+ para que el potencial de accin no se produzca. 3- Finalmente, al disminuir la densidad de canales de Na+ a 0,003 S/cm, o lo que es semejante, al aplicar una mayor cantidad de TTX, observamos que ya no se produce el potencial de accin, debido a que hemos suminisrado la cantidad precisa de tetrodotoxina para que el potencial de accin no se genere.
Podemos observar que a medida que aplicamos mayor cantidad de TTX o disminuimos la densidad de canales de Na+ , la despolarizacin ocurrida en el potencial de accin ( entrada de iones Na+ al medio intracelular) tarda ms tiempo en producirse, debido a que cada vez entran
menos iones Na+ del medio extracelular, ya que cada vez hay menos canales de Na+ funcionando con normalidad. En cambio, observamos que la repolarizacin de dicho potencial de accin no se ve modificada, ya que al no bloquear los canales de K+, stos no se ven afectados en su normal funcionamiento, permitiendo as la salida de iones K+ del medio intracelular al extracelular en condiciones totalmente normales.
Cabe destacar que tanto en la aplicacin de agentes analgsicos bloqueantes tanto de canales de Na+ como de K+ como en la aplicacin de TTX observamos siempre una pequea despolarizacin inicial, que no es debida a la activacin de dichos canales voltaje-dependientes sino al propio estmulo suministrado. Como conclusin, a la hora de bloquear potenciales de accin es ms eficaz la aplicacin de tetrodotoxina que la de agentes analgsicos locales como la procana y lidocana, ya que como hemos podido comprobar se necesita menos cantidad de TTX (al necesitar menor cantidad se produce una mayor densidad de canales de Na+, 0,03 S/cm) que de agentes analgsicos, de los que se necesita una mayor cantidad (al necesitar mayor cantidad se produce una menor densidad de canales de Na+, 0,005 S/cm) para bloquear un potencial de accin, por lo que ser ms efectivo si suministramos TTX que dichos agentes analgsicos locales.
Vous aimerez peut-être aussi
- MACARTHUR, John. (2017) - El Pastor Como Teólogo. Interpretar y Aplicar La Palabra de Dios Con PrecisiónDocument213 pagesMACARTHUR, John. (2017) - El Pastor Como Teólogo. Interpretar y Aplicar La Palabra de Dios Con PrecisiónCesar Augusto Sacrab Macz82% (11)
- El MaridajeDocument8 pagesEl MaridajeLaleska Salinas FallaPas encore d'évaluation
- Qué Es y Cómo Funciona La Bomba Sodio PotasioDocument9 pagesQué Es y Cómo Funciona La Bomba Sodio PotasioNataliaAndreaAristizabalSuarez100% (2)
- Cap5 Guyton PDFDocument8 pagesCap5 Guyton PDFAnna Lopez100% (1)
- Reporte Practica 4Document8 pagesReporte Practica 4Alan Jack Prieto GilPas encore d'évaluation
- Clasificación Del GlaucomaDocument2 pagesClasificación Del GlaucomaAndreas Schilling MoralesPas encore d'évaluation
- Seminario Biopotenciales FisiologiaDocument9 pagesSeminario Biopotenciales Fisiologiayamirjossue100% (9)
- Potencial de MembranaDocument45 pagesPotencial de MembranaKary.lili100% (1)
- Tema 3Document23 pagesTema 3MariaPas encore d'évaluation
- Schunemann - El Papel de La VíctimaDocument11 pagesSchunemann - El Papel de La Víctimavalcarsalson100% (1)
- Guía de Seminario 3 Excitabilidad, Potencial de Acción y Sinapsis.Document13 pagesGuía de Seminario 3 Excitabilidad, Potencial de Acción y Sinapsis.zScratPas encore d'évaluation
- Actividad 4 - 5Document3 pagesActividad 4 - 5ElectraPas encore d'évaluation
- Taller5 SolucionesDocument4 pagesTaller5 Solucionesssmrt.2016Pas encore d'évaluation
- Informe Potencial de AcciónDocument16 pagesInforme Potencial de AcciónFernanda Arredondón100% (2)
- TP Potenciales y Sinapsis PDFDocument10 pagesTP Potenciales y Sinapsis PDFSabrina PortelliPas encore d'évaluation
- Practica No. 5Document33 pagesPractica No. 5Ania Jessa RuizPas encore d'évaluation
- Informe Bases Ionicas y Potencial de AxonDocument7 pagesInforme Bases Ionicas y Potencial de AxonSara AcostaPas encore d'évaluation
- II Examen Parcial de Psicofisiolgía IarregloDocument21 pagesII Examen Parcial de Psicofisiolgía IarregloBlanca Malca CaveroPas encore d'évaluation
- Práctica 5 Excitabilidad NeuronalDocument14 pagesPráctica 5 Excitabilidad NeuronalJuan Pablo V HernandezPas encore d'évaluation
- Experimento de Laboratorio Con NERVEDocument16 pagesExperimento de Laboratorio Con NERVENicoll Perez ManosalvaPas encore d'évaluation
- Practica 3 FisiologiaDocument14 pagesPractica 3 FisiologiaLuisa RVPas encore d'évaluation
- Bomba Calcio PotasioDocument4 pagesBomba Calcio PotasioAlberto LeoperPas encore d'évaluation
- Guia de Neuro CompletaDocument109 pagesGuia de Neuro CompletaCatherine María de los Ángeles Mamani ApazaPas encore d'évaluation
- Laboratorio Simulación de Potenciales de Acción y Modelo HHDocument11 pagesLaboratorio Simulación de Potenciales de Acción y Modelo HHangie paezPas encore d'évaluation
- M3 Qué DecirDocument7 pagesM3 Qué DecirRaïssaDomonPas encore d'évaluation
- Simulación de Potencial de AcciónDocument12 pagesSimulación de Potencial de AcciónAngel E. RockPas encore d'évaluation
- Capítulo 5Document7 pagesCapítulo 5Rashel MoscosoPas encore d'évaluation
- Simulacion Por ComputadoraDocument17 pagesSimulacion Por ComputadoraJeeniffer CookieePas encore d'évaluation
- Prueba de Fisiologia PDFDocument4 pagesPrueba de Fisiologia PDFsebastian camusPas encore d'évaluation
- Potenciales de Memrana y Potenciales de AcciónDocument17 pagesPotenciales de Memrana y Potenciales de AcciónGabriela Hu MaPas encore d'évaluation
- Experimento de Laboratorio Con NERVEDocument18 pagesExperimento de Laboratorio Con NERVENicoll Perez ManosalvaPas encore d'évaluation
- Potencial Electroquimico de Los IonesDocument18 pagesPotencial Electroquimico de Los Ionesjenny salas fernandezPas encore d'évaluation
- Fis U3 P3e1 LuclDocument11 pagesFis U3 P3e1 LuclAlejandra MartinezPas encore d'évaluation
- SEMINARIO INOR, Ampliacion Metales AlcalinosDocument21 pagesSEMINARIO INOR, Ampliacion Metales AlcalinosaltiPas encore d'évaluation
- Práctica de Anestésicos LocalesDocument8 pagesPráctica de Anestésicos LocalesDulce Hernández VPas encore d'évaluation
- El Efecto FotoelectricoDocument9 pagesEl Efecto FotoelectricoPaola Alexandra MoraPas encore d'évaluation
- Potencial de Acción - FisiologíaDocument6 pagesPotencial de Acción - FisiologíaDara DosPas encore d'évaluation
- Capitulo 5 FisiologiaDocument4 pagesCapitulo 5 FisiologiaBárbara Mérida100% (1)
- Cañón de PlasmaDocument15 pagesCañón de Plasmaomar2323Pas encore d'évaluation
- La Comunicación Intraneuronal e InterneuronalDocument3 pagesLa Comunicación Intraneuronal e InterneuronalErwin Florez Rojas100% (1)
- Módulo 2Document8 pagesMódulo 2sasha.angel.880Pas encore d'évaluation
- 1 Informe de Laboratorio de Física ModernaDocument4 pages1 Informe de Laboratorio de Física ModernaAndres Yepes AcostaPas encore d'évaluation
- 04 - 2 Excitabilidad II (Mecanismos de Excitabilidad Celular)Document6 pages04 - 2 Excitabilidad II (Mecanismos de Excitabilidad Celular)Adolfo Uribe VidalPas encore d'évaluation
- Fisiología Médica IDocument156 pagesFisiología Médica ICristóbal Muñoz Pérez100% (3)
- Potenciales de Membrana y Potenciales de AccionDocument31 pagesPotenciales de Membrana y Potenciales de AccionJordi M' Gtz50% (2)
- Simulación Por Computadora Del Potencial de AcciónDocument15 pagesSimulación Por Computadora Del Potencial de AcciónRicardo RZPas encore d'évaluation
- Fases de Potencial de AccionDocument50 pagesFases de Potencial de Accionjose antonio soto floresPas encore d'évaluation
- Potencial de Accion TrabajoDocument7 pagesPotencial de Accion TrabajoLH DiazPas encore d'évaluation
- Capitulo 5 Potenciales de Membrana y Potenciales de AccionDocument5 pagesCapitulo 5 Potenciales de Membrana y Potenciales de AccionEvelynPas encore d'évaluation
- Tema 5 Fisiologia de La Membrna, Nervio y MusculoDocument6 pagesTema 5 Fisiologia de La Membrna, Nervio y MusculoNoelia Teresa Chalco VillaPas encore d'évaluation
- Neurona, Neuroglía y SinapsisDocument36 pagesNeurona, Neuroglía y SinapsisnataliaPas encore d'évaluation
- Taller Neurociencias Potencial NeuronalDocument6 pagesTaller Neurociencias Potencial NeuronalLeidy Paola Cancelado SuarezPas encore d'évaluation
- Practicas 1y2 Fisiologia - 3CM11Document12 pagesPracticas 1y2 Fisiologia - 3CM11Brenda JocelynPas encore d'évaluation
- Cap.6.6 Tsokos Fisica NuclearDocument10 pagesCap.6.6 Tsokos Fisica NuclearRina Diaz EscobarPas encore d'évaluation
- Preinforme 2 FQDocument5 pagesPreinforme 2 FQIngrithFierroPas encore d'évaluation
- Guía Resuelta Cardio y Resp UBA Cat 1Document97 pagesGuía Resuelta Cardio y Resp UBA Cat 1Denise IzaiasPas encore d'évaluation
- Practica 5 "SIMULACIÓN POR COMPUTADORA DEL POTENCIAL DE ACCIÓN "Document18 pagesPractica 5 "SIMULACIÓN POR COMPUTADORA DEL POTENCIAL DE ACCIÓN "Haylie RGPas encore d'évaluation
- Práctica 13 Potenciales de Acción - CuadernilloDocument13 pagesPráctica 13 Potenciales de Acción - CuadernillojuanPas encore d'évaluation
- Simulación Con NeuronDocument13 pagesSimulación Con NeuronLuiguiAlexisCheroNunura100% (3)
- Preinforme 2 FQDocument5 pagesPreinforme 2 FQIngrithFierroPas encore d'évaluation
- Practica 6Document10 pagesPractica 6sendthepainPas encore d'évaluation
- Comprobacion Experimental Del Teorema de SuperposicionDocument7 pagesComprobacion Experimental Del Teorema de SuperposicionAndres GilPas encore d'évaluation
- Cómo Empezó La Educación Física en El Renacimiento y La IlustraciónDocument2 pagesCómo Empezó La Educación Física en El Renacimiento y La IlustraciónKEVIN ALEXANDER MAYORGA GARCIAPas encore d'évaluation
- Manual de Implementación Programa 5sDocument97 pagesManual de Implementación Programa 5sJulio Armando Fabaz0% (1)
- Curriculo Practico y CriticoDocument5 pagesCurriculo Practico y CriticoAlejandra ArboledaPas encore d'évaluation
- Colestasia FINALDocument47 pagesColestasia FINALFernando González PeruggiPas encore d'évaluation
- Que Es La Psicología, Historia, Objeto, MétodoDocument5 pagesQue Es La Psicología, Historia, Objeto, MétodoDelfina BritosPas encore d'évaluation
- Analisis Carta A La Tierra y Agenda 21Document3 pagesAnalisis Carta A La Tierra y Agenda 21Paco BetancourtPas encore d'évaluation
- Instrucción Analisis Seguridad Del Trabajo ASTDocument19 pagesInstrucción Analisis Seguridad Del Trabajo ASTCarolaPeraltaPas encore d'évaluation
- Diferencias de Responsabilidad Civil y Penal en Relacion A EnfermeriaDocument3 pagesDiferencias de Responsabilidad Civil y Penal en Relacion A EnfermeriaLeslie Thalia Rojas JustinianoPas encore d'évaluation
- Semana 2Document4 pagesSemana 2Luuis EstobanPas encore d'évaluation
- García GarduñoDocument26 pagesGarcía GarduñoAmi BellerosePas encore d'évaluation
- Etnias Del EcuadorDocument114 pagesEtnias Del EcuadorJazmin MaciasPas encore d'évaluation
- Mira Por Qué NO Debes Sacrificar Todo Por Tus HijosDocument4 pagesMira Por Qué NO Debes Sacrificar Todo Por Tus HijosLouising Alvarez MontalvoPas encore d'évaluation
- Triptico VII B Psicomotricidad IDocument2 pagesTriptico VII B Psicomotricidad IdulcempezarPas encore d'évaluation
- Red Semantica de Elementos de Narracion PDFDocument1 pageRed Semantica de Elementos de Narracion PDFElmo El poopPas encore d'évaluation
- La Tabula PeutingerianaDocument14 pagesLa Tabula PeutingerianaDIETOTENPas encore d'évaluation
- Fondos de Amortización y La Enseñanza SecundariaDocument5 pagesFondos de Amortización y La Enseñanza Secundariaamerico aquinoPas encore d'évaluation
- Recurso Correa SelameDocument87 pagesRecurso Correa SelameJacob Olivos100% (4)
- Clase23OCT PDFDocument64 pagesClase23OCT PDFAdrian FdzPas encore d'évaluation
- FODA Santa BeatrizDocument26 pagesFODA Santa Beatrizmaria estherPas encore d'évaluation
- Entrevista A Carles Feixa. Por Caterine GalazDocument5 pagesEntrevista A Carles Feixa. Por Caterine GalazDianaPas encore d'évaluation
- Prólogo. Exclusión y Violencia. Breve Mirada A La Criminalidad "Contestataria" en El Puerto Rico Del Siglo XXIDocument3 pagesPrólogo. Exclusión y Violencia. Breve Mirada A La Criminalidad "Contestataria" en El Puerto Rico Del Siglo XXICarmen Ines Rivera LugoPas encore d'évaluation
- Programacion Academica-19-12-2019 16 - 21 - 24 PDFDocument5 pagesProgramacion Academica-19-12-2019 16 - 21 - 24 PDFMarcelo WaynePas encore d'évaluation
- Diabetes ExposiciónDocument22 pagesDiabetes ExposiciónArtyumPas encore d'évaluation
- Autores InteligenciaDocument5 pagesAutores InteligenciaCecilia MoralesPas encore d'évaluation
- Descripciones de PuestosDocument21 pagesDescripciones de PuestosIndhira AcostaPas encore d'évaluation