Académique Documents
Professionnel Documents
Culture Documents
Biologia Molecular Del Cancer (Conceptos Basicos) .
Transféré par
Alejandra ShalalaTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Biologia Molecular Del Cancer (Conceptos Basicos) .
Transféré par
Alejandra ShalalaDroits d'auteur :
Formats disponibles
Conceptos bsicos en biologa molecular del cncer. Susceptibilidad gentica Basic concepts in the molecular biology of cancer.
Genetic susceptibility
J. Garca-Foncillas, E. Bandrs, V. Cataln, F. Garca Amigot, N. Zabalegui
Laboratorio de Biotecnologa. rea de Terapia Celular. Departamento de Oncologa Clnica Universitaria. Universidad de Navarra
CONCEPTOS BSICOS EN BIOLOGA MOLECULAR
El ADN, localizado a nivel del ncleo de la clula, es una macromolcula de aspecto filamentoso formado por un gran nmero de desoxirribonucletidos que constituyen las unidades estructurales bsicas. Estos desoxirribonucletidos estn formados a su vez por una base nitrogenada, un azcar y un grupo fosfato. Las bases nitrogenadas son las portadoras de la informacin necesaria para sintetizar las protenas que la clula precisa en tanto que los grupos de azcar y fosfato tienen un papel estructural. En el ADN esta informacin se encuentra codificada en forma de genes que se definen como las unidades elementales de informacin y que contienen los datos necesarios para la fabricacin de una protena. La informacin codificada en un gen es transmitida a una molcula intermedia, denominada cido ribonucleico mensajero (ARNm), que es capaz de salir del ncleo y entrar en contacto con los ribosomas para iniciar la sntesis proteica. La transferencia de informacin gentica de ADN a ARNm se denomina transcripcin, el paso de ARNm a protena traduccin y el proceso global que engloba los dos previos expresin gnica. El ARNm antes de salir del ncleo sufre una maduracin durante la cual determinados fragmentos no tiles son eliminados en un fenmeno denominado "corte y empalme" o splicing. La transcripcin gnica est regulada por determinadas protenas, denominadas factores de transcripcin, que son capaces de unirse a unas regiones del ADN que anteceden a la secuencia de un gen y que se llaman regiones promotoras. La unin de factores de transcripcin-ADN a nivel de regiones promotoras pone en marcha la expresin de un gen. El ciclo vital de la clula est formado por cuatro etapas perfectamente diferenciadas. Normalmente la clula se encuentra en fase G1. En esta fase la clula realiza sus funciones fisiolgicas y es metablicamente muy activa. Cuando se va a dividir entra en un proceso que est constituido por las otras tres fases de su ciclo vital o celular. La primera etapa de esta divisin celular es la fase S o fase de sntesis. Durante este periodo se sintetiza una copia del ADN. Al final de este periodo la clula todava no dividida cuenta con dos copias de su ADN. Una vez completada la duplicacin del ADN, proceso denominado replicacin, entra en la siguiente etapa o fase G2 (intervalo 2). En este periodo se preparan los mecanismos necesarios para acometer la fragmentacin celular que se desarrollar en el siguiente paso o fase de mitosis (fase M). Una vez realizada la
separacin de ambas clulas hijas cada una con su correspondiente copia de ADN, estas vuelven otra vez a fase G0 para desarrollar su actividad fisiolgica concreta. Este proceso de replicacin es controlado por un grupo de protenas que tienen por finalidad supervisar el ciclo celular de manera que una clula no entra en una nueva fase hasta no haberse superado unas comprobaciones necesarias previas denominadas puntos de chequeo (checkpoint). La finalidad de esta supervisin radica en que la clula slo se divida cuando sea preciso y respondiendo siempre a niveles de control ms elevados a nivel supracelular. Asimismo, estas comprobaciones son necesarias para asegurar que las copias del ADN que se generan sean iguales a la molcula progenitora evitando la introduccin de fallos o errores en el proceso de duplicacin o replicacin. Una de las protenas ms importantes en este proceso de control lo constituye la protena p53 codificada por el gen p53. El ADN es una macromolcula con capacidad de reparacin. Durante la vida de una clula puede verse sometida a agresiones externas (txicos, agentes infecciosos, radiaciones, ...) que pueden daar el ADN. La protena p53 acta vigilando continuamente el ADN y detectando alteraciones a nivel de genes que pueden traducirse en protenas con estructura y funcin alterada. Si el dao producido por el agente externo no es importante, el p53 induce mecanismos de reparacin resolviendo las alteraciones observadas. Sin embargo, puede ocurrir que la lesin sea tan importante que no pueda ser reparada y en tal caso la protena p53 pone en marcha un proceso de muerte celular activa o apoptosis. Este fenmeno de apoptosis se diferencia claramente del proceso normal de necrosis o muerte celular en que en el primero la clula participa de forma activa en su destruccin constituyendo lo que algunos autores han denominado "suicidio celular", evitando de esta forma transmitir una informacin deteriorada contenida en el ADN a las clulas hijas.
PROCESO DE TRANSFORMACIN NEOPLSICA
El control de la proliferacin celular expuesto en el epgrafe previo puede alterarse en algunos de los puntos de chequeo o comprobacin del ciclo celular provocando una divisin desmesurada. Las causas que pueden ocasionar esta alteracin en las restricciones que limitan la divisin celular son en la mayora de los casos adquiridas de forma que en un momento de la vida una lesin gentica importante con un fallo en los mecanismo de reparacin puede desencadenar un proceso neoplsico. El proceso de carcinognesis implica, no obstante, varios eventos. Normalmente, existe un primer suceso, denominado iniciacin, donde un agente externo o un error endgeno coloca a la clula en una situacin de mayor susceptibilidad o predisposicin para transformarse en neoplsica. En un segundo momento se produce la conversin en clula cancerosa de una clula previamente susceptible. En el campo de la carcinognesis por agentes externos qumicos, el dimetilbenzatracina puede hacer ms sensible o susceptible a una clula produciendo un fenmeno de iniciacin. No obstante, se necesita la intervencin de otro producto, el 12-O-tetradecanoilforbol, para producir la promocin o transformacin neoplsica de una clula ya iniciada. Los genes que codifican las protenas implicadas en la regulacin de la divisin celular parecen ser los responsables de la transformacin neoplsica en sus primeras fases. Los agentes exgenos o errores endgenos pueden inducir la expresin de genes cuyas protenas activan la entrada de la clula en divisin celular. Estos genes se llaman oncogenes promotores, porque desencadenan una proliferacin descontrolada dando
lugar a una neoplasia. Entre stos destacan el myc, jun, fos, ras, etc. Asimismo, estos mismos factores exgenos o endgenos pueden simultneamente bloquear la expresin o daar otros genes cuyas protenas tienen una funcin de inhibicin de la proliferacin provocando ambos mecanismos conjuntamente una prdida de las restricciones de la divisin y un aumento de los factores promitticos. Este segundo grupo de genes con actividad de supervisin y control se denominan oncogenes supresores por su papel regulador de la proliferacin evitando el desarrollo de neoplasias. En este grupo el ms importante es el gen p53 que acta como "el guardian de la clula" por excelencia. Estos procesos producen por tanto un aumento muy significativo de protenas derivadas de oncogenes promotores que tendran que encontrarse en niveles muy reducidos o nulos y a la vez niveles bajos o alteraciones funcionales de protenas supresoras (resultado de la traduccin de oncogenes supresores). La carcinognesis conlleva a su vez una prdida del reconocimiento de las clulas tumorales como anmalas no evidencindose una adecuada respuesta inmunitaria. Se ha comprobado que tanto las protenas que se encuentran anormalmente incrementadas como aquellas anmalas pueden ser incorporadas y presentadas por los complejos de histocompatibilidad tipo 1, actuar como neoantgenos y desencadenar una respuesta inmunolgica. Estos antgenos tumorales presentados por los complejos de histocompatibilidad tipo 1 (MHC-1), en la superficie de las clulas tumorales activan a los linfocitos T cooperadores o CD4+ (T helper) provocando la liberacin de citoquinas que estimulan el crecimiento y maduracin de los linfocitos T citotxicos o CD8+. Al mismo tiempo, estos linfocitos citotxicos se unen a travs de su receptor especfico (TCR, T-cell receptor) a los antgenos presentados por los MHC-1 en la superficie de las clulas neoplsicas. Sin embargo, esto no es suficiente para desencadenar una respuesta de los CD8+ frente a la clula cancerosa. Hoy sabemos que estos linfocitos CD8+ precisan una co-estimulacin o segundo estmulo simultneo: la clula tumoral tiene que expresar a nivel de membrana una protena denominada B7 capaz de interaccionar a nivel de la membrana linfocitaria con el CD28 o con el CTLA-4 y completar el estmulo originado por el TCR desencadenando por tanto la respuesta citotxica. Sin embargo, en la clula tumoral se ha evidenciado una disminucin o ausencia de la expresin de los MHC-1 y/o de la protena B7 impidiendo por tanto que estas clulas presenten antgenos que pudieran desarrollar una respuesta inmunitaria o impidiendo completar una reaccin citotxica al faltar la co-estimulacin de la protena CD28 o CTL-4 necesaria para ello. Los puntos de control del ciclo celular son rutas reguladoras que controlan el orden y el tiempo de transicin del ciclo celular, y aseguran que etapas crticas, como la replicacin del DNA y la segregacin de cromosomas, sean completados con alta fidelidad. Los puntos de control responden al dao con parada del ciclo celular para que la clula disponga de tiempo para la reparacin e induciendo la transcripcin de genes que faciliten la reparacin. La prdida de puntos de control da como resultado inestabilidad genmica y han sido implicados en la evolucin de clulas normales en clulas cancerosas. Se conocen, como ya hemos adelantado, tres estadios donde operan los puntos de control en el ciclo celular: - Al final de la fase G1 donde el punto de control llamado punto de control de restriccin
R asegura que la clula antes de entrar en la fase S, tenga un tamao adecuado. Adems, la clula detecta si las condiciones intracelulares y extracelulares son idneas (tamao celular, presencia de nutrientes y de factores de crecimiento) para seguir adelante y comenzar la sntesis de DNA. Es el punto de control ms importante. - En la fase G2 existe un segundo punto de control llamado punto de control G2-M. En este punto la clula detecta antes de entrar en mitosis si la replicacin del DNA se ha completado correctamente y si el tamao es el adecuado para la duplicacin en dos clulas hijas. - Finalmente, en la mitosis existe el punto de control M. Este punto de control se localiza en la metafase y comprueba, antes de seguir adelante con la mitosis celular, que los cromosomas se han alineado correctamente sobre el huso mittico.
REGULACIN DEL CICLO CELULAR
El ciclo celular es regulado por la formacin secuencial, activacin e inactivacin de una serie de molculas reguladoras del ciclo celular, que incluyen un grupo de subunidades reguladoras llamadas ciclinas y otro grupo de subunidades catalticas denominadas quinasas dependientes de ciclina (CDK). La fosforilacin de protenas implicadas en los procesos que tienen lugar a lo largo del ciclo celular, como la sntesis de DNA y la mitosis, la llevan a cabo un conjunto de protenas quinasa, que catalizan la transferencia de grupos fosfato desde el ATP a la protena. Estas protenas quinasa son las CDK, que son activas enzimticamente cuando se unen a un segundo grupo de protenas llamadas ciclinas. Diferentes ciclinas se unen especficamente a diferentes CDK para formar una serie de complejos en fases especificas del ciclo celular y conducir a la clula de un estado del ciclo celular a otro. Ciclinas Las ciclinas son una familia de protenas que, como indica su nombre, son sintetizadas y destrudas durante cada ciclo celular. Hasta la fecha se han descrito las siguientes ciclinas: A, B1, B2, C, D1, D2, D3, E, F, G1, G2, H, I, K, T1 y T2. Todas ellas contienen una regin comn conocida como "cyclin box", de aproximadamente 150 aminocidos, que es un dominio relativamente conservado y es responsable de la unin y activacin de las CDK. Mutaciones en esta regin inhiben tanto la unin como la activacin. Las ciclinas C, D y E (o ciclinas G1) son protenas de vida corta que funcionan principalmente durante la fase G1 y en la transicin de G1-S, siendo destruidas por la va de la ubiquitina. La va de la ubiquitina es ATP dependiente e implica la unin covalente de molculas de ubiquitina a los sustratos diana. Las protenas modificadas de esta manera son reconocidas y degradadas por el proteosoma. La proteolisis mediada por la protena ubiquitina juega un papel crucial en el control del ciclo celular, ya que la irreversibilidad de la proteolisis provee de una fuerte direccionalidad al ciclo celular, forzando a seguir hacia delante en varias etapas crticas. La sntesis de ciclina D (D1, D2, D3), como se ver ms adelante, est inducida por factores de crecimiento. Cuando se expresa constantemente, sin la necesidad de factores
de crecimiento, las clulas tienen tendencia a mantenerse en un ciclo de divisin constante. Se le considera como un oncogn; aunque por s misma no es capaz de transformar una clula normal en cancerosa, colabora con otros oncogenes. Las ciclinas A y B son ciclinas mitticas que permanecen estables durante la interfase, pero son rpidamente proteolizadas durante la mitosis, por una va dependiente de la ubiquitina. Se ha observado que mutaciones en la ciclina A producen la inhibicin de la iniciacin de la mitosis, parando las clulas en la fase G2. En la actualidad se dispone de poca informacin acerca de las ciclinas F y G, recientemente descritas, aunque parece ser que la ciclina F acta en la transicin de la fase G2 a la fase M, y la ciclina G acta en respuesta al dao del DNA. La ciclina H, se sabe que forma complejos con la CDK7, para producir una enzima conocida como quinasa activante dependiente de ciclina que est implicada en la activacin de las quinasas CDC2 y CDK2. Quinasas dependientes de ciclina (CDK) Las CDK son una familia de protenas quinasas que se unen a ciclinas especficas y son activadas por ellas. Hasta la fecha, se han descrito al menos nueve quinasas dependientes de ciclinas: CDC2 (tambin llamada CDK1, p34 o MPF, -factor promotor de la fase M-), CDK2, CDK3, CDK4, CDK5, CDK6, CDK7, CDK8 y CDK9. Las CDK4, CDK5 y CDK6 forman complejos con las ciclinas de la familia D y funcionan durante la fase G0/G1 del ciclo. Segn otros autores, parece ser que se unen principalmente a CDK4, durante un periodo muy concreto, el final de la fase G1 y el inicio de la fase S. Una de las funciones de los complejos ciclina D/CDK4 es fosforilar la protena del retinoblastoma (Rb) y activar as la expresin de genes necesarios para la entrada en la fase S. La CDK2 puede unirse tambin a miembros de la familia de la ciclina D, pero ms comnmente se asocia con las ciclinas A y E y estn implicados en el inicio de la fase S, es decir, en la replicacin del DNA. As el complejo ciclina A/CDK2 parece tener un papel en el control de la elongacin de la sntesis de DNA. Como se menciona anteriormente, CDK7 se encuentra asociada con la ciclina H y tiene la capacidad de fosforilar tanto CDC2 como CDK2. La CDC2, se une a las ciclinas mitticas A y B. Los complejos ciclinas B y CDC2 son los ms importantes. Son rpidamente activados durante la mitosis y se asocian al huso acromtico en la metafase. La ciclina B se degrada en la transicin de la metafase a la anafase causando la inactivacin de la CDC2. Esto parece ser necesario para la finalizacin de la mitosis, ya que se ha visto que mutaciones en las ciclinas B, que evitan su degradacin, bloquean las clulas en esta etapa del ciclo celular. Parece ser que el punto de control M controla la degradacin de la ciclina B1. No todas las ciclinas y CDK funcionan como reguladoras del ciclo celular. Otras funciones que se han descrito para las ciclinas y CDK han sido la regulacin de la
transcripcin, reparacin del DNA, diferenciacin y apoptosis. Por ejemplo, diferentes complejos ciclina/CDK, como ciclina C/CDK8, ciclina T/CDK y ciclina H/CDK7, se sabe que son componentes de la maquinaria basal de transcripcin. Por otro lado, la ciclina K forma un complejo con la RNA polimerasa II a travs de la activacin de una CDK no identificada. Inhibidores de las quinasas dependientes de ciclina Adems de esta serie de reguladores positivos del ciclo celular (ciclinas y CDK) existe una familia de reguladores negativos denominados inhibidores de las quinasas dependientes de ciclinas, que bloquean la actividad de uno o varios complejos ciclinaCDK. En las clulas animales, se dividen en dos familias distintas, que difieren en estructura, mecanismo de accin y especificidad: la familia KIP/CIP y la familia INK4. Estas protenas inhibidoras de las CDK estn implicadas en la parada del ciclo celular en respuesta a varias seales antiproliferativas como privacin de factores de crecimiento, citoquinas, dao en el DNA celular, entre otras. La familia KIP/CIP incluye tres protenas estructuralmente relacionadas entre s, p21, p27 y p57, y presenta una ms amplia especificidad que la familia INK4, ya que sus miembros interactan e inhiben la actividad quinasa de los complejos ciclina E/CDK2, ciclina D/CDK4, ciclina D/CDK6, ciclina A/CDK2 y ciclina B/CDC2 y actan a lo largo del ciclo celular. La protena p21( tambin llamada Cip I, WAF1) fue el primer miembro aislado de la familia. Diferentes investigadores aislaron la p21 gracias a su capacidad para interactuar con CDK2, aunque puede inhibir otros complejos ciclinas conteniendo otras CDK, como la CDK4. Adems, p21 tambin puede unirse al antgeno nuclear de proliferacin celular (PCNA), una subunidad de la DNA polimerasa, y as inhibir directamente la sntesis de DNA. El gen p21 fue clonado como un gen inducido por la protena supresora de tumores p53. Cuando el DNA es daado, se provoca un incremento de la concentracin y de la actividad de la protena p53. Cuando se activa la protena p53 estimula la transcripcin de un gen que codifica para la protena p21. La protena p21 bloquea el ciclo celular en la transicin G1-S, unindose a complejos ciclina-CDK (ciclina D/CDK4 y ciclina E/CDK2), responsables de conducir a la clula a la fase S. Esta parada del ciclo celular permite a la clula reparar el DNA daado antes de replicarse. El gen p21, fue aislado como un gen que se acumula en clulas prximas a la senescencia, sugiriendo que esta protena puede jugar un papel importante en este proceso celular. La protena p27 media seales inhibidoras del crecimiento como la del factor de crecimiento transformante b (TGF-b) y la inhibicin por contacto. Tambin se ha demostrado que ratones que carecen de esta protena, son anormalmente grandes, con hiperplasia en diferentes rganos. La protena p57, a diferencia de la expresin ubicua de las protenas p21 y p27, tiene una ruta de expresin tejido-especfica, lo que sugiere un
papel especializado en el control de ciclo celular. La familia INK4 incluye cinco protenas, p14, p15 (INK4B), p16 (INK4A), p18 (INK4C) y p19 (INK4D), los cuales inhiben especficamente los complejos de ciclina D/CDK4 y D/CDK6 que estn implicados en el control de la fase G1. A diferencia de las protenas de la familia KIP/CIP, que se unen a complejos ciclina/CDK, la familia INK4 se une a subunidades monomricas y su mecanismo de accin consiste en competir con las ciclinas por las subunidades catalticas CDK. La protena p16 parece jugar un nico papel en la regulacin del estatus de la protena Rb. Al igual que con el gen Rb, el gen p16 est alterado en muchos tumores humanos. A pesar de la fuerte homologa que existe entre las protenas p16 y p15, stas parecen desempear diferentes funciones biolgicas. As, el nivel de la protena p15, no parece estar afectado por la protena Rb, aunque s es inducido por un factor inhibidor del crecimiento como es el TGF-b. Las protenas p18 y p19 tambin responden a estmulos extracelulares. As, algunos tipos de clulas tratadas con el interferon se altera la expresin de la p18. Adems, la interleuquina-6 induce la expresin de las protenas p16 y p18 en clulas hematopoyticas, y se correlaciona con parada del ciclo celular en G1 y diferenciacin terminal. A parte de los inhibidores de quinasas dependientes de ciclina, existen otros reguladores negativos del ciclo celular que son los formados por los productos de los genes supresores de tumores TP53 y Rb que pueden interactuar y modular las actividades de los complejos ciclina/CDK.
ONCOPROTENAS CITOPLASMTICAS TRANSMISORAS DE SEALES
En esencia, nicamente hay dos mecanismos bioqumicos por los que los protooncogenes citoplasmticos actan. Uno de los mecanismos implica la fosforilacin de protenas en residuos de serina, treonina o tirosina. Diversas oncoprotenas de esta categora, denominadas quinasas, transfieren grupos fosfato de la molcula donadora ATP a los aminocidos mencionados en la protena receptora. La fosforilacin de protenas tiene dos funciones fundamentales en transduccin de seales. En primer lugar, puede cambiar la conformacin y, como consecuencia, provocar un incremento en la actividad enzimtica de la protena fosforilada. En segundo lugar, la fosforilacin de los residuos de tirosina genera sitios de reconocimiento para protenas sealizadoras. En cualquier caso la fosforilacin contribuye a la transmisin y amplificacin de la seal mitognica. El segundo mecanismo por el que los proto-oncogenes transmiten la seal implica la actividad enzimtica GTPasa. Las protenas que se unen a GTP actan como interruptores moleculares y se denominan protenas G. La unin de GTP induce un cambio conformacional que mantiene la protena G en un estado activo, capaz de transmitir la seal mediante la interaccin con protenas efectoras. La hidrlisis del GTP a GDP, catalizada por la actividad GTPasa intrnseca, devuelve la protena G a un estado inactivo. Existen reguladores positivos que promueven la transicin de la protena G a su estado activo, unida a GTP, a travs de una actividad intercambiadora de nucletidos, y reguladores negativos o efectores que devuelven la protena G a su estado inactivo,
unida a GDP, mediante la estimulacin de la actividad GTPasa intrnseca. Protenas con actividad GTPasa El papel desempeado por la protenas con actividad GTPasa en tumorignesis fue puesto de manifiesto gracias al descubrimiento de los oncogenes de la familia ras que codifican una forma previamente desconocida de GTPasas monomricas pequeas. Se han identificado tres alelos de ras, denominados H-ras, K-ras y N-ras, por su presencia en virus con actividad transformante y por ensayos de transfeccin de DNA. La capacidad de unir nucletidos de guanina de las protenas Ras fue una de las primeras actividades bioqumicas descritas para el producto de un oncogn. El descubrimiento de una forma activada del gen ras en lneas de carcinoma de vejiga humano signific el hallazgo del primer oncogn humano, y la mutacin puntual del aminocido glicina en posicin 12 por valina fue la primera mutacin identificada en un oncogn humano. Ms importante an, la activacin de uno de los tres genes ras es la mutacin dominante ms comn encontrada en cnceres humanos. Este hecho refleja la crtica funcin que juega ras en la transduccin de la seal mitognica en numerosos tipos celulares y lo convierte en uno de los oncogenes mejor estudiados. Ras pertenece a la conocida como superfamilia de protenas Ras, cuyos miembros regulan numerosos procesos celulares, incluida la sealizacin mitognica (Ras y protenas relacionadas), la organizacin del citoesqueleto (Rho, Rac y Cdc42), funciones nucleares (Ran) y el trfico de membranas y protenas (Rab). Los miembros de la familia de protenas Ras son modificados postraduccionalmente mediante la unin de un lpido isoprenoide, el radical farnesilo, que las ancla a la cara interna de la membrana plasmtica. La asociacin a la membrana es esencial para la funcin de las protenas Ras. Ciertos dominios de estas protenas son homlogos de la subunidad implicada en la unin de nucletidos de guanina en las protenas G heterotrimricas. De hecho, las protenas de la familia Ras se unen a nucletidos de guanina (GTP y GDP). La capacidad de las protenas Ras para unirse a este tipo de nucletidos indica que funcionan de una manera semejante a otras protenas G, y que por lo tanto se encuentran en un equilibrio entre dos conformaciones: una activa, unida a GTP, y una inactiva, unida a GDP. En los ltimos tiempos se ha elucidado una gran parte de los componentes de la vas de transduccin de seales y se ha situado a las protenas de la familia Ras como reguladores cruciales de los procesos que parten de los receptores de factores de crecimiento y controlan la proliferacin y diferenciacin celular. La activacin de Ras en respuesta a la estimulacin de los receptores de factores de crecimiento est mediada por la unin de la protena adaptadora Grb2, cuyo dominio SH2 reconoce residuos de tirosina fosforilados en el receptor. A su vez, Grb2 interacciona a travs de sus dominios SH3 con el factor intercambiador de nucletidos de guanina (Guanine nuleotide Exchange Factor, GEF) Sos, localizndolo en la membrana plasmtica, donde se encuentra situado su sustrato Ras. De esta manera, Sos puede estimular el intercambio de GDP por GTP en Ras, lo que lleva a Ras desde su forma inactiva a su forma activa capaz de interaccionar con diversas molculas efectoras/sustratos. Por el contrario, la inactivacin de Ras est mediada en parte por su actividad GTPasa intrnseca. Normalmente esta actividad es baja, pero puede ser estimulada por una protena activadora de GTPasa, (GTPase Activating Protein, GAP), que convierte la forma activa
de Ras unida a GTP en la forma inactiva unida a GDP. GAP tambin contiene un dominio SH2 por el que interacciona con los receptores activados localizndose en la membrana plasmtica, lo que permite la regulacin negativa de Ras. Los procesos de activacin e inactivacin de Ras estn exquisitamente orquestados. La conversin de Ras a su forma unida a GTP le permite interaccionar con otras protenas que funcionan como efectores. Un efector de Ras es la serina treonina quinasa Raf. La activacin de Ras promueve su interaccin con Raf y localiza a esta ltima en la membrana, donde es activada y ejercita su actividad. La protena Raf as activada fosforila y activa MEK, que es una tirosina treonina quinasa. MEK a su vez fosforila las protenas ERK que son serina treonina quinasas. Las protenas ERK fosforilan entonces varias protenas, entre las que cabe destacar el factor de transcripcin Elk-135. Esta cascada de sealizacin se conoce como la ruta de las protena quinasas activadas por mitgenos (Mitogen Activated Protein kinases, MAP). La respuesta celular provocada por esta ruta de sealizacin incluye el incremento en la transcripcin de genes inmediatamente tempranos, como fos, que a su vez regulan la expresin de genes cuyos productos controlan la progresin en el ciclo celular, lo que finalmente da lugar a la sntesis de ADN y a la divisin celular. Adems de Raf la transformacin celular inducida por formas oncognicas de Ras tambin requiere la actividad de los miembros de la superfamilia de protenas Ras, Rho y Rac. Estas protenas estn implicadas en el reordenamiento del citoesqueleto de actina y regulan los cambios morfolgicos asociados con la transformacin celular inducida por el oncogn ras. Los oncogenes ras se han identificado en diversos tumores humanos. Las formas oncognicas de ras difieren de sus formas normales por mutaciones que resultan en la sustitucin de aminocidos localizados en las posiciones 12, 13, 59 y 61 en el dominio de unin a GDP/GTP de la protena. Esta oncoprotenas Ras estn fijadas en su forma activa unida a GTP a travs de un elevado intercambio de GDP por GTP o a travs de la prdida de la actividad GTPasa intrnseca.
JUN, FOS Y EL COMPLEJO TRANSCRIPCIONAL AP-1
Los genes jun y fos fueron identificados en un principio como los oncogenes v-jun y vfos, presentes en el genoma del virus del sarcoma aviar 17 y de los virus FBJ y FBR, que producen osteosarcomas en ratn, respectivamente. Los homlogos celulares de ambos oncogenes codifican protenas que son factores de transcripcin y dimerizan para formar el complejo de transcripcin denominado AP-1 (Activating Protein-1). Cada uno de ellos se engloba en una familia de protenas con actividad transcripcional ms amplia: la familia Jun, formada por c-Jun, JunB y JunD; y la familia Fos, formada por c-Fos, FosB, Fra-1 y Fra-2. El factor AP-1 puede estar compuesto por homodmeros formados por dos miembros de la familia Jun o por heterodmeros entre un miembro de la familia Jun y un miembro de la familia Fos. No se forman homodmeros entre miembros de la familia Fos. AP-1 es un factor de transcripcin que regula la expresin de genes inducidos por factores de crecimiento y promotores tumorales, como los steres de forbol. El complejo AP-1 se une a la secuencia de ADN TGACTCA desde donde regula la transcripcin de los genes adyacentes. Se conocen numerosos genes regulados por AP-1 fundamentales para la proliferacin y la diferenciacin celular, entre ellos los propios genes jun y fos. Las protenas Fos y Jun presentan claras homologas estructurales, como son el dominio de unin al ADN y el dominio encargado de la actividad transcripcional. El dominio de unin al ADN presenta dos subregiones, una rica en aminocidos bsicos, responsable
de la unin al ADN, y otra responsable de la dimerizacin, denominada cremallera de leucinas. La forma viral oncognica de la protena Jun difiere de la forma celular normal, adems de por diversas mutaciones puntuales, por la delecin de una pequea regin reguladora en el dominio aminoterminal responsable de la actividad transcripcional. v-Fos y c-Fos tambin difieren por ciertas sustituciones y por la delecin de 50 aminocidos en la regin carboxiterminal de la oncoprotena, que no afecta su capacidad para heterodimerizar y unirse al ADN. La actividad biolgica de las protenas Jun y Fos est regulada por fosforilacin. En el caso de Jun, la fosforilacin de dos serinas situadas en la regin aminoterminal, junto a la regin d, induce un incremento de su actividad transcripcional. Esta fosforilacin est mediada por la serina/treonina quinasa JNK (Jun N-terminal Kinase), que interacciona con Jun precisamente en la regin d, en respuesta a distintos estmulos, como factores de crecimiento, citoquinas inflamatorias y seales de estrs. La protena Fos tambin es activada por fosforilacin por otras quinasas activadas por factores de crecimiento, como las ERKs. Las alteraciones que presentan las formas oncognicas de estas protenas impiden su regulacin e incrementan su nivel de expresin, dando como resultado una actividad transcripcional permanente.
LOS FACTORES DE TRANSCRIPCIN MYC Y MYB
El gen myc fue inicialmente identificado como un oncogn del virus de la mielocitometosis aviar. Posteriores estudios mostraron la existencia de una familia de proto-oncogenes con actividad transcripcional compuesta por tres miembros: c-myc, nmyc y l-myc, que son frecuentemente sobreexpresados en numerosos cnceres humanos. Esta sobreexpresin se observa en neuroblastomas (n-myc), carcinomas microcticos de pulmn (n-myc y l-myc), carcinomas de mama, estmago, pulmn y colon, neuroblastomas y gliobastomas (c-myc), como consecuencia de amplificaciones; y en los linfomas de Burkitt (c-myc), como consecuencia de translocaciones. En clulas en cultivo, la sobreexpresin de c-myc da lugar a una inhibicin de la diferenciacin, una mayor sensibilidad a factores de crecimiento y una aceleracin de la proliferacin. Estudios tanto en cultivos celulares como en animales muestran que existe una cooperacin oncognica entre c-myc y Ha-ras activado, lo que indica que ninguno de los oncogenes es totalmente oncognico y que afectan distintos aspectos del control de la proliferacin celular. Adems de estar activado en tumores, c-Myc es un componente esencial de los mecanismos de sealizacin que median la transformacin por distintas oncoprotenas, como bcr-abl, el receptor de CSF-1 y Ras. Se han detectado numerosas mutaciones puntuales en el dominio de activacin transcripcional de c-myc en la zona implicada en las translocaciones en linfomas de Burkitt y otros linfomas relacionados con el SIDA, comparables con las mutaciones encontradas en el oncogn v-myc. Aunque estas mutaciones pueden afectar la actividad transcripcional de c-myc, son mucho menos importantes que la expresin alterada de c-myc que provocan las alteraciones genticas descritas. De modo que, a diferencia de lo que ocurre con otros oncogenes, es la inapropiada regulacin de la expresin de la protena myc, ms que mutaciones en la misma, lo que contribuye a la tumorignesis. El nivel de expresin de c-myc se encuentra cuidadosamente regulado: su nivel de expresin refleja el estado de proliferacin de la clula. Dicha expresin se induce rpidamente a nivel transcripcional tras la estimulacin con factores de crecimiento y es casi inexistente en las clulas
quiescentes. Durante la diferenciacin, los niveles de expresin de c-myc decrecen, y la bajada forzada de su expresin con oligonucletidos antisentido inhibe la proliferacin e induce la diferenciacin. El producto del proto-oncogn c-myc se localiza en el ncleo donde interacciona con diversas protenas a travs de varios motivos de dimerizacin. c-myc posee varios dominios: un dominio compuesto por aminocidos bsicos y otro denominado de hlicebucle-hlice, implicados en unin a ADN, y otro dominio de cremallera de leucinas por el que interacciona con Max, otro miembro de la familia Myc de protenas reguladoras de la transcripcin. Esta familia incluye tambin a las protenas Mad y Mxi. Los heterodmeros Myc-Max son activadores de la transcripcin y son necesarios para la oncognesis. Tambin se pueden formar dmeros Max-Max, Mad-Max y Mix-Max, pero stos funcionan como represores transcripcionales opuestos a la actividad de los dmeros Myc-Max. Todos estos dmeros interaccionan con la secuencia de ADN conocida como caja E, GAGCTC, a travs de la regin bsica de c-Myc. El nivel de transcripcin de los genes regulados por c-Myc depende, por tanto, de las cantidades relativas de los distintos heterodmeros presentes en la clula, lo que explica los potentes efectos que la sobreexpresin de c-Myc puede ejercer sobre las clulas. c-myc tiene efectos llamativos tanto en la progresin por el ciclo celular, como en apoptosis. La activacin del proto-oncogn c-myc en las clulas da lugar a su reentrada en el ciclo celular en la ausencia de factores de crecimiento, y su expresin en clulas crecidas con bajos niveles de nutrientes puede inducir apoptosis. Los genes regulados por c-Myc implicados en estos efectos y en la transformacin celular no son totalmente conocidos. Sin embargo, diversos estudios indican que c-Myc regula la expresin del factor de transcripcin E2F y de la fosfatasa responsable de la activacin de las ciclinas Cdc, que estn implicados en la regulacin del ciclo celular. As mismo, c-Myc regula la expresin de los genes cad y odc que son componentes necesarios del proceso de sntesis de ADN. As pues, puede concluirse que los potentes efectos de Myc observados sobre la proliferacin se deben a un efecto combinado sobre el crecimiento celular y la divisin celular, en concreto durante la transicin desde G0/G1 a S en el ciclo celular. El oncogn v-myb est presente en dos retrovirus que producen leucemias en aves, el virus de la mieloblastosis aviar, AMV, y el virus E. La expresin de la forma celular normal, el proto-oncogn c-myb, se restringe a clulas hematopoyticas inmaduras proliferativas en el epitelio del colon y en clulas neuroectodrmicas y de neuroblastoma. Sin embargo, se ha observado la expresin de c-myb en un 64% de carcinomas de mama y en algunos carcinomas de ovario. Por otro lado, se ha visto la amplificacin de c-myb en leucemias, carcinomas de colon y melanomas. c-myc codifica un factor de transcripcin que parece regular la expresin de genes relacionados con la proliferacin y diferenciacin de clulas hematopoyticas. La protooncoprotena c-Myb, a travs de un dominio rico en triptfanos, reconoce secuencias de ADN con el motivo (C/T)AAC(G/T)G. No se conoce mucho sobre los genes cuya regulacin est modulada por c-Myb, entre los que se encuentra el propio c-myb, pero, como en el caso de c-myc, su expresin est relacionada con la progresin durante las fases G1 y S del ciclo celular y la bajada en su expresin con la diferenciacin celular. v-myc y diversas formas oncognicas de c-myc mutadas codifican protenas con una elevada actividad transcripcional, ms an la sobreexpresin de c-myb tambin es oncognica. En conclusin, la hiptesis de que los oncogenes nucleares juegan un papel central en
los acontecimientos implicados en la proliferacin celular concuerda con el hecho de que sus formas celulares normales se expresan normalmente durante la proliferacin, y tanto su ARN mensajero como sus protenas tienen una vida media muy corta. Por lo tanto, los cambios en la transcripcin de estos genes dan lugar a rpidas fluctuaciones en los niveles de ARNm y protena. La expresin de c-fos, c-jun, c-myc y c-myb es insignificante en clulas quiescentes o durante su diferenciacin terminal. Cuando las clulas son estimuladas con suero o factores de crecimiento para entrar en la fase G1 del ciclo, se produce un incremento transitorio en la expresin de estos genes. Estos protooncogenes son necesarios para la transicin desde el estadio G0 al estadio G1 del ciclo celular y para progresar por fases especficas del ciclo.
SUSCEPTIBILIDAD GENTICA EN CNCER
La mayora de los cnceres son de origen espordico, pero entre el 5 y el 10% de los mismos tienen un claro componente hereditario. Los cnceres hereditarios implican generalmente la predisposicin al desarrollo de tumores concretos. La susceptibilidad se manifiesta en distintos individuos de un grupo familiar a travs de las generaciones, con un patrn compatible con una segregacin mendeliana. El cncer hereditario suele aparecer a una edad ms temprana que el espordico, y el riesgo de desarrollarlo est relacionado con el grado de parentesco. En los individuos predispuestos es frecuente la presencia de tumores de localizacin multifocal, el desarrollo bilateral de la enfermedad y la asociacin de mltiples neoplasias. Las neoplasias que afectan a los miembros de la familia suelen ser de un tipo concreto, pero tambin pueden encontrarse otros tumores o incluso una agrupacin de distintos neoplasias en una misma familia. Por otra parte la incidencia elevada de casos de cncer en una familia no implica necesariamente una base gentica, sino que pueden existir factores ambientales que afecten a dicha familia en concreto. La existencia de un cncer hereditario se demuestra objetivamente identificando la mutacin en la lnea germinal en un gen concreto. Los estudios dirigidos a caracterizar los genes implicados en los sndromes de cncer familiar, han proporcionado numerosas pruebas que apuntan a la inactivacin de los genes supresores tumorales, siendo raras las alteraciones que activen oncogenes en la lnea germinal. Es probable que el carcter dominante de las lesiones en los oncogenes tenga efectos letales e impida subsistir aquellos fetos que hereden una mutacin de este tipo. Una excepcin es el carcinoma medular de tiroides familiar y los tumores endocrinos hereditarios asociados a alteraciones en el oncogen ret. Hay que hacer hincapi en que en el cncer hereditario lo que se transmite a la descendencia no es el cncer propiamente dicho, sino un aumento en el riesgo de desarrollar la enfermedad. Esta susceptibilidad gentica al desarrollo del cncer suele heredarse como un rasgo dominante a nivel del individuo. Sin embargo las alteraciones genticas que confieren esta predisposicin son casi siempre de carcter recesivo, mantenindose el funcionamiento correcto mientras persista una copia normal del gen supresor de tumores. El cncer de mama es una enfermedad compleja y heterognea producida por la interaccin entre factores genticos y no genticos. Es la neoplasia ms comn entre las mujeres del mundo occidental, con una incidencia media aproximada del 10%. Aunque la mayora de los cnceres de mama son espordicos, entre el 5-10% de los mismos son familiares o hereditarios y forman parte del cuadro asociado a distintos sndromes de cncer familiar. El carcinoma de endometrio es la neoplasia ms frecuente que afecta al
tracto genital femenino, mientras que el cncer de ovario ocupa el cuarto lugar como causa de fallecimiento, por detrs de los de mama, recto-colon y pulmn. Las mutaciones hereditarias en los genes BRCA1 y BRCA2 incrementan el riesgo de desarrollar carcinoma de mama y ovario. Otros sndromes genticos relacionados con el desarrollo de tumores ginecolgicos son el sndrome de Li-Fraumeni, asociado con carcinoma de mama y el sndrome de Lynch tipo II, asociado al desarrollo de cncer de endometrio y ovario. En la dcada de los aos veinte, un equipo de patlogos identific una familia con una elevada incidencia de tumores, que representara el prototipo de sndrome de Lynch o cncer colorrectal no polipsico familiar o HNPCC (Hereditary Non-Polyposis Colorectal Cancer). Posteriormente Lynch realiz varios estudios en distintas familias con un historial similar al anterior, y obtuvo un patrn de enfermedad autosmica dominante caracterizada por la predisposicin al desarrollo precoz de cncer de colon proximal no polipsico y de otros tipos de cncer. A partir de estos patrones se definieron dos sndromes: el sndrome de Lynch tipo I o cncer colorrectal familiar de sitio especfico, en aquellas familias que slo desarrollaban cncer colorrectal, y el sndrome de Lynch tipo II o sndrome de cncer familiar en las que tambin aparecan tumores en otros rganos, principalmente en el tracto genital femenino. Actualmente se cree que ambos sndromes son en realidad la misma entidad y se les denomina conjuntamente cncer colorrectal no polipsico familiar o HNPCC. Cuando adems de todos los tumores tpicos del sndrome se desarrollan tambin distintos tipos de tumores dermatolgicos, se denomina al cuadro sndrome de Muir-Torre. El cncer colorrectal es la manifestacin principal del sndrome, aunque tambin hay una predisposicin al desarrollo de tumores de endometrio, ovario, estmago, tracto urinario y pncreas, entre otros. Aparentemente los afectos no tienen predisposicin al cncer de pulmn, mama, prstata, vejiga, mdula sea, laringe o cerebro. El 80% de los pacientes desarrollan cncer de colon y el 30% de las mujeres afectas desarrollan cncer de endometrio. Otras caractersticas clnicas del sndrome son la edad temprana de diagnstico del cncer de colon (entre 40-50 aos respecto a 60-70 aos en la poblacin general), en el 60% de los casos el cncer colorrectal afecta a la regin proximal y en el 25% se producen mltiples tumores primarios La posibilidad de desarrollar tumores metacrnicos despus del tratamiento es del 90% en el caso del cncer de colon y del 75% en el de endometrio. El 3-4% de todos los cnceres colorrectales se encuentran dentro del HNPCC, sin embargo, se desconoce el porcentaje de carcinomas de endometrio y ovario debidos a este sndrome. Predisposicin gentica en cncer de mama En los ltimos aos el descubrimiento de los genes ligados a la predisposicin al cncer de mama ha irrumpido en la prctica oncolgica clnica creando la necesidad de poder establecer unas pautas dirigidas a poder efectuar un consejo gentico no slo de las pacientes sino de las familias. As mismo, el estudio gentico abre una esperanzadora herramienta en aquellos ncleos familiares con una elevada incidencia de cncer de mama al poder identificar a los miembros con mayor riesgo y, por tanto, proceder a una
estrategia ms racional en el screening peridico y diagnstico precoz. Las causas de susceptibilidad son mltiples aunque efectivamente aquellas que cubren una mayor frecuencia son fundamentalmente las mutaciones en los genes BRCA1 y BRCA2 (BReast CAncer). Cada uno de estos genes presentan una estructura genmica de gran tamao, el BRCA1 cuenta con 24 exones (Fig. 1) y el BRCA2 con 27 exones, sin que se puedan sealar unas reas de su secuencia con mayor concentracin de mutaciones. De hecho, la distribucin de mutaciones en estos dos genes se sita a lo largo de toda la secuencia genmica.
Desde un punto de vista clnico es necesario tener conciencia de los patrones especficos de cncer de mama familiar, de los parmetros de vigilancia y seguimiento de las pacientes de riesgo as como de los aspectos psicolgicos de las mujeres que creen presentar un riesgo de cncer de mama sea ste real o percibido. La posibilidad de determinar el riesgo de cncer de mama ofrece una oportunidad de estructurar un adecuado plan de vigilancia y screening de las mujeres con riesgo elevado de cncer de mama. No obstante, el estudio gentico debe precederse de una adecuada evaluacin de riesgo basada en criterios establecidos o en modelos epidemiolgicos. Dado el tamao y la imposibilidad de definir los potenciales hotspot o lugares calientes de mutaciones de estos genes el estudio sistemtico de la poblacin carece de valor coste/efectividad. En esta lnea distintos programas se han desarrollado con objeto de cuantificar este nivel de riesgo de las mujeres con antecedentes familiares atendiendo tambin a las necesidades psicosociales y ofreciendo distintas estrategias de prevencin. Este ha sido el caso del National Surgical Adjuvant Breast Project (NSABP) Breast Cancer Prevention Trial donde la valoracin del riesgo de cncer de mama se efectu mediante el modelo Gail con objeto de estandarizar los criterios de inclusin. As mismo, el reconocimiento de la susceptibilidad hereditaria para el cncer de mama permite y facilita a las mujeres a riesgo enfrentarse y participar en campaas y programas de prevencin. Por otra parte, y desde un punto de vista exclusivamente epidemiolgico esta estructuracin posibilita contar con una base de datos de poblacin, punto de partida para futuros estudios y conocimiento de los patrones de gentica poblacional de nuestro medio. Inicialmente la valoracin del riesgo de cncer de mama y su consecuente consejo gentico se efectuaba en unos pocos centros por equipos multidisciplinarios donde estaban involucrados genetistas, psiclogos, onclogos mdicos, cirujanos y enfermeras.
La disponibilidad del estudio gentico no tiene por qu introducirse en todos los centros pero s el conocimiento para estimar el riesgo asociado a una paciente concreta con objeto de remitir una muestra de sangre perifrica para valoracin molecular a un grupo de centros de referencia a nivel nacional. En esta lnea, hoy en da es necesario para cualquier unidad de oncologa mdica o ginecolgica manejar unos patrones de identificacin de las mujeres con riesgo de desarrollar cncer de mama en funcin a caractersticas de la incidencia de cncer en la familia, edad de diagnstico, grado de parentesco entre las afectadas as como bilateralidad o multicentricidad. As mismo, aunque la valoracin gentica se efecte en un centro de referencia para dicho anlisis, el seguimiento y control evolutivo a largo plazo debe desarrollarse por el centro propio de la paciente y, en este sentido, es importante consensuar algunos aspectos con objeto de ofrecer unas actitudes y recomendaciones comunes y contrastadas por la literatura. Evaluacin de familias con riesgo de cncer de mama Se estima que una de cada 9 mujeres que alcanza los 85 aos en el mundo occidental desarrollar un cncer de mama en algn momento de su vida No obstante, este riesgo constituye una media poblacional en funcin a un grupo de factores sin que se pueda extrapolar una tendencia de central para las individualidades. Los factores que se han considerado en esta estimacin poblacional incluyen historia familiar de cncer, exposicin a determinados carcingenos (incluyendo hormonas exgenas) y la historia reproductiva. Distintos estudios epidemiolgicos han identificado un nmero de importantes factores que podran alterar el riesgo de cncer de mama. Sin embargo, el riesgo estimado obtenido de distintos estudios no es aditivo y, por tanto, no puede ser combinado directamente a efectos de determinar el riesgo de cncer de mama individual por varias razones: en primer lugar, el cncer de mama tiene una etiologa multifactorial, con mtiples factores genticos y ambientales que interaccionan con el desarrollo del proceso neoplsico. En segundo lugar, la importancia relativa de estos factores en el desarrollo de cada tumor individual puede variar. En este sentido, poco se conoce sobre la interrelacin de varios factores de riesgo. Por tanto, desde un punto de vista del individuo afecto de cncer, y este caso de la paciente con cncer de mama, nos centraremos en el riesgo de cncer de mama como una funcin de la historia familiar donde quizs en el futuro podamos aadir su interaccin con otros factores de riesgo (Fig. 2).
La estimacin de la proporcin de cncer de mama que se asocia con la historia familiar vara entre los distintos estudios efectuados. Dos estudios clsicos ofrecieron valores en cierta manera discrepantes: se trata del trabajo de Coldotz donde en su anlisis de 2.389 cnceres de mama prospectivamente identificados entre los individuos reclutados en el Nurses' Health Study, y del trabajo de Slattery y Kerber en un estudio de casos-controles de la base de datos poblacional de Utah as como posteriores anlisis poblacionales mediante tcnicas moleculares en la bsqueda de mujeres portadoras de alteraciones en lnea germinal. La estimacin del porcentaje de casos de cncer de mama en la poblacin asociados con una historia familiar previa se encuentra entre un 17% y un 19% en la cohorte de Utah mientras que en el Nurses' Health Study se cifra en slo un 6%. Esta discrepancia parece que pueda deberse a aspectos metodolgicos ya que en el caso de este ltimo estudio el 6% puede traducir una infravaloracin debido a la carencia de datos de la historia familiar paterna mientras que igualmente el 17-19% sobrestima la frecuencia real al incluir datos de familiares distantes. Todo ello hace pensar que la cifra real puede hallarse en un punto intermedio entre ambas estimaciones (Fig. 3).
El primer punto ms importante en la identificacin de personas con riesgo real cuantificable se centra en una adecuada, exacta y pormenorizada obtencin e interpretacin de la historia familiar. sta debe incluir detalles de procesos neoplsicos desarrollados tanto en parientes paternos como maternos as como la posicin exacta de estos miembros en el rbol familiar considerando tambin familiares no afectos. No hay que olvidar que la distribucin de los miembros afectos y sanos en el rbol genealgico nos va a ofrecer informacin sobre el patrn de herencia (dominante, recesiva,...). Siempre que sea posible, la informacin aportada por la familia sobre la naturaleza de los procesos mrbidos de miembros previos debe ser confirmada recurriendo al informe anatomopatolgicos del centro que trat a aquellos parientes o en su defecto a informes mdicos o registros de certificados de defuncin. La informacin deber ser recogida en un mnimo de tres generaciones siempre que sea posible, as como contrastar los datos referidos con al menos dos miembros con objeto tambin de maximizar la veracidad y la cantidad de los datos obtenidos. Detalles como la edad al diagnstico, edad de los miembros no afectos, histologa del tumor, bilateralidad del proceso, lugares del tumor primario o de las metstasis deben ser recogidos lo ms completamente posible. Es importante igualmente especificar la presencia de sndromes genticos en la familia ya que algunos procesos hereditarios predisponen a los individuos afectos a una variedad de neoplasias, tal es el caso del xeroderma pigmentosum, la anemia de Fanconi, el sndrome de Bloom o la ataxiatelangiectasia con una elevado riesgo de cncer de mama. Con objeto de poder de estratificar el riesgo algunos autores han dividido a las mujeres con historia familiar de cncer de mama en dos grupos: moderado riesgo y alto riesgo. El punto inicial para la clasificacin de las familias como moderado o alto riesgo arranca del anlisis de la historia familiar con objeto de determinar el espectro de tumores presentes y evaluar los potenciales patrones de herencia de la predisposicin a cncer. Las familias con moderado riesgo de cncer de mama se caracterizan por la ausencia de cncer de ovario, una edad ms avanzada de diagnstico y una menor incidencia familiar de tumores, por contra de las familias con un elevado riesgo de cncer de mama que se caracterizan por la presencia de mltiples casos de cncer de mama en parientes muy prximos (al menos tres casos) que parecen seguir un patrn autosmico dominante de herencia. En estas familias de alto riesgo el cncer de mama se diagnostica con frecuencia en una edad temprana (por debajo de los 45 aos) con presencia en ocasiones de cncer de ovario. En esto casos de alto riesgo la causa suele subyacer en una mutacin altamente penetrante con carcter autosmico penetrante en uno de los genes de predisposicin a cncer de mama BRCA1 o BRCA2. Identificacin de familias de riesgo de cncer de mama La situacin ms frecuente con la que se enfrenta la prctica clnica viene dada por un cuadro familiar sin una incidencia muy relevante que oriente sin lugar a dudas hacia un claro cuadro de cncer de mama familiar. En estos casos, la historia familiar revela tpicamente la presencia de uno o dos miembros con cncer de mama (a menudo de aparicin perimenopusica o incluso postmenopusica) y la ausencia de otros tumores distintos al cncer de mama. Esta situacin ofrece un espectro heterogneo tanto a nivel molecular como en el mbito clnico y podran contemplarse cuatro potenciales causas
subyacentes: 1. Una derivada de la combinacin de distintas alteraciones genticas (o epigenticas) combinadas o no con agentes ambientales, cada uno confiriendo un pequeo grado sobreaadido de riesgo. 2. Otro subgrupo podra estar tericamente explicado por la presencia de una mutacin de uno de los genes BRCA1 o BRCA2 con una baja penetrancia, lo cual podra justificar una mayor incidencia de cncer de mama en ese entorno familiar respecto a la poblacin general; no obstante, este planteamiento no concuerda con la constatacin de una elevada penetrancia de las mutaciones acaecidas en los genes BRCA. 3. Algunas familias puede presentar un sndrome de predisposicin hereditaria al cncer de mama pero quizs por tratarse de una familia pequea o no contar con informacin completa o fidedigna no se expone de forma clara y florida un patrn tpico de estos sndromes en toda su extensin. 4. As mismo debemos considerar que el cncer de mama constituye un proceso neoplsico con una amplia y creciente incidencia en la poblacin general lo cual significa que puede acontecer en ms de una ocasin en una familia sin tener ninguna relacin con factores hereditarios. Estas familias con estas caractersticas se etiquetan como ncleos familiares de riesgo moderado y la estimacin de riesgo se efecta usando un modelo derivado de estudios epidemiolgicos. En estos casos, este modelo de riesgo epidemiolgico permite establecer una prediccin basada en anlisis de estudios poblacionales . Valoracin de riesgo en familias con susceptibilidad a cncer de mama Algunos autores han revisado recientemente los modelos ms representativos comparndolos y evaluando el nivel de prediccin. Son modelos basados en diseos que utilizan distintos factores de riesgo, lo cual se traduce en estimaciones de riesgo para un individuo dado que difieren mnimamente. Estos datos de prediccin ofrecen una gua til a efectos de ofrecer posteriormente un adecuado consejo gentico a los miembros a riesgo de las familias. Las medidas ms frecuentes para la evaluacin del riesgo se dirigen a la estimacin del riesgo relativo o el riesgo acumulativo. El primero se define como la tasa de enfermedad en un grupo expuesto a un factor de riesgo comparado a un segundo grupo no expuesto a dicho factor. Este riesgo relativo es muy til para la valoracin de la magnitud del efecto de un factor de riesgo dado. No obstante, el uso del riesgo relativo puede no ser adecuado cuando se evala una lnea base de riesgo a nivel individual y sta es multiplicada por el valor del riesgo relativo del factor considerado. Por eso mismo, esta aproximacin es ms vlida en la estimacin poblacional de riesgo considerndose ms acertada la evaluacin basada en el riesgo acumulado que aporta un dato estadstico que traduce de forma ms asequible para el conjunto clnico sobre todo cuando se estratifican grupos de edades. En este sentido, esta prediccin basada en riesgos acumulados posibilita un enfoque distinto al poderse dirigir el riesgo a un tiempo determinado o a una extensin de vida determinada. Uno de los modelos ms utilizados deriva del estudio "Cancer and Steroid Hormone
Study (CASH)", analizado por Claus. Estos datos poblacionales conforman una base para la prediccin de riesgo en mujeres con historia previa de cncer de mama lo cual puede permitir la construccin de tablas detalladas para el clculo del riesgo acumulado de cncer de mama en una determinada edad basado en la edad de diagnstico de los miembros de primer y segundo grado de parentesco. Cuando se usan estas tablas del modelo de Claus, los individuos considerados deben encontrarse en la misma lnea (materna o paterna) pero no mezclados. Una ventaja de esta aproximacin es el hecho de que maneja riesgos acumulados ms que riesgos relativos, incorporando la edad de diagnstico de los parientes afectos en el clculo del modelo. Sin embargo, este modelo puede infraestimar significativamente el riesgo de desarrollo de cncer de mama en mujeres portadoras de mutaciones de BRCA1 o BRCA2 en ncleos familiares pequeos, y sobrestimarlo en individuos que no hayan heredado una mutacin relacionada con enfermedad donde los casos de cncer de mama sean incidentales sin ninguna relacin causal entre ellos. El otro gran modelo considerado se refiere al de Gail que calcula el riesgo de desarrollar cncer de mama mediante el uso de una frmula que contempla las variables: edad de la mujer en su menarquia, edad del primer parto, nmero de familiares de primer grado con cncer de mama, nmero de biopsias previas de mama en la mujer considerada ante lesiones de dudosa naturaleza y edad de la misma. Este modelo fue estimado a partir de los datos del estudio "Breast Cancer Detection Demonstration Project" (BCDDP). El modelo predice un riesgo acumulativo desde los 20 aos hasta los 80 corrigiendo as mismo por otras causas de mortalidad. Ha sido ampliamente usado con objeto de calcular el riesgo de desarrollo de cncer de mama en las mujeres del ensayo de quimioprevencin (NSABP Breast Cancer Chemoprevention Trial). No obstante, los estudios de validacin han mostrado que slo predice el riesgo de forma eficiente en mujeres caucasianas sometidas a screening mamogrfico que es precisamente el estrato poblacional del cual procede este modelo predictivo. En general, para la mayora de las mujeres atendidas en un servicio clnico, las tablas de Claus, diseadas para predecir el riesgo en mujeres con una historia familiar de cncer de mama, puede acoplarse mejor a las necesidades del da a da. Hay que considerar que obviamente una proporcin de mujeres de la poblacin originaria sobre la que se desarroll este modelo son portadoras de mutaciones en uno de los genes de susceptibilidad; la inclusin de estas mujeres de una forma mayoritaria podra haber conducido a una sobrestimacin del riesgo real si los factores y variables del modelo no han sido adecuadamente equilibrados y corregidos con estudios posteriores. Sin embargo, este hecho sobre el posible ajuste de los valores proporcionales no resta entidad a los resultados obtenidos. De alguna forma, los modelos de prediccin aqu presentados as como otros disponibles en la literatura pueden manifestar una mayor eficiencia en su capacidad de inferencia en tanto en cuanto la poblacin a la que se aplique su clculo ms se aproxime a las caractersticas de la poblacin sobre la que se ha desarrollado el sistema. De esta forma, sobre una poblacin de mujeres sanas sometidas a controles peridicos mamogrficos sin un especial nfasis en su carga familiar de cncer de mama puede constituir un mejor modelo el desarrollado por Gail que cualquier otro. Este modelo cuenta actualmente con programas de software diseados para la cuantificacin numrica as como para la representacin grfica del riesgo asumido por un individuo.
http://www.cfnavarra.es/salud/Anales/textos/vol24/suple1/suple4a.html
Vous aimerez peut-être aussi
- 3 (02) - El Ser Humano, Ser CreativoDocument13 pages3 (02) - El Ser Humano, Ser Creativo.......Pas encore d'évaluation
- Actividad 8 Anatomia y FisiologiaDocument9 pagesActividad 8 Anatomia y FisiologiaRosalia Mercedes Castillo Canario100% (1)
- Bioseguridad Expo I InyectoterapiaDocument16 pagesBioseguridad Expo I InyectoterapiaxxmalenaxxPas encore d'évaluation
- Ejemplo Planeador ErikaDocument22 pagesEjemplo Planeador Erikayessica yadiraPas encore d'évaluation
- Receptores ColinérgicosDocument3 pagesReceptores ColinérgicosLiz chiclote mantillaPas encore d'évaluation
- VirusDocument9 pagesVirusEdinson sanchezPas encore d'évaluation
- Tarea Axon GiganteDocument9 pagesTarea Axon Giganteitzel Guadalupe PereydaPas encore d'évaluation
- Nomenclatura de Mutaciones Génicas y CromosómicasDocument5 pagesNomenclatura de Mutaciones Génicas y CromosómicasCloudPas encore d'évaluation
- Laboratorio ManualDocument30 pagesLaboratorio ManualOMAR FERNANDO HERNANDEZ CHAVEZPas encore d'évaluation
- Mosaicismo y Cromosoma XDocument22 pagesMosaicismo y Cromosoma XtberniPas encore d'évaluation
- Teorías Sobre El Origen de La Vida 2019Document23 pagesTeorías Sobre El Origen de La Vida 2019MariaPas encore d'évaluation
- Capitulo 1Document4 pagesCapitulo 1Alazka calafatPas encore d'évaluation
- La Biodiversidad Como Diversidad Genética y de EspeciesDocument22 pagesLa Biodiversidad Como Diversidad Genética y de EspeciesMendez JosePas encore d'évaluation
- Guia Diatomeas Rios El Salvador (2.3MB) PDFDocument48 pagesGuia Diatomeas Rios El Salvador (2.3MB) PDFOscar AyalaPas encore d'évaluation
- Las Proteínas Transportadoras Determinan La Permeabilidad Selectiva de La Membrana CelularDocument3 pagesLas Proteínas Transportadoras Determinan La Permeabilidad Selectiva de La Membrana CelularWen OlivaPas encore d'évaluation
- Unidad 2 2do BguDocument23 pagesUnidad 2 2do BguJamileth MuñozPas encore d'évaluation
- Exposiciones 3-2. Segundo CicloDocument4 pagesExposiciones 3-2. Segundo CicloNAHOMY TERANPas encore d'évaluation
- Anatomia Cpu Unprg Sistema Digestivo Cap-Ix PDFDocument10 pagesAnatomia Cpu Unprg Sistema Digestivo Cap-Ix PDFMiguel Ángel Zúñiga50% (2)
- Potencial Biotico Hippodamia ConvergensDocument10 pagesPotencial Biotico Hippodamia ConvergensMelissa Mendoza EspinosaPas encore d'évaluation
- Etapa 2 - Taller Genetica Mendeliana GRUPO 30162A-954Document21 pagesEtapa 2 - Taller Genetica Mendeliana GRUPO 30162A-954Alexandra FlorezPas encore d'évaluation
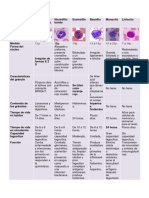
- Pérez Romo Cynthia Paola 5CMLC - Cuadro Comparativo de LeucocitosDocument2 pagesPérez Romo Cynthia Paola 5CMLC - Cuadro Comparativo de LeucocitosYvanna Ferreira100% (4)
- Cien 9 b2 p3 Est Web PDFDocument10 pagesCien 9 b2 p3 Est Web PDFshinePas encore d'évaluation
- Informe de AlgasDocument17 pagesInforme de AlgasLeidy Cely CastilloPas encore d'évaluation
- y 2. Inflamación y Reparación TisularDocument19 pagesy 2. Inflamación y Reparación TisularCarlomauro AvelloPas encore d'évaluation
- Examen de Becas 5toDocument1 pageExamen de Becas 5tojuan carlos lluncor fallaPas encore d'évaluation
- PATO GENERAL PRACTICA 10 - DIGESTIVO-modDocument20 pagesPATO GENERAL PRACTICA 10 - DIGESTIVO-modyanettPas encore d'évaluation
- Virus y Super BacteriasDocument13 pagesVirus y Super BacteriasWilliam H. BoneyPas encore d'évaluation
- Fotosíntesis y Fotorrespiración EnsayoDocument12 pagesFotosíntesis y Fotorrespiración Ensayoclaudia leonor ,acias ortegaPas encore d'évaluation
- 2 Botrytis Cinerea 2013Document5 pages2 Botrytis Cinerea 2013paul escribaPas encore d'évaluation
- Herencia Intermedia y CodominanciaDocument2 pagesHerencia Intermedia y CodominanciaCarlos JulioPas encore d'évaluation