Académique Documents
Professionnel Documents
Culture Documents
Prática 1 Lise de Células de Levedura
Transféré par
Edgard FreitasCopyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Prática 1 Lise de Células de Levedura
Transféré par
Edgard FreitasDroits d'auteur :
Formats disponibles
Prtica 1 Lise de Clulas de Levedura Objetivos Romper as clulas de Saccharomyces cerevisiae.
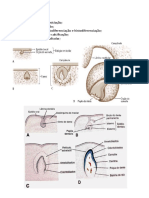
Reagentes Materiais Aparelhagens gua destilada banho de gelo centrfuga clulas de levedura (fase log tardia) prolas de vidro 0,5 m estufa etanol pipetadores freezer fluoreto de fenilmetilsulfonila (PMSF) 100 mM em etanol pipetas vrtice provetas hipoclorito de sdio 20 g/L (gua sanitria) suporte para tubos tubos de centrfuga tampo fosfato 100 mM pH 7,0 com EDTA 5 mM (tampo de lise) tubos de ensaio tubos Falcon Procedimento A Fracionamento celular OBSERVAO: MANTER TUBOS DE ENSAIO EM BANHO DE GELO 1. Em um tubo de centrfuga com tampa colocar aproximadamente 1 g (peso mido) de clulas de leveduras crescidas at a fase logartmica tardia. 2. Adicionar 4 mL de tampo de lise. 3. Ressuspender as clulas usando um vrtice. 4. Adicionar 40 L de PMSF (100 mM) em etanol. 5. Homogeneizar em vrtice. 6. Adicionar suspenso 8 mL de prolas de vidro lavadas e secas. 7. Agitar ininterruptamente em vrtice durante 1 min (processo de lise). 8. Resfriar em banho de gelo por 1 min 9. Repetir as operaes 7 e 8 por mais 4 vezes. 10. Centrifugar a suspenso de clulas + prolas de vidro a 850x g por 2 min. 1. Remover cuidadosamente o sobrenadante evitar coletar o material precipitado passandoo para um tubo Falcon limpo e identificado como LISADO. 12. Manter o tubo LISADO em banho de gelo. 13. Ressuspender o precipitado + prolas de vidro em 4 mL de tampo de lise. 14. Adicionar 40 L de PMSF (100mM) em etanol. 15. Homogeneizar em vrtice. 16. Repetir as etapas 10 a 15 por mais 2 vezes, reunindo os sobrenadantes no mesmo tubo LISADO. 17. Usando uma proveta, determinar o volume do LISADO. 18. Dividir o lisado em 3 alquotas de igual volume e transferi-las para tubos plsticos 19. Identificar os tubos com o nmero do grupo. 20. Armazenar em freezer a 20oC. Procedimento B Lavagem das prolas de vidro (Executado por monitores ou tcnica) 1. Transferir as prolas de vidro para um erlenmeyer. 2. Adicionar hipoclorito de sdio no erlenmeyer. 3. Agitar algumas vezes durante 15 min. 4. Descartar cuidadosamente o hipoclorito de sdio 5. Repetir a lavagem com hipoclorito de sdio. 6. Adicionar gua no erlenmeyer 7. Lavar as prolas. 8. Descartar cuidadosamente a gua. 9. Repetir as etapas 6 a 8 por mais 5 vezes. 10. Adicionar etanol no erlenmeyer. 1. Colocar o erlenmeyer numa estufa. 12. Aguardar a secagem das prolas. 1 g de Saccharomyces cerevisiae (PESO MIDO) 4 mL de tampo de lise 40 L de PMSF Suspenso
8 mL de prolas de vidro Agitao em vrtice Centrifugao 850X g por 2 min Precipitado Sobrenadante Suspenso Centrifugao 850X g por 2 min Precipitado Sobrenadante Tubo LISADO 4 mL de tampo de lise 40 L de PMSF REPETIR 2 X Prtica 2 Dosagem de Protena Objetivos Dosar colorimetricamente protenas no lisado de Saccharomyces cerevisiae. Reagentes Materiais Aparelhagens gua destilada papel de filtro espectrofotmetro albumina 0,2 g/L cubetas para leitura vrtice lisado de leveduras (P1) pipetadores reagente de Bradford pipetas cido fosfrico 85% ponteiras Coomassie Blue G suportes para tubos de ensaio metanol tubos de ensaio Procedimento A Curva-padro de protena 1. Adicionar em cada tubo os volumes de albumina e gua estipulados na Tabela 1. 2. Adicionar o reagente de Bradford. 3. Homogeneizar em vrtice. 4. Aguardar 5 minutos com os tubos em temperatura ambiente 5. Usar o branco para calibrar (zerar) o espectrofotmetro. 6. Ler as absorbncias a 595 nm. 7. Completar a Tabela 2. 8. Construir a curva-padro para deteco de protenas com reagente de Bradford. Tabela 1 tubos albumina 0,2 g/L (L) gua (L) reagente de Bradford (mL) branco 0 100 1,0 1 10 90 1,0 2 20 80 1,0 3 30 70 1,0 4 40 60 1,0 5 50 50 1,0 6 60 40 1,0 7 70 30 1,0 8 80 20 1,0 Tabela 2 tubos massa de protena (mg) A595 1
Procedimento B Dosagem de protenas no lisado de Saccharomyces cerevisiae OBSERVAO: para esse procedimento necessrio que o lisado seja diludo. Para isso segue o procedimento para diluio. Diluio 100X: 1. Transferir 0,1 mL do lisado para um tubo de ensaio grande identificado como L100X. 2. Adicionar 9,9 mL de gua destilada. 3. Homogeneizar em vrtice. 1. Adicionar em cada tubo os volumes de gua e amostras do lisado (devidamente diludo) estipulados na Tabela 3. 2. Adicionar o reagente de Bradford. 3. Homogeneizar em vrtice. 4. Aguardar 5 minutos com os tubos em temperatura ambiente. 5. Usar o branco para calibrar (zerar) o espectrofotmetro. 6. Ler as absorbncias a 595 nm. 7. Completar a Tabela 4. OBSERVAO: Caso a absorbncia das amostras experimentais esteja fora dos limites das absorbncias obtidas na curva-padro, discuta com o professor ou monitor um novo valor de diluio. Tabela 3 tubos L100X (L) (L) reagente de Bradford (mL) branco - 100 1,0 A1 100 - 1,0 A2 50 50 1,0 A3 30 70 1,0 A4 20 80 1,0 tubos A595 A1 A2 A3 A4 Prtica 3 Determinao da Atividade Enzimtica Objetivo Determinar a atividade da -glicosidase no lisado de Saccharomyces cerevisiae Reagentes Materiais Aparelhagens gua destilada banho de gelo banho a 30oC lisado de leveduras cubetas para leitura espectrofotmetro p-nitrofenil--glicosdeo (NPGlc) 4 mM em tampo fosfato 100 mM pH 7,0 pipetadores vrtice pipetas tampo carbonato-bicarbonato 250 mM pH 1,0 ponteiras suportes para tubos de ensaio tubos de ensaio Procedimento A Diluio do lisado de Saccharomyces cerevisiae OBSERVAO: MANTER TUBOS DE ENSAIO EM BANHO DE GELO Abaixo segue o procedimento sugerido para a diluio da preparao do lisado de Saccharomyces cerevisiae. 1. Transferir 0,2 mL do lisado de Saccharomyces cerevisiae para um tubo identificado como L10X. 2. Adicionar 1,8 mL de gua destilada gelada. 3. Homogeneizar suavemente 4. Transferir 0,4 mL de L10X para um novo tubo identificado como L50X. 5. Adicionar 1,6 mL de gua destilada gelada. 6. Homogeneizar suavemente 7. Transferir 0,2 mL de L50X para um novo tubo
identificado como L500X. 8. Adicionar 1,8 mL de gua destilada gelada. 9. Homogeneizar suavemente 10. Manter todos os tubos no gelo Procedimento B - Determinao da atividade da -glicosidase Este procedimento deve ser feito para cada uma das diferentes diluies do lisado que foram preparadas. Todos estes ensaios podem ser montados simultaneamente, iniciando o procedimento sempre pela adio do substrato. Somente quando todos os tubos j tiverem recebido o substrato dever ser iniciada a adio das diferentes diluies de lisado. 1. Preparar os tubos em banho de gelo. 2. Adicionar em cada tubo os volumes de NPGlc estipulados na Tabela 1 e 2. 3. Adicionar em cada tubo o lisado devidamente diludo. 4. Transferir todos os tubos ao mesmo tempo para o banho a 30oC. 5. Incubar os tubos pelos intervalos de tempos indicados na Tabela 1. 6. Ao remover cada tubo, interromper a reao enzimtica adicionando 2 mL de tampo carbonatobicarbonato pH 1,0. 7. Agitar manualmente 8. Deixar os tubos em temperatura ambiente. 9. Usar a gua para calibrar (zerar) o espectrofotmetro. 10. Uma vez que todos os tubos tenham sido retirados, ler as absorbncias a 420 nm. 1. Completar a Tabela 3. Tabela 1 tubos NPGlc 4 mM (mL) lisado diludo (mL) Tempo de incubao a 30C (min) 1 0,2 0,2 5 2 0,2 0,2 10 3 0,2 0,2 15 4 0,2 0,2 20 Branco de Enzima --- 0,2 20 Tabela 2 Basta preparar este tubo apenas uma nica vez, mesmo quando se trabalha com diferentes diluies do lisado tubo NPGlc 4 mM (mL) lisado diludo (mL) Tempo de incubao a 30C (min) Branco de Substrato 0,2 --- 20 Tabela 3 L10x L50X L500x
1 2 3 4 Branco de Enzima Branco de Substrato tubos A420 A420 A420 Curva Padro de p-nitrofenolato
A b s o r b n ci a a 4
Tratamento de Dados e Anlise dos Resultados PRTICA 1 - FRACIONAMENTO CELULAR PRTICA 2 - DOSAGEM DE PROTENA PRTICA 3 - DETERMINAO DA ATIVIDADE ENZIMTICA (Relatrio 1) INSTRUES: 1. Completar as tabelas com os resultados experimentais das prticas 2 e 3. 2. Construir a curva padro para quantificao de protenas com o reagente de Bradford. 3. Calcular a concentrao de protenas (mg/mL) no lisado de Saccharomyces cerevisiae. 4. Construir o grfico do ensaio de atividade da -glicosidase (nmols de produto x tempo) para cada diluio de lisado utilizada 5. Calcular a Concentrao de Atividade Enzimtica (U/mL) e a Atividade especfica (U/mg) do lisado de Saccharomyces cerevisiae. tubos massa de protena Abs595 (mg) ---
1 2 3 4 5 6 7 8 Equao de reta: y = ax + b coeficiente angular = a Intercepto no eixo y = b Massa de protena calculdada utilizando a curvapadro Volume da amostra concentrao Diluio prvia concentrao do lisado original (sem diluio) (mg) (mL) (mg/mL) (x) (mg/mL) A1 0,10 A2 0,05 A3 0,03 A4 0,02 TABELA PARA O CLCULO DA ATIVIDADE ENZIMTICA L10x L50X L500x tubos Tempo A420 produto A420 produto A420 produto (min) (nmol) (nmol) (nmol) 15 2 10 3 15 Prtica 4 Caracterizao da enzima pH timo Objetivo Determinar o efeito do pH na atividade cataltica da -glicosidase. Reagentes Materiais Aparelhagens lisado de levedura banho de gelo banho 30oC p-nitrofenil-glicosdeo (NPGlc) 8 mM em gua pipetadores espectrofotmetro pipetas tampo carbonatobicarbonato 250 mM pH 1,0 ponteiras suporte para tubos tampo fosfato 200 mM pH 7,0 tubos de ensaio tampo borato 200 mM pH 8,0 tampo borato 200 mM pH 9,0 tampo citrato 200 mM pH 4,0 tampo citrato 200 mM pH 5,0 tampo citrato 200 mM pH 6,0 Procedimento A Diluio do lisado de Saccharomyces cerevisiae
Deve ser dada preferncia para a diluio que gerou a melhor medida de atividade enzimtica na prtica anterior. Caso no seja possvel utiliz-la, abaixo segue o procedimento sugerido para a diluio da preparao do lisado de Saccharomyces cerevisiae. 1. Transferir 0,2 mL do lisado de Saccharomyces cerevisiae para um tubo identificado com L10X. 12. Adicionar 1,8 mL de gua destilada gelada. 13. Homogeneizar suavemente 14. Transferir 0,1 mL de L10X para um novo tubo identificado com L100X. 15. Adicionar 4,9 mL de gua destilada gelada. 16. Homogeneizar suavemente. 17. Manter no gelo Procedimento B Ensaio da atividade enzimtica OBSERVAO: MANTER TUBOS DE ENSAIO EM BANHO DE GELO 1. Realizar os ensaios de atividade enzimtica sobre p-nitrofenil--glicosdeo (NPGlc) em 6 diferentes valores de pH. 2. Preparar em banho de gelo, para cada pH, um conjunto de tubos para os ensaios de atividade de acordo com a Tabela 1. 3. Misturar cuidadosamente. 4. Adicionar o lisado (devidamente diludo) de Saccharomyces cerevisiae. 5. Agitar manualmente com cuidado. 6. Transferir todos os tubos do gelo ao mesmo tempo para um banho a 30oC. 7. Incubar os tubos pelos intervalos de tempos indicados na Tabela 1. 8. Ao retirar cada tubo do banho, interromper a reao enzimtica pela adio de 2 mL de tampo carbonato-bicarbonato. 9. Agitar manualmente 10. Deixar os tubos em temperatura ambiente. 1. Usar gua para calibrar (zerar) o espectrofotmetro. 12. Uma vez que todos os tubos tenham sido retirados, ler as absorbncias a 420 nm. 13. Completar as Tabelas 2, 3 e 4. 14. Determinar graficamente o pH timo da glicosidase pH = _ Tabela 1 tubos NPGlc 8 mM (mL) tampo _ pH _ (mL) lisado diludo (mL) tempo (min) 1 0,1 0,1 0,2 5 2 0,1 0,1 0,2 10 3 0,1 0,1 0,2 15 4 0,1 0,1 0,2 20 Tabela 2 pH = 4,0 pH = 5,0 pH = 6,0 tubos A420 tubos A420 tubos A420 1 1 1 Tabela 3 pH = 7,0 pH = 8,0 pH = 9,0 tubos A420 tubos A420 tubos A420 1 1 1 Tratamento de Dados e Anlise dos Resultados Prtica 4 - Caracterizao da enzima pH timo (Relatrio 2) 1. Construir os grficos para determinao da concentrao de atividade (U/ml) da - glicosidase nos diferentes valores de pH. 2. Construir a curva de pH timo (atividade relativa (%) versus pH). A atividade relativa a porcentagem de atividade enzimtica em cada pH medida em relao a maior atividade observada. 3. Determinar o valor de pH timo.
TABELA 4 - CLCULO DO VALOR DE PH TIMO Valor de pH Atividade Enzimtica presente no ensaio Atividade Enzimtica Relativa (U/ml) (%)
Prtica 5 Purificao de protenas cromatografia de troca inica Objetivo Isolar a alfa-glicosidase utilizando resina de troca inica. Procedimento A Hidratao da DEAE-Sephadex (Executado por monitores ou tcnica) 1. Pesar 0,5 g de DEAE-Sephadex em um bquer. 2. Adicionar 100 mL de tampo fosfato 10 mM pH 6,8. 3. Misturar bem utilizando um basto de vidro. 4. Decantar de um dia para o outro. Procedimento B Montagem da coluna de troca inica (Executado por monitores ou tcnica) Montagem da coluna 1. Utilizar o barril de uma seringa (~ 20 mL) como suporte da resina. 2. Prender a seringa em um suporte. 3. Colocar um pouco de l de vidro no seu interior. 4. Compactar a l de vidro na base utilizando um basto de vidro. 5. Lavar a coluna com gua destilada para retirar fragmentos de l de vidro. 6. Adaptar uma mangueira de aproximadamente 6 cm na sada da pipeta. 7. Fechar a mangueira com uma presilha. Processo de empacotamento 8. Fechar a presilha. 9. Homogeneizar com um basto de vidro a suspenso contendo a resina (Procedimento A). 10. Adicionar a suspenso at a marca de 1,0 mL. 1. Deixar decantar. 12. Repetir essa operao at a resina sedimentada ocupar o interior da seringa at 1,0 mL 13. Com a resina empacotada, lav-la com 20 mL de tampo fosfato 10 mM sem NaCl. 14. Aps a lavagem, fechar a presilha. 15. Deixar 3 m de tampo acima do topo da resina. NUNCA DEIXAR A RESINA SECAR. Procedimento C Cromatografia de troca inica Preparao da amostra 1. Descongelar o lisado, transferir uma alquota de 1,0 mL para um tubo tipo eppendorf e centrifugar a 10.000xg por 13s. Coletar o sobrenadante e usar nas etapas abaixo. 2. Parte de material (0,4 mL) ser usada na cromatografia abaixo, enquanto que o restante (0,6 mL) dever ser guardado (congelado) para a prxima aula prtica.
Cromatografia 3. Diluir 0,4 mL do sobrenadante do lisado (ver etapa 1) adicionando 0,6 mL de tampo fosfato 10 mM sem NaCl. muito importante que apenas o sobrenadante do lisado seja usado para evitar entupimento da coluna. 4. Verificar se a presilha est fechada. 5. Utilizar uma pipeta para transferir toda a amostra (devidamente diluda) homogeneamente para a coluna. 6. Colocar o tubo 1 na sada da coluna e abrir a presilha. 7. Deixar a amostra escoar pela coluna at cerca de 3 m acima do topo da resina. 8. Fechar a presilha e transferir o tubo 1 para o gelo. Eluio das protenas no retidas pela coluna 9. Adicionar cuidadosamente tampo fosfato sem NaCl (2 mL). 10. Colocar o tubo 2 na sada da coluna e abrir a presilha permitindo que o tampo flua pela resina. 1. Coletar 1 mL em cada tubo de ensaio. 12. Trocar o tubo de ensaio e sempre adicionar mais 1 mL de tampo. 13. Fechar a presilha ao final da coleta do tubo 8. 14. Adicionar cuidadosamente mais 1,0 mL de tampo. Assim, acima da resina dever haver 2,0 mL de tampo. 15. Coletar mais dois tubos, sem adicionar tampo. 16. Ao final da coleta do tubo 10, o tampo dever estar cerca de 3mm acima do topo da resina. Eluio das protenas retidas pela coluna 17. Adicionar cuidadosamente tampo fosfato com NaCl (2,0 mL). 18. Abrir a presilha e permitir que o tampo flua pela resina. 19. Coletar 1,0 mL (mililitro) em cada tubo de ensaio. 20. Trocar o tubo de ensaio e sempre adicionar mais 1 mL de tampo 21. Fechar a presilha ao final da coleta do tubo 18. 2. Adicionar 1,0 mL de tampo. Assim, acima da resina dever haver 2,0 mL de tampo. 23. Coletar mais dois tubos, sem adicionar tampo. 24. Fechar a presilha ao final da coleta do tubo 20. No deixar a coluna secar. Procedimento D Identificao das fraes que contm a -glicosidase 1. Preparar um conjunto de tubos numerados de 1 a 20. Adicionar em cada tubo 0,2 mL de NPGlc Transferir os tubos em banho de gelo. 2. Adicionar em cada um destes tubos 0,2 mL das fraes coletadas durante a cromatografia. 3. Transferir todos os tubos ao mesmo tempo para um banho de 30oC. 4. Incubar os tubos por 10 min. 5. Ao remover os tubos, adicionar em cada um 2 mL de tampo carbonato-bicarbonato pH 1,0. 6. Agitar manualmente 7. Deixar os tubos em temperatura ambiente. 8. Usar gua para calibrar (zerar) o espectrofotmetro. 9. Ler as absorbncias a 420 nm 10. Completar a Tabela 4. 1. Construir um grfico Absorbncia versus nmeros dos tubos. 12. Uma vez identificados os tubos que contm atividade enzimtica, reunir as fraes (eludas na cromatografia) correspondentes em um tubo Falcon identificado como MATERIAL DEAE Nome do grupo. Tabela 4 tubos A420 tubos A420 1 1 Procedimento E Determinao das atividades enzimticas
Diluio do sobrenadante do lisado de Saccharomyces cerevisiae MANTER OS TUBOS DE ENSAIO EM BANHO DE GELO Deve ser utilizado o procedimento de diluio que proporcionou o melhor resultado na prtica 3. Determinao da atividade da -glicosidase no sobrenadante do lisado de S. cerevisiae MANTER OS TUBOS DE ENSAIO EM BANHO DE GELO Todos os tubos deste ensaio podem ser montados simultaneamente, iniciando o procedimento sempre pela adio do substrato. Somente quando todos os tubos j tiverem recebido o substrato dever ser iniciada a adio do sobrenadante do lisado previamente diludo. 12. Preparar os tubos em banho de gelo. 13. Adicionar em cada tubo os volumes de NPGlc estipulados na Tabela 1 e 2. 14. Adicionar em cada tubo o sobrenadante do lisado devidamente diludo. 15. Transferir todos os tubos ao mesmo tempo para o banho a 30oC. 16. Incubar os tubos pelos intervalos de tempos indicados na Tabela 1. 17. Ao remover cada tubo, interromper a reao enzimtica adicionando 2 mL de tampo carbonatobicarbonato pH 1,0. 18. Agitar manualmente 19. Deixar os tubos em temperatura ambiente. 20. Usar a gua para calibrar (zerar) o espectrofotmetro. 21. Uma vez que todos os tubos tenham sido retirados, ler as absorbncias a 420 nm. 2. Completar a Tabela 3. Tabela 1 tubos NPGlc 4 mM (mL) Sobrenadante do lisado diludo (mL) Tempo de incubao a 30C (min) 1 0,2 0,2 5 2 0,2 0,2 10 3 0,2 0,2 15 4 0,2 0,2 20 BE --- 0,2 20 Tabela 2 tubo NPGlc 4 mM (mL) gua destilada (mL) Tempo de incubao a 30C (min) Branco de Substrato 0,2 0,2 20 Tabela 3 tubos A420 1 2 3 4 BE
23 Com os dados obtidos determinar a concentrao de atividade enzimtica de -glicosidase (U/mL) presente no sobrenadante do lisado. Determinao da atividade da -glicosidase no material DEAE 1. Dilua 10x o MATERIAL DEAE seguindo o procedimento sugerido abaixo Transferir 0,2 mL do MATERIAL DEAE para um tubo identificado com DEAE-10X. Adicionar 1,8 mL de gua destilada. Homogeneizar suavemente Manter no gelo 2. Adicionar em cada tubo de ensaio os volumes de NPGlc e MATERIAL DEAE (diludo 10x) estipulados na Tabela 5. Preparar os tubos em banho de gelo. 3. Transferir todos os tubos ao mesmo tempo para um banho a 30oC. 4. Incubar os tubos pelos intervalos de tempos indicados na Tabela 5. 5. Ao remover cada tubo, interromper a reao enzimtica adicionando 2 mL de tampo carbonatobicarbonato pH 1,0. 6. Deixar os tubos em temperatura ambiente. 7. Usar gua para calibrar (zerar) o espectrofotmetro. 8. Uma vez que todos os quatro tubos tenham sido retirados, ler as absorbncias a 420 nm. 9. Completar a Tabela 6. 10. Calcular a atividade da glicosidade no Material DEAE. Tabela 5 tubos NPGlc 4 mM (mL) material DEAE (diludo 10x) (mL) tempo (min) 1 0,2 0,2 5 2 0,2 0,2 10 3 0,2 0,2 15 4 0,2 0,2 20 Tabela 6 tubos A420 nmols de produto Tempo (min) 1 2 3 4 Procedimento F Dosagem de protenas Ateno O material DEAE usado neste procedimento no deve ser diludo. 8. Adicionar em cada tubo os volumes de gua e material DEAE estipulados na Tabela 7. 9. Adicionar o reagente de Bradford. 10. Homogeneizar em vrtice 16 1. Aguardar 5 minutos 12. Usar o branco para calibrar (zerar) o espectrofotmetro. 13. Ler as absorbncias a 595 nm. 14. Completar a Tabela 8 15. Tabela 7 tubos material DEAE (mL) gua (mL) reagente de Bradford
(mL) branco - 0,1 1,0 1 0,1 - 1,0 2 0,1 - 1,0 3 0,1 - 1,0 Tabela 8 tubos A595 Massa de protena (mg) Volume da amostra (mL) Concentrao de protena (mg/mL) 1 2 3 Procedimento G- Dosagem de protenas do lisado (repetio da prtica 2). 15. Diluir 20 X o lisado obtido aps centrifugao. Transferir 0,1 ml do lisado para um tubo e adicionar 1,9 ml de gua destilada. 16. Adicionar em cada tubo os volumes de gua e lisado diludo estipulado na tabela 9. 17. Homogenizar em vortex. 18. Aguardar 5 minutos. 19. Usar o branco da tabela 8 para zerar o especrofotmetro. 20.Ler a absorbncia a 595 nm. 21. Completar a Tabela 10.
Tratamento de Dados e Anlise dos Resultados (Relatrio 3) Clculos e Grficos 1. Construir o grfico necessrio para a determinao da concentrao de atividade enzimtica de alfa-glicosidase no material DEAE. Expressar os resultados em mU/mL 2. Em seguida, baseado na determinao da concentrao de protenas (mg/mL) feita no material DEAE, determinar a atividade especfica de alfa-glicosidase (mU/mg) do material DEAE. 3. Calcular a recuperao e o enriquecimento da atividade de alfa-glicosidase aps a cromatografia de troca inica. Prtica 6 Purificao de protenas SDS-PAGE
Objetivos Analisar a composio de protenas do material que contm -glicosidase eludo na cromatografia de troca-inica. 29,2 g
acrilamida gua qsp
100 mL
soluo A NNbis metilenoacrilamida 0,80 g soluo B tris 1,5 M pH 8,8 (acertar valor de pH com HCl) soluo C tris 0,5 M pH 6,8 (acertar valor de pH com HCl) 3,5 mL
gua
tampo de amostra soluo C 1,25 mL glicerol 2,50 mL SDS 10 g/L 2,0 mL azul de bromofenol 5 g/L 0,20 mL -mercaptoetanol 0,05 mL 3,03 g 14,4 g
tris glicina
SDS 1,0 g tampo de corrida gua qsp 1 L Obs.: No acertar o pH desta soluo tampo. soluo de colorao Coomassie blue R 0,1 g metanol 40 mL cido actico 10 mL gua qsp 50 mL soluo de descolorao metanol 40 mL cido actico 10 mL gua qsp 50 mL Procedimento A Preparao das amostras 1. Aplicar as seguinte amostras no gel de SDS-PAGE: a. lisado de Saccharomyces cerevisiae (30 microlitros); b. fraes eludas na cromatografia de troca-inica e que contm alfa-glicosidase, denominado Material DEAE (maior volume possvel at 1 mL) Dilise das amostras 2. Transferir para um microtubo o volume indicado de amostra. 3. Identificar o microtubo com: a. Nome da amostra. b. Nmero do grupo. 4. Adicionar gua, caso necessrio, at completar 600 L. 5. Cobrir o microtubo com um pedao de membrana de dilise. 6. Prender a membrana de dilise com um anel de borracha. 7. Transferir o microtubo para um suporte de isopor. 8. Colocar o suporte dentro de um bquer contendo gua. 9. Manter sob agitao por pelo menos 16 horas. Secagem a vcuo (Executado pelos monitores) 10. Aps a dilise, transferir as amostras para um concentrador a vcuo. 1. Secar as amostras. Desnaturao das protenas presentes nas amostras 12. Transferir para cada microtubo 20 L de tampo de amostra. 13. Transferir os microtubos para um banho fervente. 14. Incubar os
microtubos por 5 min. 15. Retirar os microtubos. 16. Aplicar as amostras no gel de eletroforese com o auxlio de micropipetadores. Procedimento B Preparao do gel de SDS-PAGE (Feito pela tcnica) Preparao do gel de separao 1. Adicionar em um tubo os volumes estipulados na Tabela 1. 2. Homogeneizar rapidamente. 3. Transferir a mistura, utilizando uma pipeta Pasteur, para as placas de vidro previamente montadas. 4. Aguardar a polimerizao cerca de 60 min. 5. Colocar o pente sobre entre as placas de vidro. Preparao do gel de empilhamento 6. Aps a polimerizao do gel de separao, adicionar em outro tubo os volumes estipulados na Tabela 2. 7. Homogeneizar rapidamente. 8. Transferir a mistura, utilizando uma pipeta Pasteur, para as placas de vidro (com o pente) contendo o gel de separao polimerizado. 9. Aguardar a polimerizao cerca de 40 min. 10. Aps a polimerizao do gel de empilhamento, retirar cuidadosamente o pente. 1. Adicionar o tampo de corrida. Tabela 1 Tabela 2 solues volume solues volume gua 4,02 mL gua 3,05 mL SDS 100 g/L 100 L SDS 100 g/L 50 L soluo A 3,3 mL soluo A 0,65 mL soluo B 2,5 mL soluo C 1,25 mL TEMED 5 L TEMED 5 L persulfato de amnio 50 L persulfato de amnio 25 L Procedimento C Eletroforese, colorao e descolorao 1. Correr a eletroforese com 100V, durante aproximadamente 40 min. 2. Desligar a fonte quando o corante marcador de frente atingir a base do gel. 3. Desconectar os cabos. 4. Retirar o gel. 5. Colocar o gel no frasco contendo a soluo de colorao. 6. Corar o gel por 40 min. 7. Retirar o gel do frasco de colorao. 8. Colocar o gel no frasco contendo a soluo de descolorao. 9. Descorar o gel. 10. Visualizar as bandas de protenas. Procedimento D Desidratao do gel (Opcional) 1. Colocar o gel num frasco contendo gua. 2. Trocar tantas vezes quanto for necessrio a gua do frasco at a remoo completado cido actico. 3. Retirar o gel hidratado do frasco com gua. 4. Colocar o gel num frasco contendo soluo de glicerol 50 g/L. 5. Molhar com a soluo de glicerol lminas de celofane natural 6. Dispor as folhas de celofane sobre placas limpas de vidro. 7. Colocar os gis sobre as lminas de celofane devidamente hidratadas e limpas. 8. Colocar outra folha de celofane previamente hidratada sobre o gel, formando assim um sanduche. 9. Retirar delicadamente as bolhas de ar que estiverem aprisionados pelas folhas de celofane. 10. Esticar as folhas e prend-las. 1. Deixar secar temperatura ambiente. SDS (288,38 g/mol)
TEMED (116,20 g/mol) N N CH3CH3 CH3CH3 CONVERSO DE PERSULFATO EM ON SULFATO
Tratamento de Dados e Anlise dos Resultados PRTICA 6 - PURIFICAO DE PROTENAS SDS-PAGE (Relatrio 4) INSTRUES: 1. Identificar a banda correspondente -glicosidase no gel de SDS-PAGE. 2. Calcular o provvel peso molecular relativo da enzima atravs dos padres utilizados na eletroforese. Prtica 7 Caracterizao da alfa-glicosidase: Km e Vmax Objetivos Caracterizar a -glicosidase de Saccharomyces cerevisiae atravs das determinaes da afinidade (Km) da enzima pelo substrato (p-nitrofenol--glicosdeo) e da velocidade mxima (Vmax) de hidrlise do substrato. Reagentes Materiais Aparelhagens gua destilada banho de gelo banho 30oC lisado de levedura (P6) cubetas para leitura espectrofotmetro p-nitrofenil-glicosdeo (NPGlc) 1,0 mM em tampo fosfato 100 mM pH 7,0 pipetadores vrtice pipetas p-nitrofenil-glicosdeo (NPGlc) 2,0 mM em tampo fosfato 100 mM pH 7,0 ponteiras suporte para tubos de ensaio p-nitrofenilglicosdeo (NPGlc) 8,0 mM em tampo fosfato 100 mM pH 7,0 tubos de ensaio tampo carbonato-bicarbonato 250 mM pH 1,0 tampo fosfato 100 mM pH 7,0 Procedimento A Diluio do lisado de Saccharomyces cerevisiae
UTILIZE A DILUIO USADA NA PRTICA 3. SOMENTE CASO NO SEJA POSSVEL, EMPREGUE O PROCEDIMENTO ABAIXO. NOTE QUE O VOLUME TOTAL NECESSRIO SER DE 5,0 mL. Abaixo segue o procedimento sugerido para a diluio da preparao do lisado de Saccharomyces cerevisiae. 18. Transferir 0,1 mL do lisado de Saccharomyces cerevisiae para um tubo identificado com L10X. 19. Adicionar 0,9 mL de gua destilada gelada. 20. Homogeneizar SUAVEMENTE. 21. Transferir 0,5 mL de L10X para um novo tubo identificado com L100X. 2. Adicionar 4,5 mL de gua destilada gelada. 23. Homogeneizar SUAVEMENTE. Procedimento B Medidas de velocidade da reao de hidrlise do substrato 1. Adicionar em cada tubo os volumes de NPGlc estipulados na Tabela 1. ATENO: prestar ateno nas diferentes concentraes de substrato. 2. Preparar os tubos em banho de gelo 3. Adicionar em cada tubo os volume de tampo e lisado (devidamente diludo) estipulados na Tabela 1. Agitar manualmente com cuidado. 4. Transferir todos os tubos do gelo para o banho a 30oC 5. Incubar todos os tubos por 40 min (OU PELO DOBRO DO MAIOR TEMPO USADO NA PRTICA 3). 6. Remover todos os tubos do banho. 7. Adicionar 2 mL de tampo carbonatobicarbonato. 8. Deixar os tubos em temperatura ambiente. 9. Homogeneizar em vrtice. 10. Usar a gua para calibrar (zerar) o espectrofotmetro. 1. Ler as absorbncias a 420 nm. 12. Completar a Tabela 2. 13. Construir os grficos necessrios para a determinao do Km e Vmax da -glicosidase para o substrato utilizado. Tabela 1 tubos NPGlc 1,0 mM (mL) NPGlc 2,0 mM (mL) NPGlc 8,0 mM (mL) tampo fosfato 100 mM pH 7 (mL) lisado diludo (mL) 1 0,02 - - 0,28 0,10 2 0,04 - - 0,26 0,10 3 0,08 - - 0,2 0,10 4 0,12 - - 0,18 0,10 5 0,16 - - 0,14 0,10 6 0,20 - - 0,10 0,10 7 - 0,16 - 0,14 0,10 8 - 0,20 - 0,10 0,10 9 - - 0,10 0,20 0,10 10 - - 0,13 0,17 0,10 1 - - 0,15 0,15 0,10 Tabela 2 tubos
[S] (no tubo de ensaio) (mM) A420 nmols de produto Tempo da reao (min) Velocidade (nmol/min) 1 2 3 4 5 6 7 8 9 10 Prtica 8 Caracterizao da alfa-glicosidase determinao de padro de inibio por maltose Objetivos Determinar o padro de inibio de maltose sobre a hidrlise de p-nitrofenil-glicosdeo (NPGlc) efetuada pela -glicosidase de Saccharomyces cerevisiae.
Reagentes Materiais Aparelhagens gua destilada banho de gelo banho 30oC lisado de levedura (P6) cubetas para leitura espectrofotmetro maltose 0,4 M em tampo fosfato 100 mM pH 7,0 pipetadores vrtice pipetas maltose 1,2 M em tampo fosfato 100 mM pH 7,0 ponteiras suporte para tubos maltose 1,6 M em tampo fosfato 100 mM pH 7,0 tubos de ensaio p-nitrofenil-glicosdeo (NPGlc) 1,0 mM em tampo fosfato 100 mM pH 7,0 pnitrofenil-glicosdeo (NPGlc) 2,0 mM em tampo fosfato 100 mM pH 7,0 p-nitrofenilglicosdeo (NPGlc) 8,0 mM em tampo fosfato 100 mM pH 7,0 tampo carbonato-bicarbonato 250 mM pH 1,0 tampo fosfato 100 mM pH 7,0
Procedimento A Diluio do lisado de Saccharomyces cerevisiae Ateno: Ser utilizada a mesma soluo de enzima j diluda para a Prtica 7 Caracterizao da enzima: Km e Vmax. No h necessidade de preparar uma nova diluio. Procedimento B Medidas da velocidade de reao de hidrlise do substrato na presena de inibidor 1. Adicionar em cada tubo os volumes de NPGlc e maltose estipulados na Tabela 1. ATENO: prestar ateno nas diferentes concentraes de substrato e inibidor. 2. Preparar os tubos em banho de gelo 3. Adicionar em cada tubo os volume de tampo e lisado (devidamente diludo) estipulados na Tabela 1. Agitar manualmente com cuidado. 4. Transferir todos os tubos do gelo para o banho a 30oC. 5. Incubar todos os tubos pelo dobro do tempo usado na prtica 7. 6. Remover todos os tubos do banho. 7. Adicionar 2 mL de tampo carbonato-bicarbonato. 8. Deixar os tubos em temperatura ambiente. 9. Usar gua para calibrar (zerar) o espectrofotmetro. 10. Ler as absorbncias a 420 nm. 1. Completar a Tabela 2. 12. Construir os grficos necessrios para a determinao do padro de inibio da -glicosidase por maltose. tubos NPGlc 1,0 mM (mL) NPGlc 2,0 mM (mL) NPGlc 8,0 mM (mL) maltose 0,4 M (mL) maltose 1,2 M (mL) tampo fosfato 100 mM pH 7 (mL) lisado diludo (mL)
tubos [S] final
(mM) [I] final tubos [S] final (mM) [I] final 1 A7 A 1 B7 B 2 A8 A 2 B8 B 3 A9 A 3 B9 B 4A 4B 10 A 10 B
5 A1 A 5 B1 B 6A 6B 12 A 12 B
Grupos 1 a 6 Grupos 7 a 12 Tratamento de Dados e Anlise dos Resultados (Relatrio 5)
1-Construir os grficos de Michaelis-Menten e Lineweaver-Burk para determinao de Vmax e Km 2-Construir o grfico de Lineweaver-Burk na presena do inibidor. 3-Determinar os valores de Km, Vmax e o padro de inibio TABELA 1 - PARA O CLCULO DE K E V tubos A420 no de mols Tempo de ensaio velocidade (unidades de abs) (nmol) (min) (nmol/min) 1 2 3 4 5 6 7 8 9 10 1 TABELA 2 - PARA O CLCULO DE K E V [S] velocidade 1/[S] 1/velocidade (mM) (nmol/min) (mM)-1 (nmol/min)-1 0,05 0,1 0,2 0,3 0,4 0,5 0,8 1 2 2,6 3 K = _ mM V = _ mU
Vous aimerez peut-être aussi
- Programação Aulas Práticas Bioquímica Aplicada - 2º Semestre 2015 Tecnologia de Alimentos Prof. Lívia Bracht Dia AulaDocument15 pagesProgramação Aulas Práticas Bioquímica Aplicada - 2º Semestre 2015 Tecnologia de Alimentos Prof. Lívia Bracht Dia AulaJONATHAN HENRIQUE BARBOSA FRANCISCOPas encore d'évaluation
- Cap 04 FermentacaoDocument75 pagesCap 04 FermentacaoFamilia Llanos AlvarezPas encore d'évaluation
- Cap 04 FermentacaoDocument75 pagesCap 04 Fermentacaofla-vi-nho9595Pas encore d'évaluation
- Cap 03 Cana, Prep. e TratamDocument126 pagesCap 03 Cana, Prep. e TratamMarcello Pinto MartinsPas encore d'évaluation
- Roteiro Das Aulas Prticas Bioqumica 2023 2Document13 pagesRoteiro Das Aulas Prticas Bioqumica 2023 2MONARA DE ANDRADE MARTINSPas encore d'évaluation
- Apostila de Bioquímica Experimental 1Document34 pagesApostila de Bioquímica Experimental 1guilherme alvesPas encore d'évaluation
- Relatório 5Document13 pagesRelatório 5Elizandra Goncalves da SilvaPas encore d'évaluation
- Roteiro Praticas, CC e ED - Bioq M1-2011-1Document16 pagesRoteiro Praticas, CC e ED - Bioq M1-2011-1Iuri SampaioPas encore d'évaluation
- Transaminase Oxalacetica PopDocument4 pagesTransaminase Oxalacetica Popjoanamariar327Pas encore d'évaluation
- Bioquimica I Pratica 6 AMILASEDocument2 pagesBioquimica I Pratica 6 AMILASEGabriel SidaniPas encore d'évaluation
- Relatório de Biomol - UFGDocument12 pagesRelatório de Biomol - UFGJanaína MoreiraPas encore d'évaluation
- Apostila de Aulas Prticas DBBM 2024Document40 pagesApostila de Aulas Prticas DBBM 2024Victoria Porto Sandre MissiattoPas encore d'évaluation
- QAF Roteiros Das Prã¡ticasDocument14 pagesQAF Roteiros Das Prã¡ticaslauany araujoPas encore d'évaluation
- Aula 5 Determinação de Cianeto em MandiocaDocument2 pagesAula 5 Determinação de Cianeto em MandiocaAbmamudalziraPas encore d'évaluation
- MET POA SLAV 39 02 Proteina BrutaDocument12 pagesMET POA SLAV 39 02 Proteina BrutaMarcelo CapistranoPas encore d'évaluation
- Relatório Da Prática de FermentaçãoDocument3 pagesRelatório Da Prática de FermentaçãoRoselene Linden100% (1)
- Apostilas de Aula Praticas BromatoDocument31 pagesApostilas de Aula Praticas BromatoBruna Suzigan VeronezPas encore d'évaluation
- Aulas Práticas PDFDocument27 pagesAulas Práticas PDFFCiênciasPas encore d'évaluation
- SebentaDocument19 pagesSebentaDanielAndersonXavierSouzaPas encore d'évaluation
- Protocolo PLFADocument27 pagesProtocolo PLFAEd SilvaPas encore d'évaluation
- Relatório Troca Ionica FINALDocument38 pagesRelatório Troca Ionica FINALAlina Ardel MartinsPas encore d'évaluation
- Materiais e ReagentesDocument4 pagesMateriais e ReagentesCristina ChavesPas encore d'évaluation
- Cinetica Enzimatica EnqDocument7 pagesCinetica Enzimatica EnqANA FLAVIA FEUSERPas encore d'évaluation
- Resumos Laboratoriais QF IIDocument17 pagesResumos Laboratoriais QF IIMariana FerreiraPas encore d'évaluation
- Abnt NBR 10908 - Aditivos para Argamassa E Concretos - Ensaios de UniformidadeDocument7 pagesAbnt NBR 10908 - Aditivos para Argamassa E Concretos - Ensaios de UniformidadeLuma SampaioPas encore d'évaluation
- Roteiro Prática 2 - Deteminação de Carboidratos TotaisDocument4 pagesRoteiro Prática 2 - Deteminação de Carboidratos TotaisRaquel MagalhãesPas encore d'évaluation
- Prelab Aula 11 - Práticas de Bioq 2Document4 pagesPrelab Aula 11 - Práticas de Bioq 2Leo Bayer PereiraPas encore d'évaluation
- NBR 10908 - 1990 - Aditivos para Argamassa e Concreto - Ensaios de UniformidadeDocument7 pagesNBR 10908 - 1990 - Aditivos para Argamassa e Concreto - Ensaios de UniformidadeRonald Rolim de MouraPas encore d'évaluation
- RELATÓRIO 1 - Purificação Do Lisozima Da Clara Do Ovo Por Cromatografia de Troca IónicaDocument35 pagesRELATÓRIO 1 - Purificação Do Lisozima Da Clara Do Ovo Por Cromatografia de Troca IónicaAlexandra Salvado0% (1)
- Roteiro Aula Prática - Qualidade Da ÁguaDocument6 pagesRoteiro Aula Prática - Qualidade Da ÁguaDjenifer Kipper100% (1)
- FANDocument10 pagesFANChristian Nilcer Chacon VidalPas encore d'évaluation
- Fasb - Faculdade de São Bernardo Química Inorgânica Iv - Laboratório - 2021 Professora: Márcia PalomaresDocument13 pagesFasb - Faculdade de São Bernardo Química Inorgânica Iv - Laboratório - 2021 Professora: Márcia PalomaresAlexandre RomaoPas encore d'évaluation
- Análises MicrobiológicasDocument21 pagesAnálises MicrobiológicasLise SoaresPas encore d'évaluation
- Hemograma ManualDocument16 pagesHemograma ManualErick2007Pas encore d'évaluation
- Lab Amilase SalivarDocument1 pageLab Amilase SalivarRita PereiraPas encore d'évaluation
- Laudo Prática JartestDocument4 pagesLaudo Prática JartestmariannaribsouzaPas encore d'évaluation
- Roteiro Experimental II 2010-1 Corrigido NovoDocument24 pagesRoteiro Experimental II 2010-1 Corrigido Novofabom007Pas encore d'évaluation
- Protocolo ELISADocument3 pagesProtocolo ELISAstefanie.sousaPas encore d'évaluation
- PURIFICAÇÃO de DNA - Fundamentos Teórico Praticos Biologia Molecular - EmbrapaDocument9 pagesPURIFICAÇÃO de DNA - Fundamentos Teórico Praticos Biologia Molecular - EmbrapaLucas Da SilvaPas encore d'évaluation
- Metodologias Lab de FrutosDocument59 pagesMetodologias Lab de FrutosFabiano Tavares de MouraPas encore d'évaluation
- Roteiro Aula Prática Enzimas Avaliação Da Atividade Da Amilase SalivarDocument2 pagesRoteiro Aula Prática Enzimas Avaliação Da Atividade Da Amilase SalivarIsabelle Reis100% (1)
- Metodo Flavonoides Totais - GeanDocument3 pagesMetodo Flavonoides Totais - GeanLeonardo PennaPas encore d'évaluation
- Protocolo - Nitrogênio-ProteínaDocument3 pagesProtocolo - Nitrogênio-ProteínaRonaldo BortolanzaPas encore d'évaluation
- Relatório Titulação Ácido-BaseDocument6 pagesRelatório Titulação Ácido-BasejvoliveerPas encore d'évaluation
- Cálculo RenalDocument4 pagesCálculo RenalFernandoPas encore d'évaluation
- Os MaiasDocument7 pagesOs MaiasÍris VilhenaPas encore d'évaluation
- Glucox 500 DolesDocument4 pagesGlucox 500 DolesAquilino VazPas encore d'évaluation
- Determinação de Cromo HexavalenteDocument8 pagesDeterminação de Cromo HexavalenteMariPas encore d'évaluation
- Rote IrosDocument32 pagesRote IrosLuna RileyPas encore d'évaluation
- Roteiro Aula Prática Proteínas e EnzimasDocument7 pagesRoteiro Aula Prática Proteínas e EnzimasJoão Victor G. SantanaPas encore d'évaluation
- Demanda Bioquímica de OxigênioDocument4 pagesDemanda Bioquímica de Oxigêniowashington willerPas encore d'évaluation
- QuímicaDocument5 pagesQuímicaAntonio CarlosPas encore d'évaluation
- CPK DolesDocument4 pagesCPK DolesAquilino VazPas encore d'évaluation
- Enalapril Farmacopeia v2 2803Document3 pagesEnalapril Farmacopeia v2 2803Gaabi FelixPas encore d'évaluation
- Projetos Em Clp Ladder Baseado No Twidosuite Parte XiiD'EverandProjetos Em Clp Ladder Baseado No Twidosuite Parte XiiPas encore d'évaluation
- Projetos Com Esp8266 Programado Em Arduino - Parte XxiD'EverandProjetos Com Esp8266 Programado Em Arduino - Parte XxiPas encore d'évaluation
- Projetos Com Esp8266 Programado Em Lua - Parte XxiD'EverandProjetos Com Esp8266 Programado Em Lua - Parte XxiPas encore d'évaluation
- PescadosDocument54 pagesPescadosEdgard FreitasPas encore d'évaluation
- Tecnologia Cervejeira PDFDocument274 pagesTecnologia Cervejeira PDFEdgard Freitas100% (5)
- Top Segurnça Alimentar PDFDocument217 pagesTop Segurnça Alimentar PDFEdgard FreitasPas encore d'évaluation
- Aula 1 - Histórico Microbiologia - Fase 5Document23 pagesAula 1 - Histórico Microbiologia - Fase 5Edgard Freitas100% (1)
- Industria Do PescadoDocument212 pagesIndustria Do PescadoEdgard Freitas100% (1)
- 8 A Importância Da Segurança Alimentar No Ambiente HospitalarDocument10 pages8 A Importância Da Segurança Alimentar No Ambiente HospitalarEdgard FreitasPas encore d'évaluation
- Instrução Normativa N - 031 - 2013Document11 pagesInstrução Normativa N - 031 - 2013Edgard FreitasPas encore d'évaluation
- Aula Leishmania 2017 PDFDocument74 pagesAula Leishmania 2017 PDFEdgard Freitas100% (1)
- Bromatologia Aula ExperimentalDocument24 pagesBromatologia Aula ExperimentalEdgard FreitasPas encore d'évaluation
- Aula 2 Classificação Biológica Dos Seres VivosDocument26 pagesAula 2 Classificação Biológica Dos Seres VivosEdgard Freitas100% (2)
- Capitulo 5 Tpoa1 Leite 2008 Parte1Document13 pagesCapitulo 5 Tpoa1 Leite 2008 Parte1Edgard FreitasPas encore d'évaluation
- Aula de Ppho e AppccDocument23 pagesAula de Ppho e AppccEdgard FreitasPas encore d'évaluation
- Livro Bromatologia Online 2016Document172 pagesLivro Bromatologia Online 2016Edgard FreitasPas encore d'évaluation
- (2625) PDFDocument384 pages(2625) PDFFabrício SouzaPas encore d'évaluation
- Ps 2023 - 2 - Destruição CriativaDocument38 pagesPs 2023 - 2 - Destruição CriativaAssinatura PremiumPas encore d'évaluation
- Remédios Caseiros para Desparasitar Gatos - PeritoAnimalDocument7 pagesRemédios Caseiros para Desparasitar Gatos - PeritoAnimalMarcos Antonio da SilvaPas encore d'évaluation
- MP - Sigacom - Importador XMLDocument10 pagesMP - Sigacom - Importador XMLThaty AnjosPas encore d'évaluation
- O Biogás Na AlemanhaDocument2 pagesO Biogás Na AlemanhaMatheus RodriguesPas encore d'évaluation
- Apostila Vigilante Defesa e ArmamentoDocument21 pagesApostila Vigilante Defesa e ArmamentoHack Security100% (9)
- Constitucional - Informativos Importantes STFDocument48 pagesConstitucional - Informativos Importantes STFRoberta GonçalvesPas encore d'évaluation
- Tratamentos de Ultima Geracao Francisco Borrello RadiestesiaDocument12 pagesTratamentos de Ultima Geracao Francisco Borrello RadiestesiaJaine Silva100% (1)
- Elementos 2 - ChavetasDocument17 pagesElementos 2 - ChavetasSamuel FelipePas encore d'évaluation
- Lição Completa Tradição e SabedoriaDocument194 pagesLição Completa Tradição e SabedoriaDaniel GomesPas encore d'évaluation
- Guia de Fabricação Queijo MussarelaDocument7 pagesGuia de Fabricação Queijo MussarelaHeloísa Laticínios100% (1)
- SlidesDocument52 pagesSlidesWillian Ricardo RitterPas encore d'évaluation
- Inquerito TrabalhoDocument10 pagesInquerito TrabalhoVenancio Rabissone Missomali100% (3)
- Bibliografia 2º AnoDocument4 pagesBibliografia 2º Ano1duartenmmf9542Pas encore d'évaluation
- RESUMO HISTOLOGIA - DentinogeneseDocument16 pagesRESUMO HISTOLOGIA - DentinogeneseSérgio Henrique Ferreira dos ReisPas encore d'évaluation
- Classes Invariáveis ExercíciosDocument6 pagesClasses Invariáveis Exercíciosandre luiz100% (1)
- Gileuza - Estágio Supervisionado em Farmácia ComercialDocument15 pagesGileuza - Estágio Supervisionado em Farmácia ComercialAngelica MartinsPas encore d'évaluation
- Alfred Hitchcock - Historias para Ler No CemiterioDocument164 pagesAlfred Hitchcock - Historias para Ler No CemiterioMagnoMendesPas encore d'évaluation
- Folder TH Da CTBCDocument2 pagesFolder TH Da CTBCBruno da CostaPas encore d'évaluation
- Instrução Normativa - in #47, de 21 de Agosto de 2019 - Qualificação e ValidaçãoDocument14 pagesInstrução Normativa - in #47, de 21 de Agosto de 2019 - Qualificação e ValidaçãoAlan CarvalhoPas encore d'évaluation
- Desafio - Projeto Integrador - Uc1Document2 pagesDesafio - Projeto Integrador - Uc1Thaisa NaianiPas encore d'évaluation
- Modulo 06 - Tecnologias - BiorremediacaoDocument73 pagesModulo 06 - Tecnologias - BiorremediacaoLuisVieiraPas encore d'évaluation
- Projeto Honey PotDocument61 pagesProjeto Honey PotInoxiaPas encore d'évaluation
- Protocolo de Ginecologia Do HC-UFMGDocument56 pagesProtocolo de Ginecologia Do HC-UFMGSabrina AraújoPas encore d'évaluation
- Direito À Cidade e Direito À Vida - Perspectivas Críticas Sobre o Urbano Na Contemporaneidade (Ana Fani Alessandri Carlos e Cibele Saliba Rizek)Document295 pagesDireito À Cidade e Direito À Vida - Perspectivas Críticas Sobre o Urbano Na Contemporaneidade (Ana Fani Alessandri Carlos e Cibele Saliba Rizek)GadPas encore d'évaluation
- Back-UPS BR - BZ1500XLBI-BRDocument3 pagesBack-UPS BR - BZ1500XLBI-BRbruno cominPas encore d'évaluation
- ATIVIDADE 1 RespondidaDocument3 pagesATIVIDADE 1 Respondidaana ameliaPas encore d'évaluation
- Preservado para Um PropósitoDocument8 pagesPreservado para Um Propósitoalanariana2644Pas encore d'évaluation
- Pronomes ÁtonosDocument14 pagesPronomes ÁtonosElizabeth Palacios chavezPas encore d'évaluation
- Solomons ResolvidoDocument142 pagesSolomons ResolvidoAmanda Ramos87% (15)