Académique Documents
Professionnel Documents
Culture Documents
Examen Uni Fisic Nxpowerlite
Transféré par
Chelvis RECopyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Examen Uni Fisic Nxpowerlite
Transféré par
Chelvis REDroits d'auteur :
Formats disponibles
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
UNIVERSIDAD NACIONAL DE INGENIERA FSICA
01. Para elevar 10 m de agua hasta el tanque elevado de un edificio, el cual se encuentra a 40 m de altura, se utiliza una bomba que tiene un motor de 2 kW. Si la eficiencia del motor es 80%, en cunto tiempo aproximadamente se logra subir el 2 agua? (g = 9,81 m/s ) g H O ' 1,00 2 cm 3 A) 36 min 20 s C) 45 min E) 1 hora B) 40 min 50 s D) 52 min 30 s A) 10 D) 2 97 B) 17 E) 26 C) 13 2
3
UNIVERSIDAD NACIONAL DE INGENIERA
A) 9,80 D) 5,66 B) 8,33 E) 4,57 C) 6,25 A) VFV D) FVV B) FFV E) VFF C) VVF
AH = 12 m
05. En la figura mostrada el bloquecito de masa mo parte del reposo desde una altura h = 12 m y se desliza sobre la superficie lisa semi-circular de radio R = 15 m. Al llegar a la parte inferior el bloquecito choca elsticamente con el bloque de masa M =3mo que se encuentra en reposo. Como resultado de esta colisin el bloque de masa M sube hasta una altura H (en metros) igual a:
07. Una lente delgada convergente de distancia focal 30 cm debe colocarse entre una fuente luminosa puntual y una pantalla, de modo que sobre sta se forme ntidamente la imagen de la fuente. La distancia entre la fuente luminosa y la pantalla es 1,50 m. Las distancias, en cm, de las dos posiciones posibles en las que se debe colocar la lente con respecto a la fuente, son:
02. Una piedra se deja caer desde cierta altura h. Despus de descender la distancia 2h/3, desde el punto inicial de su movimiento choca con otra piedra que haba partido en el mismo instante lanzada desde el piso verticalmente hacia arriba. Calcule la altura mxima a la que habra llegado la segunda piedra si no hubiese chocado con la primera. A) 3h/8 B) 5 h/4 C) h/2 D) 3h/4 E) h/3 03. En el grfico que se muestra,
xv
04. La superficie circular sobre la que se apoya la bolita es perfectamente lisa. 2 Calcule la aceleracin, en m/s , que debe tener el carrito para que la bolita adopte la posicin mostrada. 2 (g = 9,8 m/s ) Dato: Sen16 = 7/25
ib
ro s
A) 3 D) 9
Z. c
B) 4 E) 12
om
C) 6
w .L
determine el mdulo del vector T (en m), donde:
xv xxv xxv xxv xxv
T = FE + EG + DE - FD AB = AD = 5 2 m
06. Una mol de gas ideal que se encontraba bajo una presin 5 se comprime de 610 Pa isotrmicamente de 4 R hasta 2 R. (La constante universal de los gases ideales es R = 8,3 J/mol.K) Dadas las siguientes proposiciones respecto del proceso: 5 I. La presin aumenta 10 Pa. 5 II. La presin disminuye 2.10 Pa. III. La temperatura del gas es aproximadamente de 15,8 C. Indique la secuencia correcta despus de determinar si las proposiciones anteriores son verdaderas o falsas.
A) 105,5; 44,4 B) 106,5; 43,4 C) 107,5; 42,4 D) 108,5; 41,4 E) 109,5; 40,4 08. Dadas las siguientes proposiciones referentes a las leyes de Kepler sobre los movimientos planetarios: I. La Tierra describe una rbita elptica con el Sol en el centro de la elipse. II. El vector que va del Sol a la Tierra barre reas iguales en tiempos iguales.
-1-
-2-
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
UNIVERSIDAD NACIONAL DE INGENIERA
III. El cubo del perodo de la rbita de la Tierra es proporcional al cuadrado de su semieje mayor. Son correctas: A) Slo I B) Slo II C) Slo III D) I y III E) II y III 09. En agua de mar, un flotador completamente sumergido soporta a una persona de 75,0 kg con el 20% del volumen de la persona fuera del agua. Si el volumen del flotador es de 3 0,040 m , cul es la densidad media 3 del flotador en kg/m ? Datos: Densidad del agua de mar= 3 3 1,03 10 kg/m Densidad media del cuerpo humano= 2 3 9,8 10 kg/m 2 A) 6,5610 2 B) 6,7910 2 C) 6,9410 2 D) 7,0610 2 E) 7,3110 10. Desde una fuente puntual se emiten ondas sonoras tal que la intensidad es 2 de 0,026 W/m a una distancia de 4,3 m de la fuente. Cunta energa 4 sonora en 10 J, emite la fuente en una hora si su potencia se mantiene constante? A) 2,17 B) 2,27 C) 2,37 D) 2,47 E) 2,57 11. Calcule la presin manomtrica en Pa, directamente debajo de un bloque cbico de madera de 10 cm de arista y densidad 0,5 g/cm que flota con 2/3 de su volumen sumergido tal como se 2 muestra en la figura (g=9,8 m/s )
3
UNIVERSIDAD NACIONAL DE INGENIERA
14. En la figura se representa una barra conductora de masa 20 g y longitud 10 cm, suspendida por dos hilos rgidos tambin de material conductor y de masas despreciables. La barra se coloca en un campo magntico, formando la conocida balanza magntica. Si al circular una corriente I de 2 amperios, por la barra, sta se inclina formando un ngulo = 45 con la vertical, determine la intensidad
!
A) 130 D) 410
B) 230 E) 490
C) 340
13. Calcule la corriente en A, a travs de la resistencia de 20 del circuito mostrado en la figura.
12. Consideremos el modelo del tomo de Bohr de hidrgeno, donde el electrn tiene una carga negativa de -19 q=1,610 C. El electrn gira con 6 una rapidez de 2,1810 m/s y con un -11 radio de giro de 5,2 10 m. Este electrn en movimiento circular puede ser visto como una espira con corriente. Cul sera aproximadamente la intensidad de corriente de esta espira en mA? A) 1,0 B) 2,0 C) 3,0 D) 4,0 E) 5,0
de induccin magntica | B | en teslas.
Z. c
om
A) 54 minutos B) 1 hora 7 minutos C) 1 hora 14 minutos D) 1 hora 35 minutos E) 1 hora 41 minutos 16. En relacin a las propiedades del fotn, se tienen las siguientes proposiciones: I. Viaja a la velocidad de la luz en cualquier medio II. Posee una masa muy pequea, comparable con la del electrn III. No tiene masa pero transporta energa. Son correctas: A) Slo I B) Slo II C) Slo III D) I y III E) I y II 17. Utilizando el sistema de poleas ideales mostrado en la figura, se desea que el bloque de 16 kg ascienda con 2 aceleracin de 2 m/s . Determine la
!
ro s
w .L
ib
A) 0,098 D) 98
B) 0,98 E) 980
C) 9,8
A) 1,0 D) 2,5
B) 1,5 E) 3,0
C) 2,0
15. Se construye una terma solar con una caja de un material trmicamente aislante, como se muestra en la figura. La tapa superior de la caja es 2 transparente y tiene un rea de 3 m . Cunto tiempo necesitara la terma para calentar 60 litros de agua desde 20 hasta 60 C C?. Considere que la terma no tiene prdida de calor y que la densidad del agua es constante todo el tiempo. -3 -1 -1 agua=1 000 kg m ; Cagua=10 cal g (C) Intensidad de radiacin del sol que -2 ingresa por la tapa: 550 Wm (1 cal = 4,186 J)
fuerza F necesaria para lograr este objetivo.
-3-
-4-
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
UNIVERSIDAD NACIONAL DE INGENIERA
19. Establezca la veracidad o falsedad de los siguientes enunciados: I. Para la partcula, la energa mecnica total es constante si las fuerzas que actan sobre ella son todas conservativas. II. En todo choque entre dos partculas, elstico o inelstico, se c ons erva la c antidad de movimiento lineal total. III. Si la fuerza neta sobre una partcula es nula, se conserva su cantidad de movimiento lineal. A) VFF B) VVF C) VFV D) FFV E) VVV 20. Un sistema de masa resorte realiza un movimiento armnico simple, cuyas energas estn dadas segn la grfica, con m=1 kg, amplitud mxima de 10 cm y frecuencia angular de 3 rad/s. Calcule su energa potencial Ep (en mJ) en la posicin x mostrada.
UNIVERSIDAD NACIONAL DE INGENIERA
QUMICA 21. Respecto a los nmeros cunticos (n, R, mR, ms) que identifican a un electrn en un tomo, indique cules de las siguientes proposiciones son verdaderas: I. El conjunto (2, 1, 1, +1/2) es inaceptable. II. El conjunto (3, 0, 0, -1/2) describe un electrn con orbitales p. III. El nmero total de orbitales posibles para n = 3 y R= 2 es 5. A) I y II B) II y III C) I y III D) Slo II E) Slo III 23. Identifique el nombre correctamente escrito, segn las normas de la nomenclatura IUPAC. A) 2, 6, 6 - trimetilheptano B) 3-metil-3-buteno C) 3-etil-6, 6-dimetilheptano D) 3-pentino E) 3-metil-2-pentanol 24. Se electroliza una disolucin acuosa que contiene K2SO4 al 10% en masa, empleando una corriente de 8 amperios y durante 6 horas. Calcule la cantidad de agua descompuesta, en gramos. Masas atmicas: H = 1, O = 16 Constante de Faraday = 96 500 coulomb A) 48,34 B) 96,68 C) 99,34 D) 108,42 E) 124,34 25. Calcule el pH despus de la adicin de 49 mL de solucin de NaOH 0,10M a 50 mL de una solucin de HCR 0,10M durante una titulacin cido - base NaOH(ac) + HCR(ac) ! NaCR(ac) + H2O(R) A) 4 D) 1 B) 3 E) 0
2&
A) -47,24 j
v
B) -39,24 j
v
C) -32,00 j
D) -39,24 j
E) 47,24 j
18. Un bloque de 20 kg est en reposo sobre un plano inclinado rugoso que hace un ngulo de 60 con la horizontal, siendo ste el mximo ngulo tal que el bloque no resbala sobre el plano. El coeficiente de friccin cintico entre el bloque y el plano es 0,5. Calcule la fuerza, en N, que se debe aplicar al bloque, paralelamente al plano inclinado, para que empiece a moverse hacia arriba, 2 as como la aceleracin en m/s , con que posteriormente se mover si la fuerza no cesa. 2 (g = 9,8 m/s ) A) 339,5; 6,04 B) 339,5; 7,04 C) 319,5; 6,04 D) 319,5; 7,04 E) 299,5; 8,04
w .L
ib
ro s
Z. c
om
22. Los problemas ambientales, y en general la contaminacin, se presentan por la introduccin de sustancias dainas al ecosistema. En la columna izquierda se mencionan 3 problemas ambientales y en la columna derecha 3 posibles contaminantes. Determine la relacin correcta problema ambiental contaminante: I. Lluvia cida a) SOx, NOx II. Efecto invernadero b) Clorofluorocarbonos III. Agujero en la capa c) CO2, H2O de ozono A) I-a, II-b, III-c B) I-b, II-a, III-c C) I-c, II-a, III-b D) I-c, II-b, III-a E) I-a, II, c, III-b
C) 2
26. El ion sulfato, SO4 , es una especie muy estable. Qu puede afirmarse correctamente acerca de esta especie qumica? Nmeros atmicos: O = 8; S = 16 I. Es estable debido al gran nmero de formas resonantes que posee. II. Tiene geometra tetradrica.
A) 11,25 B) 22,50 C) 31,80 D) 33,75 E) 45,00
-5-
-6-
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
UNIVERSIDAD NACIONAL DE INGENIERA
III. El azufre ha expandido su capa de valencia. A) Slo I B) Slo II C) Slo III D) II y III E) I, II y III 27. Si en la molcula de H3PO4 los tomos de hidrgeno estn unidos a los tomos de oxgeno, determine el nmero de enlaces tipo sigma () que presenta la molcula. Nmeros atmicos: H = 1; O = 8; P = 15 Electronegatividades: H = 2,1; O = 3,5; P = 2,1 A) 8 B) 7 C) 6 D) 5 E) 4 28. Una fbrica de reactivos qumicos vende cido clorhdrico concentrado, H C R ( a c ) , c o n l a s s iguiente s especificaciones: molalidad = 15,4 mol/kg densidad = 1,18 g/mL Ya que es un producto controlado, la polica necesita saber cul es su concentracin, pero expresado como normalidad (eq/L). Qu valor de normalidad le corresponde a este cido? Masa molar HCR = 36,5 g/mol A) 5,82 B) 11,63 C) 15,62 D) 17,45 E) 23,26 29. Los estados de oxidacin del circonio en ZrO(NO3)2 y del mercurio en Hg2(NO2)2 son respectivamente: A) +2, +1 B) +2, +2 C) +4, +2 D) +1, +1 E) +4, +1 30. Se sintetiza pentafluoruro de yodo, IF5, en un matraz de 5,00 L, por reaccin entre 11 g de I2(s) y 11 g de F2(g). Si la reaccin procede hasta que uno de los reactantes se consume totalmente, cul es la fraccin molar del IF5 en el matraz al final de la reaccin, si la temperatura lleg a los 125 C? I2(s) + 5F2(g) ! 2IF5(g) Masas molares (g/mol): I2=253, F2=38 A) 0,54 B) 0,47 C) 0,27 D) 0,24 E) 0,13 31. Un recipiente de 10 L contiene una mezcla equimolar de gas nitrgeno (N2) y helio (He) a una presin de 15 atm. Cuntos globos se pueden llenar con esta mezcla de gases a 1 atm de presin, si la capacidad de cada globo es de 1 L? Considere que la temperatura en ambos sistemas es la misma. A) 10 B) 15 C) 75 D) 125 E) 150
UNIVERSIDAD NACIONAL DE INGENIERA
Reaccin: C3H8(g) + O2(g) ! CO2(g) + H2O(g) (sin balancear) Masas atmicas: H = 1; C = 12; O = 16 A) 100 B) 120 D) 476 E) 571 E) Las variaciones de la presin atmosfrica producen grandes cambios en la solubilidad de los slidos en los lquidos. 35. Para la equilibrio: siguiente reaccin 1 O2(g) 2 en
C) 298
NO2(g) NO(g) +
&
33. Indique las bases conjugadas de las especie qumicas H2S y HCO3 en solucin acuosa, respectivamente. A) S y CO3
2& 2&
seale la alternativa correcta. A) Kp = Kc / RT 3/2 B) Kp = Kc (RT) C) Kp = Kc / (RT)3 D) Kp = Kc RT E) Kp = Kc / RT 36. Dados los siguientes valores de potenciales estndares de reduccin a 25 C: Cu(ac)%e & ! Cu(s) Cu(ac)%2e & ! Cu(s)
2% %
om
-
B) HS y CO3
ro s
C) OH y H3O 2D) S y H2CO3 + E) H3S y H2CO3
ib
Z. c
32. Un quemador utiliza gas propano (C3H8)como combustible y aire como oxidante. Si se conoce que el quemador necesita un 20% de extra de oxgeno (O2), para un trabajo adecuado, calcule el volumen de aire (en L), medido a iguales condiciones de presin y temperatura, que requiere la combustin de 20 L de propano en dicho quemador. Considere que el aire contiene 21% de oxgeno (O2) y 79% de nitrgeno (N2) en volumen.
34. La solubilidad de una sustancia en un lquido depende de la naturaleza del soluto, del solvente, de la temperatura y de la presin. Al respecto, marque la alternativa correcta. A) La solubilidad de los gases en los lquidos vara inversamente con la presin parcial del gas que se disuelve. B) La solubilidad de NaCl en agua aumenta conforme aumenta la temperatura. C) La solubilidad del CO2(g) disminuye con el aumento de su presin sobre el lquido en el cual se disuelve. D) Los cuerpos que al disolverse desarrollan calor son menos solubles en fro que en caliente.
w .L
0,52 V 0,34 V
indique, cules de las siguientes proposiciones son verdaderas: I. El Cu se oxida con mayor 2+ facilidad que el Cu
% 2%
II. La reaccin 2Cu(ac) ! Cu(ac)%Cu(s) es espontnea a 25 C III. El potencial estndar
%
de
la
reaccin 2Cuac%2e & ! 2Cu(s) es 0,52 V A) I y II D) Slo II B) I y III E) Slo III C) II y III
-7-
-8-
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
UNIVERSIDAD NACIONAL DE INGENIERA
37. Dadas las siguientes proposiciones referidas a la nanotecnologa: I. Los nanotubos de carbono son mucho ms fuertes que el acero y mucho ms ligeros que ste. II. La nanotecnologa ha creado materiales ms tiles con propiedades nicas. III. Los nanotubos de carbono pueden usarse para almacenar hidrgeno. Son correctas: A) Slo I B) Slo II C) Slo III D) II y III E) I, II y III 38. Identifique el caso que corresponde a una sustancia elemental. A) Cemento B) Agua de mar C) Bronce D) Diamante E) cido muritico 39. Considerando solamente las fuerzas intermoleculares, indique qu sustancia lquida presenta mayor viscosidad. A) CH3OH(R) B) CH4(R) C) H2C=O(R) D) (CH3)2C=O(R) E) CH2OHCH2OH(R) 40. Comparando los elementos qumicos Mg, K y Ca, seale la alternativa que presenta la secuencia correcta, despus de determinar si las proposiciones siguientes son verdaderas (V) o falsas (F) I. El orden decreciente de la primera energa de ionizacin (EI) es: EICa > EIK > EIMg II. El orden decreciente del radio atmico (r) es: rMg > rK >rCa III. El magnesio, Mg, tiene la mayor electronegatividad. Nmeros atmicos: Ca, calcio =20 K, potasio=19, Mg, magnesio=12 A) VVF B) VFF C) FFV D) FVF E) VVV
UNIVERSIDAD NACIONAL DE INGENIERA RESOLUCIN
01. Por eficiencia Y n = M H O ' 2 V
m.g.h/t 2.103 Yt' 103 . (10) 9,81 . (40) 0,8 2 . 103
Ptil Pentregada
Segunda piedra h g ' VO t & t 2 ........ (2) 2 3 2 (1) + (2): h = VO t Y t '
2
h Vo
80% '
En (1): 2h g h 2 3gh 2 ' Y VO2 ' 3 2 V2 4 O2 La altura mxima alcanzada por la segunda piedra es: hmx = VO2 2g hmx = 3h 8 Rpta. A
2
Y t = 2 452,5 s | t = 40,875 min 40 min 52,5 s
om
Rpta. B
w .L
ib
ro s
Z. c
02.
03.
Primera piedra
2h = 3 2h g = t 2 ...... (1) 3 2
-9-
- 10 -
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
UNIVERSIDAD NACIONAL DE INGENIERA
xv xxv xxv xxv xxv
UNIVERSIDAD NACIONAL DE INGENIERA
Por ley de senos: FR mg ' Sen16 Sen37 Y a = 4,57 m/s
2
T = FE % EG % DE & FD
xv xxv xxv xxv
04. Haciendo el DCL de la esfera:
Luego: & e= 2 1 V1&V2 1= 2&1 V1&0
T = FG % DE % DF
xv xxv xxv xxv
T = DF % FG % DE
xv xxv xxv
V1 = 2 - 1 ................... (3) (2) + (3): Rpta. E 2 = V1 2 ................. (4)
T = DG % DE
xv xxv xxv xxv xxv
T = DG % DA % AH % HE
xv xxv xxv xxv xxv
05. M = 3mo
T = DG % AH % DA % HE
xxv
om
Hallando grficamente la resultante:
Despus del choque (para M = 3mo) Por conservacin de la energa mecnica: 2 = 2gH |
2
Z. c
ro s
DG
xv xxv xxv xxv
V1 4
= 2gH
ib
T = 2 DG + DA + HE
w .L
Antes del choque (mo) Em 'Em
o F
2gh h 12 m = 2gH | H = = =3m 4 4 4 Rpta. A 06. Datos: n = 1; R = 8,3 J/mol.K 5 -3 3 Pi = 6.10 Pa v Vi = 4 R = 4.10 m Grficamente:
xv
El mdulo del vector T es:
mo gh =
2
1 2 mo V1 2
V1 = 2gh ...................... (1) En el choque:
xv
xxv
|T| =
|2DG| % |DA| % |HE|
xxv
xxv
| T | = 242 % (5 2)2 % (5 2)2
!
xv
xv
| T | = 26
P Sistema(antes) = P Sistema(despus) moV1 + M(0) = mo1 + M2 moV1 = mo1 + 3mo2 V1 = 1 + 32 ................ (2)
Rpta. E
- 11 -
- 12 -
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
UNIVERSIDAD NACIONAL DE INGENIERA
I. Falso Resolviendo: o1 = 108,5 cm o2 = 41,46 cm
5
UNIVERSIDAD NACIONAL DE INGENIERA
75 + f 0,04 = 1,03 10
3
0,8 75 9,8 10
2
% 0,04
Aument 6.10 Pa II. Falso Respecto a la proposicin anterior III. Verdadero Usando: 08. I.
Rpta. D Falso De la 1 ley de Kepler, la trayectoria es elptica con el Sol en uno de sus focos
Operando: 2 3 f = 731 = 7,31.10 kg/m Rpta. E 10. De la ecuacin de intensidad sabemos: Energa Energa I= ' (rea)(Tiempo) 4R 2 (Tiempo) Y 0,026 = Energa 4 . (4,3)2 . (3 600)
2
La presin manomtrica debajo del bloque es: P = Paceite + Pagua P = ac gh1 + aggh2 ...... (I) Si el cubo flota: mg = Eac + Eag cubogVcubo = acgVac + aggVagua 3 3 2 2 0,5.10 .9,8.0,1 = acg(0,1 .h1) + agg(0,1 .h2) 3 0,5.10 .9,8.0,1 = acgh1 % aggh2 P En la ecuacin I: P = 490 Pa
| T = 288,8 K < > 15,8 C Rpta. B 07. f = 30 cm
ro s
III. Falso 2 3 De la 3 ley, T D.P R T = periodo; R=semieje mayor Rpta. B 09. Por equilibrio: 'Pesos = 'Empujes mpg + mfg = Ep + Ef
Z. c
om
II. Verdadero De la 2 ley las reas barridas es D.P. al tiempo
0,026 4(4,3) 3 600 = Energa
4
Rpta. E 12.
Operando: 2,1748.10 J = Energa
w .L
ib
Rpta. A 11. I= q 2R ; donde: t = t V qV 2R 1,6 . 10&19 . 2,18.106 2 . 5,2 . 10&11 ' 10&3 A
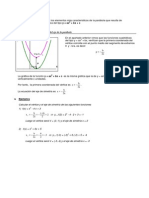
De la figura: i = 150 - o Luego: 1 1 1 ' % f o i 1 1 1 ' % 30 o 150&o o - 150o + 4 500 = 0
2
mp + fVf = H O (Vsp + Vsf)
2
I=
mp + fVf = H O (0,8Vp + Vf)
2
Se sabe para la persona: m m p = p Y Vp = p Vp p Reemplazando: mp + fVf = H O 0,8 2 mp p % Vf
I=
I = 1 mA Rpta. A
- 13 -
- 14 -
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
UNIVERSIDAD NACIONAL DE INGENIERA
13. 16. I.
UNIVERSIDAD NACIONAL DE INGENIERA
Verdadero Un fotn viaja a la velocidad de la luz sin importar el medio en el que se propaga II. Falso El fotn es considerado de masa nula. III. Faslo Un fotn transporta energa Rpta. A 18.
Rpta. B Rpta. E 15. La energa que necesita el agua para ser calentada desde 20 C hasta 60 es: C, E = Q = mCeT E = (60 10 )(1)(40) cal E = (24 10 )(4,186) J La intensidad de radiacin es: P E E I= | t ' ' A At AI t= (24105)(4,186) = 6 088,7 s (3)(550)
5 3
Z. c
VAB = VAX + VXB 82,5 = 30i + 20(4i) i = 0,75 A Por la resistencia de 20 circula la corriente: I = 4i = 4(0,75) I=3A
Del tringulo: Fmagn. = mg BIL = mg -3 B 2 0,1 = (20 . 10 )(9,8) B = 0,98 T
17.
Si 60 es el mximo ngulo para que = el bloque no resbale: s =Tg60 3 la fuerza F, para que empiece a subir el bloque es: F=10 3 g+fs F=10 3 g+s N F=10 3 g+( 3 )(10 g) = 20 3 g F = 339,5 N
v v
ib
ro s
om
14.
w .L
3F = ma F-10 3 g-fk = ma F-10 3 g -k N = ma
! !
3F = ma
!
339,5-10 3 g-(0,5)(10 g)=20 a 2 a =6,04 m/s Rpta. A
4F - mg = m a 4F - (16)(9,81) = 16(2) 4F = 188,96 F = 47,24 N
! v
Como la barra est en equilibrio:
xv xv
19. I.
t = 1 h 41 min Rpta. E
'F ' 0
F = -47,24 j Rpta. A
Verdadero De la proposicin, como el trabajo de las fuerzas no conservativas es FNC nula (W = 0), en consecuencia la energa mecnica se conserva.
- 15 -
- 16 -
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
UNIVERSIDAD NACIONAL DE INGENIERA
II. Verdadero En todo choque se conserva la cantidad de movimiento lineal total. III. Verdadero Sabemos: I'FR.t , si la fuerza Sabemos: (Vmx = .A) EM = EM = EM = 1 2 m Vmx 2 1 2 m(.A) 2 m2 . A 2 2
UNIVERSIDAD NACIONAL DE INGENIERA
III. Verdadero Si n = 3; R = 2 Valores permitidos: mR = -R, ..., 0, ..., + R Y -2; -1; 0; +1; +2 Cantidad de valores representa nmeros de orbitales = 5 Rpta. E C) Falsa
resultante es nula, entonces el impulso es nulo, por ende:
El nombre correcto es: 5-etil-2, 2-dimetilheptano
D) Falsa
(1)(3)2(10&1)2 EM = 2 EM = 45 mJ
El nombre correcto es: 2-pentino 22. I. Lluvia cida II. Efecto invernadero III. Agujero de la capa de ozono a. SOx , NOx b. Clorofluorocarbonos c. CO2 , H2O Relacionando: I-a ; II-c ; III-b Rpta. E 23. A) Falsa E) Verdadera
Z. c
Se conserva la movimiento lineal.
cantidad
de
En x: La energa potencial y cintica son iguales. Entonces: E EP = M 2 EP = 22,50 mJ
om
Rpta. E
ib
ro s
Nombre correcto es: 3-metil-2-pentanol Rpta. E
w .L
20.
Rpta. B
m = 1 kg A = 10 cm = 3 rad/s
21. Respecto a los nmeros cunticos (n, l, mR, ms) para un electrn: I. Falso S es aceptable el juego (2, 1, 1, +1/2) II. Falso R 9 El juego (3; 0; 0; -1/2), el cual R = 0 describe un subnivel sharp(s), con orbitales (s)
El nombre correcto es: 2, 2, 6 - trimetilheptano
24. En la electrlisis del K2SO4(ac); no se electroliza, lo que ocurre es la descomposicin del agua tanto en el ctodo como en el nodo, en el ctodo se libera H2(g) y en el nodo O2(g) Luego: mH O que se descompone = ?
2
B) Falsa
I=8A t = 6 h = 21 600 s 96 500 F ------- 9 g H2O 8(21 600) F ---- mH O
2
mH O = 16,11 g El nombre correcto es: 2-metil-1-buteno
2
No hay clave
- 17 -
- 18 -
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
UNIVERSIDAD NACIONAL DE INGENIERA
Observacin: Si el tiempo es 36 h, se tiene: 5 t = 1,296 10 s Eq&g mH O = I.t 2 26,8 9 5 mH O = 8 1,296 10 =96,696 g 2 96 500 Rpta. B I. verdadero: Presenta 6 estructuras resonantes II. Verdadero El tomo de azufre presenta 3 hibridacin sp razn por la cual presenta geometra tetradrica. III. Verdadero El tomo de azufre expande sus orbitales. Rpta. E 26. Se representa el diagrama del ion sulfato
&2 ( SO4 ):
UNIVERSIDAD NACIONAL DE INGENIERA
30. En un matraz:
%mSTO=
m STO m Sol
. 100 < >
562,1 .100 1 562,1
a) Determinando el reactivo limitante (RL) y reactivo en exceso (RE): 0,043 I2 = = 0,043 (reactivo limitante) 1 F2 = 0,289 = 0,057 (reactivo en exceso) 5
% mSTO = 35,98 molaridad (M) = %mSTO.10.DSol M STO 35,98(10).1,18 =11,63 36,5
25.
b) Determinando las moles de (IF5) y (F2):
ro s
Z. c
N = 11,63 Rpta. B 29. Determina el estado de oxidacin (EO): ZrO(NO3)2 c) Determinando la fraccin molar (IF5): H2 (NO2)2
1.10&4 99.10&3 HCl(ac) [ ] : 1,01.10
= MR (1) ! MR = 1,01.10
-3
En la disociacin: !
-3
1% H(ac)
Contiene 7 enlaces sigma () %
-3
1& Cl(ac)
1,01.10
1,01.10
-3
Pero: pH = -Log [H ] Reemplazando valores: -3 pH= -Log 1,01.10 = 2,995 Rpta. B
1+
28. cido clorhdrico(HCl) Rpta. A Rpta. E
- 19 -
Pero: N &g no neutralizados Eq = MR . Vt
Rpta. B
w .L
Luego: -4 -4 N &g v (No neutralizados)=(50-49)10 =1.10 Eq
27. Se representa el diagrama molecular de la molcula H3PO4
ib
om
molaridad ( M ) =
- 20 -
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
UNIVERSIDAD NACIONAL DE INGENIERA
31. Calculando el volumen de la mezcla a las condiciones de cada globo a temperatura constante: P1.V1 = P2.V2 (15 atm)(10 L) = (1 atm).Vtotal Vtotal = 150 L (Mezcla) Entonces: Vtotal 150 L N globos = ' =150 Vglobo 1 L Rpta. B Rpta. E 32. De los datos: 1C3H8(g)+5O2(g) ! 3CO2(g) + 4H2O(g) 1V 20 L 5V VO 0 VO = 100 L
2 2
UNIVERSIDAD NACIONAL DE INGENIERA
35. De la reaccin: 1 1 u n = 1% -1 = 2 2 Entonces: Kp = Kc. (RT) Kp = Kc.(RT)
1/2 n
33. Segn Brnsted y Lowry:
III. Verdadero Los nanotubos de carbono pueden utilizarse para almacenar gases. Rpta. E 38. El diamante es carbono, una sustancia elemental. Las dems opciones son mezclas.
= Kc. RT Rpta. D
36. I.
Como el quemador requiere 20% extra de O2: VO
2
B) (Verdadero) El proceso de solvatacin del NaCl en agua es endotrmico
w .L
ib
34. Analizando las proposiciones: A) (Falso) La solubilidad de los gases en lquidos aumenta al aumentar la presin ejercida sobre la solucin formada.
Falso 1+ Cu + e ! Cu g = 0,52 V 2+ Cu + 2e ! Cu g = 0,34 V 1+ Por lo tanto el Cu se reduce con mayor facilidad II. Verdadero 1+ Cu + e ! Cu g = 0,52 V 1+ 2+ Cu ! Cu + e g = 0,18 V 1+ 2 2Cu ! Cu + Cu g = 0,70 V III. Verdadero 1+ Cu + 1e ! Cu 1+ 0 Y 2Cu + 2e ! 2Cu g = 0,52
om
Rpta. D 39. La viscosidad aumenta al aumentar la intensidad de las fuerzas intermoleculares. Las fuerzas intermoleculares ms intensas son los puentes de hidrgeno, en consecuencia el lquido ms viscoso es: CH2OHCH2OH Etanodiol
C) (Faslo) La solubilidad del CO2(g) aumenta con la presin D) (Falso) Si la solvatacin es exotrmica, el soluto es ms soluble a temperaturas bajas.
ro s
Z. c
= (100+20) L = 120 L 37. I.
Rpta. C Rpta. E Verdadero Los nanotubos de carbono poseen ms resistencia a la ruptura que el acero y son ms ligeros. II. Verdadero La nanotecnologa ha creado materiales que disminuyen costos y aumentan la eficiencia. 40. IA ! K IIA Mg Ca
(Total) Entonces: Vaire ------ 100% 0 Vaire =120 L . VO
2
100% =571 L 21%
----- 21% Rpta. E
E) (Falso) La solubilidad de slidos no es afectada por la presin atmosfrica Rpta. B
(Total)
- 21 -
- 22 -
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
CENTRO DE ESTUDIO PITGORAS
EXAMEN DE ADMISIN 2012-I
UNIVERSIDAD NACIONAL DE INGENIERA
I. Falso Orden decreciente de la primera energa de ionizacin (EI): EIMg > EICa > EIK II. Falso Orden decreciente del radio atmico (r): rK > rCa > rMg III. Verdadero El magnesio es el ms electronegativo. Rpta. C
UNIVERSIDAD NACIONAL DE INGENIERA
- 23 -
w .L
ib
ro s
Z. c
om
- 24 -
Vous aimerez peut-être aussi
- Simulacro de Letras.Document6 pagesSimulacro de Letras.loqueno1598740Pas encore d'évaluation
- 2do Seminario FísicaDocument7 pages2do Seminario FísicaCarlos AvalosPas encore d'évaluation
- Examen de admisión UNI 2010: Resolución de problemas de Física, Química y MatemáticasDocument27 pagesExamen de admisión UNI 2010: Resolución de problemas de Física, Química y MatemáticasJuan AguilarPas encore d'évaluation
- Solucionario Fisica y Quimica - Admision UNI 2011-2 - TrilceDocument23 pagesSolucionario Fisica y Quimica - Admision UNI 2011-2 - TrilceRubensaiD0% (2)
- Fisica Eliminatoria AnfeiDocument8 pagesFisica Eliminatoria AnfeiJorge VillalobosPas encore d'évaluation
- Examen Uni de FisIca Quimica 2010 2 - Por La Academia PamerDocument20 pagesExamen Uni de FisIca Quimica 2010 2 - Por La Academia Pamer1MONOGRAFIASPas encore d'évaluation
- Simulacro ListoDocument8 pagesSimulacro Listounicito22Pas encore d'évaluation
- 1º Global-1Document10 pages1º Global-1Gianina Di GiacomoPas encore d'évaluation
- Examen 4 de Matemáticas y CienciasDocument12 pagesExamen 4 de Matemáticas y CienciasMaster x07Pas encore d'évaluation
- Eliminatoria Física 6CCBDocument7 pagesEliminatoria Física 6CCBAlfonso IbarraPas encore d'évaluation
- Examen FísicaDocument3 pagesExamen FísicaJOSE FREDDI SAAVEDRA BAYONAPas encore d'évaluation
- Nuestras Redes: InformesDocument15 pagesNuestras Redes: InformesRosa Valdez GonzalesPas encore d'évaluation
- Maratón Física - 12 de MarzoDocument10 pagesMaratón Física - 12 de Marzocristian huarcayaPas encore d'évaluation
- Simulacro 02 Física QuímicaDocument10 pagesSimulacro 02 Física QuímicaYuleimy LucasPas encore d'évaluation
- FísicaDocument8 pagesFísicaLois MendesPas encore d'évaluation
- Fisica Dynamic 2019-IDocument4 pagesFisica Dynamic 2019-ISol TapullimaPas encore d'évaluation
- Las Fijas - FísicaDocument8 pagesLas Fijas - FísicaAdolfo AdolfoPas encore d'évaluation
- Fisica Ord Suplente ExamenDocument2 pagesFisica Ord Suplente ExamenManuel Eslava ValeraPas encore d'évaluation
- Exámenes 2015 - I PDFDocument6 pagesExámenes 2015 - I PDFMaria AquisePas encore d'évaluation
- Cuarto Simulacro de Examen de Admision Universidad Nacional de Ingenieria Ciclo Semestral UNI - 2012 Fisica y QuimicaDocument6 pagesCuarto Simulacro de Examen de Admision Universidad Nacional de Ingenieria Ciclo Semestral UNI - 2012 Fisica y QuimicaHeyner Oswaldo Salvador GonzaPas encore d'évaluation
- REPASO 2do PARCIAL 2022-1Document2 pagesREPASO 2do PARCIAL 2022-1Luis Carlos Bonilla AldanaPas encore d'évaluation
- FÍSICADocument10 pagesFÍSICAJOSE FREDDI SAAVEDRA BAYONAPas encore d'évaluation
- Cuestionario de repaso Unidad 4 2do BGU Área de Matemática y FísicaDocument10 pagesCuestionario de repaso Unidad 4 2do BGU Área de Matemática y FísicaBrigitte BarreraPas encore d'évaluation
- Banco de Preguntas de Fisica y Quimica de La UnpDocument6 pagesBanco de Preguntas de Fisica y Quimica de La UnpIsabel Palacios Nole100% (1)
- 02energia 130828150519 Phpapp01 PDFDocument6 pages02energia 130828150519 Phpapp01 PDFWalter Silva SerranoPas encore d'évaluation
- Olimpiada Online de Física 2015Document13 pagesOlimpiada Online de Física 2015orlan2_rPas encore d'évaluation
- Impreso Fisica Extra Titular ExamenDocument2 pagesImpreso Fisica Extra Titular ExamenManuel Eslava ValeraPas encore d'évaluation
- 2 Fisica Guia DominaDocument17 pages2 Fisica Guia DominaI.q. FernandezPas encore d'évaluation
- Fijas 2022Document5 pagesFijas 2022Hongito Hongito HhongitoPas encore d'évaluation
- Impreso Fisica Ord Titular ExamenDocument2 pagesImpreso Fisica Ord Titular ExamenManuel Eslava ValeraPas encore d'évaluation
- Final de Física IDocument1 pageFinal de Física ICarlos CalderazoPas encore d'évaluation
- Solucionario Fisica y Quimica - Admision UNI 2011-2 - PamerDocument21 pagesSolucionario Fisica y Quimica - Admision UNI 2011-2 - PamerRubensaiDPas encore d'évaluation
- Enunciados Examenes Selectividad Fisica Andalucia 2002-2013Document145 pagesEnunciados Examenes Selectividad Fisica Andalucia 2002-2013Clases Particulares Online Matematicas Fisica Quimica100% (2)
- Examen de Fisica-Oct2014Document7 pagesExamen de Fisica-Oct2014Luis Alberto Mendoza SalasPas encore d'évaluation
- FISICADocument7 pagesFISICAMichell Quiroz OlivaresPas encore d'évaluation
- Practica Fis99Document23 pagesPractica Fis99Frank Ragnar Cayllagua0% (2)
- Primer Parcial de Fisica 1 Años 1997 A 2019Document137 pagesPrimer Parcial de Fisica 1 Años 1997 A 2019alejandro gonsalezPas encore d'évaluation
- Repasito 25 Oct - FísicaDocument2 pagesRepasito 25 Oct - FísicaoberhPas encore d'évaluation
- Ondas MecánicasDocument8 pagesOndas MecánicasJaime Angel Ortiz DiazPas encore d'évaluation
- Análisis de pruebas de pulso isotérmicas y reacciones químicasDocument2 pagesAnálisis de pruebas de pulso isotérmicas y reacciones químicascaroPas encore d'évaluation
- Examen Diagnóstico. Módulo 8. Ingenierías Y Tecnologías: MatemáticasDocument23 pagesExamen Diagnóstico. Módulo 8. Ingenierías Y Tecnologías: MatemáticasMafer VazquezPas encore d'évaluation
- Exámenes Física - A y BDocument2 pagesExámenes Física - A y B123rtsPas encore d'évaluation
- 2º Examen Test - 22 - 23 - IE - IM11 - 13 - ModA - ResolucionDocument7 pages2º Examen Test - 22 - 23 - IE - IM11 - 13 - ModA - ResolucionMarta Sanz CerroPas encore d'évaluation
- Examen 2 de Matemáticas y CienciasDocument10 pagesExamen 2 de Matemáticas y CienciasMaster x07Pas encore d'évaluation
- Agm - Fisica 2022 - Enunciado - Descargas - Academia PitagorasDocument11 pagesAgm - Fisica 2022 - Enunciado - Descargas - Academia Pitagorassafemahuro9795Pas encore d'évaluation
- 2004-2005OFisica PSeleccion 2004-05Document4 pages2004-2005OFisica PSeleccion 2004-05Pau Sabater NácherPas encore d'évaluation
- 02 Uni 2022 Ii Tercera Prueba Solucionario Admisión Universidad Ingeniería Física Química 2022-2 PDFDocument6 pages02 Uni 2022 Ii Tercera Prueba Solucionario Admisión Universidad Ingeniería Física Química 2022-2 PDFvez siaPas encore d'évaluation
- Fisica - Niv 1 RDocument6 pagesFisica - Niv 1 RyamsPas encore d'évaluation
- Física tercer grado tareasDocument7 pagesFísica tercer grado tareasMichell Quiroz OlivaresPas encore d'évaluation
- EXAMEN DE RECUPERACIÓN DE 4TO GRADO I. E. Pr. CIENCIAS 1Document2 pagesEXAMEN DE RECUPERACIÓN DE 4TO GRADO I. E. Pr. CIENCIAS 1yover.julian.16Pas encore d'évaluation
- Banco 1Document44 pagesBanco 1Sergio GalánPas encore d'évaluation
- Ingeniería química. Soluciones a los problemas del tomo ID'EverandIngeniería química. Soluciones a los problemas del tomo IPas encore d'évaluation
- Problemas resueltos de Hidráulica de CanalesD'EverandProblemas resueltos de Hidráulica de CanalesÉvaluation : 4.5 sur 5 étoiles4.5/5 (7)
- Experiencias sobre circuitos eléctricos en serie operados por corriente directaD'EverandExperiencias sobre circuitos eléctricos en serie operados por corriente directaPas encore d'évaluation
- Caracterización química, morfológica y estructural de materialesD'EverandCaracterización química, morfológica y estructural de materialesPas encore d'évaluation
- Fucsina ÁcidaDocument1 pageFucsina ÁcidaChelvis REPas encore d'évaluation
- Diapos de Ortorrombico - UncpDocument23 pagesDiapos de Ortorrombico - UncpChelvis REPas encore d'évaluation
- Inforde de GestionDocument6 pagesInforde de GestionChelvis REPas encore d'évaluation
- Diapos de Ortorrombico - UncpDocument1 pageDiapos de Ortorrombico - UncpChelvis REPas encore d'évaluation
- Instalacionesporcinas 100727191502 Phpapp02Document80 pagesInstalacionesporcinas 100727191502 Phpapp02Chelvis REPas encore d'évaluation
- LaboratorioDocument11 pagesLaboratorioChelvis REPas encore d'évaluation
- JoseDocument2 pagesJoseChelvis REPas encore d'évaluation
- Instalacionesyequipoaves 130619140432 Phpapp02Document32 pagesInstalacionesyequipoaves 130619140432 Phpapp02Anonymous Yeut3wFVbPas encore d'évaluation
- Hola CompañeroDocument1 pageHola CompañeroChelvis REPas encore d'évaluation
- Plan Curricular 2013 Carrera Profesional Ing. QuimicaDocument57 pagesPlan Curricular 2013 Carrera Profesional Ing. QuimicaChelvis REPas encore d'évaluation
- La BocaDocument1 pageLa BocaChelvis REPas encore d'évaluation
- Romero ACEITEDocument37 pagesRomero ACEITEChelvis REPas encore d'évaluation
- BÁSQUETBOLDocument5 pagesBÁSQUETBOLChelvis REPas encore d'évaluation
- MolleDocument6 pagesMolleChelvis RE100% (2)
- Dinamica LiderazgoDocument1 pageDinamica LiderazgoChelvis REPas encore d'évaluation
- Francisco Núñez de Pineda y BascuñánDocument5 pagesFrancisco Núñez de Pineda y BascuñánChelvis REPas encore d'évaluation
- Dinamica CreatividadDocument1 pageDinamica CreatividadChelvis REPas encore d'évaluation
- 2010 II 04 TermoquimicaDocument47 pages2010 II 04 TermoquimicamirazelPas encore d'évaluation
- Ley UniversitariaDocument60 pagesLey UniversitariaRider Bendezú100% (2)
- 2010 II 02 Gas RealDocument63 pages2010 II 02 Gas RealChelvis REPas encore d'évaluation
- GraficaelementosparabolaDocument4 pagesGraficaelementosparabolamelind1616Pas encore d'évaluation
- Boletin de Ingenieria OkDocument3 pagesBoletin de Ingenieria OkChelvis REPas encore d'évaluation
- Manrique Palomino Ingrit EP IndustrialDocument24 pagesManrique Palomino Ingrit EP IndustrialChelvis REPas encore d'évaluation
- 2010 II 03 Primera LeyDocument40 pages2010 II 03 Primera LeyChelvis REPas encore d'évaluation
- Francisco Núñez de Pineda y BascuñánDocument5 pagesFrancisco Núñez de Pineda y BascuñánChelvis REPas encore d'évaluation
- El Atomo y La Estructura AtomicaDocument39 pagesEl Atomo y La Estructura Atomicakrentv16Pas encore d'évaluation
- Estructura y Propiedades D Ela Molecula.2011Document38 pagesEstructura y Propiedades D Ela Molecula.2011Chelvis REPas encore d'évaluation
- Cálculo Del EpicentroDocument3 pagesCálculo Del EpicentroRoly_RootsPas encore d'évaluation
- Algebra Lineal 2D FIQDocument4 pagesAlgebra Lineal 2D FIQChelvis REPas encore d'évaluation
- El Por QuéDocument2 pagesEl Por QuéChelvis REPas encore d'évaluation
- Reglamento de Tenencia de MascotasDocument11 pagesReglamento de Tenencia de Mascotasdiego cusapaz limaPas encore d'évaluation
- Endo Toxin ADocument64 pagesEndo Toxin ARocìoCruzRodríguez100% (1)
- Otitis Causada Por NeumococoDocument1 pageOtitis Causada Por Neumococoleidy camachoPas encore d'évaluation
- Las Diátesis HemorrágicasDocument4 pagesLas Diátesis HemorrágicasDanellys GutierrezPas encore d'évaluation
- Fase 1 Reconocimiento - Contextualización de La Psicología Organizacional - Elizabet AriasDocument6 pagesFase 1 Reconocimiento - Contextualización de La Psicología Organizacional - Elizabet Ariaselizabeth ariasPas encore d'évaluation
- INFORME 4 - Intro, Conclu y ObsDocument4 pagesINFORME 4 - Intro, Conclu y ObsJhon Angel Salcedo AgueroPas encore d'évaluation
- Maratón Escolar MargosDocument4 pagesMaratón Escolar MargosAmador Coz TuctoPas encore d'évaluation
- Declaración Jurada de Recepción de Bienes-AclaraciónDocument4 pagesDeclaración Jurada de Recepción de Bienes-AclaraciónDayana Aduviri SucapucaPas encore d'évaluation
- Cuadro Etapas Desarrollo PDFDocument4 pagesCuadro Etapas Desarrollo PDFGisela Montaño LudusPas encore d'évaluation
- Examenes Psicologia EducativaDocument44 pagesExamenes Psicologia EducativanatalyPas encore d'évaluation
- Pañalera EmilyDocument9 pagesPañalera EmilyalfonsoPas encore d'évaluation
- Condicionamiento clásico vs operante: diferencias y aplicacionesDocument10 pagesCondicionamiento clásico vs operante: diferencias y aplicacionesElder ArroyoPas encore d'évaluation
- Pollo RostizadoDocument1 pagePollo RostizadoDaniel Quezada VaraPas encore d'évaluation
- Comprensión LectoraDocument32 pagesComprensión LectoraPryscilla Ugas WisnarPas encore d'évaluation
- Lienzo Propuesta de ValorDocument1 pageLienzo Propuesta de ValorGanaderia OpPas encore d'évaluation
- Ejercicio CostosDocument10 pagesEjercicio CostosJennifer Lilian Cañon RodriguezPas encore d'évaluation
- All Pet Food Magazine Julio 2021Document48 pagesAll Pet Food Magazine Julio 2021juraguimaPas encore d'évaluation
- Como Si Estuvieran ComprandoDocument27 pagesComo Si Estuvieran ComprandoLeonardo CardenasPas encore d'évaluation
- Resumen de Capitulos Del Libro Tus Zonas Erroneas - Williams Tixe UrsuaDocument8 pagesResumen de Capitulos Del Libro Tus Zonas Erroneas - Williams Tixe Ursuaemanuel tvPas encore d'évaluation
- Pre 3Document5 pagesPre 3sashaPas encore d'évaluation
- Línea Del TiempoDocument3 pagesLínea Del TiempoDiana JuarezPas encore d'évaluation
- Acta de Constitucion HNGAIDocument3 pagesActa de Constitucion HNGAITeresa QuispePas encore d'évaluation
- Ergonomia Mapa ConceptualDocument2 pagesErgonomia Mapa ConceptualSheilly Mendoza MartinPas encore d'évaluation
- 1 de Cada 3 Personas en El Mundo No Tiene Acceso Al Agua PotableDocument3 pages1 de Cada 3 Personas en El Mundo No Tiene Acceso Al Agua PotableGastón MezzettaPas encore d'évaluation
- Libro de No MetalicosDocument77 pagesLibro de No Metalicosanon_427329861Pas encore d'évaluation
- Definiciones Básicas de NutriciónDocument15 pagesDefiniciones Básicas de NutriciónMaria Jose Castillo PolancoPas encore d'évaluation
- Estudio de Modelos en Articulador New SimplexDocument10 pagesEstudio de Modelos en Articulador New SimplexDanika Quispe Humpiri100% (1)
- Verruga Eliminarlas NaturalmenteDocument9 pagesVerruga Eliminarlas NaturalmenteluluvsanPas encore d'évaluation
- Síndrome de Addison SeminarioDocument19 pagesSíndrome de Addison SeminarioCristhian Gustavo Marín CorreaPas encore d'évaluation
- Mapa Conceptual Muestreo AleatorioDocument1 pageMapa Conceptual Muestreo AleatorioJuan David Castro Correa0% (1)