Académique Documents
Professionnel Documents
Culture Documents
Balanceo de Ecuaciones Químicas
Transféré par
Denisse Guizado Cicenia0 évaluation0% ont trouvé ce document utile (0 vote)
65 vues18 pagesCopyright
© © All Rights Reserved
Formats disponibles
PPTX, PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PPTX, PDF, TXT ou lisez en ligne sur Scribd
0 évaluation0% ont trouvé ce document utile (0 vote)
65 vues18 pagesBalanceo de Ecuaciones Químicas
Transféré par
Denisse Guizado CiceniaDroits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PPTX, PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 18
Es anteponer coeficientes a las frmulas,
para tener cantidades iguales de tomos
de un mismo tipo entre los reactivos y los
productos.
Las principales son:
Por tanteo o inspeccin, y Mtodos de las
ecuaciones Redox
Balanceo de ecuaciones qumicas
La palabra Redox proviene de la unin de
las abreviaturas reduccin y oxidacin.
El mtodo Redox se lo utiliza para igualar
ecuaciones complejas.
Se consideran de dos tipos:
a) Mtodo del intercambio del nmero de
Oxidacin
b) Mtodo del in electrn
Balanceo de ecuaciones qumicas
MTODO DE LAS ECUACIONES REDOX
a) Precisar N de oxidacin en reactivos y
productos; escribirlos sobre c/elemento e
identificar los que sufren cambios.
b) Vincular los elementos que aumentan y
disminuyen su nmero de oxidacin;
c) Anotar, el que aumenta como oxidacin;
y, el que disminuye como reduccin,
Balanceo de ecuaciones qumicas
MTODO DEL INTERCAMBIO DEL NMERO
DE OXIDACIN
d) Determinar factores que al multiplicar los
nmeros hallados de oxidacin y
reduccin, proporcionen una igualdad. El
nmero de electrones ganados debe ser
igual al nmero de electrones perdidos.
e) Ubicar los coeficientes frente a las
frmulas implicadas y complete el
balanceo por tanteo.
Balanceo de ecuaciones qumicas
MTODO DEL INTERCAMBIO DEL NMERO
DE OXIDACIN
6+ 5+ 4+ 3+ 2+ 1+ 0 1- 2- 3- 4- 5- 6-
O x id a c i n
R
e d uc ci n
Balanceo de ecuaciones qumicas
MTODO DEL INTERCAMBIO DEL NMERO
DE OXIDACIN
oxida en 5, porque el N pasa de 3 a +2, ( = 5);
N
H
3
+ O
2
N O + H
2
O
Balancear la siguiente ecuacin:
NH
3
+ O
2
NO + H
2
O
Ejemplo 1
-3
0
+2
-2
-2
oxida 5
reduce 2 x 2 = 4
4
5
oxida en 5, porque el N pasa de 3 a +2, ( = 5);
N
H
3
+ O
2
N O + H
2
O
Balancear la siguiente ecuacin:
NH
3
+ O
2
NO + H
2
O
Ejemplo 1
Con tanteo, terminamos de balancear la ecuacin
Obtenemos: 4NH
3
+ 5O
2
0
4NO + 5H
2
O;
4NH
3
+ 5O
2
4NO + 6H
2
O
4
5
-3
0
+2
-2
-2
oxida 5
reduce 2 x 2 = 4
reduce 4, de 0 a 2 = 2, y como son 2; 2 x 2 = 4
4 x 5 = 20 5 x 4 = 20
20 = 20
oxida reduce
4 5
2
3
K Cl O
3
+ C
K Cl + C O
2
Balancear la siguiente ecuacin:
KClO
3
+ C KCl + CO
2
Ejemplo 2
2
3
+1 +5 -2
0 +1 -1
+4
-2
reduce 6
oxida 4
2 3
2
3
H N O
3
+ H
2
S
N O + S + H
2
O
Balancear la siguiente ecuacin:
HNO
3
+ H
2
S NO + S + H
2
O
Ejemplo 3
2
3
+1 +5 -2
+1 -2 +2 -2
0
+1 -2
reduce 3
oxida 2
2 3 4
2HNO
3
+ 3H
2
S 2NO + 3S + 4H
2
O
6
1
K
2
Cr
2
O
7
+ Fe Cl
2
+ H Cl
Cr Cl
3
+ K Cl + Fe Cl
3
+ H
2
O
Balancear la siguiente ecuacin:
K
2
Cr
2
O
7
+ FeCl
2
+ HCl CrCl
3
+ KCl + FeCl
3
+ H
2
O
Ejemplo 4
6
1
+1 +6 -2 +2 -1 +1 -1 +3 -1 +1 -1 +3 -1 +1 -2
oxida 1
reduce 3
6 1 2
x 2 = 6
2 14 7
K
2
Cr
2
O
7
+ 6FeCl
2
+ 14HCl 2CrCl
3
+ 2KCl + 6FeCl
3
+ 7H
2
O
2
5
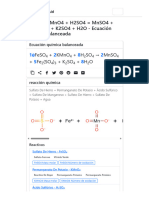
Balancear la siguiente ecuacin:
FeSO
4
+ KMnO
4
+ H
2
SO
4
Fe
2
(SO
4
)
3
+ MnSO
4
+ K
2
SO
4
+ H
2
O
Ejercicio
2
5
+2 +6 -2 +7 -2 +1 +6 -2 +3 +2 +6 -2 +1+6 -2 +1 -2
oxida 1
reduce 5
2 5
x 2 = 2
2
8 8
K
2
Cr
2
O
7
+ 6FeCl
2
+ 14HCl 2CrCl
3
+ 2KCl + 6FeCl
3
+ 7H
2
O
Fe S O
4
+ K Mn O
4
+ H
2
S O
4
Fe
2
(SO
4
)
3
+ Mn S O
4
+ K
2
SO
4
+ H
2
O
10
Es aplicable a reacciones con
especies inicas (tambin se pueden
transformar las especies moleculares
a iones), y se utilizan ecuaciones
parciales, una que exprese oxidacin
y la otra reduccin.
Balanceo de ecuaciones qumicas
MTODO DEL IN ELECTRN
Balanceo de ecuaciones qumicas
MTODO DEL IN ELECTRN
Ejemplo 1
NaI + Fe
2
(SO
4
)
3
I
2
+ FeSO
4
+ Na
2
SO
4
a) Transformar la ecuacin en forma
inica (si no la est), y observar cules son
los elementos que cambian su nmero de
oxidacin:
Na
1+
+ I
1-
+ Fe
2
3+
I
2
+ Fe
2+
+ Na
1+
Balanceo de ecuaciones qumicas
MTODO DEL IN ELECTRN
Ejemplo 1
b) Construir 2 semi-reacciones con
los iones de la ecuacin; una semi-
reaccin de oxidacin, y otra semi-
reaccin de reduccin.
Na
1+
+ I
1-
+ Fe
2
3+
I
2
+ Fe
2+
+ Na
1+
I
1-
I
2
Fe
2
3+
Fe
2+
semi-reaccin de oxidacin
semi-reaccin de reduccin
Balanceo de ecuaciones qumicas
MTODO DEL IN ELECTRN
Ejemplo 1
c) Igualar tomos de cada lado.
Na
1+
+ I
1-
+ Fe
2
3+
I
2
+ Fe
2+
+ Na
1+
I
1-
I
2
Fe
2
3+
Fe
2+
semi-reaccin de oxidacin
semi-reaccin de reduccin
2
Agregar
H
2
O por falta de O
2
en un lado, y en el
otro, H
+
, para soluciones cidas.
En
bsicas, se agrega OH
-
por falta de O
2
.
contrarrestando en el otro lado con H
2
O.
2
Balanceo de ecuaciones qumicas
MTODO DEL IN ELECTRN
Ejemplo 1
c) Igualar las cargas agregando e
-
en las
2 semi-ecuaciones
Na
1+
+ I
1-
+ Fe
3+
I
2
+ Fe
2+
+ Na
1+
I
1-
I
2
Fe
2
3+
Fe
2+
de oxidacin
de reduccin
2 + 2e
-
+ 2e
-
y multiplique cada
ecuacin por un nmero que iguale las
cantidades de electrones en las 2
ecuaciones.
2
Balanceo de ecuaciones qumicas
MTODO DEL IN ELECTRN
Ejemplo 1
Na
1+
+ I
1-
+ Fe
2
3+
I
2
+ Fe
2+
+ Na
1+
I
1-
I
2
Fe
2
3+
Fe
2+
de oxidacin
de reduccin
2 + 2e
-
+ 2e
-
2
e) Sumar las dos ecuaciones parciales,
y simplifique las especies iguales que
estn en cada lado de la ecuacin total:
Balanceo de ecuaciones qumicas
MTODO DEL IN ELECTRN
Ejemplo 1
Na
1+
+ I
1-
+ Fe
2
3+
I
2
+ Fe
2+
+ Na
1+
I
1-
I
2
Fe
2
3+
Fe
2+
de oxidacin
de reduccin
2
2
Obteniendo:
2I
1-
+ Fe
2
3+
I
2
+ 2Fe
2+
Na
1+
+ 2I
1-
+ Fe
2
3+
I
2
+ 2Fe
2+
+ Na
1+
2NaI + Fe
2
(SO
4
)
3
I
2
+ 2FeSO
4
+ Na
2
SO
4
Transformando a ecuacin molecular, tenemos:
Vous aimerez peut-être aussi
- Balanceo de Ecuaciones Quimicas.Document10 pagesBalanceo de Ecuaciones Quimicas.lol coitaPas encore d'évaluation
- Balanceo RedoxDocument17 pagesBalanceo RedoxSantiago MacettoPas encore d'évaluation
- Nomenclatura - Binarios ModificadoDocument18 pagesNomenclatura - Binarios ModificadoAmy Rodriguez ReyesPas encore d'évaluation
- Taller Balanceo de Ecuaciones Clei 5Document1 pageTaller Balanceo de Ecuaciones Clei 5marinati660% (1)
- Nomenclatura InorganicaDocument2 pagesNomenclatura InorganicaAndrea MadridPas encore d'évaluation
- RedoxDocument10 pagesRedoxprofesor manuelPas encore d'évaluation
- Balanceo Ión Electrón en Medio AcidoDocument7 pagesBalanceo Ión Electrón en Medio AcidoFrancis Drake Fernandez CastroPas encore d'évaluation
- GUIA No 2 VALENCIA Y NUMEROS DE OXIDACIONDocument3 pagesGUIA No 2 VALENCIA Y NUMEROS DE OXIDACIONJenniferSolartePas encore d'évaluation
- Valencia y Número de OxidaciónDocument6 pagesValencia y Número de OxidaciónLuz AnitaPas encore d'évaluation
- FeSO4 + KMnO4 + H2SO4 MnSO4 + Fe2 (SO4) 3 + K2SO4 + H2O - Ecuación Química BalanceadaDocument5 pagesFeSO4 + KMnO4 + H2SO4 MnSO4 + Fe2 (SO4) 3 + K2SO4 + H2O - Ecuación Química BalanceadaGontanjimT.JiménezPas encore d'évaluation
- Tabla de Electronegatividad de Los ElementosDocument3 pagesTabla de Electronegatividad de Los ElementosCesar Garrido100% (1)
- Reacciones REDOXDocument73 pagesReacciones REDOXingrriPas encore d'évaluation
- 3°electivo - PPT N°1 Redox (7485)Document28 pages3°electivo - PPT N°1 Redox (7485)profesora María Antonieta TorresPas encore d'évaluation
- Números Cuánticos y Configuración ElectrónicaDocument46 pagesNúmeros Cuánticos y Configuración ElectrónicaJenny Castro JaraPas encore d'évaluation
- Puestos Organicos e InorganicosDocument26 pagesPuestos Organicos e InorganicosKENNIERT BARENO SALCEDOPas encore d'évaluation
- REDOX 6A EjercicioDocument2 pagesREDOX 6A EjercicioJ.R. OlveraPas encore d'évaluation
- Una Fiesta Muy Elemental PDFDocument2 pagesUna Fiesta Muy Elemental PDFKatherine Martínez RodríguezPas encore d'évaluation
- Hid Roxi DosDocument5 pagesHid Roxi DosjosePas encore d'évaluation
- Números de OxidaciónDocument2 pagesNúmeros de OxidaciónFrancisco MartínezPas encore d'évaluation
- Ejercicios de AromáticosDocument5 pagesEjercicios de AromáticosJuan AguilarPas encore d'évaluation
- Clase de Ácidos CarboxílicosDocument47 pagesClase de Ácidos CarboxílicosJuan Wilfredo Hernandez DiazPas encore d'évaluation
- Química Secundaria.Document8 pagesQuímica Secundaria.AbiRuizArevaloPas encore d'évaluation
- Presentacion SolubilidadDocument36 pagesPresentacion Solubilidadyho nnyPas encore d'évaluation
- Estructuras de Lewuis Con Cargas Formales.Document6 pagesEstructuras de Lewuis Con Cargas Formales.Zyanya MendozaPas encore d'évaluation
- Hidrocarburos Aromaticos CloradosDocument15 pagesHidrocarburos Aromaticos Cloradosjorge armando serrano valetaPas encore d'évaluation
- Taller Nomenclatura 2019Document8 pagesTaller Nomenclatura 2019Vanessa Velandia ÁvilaPas encore d'évaluation
- Números de Oxidación y Electrones de ValenciaDocument15 pagesNúmeros de Oxidación y Electrones de ValenciaPilar Inga Solórzano100% (1)
- Prueba de NomenclaturaDocument2 pagesPrueba de NomenclaturaRoquePas encore d'évaluation
- Tabla de Cationes y AnionesDocument1 pageTabla de Cationes y AnionesTomas Cardona Canul50% (2)
- Números de OxidaciónDocument15 pagesNúmeros de OxidaciónMariana Soto50% (2)
- 1 Nomenclatura Organica AlcanosDocument29 pages1 Nomenclatura Organica AlcanosLiz Jaime100% (1)
- Parcial 1 PDFDocument3 pagesParcial 1 PDFAndres Serna100% (1)
- 63 A 71 Con Tabla OxisalesDocument2 pages63 A 71 Con Tabla OxisalesDanna GarcíaPas encore d'évaluation
- ÓxidosDocument7 pagesÓxidosOscar Reluz MuroPas encore d'évaluation
- Ejercicios de PreEntrenamiento - QI - IChO 2022Document24 pagesEjercicios de PreEntrenamiento - QI - IChO 2022Peti CicchePas encore d'évaluation
- Alcholes y FenolesDocument21 pagesAlcholes y FenolesmarcoPas encore d'évaluation
- Alcanos, Alquenos, Alquinos Propiedades FisicasDocument11 pagesAlcanos, Alquenos, Alquinos Propiedades Fisicasparatodox50% (2)
- PH TeoriaDocument7 pagesPH Teoriaklissman Alvarado garciaPas encore d'évaluation
- Taller Reacciones Quimicas OrganicasDocument1 pageTaller Reacciones Quimicas OrganicasMaicol MedinaPas encore d'évaluation
- Que Pasa Cunado Chocan Los Atomos ActividadDocument6 pagesQue Pasa Cunado Chocan Los Atomos ActividadHumberto CortezPas encore d'évaluation
- Aniones y CationesDocument4 pagesAniones y CationesYilmar Banquez LastrePas encore d'évaluation
- Oxianiones 97Document52 pagesOxianiones 97Mariana RojasPas encore d'évaluation
- Ejercicios de Estructura AtomicaDocument13 pagesEjercicios de Estructura AtomicaRogers M Gonzalez U100% (1)
- Ejercicios de Compuestos QuímicosDocument3 pagesEjercicios de Compuestos QuímicosPorque Callar Cuando Nací GritandoPas encore d'évaluation
- Experiencias de GlúcidosDocument47 pagesExperiencias de GlúcidosCarlos Alfredo López0% (1)
- Propiedades Periodicos - ProfDocument44 pagesPropiedades Periodicos - ProfOxana ShtefanPas encore d'évaluation
- Mentaberry 1 Introduccion A La Biotecnologia PDFDocument67 pagesMentaberry 1 Introduccion A La Biotecnologia PDFVerushka Milagros Farfan GiraldesPas encore d'évaluation
- Deber de EnlacesDocument4 pagesDeber de EnlacesaatapiaPas encore d'évaluation
- Ecuacion Quimica y Su Simbologia - Balanceo de Ecuaciones QuimicasDocument32 pagesEcuacion Quimica y Su Simbologia - Balanceo de Ecuaciones Quimicaskarelys ortegaPas encore d'évaluation
- Banco de Preguntas de Quimica de SecundariaDocument4 pagesBanco de Preguntas de Quimica de SecundariaJhon Kenneth Panduro100% (1)
- Reactivo Limitante y e ExcesoDocument4 pagesReactivo Limitante y e ExcesoMartin CrispinoPas encore d'évaluation
- Reacciones EndotermicasDocument1 pageReacciones EndotermicasSocorro Arcelia Cordero Cruz100% (1)
- Taller Enlaces - Números de Oxidación 8º 2020 Semana 3 Julio PDFDocument4 pagesTaller Enlaces - Números de Oxidación 8º 2020 Semana 3 Julio PDFJuan José MontesPas encore d'évaluation
- Nomenclatura Quimica Inorganica 2019Document26 pagesNomenclatura Quimica Inorganica 2019Nubia Patricia Parada Rivera100% (1)
- Estructura-Atómica EjerciciosDocument2 pagesEstructura-Atómica EjerciciosDixi PixiPas encore d'évaluation
- Eteres Epoxidos y SulfurosDocument31 pagesEteres Epoxidos y SulfurosCarlos Torres VelaPas encore d'évaluation
- Evaluacion Estequiometria Grado Once Iete de 2016Document5 pagesEvaluacion Estequiometria Grado Once Iete de 2016Diana Carolina Burbano RuanoPas encore d'évaluation
- Hoja de Trabajo No. 1 Química OrgánicaDocument1 pageHoja de Trabajo No. 1 Química OrgánicaajumayenaPas encore d'évaluation
- Balance ReaccionesDocument5 pagesBalance ReaccionesDiego Fernando Ramos Acevedo0% (1)
- Reacciones y Ecuaciones QuimicasDocument4 pagesReacciones y Ecuaciones QuimicasLudovikPas encore d'évaluation
- Capítulo 104Document22 pagesCapítulo 104Frank Huingo TelloPas encore d'évaluation
- Factores Físicos y Psíquicos, y Componentes Del Sistema de La Memoria.Document1 pageFactores Físicos y Psíquicos, y Componentes Del Sistema de La Memoria.Adriana RodriguezPas encore d'évaluation
- CirugiaDocument28 pagesCirugiaDanika KitschPas encore d'évaluation
- Bolivia Perfil Pollos A La Brasa PDFDocument65 pagesBolivia Perfil Pollos A La Brasa PDFGaboi7 Casti100% (1)
- 4-Formula Minima - MolecularDocument25 pages4-Formula Minima - MoleculardrlucioPas encore d'évaluation
- Trastornos Hemodinamicos CR TestDocument207 pagesTrastornos Hemodinamicos CR TestJose Benito Guevara Conrado100% (1)
- Fabricación de Cables de CobreDocument2 pagesFabricación de Cables de CobreEduardo RomeroPas encore d'évaluation
- Cruz Velarde, Jesus PDFDocument55 pagesCruz Velarde, Jesus PDFAndi Soto PozoPas encore d'évaluation
- Triptico RespiraciónDocument2 pagesTriptico RespiraciónAnly MendozaPas encore d'évaluation
- HT 5227XX GUARD TANK STRUCTURAL ALUMINIUM (EID-187 V.02) 1.pdf FICHA TECNICADocument2 pagesHT 5227XX GUARD TANK STRUCTURAL ALUMINIUM (EID-187 V.02) 1.pdf FICHA TECNICADennis MendozaPas encore d'évaluation
- Mapa de Articuladores y RCDocument1 pageMapa de Articuladores y RCIxcell Treminio100% (1)
- CARBOHIDRATOSDocument19 pagesCARBOHIDRATOSRamírez Gerardo Andrea LizbethPas encore d'évaluation
- Proceso Enfermero - Campo Clinico - QuirurgicaDocument13 pagesProceso Enfermero - Campo Clinico - Quirurgicagostrider720Pas encore d'évaluation
- Español Anaesthesia - 2018 - Nimmo - Guidelines For The Safe Practice of Total Intravenous Anaesthesia TIVA - En.esDocument14 pagesEspañol Anaesthesia - 2018 - Nimmo - Guidelines For The Safe Practice of Total Intravenous Anaesthesia TIVA - En.esDominik Chirito PastorPas encore d'évaluation
- Artropofauna de La Necromasa E. GrandifloraDocument10 pagesArtropofauna de La Necromasa E. GrandifloraOscar ZaratePas encore d'évaluation
- Practica Laboratorio 3 Anatomia y Morfologia VegetalDocument23 pagesPractica Laboratorio 3 Anatomia y Morfologia VegetalFredy MauricioPas encore d'évaluation
- Cuadro Médico Adeslas MUFACE PontevedraDocument132 pagesCuadro Médico Adeslas MUFACE PontevedraJose PradoPas encore d'évaluation
- Check List - Levantamiento SernageominDocument4 pagesCheck List - Levantamiento SernageominCristian Gonzalo Yaupe SilvaPas encore d'évaluation
- Aportes A La Biologia CientificosDocument12 pagesAportes A La Biologia CientificosPedro MartinezPas encore d'évaluation
- Morfologia Cacao y PapayaDocument4 pagesMorfologia Cacao y PapayaDiego MartinezPas encore d'évaluation
- Accidentes Tránsito 2021Document9 pagesAccidentes Tránsito 2021bren alvaPas encore d'évaluation
- DE044934Document6 pagesDE044934Jc FloresPas encore d'évaluation
- Analisis Bromatologico de FrutasDocument14 pagesAnalisis Bromatologico de Frutasolivera100% (1)
- La Paidofilia o PedofiliaDocument4 pagesLa Paidofilia o PedofiliaGiovana Marissa Suca Benites100% (2)
- Calendario Mano de ObraDocument1 pageCalendario Mano de ObraJOSE VENTURA ANGELESPas encore d'évaluation
- Forceps DentalesDocument26 pagesForceps DentalesKenya HerreraPas encore d'évaluation
- Guia Etica 3Document4 pagesGuia Etica 3ricardo torresPas encore d'évaluation
- Concepto de Intemperismo y ErosiónDocument3 pagesConcepto de Intemperismo y ErosiónSaúl NavaPas encore d'évaluation
- Resumen y Abstract AguasDocument2 pagesResumen y Abstract AguasVictor MaldonadoPas encore d'évaluation
- Superconductores - Efecto MeissnerDocument3 pagesSuperconductores - Efecto MeissnerSergio FlorezPas encore d'évaluation