Académique Documents
Professionnel Documents
Culture Documents
Material de Estudio (Parte 1)
Transféré par
Alejandra Anahí Recalde Monar0 évaluation0% ont trouvé ce document utile (0 vote)
65 vues10 pagesquimica
Copyright
© © All Rights Reserved
Formats disponibles
PPTX, PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentquimica
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PPTX, PDF, TXT ou lisez en ligne sur Scribd
0 évaluation0% ont trouvé ce document utile (0 vote)
65 vues10 pagesMaterial de Estudio (Parte 1)
Transféré par
Alejandra Anahí Recalde Monarquimica
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PPTX, PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 10
Material de estudio (Parte 1)
El átomo y los modelos atómicos
• Todo está hecho de átomos. Si dividimos una
Atomista
sustancia muchas veces, llegaremos a ellos.
Siglo V a.C • Las propiedades de la materia varían según como se
Leucipo y agrupen los átomos.
Demócrito • Los átomos no pueden verse porque son muy
Las
pequeños
Primeras
Teorías • Los átomos no existen. No hay límite para dividir la
Continuista
materia.
Se mantuvo • Si las partículas, llamadas átomos, no pueden verse,
vigente entonces es que no existen.
durante • Todas las sustancias están formadas por las
más de combinaciones de los 4 elementos básicos: agua, aire,
Aristóteles 2000 años tierra y fuego.
Teoría atómica de Dalton
La teoría atómica de Dalton se basa en los
siguientes enunciados:
• La materia está formada por átomos,
que son partículas indivisibles e
indestructibles.
• Todos los átomos de un mismo El modelo atómico
elemento químico son iguales en masa y de Dalton fue el
propiedades y diferentes de los átomos primer modelo
de cualquier otro elemento. atómico con bases
científicas,
• Los compuestos se forman por propuesto entre
combinaciones de átomos de diferentes 1803 y 1807 por
elementos John Dalton
Naturaleza eléctrica de la
materia Estructura atómica
Existen dos fenómenos eléctricos en la La existencia de cargas eléctricas y los
materia: atracción y repulsión. experimentos con tubos de descarga
demuestran que el átomo es divisible,
las partículas que forman el átomo son:
• Electrones: partículas con cargas
negativas.
• Protones: partículas con carga
positiva.
La carga eléctrica es una propiedad de • Neutrones: partículas sin carga.
la materia.
La masa de protones y neutrones es
Puede ser positiva (+) o negativa (-). mucho mayor que la de los electrones.
Las cargas del mismo tipo se repelen y Un átomo es neutro si tiene el mismo
las de distinto tipo se atraen. numero de protones y electrones.
Modelo de Thomson Modelo de Rutherford
El átomo es una esfera maciza de carga
positiva en la que se encuentran El átomo esta compuesto por un
incrustados pequeño núcleo central con
los protones y neutrones, en el que
electrones. se encuentra casi toda la masa del
átomo y una zona externa
(corteza) en la que los electrones
Un ion es un átomo que ha ganado o
están en continuo movimiento.
perdido uno o más electrones
electrones:
Si pierde uno o más electrones,
adquiere carga neta positiva y se
convierte en catión; si gana uno o más
electrones adquiere carga neta negativa
y se transforma en un anión.
Los electrones que están más
cerca del núcleo son los que
Modelo atómico de Bohr poseen menos energía y los que
están más lejos son los que tienen
Bohr logró en 1913 establecer un más energía.
nuevo modelo atómico donde:
1 - El electrón gira alrededor del
núcleo en un conjunto fijo de órbitas
permitidas.
2.- Los electrones viajan en niveles
predeterminados de energía.
Los electrones pueden saltar de un
nivel energético menor a uno mayor
si les proporciona energía.
Cuando los electrones regresan a su
nivel de energía estacionario, liberan
luz.
En cada nivel todos sus
electrones tienen la
Modelo mecano cuantico misma energía
Es el actual modelo: este modelo
se expuso por vez primera en
1925 por Schrodinger y
Heisenberg.
• Los electrones no tienen una
trayectoria fija.
• Los orbitales atómicos son zonas
de mayor probabilidad de
encontrar a los electrones.
• Se habla de una nube difusa de
carga electrónica
El núcleo está Los electrones casi
en el corazón no contribuyen a la
del átomo, masa del átomo,
compone más pero son su parte
del 99,9% de su más activa, los
masa responsables de los
enlaces
Cuando los electrones pasan de un nivel de energía a
otro no se mueven, desaparecen de un nivel y
aparecen en el siguiente inmediatamente
Configuración electrónica
La configuración electrónica de un DIAGRAMA DE MÖELLER
átomo es el modo en que están
distribuidos los electrones
alrededor del núcleo de ese
átomo. Es decir, cómo se reparten
esos electrones entre los distintos
niveles y orbitales.
Para representar la configuración electrónica de un
átomo se escriben los nombres de los orbitales (1s,
2p, etc.) y se coloca como superíndice el número de
electrones que ocupan ese orbital o ese grupo de
orbitales.
Ejemplos:
Vous aimerez peut-être aussi
- Modelos AtómicosDocument4 pagesModelos AtómicosRaulZorrillaPas encore d'évaluation
- Cruadro Comparativo - Modelos AtomicosDocument5 pagesCruadro Comparativo - Modelos AtomicosElePas encore d'évaluation
- Tabla Periodica para Segundo de SecundariaDocument9 pagesTabla Periodica para Segundo de SecundariaBelen ZambranoPas encore d'évaluation
- Nomenclatura Inorganica-Segunda ParteDocument20 pagesNomenclatura Inorganica-Segunda ParteOdile VictoriaPas encore d'évaluation
- Proyecto TesisDocument25 pagesProyecto TesislizbethPas encore d'évaluation
- Modelos Atomicos-Challa Choqque Marco Antonio PDFDocument3 pagesModelos Atomicos-Challa Choqque Marco Antonio PDFMarco Antonio Challa ChoqquePas encore d'évaluation
- Cuadernillo - Pdfactividades de QuimicaDocument41 pagesCuadernillo - Pdfactividades de QuimicadnielahPas encore d'évaluation
- Tabla de Números de OxidaciónDocument1 pageTabla de Números de OxidaciónJuan Carlos Bergman VillarroelPas encore d'évaluation
- Anhídridos PrácticaDocument1 pageAnhídridos PrácticaWENDY GUAMAN MENDOZAPas encore d'évaluation
- Tabla PeriodicaDocument12 pagesTabla PeriodicaOlindaPas encore d'évaluation
- Quimica GeneralDocument10 pagesQuimica GeneralVR RGPas encore d'évaluation
- FÍSICA - 1 Práctica 6toDocument1 pageFÍSICA - 1 Práctica 6tokarina huayhuaPas encore d'évaluation
- Quimica - Sem6 - Unidades Químicas de MasaDocument3 pagesQuimica - Sem6 - Unidades Químicas de MasaLas Mandarinas De YoongiPas encore d'évaluation
- El Problema Del Botadero de Basura de Kjara Kjara - Trabajo Final CorregidoDocument14 pagesEl Problema Del Botadero de Basura de Kjara Kjara - Trabajo Final CorregidoFer ChunchoCoronelPas encore d'évaluation
- Guía de Aprendizaje-Calculos QuímicosDocument3 pagesGuía de Aprendizaje-Calculos QuímicosMore AndreaPas encore d'évaluation
- Determinacion de FE y FMDocument24 pagesDeterminacion de FE y FMLaura Massiel SanchezPas encore d'évaluation
- Cómo hacer un ensayo en 7 pasosDocument2 pagesCómo hacer un ensayo en 7 pasosyerkoPas encore d'évaluation
- Quimica 8Document8 pagesQuimica 8ivcscribdPas encore d'évaluation
- Evaluacion 3 Sexto MezclasDocument3 pagesEvaluacion 3 Sexto MezclasAna María López100% (1)
- Estrategias y Evidencias PDFDocument2 pagesEstrategias y Evidencias PDFmaytebech-1Pas encore d'évaluation
- Ejercicios - Reacciones Químicas-5to.Document2 pagesEjercicios - Reacciones Químicas-5to.DahyanaPas encore d'évaluation
- Exa - Qui.3er. Trim.2019Document2 pagesExa - Qui.3er. Trim.2019ceboso14Pas encore d'évaluation
- Geometría molecular UNAD tarea 2Document8 pagesGeometría molecular UNAD tarea 2Vanessa JimenezPas encore d'évaluation
- Masa MolarDocument2 pagesMasa MolarBalanceFenomenosPetroleos-uisPas encore d'évaluation
- Química inorgánica: reacciones balanceadas y cálculosDocument2 pagesQuímica inorgánica: reacciones balanceadas y cálculosMarcoAntonioDiazCotrinaPas encore d'évaluation
- Guia Reacciones QuimicasDocument6 pagesGuia Reacciones QuimicasJULIANA BARRIONUEVO BAUTISTAPas encore d'évaluation
- Version 2013 Manual de NomenclaturaDocument32 pagesVersion 2013 Manual de NomenclaturaJuan K MarroquinPas encore d'évaluation
- Números de oxidación y enlaces químicosDocument4 pagesNúmeros de oxidación y enlaces químicosJuan José MontesPas encore d'évaluation
- Geometria MolecularDocument3 pagesGeometria MolecularRolando Esteban Montero ArismendiPas encore d'évaluation
- 1 y 2 Clase de Quimica EjerciciosDocument17 pages1 y 2 Clase de Quimica EjerciciosJuan RomanPas encore d'évaluation
- Evaluacion Ley de Charles ProcesoDocument3 pagesEvaluacion Ley de Charles ProcesoStephania SaavedraPas encore d'évaluation
- Prueba de Diagnóstico HC-072 HC-092Document16 pagesPrueba de Diagnóstico HC-072 HC-092nicolecastrojaraPas encore d'évaluation
- Ficha de Trabajo Sales OxisalesDocument6 pagesFicha de Trabajo Sales OxisalesEnver Garcia100% (1)
- Balanceo RedoxDocument17 pagesBalanceo RedoxSantiago MacettoPas encore d'évaluation
- 10.quimica 3er Año Guia 6Document8 pages10.quimica 3er Año Guia 6Karlo TacPas encore d'évaluation
- Mini Ensayo Psu QuimicaDocument10 pagesMini Ensayo Psu QuimicaAllison BecerraPas encore d'évaluation
- Quimica 2003 04 Resuelto PDFDocument25 pagesQuimica 2003 04 Resuelto PDFnellyPas encore d'évaluation
- Unidades Quimicas SabDocument4 pagesUnidades Quimicas SabLUISA ESPERANZA JORDAN CHOQQUEPas encore d'évaluation
- Clasificación de Los Compuestos OrgánicosDocument24 pagesClasificación de Los Compuestos OrgánicosOmar MaciasPas encore d'évaluation
- CB33-11 Disoluciones II 2015 PDFDocument12 pagesCB33-11 Disoluciones II 2015 PDFFeña Ibarra FuentesPas encore d'évaluation
- Método Del Tanteo 1er GradoDocument2 pagesMétodo Del Tanteo 1er GradoB123Pas encore d'évaluation
- TerceroDocument5 pagesTerceroYasmin Alcantara0% (1)
- Taller Velocidad de ReacciónDocument3 pagesTaller Velocidad de ReacciónPaula Andrea Martínez ZamoraPas encore d'évaluation
- Práctica. Radio Iónico y Especies IsoelectrónicasDocument5 pagesPráctica. Radio Iónico y Especies IsoelectrónicasAlessandro VillafuertePas encore d'évaluation
- Examen de CC NN Noveno Grado Teoría AtómicaDocument5 pagesExamen de CC NN Noveno Grado Teoría AtómicaAlexis Raúl Hernández MejíaPas encore d'évaluation
- 1° - Química - I - Ii BimDocument57 pages1° - Química - I - Ii BimSami Galicia Mendez100% (1)
- SEMANA 2 Función OxidosDocument44 pagesSEMANA 2 Función OxidosAlex ZtePas encore d'évaluation
- Cartilla Optativa1 Quimica Inorganica. 1°cuat.2021Document100 pagesCartilla Optativa1 Quimica Inorganica. 1°cuat.2021Javier R. MoralesPas encore d'évaluation
- Practica QuímicaDocument15 pagesPractica Químicaheidi monestelPas encore d'évaluation
- 1 BIOL ActDocument52 pages1 BIOL ActE.F C.L.Pas encore d'évaluation
- Examen Extraordinario Química 2010Document3 pagesExamen Extraordinario Química 2010hectorraes100% (4)
- Taller de Química Hidruros Metálicos DiferenciadoDocument1 pageTaller de Química Hidruros Metálicos DiferenciadoPaty Limonerita LindaPas encore d'évaluation
- NOMENCLATURADocument14 pagesNOMENCLATURAbaterod3Pas encore d'évaluation
- Estructura de La Materia 2Document45 pagesEstructura de La Materia 2MaríaPas encore d'évaluation
- Ud 4. El à TomoDocument19 pagesUd 4. El à TomoUnai EstevePas encore d'évaluation
- El ÁtomoDocument16 pagesEl ÁtomoDaniel OrtuñoPas encore d'évaluation
- Modelos Atomicos QUIMICADocument42 pagesModelos Atomicos QUIMICAMaycol FernandoPas encore d'évaluation
- EXPOSICION DE FISICA MODERNA Nucleo AtomicoDocument39 pagesEXPOSICION DE FISICA MODERNA Nucleo AtomicoEstefanny Estrada MoralesPas encore d'évaluation
- La estructura y evolución del modelo atómico a través de la historiaDocument14 pagesLa estructura y evolución del modelo atómico a través de la historiaDarlin PatoPas encore d'évaluation
- Planilla de Excel para Informe de Gastos de EmpleadosDocument4 pagesPlanilla de Excel para Informe de Gastos de EmpleadosEduar Irigoin VasquezPas encore d'évaluation
- Z-One-penal-codigo Organico Integral Penal CoipDocument255 pagesZ-One-penal-codigo Organico Integral Penal CoipCristina BastidasPas encore d'évaluation
- Recopilado Inv Penal IIDocument36 pagesRecopilado Inv Penal IIAlejandra Anahí Recalde MonarPas encore d'évaluation
- Comunicación y formación de equiposDocument25 pagesComunicación y formación de equiposAlejandra Anahí Recalde MonarPas encore d'évaluation
- Parte 2 - G5Document2 pagesParte 2 - G5Alejandra Anahí Recalde MonarPas encore d'évaluation
- Test DISCDocument8 pagesTest DISCAlejandra Anahí Recalde MonarPas encore d'évaluation
- Adolescentes Infra IN FAMILIADocument8 pagesAdolescentes Infra IN FAMILIAAlejandra Anahí Recalde MonarPas encore d'évaluation
- 6C 1P - Usufructo - Copia 1: ¿Cuál Es La Definición de Usufructo?Document4 pages6C 1P - Usufructo - Copia 1: ¿Cuál Es La Definición de Usufructo?Alejandra Anahí Recalde MonarPas encore d'évaluation
- Recopilado Inv Penal IIDocument36 pagesRecopilado Inv Penal IIAlejandra Anahí Recalde MonarPas encore d'évaluation
- Guion Audiencia en Procedimiento Sumario AlimentosDocument8 pagesGuion Audiencia en Procedimiento Sumario AlimentosVinicio Calles100% (1)
- Delitos Contra El Derecho A La Propiedad Leinner TamayoDocument8 pagesDelitos Contra El Derecho A La Propiedad Leinner TamayoAlejandra Anahí Recalde MonarPas encore d'évaluation
- Parte 2 - G5Document2 pagesParte 2 - G5Alejandra Anahí Recalde MonarPas encore d'évaluation
- Objetivos VerbosDocument7 pagesObjetivos VerbosAlejandra Anahí Recalde MonarPas encore d'évaluation
- ExpresiónDocument106 pagesExpresiónAlejandra Anahí Recalde MonarPas encore d'évaluation
- Personas (Clase 5)Document26 pagesPersonas (Clase 5)Alejandra Anahí Recalde MonarPas encore d'évaluation
- Menu Nuevo 18x25 (Marzo2023)Document8 pagesMenu Nuevo 18x25 (Marzo2023)Alejandra Anahí Recalde MonarPas encore d'évaluation
- Deber de armaduras: revisión del intentoDocument4 pagesDeber de armaduras: revisión del intentoAlejandra Anahí Recalde MonarPas encore d'évaluation
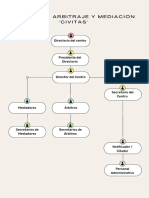
- Organigrama CIVITAS PDFDocument1 pageOrganigrama CIVITAS PDFAlejandra Anahí Recalde MonarPas encore d'évaluation
- DensidadDocument1 pageDensidadAlejandra Anahí Recalde MonarPas encore d'évaluation
- Platón - Quien FueDocument1 pagePlatón - Quien FueAlejandra Anahí Recalde MonarPas encore d'évaluation
- Plantilla3 Ale - DigitaalDocument1 pagePlantilla3 Ale - DigitaalAlejandra Anahí Recalde MonarPas encore d'évaluation
- Modos de Orar 2021Document23 pagesModos de Orar 2021Alejandra Anahí Recalde MonarPas encore d'évaluation
- Formal 1Document3 pagesFormal 1Alejandra Anahí Recalde MonarPas encore d'évaluation
- Como Hacer de La Oracion Una PrioridadDocument10 pagesComo Hacer de La Oracion Una PrioridadAlejandra Anahí Recalde MonarPas encore d'évaluation
- Plantilla 13.Document1 pagePlantilla 13.Alejandra Anahí Recalde MonarPas encore d'évaluation
- Wholer y La UreaDocument4 pagesWholer y La UreaMitzi QuirozPas encore d'évaluation
- Plantilla 15.Document1 pagePlantilla 15.Alejandra Anahí Recalde MonarPas encore d'évaluation
- Formal 2Document3 pagesFormal 2Alejandra Anahí Recalde MonarPas encore d'évaluation
- Apunte 4Document1 pageApunte 4Alejandra Anahí Recalde MonarPas encore d'évaluation
- Formal 3Document3 pagesFormal 3Alejandra Anahí Recalde MonarPas encore d'évaluation
- Diuresis: Factores que modifican la eliminación de agua por el riñónDocument11 pagesDiuresis: Factores que modifican la eliminación de agua por el riñónGabriel OtaPas encore d'évaluation
- 2019 18 07 19 Modelo Ciencias BiologiaDocument45 pages2019 18 07 19 Modelo Ciencias BiologiaSopa RoeckelPas encore d'évaluation
- Absorción de Glucosa y PeristaltismoDocument15 pagesAbsorción de Glucosa y PeristaltismoJassmin LariosPas encore d'évaluation
- Trabajo de CristalograficaDocument9 pagesTrabajo de CristalograficaWilliamsRafaelMataRimacPas encore d'évaluation
- Curva de Titulación de La GlicinaDocument7 pagesCurva de Titulación de La GlicinaFabiana OrdoñezPas encore d'évaluation
- Fluidos 3Document14 pagesFluidos 3Fito MenaPas encore d'évaluation
- Hydromatic PucallpaDocument2 pagesHydromatic PucallpaArnolPas encore d'évaluation
- Preparación y Valoración de Nitrato de Plata 0Document3 pagesPreparación y Valoración de Nitrato de Plata 0Edd de La ComarcaPas encore d'évaluation
- 1Document10 pages1Arlet BibriescaPas encore d'évaluation
- Célula como unidad estructural y funcional de la vidaDocument16 pagesCélula como unidad estructural y funcional de la vidasegg_mnPas encore d'évaluation
- Definicion de LewisDocument6 pagesDefinicion de LewisbryanPas encore d'évaluation
- Terminacion Cervical y Tipos de CoronasDocument24 pagesTerminacion Cervical y Tipos de CoronasJuan Martin Fierro Aquinto86% (7)
- Carpinteria MetalicaDocument10 pagesCarpinteria MetalicaEfrain Sotelo BuatistaPas encore d'évaluation
- Dalinde DR530 IPT 230309 VIV SubmittalDocument35 pagesDalinde DR530 IPT 230309 VIV Submittalerick100% (1)
- COTAMANIADocument15 pagesCOTAMANIAEdgar Cota Mamani100% (6)
- Informe-1-Text De-SuelosDocument7 pagesInforme-1-Text De-Suelos'CamiloVelasquezPas encore d'évaluation
- III BIM - BIOLOGIA - 4TO AÑO - Guia 2 - Fotosíntesis IDocument8 pagesIII BIM - BIOLOGIA - 4TO AÑO - Guia 2 - Fotosíntesis Iprofesormiguel241Pas encore d'évaluation
- Aditivos para El ConcretoDocument36 pagesAditivos para El ConcretoMichel QuiñonesPas encore d'évaluation
- Formulacion de AgaresDocument12 pagesFormulacion de AgaresAntonello LedezmaPas encore d'évaluation
- SEMINARIO 3 Cinética Química, Equilibrio Químico y Equilibrio Acido Base 123 ADocument12 pagesSEMINARIO 3 Cinética Química, Equilibrio Químico y Equilibrio Acido Base 123 ASandra CordovaPas encore d'évaluation
- Clase 7 (Cubiertas)Document31 pagesClase 7 (Cubiertas)Juan Andres Hodeg JimenezPas encore d'évaluation
- Informe de Constantes FisicaDocument13 pagesInforme de Constantes FisicaLeonardo Albengrin100% (5)
- Operaciones de ReacciónDocument28 pagesOperaciones de ReacciónMarcioLazPas encore d'évaluation
- Investigacion Centrales TermicasDocument7 pagesInvestigacion Centrales TermicasSamuel DiazPas encore d'évaluation
- Trampas Quimicas. ExposicionDocument27 pagesTrampas Quimicas. ExposicionRaúl FloresPas encore d'évaluation
- Terp EnosDocument23 pagesTerp EnosElmer Lopez BrionesPas encore d'évaluation
- Fisiologia RenalDocument8 pagesFisiologia RenalVitor LópezPas encore d'évaluation
- Análisis exergético y exergoeconómico de plantas de generación de energía solar con cilindros parabólicosDocument10 pagesAnálisis exergético y exergoeconómico de plantas de generación de energía solar con cilindros parabólicosJessica MejiaPas encore d'évaluation
- Ensayo Bloques de MotoresDocument3 pagesEnsayo Bloques de MotoresLauraHernandezPas encore d'évaluation
- Enzimas y factores que afectan su actividadDocument2 pagesEnzimas y factores que afectan su actividadIsabel Fernandez RiveraPas encore d'évaluation