Académique Documents
Professionnel Documents
Culture Documents
INCERTIDUMBRE
Transféré par
Lucía0 évaluation0% ont trouvé ce document utile (0 vote)
8 vues9 pagesPrincipio de incertidumbre
Titre original
INCERTIDUMBRE (1)
Copyright
© © All Rights Reserved
Formats disponibles
PPTX, PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentPrincipio de incertidumbre
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PPTX, PDF, TXT ou lisez en ligne sur Scribd
0 évaluation0% ont trouvé ce document utile (0 vote)
8 vues9 pagesINCERTIDUMBRE
Transféré par
LucíaPrincipio de incertidumbre
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PPTX, PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 9
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
FACULTAD DE QUÍMICA E INGENIERÍA QUÍMICA
E.A.P QUÍMICA
DEPARTAMENTO ACADÉMICO DE FISICOQUÍMICA
CURSO: INTRODUCCIÓN A LA QUÍMICA CUÁNTICA
EL PRINCIPIO DE INCERTIDUMBRE DE HEISENBERG
WERNER HEISENBERG (1901-1976)
• Físico y Premio Nobel 1932 alemán («por la
creación de la mecánica cuántica, cuya
aplicación tiene, entre otras cosas, el estudio y
descubrimiento de las formas alotrópicas del
hidrógeno»)
• Desarrolló un sistema de mecánica cuántica y
cuya indeterminación o principio de
incertidumbre ha ejercido una profunda
influencia en la física y en la filosofía del siglo
XX.
• Estuvo a cargo de la investigación científica del
proyecto de la bomba atómica alemana durante
la II Guerra Mundial. Bajo su dirección se intentó
construir un reactor nuclear en el que la reacción
en cadena se llevara a cabo con tanta rapidez
que produjera una explosión, pero estos intentos
no alcanzaron éxito. Estuvo preso en Inglaterra
después de la guerra.
IMAGINA A UN EXPERIMENTADOR TRATANDO DE
MEDIR LA POSICIÓN Y EL MOMENTO DE UN
ELECTRÓN DISPARÁNDOLA UN FOTÓN.
• En 1924 comenzó a desarrollar un sistema de mecánica
cuántica, denominado mecánica matricial, en el que la
formulación matemática se basaba en las frecuencias y
amplitudes de las radiaciones absorbidas y emitidas por
el átomo y en los niveles de energía del sistema atómico.
El principio de incertidumbre desempeñó un importante
papel en el desarrollo de la mecánica cuántica y en el
progreso del pensamiento filosófico moderno. Estableció
incluso una fórmula que relaciona la indeterminación en
la medida de la cantidad de movimiento (Δp) y de la
posición (Δx)
Heisenberg hace su experimento con un microscopio
muchísimo más potente y preciso que cualquiera que
existiera entonces.
• De modo que, en el microscopio de Heisenberg, un fotón
incide sobre el electrón y luego llega al microscopio. Pero
para detectar la posición del electrón con mucha precisión
hace falta un fotón de onda muy corta, es decir, con
mucha energía. Un fotón de radiación gamma: y cuando
ese fotón muy energético choca con el electrón, lo manda
disparado en una dirección determinada,
independientemente de la velocidad que tuviera antes. Al
saber muy bien dónde estaba el electrón no tenemos ni
idea de cómo de rápido va.
EL ELECTRÓN SE VE ALTERADO POR EL
FOTÓN
• La cuestión es que la luz no es infinitamente
divisible: está formada por cuantos de energía, los
fotones. Y el “tamaño energético” de cada uno de
esos pedazos discretos es mayor cuanto más corta
es la longitud de onda. No es posible utilizar
radiación gamma y emitir una cantidad tan
pequeña como queramos – la energía mínima
emitida es un fotón muy energético. Si la física
clásica fuera cierta, podríamos coger radiación de
longitud de onda arbitrariamente corta (muy
precisa) y sin embargo emitir una cantidad
arbitrariamente pequeña de esa radiación (que
apenas afectase al electrón).
• La clave de la cuestión, si has entendido la idea del
experimento, es que la limitación para poder “ver”
el electrón no se debe a que el microscopio no sea
suficientemente bueno, ni que su diseño sea
defectuoso: se debe a la dualidad onda-corpúsculo
de la materia y la energía.
¿POR QUÉ APARECE ESTE LÍMITE A LA HORA DE
DETERMINAR LA POSICIÓN Y EL MOMENTO LINEAL EN
MECÁNICA CUÁNTICA?
CONCLUSIÓN
El principio de incertidumbre significa que no se puede hablar de la posición y del
momento del electrón orbital como si tuvieran ambos, a la vez, valores definidos.
De este modo según la teoría cuántica, las orbitas definidas por la teoría de Bohr se
reemplazan por regiones difusas en las cuales pueden encontrarse los electrones.
A causa del principio de incertidumbre, el orden que impere en el futuro en un
sistema atómico, no se puede predecir con exactitud, como aseguraba anteriormente
la mecánica clásica.
En lugar de eso, solo puede predecir la Probabilidad de que un electrón este en
determinado punto en un tiempo determinado
¡¡¡GRACIAS!!!
Vous aimerez peut-être aussi
- 12Document18 pages12LucíaPas encore d'évaluation
- Angulo de Refraccion TotalDocument5 pagesAngulo de Refraccion TotalLucíaPas encore d'évaluation
- Diagrama de SolubilidadDocument14 pagesDiagrama de SolubilidadLucíaPas encore d'évaluation
- Manual de Laboratorio de Electricidad y Magnetismo Fisica IIIDocument76 pagesManual de Laboratorio de Electricidad y Magnetismo Fisica IIILucíaPas encore d'évaluation
- Instrumentacion Ley de OhmDocument11 pagesInstrumentacion Ley de OhmLucíaPas encore d'évaluation
- Informe 1 QG 2Document14 pagesInforme 1 QG 2LucíaPas encore d'évaluation
- Informe 8 Química General 2 UnmsmDocument19 pagesInforme 8 Química General 2 UnmsmLucíaPas encore d'évaluation
- Informe 1 QG 2Document14 pagesInforme 1 QG 2LucíaPas encore d'évaluation
- El Principio de SuperposiciónDocument14 pagesEl Principio de SuperposiciónernestoracalPas encore d'évaluation
- Exposicion QuarksDocument19 pagesExposicion QuarksBaltazarNicolasSieteSoles100% (1)
- 10-Diodo de JunturaDocument16 pages10-Diodo de JunturaJhanier MenesesPas encore d'évaluation
- Tarea Fisica ModernaDocument6 pagesTarea Fisica ModernaGustavo GarcíaPas encore d'évaluation
- Presentacion Didactica Union PN en Tecnologia CMOSDocument30 pagesPresentacion Didactica Union PN en Tecnologia CMOSSanchez Acolt Uriel EfrainPas encore d'évaluation
- TALLER Diodos y Sus Aplicaciones-1Document5 pagesTALLER Diodos y Sus Aplicaciones-1laperra75Pas encore d'évaluation
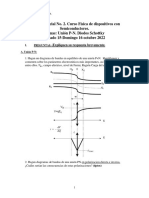
- Examen Parcial 2 - FDS 2022Document7 pagesExamen Parcial 2 - FDS 2022Cristian TorresPas encore d'évaluation
- 3-Configuración ElectrónicaDocument17 pages3-Configuración ElectrónicaJhon E Muchica RuizPas encore d'évaluation
- f.8 El Atomo de Helio (Última Versión2017A)Document24 pagesf.8 El Atomo de Helio (Última Versión2017A)Lore ArronaPas encore d'évaluation
- SYC - Catalogo Julio 2007Document76 pagesSYC - Catalogo Julio 2007eballiriPas encore d'évaluation
- Mecánica Cuántica y Álgebra de OperadoresDocument62 pagesMecánica Cuántica y Álgebra de OperadoresOlaf Durán100% (1)
- 4ElectroAnalo PDFDocument5 pages4ElectroAnalo PDFRodrigo SiñaniPas encore d'évaluation
- Repaso: Dispositivos Auxiliares de Disparo: Clase PrácticaDocument27 pagesRepaso: Dispositivos Auxiliares de Disparo: Clase PrácticaronaldPas encore d'évaluation
- Ejercicios Estructura AtomicaDocument5 pagesEjercicios Estructura Atomicaangel rojo falconPas encore d'évaluation
- SCR 1Document19 pagesSCR 1Francisco Marcelo Pereira HernándezPas encore d'évaluation
- Preguntas de Ley de BraggDocument6 pagesPreguntas de Ley de BraggNegro YepezPas encore d'évaluation
- Atomo ResueltosDocument45 pagesAtomo ResueltosJorge PibaquePas encore d'évaluation
- Simbologia EletricaDocument7 pagesSimbologia EletricaMario AriasPas encore d'évaluation
- Dualidad Onda ParticulaDocument2 pagesDualidad Onda ParticulaLuis Guerra Hidalgo100% (1)
- Constante de PlanckDocument4 pagesConstante de PlanckAnibal SierraPas encore d'évaluation
- 3eso Examenàtom PiDocument3 pages3eso Examenàtom Pi3estherPas encore d'évaluation
- 02 Configuración Electrónica y Numeros Cuanticos 2019Document9 pages02 Configuración Electrónica y Numeros Cuanticos 2019Edwis Castañeda VelásquezPas encore d'évaluation
- Símbolos de TransistoresDocument3 pagesSímbolos de TransistoresvicorePas encore d'évaluation
- Interpretación de BohmDocument15 pagesInterpretación de BohmSergio Palomo NevadoPas encore d'évaluation
- Ejercicios de Distribucion Electronica-1Document2 pagesEjercicios de Distribucion Electronica-1Luis Antonio Molloapaza0% (2)
- Teoría Atómica de BohrDocument9 pagesTeoría Atómica de BohrBayron Villalobos CutzPas encore d'évaluation
- Labo 01 (Previo)Document18 pagesLabo 01 (Previo)EtnicO3Pas encore d'évaluation
- Laboratorio N°1 Micro Nano Sistemas Electronicos-Diaz Machuca DanielDocument14 pagesLaboratorio N°1 Micro Nano Sistemas Electronicos-Diaz Machuca Danieldaniel diazPas encore d'évaluation
- Ecite2012 PDFDocument446 pagesEcite2012 PDFAlejandro Loya OlivasPas encore d'évaluation