Académique Documents
Professionnel Documents
Culture Documents
Cours 2 Chimie-eleve-TRAFI 2BAC
Transféré par
Enidroun Out0 évaluation0% ont trouvé ce document utile (0 vote)
44 vues9 pagesCopyright
© © All Rights Reserved
Formats disponibles
PPTX, PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PPTX, PDF, TXT ou lisez en ligne sur Scribd
0 évaluation0% ont trouvé ce document utile (0 vote)
44 vues9 pagesCours 2 Chimie-eleve-TRAFI 2BAC
Transféré par
Enidroun OutDroits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PPTX, PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 9
Chapitre : 2 -Chimie-
Suivi temporel d’une réaction chimique
I- Introduction :
Effectuer le suivi temporel d’une transformation chimique , c’est connaître
la composition du mélange réactionnel à chaque instant ( la cinétique
chimique ) .
Pour suivre l’évolution du système chimique au cours de la transformation,
il suffit de connaître l’avancement x en fonction du temps t :
II- Vitesse de réaction et le temps de demi-réaction :
1- Vitesse volumique de réaction :
La vitesse volumique v(t) d’une réaction se déroulant dans un volume
constant V est la valeur de la dérivée temporelle de l’avancement x
de la réaction , divisée par le volume V : ………………………………
Avec :
v(t) : ………………………………………………………………………
V : ………………………………………………………………………
𝒅𝒙 : ……………………………………...........………….………………
𝒅𝒕
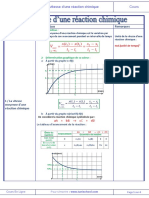
2- Détermination graphique de la vitesse de réaction :
On trace la tangente de la courbe x = f(t) au point d’abscisse ti.
En calculant le coefficient directeur a=dx/dt à l’instant ti de la tangente
à la courbe et en le divisant par le volume V.
a = dx/dt = =
Remarque :
La vitesse de réaction ………………….. avec le temps car la concentration
des réactifs est ……………………….. au cours de la transformation .
3- Le temps de demi-réaction t1/2 :
a) Définition :
Le temps de demi-réaction t1/2 d’un système chimique est …………………
…………....….. pour que l’avancement parvienne à la moitié de sa valeur
finale : ……………………… .
Si la transformation est totale on aura : ………………………
b) Détermination du temps de demi-réaction :
On le détermine graphiquement à partir de la courbe des variations de l'avancement
𝒙 = 𝒇(𝒕) :
On détermine la valeur de l'avancement final 𝒙𝒇 par le traçage d’une asymptote
à la courbe.
On détermine 𝒙𝒇/𝟐 sur la courbe .
On détermine le point d'intersection de la ligne horizontale de l'ordonnée 𝒙𝒇/2
avec la courbe.
L’abscisse du point d'intersection représente le temps de demi-réaction 𝒕𝟏⁄𝟐 .
1-
Vous aimerez peut-être aussi
- Chapitre-2 - Suivi Temporel D'une Transformation Chimique - Vitesse de RéactionDocument5 pagesChapitre-2 - Suivi Temporel D'une Transformation Chimique - Vitesse de Réactiona houssPas encore d'évaluation
- Cours 2 - Suivi TemporelDocument9 pagesCours 2 - Suivi TemporelHamza BerahmaPas encore d'évaluation
- Cours Vitesse de ReactionDocument3 pagesCours Vitesse de ReactioncristyenPas encore d'évaluation
- Lecon 2 Chimie Vitesse D Une Reaction ChimiqueDocument1 pageLecon 2 Chimie Vitesse D Une Reaction ChimiqueKais GuesmiPas encore d'évaluation
- Cours 1 - Suivi Temporel D'une Transformation (WWW - AdrarPhysic.Fr) - 7Document1 pageCours 1 - Suivi Temporel D'une Transformation (WWW - AdrarPhysic.Fr) - 7salhiPas encore d'évaluation
- Cinetique ChimiqueDocument4 pagesCinetique ChimiqueHoussam MazouzPas encore d'évaluation
- Suivi Temporel D - Une TransformationDocument6 pagesSuivi Temporel D - Une TransformationerrairachidPas encore d'évaluation
- 2.déterminer La Vitesse de Réaction Et Le Temps de Demi-Réaction PDFDocument3 pages2.déterminer La Vitesse de Réaction Et Le Temps de Demi-Réaction PDFkimmikPas encore d'évaluation
- Cinetique ChimiqueDocument8 pagesCinetique ChimiqueFranck MomoPas encore d'évaluation
- Modelisation Des Transformations Chimiques Bilan de La Matiere Resume de Cours 2Document2 pagesModelisation Des Transformations Chimiques Bilan de La Matiere Resume de Cours 2Lazreg ImedPas encore d'évaluation
- c9 TC Inter Prof Sbiro (WWW - Pc1.ma)Document2 pagesc9 TC Inter Prof Sbiro (WWW - Pc1.ma)cpm fessaisPas encore d'évaluation
- Suivi Temporel D'une Transformation Chimique - Vitesse de RéactionDocument7 pagesSuivi Temporel D'une Transformation Chimique - Vitesse de RéactionKamal BdPas encore d'évaluation
- 2 - Suivi Temporel D'une Transformation - Vitesse de RéactionDocument31 pages2 - Suivi Temporel D'une Transformation - Vitesse de Réactionlahcen essPas encore d'évaluation
- Série D'exercices Vitesse de RéactionDocument4 pagesSérie D'exercices Vitesse de Réactionothmane GbPas encore d'évaluation
- Cours Suivi TemporelDocument3 pagesCours Suivi Temporelathn.maryamPas encore d'évaluation
- Exercices 2 Suivi TemporelDocument1 pageExercices 2 Suivi TemporelayoubbouuderqaPas encore d'évaluation
- Exercices 2 Suivi TemporelDocument1 pageExercices 2 Suivi Temporelكورة لايفPas encore d'évaluation
- Devoir Rapide 1 S1Document2 pagesDevoir Rapide 1 S1obaha6490Pas encore d'évaluation
- Résumé Chimie TT L'annéeDocument6 pagesRésumé Chimie TT L'annéeWiem BenchahbounPas encore d'évaluation
- Cours de Cinétique ChimiqueDocument6 pagesCours de Cinétique Chimiqueilyes fellagPas encore d'évaluation
- Série N°9-9Document3 pagesSérie N°9-9Jihad ELPas encore d'évaluation
- Explication Et Interprétation Au Niveau Microscopique:: La Concentration Des RéactifsDocument4 pagesExplication Et Interprétation Au Niveau Microscopique:: La Concentration Des RéactifsALPHA designPas encore d'évaluation
- TP GRDocument6 pagesTP GRMalouda Merzkani100% (3)
- Serir SuiviDocument7 pagesSerir Suivikhaoula elhansaliPas encore d'évaluation
- Cours - Suivi TemporelDocument7 pagesCours - Suivi TemporelRedouane Reda100% (2)
- Chapitre 2, Suivi Temporel D'une Transformation Chimique, Cours, Activités, Exercices D'application, 2BAC BIOF PR JENKAL RACHIDDocument11 pagesChapitre 2, Suivi Temporel D'une Transformation Chimique, Cours, Activités, Exercices D'application, 2BAC BIOF PR JENKAL RACHIDKarim EL HAJJIPas encore d'évaluation
- 01 La Cinétique ChimiqueDocument4 pages01 La Cinétique ChimiqueIlyes Ben JemaaPas encore d'évaluation
- Cours DR BENAMIRA MESSAOUD Cinétique Chimique Master 2 Chimie Des MatériauxDocument66 pagesCours DR BENAMIRA MESSAOUD Cinétique Chimique Master 2 Chimie Des MatériauxaminePas encore d'évaluation
- Chapitre 1Document5 pagesChapitre 1Manel AbrichePas encore d'évaluation
- Cinétique Chimique PDFDocument6 pagesCinétique Chimique PDFAzizElheniPas encore d'évaluation
- Temps Et Evolution Chimique PDFDocument31 pagesTemps Et Evolution Chimique PDFludovicPas encore d'évaluation
- Chapitre 1 Cinetique1Document6 pagesChapitre 1 Cinetique1stevPas encore d'évaluation
- serie-2-suivi-temporelle-d-une-transformation-chimiqueDocument7 pagesserie-2-suivi-temporelle-d-une-transformation-chimiquee.maskarPas encore d'évaluation
- 2 Suivi Temporel D Une TransformationDocument5 pages2 Suivi Temporel D Une Transformationfoud18Pas encore d'évaluation
- Série D'exercices de Révision Corrigées de Chimie Suivi Temporel d'1 Transformation Vitesse de La Réaction p.SBIRO Abdelkrim (WWW - Pc1.ma)Document19 pagesSérie D'exercices de Révision Corrigées de Chimie Suivi Temporel d'1 Transformation Vitesse de La Réaction p.SBIRO Abdelkrim (WWW - Pc1.ma)Yacine Ait El Houss100% (15)
- Cours Avancement D'une Reaction 2015Document2 pagesCours Avancement D'une Reaction 2015Daghsni SaidPas encore d'évaluation
- Cour Cinétique Chimique 2013 2014 (Afdal Ali) PDFDocument6 pagesCour Cinétique Chimique 2013 2014 (Afdal Ali) PDFMontassar DkhiliPas encore d'évaluation
- Manuel Unité de Conception 2STMDocument83 pagesManuel Unité de Conception 2STMKAYTO YTPas encore d'évaluation
- Exercice 30 Suivi Temporel D'une Transformation ChimiqueDocument5 pagesExercice 30 Suivi Temporel D'une Transformation ChimiqueMoulayMoulyPas encore d'évaluation
- Resumé Suivi Temporel D'une Transformation ChimiqueDocument1 pageResumé Suivi Temporel D'une Transformation ChimiqueZakaria BelaaroussiPas encore d'évaluation
- Chimie: (07 Points)Document10 pagesChimie: (07 Points)Aymen ToumiPas encore d'évaluation
- Suivi Temporel D - Une TRSF ChimiqueDocument4 pagesSuivi Temporel D - Une TRSF ChimiquemedPas encore d'évaluation
- Ch3 1vitesse ReactionDocument4 pagesCh3 1vitesse Reactionbessama84Pas encore d'évaluation
- ExosDocument12 pagesExosHedi SPas encore d'évaluation
- Hydrologie UrbaineDocument7 pagesHydrologie Urbainelimmoud100% (1)
- 2015 09 04 Cours ET 1A ImpDocument63 pages2015 09 04 Cours ET 1A ImpFarhat ThamerPas encore d'évaluation
- Séance_5Document8 pagesSéance_5yasminati07Pas encore d'évaluation
- Les Transformations Chimiques Qui S Effectuent Dans Les 2 Sens Cours 2Document4 pagesLes Transformations Chimiques Qui S Effectuent Dans Les 2 Sens Cours 2Mohamed B'nPas encore d'évaluation
- Simili 2 À Distance SMDocument7 pagesSimili 2 À Distance SMSAIDPas encore d'évaluation
- Examens Nationaux PC de 2008 À 2022 ELHAFYANI BMSDocument212 pagesExamens Nationaux PC de 2008 À 2022 ELHAFYANI BMSFatima zahra sbissiiiPas encore d'évaluation
- Cours - Chimie - RESUME CINETIQUE CHIMIQUE - Bac Sciences Exp (2015-2016) MR Daghsni SahbiDocument3 pagesCours - Chimie - RESUME CINETIQUE CHIMIQUE - Bac Sciences Exp (2015-2016) MR Daghsni SahbiKais Ben Aicha100% (2)
- Cours 3 Chimie-eleve-TRAFI 2BACDocument13 pagesCours 3 Chimie-eleve-TRAFI 2BACEnidroun OutPas encore d'évaluation
- 3 - Suivi de L'évolution D'une Transformation ChimiqueDocument3 pages3 - Suivi de L'évolution D'une Transformation ChimiqueOmar ait taleb aliPas encore d'évaluation
- Chapitre - CH2 - Vitesse de ReactionDocument5 pagesChapitre - CH2 - Vitesse de Reactionmohamed laghribPas encore d'évaluation
- 1bac Resume Travail Et Energie PotentielDocument2 pages1bac Resume Travail Et Energie PotentielEnidroun OutPas encore d'évaluation
- Chap 08Document8 pagesChap 08Enidroun OutPas encore d'évaluation
- Chapitre 1 Melanges IdentificationDocument5 pagesChapitre 1 Melanges IdentificationEnidroun OutPas encore d'évaluation
- Chapitre 7 Mecanismes ReactionnelsDocument4 pagesChapitre 7 Mecanismes ReactionnelsEnidroun OutPas encore d'évaluation
- Quantité de Matière: I - Masse Et Nombre D'entités ChimiquesDocument1 pageQuantité de Matière: I - Masse Et Nombre D'entités ChimiquesEnidroun OutPas encore d'évaluation
- 10-11 Ester +evolutionDocument11 pages10-11 Ester +evolutionEnidroun OutPas encore d'évaluation
- RA18 C4Lycee PHCH Retard-Distance-Vitesse-Propagation-Onde 1064962Document10 pagesRA18 C4Lycee PHCH Retard-Distance-Vitesse-Propagation-Onde 1064962Enidroun OutPas encore d'évaluation
- Le Modele de L Atome CoursDocument6 pagesLe Modele de L Atome CoursEnidroun OutPas encore d'évaluation
- DST 04 Ts 03-04Document3 pagesDST 04 Ts 03-04Enidroun OutPas encore d'évaluation
- Cours Associations de DipolesDocument2 pagesCours Associations de DipolesEnidroun OutPas encore d'évaluation
- Cours Elct03 ProfDocument56 pagesCours Elct03 ProfEnidroun OutPas encore d'évaluation
- I - Le Principe D'inertieDocument1 pageI - Le Principe D'inertieEnidroun OutPas encore d'évaluation
- ExtraitDocument8 pagesExtraitEnidroun OutPas encore d'évaluation
- DS6 FR ArDocument4 pagesDS6 FR ArEnidroun OutPas encore d'évaluation
- Cours05 04Document7 pagesCours05 04Enidroun OutPas encore d'évaluation
- Le Courant Electrique Continu Cours FRDocument5 pagesLe Courant Electrique Continu Cours FREnidroun OutPas encore d'évaluation
- Cours 4 Pysique Eleve TRAFI 2BACDocument22 pagesCours 4 Pysique Eleve TRAFI 2BACEnidroun OutPas encore d'évaluation
- RA16 C3 ST Signa Et Infol N.D 581422Document5 pagesRA16 C3 ST Signa Et Infol N.D 581422Enidroun OutPas encore d'évaluation
- Rapport de L'évaluation Diagnostique WWW Newotnscienc ComDocument3 pagesRapport de L'évaluation Diagnostique WWW Newotnscienc ComEnidroun Out100% (3)
- Cours 5 Chimie-eleve-TRAFI 2BACDocument17 pagesCours 5 Chimie-eleve-TRAFI 2BACEnidroun OutPas encore d'évaluation
- Synthese Ci9Document1 pageSynthese Ci9Enidroun OutPas encore d'évaluation
- Modulation Analogique Etudiant - 2Document37 pagesModulation Analogique Etudiant - 2houda_01Pas encore d'évaluation
- Cours 4 Chimie-eleve-TRAFI 2BACDocument8 pagesCours 4 Chimie-eleve-TRAFI 2BACEnidroun OutPas encore d'évaluation
- Cours 3 Chimie-eleve-TRAFI 2BACDocument13 pagesCours 3 Chimie-eleve-TRAFI 2BACEnidroun OutPas encore d'évaluation
- Cours 4 C TRAFI 2BACDocument9 pagesCours 4 C TRAFI 2BACEnidroun OutPas encore d'évaluation
- Cours 5 C TRAFI 2BACDocument18 pagesCours 5 C TRAFI 2BACEnidroun OutPas encore d'évaluation
- Cours 2 P TRAFI 2BACDocument10 pagesCours 2 P TRAFI 2BACEnidroun Out100% (1)
- Rapport de Test Diagnostique TCSDocument3 pagesRapport de Test Diagnostique TCSEnidroun Out100% (3)
- BL 1Document22 pagesBL 1Enidroun OutPas encore d'évaluation