Académique Documents
Professionnel Documents
Culture Documents
Os Chimie Ch7 Ex Suppl
Transféré par
Sarah Taibi El KettaniCopyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Os Chimie Ch7 Ex Suppl
Transféré par
Sarah Taibi El KettaniDroits d'auteur :
Formats disponibles
Nom : Groupe : Date :
Exercices supplémentaires
CHAPITRE 7 :
L’ÉTUDE QUALITATIVE DE L’ÉTAT D’ÉQUILIBRE
7.1 QU’EST-CE QUE L’ÉQUILIBRE CHIMIQUE ?
1. Lequel des énoncés suivants est vrai ?
A. Lorsqu’un système est à l’équilibre, la loi de la conservation de la matière ne s’applique plus.
B. Lorsqu’un système est à l’équilibre, la masse des réactifs est la même que celle des produits.
C. Lorsqu’un système est à l’équilibre, la quantité de réactifs et la quantité de produits demeurent
constantes.
D. Lorsqu’un système est à l’équilibre, le nombre de molécules des réactifs est le même que
le nombre de molécules des produits.
2. Vous placez du dihydrogène gazeux et du diiode gazeux dans un contenant que vous fermez
hermétiquement. Ces deux gaz réagissent ensemble selon l’équation suivante :
H2(g) + I2(g) ⇋ 2 HI2(g)
Incolore Violet Incolore
Après un certain temps, vous constatez que la couleur du système se stabilise et que l’équilibre
est atteint. Lequel des énoncés suivants caractérise ce système ?
A. La concentration des réactifs et la concentration du produit sont égales.
B. La réaction chimique s’est arrêtée complètement.
C. La vitesse de synthèse de l’iodure d’hydrogène est égale à celle de sa décomposition.
D. Le système ne contient plus de réactifs.
3. Lequel des systèmes suivants peut atteindre l’équilibre ?
A. Une bonbonne d’hélium dont la pression est constante.
B. Un verre qui contient une quantité constante d’eau.
C. Un thermomètre à alcool qui indique une température constante.
D. Un aquarium dont l’eau est saturée d’oxygène.
4. Laquelle des propriétés suivantes n’est pas une propriété macroscopique d’un système à l’équilibre ?
A. Le pH.
B. La pression.
C. La vitesse de réaction.
D. La température.
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 7 N38327
1
Nom : Groupe : Date :
5. Soit le graphique suivant :
À partir de quel moment l’équilibre est-il atteint ?
A. 6 min
B. 13 min
C. 20 min
D. 0 min
6. Lequel des énoncés suivants décrit une réaction réversible ?
A. Un mélange d’eau et de glace.
B. La dissolution du sulfate de cuivre produisant une solution d’un bleu limpide.
C. Un mélange d’hélium et d’argon.
D. Une flaque d’eau qui s’évapore.
7.2 L’EFFET DE DIFFÉRENTS FACTEURS SUR L’ÉQUILIBRE
1. Lequel des énoncés suivants est en accord avec le principe de Le Chatelier ?
A. Lorsqu’on augmente la concentration d’un réactif, la réaction directe est favorisée,
puisque le système s’oppose au changement en utilisant le surplus pour former des produits.
B. Lorsqu’on augmente la concentration d’un réactif, la réaction inverse est favorisée,
puisque le système s’oppose au changement en utilisant le surplus pour former
une plus grande quantité de réactifs.
C. Lorsqu’on augmente la concentration d’un réactif, aucune réaction n’est favorisée,
puisque le système s’oppose au changement en bloquant la transformation.
D. Lorsqu’on augmente la concentration d’un réactif, la vitesse de la réaction augmente,
puisque le système cherche à rétablir les concentrations initiales des réactifs et des produits.
2. Le monoxyde de carbone réagit avec le dioxygène pour produire du dioxyde de carbone jusqu’à
ce que l’équilibre suivant soit atteint :
2 CO(g) + O2(g) ⇋ 2 CO2(g)
Si on laisse s’échapper le dioxyde de carbone, comment varie la concentration de chacune des
substances de la réaction ?
A. [CO] diminue, [O2] diminue, [CO2] augmente.
B. [CO] augmente, [O2] augmente, [CO2] diminue.
C. [CO] diminue, [O2] augmente, [CO2] diminue.
D. [CO] augmente, [O2] augmente, [CO2] augmente.
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 7 N38327
2
Nom : Groupe : Date :
3. Soit la réaction suivante à l’équilibre :
4 HCl(g) + O2(g) ⇋ 2 H2O(l) + 2 Cl2(g)
Si on injecte du dioxygène dans le système, comment varie la concentration de l’eau ?
A. La concentration de l’eau ne change pas, puisque l’eau est liquide.
B. La concentration de l’eau ne change pas, puisqu’aucune réaction n’est favorisée.
C. La concentration de l’eau augmente, puisque la réaction directe est favorisée.
D. La concentration de l’eau diminue, puisque la réaction inverse est favorisée.
4. Lorsque Charles mélange une solution de nitrate d’argent avec du dichlorure de cuivre, il se produit
une réaction de précipitation, jusqu’à ce que l’équilibre suivant soit atteint :
2 AgNO3(aq) + CuCl2(aq) ⇋ 2 AgCl(s) + Cu(NO3)2(aq)
Lequel des changements suivants permet de favoriser la réaction inverse ?
A. L’ajout de nitrate d’argent (AgNO3) solide.
B. L’ajout de dichlorure de cuivre (CuCl2) solide.
C. L’ajout de chlorure d’argent (AgCl) solide.
D. L’ajout de dinitrate de cuivre (Cu(NO3)2) solide.
5. Julie verse un mélange de diiode, d’alcool et d’eau dans un bécher. Après un certain temps, l’équilibre
suivant est atteint :
I2(aq-alcool) + 2 H2O(l) ⇋ I−(aq) + IO3−(aq) + 6 H+(aq)
Lequel des changements suivants permet de favoriser la réaction directe ?
A. L’ajout d’un acide.
B. L’ajout de diiode solide.
C. L’ajout d’eau.
D. L’ajout d’iodure de potassium (KI).
6. Un mélange de N2 et de H2 est placé dans un ballon jusqu’à ce que l’équilibre suivant soit atteint :
N2(g) + 3 H2(g) ⇋ 2 NH3(g) ΔH = −92,2 kJ
Comment varie la concentration de chacune des substances de la réaction si on chauffe le système ?
A. [N2] augmente, [H2] augmente, [NH3] augmente.
B. [N2] augmente, [H2] augmente, [NH3] diminue.
C. [N2] diminue, [H2] diminue, [NH3] diminue.
D. [N2] diminue, [H2] diminue, [NH3] augmente.
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 7 N38327
3
Nom : Groupe : Date :
7. Après une diminution de la température, la réaction inverse d’un des systèmes suivants est favorisée.
De quel système s’agit-il ?
A. C(s) + 2 H2(g) ⇋ CH4(g) ΔH = −75,2 kJ
B. 4 HCl(g) + O2(g) ⇋ 2 Cl2(g) + 2 H2O(g) + 131 kJ
C. H2(g) + I2(g) + 53 kJ ⇋ 2 HI(g)
D. C2H2(g) + 2 H2(g) ⇋ C2H6(g) + Énergie
8. Lequel des systèmes suivants ne subit pas de changement après une variation de la pression ?
A. Zn(s) + 2 HCl(aq) ⇋ ZnCl2(aq) + H2(g)
B. C(s) + O2(g) ⇋ CO2(g)
C. HCl(g) + NH3(g) ⇋ NH4Cl(s)
D. CO(g) + 2 H2(g) ⇋ CH3OH(g)
9. Soit la réaction suivante à l’équilibre :
C2H6(g) + Énergie ⇋ C2H2(g) + 2 H2(g)
Si on augmente la pression du système, comment varie la concentration de chacune des substances
de la réaction ?
A. [C2H6] augmente, [C2H2] diminue, [H2] diminue.
B. [C2H6] diminue, [C2H2] augmente, [H2] augmente.
C. [C2H6] diminue, [C2H2] diminue, [H2] diminue.
D. [C2H6] augmente, [C2H2] augmente, [H2] augmente.
10. Jean-François place du dihydrogène et du diiode dans un ballon. L’équilibre suivant est atteint.
H2(g) + I2(g) + 53 kJ ⇋ 2 HI2(g)
Incolore Violet Incolore
Si Jean-François ajoute un catalyseur dans le ballon, qu’arrive-t-il à la couleur du système ?
A. La couleur violette devient moins intense, parce que la réaction directe est favorisée.
B. La couleur violette devient moins intense, parce que le catalyseur diminue la concentration
de l’ensemble des substances.
C. La couleur n’est pas modifiée, puisqu’aucune réaction n’est favorisée.
D. La couleur violette devient plus intense, parce que la réaction inverse est favorisée.
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 7 N38327
4
Nom : Groupe : Date :
7.3 LES APPLICATIONS DE L’ÉQUILIBRE
1. Soit la réaction suivante à l’équilibre :
CaCl2(aq) + Na2C2O4(aq) ⇋ CaC2O4(s) + 2 NaCl(aq)
Laquelle des modifications suivantes permet d’obtenir plus de CaC2O4 ?
A. Augmenter la pression.
B. Retirer le CaC2O4 au fur et à mesure qu’il se forme.
C. Ajouter du dichlorure de calcium.
D. Ajouter un catalyseur.
2. L’acide chlorhydrique réagit en présence du dioxygène jusqu’à ce que l’équilibre suivant soit atteint :
4 HCl(g) + O2(g) ⇋ 2 H2O(g) + 2 Cl2(g) + 113 kJ
Laquelle des modifications suivantes permet d’obtenir plus de dichlore ?
A. Diminuer la pression.
B. Augmenter la température.
C. Retirer le dioxygène.
D. Liquéfier l’eau.
3. Dans l’industrie, le méthanol est produit par la réaction entre le monoxyde de carbone
et le dihydrogène. Cette réaction est illustrée par l’équation suivante :
CO(g) + 2 H2(g) ⇋ CH3OH(g) + Énergie
Lequel des énoncés suivants présente une condition qui favorise la production du méthanol ?
A. Une augmentation de la température.
B. Une augmentation de la pression.
C. Le retrait du dihydrogène.
D. L’ajout d’un catalyseur approprié.
4. Il existe plusieurs méthodes de production du dihydrogène. L’une d’entre elles consiste à faire réagir
un acide avec un métal. Par exemple :
Mg(s) + 2 HCl(aq) ⇋ MgCl(aq) + H2(g)
Laquelle des modifications suivantes ne permet pas de favoriser la production du dihydrogène ?
A. Retirer le dihydrogène au fur et à mesure qu’il se forme.
B. Diminuer la pression.
C. Ajouter du magnésium.
D. Augmenter la concentration de l’acide chlorhydrique.
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 7 N38327
5
Nom : Groupe : Date :
5. L’ammoniac peut être produit selon l’équation suivante :
N2(g) + 3 H2(g) ⇋ 2 NH3(g) ΔH = −92,2 kJ
Lesquelles des modifications suivantes permettent de produire de l’ammoniac plus rapidement ?
A. Diminuer la température.
B. Ajouter un catalyseur.
C. Augmenter la pression.
D. Injecter du diazote.
SYNTHÈSE DU CHAPITRE 7
1. Une augmentation de la pression favorise la réaction directe d’un des systèmes suivants.
De quel système s’agit-il ?
A. H2(g) + I2(g) ⇋ 2 HI(g)
B. C(s) + O2(g) ⇋ CO2(g)
C. PCl5(g) ⇋ PCl3(g) + Cl2(g)
D. 4 HCl(g) + O2(g) ⇋ 2 H2O(g) + 2 Cl2(g)
2. Une augmentation de la température ne favorise pas la réaction directe d’un des systèmes suivants.
De quel système s’agit-il ?
5
A. N2(g) + O2(g) ⇋ N2O5(g) ΔH = +42,5 kJ
2
B. C(s) + 2 H2(g) ⇋ CH4(g) ΔH = −75 kJ
C. N2(g) + O2(g) + 181 kJ ⇋ 2 NO(g)
D. H2O(l) ⇋ H2O(g)
3. Laquelle des modifications suivantes favorise toujours la réaction directe d’un système à l’équilibre ?
A. L’augmentation de la température.
B. L’augmentation de la pression.
C. L’ajout d’un catalyseur.
D. La diminution de la concentration d’un produit.
4. Soit la réaction suivante :
2 SO2(g) + O2(g) ⇋ 2 SO3(g) + 106 kJ
À quel moment peut-on dire que l’équilibre est atteint ?
A. Lorsque la concentration de SO2 est égale à la celle de SO3.
B. Lorsque les concentrations de toutes les substances de la réaction demeurent constantes.
C. Lorsque les concentrations de toutes les substances de la réaction sont égales.
D. Lorsque la concentration de SO2 est le double de celle de O2.
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 7 N38327
6
Nom : Groupe : Date :
5. Émilie place du diazote et du dihydrogène dans un contenant. Après un certain temps,
l’équilibre suivant est atteint :
N2(g) + 3 H2(g) ⇋ 2 NH3(g) + Énergie
Quel est l’effet d’une augmentation de la concentration du dihydrogène sur la concentration
de chacune des substances de la réaction ?
A. [N2] diminue, [H2] diminue, [NH3] augmente.
B. [N2] augmente, [H2] augmente, [NH3] augmente.
C. [N2] diminue, [H2] augmente, [NH3] augmente.
D. [N2] augmente, [H2] augmente, [NH3] diminue.
6. Il est possible d’éliminer certains ions nuisibles présents dans l’eau à l’aide d’une réaction
de précipitation. Par exemple, l’ion plomb précipite en présence de l’ion polyatomique sulfate
selon l’équation suivante :
Pb2+(aq) + SO42−(aq) ⇋ PbSO4(s)
Comment peut-on obtenir une plus grande quantité de précipité ?
A. En retirant le sulfate de plomb au fur et à mesure de sa formation.
B. En ajoutant du sulfate de disodium (Na2SO4).
C. En ajoutant un catalyseur.
D. En augmentant la pression.
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 7 N38327
7
Nom : Groupe : Date :
DÉFIS DU CHAPITRE 7
1. Observez chacun des graphiques suivants et indiquez s’il peut illustrer un système qui est parvenu
à l’équilibre. Expliquez chacune de vos réponses.
a) b)
c) d)
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 7 N38327
8
Nom : Groupe : Date :
2. Très abondant sur la Terre, le calcaire est une roche sédimentaire constituée principalement
de carbonate de calcium. La chaux, produit dérivé de cette roche, comporte de multiples applications,
dont la fabrication du ciment, du béton, du verre et de la pâte à papier, l’amélioration du pH des sols
agricoles, ainsi que le traitement de l’eau.
On peut représenter l’équilibre entre le carbonate de calcium et la chaux à l’aide
des équations suivantes :
Sous l’action de la chaleur, le carbonate de calcium se décompose
pour produire de la chaux vive (CaO), selon l’équation suivante :
CaCO3(s) ⇋ CO2(g) + CaO(s)
En présence d’eau, la chaux vive se transforme en chaux éteinte
(Ca(OH)2) :
CaO(s) + H2O(l) ⇋ Ca(OH)2(s)
Pour finir, le dioxyde de carbone présent dans l’atmosphère
réagit avec la chaux éteinte pour produire à nouveau du
carbonate de calcium :
Ca(OH)2(s) + CO2(g) ⇋ CaCO3(s) + H2O(l)
Le schéma ci-contre illustre sommairement le cycle que
ces réactions entraînent.
Quel est l’effet de l’augmentation du taux de dioxyde de carbone dans l’atmosphère sur la production
du carbonate de calcium ? Expliquez votre réponse.
3. Le graphique suivant illustre la vitesse de la réaction
directe et de la réaction inverse en fonction du temps
pour un système à l’équilibre.
Si on ajoute un catalyseur à ce système,
comment sera modifiée la courbe du graphique ?
Expliquez votre réponse.
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 7 N38327
9
Vous aimerez peut-être aussi
- Os Chimie Corrige ch5Document21 pagesOs Chimie Corrige ch5Amellie Gendron100% (7)
- CHI5062 Eval ch8Document15 pagesCHI5062 Eval ch8Sarah Taibi El KettaniPas encore d'évaluation
- Exercices Post-Examen 2 - FDocument8 pagesExercices Post-Examen 2 - FSarah Taibi El KettaniPas encore d'évaluation
- CHI5062 Eval ch7Document5 pagesCHI5062 Eval ch7Sarah Taibi El KettaniPas encore d'évaluation
- Exercices: L'énergie Et Ses FormesDocument29 pagesExercices: L'énergie Et Ses FormesSarah Taibi El Kettani100% (2)
- Exercices: Qu'est-Ce Que La Vitesse de Réaction ?Document27 pagesExercices: Qu'est-Ce Que La Vitesse de Réaction ?Sarah Taibi El KettaniPas encore d'évaluation
- Exercices: La Réactivité Chimique Des GazDocument12 pagesExercices: La Réactivité Chimique Des GazSarah Taibi El Kettani67% (3)
- Exercices: Les Lois Simples Des GazDocument29 pagesExercices: Les Lois Simples Des GazSarah Taibi El Kettani100% (1)
- Os Chimie ch5 Ex Suppl CorrDocument16 pagesOs Chimie ch5 Ex Suppl CorrSarah Taibi El KettaniPas encore d'évaluation
- Os Chimie ch6 Ex SupplDocument12 pagesOs Chimie ch6 Ex SupplSarah Taibi El KettaniPas encore d'évaluation
- Os Chimie ch6 Ex Suppl CorrDocument12 pagesOs Chimie ch6 Ex Suppl CorrSarah Taibi El Kettani100% (1)
- Boite Pharmacie (BPH) Chek-List ModuleDocument3 pagesBoite Pharmacie (BPH) Chek-List Modulekassou hse100% (2)
- Chimie 2nd C Evaluation 3Document2 pagesChimie 2nd C Evaluation 3FREDERIC NOUGEPas encore d'évaluation
- TP 2 Godet FernandezDocument5 pagesTP 2 Godet Fernandezsos cissonPas encore d'évaluation
- Article IDDocument4 pagesArticle IDImoona iiPas encore d'évaluation
- Etude de La Qualite Des Huiles - Mohammed FEDOUL - 4025Document43 pagesEtude de La Qualite Des Huiles - Mohammed FEDOUL - 4025TAMKOUKT MohamedPas encore d'évaluation
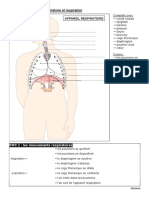
- Appareil Respiratoire Et RespirationDocument4 pagesAppareil Respiratoire Et Respirationwaly sowPas encore d'évaluation
- M GP - Env 2019 07Document67 pagesM GP - Env 2019 07Mebarek Bahri100% (1)
- Fiche TD GntiqueDocument10 pagesFiche TD Gntiquesky larPas encore d'évaluation
- Support de Formation CBRDocument90 pagesSupport de Formation CBRaziz baaouichPas encore d'évaluation
- Exercices Sur Réaction Chimique 3emeDocument1 pageExercices Sur Réaction Chimique 3emeIbrahima Thiaw100% (1)
- Série D'exercices #8 - Sciences Physiques Masse Volumique Et Densité - Les États Physiques de La Matière - 1ère AS (2011-2012) MR Adam BoualiDocument2 pagesSérie D'exercices #8 - Sciences Physiques Masse Volumique Et Densité - Les États Physiques de La Matière - 1ère AS (2011-2012) MR Adam BoualiLotfi HammamiPas encore d'évaluation
- Tehnologie Farmaceutica Vol 4Document340 pagesTehnologie Farmaceutica Vol 4Funebre NimoPas encore d'évaluation
- Classification Des Acides Et Des BasesDocument3 pagesClassification Des Acides Et Des BasesMohamed A S Doumbia100% (1)
- Trans 2 Sens Cours FilaliDocument5 pagesTrans 2 Sens Cours FilaliMohammed HassaniPas encore d'évaluation
- Nernst PDFDocument2 pagesNernst PDFPS HadjerPas encore d'évaluation
- J1302 - Transfert de Matières Et de Chaleur Au Sein Des AdsorbantsDocument8 pagesJ1302 - Transfert de Matières Et de Chaleur Au Sein Des AdsorbantsfahimPas encore d'évaluation
- Récap TP 2018 2019 FR PDFDocument49 pagesRécap TP 2018 2019 FR PDFGhina El EssPas encore d'évaluation
- Cours Respiratoire1Document117 pagesCours Respiratoire1Rachida FAOUZI100% (1)
- c03 Lubrification A05Document26 pagesc03 Lubrification A05haoues23Pas encore d'évaluation
- Quantité de HHO Idéale - Générateur HHODocument5 pagesQuantité de HHO Idéale - Générateur HHOFlorine RazaiarimalalaPas encore d'évaluation
- COURS Chim224 VG 2022-2023Document87 pagesCOURS Chim224 VG 2022-2023Salim SaoudPas encore d'évaluation
- Ziani Module Biologie Moléculaire Et Génie Génétique L3 MicobiologieDocument122 pagesZiani Module Biologie Moléculaire Et Génie Génétique L3 MicobiologieOwassiPas encore d'évaluation
- Dermatites de Contact Professionnelles Chez Les Personnels de SantéDocument19 pagesDermatites de Contact Professionnelles Chez Les Personnels de Santéfayssal bouakazPas encore d'évaluation
- D49 3017 FR PDFDocument13 pagesD49 3017 FR PDFJose ValenciaPas encore d'évaluation
- Chapitre N 14 - LES ACIDES AMINESDocument10 pagesChapitre N 14 - LES ACIDES AMINESIngenieur Agro100% (1)
- 31 - Pression-Temperature - RélationDocument1 page31 - Pression-Temperature - RélationLucaPas encore d'évaluation
- 15 C3a9lectrolyseDocument10 pages15 C3a9lectrolyseazerfazPas encore d'évaluation
- Recueil Produits Chimiques 2-12-11Document114 pagesRecueil Produits Chimiques 2-12-11Fatimazahra SahriPas encore d'évaluation
- AcétonitrileDocument11 pagesAcétonitrileyodhurPas encore d'évaluation
- ChapII BIOENERGETIQUEDocument16 pagesChapII BIOENERGETIQUEbessama84100% (1)