Académique Documents
Professionnel Documents
Culture Documents
Chimie Revision
Transféré par
runes_of_magic22Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Chimie Revision
Transféré par
runes_of_magic22Droits d'auteur :
Formats disponibles
XIe YuanHong
Chapitre 9: La thorie des collisions 9.1 Les types de collisions Dans une collision lastique, les particules des ractifs se heurtent les unes aux autres et il ny a aucune raction. Dans une collision efficace, les particules de ractifs se heurtent et entranent une raction qui les transforme en produit. Toutefois, afin que la transformation ait lieu, les particules de ractifs doivent se heurter dune orientation approprie (gomtrie de collision approprie) et doivent aussi avoir une nergie de collision gale ou suprieure lnergie dactivation (Ea) de la raction. Afin de briser les liaisons des particules dans les ractifs et commencer former des liaisons dans les produits, les ractifs doivent entrer en collision avec une nergie de collision suffisante. Cette nergie dpend de lnergie cintique des particules qui se heurtent. La temprature est une mesure de lnergie cintique moyenne des particules dune substance. La courbe de distribution de Maxwell permet de reprsenter la distribution du nombre de collisions entre les particules dune substance une temprature donne, en fonction de lnergie cintique de chaque collision. La ligne pointille du graphique indique le niveau minimal dnergie dactivation que doivent possder les particules pour quil y ait une raction. La partie ombre dsigne donc toutes les particules de produits ayant une nergie gale ou suprieure lnergie dactivation.
XIe YuanHong
La vitesse de raction est dicte par la valeur de lnergie dactivation. Ainsi, plus lnergie dactivation est grande, plus la raction est lente puisquil y a peu de particules possdant cette quantit dnergie et ainsi atteindre le niveau de lnergie dactivation. linverse, les ractions qui ont une nergie dactivation faible sont des ractions plus rapides. De plus, le nombre de collisions efficaces pour une certaine priode de temps peut aussi influencer la vitesse de raction. Ainsi, la vitesse de raction augmentera lorsquil y a plus de collisions efficaces et vice versa. Toute variation de la nature des ractifs, de la concentration de ces-derniers, de la surface de contact entre les ractifs ainsi que lajout dun catalyseur peuvent tous modifier la vitesse de raction. (Voir laboratoires concerns pour plus dinformations) 9.2 Le mcanisme ractionnel expliqu par la thorie des collisions Lorsquune collision entre les particules de ractif est efficace, le complexe activ se forme puis se rompt en formant de nouvelles particules de produit. Toutefois, la raction peut se drouler en plusieurs tapes. Ainsi, dans une raction complexe, il y a plusieurs tapes quon nomme ractions lmentaires. Ltape dterminante du mcanisme ractionnel est celle dont le niveau dnergie du complexe activ est le plus lev. Elle dicte donc la vitesse de la raction globale. Chapitre 10 : Les facteurs qui influencent la vitesse de raction Normalement, les ractions homognes sont plus rapides que celles htrognes, toutefois, deux ractions homognes qui font intervenir des particules de ractifs diffrentes ne se droulent pas ncessairement la mme vitesse. Les cinq facteurs qui influencent la vitesse de raction est la nature des ractifs, la surface de contact du ractif, la concentration des ractifs, la temprature du milieu ractionnel et finalement, les catalyseurs. En lien avec la nature des ractifs, la vitesse de raction dpend surtout de deux facteurs : - la phase dans laquelle les ractifs se trouvent. Aqueuse > Gazeuse > Liquide > Solide La raction est la plus rapide dans le cas des ions aqueuse parce que ces derniers sont disperss uniformment dans la solution et sont entours de molcules deau auxquelles ils sont faiblement lis. Ainsi, il leur faut moins dnergie pour briser leur lien et la raction se fait donc plus rapidement. - le nombre et la force des liaisons briser dans les ractifs. Lnergie dactivation dune raction reprsente la barrire dnergie quil faut franchir pour quune raction se produise. Lnergie interne contenue dans les particules des ractifs, que ce soit lnergie potentiel intramolculaire, qui unissent les atomes de ractif
XIe YuanHong
entre eux dans les molcules, ou lnergie cintique, aussi appele enthalpie, correspondra alors la somme de toutes ces nergies. Plus le niveau dnergie de ces forces de liaison intramolculaire est lev, plus il est difficile de briser les molcules pour quelles forment le complexe activ. Ainsi, il leur faudra alors plus dnergie pour performer une raction. Une augmentation de la surface de contact du ractif augmentera aussi la vitesse de raction. En effet, les surfaces de contact accru entre les ractifs permettront une augmentation de collisions efficaces et donc, une augmentation de la vitesse de raction. videmment, plus le solide est sous forme de particules fines, plus la surface de contact augmente et donc plus la vitesse sera grande. Le troisime facteur qui influence la vitesse de raction est la vitesse de raction. Plus la concentration des ractifs est leve, plus la vitesse de raction est grande. En effet, lorsquon augmente la raction, le nombre de particules de ractifs prsents est plus grand, ainsi, il y a plus de collisions efficaces et en se basant sur la thorie de collisions, nous pouvons alors dduire que la vitesse augmentera en consquent. La loi des vitesses de raction est une relation mathmatique entre la vitesse de raction et la concentration des ractifs, et elle dpend des coefficients stchiomtriques des ractifs qui apparaissent dans lquation balance suivante : V=k[A]x[B]y o x et y tant les coefficients stchiomtriques des ractifs et k, la constante de
vitesse. Gnralement, une augmentation de la temprature du milieu ractionnel augmente la vitesse de raction. Ainsi, dans la graphique de la courbe de Maxwell, la courbe de la raction dont la temprature a t augmente sera plus aplatie. Ainsi, une plus grande partie des particules ont assez dnergie pour ragir. Cela sexplique par une augmentation de lnergie cintique des particules de ractif lorsque nous haussons la temprature. Ainsi, les particules bougent plus vite, permettant une augmentation de collisions efficaces et donc aussi, augmentera la vitesse de raction. Les catalyseurs sont des substances qui augmentent la vitesse de raction sans changer le rsultat de la transformation et sans tre consomm par la raction. Ainsi, il ne fait nullement varier le nombre de particules de ractifs, ni leur donne de lnergie. Lutilisation dun catalyseur ne fait que baisser lnergie dactivation, ce qui permet plus de particules davoir lnergie cintique suffisante pour ragir. Un inhibiteur, par contre, diminuera la vitesse de raction, agissant en augmentant lnergie dactivation de la raction chimique.
XIe YuanHong Chapitre 11 Lquilibre chimique Un quilibre statique est ce qui reste au mme point ou qui est maintenu immobile alors quun quilibre dynamique est le rsultat de deux processus opposs seffectuant la mme vitesse de sorte quaucun changement visible na lieu dans le systme ractionnel. Trois types dquilibre dynamique existent : -lquilibre des phases ou quilibre physique -lquilibre de solubilit -lquilibre chimique Un quilibre est qualifi dquilibre de phases quand une seule substance se trouve dans plusieurs phases lintrieur dun systme la suite dune transformation physique (e.g dans une bouteille de boisson gazeuse, le CO2 passe de ltat gazeuse ltat liquide.) Lquilibre de solubilit est ltat dans lequel un solut est dissous dans un solvant ou une solution et o le solut en excs est en contact avec la solution sature. (e.g dans une tasse de th, on verse beaucoup de sucre jusqu ce quil y a un dpt de sucre au fond de la tasse. vue dil, il ne semble pas y avoir de changement, pourtant le sucre de dissous toujours, mais la mme quantit de sucre dissoute sest solidifi en mme temps que la dissolution.) Lquilibre chimique est un quilibre dynamique rsultant de deux ractions chimiques opposs qui seffectuent la mme vitesse, laissant ainsi la composition du systme inchange. (e.g H2(g) + I2(g)2HI(g) ) Certaines ractions sont irrversibles, cest--dire quelles ne peuvent se produire dans un seul sens alors que dautres sont rversibles et ces-dernires sont donc des ractions pouvant se produire dans les deux sens. Lirrversibilit dune raction est souvent cause par lincapacit du systme dcomposer les produits en ractifs. La combustion dune bche en est le parfait exemple car il est impossible de refaire du bois et de loxygne partir de la cendre et de la fume. Ainsi, une raction est irrversible lorsquelle est complte et elle cesse lorsquun seul ou tous les ractifs sont entirement consomms. Dans le cas des ractions rversibles, les ractifs se transforment en produits, et les produits se transforment leur tour pour redevenir des ractifs. Et lorsque la vitesse de ces deux ractions opposes est gale, lquilibre chimique est atteint. Toutefois, il y a trois conditions ncessaires pour obtenir lquilibre : il doit avoir une transformation rversible dans un milieu ferm dont les proprits macroscopiques restent constantes. Lquilibre ne peut donc tre atteint que seulement si la raction est rversible. De plus, lorsquun ou plusieurs produits issus dune raction chimique se dissipent dans le milieu environnant, il sera impossible que la raction atteigne lquilibre puisquil y aura alors un change de matire entre le systme et le milieu environnant. (Bien sr, si la raction nimplique pas dchange de matire avec le milieu environnant, la raction peut se produire dans un systme ouvert) Voila pourquoi il faut que la raction se passe dans un systme ferm dans le cas o des produits sous forme gazeuse sont impliqus. Finalement, bien que ltat dquilibre soit un changement visible lil nu, il ny a plus de changements
XIe YuanHong visibles lorsque lquilibre est atteint. Tout semble immobile, comme peuvent le tmoigner les proprits macroscopiques des substances, cest--dire la couleur, le volume, le pH, la temprature, la pression, etc. Bref, des proprits qui sont observables ou mesurables. Lquilibre dans un systme se caractrise donc par la constance de ces proprits macroscopiques. Le principe de Le Chatelier stipule que pour chaque changement qui se produit dans un systme, ce-dernier va ragir de manire sopposer partiellement ce changement jusqu ce que le systme ait atteint un nouvel tat dquilibre. Lancien quilibre ne pourra donc plus jamais atteint. Afin de sopposer ces modifications, le systme va toujours favoriser un des deux sens de la raction, soit le sens direct ou inverse. Selon le principe de Le Chatelier, dans un systme lquilibre : -une augmentation de la concentration dune substance dplace lquilibre en favorisant la raction permettant de diminuer la concentration de cette substance et vice versa. -toute augmentation de la temprature influencera le systme de sorte quil favorisera la raction endothermique et vice versa. -toute augmentation de la pression par une diminution de volume entrainera le systme favoriser la raction qui produit le moins de molcules de produits. Une augmentation de la pression entrainera leffet inverse. Lajout dun catalyseur ne favorisera aucun ct de la raction puisque cela fera juste que lquilibre sera atteinte plus rapidement. Chapitre 12 Laspect quantitatif de lquilibre chimique La constante dquilibre (Kc), aussi appele la loi de lquilibre, est une relation tablissant qu une temprature donne, dans toute raction chimique lmentaire lquilibre, il y a un rapport entre la concentration des produits et celle des ractifs. Cette loi sexprime par lexpression suivante : Kc= [C]c [D]d o a, b, c et d correspondent aux coefficients stchiomtriques des substances [A]a [B]b Prenons par exemple la raction suivante : aA(g)+bB(g)cC(g)+dD(g) Lorsque le systme est lquilibre, la vitesse du sens direct et inverse est pareille. Ainsi : Vdir= kdir [A]a [B]b Vinverse= kinverse [C]c [D]d Vdir = Vinverse kdir [A]a [B]b = kinverse [C]c [D]d
kdirect = [C]c [D]d = Kc kinverse [A]a [B]b La constant dquilibre de la raction inverse est par consquent : 1 Kc Pour les exemples de calculs de la constance dquilibre laide des concentrations initiales et de la concentration dune substance, voir manuel p.316-317
Vous aimerez peut-être aussi
- Luxembourg ChiffresDocument56 pagesLuxembourg ChiffresyeuminhPas encore d'évaluation
- Activite TP05 Composition de L Atmosphere Fiche - EleveDocument3 pagesActivite TP05 Composition de L Atmosphere Fiche - EleveEmma RoemerPas encore d'évaluation
- 1 1infra-1 2caracterDocument95 pages1 1infra-1 2caracterwzaydanPas encore d'évaluation
- 1.SHP IntroDocument26 pages1.SHP Introfranck nzauPas encore d'évaluation
- Fonds Mohammed VI Pour L'investissementDocument5 pagesFonds Mohammed VI Pour L'investissementasma asmaPas encore d'évaluation
- Guidecourtscouverts 1Document42 pagesGuidecourtscouverts 1maryam haqiqatPas encore d'évaluation
- Côte D'ivoire TEMPLATE - Bassam 30juinDocument2 pagesCôte D'ivoire TEMPLATE - Bassam 30juinDeloumeauxPas encore d'évaluation
- Droit de La RetractationDocument4 pagesDroit de La RetractationKarima KhribchiPas encore d'évaluation
- (GRAMM-R. Études de Linguistique Française - GRAMM.Document220 pages(GRAMM-R. Études de Linguistique Française - GRAMM.Boujemaa Rbii100% (1)
- 11 GranulatDocument32 pages11 GranulatFatre 1980Pas encore d'évaluation
- Ankylostomose L3Document52 pagesAnkylostomose L3Sahouin Claude Medard100% (2)
- Attache Territorial - Composition 2014Document6 pagesAttache Territorial - Composition 2014CarolinePas encore d'évaluation
- Guide Santé SONEPAR ActifsDocument36 pagesGuide Santé SONEPAR ActifsmarcotkPas encore d'évaluation
- 2014 Liban Exo1 Sujet LaitYaourt 6ptsDocument4 pages2014 Liban Exo1 Sujet LaitYaourt 6ptsAlicherif BenaissaPas encore d'évaluation
- Lettre de MotivationDocument2 pagesLettre de MotivationbhhbsckPas encore d'évaluation
- COURS Excel 2007 GraphiqueDocument15 pagesCOURS Excel 2007 GraphiqueDje RachidPas encore d'évaluation
- Mémoire de Fin D'année - Google AnalyticsDocument66 pagesMémoire de Fin D'année - Google Analyticsjollet_pierre+scribd100% (1)
- Tenda ModemDocument2 pagesTenda Modemtighrine faredjPas encore d'évaluation
- Guide Installation RenolinkDocument2 pagesGuide Installation Renolinklacan illisiblePas encore d'évaluation
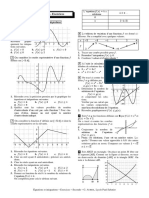
- Équations Et Inéquations - Exercices: UriolDocument3 pagesÉquations Et Inéquations - Exercices: UriolMinecraft ArabicPas encore d'évaluation
- Document 567901Document236 pagesDocument 567901Bayari ArPas encore d'évaluation
- Le Commerce Frontalier en Afrique CentraDocument525 pagesLe Commerce Frontalier en Afrique CentraVanessa HouingPas encore d'évaluation
- Chap2 - CollecteDeDonnéesDocument2 pagesChap2 - CollecteDeDonnéesوليد بن عمرPas encore d'évaluation
- Manuel Utilisateur Configuration, Test Et Exécution de Programmes CNDocument348 pagesManuel Utilisateur Configuration, Test Et Exécution de Programmes CNetudes ameurplasticsPas encore d'évaluation
- Le Travail SaisonnierDocument3 pagesLe Travail SaisonnierMohamed LaarjPas encore d'évaluation
- La Planète Terre - SVTDocument45 pagesLa Planète Terre - SVTnsalemPas encore d'évaluation
- Audit - Integrité Et DimensionDocument18 pagesAudit - Integrité Et DimensionB.I94% (16)
- CourDocument84 pagesCourKim Jae-hwaPas encore d'évaluation
- TD1.D1 EnvironnementDeTravail 1Document15 pagesTD1.D1 EnvironnementDeTravail 1Nasreddine MarzoukiPas encore d'évaluation
- Liason ChimiqueDocument7 pagesLiason Chimiquesalah mebrouk100% (1)