Académique Documents
Professionnel Documents
Culture Documents
Devoir de Controle 2 2èmme 2023
Transféré par
hbibTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Devoir de Controle 2 2èmme 2023
Transféré par
hbibDroits d'auteur :
Formats disponibles
Ministère de l’éduction 2022 /2023
Devoir de contrôle n°2 Durée :1H
SCIENCES PHYSIQUES Mr : Assalah. A
Lycée rue Ibn Sina Kébili 2èmeannée
.Sc3
➢ Donner les expressions littérales avant l’application numérique. Nom :…………………………………..
➢ Il est absolument interdit d’utiliser le correcteur. Prénom :………………………………
Chimie (8 points)
On donne:
M(N) 14 g.mol-1 ; M(O) = 16 g.mol-1 ;M(Na) = 23 g.mol-1;M(S)= 32 g.mol-1 ;et . M(Ag) = 108 g. mol-1
Le sulfate de sodium (Na2SO4) est un électrolyte fort très soluble dans l’eau pure.
On dissout dans l’eau pure une masse m1 de sulfate de sodium, afin d’obtenir une solution (S1) de
concentration molaire C1 = 0,04 mol.L-1 et de volume V1 =250 mL
1-
a- Corriger les phrases suivantes : (A2,1,5pt)
❖ Le sulfate de sodium se dissocie partiellement dans l’eau.
……………………………………………………………………………………………………………………………………………..
❖ La dissociation ionique du sulfate de sodium dans l’eau fournit les ions Na+ et SO4-
………………………………………………………………………………………………………………………………………………
❖ Le sulfate de sodium conduit le courant électrique mieux que l’eau pure.
…………………………………………………………………………………………………………………………………...............
b- Ecrire l’équation de dissociation ionique de (Na2SO4) dans l’eau pure. (A2,0.5pt)
………………………………………………………………………………………………………………………………………………
c- Calculer m1. (A2,0.75pts)
………………………………………………………………………………………………………………………………………………
…..……………………………………………………………………………………………………………………………………………
d- Déterminer la molarité des ions provenant de cette ionisation. (A2,1pt)
………………………………………………………………………………………………………………………………………………
………………………………………………………………………………………………………………………………………………
2- On prélève de la solution (S1) un volume Vp = 100 cm3, auquel on ajoute une solution aqueuse (S2) de
nitrate d’argent (AgNO3) de concentration C2 =0,4 mol.L-1 de volume V2 =100 cm3.
a- Qu’observe-t-on ? (A2,0.25pt)
…………………………………………………………………………………………………………………………………………………..
b- Préciser la nature de la réaction qui a eu lieu. (A2,0.5pt)
…………………………………………………………………………………………………………………………………………………
………………………………………………………………………………………………………………………………………………..
c- Ecrire l’équation globale puis l’équation simplifiée de cette réaction chimique. De quoi dépend cette
réaction ? (A2,0.75ps)
…………………………………………………………………………………………………………………………………………………
…………………………………………………………………………………………………………………………………………………
…………………………………………………………………………………………………………………………………………………
d- Montrer que l’un des deux réactifs est en excès par rapport à l’autre. (A2,1,5 pts)
…………………………………………………………………………………………………………………………………………………
…………………………………………………………………………………………………………………………………………………
e- Calculer la masse m du produit obtenu. Donner son nom. (C, 1,25 pt)
……………………………………………………………………………………………………………………………………………………………….
………………………………………………………………………………………………………………………………………………………………
Physique (12 points)
Exercice 1(3,5points)
On visualise sur l’écran d’un oscilloscope, la tension délivrée par un GBF
1- Compléter les phrases suivantes :( A1, 2pots)
✓ La tension est variable car elle…………………………………………………………………………………………………….
……………………………………………………………………......................................................................................................
.
Lycée Ibn Sina Kébili Page 1
…………………………………………………………………………………………………
✓ La tension est périodique car elle……………………………………..
…………………………………………………………………………………………………
……………………………………………………………………………………………….
✓ La tension est alternative car elle…………………………………..
…………………………………………………………………………………………………
…………………………………………………………………………………………………
…………………………………………………………………………………………………
…………………………………………………………………………………………………
2- On associe à ce générateur une diode D et un résistor de
résistance R comme l'indique la figure -contre.
a- Représenter les fils de connexions reliés à l'oscilloscope pour
visualiser la tension aux bornes du résistor. (A2,0,5pt)
b- Représenter avec la même échelle de la figure-1- la tension observée sur
l'oscilloscope aux bornes du résistor. (A2,1pt)
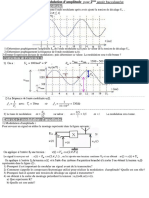
Exercice 2(8,5points)
Sur l’écran d’un oscilloscope, on visualise les tensions électriques u1(t) et u2(t), on
obtient les courbes représentées sur la figure-2-.( ci- dessous)
1-
a- Déterminer, pour les deux tensions, la période commune. Déduire leur fréquence. (A2, 1pt)
…………………………………………………………………………………………………………………………………………………
…………………………………………………………………………………………………………………………………………………
b- Quelle est la valeur de la tension efficace de chaque tension ? (A2,1pt)
…………………………………………………………………………………………………………………………………………………
…………………………………………………………………………………………………………………………………………………
2- Les tensions u1(t) et u2(t), sont en réalité les tensions électriques respectives aux bornes du circuit
primaire et secondaire d’un transformateur.
a- Déterminer le rapport de transformation du transformateur. (A2,1pt)
………………………………………………………………………………………………………………………………………………………
………………………………………………………………………………………………………………………………………………………
b- S’agit-il d’un transformateur abaisseur ou élévateur de tension ? Justifier. (A2,1pt)
…………………………………………………………………………………………………………………………………………………
………………………………………………………………………………………………………………………………………………
c- Comparer N1 et N2 respectivement le nombre de spires du primaire et le nombre de spires du
secondaire. (A2,0.5pt)
………………………………………………………………………………………………………………………………………..
3- Le Transformateur est supposé idéal, le secondaire est traversé par un courant efficace I2.
a- Calculer I2, sachant que le primaire du transformateur est parcouru par un courant efficace
l1 = 0,3A. (C,1pt)
………………………………………………………………………………………………………………………………………………..
b- Déduire la valeur de la puissance électrique développée par le circuit primaire. (A2,1pt)
………………………………………………………………………………………………………………………………………………..
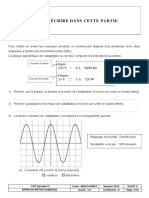
4- La tension u2(t) est redressée par double alternance.
a- Représenter l’allure de la courbe représentative de la tension redressée, (A2, 1pt)
b- Déduire la fréquence et l’amplitude de cette tension redressée. (A2 , 1pt)
………………………………………………………………………………………………………………………………………………….
Lycée Ibn Sina Kébili Page 2
Lycée Ibn Sina Kébili Page 3
Vous aimerez peut-être aussi
- Devoir de Contrôle N°2 - Sciences Physiques - 2ème Sciences (2013-2014) MR ZAOUAM ABDELHAMIDDocument3 pagesDevoir de Contrôle N°2 - Sciences Physiques - 2ème Sciences (2013-2014) MR ZAOUAM ABDELHAMIDMohamed HamdenePas encore d'évaluation
- Dev c3 2018 1ereDocument2 pagesDev c3 2018 1ereBoussetta ZouhaierPas encore d'évaluation
- Proff:Ben Abdallah.A Durée: 1heureDocument2 pagesProff:Ben Abdallah.A Durée: 1heureFatma Ben AbdallahPas encore d'évaluation
- DC1 2eme InfoDocument3 pagesDC1 2eme InfoRiadh MarouaniPas encore d'évaluation
- UntitledDocument2 pagesUntitledaliPas encore d'évaluation
- Devoir de Contrôle N°1 - Physique - 1ère AS (2010-2011) MR Boussada 2Document5 pagesDevoir de Contrôle N°1 - Physique - 1ère AS (2010-2011) MR Boussada 2Hanine HmidaPas encore d'évaluation
- 22 23 Devoir de Controle N2.1annee DYDocument4 pages22 23 Devoir de Controle N2.1annee DYslouati470Pas encore d'évaluation
- Série D'exercices Corrigées Modulation D'amplitude Sujets Bac SC Mathématique p.SBIRO Abdelkrim (WWW - Pc1.ma)Document14 pagesSérie D'exercices Corrigées Modulation D'amplitude Sujets Bac SC Mathématique p.SBIRO Abdelkrim (WWW - Pc1.ma)medPas encore d'évaluation
- Devoir de Contrôle N°1 - Physique - 1ère AS (2011-2012) MR BougazalaDocument2 pagesDevoir de Contrôle N°1 - Physique - 1ère AS (2011-2012) MR BougazalaMaher MessaoudiPas encore d'évaluation
- Devoir de Contrôle N°1 - 2ème Info (2023-2024) MR Abdelhamid GalaiDocument2 pagesDevoir de Contrôle N°1 - 2ème Info (2023-2024) MR Abdelhamid GalaiabdelhamidPas encore d'évaluation
- Devoir de Synthèse N°2 - Technologie - 2ème SC (2012-2013) MR Neji MohamedDocument5 pagesDevoir de Synthèse N°2 - Technologie - 2ème SC (2012-2013) MR Neji MohamedAdel KmimechPas encore d'évaluation
- Devoir de Contrôle N°1 - Sciences Physiques - 1ère AS (2017-2018) MR Khedimi SamiDocument3 pagesDevoir de Contrôle N°1 - Sciences Physiques - 1ère AS (2017-2018) MR Khedimi SamiMariem NejimaPas encore d'évaluation
- Devoir de Syntese 1 - 2eme 2008Document34 pagesDevoir de Syntese 1 - 2eme 2008Kheria ZitouniPas encore d'évaluation
- Devoir de Controle1-2scDocument4 pagesDevoir de Controle1-2scBoussetta ZouhaierPas encore d'évaluation
- Devoir de Cont N°1 1ere A.S2 2020Document3 pagesDevoir de Cont N°1 1ere A.S2 2020Mohamed HamdenePas encore d'évaluation
- Devoir de Controle N°1 1eres2017Document2 pagesDevoir de Controle N°1 1eres2017Daghsni SaidPas encore d'évaluation
- Devoir de Contrôle N°3 2014 2015 (Ramzi Rebai)Document2 pagesDevoir de Contrôle N°3 2014 2015 (Ramzi Rebai)trifi rachedPas encore d'évaluation
- Devoir de Contrôle N°3 - Sciences Physiques - 1ère AS (2014-2015) MR RAMZI REBAIDocument2 pagesDevoir de Contrôle N°3 - Sciences Physiques - 1ère AS (2014-2015) MR RAMZI REBAIwalidPas encore d'évaluation
- Efm108 V2 2022Document2 pagesEfm108 V2 2022testPas encore d'évaluation
- Devoir de Contrôle N°1 - Physique - 1ère AS (2010-2011) MR BoussadaDocument4 pagesDevoir de Contrôle N°1 - Physique - 1ère AS (2010-2011) MR BoussadaHfd NourPas encore d'évaluation
- Devoir de Contrôle N°3 - Physique - 1ère AS (2015-2016) MR Bayrem GhidaouiDocument3 pagesDevoir de Contrôle N°3 - Physique - 1ère AS (2015-2016) MR Bayrem GhidaouiwalidPas encore d'évaluation
- 03 - S - Régional - PC - Fes - Meknes - 2022 (WWW - Pc1.ma)Document4 pages03 - S - Régional - PC - Fes - Meknes - 2022 (WWW - Pc1.ma)قناة الفيزياء و الكيمياء للجميع بالثانوي100% (1)
- 2022 3ac BiofDocument1 page2022 3ac BiofAyoub Benabdeljalil100% (1)
- Devoir de Contrôle N°1 - Sciences Physiques - 1ère AS (2012-2013) MR JLIDI NABILDocument0 pageDevoir de Contrôle N°1 - Sciences Physiques - 1ère AS (2012-2013) MR JLIDI NABILMouf55Pas encore d'évaluation
- Chimie:: L.S. A.T Ksar Gafsa A. S: 2010-2011 Classe: 1S Date: 18/04/2011Document2 pagesChimie:: L.S. A.T Ksar Gafsa A. S: 2010-2011 Classe: 1S Date: 18/04/2011aliPas encore d'évaluation
- 1 ds3 2008 2009Document3 pages1 ds3 2008 2009boustakatbPas encore d'évaluation
- DS2 2022 2023. Copie 2Document2 pagesDS2 2022 2023. Copie 2Riadh MarouaniPas encore d'évaluation
- Efm108 V1 2022Document3 pagesEfm108 V1 2022testPas encore d'évaluation
- Dev Synt1 1sDocument3 pagesDev Synt1 1sSahbi Mabrouki YamenPas encore d'évaluation
- 2018 Est PC-3APIC (WWW - Pc1.ma)Document2 pages2018 Est PC-3APIC (WWW - Pc1.ma)Int AbdellPas encore d'évaluation
- Devoir de Contrôle N°2 - Sciences Physiques - 1ère AS (2010-2011) Mme Liala 2 PDFDocument4 pagesDevoir de Contrôle N°2 - Sciences Physiques - 1ère AS (2010-2011) Mme Liala 2 PDFNadhir SakouhiPas encore d'évaluation
- Efm108 V3 2022Document2 pagesEfm108 V3 2022testPas encore d'évaluation
- Devoir de Contrôle N°1 - Sciences Physiques - 2ème TI (2018-2019) MR Bellili ChokriDocument2 pagesDevoir de Contrôle N°1 - Sciences Physiques - 2ème TI (2018-2019) MR Bellili ChokrigeupierPas encore d'évaluation
- Devoir de Contrôle #1 : Nom Et Prénom ..N° .Document2 pagesDevoir de Contrôle #1 : Nom Et Prénom ..N° .dhouhaPas encore d'évaluation
- Devoir de Synthèse N°1 - Physique - 1ère AS (2010-2011) MR BOUSSADADocument4 pagesDevoir de Synthèse N°1 - Physique - 1ère AS (2010-2011) MR BOUSSADAAicha TennichPas encore d'évaluation
- DS N1 2022 2023 2eme SC ExpDocument3 pagesDS N1 2022 2023 2eme SC ExpAhmed Yassine RattaziPas encore d'évaluation
- 4-Application 1 TD Calcul de Icc ÉquilibréDocument3 pages4-Application 1 TD Calcul de Icc Équilibrédadou1810Pas encore d'évaluation
- Devoir de Synthèse N°3 - Sciences Physiques - 2ème Sciences (2010-2011) MR Adam Bouali 2Document4 pagesDevoir de Synthèse N°3 - Sciences Physiques - 2ème Sciences (2010-2011) MR Adam Bouali 2walidPas encore d'évaluation
- Devoir de Contrôle N°2 - Physique - 2ème Sciences Exp (2006-2007)Document8 pagesDevoir de Contrôle N°2 - Physique - 2ème Sciences Exp (2006-2007)Boubaker ChaabaniPas encore d'évaluation
- Devoir de Synthèse N°2 - Sciences Physiques - 2ème Sciences (2010-2011) MR Adam BoualiDocument4 pagesDevoir de Synthèse N°2 - Sciences Physiques - 2ème Sciences (2010-2011) MR Adam BoualiwalidPas encore d'évaluation
- 2ème Sciences 1Document4 pages2ème Sciences 1Boussetta ZouhaierPas encore d'évaluation
- (Sciences Physiques) : Devoir de Controle N°1Document3 pages(Sciences Physiques) : Devoir de Controle N°1Amine NouarPas encore d'évaluation
- CHIMIE (8 Points) : Fe O O NDocument3 pagesCHIMIE (8 Points) : Fe O O NSakri AwatefPas encore d'évaluation
- Evaluation 2ndeDocument4 pagesEvaluation 2ndeSteve FASSEUPas encore d'évaluation
- Examen INTRA LAAYOUNEDocument7 pagesExamen INTRA LAAYOUNEyounesselghazouani123Pas encore d'évaluation
- Controle 2 - 1 S2 PC 1bac FRDocument3 pagesControle 2 - 1 S2 PC 1bac FRAlae AnouarPas encore d'évaluation
- Devoir de Synthèse N°1 1ére AS 2019Document4 pagesDevoir de Synthèse N°1 1ére AS 2019Mohamed Hamdene100% (1)
- Exercices Corrigées Modulation D'amplitude Sujets Bac SC Mathématique PDFDocument14 pagesExercices Corrigées Modulation D'amplitude Sujets Bac SC Mathématique PDFZolly X666Pas encore d'évaluation
- DCN2-1ere 2021f-ConvertiDocument2 pagesDCN2-1ere 2021f-ConvertiBoussetta ZouhaierPas encore d'évaluation
- Devoir de Contrôle N°1 - Sciences Physiques - 3ème Math (2012-2013) MR Amiche RiadhDocument3 pagesDevoir de Contrôle N°1 - Sciences Physiques - 3ème Math (2012-2013) MR Amiche RiadhdhouhaPas encore d'évaluation
- Devoir de Contrôle N°3 - Physique - 2ème Info (2010-2011) MR Ben Abdejlil SamiDocument4 pagesDevoir de Contrôle N°3 - Physique - 2ème Info (2010-2011) MR Ben Abdejlil SamicLooDyPas encore d'évaluation
- Devoir de Controle N 1Document3 pagesDevoir de Controle N 1Jelliti FathiPas encore d'évaluation
- Devoir de Contrôle N°1 - Physique - 1ère AS (2009-2010) MR Akermi AbdelkaderDocument2 pagesDevoir de Contrôle N°1 - Physique - 1ère AS (2009-2010) MR Akermi AbdelkaderHanine HmidaPas encore d'évaluation
- Dev Synt2 1ereDocument3 pagesDev Synt2 1ereSahbi Mabrouki YamenPas encore d'évaluation
- BREVET Physique-Chimie 2012Document7 pagesBREVET Physique-Chimie 2012sunnyaumPas encore d'évaluation
- Devoir de Contrôle N°1 - Physique - 2ème Sciences (2010-2011) MR Adam Bouali PDFDocument3 pagesDevoir de Contrôle N°1 - Physique - 2ème Sciences (2010-2011) MR Adam Bouali PDFAnis FriguiPas encore d'évaluation
- Sujet2015 CAP CPourEnvoibDocument2 pagesSujet2015 CAP CPourEnvoibpaulardPas encore d'évaluation
- Devoir de Contrôle N°1 - Physique - 1ère AS (2010-2011) MR Adam BoualiDocument2 pagesDevoir de Contrôle N°1 - Physique - 1ère AS (2010-2011) MR Adam BoualiKehlani ParrishPas encore d'évaluation
- Devoir de Contrôle N°1 - Physique - 1ère AS (2010-2011) MR Adam BoualiDocument2 pagesDevoir de Contrôle N°1 - Physique - 1ère AS (2010-2011) MR Adam BoualiOmar BEN MABROUKPas encore d'évaluation
- Rappel de Mecaniqueing160Document6 pagesRappel de Mecaniqueing160Ahmed ZidanePas encore d'évaluation
- Limites D'atterbergDocument7 pagesLimites D'atterbergMohamed soheib MekraouiPas encore d'évaluation
- Djamaa El Djazair: Code CN HVAC F 003 01 Objet: Calcul Des Pertes de Charge Des Ventilo ConvecteursDocument169 pagesDjamaa El Djazair: Code CN HVAC F 003 01 Objet: Calcul Des Pertes de Charge Des Ventilo ConvecteursagaPas encore d'évaluation
- Ch1-Generalites TurbomDocument5 pagesCh1-Generalites TurbomHermas SEYIKPE100% (1)
- Devoir de Synthèse N°1 2014 2015 (Lotfi)Document12 pagesDevoir de Synthèse N°1 2014 2015 (Lotfi)Ines BhaPas encore d'évaluation
- TP 2 VibrationDocument4 pagesTP 2 VibrationOussama Abdesslam AÏSSAPas encore d'évaluation
- Capteurs Et Actionneurs ExercicesDocument1 pageCapteurs Et Actionneurs Exercicesbatmat 1492Pas encore d'évaluation
- TP 1Document5 pagesTP 1selmi nourelhouda100% (1)
- Cour Cine 2020-2021 Final-1Document79 pagesCour Cine 2020-2021 Final-1Salah InePas encore d'évaluation
- Aermec Depl NRP FRDocument12 pagesAermec Depl NRP FRMohamed Anouar BidaPas encore d'évaluation
- 00main PDFDocument19 pages00main PDFLahoucine IbellaPas encore d'évaluation
- Physique Des MatériauxDocument65 pagesPhysique Des Matériauxbrahim.mosta20052017Pas encore d'évaluation
- Ancrage Ipe300Document10 pagesAncrage Ipe300Mahdi DakPas encore d'évaluation
- 2005 AmSud Sujet Exo3 Cinetique Sapo 6 5ptsDocument3 pages2005 AmSud Sujet Exo3 Cinetique Sapo 6 5ptskhamis faridPas encore d'évaluation
- FaculteDocument12 pagesFaculteferyal mrdPas encore d'évaluation
- RDM 1BCO Chap2 Eco 2012-2013Document29 pagesRDM 1BCO Chap2 Eco 2012-2013KamalMousser100% (1)
- Tables de Teneur en Humidité PDFDocument37 pagesTables de Teneur en Humidité PDFferhatiPas encore d'évaluation
- RamanDocument39 pagesRamanrodrigue yan100% (1)
- Power Point Cours Diagraphies IV L3 OnlineDocument24 pagesPower Point Cours Diagraphies IV L3 OnlinepcPas encore d'évaluation
- Phénomène DinductionDocument13 pagesPhénomène Dinductionernestadou7800Pas encore d'évaluation
- V5329ACDocument4 pagesV5329ACtarek.amirechePas encore d'évaluation
- HydrodynamiqueDocument8 pagesHydrodynamiqueKenz L'AïdPas encore d'évaluation
- Devoir 2021 ItDocument4 pagesDevoir 2021 ItTHONYPas encore d'évaluation
- Chapitre 4 - La Liquéfaction, Le Transport Et Les Techniques de Stockage de GNLDocument26 pagesChapitre 4 - La Liquéfaction, Le Transport Et Les Techniques de Stockage de GNLHabib MhamedPas encore d'évaluation
- But de TPDocument20 pagesBut de TPHamza Amdouni0% (1)
- Comment Choisir La Meilleure IRM Pour Votre BesoinDocument17 pagesComment Choisir La Meilleure IRM Pour Votre BesoinSirine Ben ChamesPas encore d'évaluation
- IntroductionDocument8 pagesIntroductionIl IasPas encore d'évaluation
- K Epsilon ModeleDocument2 pagesK Epsilon ModeleSalim Benmansour100% (1)
- Hydrau SoutDocument3 pagesHydrau SoutToufikJalalEddine100% (1)
- Manuel Gas LiftDocument99 pagesManuel Gas LifthamdiiiiiiiiiiiiiiiiPas encore d'évaluation