Académique Documents
Professionnel Documents
Culture Documents
Résumé Dosage 2
Transféré par
Scriblou67%(3)67% ont trouvé ce document utile (3 votes)
2K vues2 pagesSQ
Copyright
© © All Rights Reserved
Formats disponibles
PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentSQ
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PDF, TXT ou lisez en ligne sur Scribd
67%(3)67% ont trouvé ce document utile (3 votes)
2K vues2 pagesRésumé Dosage 2
Transféré par
ScriblouSQ
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 2
Prof : Trabelsi Mohamed
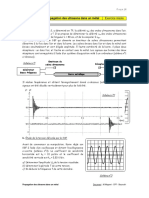
Dosage dun acide fort par une base forte
1-Exemple : dosage de HCl par NaOH :
La courbe de pH = f(VB) prsente trois parties et un seul
point dinflexion :
Lquation de la raction de dosage :
H3O+ + OH2H2O
1-Coordonnes de point dquivalence :
-On dtermine les coordonnes de point dquivalence
E ( VBE , pHE ) a partir de la mthode des tangentes
parallles
2-A lquivalence : pHE = 7
Alors la solution lquivalence est une solution neutre :
CA .VA = CB .VBE
-Pour un dosage acide fort base forte lquivalence pH
ne change pas aprs dilution
3-Remarque important :
Acide fort :
pH = -logCa
Ca = 10-pH
Aprs dilution : Ca diminue et pH augmente
Base fort :
pH = pKe + log Cb
Cb = 10pH- pKe
Aprs dilution : Cb diminue et pH diminue
Acide faible :
pH =
Ca =
= 2pH + log
Aprs dilution : Ca diminue et pH augmente
Base faible :
pH = + +
Cb =
= 2pH - - log
Aprs dilution : Cbdiminue et pH diminue
Niveau : 4 Sc
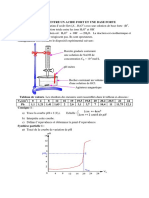
Dosage dun acide faible par une base forte
1-Exemple :dosage de CH3COOH par NaOH :
Dosage dune base faible par un acide fort
1-Exemple : dosage de NH3 par HCl :
La courbe de pH = f(VB) prsente trois parties et deux
points dinflexion :
Lquation de la raction de dosage :
CH3COOH + OH CH3COO- + H2O
1-Coordonnes de point dquivalence :
-On dtermine les coordonnes de point dquivalence
E (VBE, pHE) a partir de la mthode des tangentes
parallles
2-A lquivalence : pHE 8,7
Alors la solution lquivalence est une solution basique
CA .VA = CB .VBE
3-demi-quivalence :
VB =
La courbe de pH = f(Va) prsente trois parties et deux
points dinflexion :
Lquation de la raction de dosage :
NH3 + H3O+
N+
+ H2O
1-Coordonnes de point dquivalence :
-On dtermine les coordonnes de point dquivalence
E ( VAE , pHE ) a partir de la mthode des tangentes
parallles
2-A lquivalence : pHE 5,7
Alors la solution lquivalence est une solution dacide :
CB .VB = CA .VAE
3-demi-quivalence :
VA =
=1
+
Ka = alors pKa = pH 4,7
4-A lquivalence :
.
pHE = + + +
aprs calcul : pHE 8,7
=1
Ka = + alors pKa = pH 9.25
4-A lquivalence :
.
pHE = +
Aprs calcul : pHE 5,7
Remarque important :
-Une solution tampon est une solution qui maintient approximativement le pH malgr laddition de petites quantits dun
acide ou dune base ou malgr une dilution
-A la demi quivalence pH reste constante aprs dilution car pH = pKa la demi quivalence
Remarque : Aprs dilution Ka ne change pas / Aprs dilution la valeur de pKa ne change pas / aprs dilution le taux davancement final varie
Vous aimerez peut-être aussi
- Sujets Des Examens Nationaux Du BAC SM Depuis 2008 Jusquà 2018 ÉlectricitéDocument33 pagesSujets Des Examens Nationaux Du BAC SM Depuis 2008 Jusquà 2018 ÉlectricitéCédric Sorgho100% (4)
- Cours Dosage Acide BaseDocument9 pagesCours Dosage Acide BaseBoussetta Zouhaier100% (1)
- Acide Et Base - DosageDocument33 pagesAcide Et Base - Dosagemohamed saidi50% (2)
- Série D'exercices - Chimie - Les Acides Et Les Bases de Bronsted - 3ème Sciences Exp (2018-2019) MR Mejri Chokri PDFDocument2 pagesSérie D'exercices - Chimie - Les Acides Et Les Bases de Bronsted - 3ème Sciences Exp (2018-2019) MR Mejri Chokri PDFMahmoud Essahbi Sahbi Daghsni75% (4)
- Analogie Electrique - MecaniqueDocument2 pagesAnalogie Electrique - Mecaniqueben mamia100% (3)
- Série D'exercices N°10 - Sciences Physiques Dosage Acido Basique - Bac Sciences Exp (2011-2012) MR ALIBI ANOUAR 3Document8 pagesSérie D'exercices N°10 - Sciences Physiques Dosage Acido Basique - Bac Sciences Exp (2011-2012) MR ALIBI ANOUAR 3Tawfiq Weld EL Arbi75% (4)
- Série 1 - Dosage Acido-BasiqueDocument2 pagesSérie 1 - Dosage Acido-BasiqueAzdine MC100% (1)
- Cours - Chimie Dosage - Bac Technique (2010-2011) Elève RadhouaneDocument5 pagesCours - Chimie Dosage - Bac Technique (2010-2011) Elève RadhouaneTawfiq Weld EL ArbiPas encore d'évaluation
- 08 TS Chimie Cours - Reactions Acido-Basiques-2Document4 pages08 TS Chimie Cours - Reactions Acido-Basiques-2foufoudoudouPas encore d'évaluation
- Série Corrigée N°7 - Chimie Série PH Des Solutions Aqueuses - Bac Mathématiques (2013-2014) MR BARHOUMI EzzedineDocument3 pagesSérie Corrigée N°7 - Chimie Série PH Des Solutions Aqueuses - Bac Mathématiques (2013-2014) MR BARHOUMI EzzedineAicha Daou50% (2)
- Serie #8 Determination D Une Quantite de Matiere A L Aide D Une Reaction ChimiqueDocument2 pagesSerie #8 Determination D Une Quantite de Matiere A L Aide D Une Reaction ChimiqueMahmoud Essahbi Sahbi Daghsni67% (3)
- Interaction Onde MatièreDocument6 pagesInteraction Onde Matièreأسماء النخليPas encore d'évaluation
- BAC SM 2008 2018 Acide Et BaseDocument14 pagesBAC SM 2008 2018 Acide Et BaseHAMADA1972100% (2)
- Exercices 4 La Conductance Et La Conductivité Non CorrigeDocument1 pageExercices 4 La Conductance Et La Conductivité Non CorrigeMajed Gharib100% (1)
- Devoir 1 PCDocument2 pagesDevoir 1 PCMouhibi Abdellah100% (2)
- Série D'exercices - Chimie Série Acide Base Acide Base - 2ème Sciences (2012-2013) MR Chouket HasenDocument2 pagesSérie D'exercices - Chimie Série Acide Base Acide Base - 2ème Sciences (2012-2013) MR Chouket HasenRamzi Tarchouni75% (4)
- Cours de Soir Biof Final 2 SemestreDocument88 pagesCours de Soir Biof Final 2 SemestreMohamed El OuahdaniPas encore d'évaluation
- Série 1 - Équilibre ChimiqueDocument6 pagesSérie 1 - Équilibre ChimiqueMed RT100% (1)
- Les Ondes1Document2 pagesLes Ondes1EL Omrani Said100% (1)
- Cours - Chimie Les Amines Aliphatiques - 3ème Sciences Exp (2013-2014) MR Chouket HasenDocument5 pagesCours - Chimie Les Amines Aliphatiques - 3ème Sciences Exp (2013-2014) MR Chouket HasenLotfi BoucharebPas encore d'évaluation
- c8 1bac Biof - Dosage Direct Prof - Sbiro (WWW - Pc1.ma)Document3 pagesc8 1bac Biof - Dosage Direct Prof - Sbiro (WWW - Pc1.ma)Majed Gharib100% (3)
- Examen Blanc Physique Chimie Bac DDocument4 pagesExamen Blanc Physique Chimie Bac Dkouassi hermann ulrich koffi100% (1)
- Chap. 2 Ondes Mécaniques Progressives Périodiques - CopieDocument7 pagesChap. 2 Ondes Mécaniques Progressives Périodiques - Copiemohamed laghribPas encore d'évaluation
- OMPPBIOFDocument3 pagesOMPPBIOFYassir Ksakass25% (4)
- Série00 Révision 2bac BiofDocument1 pageSérie00 Révision 2bac Biofnait100% (1)
- 3éme SC Acide Carboxiliques Et Ses DérivésDocument4 pages3éme SC Acide Carboxiliques Et Ses DérivésJihed HorchaniPas encore d'évaluation
- Cours - Chimie - Les Acides Et Les Bases - Bac Sciences Exp (2014-2015) MR NabilDocument6 pagesCours - Chimie - Les Acides Et Les Bases - Bac Sciences Exp (2014-2015) MR NabilAliMchirgui100% (4)
- Acide Et Base - Dosage (Récupération Automatique)Document39 pagesAcide Et Base - Dosage (Récupération Automatique)Driss Droussi100% (3)
- Cours - Chimie Solution Aqueuse D'acide - 2ème Sciences (2014-2015) MR Mekni NejibDocument2 pagesCours - Chimie Solution Aqueuse D'acide - 2ème Sciences (2014-2015) MR Mekni Nejibمحمد أمين أحمدي100% (4)
- 5 Suivi D'une Transrormation Chimique PDFDocument16 pages5 Suivi D'une Transrormation Chimique PDFbrini med100% (2)
- CorrectionSPC BAC2012Document4 pagesCorrectionSPC BAC2012Letudiant.fr0% (2)
- Acide Base ExercicesDocument36 pagesAcide Base Exerciceschaari abdelouahadPas encore d'évaluation
- Ondes-Exercices Prof - Hadjyne (WWW - Pc1.ma)Document4 pagesOndes-Exercices Prof - Hadjyne (WWW - Pc1.ma)Med Brini100% (1)
- Devoir 2 Hikma 2020 2bac SM Prof - Kraidy (WWW - Pc1.ma)Document4 pagesDevoir 2 Hikma 2020 2bac SM Prof - Kraidy (WWW - Pc1.ma)Majed Gharib100% (1)
- Série D'exercice RLC ForcéDocument5 pagesSérie D'exercice RLC ForcéAdam Chabchoub100% (7)
- Exercices 2 Les Lois de NewtonDocument1 pageExercices 2 Les Lois de Newtonالغزيزال الحسن EL GHZIZAL Hassane100% (5)
- Cours de 2bac BIOF de Semestre 1, ChrikiDocument105 pagesCours de 2bac BIOF de Semestre 1, ChrikiACHRAF DOUKARNE100% (1)
- Exercice Bac Blanc Physique Ondes Sonores PDFDocument3 pagesExercice Bac Blanc Physique Ondes Sonores PDFYassir Rochd50% (2)
- Resume Chute Libre - Projectile FilaliDocument2 pagesResume Chute Libre - Projectile FilaliMohamed Hammouch100% (7)
- Couple Acide - Base: ExercicesDocument16 pagesCouple Acide - Base: ExercicesAhamadi ElhouyounPas encore d'évaluation
- Série D'exercices - Physique Les Ondes Mécaniques - Bac Sciences Exp (2012-2013) MR BARHOUMI Ezedine PDFDocument3 pagesSérie D'exercices - Physique Les Ondes Mécaniques - Bac Sciences Exp (2012-2013) MR BARHOUMI Ezedine PDFMohamed El Ouahdani100% (1)
- Ultrasons MétalDocument4 pagesUltrasons MétalAicha Daou100% (6)
- Cours Lycée Pilote - Chimie - Hydrocarbures - 2ème Sciences (2013-2014) MR Abdelhamid GalaïDocument3 pagesCours Lycée Pilote - Chimie - Hydrocarbures - 2ème Sciences (2013-2014) MR Abdelhamid GalaïElghram Marwan50% (4)
- Resume RadioactiviteDocument2 pagesResume Radioactiviteben mamia100% (1)
- Cours Mouvement de Rotation D PDFDocument7 pagesCours Mouvement de Rotation D PDFmohamed laghrib100% (4)
- Contrôle 25Document3 pagesContrôle 25nabla199100% (1)
- Cours 1 Mouvement D'un Projectile Dans Le Champ de PesanteurDocument3 pagesCours 1 Mouvement D'un Projectile Dans Le Champ de Pesanteurmohsine100% (2)
- 2Bm 16-17-S1 Ds1A Belkhatir FRDocument3 pages2Bm 16-17-S1 Ds1A Belkhatir FRBaba Mhd Yara0% (1)
- Série D'exercice 01Document2 pagesSérie D'exercice 01Ayman gamerPas encore d'évaluation
- C2 Champ ElectrostatiqueDocument15 pagesC2 Champ ElectrostatiqueSamir JemniPas encore d'évaluation
- Examen Blanc 2021 Physique Chimie SMDocument9 pagesExamen Blanc 2021 Physique Chimie SMTesteur Mohammedia100% (1)
- Transformations Spontanees Dans Les Piles Et Production D Energie Exercices Non Corriges 1 1Document3 pagesTransformations Spontanees Dans Les Piles Et Production D Energie Exercices Non Corriges 1 1Ibtihel BoughanmiPas encore d'évaluation
- Chapitre 2 - PH Des Solutions AqueusesDocument11 pagesChapitre 2 - PH Des Solutions AqueusesBeatrice Florin100% (1)
- Exercice Corrige Bac Blanc Physique Ondes Sonores PDFDocument2 pagesExercice Corrige Bac Blanc Physique Ondes Sonores PDFYassir Rochd0% (1)
- 6129e58d84154reactions Acide Base Solutions Tampons Chimie TermDocument7 pages6129e58d84154reactions Acide Base Solutions Tampons Chimie TermPrince Informaticien GamesPas encore d'évaluation
- Variation Du PH Au Cours Des Dosages Acide PDFDocument13 pagesVariation Du PH Au Cours Des Dosages Acide PDFAzizElheniPas encore d'évaluation
- Le PH 6. Le Dosage Des Solutions Dacides Et Des Bases Faibles - Theorie - 2014Document15 pagesLe PH 6. Le Dosage Des Solutions Dacides Et Des Bases Faibles - Theorie - 2014RachidaPas encore d'évaluation
- Cours 5 C TRAFI 2BACDocument18 pagesCours 5 C TRAFI 2BACEnidroun OutPas encore d'évaluation
- Cours Dosage Acide Base 3Document8 pagesCours Dosage Acide Base 3Boussetta ZouhaierPas encore d'évaluation
- ActivitesDocument4 pagesActivitesMamadou DembaPas encore d'évaluation
- TP2 WordDocument2 pagesTP2 WordScriblouPas encore d'évaluation
- B.technologies Web Chapitre 3 (CSS)Document21 pagesB.technologies Web Chapitre 3 (CSS)ScriblouPas encore d'évaluation
- Exercice Et SolutionsDocument44 pagesExercice Et SolutionsScriblouPas encore d'évaluation
- 2a Examen PratiqueDocument23 pages2a Examen PratiqueScriblouPas encore d'évaluation
- Correction de La Série n3 InfoDocument11 pagesCorrection de La Série n3 InfoScriblouPas encore d'évaluation
- 2 - Série Sous ProgrammesDocument8 pages2 - Série Sous ProgrammesScriblouPas encore d'évaluation
- Série Pile Math 1 SCDocument3 pagesSérie Pile Math 1 SCScriblouPas encore d'évaluation
- Integral 1Document6 pagesIntegral 1ScriblouPas encore d'évaluation
- Série Réaction Acide BaseDocument5 pagesSérie Réaction Acide BaseScriblouPas encore d'évaluation
- Trigonometrie SyntheseDocument156 pagesTrigonometrie SyntheseScriblouPas encore d'évaluation
- Echelle Pka PDFDocument1 pageEchelle Pka PDFScriblou100% (2)